É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Nafion-Sal modificado hidrofóbico para imobilização de enzimas e Estabilização
Neste Artigo
Resumo
Este artigo vai descrever o procedimento para a síntese de uma membrana Nafion hidrofobicamente modificado imobilização de enzimas e como para imobilizar proteínas e / ou enzimas no interior da membrana e testar a sua actividade específica.
Resumo
Durante a última década, tem havido uma riqueza de aplicação para as enzimas imobilizadas e estabilizadas incluindo biocatálise, biossensores, e células de biocombustível. 1-3 Em aplicações mais bioelectrochemical, enzimas ou organelas são imobilizados sobre uma superfície do eléctrodo com a utilização de algum tipo de polímero de matriz. Este andaime polímero deve manter as enzimas estável e permitir a difusão fácil de moléculas e iões dentro e para fora da matriz. A maioria dos polímeros utilizados para este tipo de imobilização são baseados em poliaminas ou poliálcoois - polímeros que imitam o ambiente natural das enzimas que eles encapsular e estabilizar a enzima através de hidrogénio ou ligações iónicas. Outro método para a estabilização de enzimas envolve o uso de micelas, que contêm regiões hidrofóbicas que podem encapsular e estabilizar as enzimas 4,5. Em particular, o grupo Minteer desenvolveu um polímero baseado em micelar Nafion comercialmente disponível. 6,7 Nafionem si é um polímero micelar que permite a difusão de canal-assistida de protões e de outros catiões pequenas, mas as micelas e os canais são extremamente pequeno e que o polímero é muito ácida, devido às cadeias sulfónicos lado ácido, o que é desfavorável para a imobilização de enzimas. No entanto, quando Nafion é misturado com um excesso de hidrofóbicos sais de amónio de alquilo tais como brometo de tetrabutilamónio (TBAB), os catiões de amónio quaternário substituir os protões e tornar-se os contra-iões para os grupos sulfonato sobre as cadeias laterais de polímero (Figura 1). Isto resulta em maiores micelas e canais dentro do polímero que permitem a difusão de grandes substratos e iões que são necessários para a função enzimática, tais como dinucleótido adenina nicotinamida (NAD). Este modificado Nafion polímero tem sido usado para imobilizar muitos tipos diferentes de enzimas, bem como as mitocôndrias para uso em biossensores e células de biocombustível. 8-12 Este documento descreve um novo processo para fazer este microfoneEllar polímero membrana imobilização de enzimas que podem estabilizar as enzimas. A síntese da membrana micelar enzima imobilização, o procedimento para a imobilização de enzimas dentro da membrana, e os ensaios para estudar a actividade enzimática específica da enzima imobilizada são detalhados abaixo.
Protocolo
1. Modificação do Nafion com sais de amónio quaternário
- Agitar uma garrafa de suspensão Nafion 5% w / v vigorosamente durante aprox. 30 segundos para assegurar que Nafion é suspenso uniformemente na solução.
- Pipetar fora 2 mL da Nafion agora re-suspenso em um frasco de vidro (volume frasco pode conter de 2,5 mL a 10 mL).
- Medir um excesso de 3 vezes molar (em relação aos grupos de ácido sulfónico no polímero Nafion) do sal de amónio de alquilo brometo de (massas adequadas são mostrados na Tabela 1) e adicionar este ao frasco contendo o 2 mL de Nafion.
- Vortex do frasco a 1500 rpm por 10-15 minutos.
- Despeje a solução viscosa em uma bandeja de plástico pesando que mede aprox. 3 x 3 polegadas, e usar uma pipeta para transferir qualquer solução residual a partir do frasco para a bandeja de pesagem.
- Permitir que os solventes para evaporar para fora do barco pesar, deixando um amarelo / castanho película transparente, sobre a parte inferior da bandeja de pesagem (Figura 2). A taxa de evaporação de solvente deve ser tal que é necessário mais do que 6 horas para todo o solvente se evapore. Se o solvente evapora muito rápido, um material branco duro vai formar, em vez de um filme transparente, indicando que a estrutura micelar do polímero foi destruído, e você deve re-iniciar o procedimento. Se a evaporação de solventes, é muito lento, um de-umidificador pode ser necessário, porque muito lento de evaporação normalmente leva a um gel, brega laranja e você deve re-iniciar o procedimento. Gamas de temperatura típicas para a evaporação do solvente são de 20 - 37 ° C. As condições reais de secagem são uma função da humidade relativa e à temperatura da sala, mas é importante que a secagem ser lento para manter a estrutura micelar, mas não demasiado lenta para permitir a formação do gel.
- Encher o barco com pesar 18M Ωcm água deionizada (10-20 mL de água), tampe e deixe de molho por 12-24 horas para remover o excesso de sais de amônio alquílicos de brometo e HBr.
- Verter (ou pipeta) para fora da água e enxaguar 3 vezes com água DI suficiente para encher o tabuleiro de cada vez. Tenha cuidado para não perder nenhum do filme de polímero durante esta etapa.
- Permitir que a bandeja de pesagem para sentar descoberto até que o polímero é completamente seca Neste ponto, o polímero deve ser uma película transparente e um pouco quebradiço plástico. Novamente, se o ar é muito húmido, um de-humidificador pode ser necessário para completar a evaporação de uma forma atempada.
- Usando uma espátula, cuidadosamente remover o filme seco a partir da bandeja de pesagem e transferi-lo para um frasco de vidro limpo.
- Adicionar 2 mL de etanol e 3 cerâmicos grânulos de mistura, e vórtice durante 4 horas ou até que a película de polímero é completamente re-suspenso.
2. Imobilização de enzimas em TBAB-Modified Nafion para ensaios de atividade
- Para uma enzima seca, pesam-se 1-10 mg da enzima em um tubo de microcentrífuga de 1,5 ml, e adicionar 1 mL de tampão de fosfato 100 mM pH 7 para criar um 1-10 mg / mL de solução enzimática. For uma enzima que está em solução, usar um ácido bicinconínico (BCA) ensaio de 13 para determinar a quantidade de proteína, e adicionar uma quantidade apropriada de tampão fosfato 100 mM para trazer a concentração de proteína para 1-10 mg / mL. ML mg / 1-10 geralmente corresponde a 1-50 nanomoles / mL.
- Para 120 uL de 1 mg / mL solução de enzima, adicionar 60 uL da solução de Nafion alquilo-amónio modificada, e vórtice durante 10 segundos. (Esta mistura pode ser aumentado para um grande número de repetições. Mantenha a razão de solução de enzima a-polímero em 2:1.)
- Pipetar 60 da solução de enzima / polímero para o fundo de 3 separadas 1 cm 2 cuvetes, e permitir que a secar durante a noite.
3. Ensaio da enzima desidrogenase NAD-dependente Imobilizado
- Para a cuvete, adicionar 1,3 mL de 50 mM de pirofosfato de sódio (pH 8,8), 1,5 mL de 15 mM NAD (recentemente preparado), e 0,1 mL de água.
- Coloque a cuvete num espectrofotómetro UV / Vis (Evolut ThermoScientific ieion 260 Bio e Thermo Spectronic Genesys 20) ajustado para um comprimento de onda de 340 nm.
- Zerar o espectrômetro, e depois adicionar 0,1 ml de etanol. Misturar os reagentes suavemente pipetando a solução cima e para baixo 5 vezes. Para um espaço em branco, usar 0,1 mL de água adicional, em vez do 0,1 mL de etanol.
- Ler a absorvância a 340 nm a 5 minutos após os reagentes foram adicionados à cuvete e 20 minutos depois. Traçar os dois pontos de dados para obter uma inclinação que pode ser usado para os cálculos da actividade.
4. Ensaio de Imobilizados PQQ-dependentes Desidrogenases
- Para a cuvete, adicionar 1,5 mL de fosfato de sódio (pH 7,3) e 200 uL de 600 PMS uM.
- Coloque a cuvete num espectrofotómetro UV / Vis definido para um comprimento de onda de 600 nm e, em seguida, zero, o espectrómetro.
- Adicionar 100 uL de 700 uL DCIP e 200 uL do substrato de interesse (etanol, acetaldeído, glicerol, glucose, gliceraldeído ou), e misturar os reagentes suavemente pipetando a solutião cima e para baixo 5 vezes. Para um espaço em branco, usar 200 uL de água em vez do substrato de interesse.
- Ler a absorvância a 600 nm a 5 minutos após os reagentes foram adicionados à cuvete e 20 minutos depois.
5. Ensaio de glucose oxidase imobilizada
- Para a cuvete, adicionar 2,0 mL de uma solução contendo 0,2 M de ácido p-hidroxibenzóico, azida de sódio 0,02% (w / v), 128 U de peroxidase, 0,3 mM de 4-aminoantipirina, 1 M de fosfato de potássio, e 50 mM de glucose. Misturar a solução pipetando para cima e para baixo 5 vezes.
- Coloque a cuvete de um conjunto espectrofotómetro UV / Vis para um comprimento de onda de 510 nm.
- Ler a absorvância a 510 nm a 5 minutos após os reagentes foram adicionados à cuvete e, novamente, em 20 minutos depois.
6. Os resultados representativos
A estrutura micelar do polímero Nafion modificada pode ser interrompido por secagem do sal original / polímero co-fundido filme muito fast A Figura 2 mostra uma mistura de sal / polímero que tenha sido seca correctamente resultando em um filme transparente castanho, luz. Um filme que seca muito rápido pode resultar em opacos, flocos brancos de polímero devido ao facto de o processo de secagem pode destruir a estrutura micelar.
Uma vez que o Nafion modificado polímero e enzima foram misturados e co-moldada sobre o fundo de uma cuvete, ensaios de actividade enzimática pode ser usado para avaliar a estabilidade da enzima dentro do filme de polímero. Tabelas 2-4 mostram os resultados do ensaio de duas enzimas desidrogenase e glicose oxidase imobilizada em vários filmes de Nafion modificados, respectivamente. Note-se a maior actividade das enzimas que são imobilizadas vs as enzimas em solução tampão, mostrando que os polímeros Nafion modificadas podem efectivamente aumentar a actividade de certas enzimas (chamado superactivity). Outras enzimas têm limitações de transporte que diminuem a sua actividade específica quando imobilizá-los no polímero (celulases e amilases ou seja, cujos substratos são macromoléculas bastante grandes).
| Sal de amônio quaternário usado | 3 vezes superior |
| T3A (brometo de tetrapropilamónio) | 32,37 mg / ml |
| TBAB (brometo de tetrabutilamónio) | 39,19 mg / ml |
| TPAB (brometo de tetrapentylammonium) | 46,01 mg / ml |
| TEHA (brometo de triethylhexylammonium) | 32,37 mg / ml |
| AHMT (brometo de trimethylhexylammonium) | 27,25 mg / ml |
| TMOA (brometo de trimethyloctylammonium) | 30,66 mg / ml |
| TMDA (brometo de trimethyldecylammonium) | 34,07 mg / ml |
| TMDDA (brometo de trimethyldodecylammonium) | 37,48 mg / ml |
| TMTDA (brometo de trimethyltetradecylammonium) | 40,89 mg / ml |
| TMHDA (brometo de trimethylhexadecylammonium) | 44,31 mg / ml |
| TMODA (brometo de trimethyloctadecylammonium) | 47,71 mg / ml |
Tabela 1. Quantidades de sais de tetra-alquil amónio a utilizar para Nafion modificação de polímeros.
| Tipo de Nafion | A actividade enzimática (U / g) |
| Tampão (sem polímero) | 16,63 ± 8,11 |
| Nafion (un-mod.) | 9,25 ± 2,21 |
| TMTDA | 3,23 ± 2,92 |
| TBAB | 3,93 ± 3,33 |
| TMDDA | 4,19 ± 1,04 |
| TMOA | 3,51 ± 1,11 |
| TMDA | 8,00 ± 4,53 |
| AHMT | 1,68 ± 1,39 |
| TMHDA | 4,83 ± 0,99 |
| TMODA | 10,45 ± 3,20 |
Tabela 2 NAD-dependente actividade de desidrogenase de glucose imobilizada em seleccionados polímeros modificados Nafion (nota: actividade imobilizada é uma função da actividade específica inicial da enzima)..
| Tipo de Nafion | A actividade enzimática (mU / g) |
| Tampão (sem polímero) | 7,18 ± 0,51 |
| Nafion (un-mod.) | 70,1 ± 0,5 |
| TMTDA | 133 ± 6 |
| TBAB | 244 ± 4 |
| TMDDA | 221 ± 6 |
| TMOA | 1,78 ± 0,63 |
| TMDA | 206 ±5 |
| TEHA | 40,1 ± 50,6 |
| TMHDA | 0 |
| TMODA | 1,45 ± 0,06 |
Tabela 3 PQQ-dependente actividade de desidrogenase de glucose imobilizada em seleccionados polímeros modificados Nafion (nota: actividade imobilizada é uma função da actividade específica inicial da enzima)..
| Tipo de Nafion | A actividade enzimática (U / g) |
| Tampão (sem polímero) | 103,61 ± 3,15 |
| Nafion (un-mod.) | 19,93 ± 10,10 |
| TMTDA | 247,25 ± 12,49 |
| TBAB | 152,27 ± 5,29 |
| TMDDA | 262,05 ± 6,26 |
| TMOA | 129,18 ± 2,31 |
| TMDA | 141,23 ± 1,97 |
| AHMT | 131,75 ± 2,89 |
| TMHDA | 132,50 ± 1,18 |
| TMODA | 136,50 ± 0,96 |
. Tabela 4 representativas actividade de oxidase de glicose específica imobilizado na seleccionados polímeros modificados Nafion (nota: actividade imobilizada é uma função da actividade específica inicial da enzima).
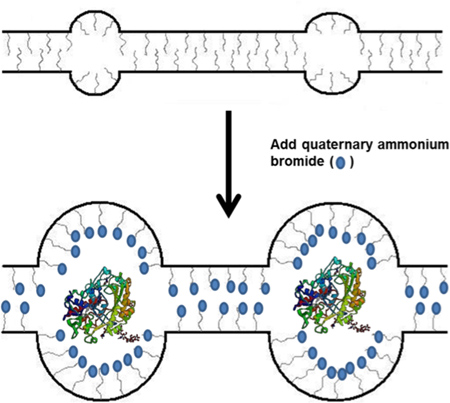
Figura 1. Esquemática da incorporação TBAB em Nafion polímero e subsequente utilização na imobilização de enzimas.

Figura 2. Fotografia óptica de um primeiro co-cast filmes de Nafion e TBAB. Retardar a secagem produz um transparente, filme castanho claro cobrindo o bottom da bandeja de pesagem.
Discussão
No processo descrito, os sais de tetra-alquil amónio são utilizados para modificar Nafion comercial para criar polímeros micelares que podem ser usados para imobilizar e estabilizar as enzimas. Os ensaios descritos no procedimento revelam que o polímero pode ser usado para imobilizar uma grande variedade de enzimas com uma elevada retenção de actividade. Se a enzima de interesse tem uma actividade muito baixa ou é impuro, uma concentração mais elevada pode ser necessária e não deve afectar o processo de...
Divulgações
Não há conflitos de interesse declarados.
Agradecimentos
Os autores agradecem o Escritório de Pesquisa Naval, United Soybean Board, e Fundação Nacional de Ciência para o financiamento.
Materiais
| Name | Company | Catalog Number | Comments |
| Nome do reagente | Companhia | Número de Catálogo | |
| Nafion | Sigma-Aldrich | 70160 | |
| Brometo de tetra sais alquilamónio | Sigma-Aldrich | n / a | |
| Álcool desidrogenase | Sigma-Aldrich | A3263 | |
| Nicotinamida adenina dinucleotídeo (NAD) | Simga-Aldrich | N7004 | |
| Pirofosfato de sódio | Sigma-Aldrich | P8010 | |
| Fenazina metossulfato (PMS) | Sigma-Aldrich | P9625 | |
| 2,6 Dichloroindophenol-(DCIP) | Sigma-Aldrich | D1878 | |
| Glucose oxidase | Sigma-Aldrich | G7141 | |
| Ácido 4-hidroxibenzóico | Sigma-Aldrich | 240141 | |
| A azida de sódio | Sigma-Aldrich | S8032 | |
| Peroxidase | Sigma-Aldrich | P8375 | |
| 4-aminoantipirina | Sigma-Aldrich | 06800 | |
| UV / Vis Espectrofotômetro | Thermo | Evolução Bio 260 ou Spectronic Genesys 20 | |
| Vortex Genie | |||
| Balança analítica |
Referências
- Calabrese-Barton, S., Gallaway, J., Atanassov, P. Enzymatic biofuel cells for implantable and microscale devices Chem. Rev. 104, 4867-4886 (2004).
- Cracknell, J. A., Vincent, K. A., Armstrong, F. A. Enzymes as Working or Inspirational Electrocatalysts for Fuel Cells and Electrolysis. Chem. Rev. 108, 2439-2461 (2008).
- Minteer, S. D., Liaw, B. Y., Cooney, M. J. Enzyme-Based Biofuel Cells. Curr. Opin. Biotechnol. 18, 228-234 (2007).
- Callahan, J. W., Kosicki, G. W. The Effect of Lipid Micelles on Mitochondrial Malate Dehydrogenase. Canadian Journal of Biochemistry. 45, 839-851 (1967).
- Martinek, K. Modeling of the Membrane Environment of Enzymes: Superactivity of Laccase Entrapped into Surfactant Reversed Micelles in Organic Solvents. Biokhimiya. 53, 1013-1016 (1988).
- Moore, C. M., Akers, N. L., Hill, A. D., Johnson, Z. C., Minteer, S. D. Improving the Environment for Immobilized Dehydrogenase Enzymes by Modifying Nafion with Tetraalkylammonium Bromides. Biomacromolecules. 5, 1241-1247 (2004).
- Schrenk, M. J., Villigram, R. E., Torrence, N. J., Brancato, S. J., Minteer, S. D. Effects of Mixture Casting Nafion with Quaternary Ammonium Bromide Salts on the Ion-Exchange Capacity and Mass Transport in the Membranes. J. Membr. Sci. 205, 3-10 (2002).
- Akers, N. L., Moore, C. M., Minteer, S. D. Development of Alcohol/O2 Biofuel Cells Using Salt-Extracted Tetrabutylammonium Bromide/Nafion Membranes to Immobilize Dehydrogenase Enzymes. Electrochim. Acta. 50, 2521-2525 (2005).
- Sokic-Lazic, D., Minteer, S. D. Citric Acid Cycle Biomimic on a Carbon Electrode. Biosens. Bioelectron. 24, 939-944 (2008).
- Arechederra, R. L., Minteer, S. D. Complete Oxidation of Glycerol in an Enzymatic Biofuel Cell. Fuel Cells. 9, 63-69 (2009).
- Germain, M., Arechederra, R. L., Minteer, S. D. Nitroaromatic Actuation of Mitochondrial Bioelectrocatalysis for Self-Powered Explosive Sensors. J. Am. Chem. Soc. 130, 15272-15273 (2008).
- Addo, P. K., Arechederra, R. L., Minteer, S. D. Evaluating Enzyme Cascades for Methanol/Air Biofuel Cells Based On NAD+-Dependent Enzymes. Electroanalysis. 22, 807-812 (2010).
- Smith, P. K., Krohn, R. I., Hermanson, G. T., Mallia, A. K., Gartner, F. H., Provenzano, M. D., Fujimoto, E. K., Goeke, N. M., Olson, B. J., Klenk, D. C. Measurement of protein using bicinchoninic acid. Analytical Biochemistry. 150, 76-85 (1985).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados