Method Article
O Modelo Monoiodoacetate da osteoartrite Dor no mouse
Neste Artigo
Resumo
A osteoartrite (OA), ou doença degenerativa das articulações, é uma condição debilitante associada a dor que permanece apenas parcialmente controlada por analgésicos disponíveis. Os modelos animais estão sendo desenvolvidos para melhorar a nossa compreensão dos mecanismos da dor relacionada com a OA. Aqui nós descrevemos a metodologia para o modelo monoiodoacetate de dor OA no mouse.
Resumo
Um dos principais sintomas de pacientes com osteoartrite (OA) é a dor que é desencadeada por alterações periféricas, bem como centrais dentro das vias de dor. Os tratamentos atuais para dor OA, tais como AINEs ou opiáceos são nem suficientemente eficaz nem desprovido de efeitos colaterais prejudiciais. Modelos animais de OA estão sendo desenvolvidos para melhorar a nossa compreensão dos mecanismos da dor relacionada com a OA e definir novos alvos farmacológicos para a terapia. Actualmente modelos disponíveis de OA em roedores incluem intervenções cirúrgicas e químicas em uma articulação do joelho. O modelo monoiodoacetate (MIA) se tornou um padrão para a modelagem de interrupção conjunto em OA em ambos os ratos e camundongos. O modelo, que é mais fácil de realizar, no rato, envolve a injecção de MIA em uma articulação do joelho, que induz respostas de dor semelhante rápidas no membro ipsilateral, o nível do qual pode ser controlada por injecção de doses diferentes. injecção intra-articular de condrócitos MIA perturba glicólise através da inibição glyceraldeído desidrogenase-3-fosfatase e resulta em morte de condrócitos, neovascularização, necrose do osso subcondral e colapso, bem como a inflamação. As mudanças morfológicas da cartilagem articular e do osso interrupção são reflexo de alguns aspectos da patologia do paciente. Junto com lesões articulares, MIA induz injeção referido sensibilidade mecânica na pata traseira e peso déficits ipsilaterais de rolamento que são mensuráveis e quantificáveis. Essas mudanças de comportamento se assemelham a alguns dos sintomas relatados pela população de pacientes, validando assim a injeção de MIA no joelho como um modelo pré-clínico útil e relevante de dor OA.
O objetivo deste artigo é descrever a metodologia de injeções intra-articulares de MIA e as gravações comportamentais do desenvolvimento associado de hipersensibilidade com uma mente para destacar as medidas necessárias para dar gravações consistentes e confiáveis.
Introdução
Clinicamente, a osteoartrite (OA), ou doença degenerativa das articulações, é uma condição dolorosa e debilitante caracterizada por uma perda progressiva de cartilagem articular, inflamação moderada dos tecidos em torno das articulações e algumas vezes formação de osteófitos e quistos ósseos. Os pacientes com OA relatar dor persistente 1 e exibição aumento da sensibilidade à pressão e estímulos nocivos na artrite conjunta 2-4. No momento, não há cura para a OA com abordagens e analgésicos terapêuticas disponíveis são prescritos para aliviar a dor associada com esta condição, com algum grau de sucesso 5. No entanto, dor OA continua a ser um clínicos modelos de emissão e de animais da OA estão sendo desenvolvidos para melhorar a nossa compreensão dos mecanismos da dor relacionada com a OA e divulgar novos alvos para a terapia.
Existem vários modelos animais de OA disponíveis com diferentes características 6. Os métodos cirúrgicos, como o anteriortransecção do ligamento cruzado, pode ser utilizado. No entanto, envolvem a intervenção cirúrgica hábil e são realizados principalmente no rato, enquanto que a desestabilização do menisco medial (DMM) é utilizado no ratinho. Desenvolvimento espontâneo da OA ocorre na cobaia e degeneração da articulação espontânea foi relatada em ratos pretos C57 de 3 a 16 meses de idade 7,8. Modelos OA espontâneos não envolvem qualquer intervenção para induzir a doença, mas eles têm variabilidade inerente, e, como tal, incorrer em maiores números e custa 9,10. modelos induzidas quimicamente, por outro lado, necessitam de muito menos invasiva do que os procedimentos cirúrgicos modelos, e como tal, são mais fáceis de implementar e permitem o estudo de lesões da OA em diferentes fases. Estes modelos incluem injecções únicas no joelho de agentes inflamatórios, imunotoxinas, colagenase, papaína, ou monoiodoacetate, que podem ser tóxicos se escapar do espaço da articulação. De todos os modelos químicos de OA, MIA é o mais frequentemente utilizado, particularly para testar a eficácia de agentes farmacológicos para o tratamento de dor, como este modelo gera um fenótipo reprodutível e robusto, e rápido da dor do tipo que pode ser graduada, alterando MIA dosagem 11-15.
injecção intra-articular de MIA em roedores reproduz lesões OA-like e deterioração funcional que pode ser analisada e quantificada. MIA é um inibidor da gliceraldeído-3-fosfatase, interrompendo a glicólise celular e eventualmente resultando em morte celular 16,17. Injecção intra-articular de MIA provoca a morte celular dos condrócitos, conduzindo a degeneração da cartilagem e do osso subcondral alterações subsequentes, tais como a aparência de osso osteófitos 18,19.
Como o utilitário de MIA no rato foi descrito antes de 20, neste artigo vamos nos concentrar sobre a metodologia de OA induzida por MIA em camundongos já que este modelo está sendo usado cada vez mais com a disponibilidade de ratinhos knock-out. Nós descrevemos um procedimento para a INJECção de volumes muito reduzidos para o joelho e métodos para medir a sensibilidade a estímulos nocivos e não nocivos nos membros posteriores.
A repartição da metodologia vai ajudar a reduzir a variabilidade, e como tal, o modelo de refinar e reduzir o número de animais necessários para o estudo.
Protocolo
Procedimentos envolvendo indivíduos animais foram aprovados pelo Comitê de Ética do Kings College de Londres e estão em conformidade com os Regulamentos do Reino Unido Escritório Internos (Animais procedimentos científicos Act 1986).
1. injecção intra-articular de Monoiodoacetate no joelho
- Casa 8 -. 10 semanas de idade ratos em grupos de 5 em um 12 hr ciclo de luz / escuridão (luzes acesas às 07:00) com comida e água ad libitum Deixe os ratos aclimatar durante 1 semana antes do início do experimento.
- Randomize e ratos gaiola em grupos de 5. Use o número de animais como códigos para cegar o experimentador aos tratamentos. Use pesos corporais como parâmetros para a randomização.
- No dia da injecção, recentemente preparar a solução de monoiodoacetate em solução salina estéril (NaCl a 0,9%) para as concentrações desejadas. Use solução salina estéril para injectáveis num grupo separado de ratinhos de controlo. A dose mais elevada de recomendar MIA é de 1 mg em 10 ul.
Cuidado: Monoiodoacetate é verY tóxico. Portanto, recomenda-se a utilização de luvas e máscara são usados no manuseio do pó e preparar a solução. A solução deve ser esterilizada por filtração com um filtro de 0,22 um. - Anestesiar ratos utilizando um carrinho de anestésico por primeiro colocando-os numa câmara de entrega de 2% de isoflurano em mistura O2 (taxa de fluxo de 1,5 L / min) e, em seguida, transferir os ratos para a secção do nariz do cone, que também proporciona a mistura de 2% de isoflurano-O2 , e como tal, mantém a anestesia durante a injecção. Coloque vet pomada sobre os olhos para evitar a sua secagem sob anestesia. Usar vestido cirúrgico, luvas e máscara durante a realização de procedimento de injeção.
- Confirmar anestesia, verificando a falta de resposta a um estímulo de aperto sobre as patas traseiras do animal.
- Uma vez que o animal está sob anestesia, coloque-o em sua parte traseira. Aparar e limpar a área ao redor da articulação do joelho com álcool. Povidona iodo ou cloro-hexidina podem ser utilizados, assim como fou desinfecção. O tendão patelar (linha branca abaixo da patela) se tornará visível.
- A fim de estabilizar o local de injecção, manter o joelho ainda, numa posição dobrada, colocando o dedo indicador sob a articulação do joelho e o polegar sobre a superfície anterior da articulação do tornozelo. preferência conjunta não é necessária.
- Para localizar o local exacto de injecção, executa uma agulha 26 G ligada a uma seringa na horizontal ao longo do joelho (de modo a não perfurar a pele com a ponta) até encontrar a diferença abaixo da patela. Aplique uma leve pressão para marcar a área e, em seguida, levante a agulha e seringa verticalmente para a injecção. Inserir a agulha na área marcada, através do tendão patelar, perpendicular à tíbia. Sem resistência deve ser sentida.
- Use polegar como um guia e injectar superficial relativamente ao local de entrada. Após a injeção, massagear o joelho para assegurar uma distribuição uniforme da solução. Descarte a agulha imediatamente na afiadas bin.
- Coloque os ratos de volta em uma gaiola limpa em uma esteira aquecida e permitir-lhes para se recuperar. Manter uma vigilância constante sobre os animais até que recupere a consciência adequado, que é medido por eles recuperar decúbito esternal. Quando os animais são recuperados, voltar para sua gaiola.
Nota: Sugere-se para as melhores práticas e formação finalidades que um corante é usado e imediata dissecção post-mortem realizados para confirmar a localização correta da injeção.
2. Medição da Mecânica de hipersensibilidade (alodinia)
Nota: os limiares de retirada mecânica estática são avaliadas através da aplicação de filamentos de von Frey na superfície plantar da pata traseira.
- Traga ratos para o quarto comportamental e deixar os animais sem restrições aclimatar em cubículos acrílicos (8 cm x 5 cm x 10 cm) em cima de uma grade de malha de arame.
- Trem ratos por manuseio e habituação 2 horas para as celas para dois dias antes da aplicação cabelos von Frey, a fimpara limitar o stress e deambulação durante a aplicação dos cabelos de von Frey. No dia do teste, os animais habituar aos compartimentos para até 60 minutos antes do teste. Usar vestidos, luvas e máscaras durante todos os experimentos comportamentais.
- Aplicar cabelos de von Frey calibrados (fibras de nylon flexível de diâmetro crescente que exercem os níveis de força definida como calibrado pela empresa fabricante e expressou-se em gramas (g)) à superfície plantar da pata traseira até que as curvas de fibra. Use 0,008, 0,02, 0,04, 0,07, 0,16, 0,4, 0,6, e 1,0 g de fibras durante o teste.
- Mantenha cada cabelo no lugar durante 3 segundos ou até a pata for retirada, este último definindo uma resposta positiva. Começando com uma força de estímulo de 0,07 g, aplicar cabelos de acordo com o "método de cima para baixo" 21: marca como X uma resposta de retirada e O uma ausência de resposta. Aplicar em ordem crescente de força, até 1 g (força de corte), até que uma resposta seja detectado.
- Re-testar a pata, repetindoo passo 2.2.1, começando com o filamento, que exerce uma força inferior a um, que produziu uma retirada.
- Em seguida, aplique os filamentos restantes sequencialmente, pela força descendente, até que ocorra nenhuma retirada. Reaplicar filamentos em ordem crescente até que uma resposta é observada. Continuar até que uma sequência de seis respostas é obtido (por exemplo, OXOXOX), a fim de obter o valor "K", referindo-se os valores de tabela 21.
- Expressar os valores de retirada da pata 50% limiares de retirada da pata em gramas. Utilizar a fórmula (10 [δ Xr + K]) / 10000 em que Xr = valor do último filamento de von Frey utilizado em sequência (em unidades log), k = valor tabular, e δ = diferença média em forças entre as fibras. Sempre que for detectada nenhuma resposta, utilizar a resposta máxima de 1 g 21,22.
- Seguindo o procedimento descrito acima (2.2.1-2.2.4), avaliar os limiares mecânicos de ambas as patas traseiras antes MIA injection como valores de linha de base. Após a injecção, avaliar os limiares de as patas ipsilateral e contralateral em intervalos regulares dia durante várias semanas após MIA para averiguar o desenvolvimento de alodinia mecânica.
Nota: Por exemplo, nós relatamos limiares medidos 0, 3, 5, 7, 10, 14, 21 e 28 dias após a injecção de MIA. Animais são considerados alodínico quando eles exibem uma resposta de 0,1 g ou menos. respostas normais são abrangidos 0,6 - Faixa 1 g.
3. Medição da Déficit de suporte de peso
Nota: As alterações na capacidade de peso são medidos utilizando um testador de peso incapacitance.
- Treinar cada mouse para andar em uma câmara de Plexiglass em cima do aparelho e sentar-se na caixa de exploração. Posicione o mouse na frente da caixa de exploração, levantar a entrada até 45 °, e permitir que o mouse para entrar e fechar a caixa. Permitir que os animais se desloquem livremente até que adotar uma postura sentada. Este treinamento leva pelo menos dois dias e garante que o animal ainda e não é leaning em ambos os lados da câmara. Calibrar o aparelho antes da utilização, com um peso de verificação de 100 g (ou de acordo com instruções do equipamento).
- Certifique-se de que cada pata traseira é colocado na plataforma de gravação apropriado 11. A duração de cada medição é de 1 segundo, de acordo com as instruções do fabricante.
- Recolha três medições do peso suportado em cada pata traseira do bloco de gravação para cada sessão de gravação e usar o valor médio para calcular a diferença de peso suportado pelo patas ipsilateral e contralateral. valores expressos como a diferença entre as patas contralateral e ipsilateral em gramas.
- Avaliar peso rolamento alterações antes da injecção MIA como valores basais. Em seguida, as avaliações repetidas em intervalos regulares ao longo de várias semanas para averiguar o desenvolvimento de mudanças de portão. Por exemplo, nós relatamos limiares medidos em 0, 3, 5, 7, 10, 14, 21 e 28 dias após a injecção de MIA.
Nota: Um peso normal bvalor earing de 50% representa uma distribuição de peso igual em hindlimb ipsilateral e contralateral. Animais considerados exibição hipersensíveis um rolamento de peso mudança de aproximadamente 45%. Medições de limiares mecânicos e défices de peso do rolamento pode ser realizada da mesma ratinhos, como nem o ponto final afecta o outro. Para a avaliação farmacológica, cada grupo de animais devem ser testados em conjunto vezes após a administração em linha com o perfil farmacocinético do composto utilizado.
Resultados
Temos relatado recentemente que a injecção de 0,5-1 mg MIA nos induz conjuntos rato joelho referida hipersensibilidade mecânica (alodinia) na pata posterior ipsilateral e rolamento de peso déficits para até 4 semanas, embora latências são 23 dose-dependente.
Os dados apresentados na Figura 1 constitui um exemplo do decurso de tempo de hipersensibilidade mecânica induzida por MIA nas patas traseiras ipsilaterais na sequência de uma gama de doses injectadas no joelho. Especificamente, a dose mais baixa de MIA (0,5 mg / murganho) induziu um decréscimo de 50% de limiares em comparação com a de injecção de soro fisiológico no dia 10, e os limiares diminuiu para 70% daqueles dos controlos de solução salina por dia 28 após a injecção. A dose intermédia de 0,75 mg de MIA resultou num decréscimo gradual em limites que foram 80% inferiores aos limites de controlo de solução salina no dia 10 e manteve-se baixa até ao dia 28. A dose mais elevada de 1 mg MIA foi associado com um sinalgota ificant no limiar no dia 5 e uma redução ainda maior no dia 10, que foi mantido até ao dia 28.
Os dados apresentados na Figura 2 fornecem exemplos de mudanças de peso do rolamento que estão associados com a injecção MIA nas articulações do joelho. Neste conjunto de experiências, enquanto que a dose de 0,5 mg MIA não induziu alterações significativas no peso de rolamento durante toda a duração de 28 dias do estudo, a 0,75 mg de dose MIA resultou numa redução significativa do peso suportado pela pata ipsilateral do dia 10 em diante. Notavelmente, rolamento de peso assimetria associada com 0,75 mg de MIA pode produzir resultados variáveis e inconsistentes entre os estudos 23. Em vez disso, a dose de 1 mg MIA geralmente induz peso reprodutível rolamento assimetria e os dados na Figura 2, demonstram uma redução significativa do peso suportado na pata traseira ipsilateral do dia 3 até ao final do período de observação. Como esperado, salianimais tratados com ne não mostrou rolamento de peso mudanças.
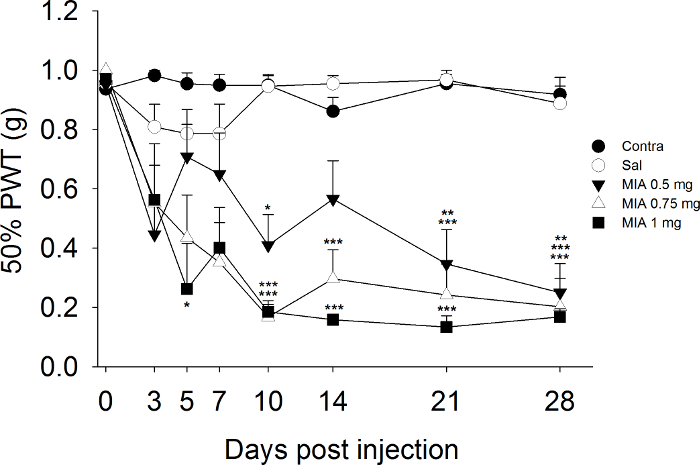
Figura 1. Desenvolvimento de alodinia mecânica Pós MIA Injection. Limiares de retirada da pata das patas traseiras ipsilateral e contralateral foram avaliadas antes e após a injeção de MIA (0,5, 0,75 e 1 mg / mouse) e soro fisiológico (NaCl 0,9%), n = 8 - 10 ratinhos / grupo. * P <0,05, ** P <0,01, *** P <0,001 versus grupo tratado com solução salina; Two-way medições repetidas ANOVA seguido de Student Newman-Keuls post hoc teste. Por favor clique aqui para ver uma versão maior desta figura.
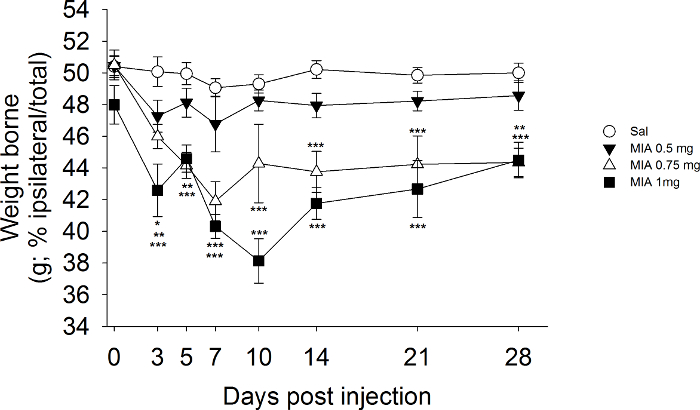
Figura 2. Desenvolvimento de Déficit de suporte de pesoInjeção s Pós MIA. Mudanças na distribuição de peso corporal entre os dois membros posteriores foram calculadas como [(peso suportado em ipsilateral pata / soma do peso suportado nas patas ipsilateral e contralateral) * 100] foram avaliadas antes e após a injeção de MIA ( 0,5, 0,75, e 1 mg / ratinho) e solução salina (NaCl a 0,9%), n = 8 - 10 ratos / grupo. * P <0,05, ** P <0,01, *** P <0,001 versus grupo tratado com solução salina. Two-way medições repetidas ANOVA seguido de Student Newman-Keuls post hoc teste. Por favor clique aqui para ver uma versão maior desta figura.
Discussão
Com esta metodologia, nós descrevemos um método preferido para a indução de dor OA, como no rato por uma injecção intra-articular de MIA numa articulação do joelho e avaliação da sensibilidade a estímulos não nocivos e tóxicos nos membros posteriores. injeção de MIA está associada com o comportamento da dor persistente, ou seja alterado o peso dos membros posteriores rolamento e desenvolvimento de hipersensibilidade mecânica referido (alodinia). Tais medições estáticas podem ser complementadas por análise de marcha em uma esteira ou por análise de passarela em animais que se movem livremente. Modelos MIA são sensíveis a terapias convencionais para aliviar a dor 24, o que indica que eles podem ser úteis para discernir abordagens terapêuticas. Embora a injecção de MIA não é tecnicamente difícil, a cápsula da articulação podem ser perfuradas durante a injecção, resultando em derrame de MIA fora da cápsula, e subsequente incapacidade para induzir toxicidade dos condrócitos. Na verdade, injeção sistêmica de MIA pode ser fatal em roedores umand possíveis efeitos de MIA em tecidos que não sejam os condrócitos células podem confundir os resultados, além de ser indesejável. Como tal, deve sublinhar-se que um grande cuidado deve ser dada para a injecção de MIA, uma vez que é um componente crítico do modelo, e confiança deve ser dada a injecção ocorre para o espaço articular. Este protocolo ajuda a conseguir isso.
Os protocolos aqui descritos destinam-se a garantir que os animais proporcionam respostas de dor-like consistentes durante todo o período de teste. Além disso, eles permitem o ajuste da gravidade da doença por alteração da dose de MIA utilizado para induzir a patologia 15,23. A rápida indução de ambos estado de doença e comportamento de dor-como permitir a avaliação oportuna de compostos modificadores da dor. Isto é vantajoso em relação existente cirúrgica e espontaneamente o desenvolvimento de modelos de OA, que podem levar um longo período de tempo para se desenvolver a hipersensibilidade. Além disso, particularmente para os modelos espontâneos, a doença PatholO logia não manifestar-se em todos os animais (aproximadamente 20 - 80% 7), enquanto que o modelo de MIA está associada com incidência significativa de respondedores. Além disso, os modelos espontâneos não são adequados para medições de mudanças na sustentação de peso, como a OA desenvolve-se em ambos os joelhos. Ao considerar as medidas comportamentais, os animais devem ser mantidos calmo e relaxado durante as avaliações. Isto é conseguido, conforme detalhado no protocolo, pela formação inicial antes de medidas de gravação e pela manipulação repetitiva, que permite animais para se familiarizar com o experimentador. Um ponto chave para reduzir o stress é usar o mesmo experimentador para o teste comportamental todo, como a mudança constante irá induzir os problemas anteriormente mencionados. Como qualquer modelo, o modelo de MIA da OA traz limitações, tais como a rapidez de interrupção conjunto, que não se assemelha o lento desenvolvimento da patologia OA em pacientes. Uma maneira de superar este problema seria para complementar este modelo com um sumodelo rgical da OA. A utilização do modelo químico de MIA em desenvolvimento composto permite a utilização de protocolos preventivos e terapêuticos sobre o desenvolvimento e manutenção da dor OA semelhante. Finalmente, o modelo MIA irá complementar os estudos de características fenotípicas de ratos knock-out, ajudando a entender melhor a doença OA.
Divulgações
None of the authors have competing interests or conflicting interests.
Agradecimentos
JSV é apoiado por uma bolsa de colaboração para MM pela Comissão Europeia (GAN 603191-PAINCAGE).
Materiais
| Name | Company | Catalog Number | Comments |
| Monoiodoacetate | Sigma-Aldrich | I-2512-25G | ≥ 98% purity |
| 0.9% Saline | Mini-Plasco basic | 365 4840 | |
| Isoflurane | Merial | DNI 4090/1 | |
| 26 G Needle | Fisher Scientific | 12947606 | |
| 50 μl Hamilton Syringe | Sigma-Aldrich | 20701 | |
| Von Frey Hairs | Linton Instruments | NC 122775-99 | |
| Incapacitance tester | Linton Instruments | Delivery on Request | |
| Testing Cage Rack | Ugo Basile | 37450 | |
| Compact Anesthetic system | Vet-Tech | AN001B | |
| Medical O2 | BOC | 101-F | |
| Aldasorbers | Vet -Tech | AN006A |
Referências
- Farrell, M., Gibson, S., McMeeken, J., Helme, R. Pain and hyperalgesia in osteoarthritis of the hands. J. Rheumatol. 27 (2), 441-447 (2000).
- Kuni, B., Wang, H., Rickert, M., Ewerbeck, V., Schiltenwolf, M. Pain threshold correlates with functional scores in osteoarthritis patients. Acta. Orthop. 86 (2), 215-219 (2015).
- Wylde, V., Hewlett, S., Learmonth, I. D., Dieppe, P. Persistent pain after joint replacement: prevalence, sensory qualities, and postoperative determinants. Pain. 152 (3), 566-572 (2011).
- Wylde, V., Palmer, S., Learmonth, I. D., Dieppe, P. Test-retest reliability of Quantitative Sensory Testing in knee osteoarthritis and healthy participants. Osteoarthr. Cartil. 19 (6), 655-658 (2011).
- Hunter, D. J. Pharmacologic therapy for osteoarthritis--the era of disease modification. Nat. Rev. Rheumatol. 7 (1), 13-22 (2011).
- Lampropoulou-Adamidou, K., et al. Useful animal models for the research of osteoarthritis. Eur. J. Orthop. Surg. Traumatol. 24 (3), 263-271 (2014).
- Yamamoto, K., Shishido, T., Masaoka, T., Imakiire, A. Morphological studies on the ageing and osteoarthritis of the articular cartilage in C57 black mice. J. Orthop. Surg. (Hong Kong). 13 (1), 8-18 (2005).
- Huebner, J. L., Hanes, M. A., Beekman, B., TeKoppele, J. M., Kraus, V. B. A comparative analysis of bone and cartilage metabolism in two strains of guinea-pig with varying degrees of naturally occurring osteoarthritis. Osteoarthr. Cartil. 10 (10), 758-767 (2002).
- Thysen, S., Luyten, F. P., Lories, R. J. Targets, models and challenges in osteoarthritis research. Dis Model Mech. 8 (1), 17-30 (2015).
- Longo, U. G., et al. Osteoarthritis: new insights in animal models. Open. Orthop. J. 6, 558-563 (2012).
- Bove, S. E., et al. Weight bearing as a measure of disease progression and efficacy of anti-inflammatory compounds in a model of monosodium iodoacetate-induced osteoarthritis. Osteoarthr. Cartil. 11 (11), 821-830 (2003).
- Pomonis, J. D., et al. Development and pharmacological characterization of a rat model of osteoarthritis pain. Pain. 114 (3), 339-346 (2005).
- Schuelert, N., McDougall, J. J. Grading of monosodium iodoacetate-induced osteoarthritis reveals a concentration-dependent sensitization of nociceptors in the knee joint of the rat. Neurosci. Lett. 465 (2), 184-188 (2009).
- Vonsy, J. L., Ghandehari, J., Dickenson, A. H. Differential analgesic effects of morphine and gabapentin on behavioural measures of pain and disability in a model of osteoarthritis pain in rats. Eur. J. Pain. 13 (8), 786-793 (2009).
- Im, H. J., et al. Alteration of sensory neurons and spinal response to an experimental osteoarthritis pain model. Arthritis Rheum. 62 (10), 2995-3005 (2010).
- Sabri, M. I., Ochs, S. Inhibition of glyceraldehyde-3-phosphate dehydrogenase in mammalian nerve by iodoacetic acid. J. Neurochem. 18 (8), 1509-1514 (1971).
- van der Kraan, P. M., Vitters, E. L., van de Putte, L. B., van den Berg, W. B. Development of osteoarthritic lesions in mice by 'metabolic' and 'mechanical' alterations in the knee joints. Am. J. Pathol. 135 (6), 1001-1014 (1989).
- Guingamp, C., et al. Mono-iodoacetate-induced experimental osteoarthritis: a dose-response study of loss of mobility, morphology, and biochemistry. Arthritis Rheum. 40 (9), 1670-1679 (1997).
- Janusz, M. J., et al. Moderation of iodoacetate-induced experimental osteoarthritis in rats by matrix metalloproteinase inhibitors. Osteoarthr. Cartil. 9 (8), 751-760 (2001).
- Marker, C. L., Pomonis, J. D. The monosodium iodoacetate model of osteoarthritis pain in the rat. Methods Mol. Biol. 851, 239-248 (2012).
- Chaplan, S. R., Bach, F. W., Pogrel, J. W., Chung, J. M., Yaksh, T. L. Quantitative assessment of tactile allodynia in the rat paw. J. Neurosci. Methods. 53 (1), 55-63 (1994).
- Dixon, W. J. Efficient analysis of experimental observations. Ann. Rev. Pharmacol. Toxicol. 20, 441-462 (1980).
- Ogbonna, A. C., Clark, A. K., Gentry, C., Hobbs, C., Malcangio, M. Pain-like behaviour and spinal changes in the monosodium iodoacetate model of osteoarthritis in C57Bl/6 mice. Eur. J. Pain. 17 (4), 514-526 (2013).
- Fernihough, J., Gentry, C., Malcangio, M., Fox, A., Rediske, J., Pellas, T., Kidd, B., Bevan, S., Winter, J. Pain related behaviour in two models of osteoarthritis in the rat. Pain. 112 (1-2), 83-93 (2004).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados