Method Article
Definido e Geração de Scalable de células de hepatócitos-like de células-tronco pluripotentes humanas
Neste Artigo
Resumo
O método aqui apresentado descreve um sistema de diferenciação -Ready escalável e boas práticas de fabrico (BPF) para gerar células de hepatócitos-like humanos a partir de células-tronco pluripotentes. Ele serve como um sistema eficaz e padronizado para gerar células de hepatócitos-like humanos para a pesquisa básica e aplicada fígado humano.
Resumo
células-tronco pluripotentes humanas (hPSCs) possuem grande valor para a investigação biomédica. hPSCs pode ser dimensionado e diferenciada a todos os tipos de células encontradas no corpo humano. A diferenciação das células para hPSCs de hepatócitos humanos (como-HLCS) tem sido extensivamente estudado, e protocolos de diferenciação eficientes foram estabelecidas. A combinação de matriz extracelular e os estímulos biológicos, incluindo factores de crescimento, citoquinas, e as moléculas pequenas, tornaram possível para gerar HLCS que se assemelham a hepatócitos humanos primários. No entanto, a maioria dos procedimentos ainda empregam componentes indefinidos, dando origem a variações de lote para lote. Este serve como uma barreira significativa para a aplicação da tecnologia. Para resolver esta questão, desenvolvemos um sistema definido para a diferenciação de hepatócitos usando lamininas recombinantes humanos como matrizes extracelulares, em combinação com um processo de diferenciação sem soro. Altamente especificação hepatócito eficiente foi alcançada, com detrado melhorias tanto na função HLC e fenótipo. Importante, este sistema é fácil de escalar usando pesquisa e GMP-grade HPSC linhas avanços promissores na modelagem e terapias à base de células.
Introdução
tecido humano primário e os tipos de células derivados são usados regularmente, tanto para a triagem baseada em células e na clínica. No entanto, o acesso a essas células é severamente limitada devido à insuficiente doação de órgãos e perda de fenótipos celulares pós-isolamento 1. hPSCs representam uma alternativa promissora para o tecido primária e facilitar a geração de células somáticas humanas geneticamente definidas e renováveis. células de hepatócitos-like (HLCS) derivadas de hPSCs já mostraram promessa neste campo. HLCS assemelhar-se hepatócitos primários humanos em vários aspectos, incluindo a morfologia celular, a expressão do gene do hepatócito, a função metabólica e sensibilidade a drogas e vírus 2, 3, 4, 5, 6, 7, 8. Além disso, a proliferação ilimitada ecapacidade de auto-renovação de ambos os hPSCs pesquisadores e GMP-grade facilita a sua aplicação 9, 10.
Mais de uma década de pesquisa tem produzido um número de hepatócitos eficiente procedimentos de diferenciação 2, 3, 5, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20. No entanto, a maioria destes sistemas utilizam componentes indefinidos e / ou a transdução virai para conduzir especificação hepatocelular. Para melhorar a fiabilidade da tecnologia em escala, é importante desenvolver uma diferenciação de hepatócitos robustasistema que é verdadeiramente definido e livre de xeno, e GMP-compatível.
As lamininas (LNs) são importantes proteínas da matriz extracelular que podem influenciar a adesão celular, proliferação, migração, e diferenciação. As lamininas são glicoproteínas heterotriméricas compostas de um α, um β, e uma cadeia γ. Recentemente, lamininas humanos recombinantes foram produzidos e utilizados em biologia celular. LN-511 foi mostrada para apoiar a manutenção da hPSCs 21, enquanto uma mistura de LN-521 e E-caderina permite derivação clonal e a expansão de células estaminais embrionárias humanas 22. LN-111, por outro lado, suporta a manutenção de células-hepatoblast como derivados de hPSCs 23. No entanto, antes do nosso relatório, lamininas 521 e 111 não tinham sido utilizados para gerar HLCS com características maduras a partir hPSCs 10.
Aqui, os procedimentos detalhados para a cultura hPSCs no LN-521e diferenciando-as em ambos os LN-521 ou uma mistura de LN-521 e LN-111 (LN-521 / LN-111). Nós otimizamos o protocolo de diferenciação usando semeadura de uma única célula para gerar uma monocamada altamente reprodutível e homogénea de HLCS em vários formatos 14. Acreditamos que o nosso sistema de diferenciação definido representa um método simples e de baixo custo para a fabricação de HLCS ativas para aplicação, o que representa um avanço significativo no campo.
Protocolo
NOTA: informações do fornecedor para todos os reagentes utilizados neste protocolo foi listado na Tabela 1. Todos os meios de comunicação / placas deve ser estéril e, pelo menos, à temperatura ambiente quando as células estão a ter contato direto com eles.
1. Passaging pluripotentes humanas Células-Tronco (hPSCs) sobre laminina 521
NOTA: O procedimento passaging celular descrito abaixo é baseado em células individuais e é ideal para a derivação de uma população homogênea de células de hepatócitos-like de hPSCs. Colony chapeamento é também aplicável e tenha sido descrito anteriormente 24.
- Prepare a placas revestidas com laminina, conforme necessário.
- Descongelar o estoque de 100 ug / ml de laminina recombinante 521 (LN-521) a 4 ° C.
- Dilui-se a descongeladas LN-521 em gelo-frio 1x DPBS (com Ca2 + / Mg2 +) para fazer uma solução a 5 jig / mL.
- Adicionar 1 mL de 5 ug / ml-521 LN solução para revestir uma cavidade de uma placa de 6 poçose rock para espalhar uniformemente no poço.
- Incubam-se as placas num banho a 37 ° C / 5% de CO 2 incubadora de cultura de células durante 2 - 4 horas para uso urgente ou em um 4 ° C frigorífico durante a noite.
- Armazenar as placas revestidas com laminina num frigorífico a 4 ° C conforme necessário. Manter as placas sobre uma superfície plana e selá-los para evitar a evaporação e a contaminação.
NOTA: Nunca deixe os poços revestidos secar; carregá-las com adicional 1x DPBS (com Ca 2+ / Mg 2+), se necessário. Use as placas dentro de 2 semanas.
- Permitir que o número necessário de placas pré-revestidas para alcançar a temperatura ambiente antes da sua utilização ou incubar as placas a 37 ° C durante 0,5-1 h.
- Aspirar cuidadosamente a solução de revestimento LN-521 sem danificar a superfície revestida. Nota: É crítico para não danificar a superfície revestida antes de semear as células nele.
- Imediatamente adicionar 1 mL de meio de pré-aquecido suplementado com mTeSR1-quinase 10 uM Rho-associado (ROCHA) Y2 inibidor7632 para um poço de uma placa de 6 poços. Deixar a placa na incubadora de cultura de células para receber células.
NOTA: Nunca permita que os poços revestidos com laminina para secar. - Aspirar o meio de hPSCs bem mantida a cerca de 75% a 85% de confluência. Lavam-se as células a partir de um poço de uma placa de 6 poços uma vez com 1 mL de temperatura ambiente 1x DPBS (sem Ca2 + / Mg2 +).
- Adicionar 0,5 mL de 1x Accutase às células e incuba-se a 37 ° C durante 6-8 minutos para dissociar as células.
NOTA: Para verificar se a digestão é longo o suficiente ou não, bata suavemente a placa e verificar se as células podem desprender facilmente. Se sim, então é hora de parar a reacção enzimática; se não, estender a digestão para um extra de 1-2 min. - Terminar a dissociação por adição de 2 ml de meio fresco suplementado com mTeSR1 10 uM Y27632 para as células. Pipeta cima e para baixo usando uma ponta P1000 várias vezes para fazer uma suspensão de uma única célula.
- Contar as células viáveis utilizando um hemocitômetro.Use Trypan Blue a mancha e excluir as células mortas 14
- Calcular o número total de células necessárias. Para Passaging HPSC rotina, Seed 4 x 10 5 a 5 x 10 5 células por poço de uma placa de 6 poços (isto é, 4,21 x 10 4-5,26 x 10 4 por cm 2). Para passaging hPSCs para a diferenciação de hepatócitos, semear 6,5 x 10 5 a 7,5 x 10 5 (isto é, 6,84 x 10 4 7,89 x 10 a 4 por cm 2) células por poço de uma placa de 6 poços.
NOTA: A densidade de semeadura para cada linha de células pode precisar otimização mínima com base na densidade empírica dada aqui para a diferenciação hepática. - Transferir a suspensão de célula necessária para uma solução estéril de 15 mL ou 50 mL tubo de centrífuga e centrifugar a 115 xg durante 3 minutos à temperatura ambiente.
- Aspirar o sobrenadante lentamente e em seguida ressuspender o sedimento de células em meio fresco, quente mTeSR1 suplementado com 10 uM quinase Rho-associado (ROCHA) inhibitoR Y27632, utilizando um meio adequado para tornar a densidade de células desejada.
NOTA: O uso de inibidor ROCHA é altamente recomendado, a fim de melhorar a aderência celular e taxa de sobrevivência. - Semear as células às placas preparadas e rock-los frente e para trás e para os lados para distribuir uniformemente as células.
NOTA: É fundamental para assegurar que as células são distribuídas uniformemente nos poços se a placa é para cultura de células de rotina ou experimentação diferenciação de hepatócitos. - Colocar as placas na incubadora de células e manter as células a 37 ° C / 5% de CO 2 durante 24 h para lhes permitir ligar e recuperar.
- Examinar as células no dia seguinte e retirar inibidor ROCHA se o contato célula-célula foi estabelecida. Manter as células em meio mTeSR1 para a cultura de rotina ou mudar para o meio de diferenciação, conforme necessário.
NOTA: Se as células foram semeadas com a densidade mencionado, a confluência deve ser ideal para a manutenção de rotina ou differentiatio hepatócitosn.
2. Diferenciar hPSCs a células de hepatócitos-like sobre recombinantes lamininas
- Prepare meio de diferenciação.
- Adicione solução estoque a activina A humana: Activina humana dissolver-se um pó para fazer uma solução estoque / ml 100 ug de albumina de soro bovino estéril 0,2% (BSA) / DPBS. Fazer pequenas alíquotas e armazená-las a -20 ° C. Use a 1: 1.000.
- Faça rato Wnt solução de 3a: dissolver rato Wnt 3a pó para fazer uma solução estoque / mL 10 ug em estéril 0,2% BSA / DPBS. Fazer pequenas alíquotas e armazená-las a -20 ° C. Use a 1: 200.
- Adicione solução de factor de crescimento de hepatócitos humanos (HGF): dissolver pó de HGF humano para fazer uma solução estoque / ml 10 ug em estéril 0,2% de BSA / DPBS. Fazer pequenas alíquotas e armazená-las a -20 ° C. Use a 1: 1.000.
- Adicione solução de oncostatina M (OSM): dissolver a oncostatina M (OSM) pó para fazer uma solução estoque / ml 20 ug em estéril 0,2% de BSA / DPBS. Faça pequenas alíquotas e srasgou-se a -20 ° C. Use a 1: 1.000.
- Adicione 500 mL de meio de escorvamento da endoderme: 2% de suplemento B27 (50x, menos a vitamina A) e 1% de penicilina / estreptomicina (concentrações finais a 100 UI / mL e 100 ug / ml, respectivamente); topo até 500 mL usando Roswell Park Memorial Institute 1640 (RPMI 1640) meio basal. NOTA: Guarde o estoque a 4 ° C e usar dentro de duas semanas. forma aliquota do estoque e adicionar fresco (concentrações finais de 100 ng / mL e 50 ng / mL, respectivamente) e Activina A Wnt 3a em cada mudança de meio.
- Adicione 500 mL de meio / DMSO diferenciação KSR: 80% Knockout DMEM (KO-DMEM), 20% de substituição de soro nocaute (KSR), 0,5% GlutaMAX, 1% de aminoácidos não essenciais (NEAA), 0,1 mM de beta-mercaptoetanol, 1% de DMSO e 1% de penicilina / estreptomicina (concentrações finais a 100 UI / mL e 100 ug / ml, respectivamente). Filtrar sob vácuo. Armazenar a 4 ° C e utilizar no prazo de duas semanas.
- Adicione 500 ml de meio de maturação HepatoZYME: 1% GlutaMAX, 10 pM hidrocortisona sal 21-hemi-succinato de sódio (HCC), e 1% de penicilina / estreptomicina (concentrações finais a 100 UI / mL e 100 ug / ml, respectivamente); topo até 500 mL usando HepatoZYME meio basal. NOTA: Guarde o estoque a 4 ° C e usar dentro de duas semanas. forma aliquota do estoque e adicionar HGF fresco e OSM (concentrações finais de 10 ng / mL e 20 ng / mL, respectivamente) para cada mudança de meio.
- hPSCs de semente, para diferenciação de hepatócitos no LN-521, como descrito na secção 1. Se LN-521 / LN-111 é para ser utilizado como o substrato, revestir as placas com LN-521 e LN-111 (1: 3) em a concentração laminina final de 5 ug / ml; o resto tratamento deve ser o mesmo que placas LN-521-revestidos puros.
NOTA: LN-521 / LN-111 não é o ideal para a cultura de rotina de hPSCs; ela só é usada para experimentos de diferenciação. - Verifique a confluência celular 24 h após a semeadura. Iniciado diferenciação celular uma vez que a confluência celular alcança cerca de 40%. Retirar o meio mTeSR1 passado e adicionar meio-aspirante endoderme fresco suplementado com 100 ng / mL Activina A e 50 ng / mL Wnt 3a. Ligue para este dia diferenciação 1.
NOTA: É altamente recomendável para iniciar a diferenciação do dia após a semeadura das células. - Mudar o meio-aspirante endoderme a cada 24 h, durante 3 dias para as células-tronco embrionárias humanas (hESCs). Quanto às células-tronco pluripotentes induzidas pelo homem (hiPSCs), estender este estágio por mais 2 dias para preparar as células para células da endoderme-como definitivos, mas usar o meio-aspirante endoderme suplementado apenas com 100 ng / mL Activina A para estes dois dias 12 .
NOTA: Para assegurar especificação endoderme bem sucedida, pode-se examinar a expressão dos marcadores da endoderme, como Foxa2 e Sox17. De acordo com a coloração por imunofluorescência, mais de 80% das células derivadas são positivas para ambos os marcadores em nosso laboratório. - Mudar para médio KSR / DMSO diferenciação no dia 4 (para hESCs) / dia 6 (para hiPSCs). Mudar o meio dAily para os primeiros 3 dias e, em seguida, no quinto dia deste estágio de diferenciação.
NOTA: Não é necessária alimentação no quarto dia deste estágio de diferenciação. Use não suplementado KO-DMEM para lavar as células de uma vez antes da mudança de meio, se há muitas células mortas. Para verificar se a diferenciação para esta fase for bem sucedida ou não, pode-se testar a expressão de marcadores de células progenitoras hepáticas, como a AFP, CK19, e HNF4A. Cerca de 90% das células será positivo para estes marcadores com base na nossa experiência. - Após 5 dias de o estágio de diferenciação KSR / DMSO, mude para o estágio de maturação HepatoZYME. Lave as células uma vez com meio basal HepatoZYME simples após remoção do meio KSR / DMSO. Adicionar HepatoZYME maturação meio suplementado com 10 ng / mL de HGF e 20 ng / ml OSM.
- Mudar o meio a cada 48 h durante 7 - 10 dias, altura em que as células estão prontas para a caracterização do padrão ou utilização posterior.
NOTA: exames expressão do marcador de hepatócitos, metabólicasOs testes de função (como a atividade do citocromo P450), uréia e testes de secreção de albumina, testes de armazenamento de glicogênio, e os testes de absorção de indocianina verde (ICG) são métodos de caracterização típicos.
NOTA: A linha do tempo do protocolo de diferenciação é mostrado na Figura 5. Em nosso laboratório, nós rotineiramente verificar os níveis dos HLCS derivados específicos de hepatócitos expressão do marcador, a secreção de albumina e do citocromo P450 (CYP) 3A e 1A2 atividade.
Resultados
Diferenciação hepatocelular de hPSCs
Uma linha humana embrionária das células estaminais, H9, e uma linha de células-tronco pluripotentes induzidas pelo homem, 33D6, foram utilizados para a diferenciação de hepatócitos. Os resultados nas figuras 1-3 são a partir de células H9, ao passo que aqueles na Figura 4 são células de 33D6. células individuais semeadas em lamininas estabeleceu contato célula-célula após 24 h. Após as células atingiram cerca de 40% de confluência, o processo foi iniciado diferenciação (Figura 1A e Figura 4A). Em lamininas (ambos LN-521 e LN-521 / LN-111), estas células passaram por alterações morfológicas sequenciais e deu origem a HLCS polarizados (Figura 1 e Figura 4A).
Hepatócito-like Caracterização celular
day 18 HLCS foram recolhidas e avaliadas quanto à expressão de marcadores de hepatócitos representante, HNF4A e ALB (Figura 2A). A imunocoloração de dia 18 HLCS mostrou que cerca de 90% das células expressaram HNF4α (Figura 2B). Estas células polarizadas lamininas e exibiu uma aparência poligonal, tal como indicada por E-caderina e F-actina expressão (Figura 2B).
P450 atividade (CYP) citocromo também foi avaliado. Os CYP450s realizar uma importante função metabólica dos hepatócitos. Dia 18 HLCS derivados de uma mistura de proteínas, tais como gelatinoso Matrigel, LN-521, LN-521 ou / LN-111, foram testadas para a actividade do CYP3A. HLCS demonstraram significativamente maior a actividade do CYP3A no substratos de laminina que em matrigel (Figura 3). Importante, quando comparado com hepatócitos primários humanos comerciais (HU1339) re-plaqueadas sobre estes substratos, HLCS tem cerca de 10 vezes mais elevados níveisda actividade do CYP3A 10.
A diferenciação de hiPSCs foi semelhante ao de hESCs. As células exibiram alterações sequenciais na aparência (Figura 4A). HLCS derivados expressa um factor de transcrição de hepatócitos chave, HNF4α (Figura 4B), e possuía a actividade do CYP3A e albumina segregada (Figura 4C e D). Notavelmente, HLCS derivados de 33D6 exibida CYP3A reduzida em comparação com as células H9 derivados HLCS (Figura 3), mas ainda era comparável aos hepatócitos humanos primários 10. No entanto, a secreção de albumina dessas HLCS foi muito menor do que em hepatócitos primários 10.
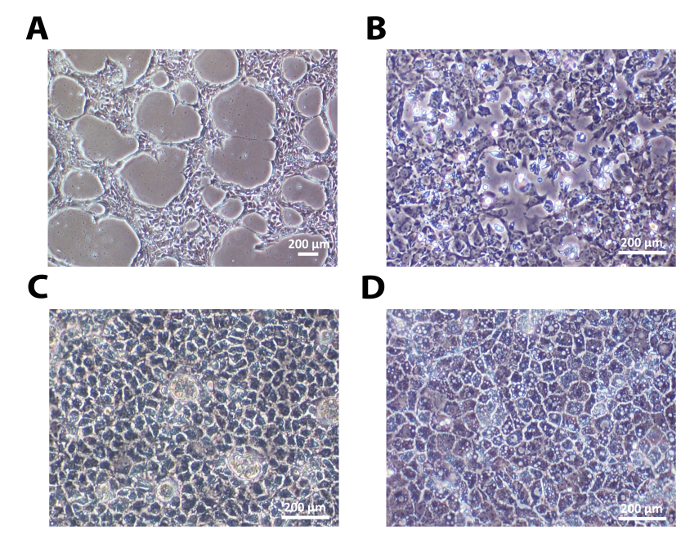
Figura 1: Os sequenciais alterações morfológicas durante hepática Diferenciação. </ strong> (A) hESCs indiferenciadas semeadas como células individuais atingiu cerca de 40% de confluência 24 h após a semeadura. (B) Após o condicionamento, as células exibiram a morfologia típica endodérmico no dia 4. (C) Ao atingir o estágio hepatoblast-like, eles mostraram uma forma poligonal clara no dia 9. (D) Após a fase de maturação, HLCS polarizadas estavam prontos para caracterização adicional mostrado no dia 18. barra de escala = 200 pm. Por favor clique aqui para ver uma versão maior desta figura.
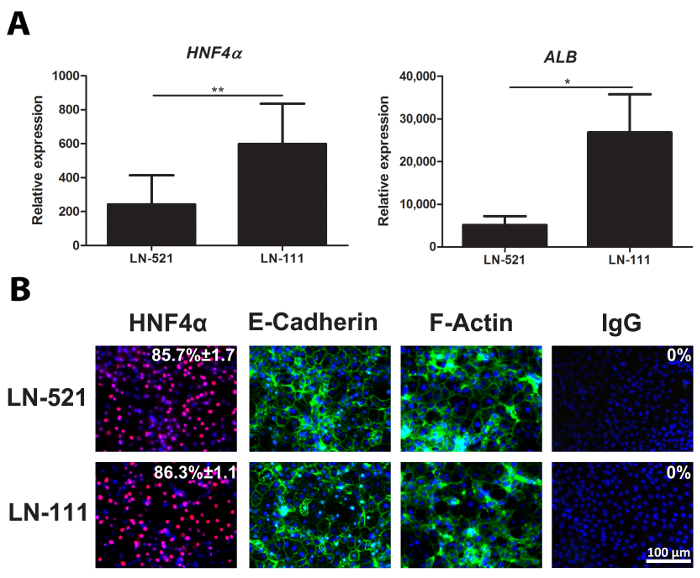
Figura 2: Caracterização de HLCS. (A) A expressão gênica de marcadores específicos de hepatócitos, HNF4A (esquerda) e ALB (direita). O nível de expressão foi analisada usando dia 18 HLCS derivadosde hESCs em ambos LN-521 e LN-521 / LN-111, e foi normalizada para o gene doméstico de GAPDH e expressos relativamente ao hESCs. Os resultados representam três réplicas biológicas, e as barras de erro representam o desvio padrão (DP). * P <0,05, ** p <0,01; teste t não emparelhado. Expressão (B) Proteína de um marcador chave hepática, HNF4α, e marcadores de polarização, caderina-E e F-actina. Dia 18 HLCS sobre LN-521 e LN-521 / LN-111 foram coradas para os marcadores acima e contra-coradas com Hoechst 33342. Um controlo negativo foi efectuada com o correspondente imunoglobulina G (IgG). A percentagem de células positivas e HNF4α-SD é mostrado. Esta foi calculada a partir de quatro campos aleatórios de vista. As imagens foram tiradas com ampliação de 20x. Barra de escala = 100 pm. Por favor clique aqui para ver uma versão maior desta figura.
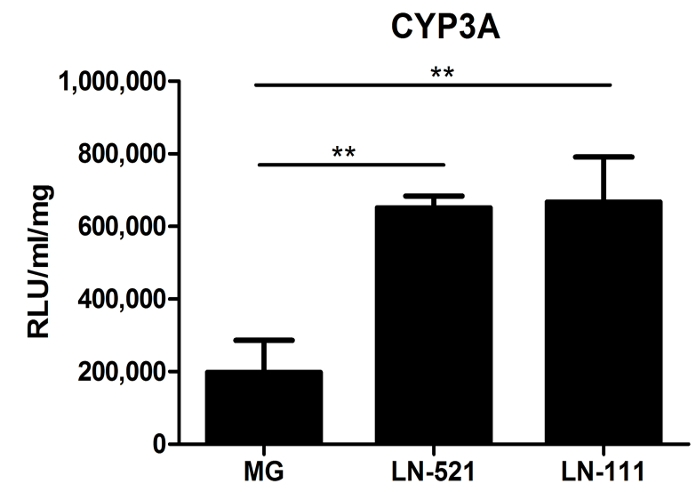
Figura 3: Metabolic Caracterização Função de HLCS. a actividade do citocromo P450 de CYP3A de células cultivadas sobre Matrigel (MG), LN-521, LN-521 ou / LN-111, que foi testado. Os dados representam três repetições biológicas, e as barras de erro representam SD. ** P <0,01; one-way ANOVA com o teste post-hoc de Tukey. Por favor clique aqui para ver uma versão maior desta figura.
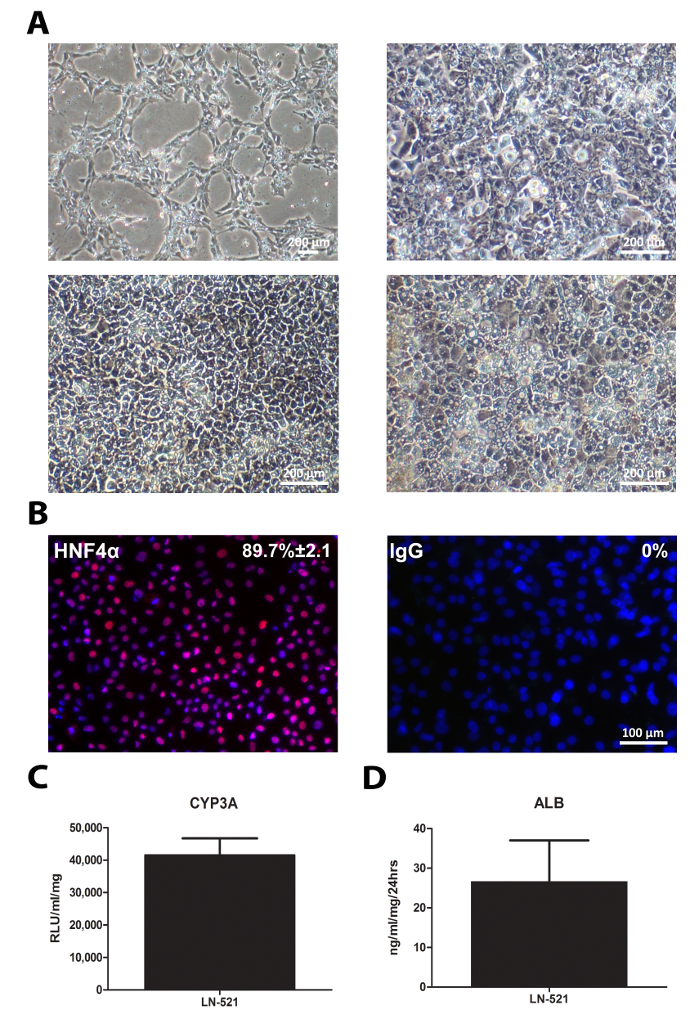
Figura 4: Caracterização padrão de HLCS. hiPSCs cultivadas em LN-521 foram diferenciadas em HLCS. testes normalizados de caracterização foram realizadas no dia 17 HLCS. (A) A morfologia sequencial das células durante a diferenciação hepática; o r pontos de tempo mostrados células epresent nos dias 1, 4, 9 e 17. (B) imunocoloração de expressão HNF4α. A percentagem de células positivas e o DP é mostrado com base em quatro campos aleatórios de vista. As imagens foram tiradas com ampliação de 20x. Barra de escala = 100 pm. Atividade de CYP3A (C) no dia 17 HLCS. Os dados representam seis repetições biológicas, ea barra de erro representa o SD. Secreção (D) Albumina de HLCS derivados ao longo de 24 h em cultura. Os dados representam quatro repetições biológicas, ea barra de erro representa SD. Por favor clique aqui para ver uma versão maior desta figura.

Figura 5: tempo de vida do esquemática do protocolo de diferenciação.t = "_ blank"> Clique aqui para ver uma versão maior desta figura.
Discussão
Para avançar a pesquisa humana de células-tronco pluripotentes e medicina translacional, sistemas livres de xeno que cumprem com as actuais orientações de boas práticas de fabricação são necessários. Chave para qualquer processo de diferenciação é a matriz extracelular (ECM). O ECM não só apoia a fixação das células, mas também permite o acesso a factores-chave de sinalização, influenciando a determinação celular e fenótipo 25, 26.
As lamininas são proteínas multifuncionais da matriz extracelular in vivo. No fígado, secreção de laminina é crucial para a regeneração do fígado após hepatectomia parcial 27 e é necessária para a manutenção de células progenitoras hepáticas 28. A importância da lamininas em manutenção fígado e regeneração foi a base para testar comercialmente disponíveis lamininas humanos recombinantes em nosso sistema de diferenciação de hepatócitos.
ele Superiorpatocyte diferenciação foi conseguida em LN-521 e LN-521 / LN-111 substratos quando comparado com Matrigel. HLCS derivados foram claramente polarizado e organizado no prato, e sua função celular foi significativamente melhorada quando comparado com os seus homólogos mistura de proteína gelatinosos. Subjacente a estas melhorias foi a regulação negativa dos contaminantes Colon-, a fibroblastos e haste genes associados a células sobre as lamininas, bem como uma diminuição na proliferação de células e expressão de genes associada à migração 10.
Em conclusão, o protocolo aqui descrito gera células de hepatócitos, como que estão mais próximos na natureza para hepatócitos humanos adultos. O processo é reprodutível, passível de automação, e pode ser escalado para aplicação de forma rentável. Importante, a variação lote-a-lote foi significativamente diminuída em comparação com as técnicas que utilizam Matrigel, resultando em um sistema de diferenciação melhorada para os investigadores neste campo.
Divulgações
Dr. David C. Hay é uma co-fundador e diretor do Stemnovate Limited.
Agradecimentos
Este trabalho foi apoiado com prêmios do Reino Unido Regenerative Medicine Platform (MRC MR / L022974 / 1 e MR / K026666 / 1) e uma bolsa de estudos China.
Materiais
| Name | Company | Catalog Number | Comments |
| Human Recombinant Laminin 521 | BioLamina | LN521-02 | |
| Human Recombinant Laminin 111 | BioLamina | LN111-02 | |
| Recombinant mouse Wnt3a | R&D Systems | 1324-WN-500/CF | |
| Human Activin A | Peprotech | 120-14E | |
| Human Hepatocyte Growth Factor | Peprotech | 100-39 | |
| Human Oncostatin M | Peprotech | 300-10 | |
| Rho-associated kinase (ROCK) inhibitor Y27632 | Sigma-Aldrich | Y0503-1MG | |
| Hydrocortisone 21-hemisuccinate sodium salt | Sigma-Aldrich | H4881 | |
| DMSO | Sigma-Aldrich | D5879 | |
| mTeSR1 medium | STEMCELL Technologies | 05850 | |
| RPMI 1640 | Life Technologies | 21875 | |
| Knockout DMEM | Life Technologies | 10829 | |
| HepatoZYME | Life Technologies | 17705 | |
| B27 supplement | Life Technologies | 12587-010 | |
| Knockout Serum Replacement | Life Technologies | 10828 | |
| GlutaMax | Life Technologies | 35050 | |
| Non-essential amino acids | Life Technologies | 11140 | |
| 2-mercaptoethanol | Life Technologies | 31350 | |
| Accutase | Millipore | SCR005 | |
| DPBS with Calcium and Magnesium | ThermoFisher | 14040133 |
Referências
- Forbes, S. J., Gupta, S., Dhawan, A. Cell therapy for liver disease: From liver transplantation to cell factory. J Hepatol. 62 (1 Suppl), S157-S169 (2015).
- Hay, D. C., et al. Highly efficient differentiation of hESCs to functional hepatic endoderm requires ActivinA and Wnt3a signaling. Proc Natl Acad Sci U S A. 105 (34), 12301-12306 (2008).
- Hay, D. C., et al. Direct differentiation of human embryonic stem cells to hepatocyte-like cells exhibiting functional activities. Cloning Stem Cells. 9 (1), 51-62 (2007).
- Medine, C. N., et al. Developing high-fidelity hepatotoxicity models from pluripotent stem cells. Stem Cells Transl Med. 2 (7), 505-509 (2013).
- Szkolnicka, D., et al. Accurate prediction of drug-induced liver injury using stem cell-derived populations. Stem Cells Transl Med. 3 (2), 141-148 (2014).
- Zhou, X., et al. Modulating innate immunity improves hepatitis C virus infection and replication in stem cell-derived hepatocytes. Stem Cell Reports. 3 (1), 204-214 (2014).
- Rashidi, H., Alhaque, S., Szkolnicka, D., Flint, O., Hay, D. C. Fluid shear stress modulation of hepatocyte-like cell function. Arch Toxicol. 90 (7), 1757-1761 (2016).
- Szkolnicka, D., et al. Reducing Hepatocyte Injury and Necrosis in Response to Paracetamol Using Noncoding RNAs. Stem Cells Transl Med. 5 (6), 764-772 (2016).
- Wang, Y., Hay, D. C. Mass production of stem cell derived human hepatocytes for experimental medicine. Expert Rev Gastroenterol Hepatol. 10 (7), 769-771 (2016).
- Cameron, K., et al. Recombinant Laminins Drive the Differentiation and Self-Organization of hESC-Derived Hepatocytes. Stem Cell Reports. 5 (6), 1250-1262 (2015).
- Cai, J., et al. Directed differentiation of human embryonic stem cells into functional hepatic cells. Hepatology. 45 (5), 1229-1239 (2007).
- Sullivan, G. J., et al. Generation of functional human hepatic endoderm from human induced pluripotent stem cells. Hepatology. 51 (1), 329-335 (2010).
- Duan, Y., et al. Differentiation and enrichment of hepatocyte-like cells from human embryonic stem cells in vitro and in vivo. Stem Cells. 25 (12), 3058-3068 (2007).
- Szkolnicka, D., Farnworth, S. L., Lucendo-Villarin, B., Hay, D. C. Deriving functional hepatocytes from pluripotent stem cells. Curr Protoc Stem Cell Biol. 30, 1-12 (2014).
- Rashid, S. T., et al. Modeling inherited metabolic disorders of the liver using human induced pluripotent stem cells. J Clin Invest. 120 (9), 3127-3136 (2010).
- Si-Tayeb, K., et al. Highly efficient generation of human hepatocyte-like cells from induced pluripotent stem cells. Hepatology. 51 (1), 297-305 (2010).
- Touboul, T., et al. Generation of functional hepatocytes from human embryonic stem cells under chemically defined conditions that recapitulate liver development. Hepatology. 51 (5), 1754-1765 (2010).
- Touboul, T., et al. Stage-specific regulation of the WNT/beta-catenin pathway enhances differentiation of hESCs into hepatocytes. J Hepatol. 64 (6), 1315-1326 (2016).
- Mathapati, S., et al. Small-Molecule-Directed Hepatocyte-Like Cell Differentiation of Human Pluripotent Stem Cells. Curr Protoc Stem Cell Biol. 38, 1-1 (2016).
- Takayama, K., et al. Efficient generation of functional hepatocytes from human embryonic stem cells and induced pluripotent stem cells by HNF4alpha transduction. Mol Ther. 20 (1), 127-137 (2012).
- Rodin, S., et al. Long-term self-renewal of human pluripotent stem cells on human recombinant laminin-511. Nat Biotechnol. 28 (6), 611-615 (2010).
- Rodin, S., et al. Clonal culturing of human embryonic stem cells on laminin-521/E-cadherin matrix in defined and xeno-free environment. Nat Commun. 5, 3195 (2014).
- Takayama, K., et al. Long-term self-renewal of human ES/iPS-derived hepatoblast-like cells on human laminin 111-coated dishes. Stem Cell Reports. 1 (4), 322-335 (2013).
- Medine, C. N., Lucendo-Villarin, B., Zhou, W., West, C. C., Hay, D. C. Robust generation of hepatocyte-like cells from human embryonic stem cell populations. J Vis Exp. (56), e2969 (2011).
- Sales, V. L., et al. Transforming growth factor-beta1 modulates extracellular matrix production, proliferation, and apoptosis of endothelial progenitor cells in tissue-engineering scaffolds. Circulation. 114 (1 Suppl), I193-I199 (2006).
- Taylor-Weiner, H., Schwarzbauer, J. E., Engler, A. J. Defined extracellular matrix components are necessary for definitive endoderm induction. Stem Cells. 31 (10), 2084-2094 (2013).
- Martinez-Hernandez, A., Delgado, F. M., Amenta, P. S. The extracellular matrix in hepatic regeneration. Localization of collagen types I, III, IV, laminin, and fibronectin. Lab Invest. 64 (2), 157-166 (1991).
- Lorenzini, S., et al. Characterisation of a stereotypical cellular and extracellular adult liver progenitor cell niche in rodents and diseased human liver. Gut. 59 (5), 645-654 (2010).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados