Method Article
Uma esofactomia de Ivor Lewis projetada para minimizar complicações anastomóticas e otimizar a função do conduíte
Neste Artigo
Resumo
Descrevemos uma nova técnica anastogásótica intratorácica, projetada para criar uma anastomose de grande diâmetro, mantendo simultaneamente o suprimento sanguíneo do conduíte para minimizar a incidência de vazamentos e estratos. A construção e orientação do conduíte estomacal projetado para otimizar a função do trato gastrointestinal superior também é descrita.
Resumo
Descrevemos uma nova técnica anastomótica esofagotrica ("lado a lado: linha de grampo sobre grampo", STS) para anastomoses intratorácicos projetados para criar uma anastomose de grande diâmetro, mantendo simultaneamente o suprimento de sangue do conduíte. Esta técnica visa minimizar a incidência de vazamentos e estratos anastomóticos, que é uma fonte freqüente de morbidade e mortalidade ocasional após a esofactomia. Analisamos os resultados desta técnica de STS em 368 pacientes e comparamos os resultados com 112 pacientes submetidos a anastomoses esofagotéricos utilizando um grampeador de ponta a ponta (EEE) em um intervalo de tempo de 8 anos em nossa instituição.
A técnica sts envolve alinhar o esôfago intratorácico restante sobre a ponta da linha de grampo de curva menor de um tubo estomacal, criado como um conduíte de substituição para o esôfago. Um dispositivo de grampeamento linear corta e regrampeia a linha de grampo do conduíte para a parede lateral do esôfago de forma lado a lado. O lúmen comum aberto é então fechado em duas camadas de suturas.
Houve um total de 12 (3,8%) vazamentos anastomóticos em pacientes submetidos à anastomose esofágica de STS. Dois dos oito pacientes (25%) teve vazamentos anastomóticos após esofactomia para achalasia de estágio final em comparação com uma taxa de vazamento de 2,8% (10/336) após esofectomia para outras condições. Dezoito (5,2%) os pacientes necessitaram de uma mediana de 2 dilatações para restrição anastomótica após a anastomose sts. A alimentação suplementar de jejunostomia foi necessária em apenas 11,1% dos pacientes submetidos a anastomoses de STS após a alta hospitalar. Em contrapartida, os pacientes submetidos a anastomoses da EEE demonstraram vazão anastomótica e taxas de restrição de 16,1% e 14,3% respectivamente (p<0,01). A análise temporal dos estudos de contraste pós-operatório, seguindo a técnica do STS, tipicamente demonstrou um conduíte de diâmetro reto/uniforme com contraste essencialmente completo esvaziando-se no intestino delgado em 3 minutos em 88,4% dos pacientes.
A incidência de vazamentos enastomóticos esofagotéricos e restrições foram extremamente baixas utilizando esta nova técnica anastomótica. Além disso, acreditamos que, com base em análises de tempo e qualitativas de estudos de contraste pós-operatório, essa técnica parece otimizar a função do trato gastrointestinal superior pós-operatório; no entanto, são necessários mais estudos comparativos.
Introdução
Vazamentos anastomóticos esofagotéricos representam uma complicação não incomum após a esofactomia1. Além disso, um vazamento anastomótico tem sido associado a desfechos desfavoráveis a longo prazo, incluindo reinternação hospitalar, mortalidade precoce e, ocasionalmente, má qualidade de vida2,3,4. Uma restrição anastomótica representa uma complicação a longo prazo, que também pode ser uma consequência de um vazamento anastomótico5. As restrições anastomóticas tanto impactam negativamente a qualidade de vida quanto aumentam o custo do cuidado.
À medida que mais pacientes com câncer de esôfago estão vivendo mais como resultado da detecção endoscópica de adenocarcinoma em estágio inicial e terapia de quimioradiação por indução para cânceres mais avançados localmente, a otimização da função do conduíte estomacal também se torna importante. A "função" do conduíte gástrico, no entanto, depende da gravidade para a drenagem. A construção e a orientação do conduíte gástrico podem afetar a função do trato gastrointestinal superior e, portanto, a "função" do conduíte ruim pode ser resultado de problemas técnicos.
Usamos uma nova técnica "lado a lado: linha de grampo on-staple" (STS) para anastomose esofágica intratorácica desde 2009. Esta técnica é projetada para criar uma anastomose de diâmetro maior em comparação com as anastomoses feitas com grampeadores de ponta a ponta (EEE) ao mesmo tempo mantendo o suprimento sanguíneo de conduíte para reduzir a incidência de vazamentos e restrições anastomóticas. Descrevemos esta nova técnica anastomótica e também descrevemos construção e orientação de conduítes gástricos para otimizar a função. Comparamos os resultados desta técnica de STS com as anastomoses realizadas com grampeadores EEE durante um intervalo de tempo de 8 anos em nossa instituição.
Protocolo
Este estudo foi aprovado pela Indiana University-Purdue University em Indianápolis institutional review board (1109006832). Este procedimento foi realizado em todos os pacientes que necessitaram de ressecção e ressecção do esôfago intratrácico distal para doenças malignas ou benignas desde 2009 no Indiana University Hospital.
1. Fase pré-anestesia
- Coloque um cateter peridural.
- Obter acesso venoso central padrão e radial.
- Anestesiae e entubar utilizando um tubo endobrônquico duplo do lado esquerdo do lúmen para ventilação pulmonar seletiva durante a fase torácica da operação.
2. Fase inicial de laparotomia
- Realize uma laparotomia midline superior, incluindo excisão do processo zyphoid com elecaucautery. Coloque um retrátil de parede abdominal auto-retida para exposição à cavidade peritoneal.
- Realize uma ampla manobra kocher, que mobiliza todo o duodeno do retroperitônio. Esta manobra não só endireita o conduíte gástrico, mas também permite que porções bem vascularizadas do conduíte estomacal sejam avançadas acima do arco azygos.
- Coloque temporariamente uma esponja de laparotomia de tamanho padrão sob o duodeno para elevar o conduíte, que é removido na fase final de laparotomia.
- Divida o ligamento gastrocólco cauterizando e dividindo os vasos sanguíneos omentais com um dispositivo de energia padrão. Evite a manipulação dos vasos gastroepiplóicos certos colocando uma sonda nasogástrica ao longo da curvatura maior, que é usada como "alça" retraindo o estômago para cima.
- Marque o peritômio circunferencialmente ao redor das crus diafragmáticas com elepuleterismo e coloque temporariamente um dreno de Penrose ao redor do esôfago intraabdominal.
- Liga os vasos gastroepiplóicos esquerdos e curtos com uma combinação de sutura e clipes cirúrgicos. Então divida.
- Em casos de malignidade, mobilize os tecidos linfáticos celíacos do aspecto superior do pâncreas, o que inclui ligadura e divisão tanto da artéria gástrica esquerda quanto da veia.
- Limpe a menor curva gástrica de gordura e vasos sanguíneos tipicamente de 3 a 5 cm distal à junção gastroesofágica com endostaplers vasculares. Em casos de malignidade, planeje as operações para alcançar o estômago distal livre de tumores de 3 a 5 cm e 5 a 7 cm margens cirúrgicas esofágicas proximais. Como os locais tumorais variam do meio-esôfago ao cardia gástrico, alcançar estômago distal adequado e margens esofágicas proximais resulta em conduítes de comprimentos variados e associais esofágicos mais baixos ou mais elevados. O local específico da clareira da curva menor é, portanto, um pouco variável e dependente da localização exata do tumor.
- Corte o fundus gástrico superior e o coração do restante do estômago normalmente usando entre 3 e 5 60 mm grampeadores endoscópicos a partir da maior curva gástrica para a área limpa na curva gástrica menor.
- Criação de conduítes gástricos
- Debulk menor gordura omental ao redor dos vasos gástricos certos, o que permite que o conduíte seja endireitado, bem como alongado. A divisão dos vasos gástricos certos à medida que se inserem na curva menor na incisura proporcionará um alongamento adicional.
- Fixar o estômago em três pontos e proporcionar retração externa(Figura 1).
- Crie um conduíte de diâmetro uniforme estreito (média de 7-8 cm) com um fogo inicial do grampeador de 100 mm, que fornece duas linhas de grampos de 4,8 mm visando um pouco abaixo da linha de grampo anterior. A conclusão da construção do conduíte geralmente requer 2 ou 3 incêndios adicionais do tri-grampeador endoscópico de 60 mm na área desmatada na curva gástrica menor. Em casos de malignidade, envie o defeito estomacal como a "margem distal do estômago" para análise patológica da seção congelada.
- Inspecione a ponta do conduíte. Dentro de 3 a 5 min, o sangramento vermelho brilhante punctate é geralmente visto através da linha de grampo de curva menor representando boa perfusão de conduíte. Se não houver escorrendo vermelho brilhante, apare ligeiramente a ponta do conduíte com outro grampeador de 100 mm até que se vista um sangramento punctate. Os tri-grampeadores não são usados para cortar conduítes como cortar e refazer a ponta do conduíte durante a anastomose intratorácica pode ser difícil.
- Realize uma pyloroplastia Heineke-Mikulicz padrão, a fim de garantir o bom esvaziamento do conduíte.
- Inicialmente, estimar o quão alto no peito o conduíte atingirá esticando confortavelmente o conduíte em direção ao pescoço sem tensão indevida.
- Abra a pleura certa através das cruas diafragmáticas. Coloque a ponta do conduíte no peito direito mantendo a linha de grampo de curva menor voltada para a direita.
- Feche temporariamente o abdômen com algumas suturas fasciais interrompidas e grampos de pele.
3. Fase torácica
- Coloque o paciente na posição de decúbito lateral esquerdo.
- Realize uma serratus muscular poupando toracotomia direita através doespaço intercostal 5. Divida o músculo intercostal sob a incisão dentro de 3 a 5 cm do corpo vertebral posteriormente e o esterno anteriormente, permitindo movimento adicional das costelas5 e 6com risco mínimo de fratura ou contusão.
- Extirno o arco da veia azygos e divida o ligamento pulmonar inferior. Em casos de malignidade, realize a dissecção em bloco mobilizando os dois terços distais do esôfago intratorácico com todos os tecidos moles circundantes desde o pericárdio anteriormente até os vasos sanguíneos esofágicos posteriormente. Cuidadosamente ocluir linfáticos com clipes cirúrgicos antes da divisão durante esta dissecção.
- Entregue o conduíte no peito direito até que não haja redundância, limitando a tensão nos pedículos vasculares gastroepiplóiccertos direito e direito para determinar a extensão superior da dissecção esofágica necessária.
- Ao nível da carina traqueal, disseque a parede esofágica dos tecidos moles mediastinal ao redor superiormente a um nível onde a ponta do conduíte atinge sem tensão, que geralmente é 3 a 5 cm superior à carina. Mais uma vez, no entanto, dadas as diferentes localizações de tumores e comprimento dos conduítes estomacais criados durante a fase abdominal, estabelecer anastomoses mais baixoperto perto da carina para tumores cardíacos gástricos e mais alto na entrada torácica para tumores envolvendo o esôfago intratrácico médio.
- Criação da anastomose esofagotrica
- Alinhe o aspecto lateral esquerdo médio do terço superior do esôfago intratorácico sobre a linha de grampo da curva menor.
- Coloque quatro suturas de aderência de aproximadamente 2 a 3 cm de distância para manter o alinhamento(Figura 2).
- Transcção do esôfago 1 cm distal ao conjunto inferior de suturas de aderência. Em casos de malignidade, envie um anel de esôfago neste nível como a "margem esofágica proximal" para exame patológico de seção congelada antes do processo.
- Crie uma abertura correspondente de 1 a 2 cm no conduíte através da linha de grampo de curva menor.
- Coloque suturas interrompidas dentro do lúmen comum, incorporando o conduíte adjacente e as paredes esofágicas começando no meio através da linha de grampo de curva menor e progredindo para ambos os lados (Figura 3).
- Coloque a bigorna estreita de um grampeador endoscópico de 45 mm com uma altura de grampo de 4,1 mm no lúmen esofágico e a bigorna grande no conduíte. Para otimizar o comprimento da comunicação lado a lado entre o esôfago e o conduíte, corte 5 mm da ponta de plástico distal do cartucho do grampeador com uma serra oscilante.
- Atire o grampeador, que corta e regrampeia a linha de grampo de curva menor(Figura 4). O comprimento da extremidade de corte do esôfago é geralmente um pouco maior do que a borda do conduíte gástrico, por isso remova uma elipse do conduíte sobre a linha de grampo de curva menor em vez de estender o aluguel lateralmente, preservando o suprimento de sangue colateral(Figura 4 inset).
- Feche o lúmen comum aberto em duas camadas de suturas começando com uma camada interna de sutura de poliglactina 3-0 invertida seguida por uma segunda camada de seda 3-0 interrompida usando uma técnica de Lembert(Figura 5).
- Sobre a costura do aspecto superior da linha de grampo de conduíte de menor curva com suturas de seda interrompidas 3-0 em uma moda Lembert estendendo-se inferiormente, até que os vasos gástricos certos são encontrados.
- Faça com que o anestesiologista coloque uma sonda nasogástrica no conduíte até o nível dos crus por palpação.
- Para anastomoses criados perto da inleta torácica, use um retalho pleural para selar a anastomose no mediastino posterior. Para anastomoses no aspecto médio do mediastino posterior, mobilize um tapinha de gordura pericárdica do mediastino anterior e livremente embrulhado para cobrir a nastomose esofagotrica(Figura 6 e Figura 7).
- Insira e posicione dois tubos torácicos 28-franceses dentro do hemithorax direito, um anterior e outro posterior, ao lado, mas não abutting o conduíte. Feche a incisão da toracotomia.
4. Re-laparotomia: fase "double flip"
- Retorne o paciente à posição supina e reabra a incisão da laparotomia média.
- Inspecione a gordura gastroepiplóica direita e empurre cuidadosamente qualquer excesso de gordura para cima através do diafragma esquerdo crus no peito.
- Fixar a gordura gastroepóica certa e o conduíte às cruas diafragmáticas com suturas de seda interrompidas 2-0(Figura 8). Coloque um tubo de jejunostomia alimentar em pacientes selecionados, principalmente em pacientes idosos ou pacientes com déficit nutricional pré-operatório.
- Feche formalmente a incisão da laparotomia média.
- Manter os pacientes entubados na noite da cirurgia com extubação planejada na manhã seguinte.
- Fornecer controle da dor com cateteres peridurais colocados pouco antes da indução anestésia durante os primeiros 3 a 4 dias, que é complementado por narcóticos intravenosos.
- Obter contraste série gastrointestinal superior 5 a 7 dias no pós-operatório para avaliar a integridade anastomótica.
- Se não for identificado vazamento anastomótico, remova a sonda nasogástrica.
- Instrua os pacientes a avançar para uma dieta regular em 2 a 3 semanas após a alta, conforme tolerado.
Resultados
De 2009 a 2017, foram identificados 368 pacientes submetidos a uma anastomose esofágica intratorácica de STS e destes 12 (3,8%) teve vazamentos anastomóticos. Cinco desses pacientes demonstraram vazamentos de grau I/II e não necessitaram de intervenção. Seis pacientes e um paciente, respectivamente, experimentaram vazamentos grau III e IV que requerem stent endoscópico e/ou intervenção cirúrgica2. Observou-se uma taxa de vazamento de 25% (2/8) após a achalasia do estágio final em comparação com uma taxa de vazamento de 2,8% (10/336) onde a esofafago foi realizada para outras condições. Foram 4 (1,1%) paciente que morreu no pós-operatório, nenhum dos quais teve uma complicação anastomótica. Dos pacientes com STS, 18 (5,0%) exigiu uma mediana de 2 dilatações para estiletes anastomóticas sintomáticas. A alimentação suplementar de jejunostomia foi necessária em apenas 11,1% desses pacientes após a alta hospitalar. Em contrapartida, dos 112 pacientes identificados que foram submetidos à anastomose de grampeador mecânico tármpio (EEE) de ponta a ponta (EEE) nesse mesmo intervalo de tempo, 16,1% e 14,3% demonstraram vazamentos anastomóticos e restrições sintomáticas respectivamente (p<0,01) apesar de todos (100%) desses pacientes mantidos em dieta limitada com alimentação de tubos de jejunostomia suplementar por pelo menos um mês após a cirurgia (Tabela 1). As comorbidades demográficas e comorbidades dos grupos STS e EEE foram estatisticamente semelhantes; no entanto, houve tendência para mais doenças cardíacas na coorte STS (Tabela 2). A análise de tempo dos estudos de contraste pós-operatório nos primeiros 208 pacientes submetidos a uma anastomose STS tipicamente demonstrou um conduíte de diâmetro reto/uniforme com essencialmente completo (>95%) contrastando esvaziamento no intestino delgado dentro de 3 min em 184 (88,4%) Pacientes. Os demais 11,6% dos pacientes estudados apresentaram quase completo (>95%) contraste esvaziamento no intestino delgado dentro de 5 minutos. Nenhum paciente estudado teve tempo de trânsito de contraste superior a 5 minutos.

Figura 1: Criação do conduíte estomacal. O estômago está preso em três pontos, que são retraídos para fora. Um conduíte de diâmetro relativamente uniforme é criado com grampeadores visando apenas inferior à linha de grampo anterior na curva menor. (Retirado com a permissão11.) Clique aqui para ver uma versão maior desta figura.
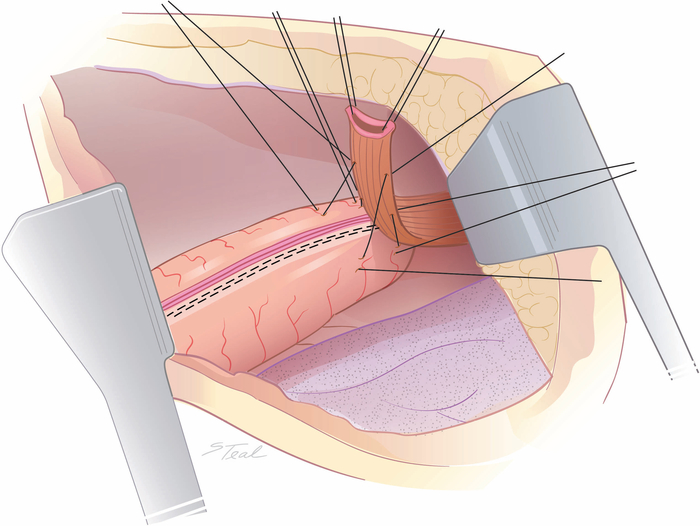
Figura 2: Alinhamento do esôfago sobre o conduíte estomacal. O aspecto lateral esquerdo médio do terço superior do esôfago intratorácico está alinhado sobre a linha de grampo de curva menor na ponta do conduíte com 4 suturas iniciais de aderência de aproximadamente 2 a 3 cm de distância. (Retirado com a permissão11.) Clique aqui para ver uma versão maior desta figura.

Figura 3: Preparação para uma comunicação lado a lado entre o esôfago e o conduíte estomacal. Um aluguel de 1 a 2 cm é feito no conduíte estomacal através da linha de grampo de curva menor. As suturas de aderência são colocadas entre o conduíte adjacente e as paredes esofágicas que começam no meio através da linha de grampo de curva menor, em seguida, duas suturas em ambos os lados. (Retirado com a permissão11.) Clique aqui para ver uma versão maior desta figura.
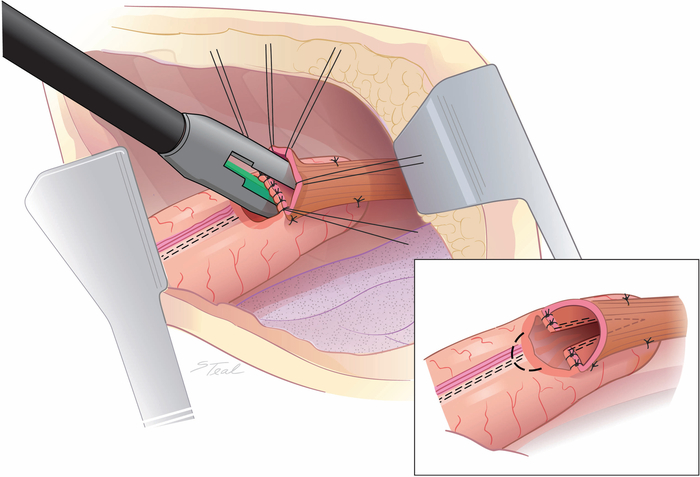
Figura 4: Criação de uma comunicação lado a lado entre o esôfago e o conduíte estomacal. Um grampeador endoscópico de 45 mm é acionado cortando e descansando a linha de grampo de curva menor. Normalmente, apenas 2/3ºs do comprimento do grampeador são usados. Uma elipse de conduíte é removida sobre a linha de grampo de curva menor (linha pontilhada) em vez de estender o aluguel lateralmente para equalizar o comprimento da extremidade de corte do esôfago e gastrotomia. (inset) (Retirado com a permissão11.) Clique aqui para ver uma versão maior desta figura.

Figura 5: Fechamento do lúmen comum aberto. O lúmen comum aberto é fechado à mão em duas camadas de suturas que começam com suturas absorvíveis interrompidas invertidas. A primeira camada de sutura é imbricada por uma segunda camada de suturas de seda lembert colocando a sutura estomacal alguns mm inferior à primeira camada de suturas. (inset) (Retirado com a permissão11.) Clique aqui para ver uma versão maior desta figura.
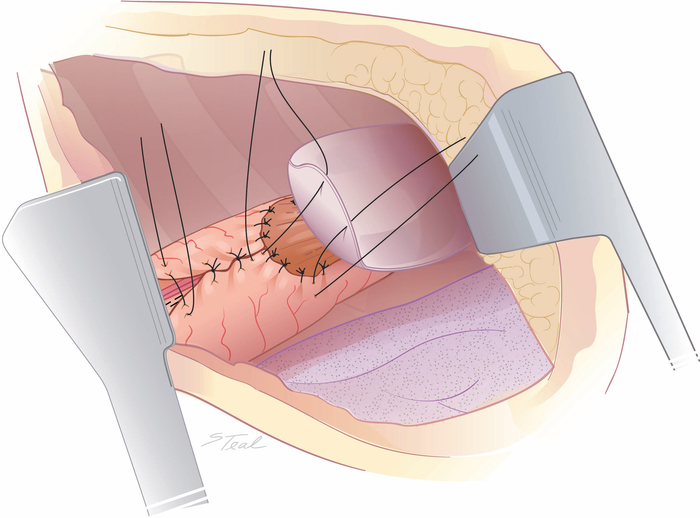
Figura 6: Sobre a costura da linha de grampo de curva menor e da bunda pleural da anastomose. O aspecto superior da linha de grampo do conduíte de menor curva pode ser costurado neste ponto com suturas de seda interrompidas inferiormente até que os vasos gástricos certos sejam encontrados. Para anastomoses estabelecidos perto da entrada torácica, um retalho de pleura mobilizada é pregado no conduíte estomacal para conter pequenos vazamentos anastomóticos. (Retirado com a permissão11.) Clique aqui para ver uma versão maior desta figura.
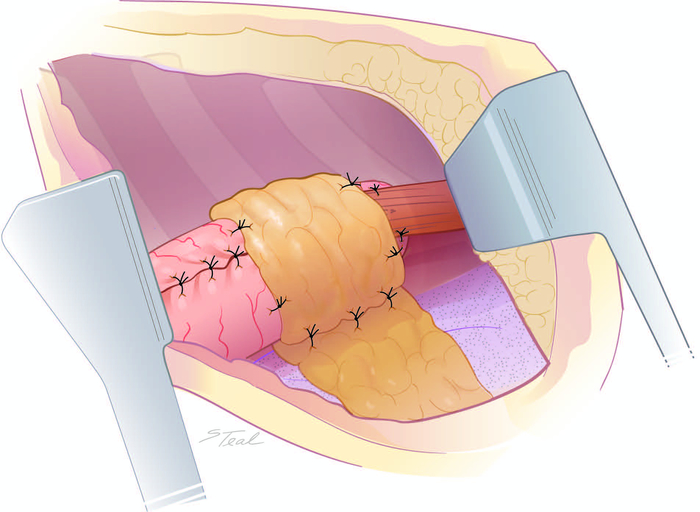
Figura 7: Bunda de tecido mole vascularizado da anastomose. A gordura pericárdica é livremente enrolada em torno de anastomoses criados no aspecto médio do mediastino posterior para conter quaisquer pequenas áreas de deiscência anastomótica. Clique aqui para ver uma versão maior desta figura.
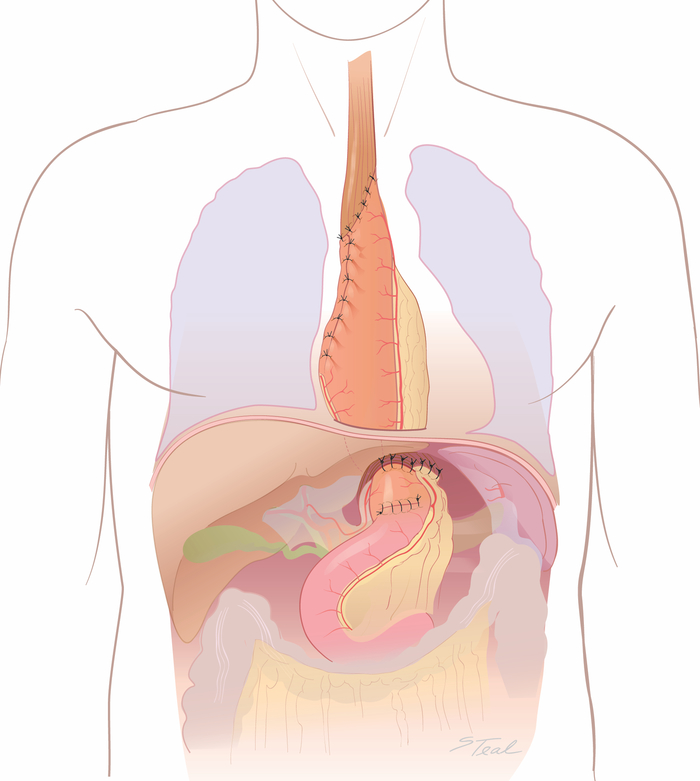
Figura 8: Fase final ("double flip"). A incisão da laparotomia é reaberta. A gordura gastroepiplóica direita e conduíte cuidadosamente pregado às cruas com 2-0 suturas de seda. (Retirado com a permissão11.) Clique aqui para ver uma versão maior desta figura.
| STS (N=368) | EEA (N=112) | |
| Vazamentos anastomóticos | 3.8%* | 16.1% |
| Estrito anastomótico | 5.2%* | 14.3% |
| Uso do tubo J-Op pós-op | 11.0%* | 100.0% |
Tabela 1. Vazamentos/restrições anastomóticas e uso de jejunostomia de alimentação pós-operatória (Uso de Tubo Pós-Op J-Tube) após alta hospitalar comparando pacientes submetidos a IST aberto e anastogás esofágico eosofágico eea toracocópico usando uma abordagem de Ivor Lewis realizada no Indiana University Simon Cancer Center de 2009 a 2017. (*p valor < 0,01, qui-quadrado)
| STS (n=278) | EEE (n=82) | Valor P | |
| Idade no Diagnóstico (yrs) | 60,3 ± 11,4 (23-84) | 60,6 ± 9,0 (38-80) | 0.80 |
| Gênero | |||
| Masculino | 228 (82.0%) | 69 (84.1%) | 0.66 |
| Fêmea | 50 (18.0%) | 13 (15.9%) | |
| Cormorbidade | |||
| Cardíaca | 114 (41.0%) | 24 (29.3%) | 0.06 |
| Diabetes Mellitus | 70 (25.2%) | 19 (23.2%) | 0.71 |
| Dpoc | 32 (11.5%) | 12 (14.6% | 0.45 |
| Histologia | |||
| Adenocarcinoma | 237 (85.3%) | 74 (90.2%) | 0.25 |
| Outros Diagnósticos | 41 (14.7%) | 8 (9.8%) | |
| Terapia Neoadjuvante | 200 (71.9%) | 59 (71.9%) | 0.99 |
Tabela 2: Comparação demográfica e de comorbidade aberta STS e anastomoses toracocópicos da EEE por meio de uma abordagem de Ivor Lewis realizada no Centro de Câncer Simon da Universidade de Indiana de 2009 a 2015. Desvio médio e padrão com intervalo dado para variáveis contínuas. Valores P para variáveis contínuas geradas pelo teste t de Student e qui-quadrado para variáveis discretas.
Discussão
A esôfago representa um procedimento cirúrgico muito extenso. A qualidade de vida adversa a longo prazo tem sido associada a pacientes que tiveram complicações pós-operatórias, incluindo vazamentos anastomóticos3. Os fatores de risco para um vazamento anastomótico incluem principalmente a criação de uma anastomose com baixo suprimento sanguíneo. Um vazamento anastomótico não só representa uma fonte significativa de morbidade pós-operatória, mas também pode comumente resultar em estofado. Uma restrição também pode ser resultado de problemas técnicos, incluindo a realização de uma anastomose de pequeno diâmetro. Além de impactar a qualidade de vida, as restrições aumentam os custos médicos globais quando a dilatação é necessária5. Realizar com precisão várias etapas é de extrema importância para minimizar complicações, bem como alcançar bons resultados funcionais do trato gastrointestinal oncológico e superior.
A anastomose esofagotrica pode ser realizada por vários métodos, incluindo costuras manuais, EEE e técnicas lineares de grampeadores representando a maioria. Um relatório da Society of Tohoracic Surgeons General Tohoracic Database citou uma taxa global de vazamento de 9,3% em pacientes submetidos a anastomoses esofágicos intratorácicos6. Enquanto a mortalidade pós-operatória por vazamento anastomótico parece estar diminuindo, as taxas de estratosdeiras subseqüentes permanecem elevadas, variando entre 10 e 56%7. Collard e Orringer descreveram uma técnica de grampeador linear para criar uma anastomose esofágica cervical lado a lado8,9. A abertura triangulada posterior formada pelo grampeador linear foi demonstrada para resultar em uma baixa taxa de vazamento, bem como resistência à rigidoridade. Um estudo retrospectivo da Clínica Mayo relatou um incidente de 5,6% de vazamento anastomótico intratorácico em 177 pacientes onde uma técnica de grampeado linear foi usada contra uma taxa de vazamento de 8,3% em 48 pacientes submetidos a uma anastomose grampeada do EEE. Embora essa diferença não tenha alcançado diferença estatística, a probabilidade de um ano de restrição foi de 32% após a anastomose eEE, em comparação com apenas 8,6% com técnicas lineares grampeadas, o que foi significativo5. Wang e colegas realizaram um estudo clínico prospectivo envolvendo 155 pacientes que foram randomizados em um dos três métodos anastomóticos esofágicos10. Impressionantemente, não foram desenvolvidas restrições pós-operatórias em pacientes submetidos a uma técnica de grampeador linear em comparação com 9,6% e 19,1% nos casos costurados à mão e circulares, respectivamente, o que foi estatisticamente significativo. Estudos anteriores envolvendo anastomoses de grampeadores lineares utilizaram a parede anterior do conduíte estomacal para o sítio anastomótico. Esta abordagem pode levar a uma faixa isquêmica de conduíte entre a linha de grampo de curva menor e a anastomose predispondo a vazamento. Novidade para nossa técnica, o suprimento de sangue colateral para a ponta do conduíte estomacal é preservado cortando e descansando a linha de grampo de curva menor.
Há limitações para o estudo. Primeiro, isso representa uma análise retrospectiva. Apesar da natureza retrospectiva, porém, utilizamos essa abordagem de STS uniformemente em todos os pacientes submetidos à cirurgia para patologia estomacal média para proximal ao longo do intervalo de estudo como uma "intenção de tratar" incluindo pacientes estáveis que sustentaram perfurações esofágicas durante a dilatação para restrição onde a reparação não era possível. Comum a qualquer técnica anastomótica intratorácica de lado a lado é a necessidade de dissecar um adicional de 3 a 4 cm de esôfago proximal, diminuindo potencialmente o comprimento da margem esofágica cirúrgica em casos de malignidade e também potencialmente resultando em algum grau de devascularização esofágica. Para evitar a devascularização, um ponto crítico é não dissecar o esôfago intratorácico mais superiormente em direção ao pescoço do que a ponta do conduíte estomacal alcançará sem tensão. Especula-se que a maior taxa de vazamento observada utilizando esta técnica para pacientes com achalasia em estágio terminal pode estar relacionada à desvascularização de uma parede esofágica espessa após mobilização para realizar uma anastomose sts onde o suprimento de sangue pré-existente pode ser ruim. A dilatação esofágica frequentemente vista em casos de achalasia torna a costura manual o lúmen comum aberto muito difícil, o que também pode ser um fator. Com base nessa experiência, acreditamos agora que a achalasia é uma contra-indicação para realizar anastomoses intratorácicos sts. Note-se que, para cânceres longos ou mais centrais, onde uma anastomose esofagotrica precisa ser criada perto da entrada torácica para alcançar uma margem esofágica proximal adequada, utilizamos uma comunicação inicial um pouco mais curta, não utilizando todo o comprimento da GIA de 45 mm, que no entanto tem potencial para ser mais propensa à formação de restrições.
Ao contrário do esôfago, o estômago é um conduíte passivo, a gravidade dependente da drenagem. Várias variáveis, incluindo diâmetro e comprimento do conduíte, bem como orientação do conduíte podem, portanto, impactar significativamente a função do trato gastrointestinal superior. A alimentação ingerida tem potencial para desligar em três locais: a anastomose esofagotrica, o corpo estomacal e a saída gástrica. A má função do conduíte pode ser resultado de problemas técnicos em qualquer uma dessas três áreas. O esvaziamento do conduíte pobre paradoxalmente pode causar mais "refluxo", não apenas impactando negativamente a qualidade de vida, mas também ocasionalmente resultando em aspiração. Abordagens "minimamente invasivas" (laparoscópicas/torácicas), que utilizam um grampeador EEE para anastomoses esofagotéricos, embora ainda representem a minoria dos casos de esoffagectomia realizados, tornaram-se cada vez mais populares. Acreditamos, no entanto, que nossa técnica aberta como descrita não só permite criações de anastomose esofagotrica esofagotrica precisa para reduzir as taxas de rigor, mas também otimiza a construção e orientação do conduíte com um conduíte estomacal não redundante direto, incluindo a piloplastia com tendência mínima para materiais alimentares ingeridos para pendurar nessas áreas em comparação com abordagens torácicas. O tempo de trânsito de contraste medido da boca para o intestino delgado em estudos de rotina pós-operatório apoiaria excelente função de conduíte com nossa técnica, porém estudos comparativos utilizando outras técnicas são necessários. Nossas observações apoiariam sintomas mínimos e auto-limitantes de "dumping" na grande maioria dos pacientes com STS, porém avaliações específicas de qualidade de vida estão em andamento. Finalmente, com a abordagem de toracotomia descrita, observamos pouca diferença em relação ao desconforto pós-operatório agudo e de longo prazo em comparação com pacientes submetidos a uma abordagem toracoscópica em nossa instituição.
Em resumo, acreditamos que esta nova técnica de STS pode reduzir significativamente a morbidade e a mortalidade ocasional de complicações anastomóticas esofagotricas após a esofactomia. A construção e orientação do conduíte, conforme descrito, otimiza adicionalmente a função do trato gastrointestinal superior. Finalmente, essa técnica é facilmente adaptada e reprodutível.
Divulgações
Os autores não têm revelações.
Agradecimentos
Nenhum.
Materiais
| Name | Company | Catalog Number | Comments |
| 100 mm Linear Stapler (ILA Autosuture, “green” cartridge, 4.8 mm staple height) | Covidien | 3973 | Surgical Stapler |
| 3-0 silk (Perma hand black, 8x18", SH needle, 1/2 circle 26 mm, C013) | Ethicon | C013D | Suture Material |
| 3-0 silk (Perma hand black, 8x30", SH needle, 1/2 circle 26 mm, C017) | Ethicon | C017D | Suture Material |
| 3-0 vicryl (Coated vicryl violet, 8x18", SH needle, 1/2 circle 26 mm, J774) | Ethicon | VCP774D | Suture Material |
| 3-0 vicryl (Coated vicryl violet, 8x27", SH needle, 1/2 circle 26 mm, J784) | Ethicon | VCP784D | Suture Material |
| 45 mm Endoscopic Stapler (Flex “green” cartridge, 4.1 mm staple height) | Ethicon | SC45A | Surgical Stapler |
| 60 mm Endoscopic Tristapler | Ethicon | SC60A | Surgical Stapler |
| Flex “green” cartridge, 4.1 mm staple height | Ethicon | GST45G | Surgical Stapler |
| Flex 60, “black” cartridge (for 60 mm Endoscopic Tristapler) | Ethicon | GST60T | Surgical Stapler |
| Foceps Debakey 7.75 inch | Jarit | 320-101 | Surgical Instrument |
| Forceps Debakey 12 inch | Jarit | 320-103 | Surgical Instrument |
| Forceps Debakey 9.5 inch | Jarit | 320-102 | Surgical Instrument |
| Needle Holder Mayo-Hegar 10 inch | Codman | 36-2019 | Surgical Instrument |
| Needle Holder Mayo-Hegar 7 inch | Codman | 36-2017 | Surgical Instrument |
| Needle Holder Mayo-Hegar 8 inch | Codman | 36-2018 | Surgical Instrument |
| Needle Holder Ryder 10 inch | Codman | 36-3005 | Surgical Instrument |
| Needle Holder Ryder 9 inch | Jarit | 121-164 | Surgical Instrument |
Referências
- Cassivi, S. D. Leaks, strictures, and necrosis: a review of anastomotic complications following esophagectomy. Seminars in Thoracic and Cardiovascular Surgery. 16, 124-132 (2004).
- Low, D. E., et al. International consensus on standardization of data collection for complications associated with esophagectomy: Esophagectomy complication consensus group (ECCG). Annals of Surgery. 262, 286-294 (2015).
- Derogar, M., Orsini, N., Sadr-Azodi, O., Langergren, P. Influence of major postoperative complications on health-related quality of life among long-term survivors of esophageal cancer surgery. Journal of Clinical Oncology. 30, 1615-1619 (2012).
- Kofoed, S. C., et al. Intrathoracic anastomotic leakage after gastroesophageal cancer resection is associated with increased risk of recurrence. Journal of Thoracic and Cardiovascular Surgery. 150, 42-48 (2015).
- Price, T. N., et al. A comprehensive review of anastomotic technique in 432 Esophagectomies. Annals of Thoracic Surgery. 95, 1154-1160 (2013).
- Kassis, E. S., et al. Predictors of anastomotic leak after esophagectomy: an analysis of the Society of Thoracic Surgeons General Thoracic Database. Annals of Thoracic Surgery. 96, 1919-1926 (2013).
- Yuan, Y., Wang, K. N., Chen, L. Q. Esophageal anastomosis. Diseases of the Esophagus. 28, 127-137 (2015).
- Collard, J. M., Romagnoli, R., Goncette, L., Otte, J. B., Kestens, P. J. Terminalized semimechanical side-to-side suture technique for cervical esophagogastrostomy. Annals of Thoracic Surgery. 65, 814-817 (1998).
- Orringer, M. B., Marshall, B., Iannectoni, M. D. Eliminated the cervical esophagogastric anastomotic leak with a side-to-side stapled anastomosis. Journal of Thoracic and Cardiovascular Surgery. 119, 277-288 (2000).
- Wang, W. P., Gao, Q., Wang, K. N., Shi, H., Chen, L. Q. A prospective randomized controlled trial of semi-mechanical versus hand-sewn or circular stapled esophagogastrostomy for prevention of anastomotic stricture. World Journal of Surgery. 37, 1043-1050 (2013).
- Kesler, K. A. Outcomes of a novel intrathoracic esophagogastric anastomotic technique. The Journal of Thoracic and Cardiovascular Surgery. 156 (4), 1739-1745 (2018).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados