Method Article
Modelo de criolesão para o estudo da regeneração muscular esquelética do pedúnculo caudal em zebrafish adulto
Neste Artigo
Resumo
Este protocolo descreve um modelo de criolesão para induzir danos profundos de vários miômeros caudais em zebrafish adultos. Este método fornece uma nova abordagem para o estudo da regeneração muscular esquelética após perda severa de tecido em vertebrados não mamíferos.
Resumo
O músculo esquelético sofre renovação e restauração após pequenas lesões através da ativação de células-tronco satélites. Lesões graves da musculatura frequentemente levam à fibrose em humanos. Em comparação com os mamíferos, os peixes-zebra possuem uma maior capacidade inata de regeneração de órgãos, fornecendo um modelo poderoso para estudar a restauração tecidual após danos extensos ao órgão. Aqui, um modelo de criolesão é descrito para induzir danos profundos a quatro miômeros do pedúnculo caudal em peixes-zebra adultos. Uma criosonda personalizada foi projetada para se ajustar à forma do corpo e lesionar de forma reprodutível a musculatura lateral da pele até a linha média. É importante ressaltar que a integridade corporal permaneceu intacta, e os peixes continuaram sua atividade de natação. As alterações no músculo esquelético foram avaliadas por coloração histológica e coloração por fluorescência das proteínas sarcoméricas em cortes teciduais. Este método abrirá novos caminhos de pesquisa visando compreender como a degeneração do músculo esquelético induz respostas reparativas e, assim, a reativação do programa miogênico em zebrafish adultos.
Introdução
Em vertebrados, partes danificadas de vários tecidos sofrem renovação homeostática e restauração durante a vida útil. Essa capacidade de renovação e restauração depende tipicamente da presença de células-tronco competentes ou da capacidade proliferativa das células maduras 1,2. O músculo esquelético compreende as miofibras pós-mitóticas, que estão associadas às células-tronco locais, denominadas células satélites3,4,5,6. Assim, esse tecido contém fontes celulares para o selamento eficiente de áreas de continuidade interrompida ou para o reparo de pequenas feridas. No entanto, maiores perdas volumétricas no músculo esquelético de mamíferos são frequentemente seguidas por reparo não regenerativo, comofibrose7. Modelos animais podem fornecer novos conhecimentos sobre os mecanismos biológicos que promovem a regeneração de órgãos extensamente danificados.
O peixe-zebra é um organismo modelo bem estabelecido com alta capacidade regenerativa. Os peixes-zebra adultos podem regenerar uma parte amputada de sua nadadeira caudal ou o ápice ressecado do ventrículo cardíaco 8,9,10,11. Além disso, um método de criolesão já foi aplicado para estudar a regeneração de nadadeiras e coração em peixes-zebra12,13,14,15. No caso dos órgãos internos, o método criolesão tem a vantagem de induzir a morte celular sem comprometer a integridade do órgão, mimetizando condições fisiológicas16,17. Os detritos teciduais são desintegrados pela depuração natural durante a cicatrização de feridas, seguida pelos processos reparativos. No entanto, ainda não foi estabelecido se esse método poderia ser aplicado ao músculo esquelético.
Em peixes, a musculatura lateral permite a flexão látero-lateral do tronco durante a natação18. Os músculos esqueléticos organizam-se em unidades metaméricas, denominadas miômeros, que são separadas por tecido conjuntivo 5,19. Os peixes-zebra podem regenerar seu músculo após pequenas rupturas teciduais, como as causadas por ablação a laser ou por arma branca20,21,22,23,24, mas ainda não se sabe se os miômeros inteiros podem se regenerar após lesão extensa. Essa lacuna no conhecimento provavelmente se deve à falta de um modelo adequado de lesão. Este protocolo estabelece uma nova abordagem para induzir lesão extensa do músculo esquelético, abrangendo múltiplos miômeros. O método de criolesão descrito baseia-se no rápido congelamento e descongelamento das miofibras com um instrumento de aço inoxidável pré-resfriado. Apesar dos extensos danos, o bem-estar dos peixes não foi severamente prejudicado. Miômeros inteiros podem ser restaurados e, portanto, este trabalho fornece um novo sistema modelo para estudar os mecanismos de regeneração da musculatura em peixes-zebra adultos.
Protocolo
Este estudo foi conduzido de acordo com todas as normas éticas pertinentes. Os peixes-zebra foram criados, criados e mantidos de acordo com as diretrizes da Federação das Associações Europeias de Zootecnia de Laboratório (FELASA)25. O alojamento dos animais e todos os procedimentos experimentais foram aprovados pelo escritório veterinário cantonal de Friburgo, Suíça.
1. Equipamento e configuração
- Organizar a produção de uma criosonda de aço inoxidável em uma oficina técnica que possa fabricar instrumentos para pesquisa.
NOTA: Forneça um design do instrumento com as dimensões específicas (Figura 1A). - Para evitar congelamento durante o manuseio da sonda durante o procedimento, insira a alça em uma ponta de pipeta e envolva-a com fita adesiva.
- Prepare um copo para a solução de trabalho de anestesia, uma colher para manusear os peixes, uma esponja úmida e um tanque com água do sistema para permitir que os peixes se recuperem após o procedimento.
- Prepare a solução de trabalho na hora antes de cada experimento. Para preparar a solução de trabalho, adicione 4 mL de solução-mãe de Tricaína a 100 mL de água do sistema em um copo.
NOTA: A solução estoque de anestesia consiste em 4 g de Tricaína dissolvida em 980 mL de água destilada. Depois de ajustar o pH para 7 com 1 M Tris-HCl, pH 9, encher a solução para 1 L com água destilada. A solução-mãe é sensível à luz e deve ser armazenada a 4 °C num frasco de âmbar.
2. Procedimento de criolesão muscular
- Inicie o procedimento mergulhando a sonda em nitrogênio líquido por um mínimo de 3 min. Molhe a esponja em água do sistema e coloque-a em uma superfície plana.
- Transfira um único peixe-zebra adulto para a solução de trabalho Tricaine e confirme sua falta de resposta tocando o peixe suavemente com a colher após 1 min ou 2 min. Se o peixe ainda estiver reativo, espere um pouco mais.
- Coloque o peixe anestesiado sobre a esponja molhada. Localizar o pedúnculo caudal posterior à nadadeira anal e anterior à nadadeira caudal.
- Retire a criosonda do nitrogênio líquido. Agite a sonda suavemente para garantir que não permaneça nitrogênio líquido residual na ponta.
- Posicionar a borda da espátula perpendicularmente ao corpo sobre o pedúnculo caudal (Figura 1C). Manter a sonda nessa posição por 6 s sem aplicar pressão (Figura 1D).
NOTA: O peso da criosonda é suficiente para garantir o contato entre o instrumento e o tecido. - Solte a criosonda do tecido e transfira os peixes para o tanque com água do sistema.
- Monitore o peixe enquanto ele retoma a respiração e a natação após acordar da anestesia. Se os movimentos operculares não ocorrerem após 30 s, estimule o peixe pipetando a água do sistema nas brânquias até que o animal inicie a respiração sozinho.
NOTA: Os peixes devem voltar a nadar dentro de alguns minutos no tanque de recuperação.
OBS: Nos dias seguintes, os peixes poderão ser filmados para monitorar sua atividade de natação (Vídeo 1 e Vídeo 2). Antes da gravação de vídeo, transfira o controle e os peixes feridos para um tanque de acasalamento translúcido e deixe-os habituar por pelo menos 1 minuto.
3. Coleta e fixação do pedúnculo caudal
- Preparar 2 mL de formalina a 4% ou outro fixador adequado para os ensaios subsequentes, uma placa de Petri, fórceps e tesoura cirúrgica.
- Eutanásia do peixe em um ponto de tempo selecionado após a criolesão, de acordo com a permissão legal dada pelo escritório veterinário regional.
NOTA: A eutanásia é realizada por uma sobredosagem de solução de tricaína (300 mg/L) durante aproximadamente 10 minutos. A perda do movimento branquial e o reflexo de pinça da nadadeira caudal confirmam a morte. Os momentos de eutanásia devem ser selecionados de acordo com a fase de regeneração: por exemplo, de 1 dia pós-criolesão (dpci) a 3 dpci para eliminação da ferida; de 3 dpci a 10 dpci para o início da regeneração muscular; de 10 dpci a 30 dpci para regeneração progressiva; e após 30 dpci para a realização da restauração tecidual. Assim, para avaliar as diferentes etapas e processos biológicos de degeneração e regeneração muscular, grupos de peixes precisam ser eutanasiados em vários momentos após a criolesão. - Coloque o peixe eutanasiado em uma placa de Petri contendo água deionizada. Utilizar tesoura para realizar um corte pelo corpo anterior e posterior ao pedúnculo caudal (Figura 1E). Deixe o tecido sangrar na água deionizada da placa de Petri.
- Recolher o pedúnculo caudal e transferi-lo com pinça para a solução de fixador preparada num tubo de microcentrífuga.
NOTA: Inverta cuidadosamente os tubos várias vezes e mantenha-os durante a noite a 4 °C.
4. Montagem do pedúnculo caudal
- Lave o tecido fixado em 1x PBS por 10 min em um balancim. Em seguida, transferi-lo para um tubo de microcentrífuga de 2 mL com sacarose a 30% pré-resfriada em água deionizada a 4 °C e inverter suavemente o tubo várias vezes. Deixar os tubos de microcentrífuga durante um mínimo de 24 h a 4 °C na posição vertical.
NOTA: O pedúnculo caudal flutuará em cima da solução de sacarose e começará a afundar à medida que o tecido desidrata. - Preencha um molde de incorporação com uma camada de 5 mm de meio de montagem O.C.T. Use pinça para ajustar o pedúnculo caudal no meio. Posicione-o na parte inferior do molde e ajuste sua orientação para cortes transversais ou coronais (Figura 1F).
- Deixe o meio congelar em uma caixa de gelo seco. Assim que o tecido estiver estabilizado na posição desejada, preencha o restante do molde antes que o O.C.T. congele completamente. Conservar o molde durante um período mínimo de 1 h a -80 °C.
NOTA: Nestas condições, os tecidos podem ser armazenados por muitos meses.
5. Cortar as seções com um criostato
- Montar um criostato com espessura de corte de 25 μm. Ajuste a temperatura da câmara para -26°C, a temperatura da amostra para -24°C e o ângulo de corte para 12°.
- Coloque o bloco congelado com o espécime no criostato, e fixe sua orientação de modo a cortar paralelamente ao fundo do bloco. Corte até chegar ao espécime e, em seguida, corte o bloco para facilitar a coleta da amostra.
- Prepare seis lâminas de adesão. Rotule as lâminas com números consecutivos para preparar réplicas da amostra.
- Inicie o corte e colete os cortes de tecido nas lâminas de adesão marcadas. Organize as seções nas lâminas de acordo com as demandas experimentais adicionais.
- Deixe as lâminas secar por 1 h em temperatura ambiente. Armazená-los em caixas fechadas a -20 °C.
NOTA: As lâminas podem ser armazenadas com segurança nesta condição por até 1 ano.
Resultados
Monitoramento dos peixes após criolesão
Para determinar o efeito da criolesão do miômero nos animais, foi realizada uma gravação em vídeo dos peixes controle e crioleado aos 1 dias pós-criolesão (dpci) e 5 dpci. Cada grupo continha cinco peixes. Em 1 dpci, os peixes crioleados estavam nadando menos ativamente, mas não apresentavam movimentos anormais, como turbilhonamento, convolução ou equilíbrio reduzido (Vídeo 1). No sistema de criação, sua posição no tanque e o consumo de alimento foram semelhantes aos dos peixes não lesionados. O comportamento normal persistiu ao longo dos dias seguintes, como exemplificado pelo vídeo em 5 dpci (Vídeo 2). Em conclusão, o procedimento de criolesão do pedúnculo caudal não afetou severamente o bem-estar dos animais.
Análise histológica dos cortes pedúnculos caudais
Para avaliar a extensão da lesão, foi selecionado o tempo de 4 dpci, que é quando o debris de miofibra foi completamente reabsorvido na ferida. Para analisar os efeitos da criolesão ao longo dos eixos dorso-ventral e anteroposterior do corpo, foram utilizados dois grupos de peixes (cortes coronal e transversal do pedúnculo caudal, respectivamente) (Figura 1F).
Os cortes foram analisados pela coloração tricrômico composta por Azul de Anilina, Fucsina Ácida e Laranja G (AFOG). Usando essa combinação de reagentes, os músculos intactos foram mostrados em laranja, a medula espinhal em vermelho escuro e a matriz colágena em azul. Para determinar o número de miômeros lesados, que são as unidades metaméricas da musculatura do peixe, uma série de cortes foi analisada (Figura 2). Os limites dos miômeros, chamados de miocommas, foram identificados pela deposição de colágeno, detectada pela coloração azul. As áreas danificadas foram determinadas pela ausência de coloração laranja. Um exame mais detalhado de espécimes com miocommas evidentes revelou que aproximadamente quatro miômeros consecutivos foram danificados, como inferido pela falta de coloração laranja (n, número de peixes = 4; Figura 3A,A'). O lado não lesionado do mesmo peixe serviu de referência interna.
Para examinar a profundidade da ferida perpendicular ao eixo do corpo, cortes transversais foram preparados usando peixe-zebra a 4 dpci e 7 dpci. Este último momento corresponde à ativação do programa miogênico e, portanto, ao início da regeneração muscular. A coloração AFOG desses espécimes mostrou uma extensa ausência de coloração alaranjada no flanco criolesionado do corpo, demarcando a zona de degeneração do músculo esquelético (Figura 3B,C). Em 4 dpci e 7 dpci, a área da ferida abrangeu tecidos da pele em direção ao septo vertical. Isso demonstra que o método de criolesão atingiu profundamente uma metade lateral do pedúnculo caudal, que permaneceu desprovida de músculo funcional por 7 dias após o procedimento. Juntos, quatro miômeros foram profundamente danificados em um lado do pedúnculo caudal.
Análise por imunofluorescência dos cortes transversais
Para avaliar a dinâmica da regeneração muscular, grupos experimentais de peixes foram eutanasiados a 4 dpci, 7 dpci, 10 dpci e 30 dpci. Os cortes transversais do pedúnculo caudal foram marcados por coloração multicolor de fluorescência usando faloidina (que se liga à actina filamentosa [F-actina]), anticorpo tropomiosina-1, que detecta uma proteína sarcômera, e DAPI, que marca núcleos. Em todos os momentos, a metade do corpo não lesionada fornecia um controle interno; tanto a F-actina quanto a tropomiosina 1 foram fortemente detectadas nas partes controle não lesadas, indicando tecido íntegro (Figura 4).
Aos 4 dpci, o lado lesado do pedúnculo caudal continha abundantes células positivas para DAPI, mas pouca ou nenhuma imunofluorescência com F-actina e tropomiosina 1 foi observada, indicando a zona da ferida com músculos degenerados (Figura 4A-B'). Aos 7 dpci, a tropomiosina 1 e a actina F puderam ser detectadas em uma parte da ferida próxima à linha média vertical do corpo (Figura 4C-D'). Esse padrão de expressão demarca a posição em que se inicia a formação de novas miofibras no pedúnculo caudal. A 10 dpci, ambos os marcadores musculares expandiram-se em direção à superfície do corpo, sugerindo regeneração progressiva do músculo esquelético (Figura 4E-F'). A 30 dpci, ambos os lados do corpo apresentaram distribuição semelhante da coloração F-actina (Figura 4G-H'). Esse achado indica que o músculo esquelético foi eficientemente restaurado após a criolesão do pedúnculo caudal.
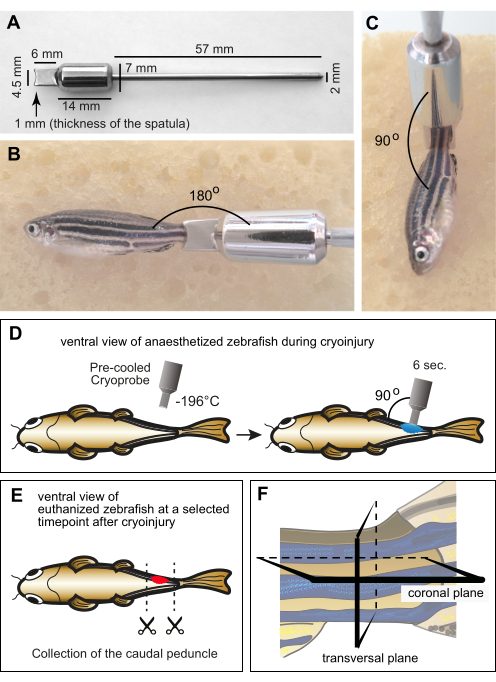
Figura 1: Configuração experimental para criolesão de miômero. (A) Dimensões da criosonda fabricada sob medida em aço inoxidável. A parte distal do instrumento consiste em uma espátula com borda côncava na profundidade de 1 mm para explicar a curvatura do corpo do peixe-zebra. A parte central da ferramenta é composta por um cilindro que funciona como um peso e um reservatório para manter a baixa temperatura da espátula durante o procedimento. A extremidade proximal do instrumento é na forma de uma alça fina de metal. (B,C) Peixes adultos anestesiados em uma esponja úmida com a criosonda no pedúnculo caudal. A sonda estava em temperatura ambiente. (B) A margem da sonda é colocada horizontalmente nas proximidades do pedúnculo caudal para exibir o tamanho relativo entre o peixe e a ferramenta. (C) Para criolesão, a ponta da ferramenta é posicionada perpendicularmente ao peixe. (D) Ilustração esquemática do procedimento de criolesão do lado ventral do peixe para mostrar as manipulações de forma abrangente. A criosonda foi pré-resfriada em nitrogênio líquido e imediatamente colocada em um dos lados dos peixes por 6 s. (E) Em um momento específico após a criolesão, os peixes foram eutanasiados e seus pedúnculos caudais foram coletados para fixação. (F) O material fixado foi processado histologicamente e seccionado nos planos coronal ou transversal. Clique aqui para ver uma versão maior desta figura.
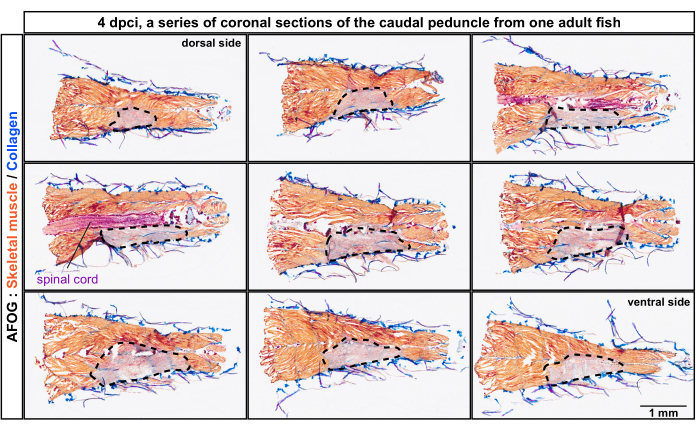
Figura 2: Análise histológica dos miômeros lesados no pedúnculo caudal desde a posição dorsal até a ventral do corpo. Coloração AFOG de uma série de cortes coronais aos 4 dias pós-criolesão (dpci). As seções são do dorsal em direção ao ventral, como indicado no topo do primeiro e do último painel. As seções são não adjacentes, com um intervalo de aproximadamente 150 μm entre elas. O músculo não lesado é detectado pela coloração laranja do músculo, enquanto o tecido lesado não possui essa coloração e parece acinzentado (área circundada por uma linha tracejada). Tecidos contendo colágeno, como a pele, são corados de azul. A medula espinhal aparece como uma estrutura semelhante a uma haste e é corada de vermelho. Número de peixes, n = 4. Clique aqui para ver uma versão maior desta figura.
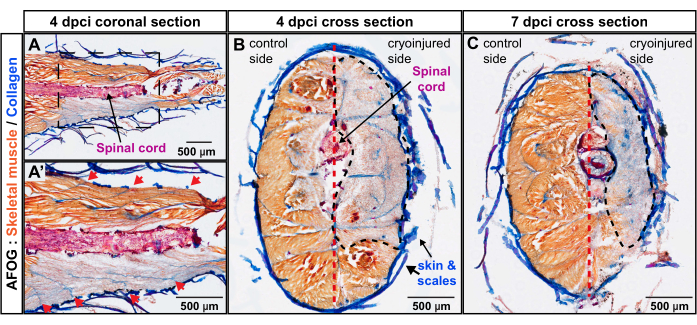
Figura 3: Avaliação da profundidade da lesão no pedúnculo caudal pela coloração AFOG. (A,A') A seção coronal está no nível da medula espinhal (uma haste horizontal corada de vermelho). A imagem inferior mostra uma área ampliada englobada por um quadro na imagem superior. Os limites sequenciais do miômero aparecem como listras colágenas (azuis) posicionadas obliquamente à medula espinhal (setas vermelhas na imagem ampliada A'). (B,C) Os cortes transversais mostram o flanco não lesado com músculos corados de laranja e o flanco crioleado com coloração acinzentada. A área danificada é cercada por uma linha tracejada preta. O septo vertical (representado com uma linha tracejada vermelha) subdivide o corpo nos lados controle e crioleado. Número de peixes, n = 4 por ponto de tempo. Clique aqui para ver uma versão maior desta figura.
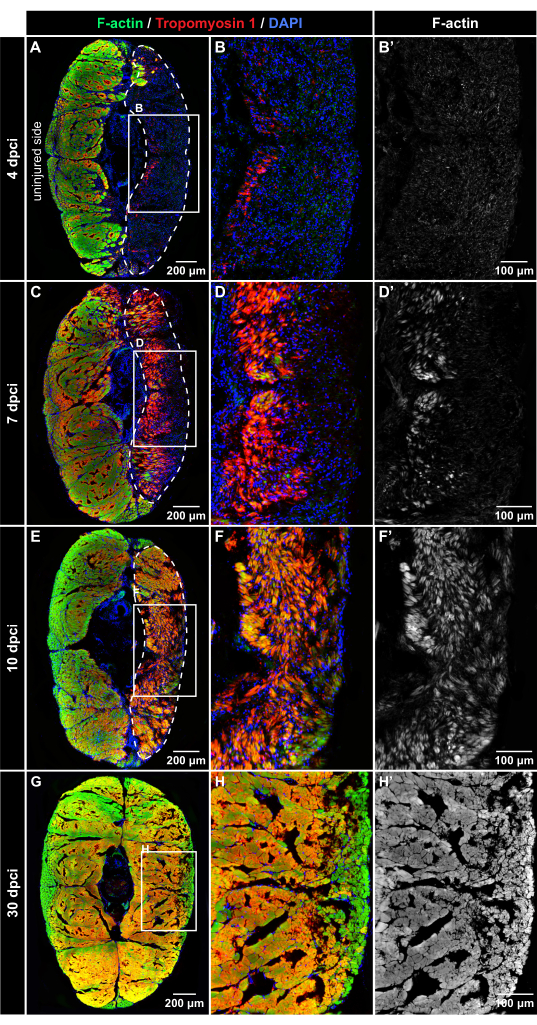
Figura 4: Detecção por imunofluorescência de proteínas musculares após criolesão. Coloração por fluorescência das seções transversais em 4 dpci, 7 dpci, 10 dpci e 30 dpci, conforme marcado no lado esquerdo e no topo dos painéis (A-B'). A 4 dpci, o tecido lesado (circundado com a linha tracejada) é DAPI-positivo (azul), mas desprovido de imunorreatividade à faloidina (verde) ou tropomiosina-1 (vermelho), sugerindo degeneração das fibras musculares após criolesão. (C-D') Aos 7 dpci, ambos os marcadores musculares emergem progressivamente na área lesionada, indicando o processo regenerativo. A tropomiosina-1 parece mais intensa que a F-actina nas fibras neoformadas. (E-F') A 10 dpci, a zona de lesão é preenchida por novas miofibras que apresentam maior intensidade de imunorreatividade à tropomiosina-1 em comparação à actina-F. (G-H') Em 30 dpci, um padrão semelhante de miofibras é detectado em ambos os lados do corpo. Os quadros nos painéis A, C, E e H abrangem as áreas que são ampliadas nas imagens adjacentes à direita. Escamas dérmicas, emanando fluorescência fora do miômero, foram apagadas das imagens usando Adobe Photoshop. Número de peixes, n = 4 por ponto de tempo. Clique aqui para ver uma versão maior desta figura.
Discussão
O zebrafish fornece um organismo modelo de vertebrado anamniota para estudar os mecanismos de regeneração muscular. A maioria dos métodos de lesão existentes, como ablação a laser ou ferimento por arma branca, resulta em ruptura tecidual relativamente pequena20,21,22,23. Ressecções maiores têm sido realizadas em músculoextraocular26. No entanto, essa abordagem cirúrgica provavelmente seria menos apropriada para a musculatura lateral devido aos riscos à saúde do corte da parede corporal. Para evitar tais procedimentos invasivos, este protocolo descreve uma forma mais branda de lesão que, no entanto, resulta em danos profundos ao pedúnculo caudal. Essa abordagem se baseia em uma manipulação superficial que permite o direcionamento muito preciso de alguns miômeros em um lado do corpo. Os pontos fortes do modelo de criolesão residem em sua reprodutibilidade e capacidade de produzir degeneração muscular extensa; Com base nesses pontos fortes, este modelo fornece um novo caminho para estudar como o corpo reage à perda muscular significativa.
A aplicação de frio extremo leva a um choque térmico, que destrói a membrana plasmática e organelas do tecido muscular afetado27. Como resultado, as miofibras lesadas sofrem morte celular "acidental"28. Consequentemente, o tecido danificado pode ser reabsorvido por mecanismos naturais de eliminação da ferida. Os peixes-zebra toleram bem o procedimento de criolesão, pois a taxa de sobrevivência neste estudo foi de quase 100%, uma vez que a sonda pré-resfriada foi posicionada corretamente no corpo durante a duração exata. No entanto, se a ferida for muito extensa (por exemplo, se for aplicada muita pressão ou se a duração da criolesão for muito longa), o peixe pode apresentar movimentos de natação aberrantes logo após o procedimento, e o animal deve ser sacrificado como um desfecho humano. Para outras espécies de peixes, o tempo de exposição à criosonda deve ser ajustado de acordo com o tamanho do corpo.
Após a criolesão, os peixes podem retomar sua atividade de natação sem qualquer sintoma de movimento anormal. No entanto, os peixes criolesionados nadam menos dinamicamente do que os peixes controle, o que indica alguns comprometimentos leves. Uma maior quantificação do comportamento dos peixes em diferentes momentos após a criolesão será necessária para determinar mudanças temporais no desempenho de natação.
O efeito do método de criolesão em outros tecidos não musculares do pedúnculo caudal ainda precisa ser elucidado. Obviamente, a camada mais externa do corpo (ou seja, a pele) é danificada pelo procedimento. Nesse contexto, o método criolesão pode fornecer uma nova estratégia para o estudo da cicatrização de feridas, regeneração de incrustações e restauração do padrão de pigmentação. Além disso, a vasculatura e a inervação dos miômeros também podem ser afetadas pela criolesão, e esses tópicos requerem maiores investigações.
O modelo de criolesão já foi utilizado para investigar a regeneração cardíaca do peixe-zebra13,14,15,29. Esse método apresentou algumas vantagens em relação ao método de ressecçãoventricular10 devido à deposição transitória de cicatriz rica em colágeno, que mimetiza melhor a resposta cicatricial do infarto em humanos30. Notavelmente, o peixe-zebra pode regenerar seu coração após múltiplascriolesões31. Curiosamente, a criolesão também tem sido aplicada na nadadeira do peixe-zebra, resultando em processoshistolíticos12. Ao contrário da amputação clássica da nadadeira, o coto crioleado remanescente contém uma margem distorcida com uma mistura de material morto e células saudáveis. Estudos com ambos os órgãos do peixe-zebra, o coração e a nadadeira, revelaram a poderosa capacidade do peixe-zebra de restaurar seus componentes funcionais originais, mesmo após extensos danos teciduais. Se o músculo esquelético crioleado ativa uma interação entre processos reparativos e regenerativos justifica estudos futuros.
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
Agradecemos a V. Zimmermann pelo cuidado com os peixes, bem como ao Dr. Thomas Bise, Dra. Catherine Pfefferli e Lea Gigon pelo início deste projeto e seus resultados preliminares. Este trabalho foi apoiado pela Swiss National Science Foundation, processo número 310030_208170.
Materiais
| Name | Company | Catalog Number | Comments |
| Program | |||
| ImageJ | National Institutes of Health (NIH) | ||
| Photoshop Version 23.5.3 | Adobe | ||
| Material/ Equipment | |||
| 35/10 mm Petri Dish | Greiner Bio-one | Item No.: 627102 | |
| Camera | Sony | / | HDR-PJ410 |
| Cryostat | Histcom | HRA C50 | |
| Formaldehyde ~36% | Sigma-Aldrich | 47630 | |
| Macro 50 mm f/2.8 EX DG lens | Sigma | / | Discontinued lense |
| Peel-A-Way Embedding Truncated Molds T8 | Polyscience, Inc. | 18985 | |
| Slides Superfrost Plus | Fisher Scientific | 12-550-15 | |
| Sponge | any | any | flat sponge, c.a. 7cm x 3 cm x 1 cm |
| Stainless steel cryoprobe | Custom-made | / | specifics in the article |
| Sucrose | Sigma-Aldrich | 84100 | |
| Surgical scissors | Any | / | |
| TCS SP2 | Leica | / | Discontinoued product |
| Tissue-Tek O.C.T. compound | Sakura Finetek | 4583 | |
| Tricaine (Anestethic) | Sigma | E10521 | |
| Dyes and Antibodies | |||
| Dapi | Sigma | 10236276001 | Concentration: 1/2000 |
| Phalloidin-Atto-565 (F-actin) | Sigma | 94072 | Concentration: 1 / 500 |
| Tropomyosin (TPM1) | DHSB | CH1 | Concentration: 1 / 50 |
| Recipies/Solutions | |||
| 1x PBS | 123 mM NaCl | Sigma | |
| 2.7 mM KCl | Sigma | ||
| 10 mM Na2HPO4 | Sigma | ||
| 1.8 mM KH2PO4 | Sigma | ||
| AFOG solution | 3 g Fuchsin | Fisher Scientific | |
| 2 g Orange G | Sigma | ||
| 1 g Anilin blue | Fulka AG | ||
| 200 ml acifidied distilled H2O (pH 1.1) |
Referências
- Muneoka, K., Allan, C. H., Yang, X., Lee, J., Han, M. Mammalian regeneration and regenerative medicine. Birth Defects Research Part C: Embryo Today: Reviews. 84 (4), 265-280 (2008).
- Carlson, B. M. Some principles of regeneration in mammalian systems. Anatomical Record. Part B, New Anatomist. 287 (1), 4-13 (2005).
- Dumont, N. A., Bentzinger, C. F., Sincennes, M. -. C., Rudnicki, M. A. Satellite cells and skeletal muscle regeneration. Comprehensive Physiology. 5 (3), 1027-1059 (2015).
- Relaix, F., et al. Perspectives on skeletal muscle stem cells. Nature Communications. 12 (1), 692 (2021).
- Tulenko, F. J., Currie, P., Cartner, S. C. Zebrafish myology. The Zebrafish in Biomedical Research. , 115-121 (2020).
- Siegel, A. L., Gurevich, D. B., Currie, P. D. A myogenic precursor cell that could contribute to regeneration in zebrafish and its similarity to the satellite cell. The FEBS Journal. 280 (17), 4074-4088 (2013).
- Corona, B. T., Wenke, J. C., Ward, C. L. Pathophysiology of volumetric muscle loss injury. Cells Tissues Organs. 202 (3-4), 180-188 (2016).
- Pfefferli, C., Jaźwińska, A. The art of fin regeneration in zebrafish. Regeneration. 2 (2), 72-83 (2015).
- Sehring, I. M., Weidinger, G. Recent advancements in understanding fin regeneration in zebrafish. WIREs Developmental Biology. 9 (1), 367 (2020).
- Poss, K. D., Wilson, L. G., Keating, M. T. Heart regeneration in zebrafish. Science. 298 (5601), 2188-2190 (2002).
- Sanz-Morejón, A., Mercader, N. Recent insights into zebrafish cardiac regeneration. Current Opinion in Genetics & Development. 64, 37-43 (2020).
- Chassot, B., Pury, D., Jaźwińska, A. Zebrafish fin regeneration after cryoinjury-induced tissue damage. Biology Open. 5 (6), 819-828 (2016).
- Chablais, F., Veit, J., Rainer, G., Jaźwińska, A. The zebrafish heart regenerates after cryoinjury-induced myocardial infarction. BMC Developmental Biology. 11, 21 (2011).
- Schnabel, K., Wu, C. C., Kurth, T., Weidinger, G. Regeneration of cryoinjury induced necrotic heart lesions in zebrafish is associated with epicardial activation and cardiomyocyte proliferation. PLoS One. 6 (4), e18503 (2011).
- Gonzalez-Rosa, J. M., Martin, V., Peralta, M., Torres, M., Mercader, N. Extensive scar formation and regression during heart regeneration after cryoinjury in zebrafish. Development. 138 (9), 1663-1674 (2011).
- Ryan, R., Moyse, B. R., Richardson, R. J. Zebrafish cardiac regeneration-Looking beyond cardiomyocytes to a complex microenvironment. Histochemistry and Cell Biology. 154 (5), 533-548 (2020).
- Jaźwińska, A., Sallin, P. Regeneration versus scarring in vertebrate appendages and heart. Journal of Pathology. 238 (2), 233-246 (2016).
- Alexander, R. The orientation of muscle fibres in the myomeres of fishes. Journal of the Marine Biological Association of the United Kingdom. 49, 163-290 (1969).
- Morin-Kensicki, E. M., Melancon, E., Eisen, J. S. Segmental relationship between somites and vertebral column in zebrafish. Development. 129 (16), 3851-3860 (2002).
- Berberoglu, M. A., et al. Satellite-like cells contribute to pax7-dependent skeletal muscle repair in adult zebrafish. Developmental Biology. 424 (2), 162-180 (2017).
- Montandon, M., Currie, P. D., Ruparelia, A. A. Examining muscle regeneration in zebrafish models of muscle disease. Journal of Visualized Experiments. (167), e62071 (2021).
- Pipalia, T. G., et al. Cellular dynamics of regeneration reveals role of two distinct Pax7 stem cell populations in larval zebrafish muscle repair. Disease Models & Mechanisms. 9 (6), 671-684 (2016).
- Ratnayake, D., et al. Macrophages provide a transient muscle stem cell niche via NAMPT secretion. Nature. 591 (7849), 281-287 (2021).
- Kaliya-Perumal, A. -. K., Ingham, P. W. Musculoskeletal regeneration: A zebrafish perspective. Biochimie. 196, 171-181 (2022).
- Aleström, P., et al. Zebrafish: Housing and husbandry recommendations. Laboratory Animals. 54 (3), 213-224 (2019).
- Saera-Vila, A., et al. Myocyte dedifferentiation drives extraocular muscle regeneration in adult zebrafish. Investigative Ophthalmology & Visual Science. 56 (8), 4977-4993 (2015).
- Baust, J. G., Gage, A. A. The molecular basis of cryosurgery. BJU International. 95 (9), 1187-1191 (2005).
- Galluzzi, L., et al. Molecular mechanisms of cell death: recommendations of the Nomenclature Committee on Cell Death 2018. Cell Death and Differentiation. 25 (3), 486-541 (2018).
- Chablais, F., Jaźwińska, A. Induction of myocardial infarction in adult zebrafish using cryoinjury. Journal of Visualized Experiments. (62), e3666 (2012).
- Chablais, F., Jaźwińska, A. The regenerative capacity of the zebrafish heart is dependent on TGFbeta signaling. Development. 139 (11), 1921-1930 (2012).
- Bise, T., Sallin, P., Pfefferli, C., Jaźwińska, A. Multiple cryoinjuries modulate the efficiency of zebrafish heart regeneration. Scientific Reports. 10 (1), 11551 (2020).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados