Method Article
Мониторинг белково-лигандных взаимодействий в клетках человека с помощью количественного внутриклеточного ЯМР в режиме реального времени с использованием биореактора высокой плотности клеток
В этой статье
Резюме
Этот протокол описывает настройку биореактора ЯМР для поддержания жизнеспособности инкапсулированных клеток человека в течение 72 ч, с последующим сбором и анализом внутриклеточных данных ЯМР с временным разрешением. Методика применяется для мониторинга внутриклеточных белково-лигандных взаимодействий в режиме реального времени.
Аннотация
Внутриклеточный ЯМР – это уникальный подход к наблюдению структурных и динамических свойств биологических макромолекул при атомном разрешении непосредственно в живых клетках. Можно наблюдать сворачивание белка, химические модификации и конформационные изменения, вызванные связыванием лигандов. Поэтому данный метод имеет большой потенциал в контексте разработки лекарственных средств. Однако короткое время жизни клеток человека, заключенных в ЯМР-спектрометре, ограничивает диапазон применения внутриклеточного ЯМР. Чтобы преодолеть эту проблему, используются биореакторы ЯМР, которые могут значительно улучшить стабильность образца клеток с течением времени и, что важно, позволяют регистрировать в реальном времени спектры ЯМР в клетке. Таким образом, эволюция таких процессов, как проникновение лиганда и связывание с внутриклеточной белковой мишенью, может контролироваться в режиме реального времени. Биореакторы часто ограничены низкой жизнеспособностью клеток при высоком количестве клеток, что приводит к компромиссу между общей чувствительностью эксперимента и жизнеспособностью клеток. Недавно мы сообщили о биореакторе ЯМР, который поддерживает высокое количество метаболически активных клеток человека в течение длительных периодов времени, до 72 ч. Эта установка была применена для мониторинга белково-лигандных взаимодействий и химической модификации белка. Мы также ввели рабочий процесс для количественного анализа данных ЯМР в реальном времени, основанный на многомерном разрешении кривой. Способ обеспечивает профили концентраций химических веществ, присутствующих в клетках, в зависимости от времени, которые могут быть дополнительно проанализированы для получения соответствующих кинетических параметров. Здесь мы приводим подробное описание установки биореактора ЯМР и его применения для мониторинга белково-лигандных взаимодействий в клетках человека.
Введение
Внутриклеточная спектроскопия ядерного магнитного резонанса (ЯМР) в последнее время стала мощным подходом к исследованию структурных и динамических свойств макромолекул в клеточной среде1,2,3,4,5,6. Внутриклеточный ЯМР преуспел в исследовании функционально значимых процессов, таких как сворачивание/неправильное сворачивание белка7,8,9, связывание металлов7,10, образование дисульфидных связей11,12 и белково-белковое взаимодействие13, взаимодействие белок-лиганд14,15,16 и взаимодействие нуклеиновых кислот-лигандов17 ,18 в живых клетках человека. Одним из ограничивающих факторов применения ЯМР в клетках является короткое время жизни клеток во время эксперимента. Решение этой проблемы предполагает использование биореакторов ЯМР. В этих устройствах постоянный поток питательной среды применяется к клеткам, которые содержатся в пределах ЯМР-спектрометра, чтобы обеспечить кислород и питательные вещества и удалить токсичные побочные продукты. После появления внутриклеточных ЯМР было разработано несколько конструкций биореакторов ЯМР для повышения жизнеспособности клеток в течение более длительных периодов времени, в которых либо бактерии, либо клетки млекопитающих инкапсулируются в гидрогель19,20,21,22 или хранятся во взвешенном состоянии и перфузируются с помощью микродиализной мембраны23. . Такие биореакторы позволили получить более длительные эксперименты ЯМР с повышенным отношением сигнал/шум (S/N)5 и, что еще более важно, могли быть использованы для исследования клеточных процессов в режиме реального времени22,23,24. Благодаря высокой химической и конформационной чувствительности ЯМР, последнее применение может дать ценную информацию о кинетике функциональных процессов в живых клетках с атомным разрешением.
В этом протоколе мы показываем, как настроить и эксплуатировать улучшенный биореактор, о котором недавно сообщалось25, который был получен путем объединения существующей модульной конструкции биореактора23 с подходом, основанным на инкапсуляции клеток в гидрогеле, которые были впервые предложены другими группами19,20,21,22,26,27 . Описано применение биореактора к внутриклеточным ЯМР-исследованиям внутриклеточного белка с наблюдением за связыванием лигандов в клетках HEK293T в режиме реального времени. В биореакторе клетки инкапсулируются с высокой плотностью в нити агарозного геля и поддерживаются высокожизнеспособными и метаболически активными в течение 72 ч, в течение которых регистрируются внутриклеточные ЯМР-эксперименты в режиме реального времени. Биореактор состоит из стеклянной трубки, которая подходит для стандартных 5 мм ЯМР-зондов, которые являются водонепроницаемыми и подключены к держателю трубки, так что внутренняя камера для отбора проб имеет внутренний диаметр 4,2 мм, высоту 38 мм и объем 526 мкл. Входное отверстие представляет собой капилляр PEEK длиной 7 метров (o.d. = 1/32", т.д. = 0,5 мм), вставленный в камеру для отбора проб до ~6 мм от нижней части, в то время как выходное отверстие представляет собой капилляр PTFE длиной 7 метров (o.d. = 1/32", т.д. = 0,5 мм), прикрепленный в верхней части держателя трубки (рисунок 1). Трубка соосно вставляется в регулируемую температуру линию, соединенную с водяной баней. Входное и выходное отверстие соединены через трубку PEEK с 4-ходовым 2-позиционным клапаном, прикрепленным к насосу FPLC для управления потоком среды и контейнером для отходов.
Биореактор применяется для изучения кинетики взаимодействия, о котором сообщалось ранее14,25, между двумя препаратами, ацетазоламидом (AAZ) и метазоламидом (MZA), в клетках человека со второй изоформой карбоангидразы человека (CA II), фармакологически значимой мишенью28,29,30, и кинетики образования внутримолекулярной дисульфидной связи, стимулируемой малой молекулой ebselen25, 31, из не содержащей меди, связанной с цинком формы человеческой меди, супероксиддисмутазы цинка (SOD1), антиоксидантного фермента, участвующего в возникновении бокового амиотрофического склероза7,8,32. Наконец, количественный анализ данных ЯМР в реальном времени выполняется в MATLAB с использованием алгоритма Multivariate Curve Resolution-Alternating Least Squares (MCR-ALS)33, с помощью которого для наблюдаемых видов получаются чистые спектральные компоненты и профили концентраций в зависимости от времени, которые могут быть дополнительно проанализированы для получения соответствующих кинетических параметров.
Протокол начинается с колбы T75 из клеток HEK293T (~ 3 x 107 клеток на колбу), временно переэкспрессирующих либо человеческий CA II (без маркировки), либо человеческий SOD1 (меченый 15N). Клетки выращивали и поддерживали в колбах Т75 с высоким содержанием глюкозы DMEM по 1:10 проходов каждые 3-4 дня и трансфицировали кДНК, кодирующей интересующий белок за 48 ч до начала эксперимента. О шагах, связанных с этим этапом, подробно сообщается в другом месте34.
протокол
1. Настройка реагента и раствора
- Для получения полного DMEM добавьте 5 мл L-глутамина 200 мМ, 5 мл пенициллина-стрептомицина 100x и 50 мл фетальной бычьей сыворотки (FBS, 10% об/об конечная концентрация) до 440 мл DMEM.
ПРИМЕЧАНИЕ: Этот раствор можно хранить при температуре 4 °C в течение 1 месяца. - Готовят раствор агарозы, растворяя 150 мг низкогелеобразующей агарозы в 10 мл фосфатно-буферного физиологического раствора (PBS) при 85 °C для получения 1,5% (мас./об.) раствора. Стерилизуйте путем фильтрации с помощью фильтра 0,22 мкм. Приготовить 1 мл аликвоты раствора агарозы в колпачках по 1,5 мл и хранить при температуре 4 °C.
- Подготовьте биореакторную среду.
- Растворить 13,4 г порошка DMEM в 1 л сверхчистого H2O.
ПРИМЕЧАНИЕ: В зависимости от применения требуемый конечный объем может отличаться (например, для среды объемом 500 мл растворить 6,7 г порошка в 500 мл H2O). - Добавьте 2% FBS, 10 мМ NaHCO3, 1x пенициллин-стрептомицин (100x) и 2% D2O (например, для среды 500 мл добавьте 10 мл FBS, 0,4 г NaHCO3, 5 мл пенициллина-стрептомицина 100x и 10 мл D2O).
- Измерьте pH с помощью pH-метра и при необходимости отрегулируйте до 7,4, добавив HCl.
ПРИМЕЧАНИЕ: Как правило, начальный рН очень близок к 7,4. - Фильтруйте среду биореактора с помощью вакуумного стерильного фильтра в стерильной стеклянной бутылке объемом 250 мл или 500 мл.
- В ламинарной проточной вытяжке запечатайте бутылку головным убором из стерильной стали с двумя шланговыми соплами и подключите их к трубке FEP (o.d. = 1/8", т.д. = 1,6 мм), которая будет подключена к насосу и к шприцевому фильтру из PTFE 0,22 мкм для забора воздуха.
- Растворить 13,4 г порошка DMEM в 1 л сверхчистого H2O.
2. Настройка биореактора
- Соберите блок потока с помощью трубки ЯМР второго проточного блока, которая впоследствии будет заменена на ту, которая содержит ячейки. Обратитесь к инструкциям по эксплуатации проточного блока для правильной сборки.
ПРИМЕЧАНИЕ: На этом этапе блок потока должен быть уже очищен (если нет, выполните шаг 4.2). - Установите водяную баню, подключенную к регулятору температуры проточного блока, на 37 °C. Поместите бутылку с резервуаром на водяную баню.
- Подключите трубку FEP резервуарного баллона к насосу.
- Поверните клапан биореактора на «байпас» и предварительно засыпьте насос средой.
- Поверните клапан биореактора в «поток» и предварительно заполните биореактор средой со скоростью 0,1 мл/мин.
3. Подготовка образца клетки
- Соберите клетки из CO2-инкубатора .
- Возьмите колбу T75 с трансфектированными клетками HEK293T из ИНКУБАТОРА CO2 и удалите отработанную среду.
- Дважды промывайте ячейки 7 мл (каждая) PBS при комнатной температуре (~20 °C).
- Используйте 2 мл трипсина / ЭДТА для отделения клеток. После добавления раствора инкубируют в течение 5 мин при комнатной температуре, чтобы отсоединить клетки.
ПРИМЕЧАНИЕ: Трансфектированным клеткам может потребоваться немного больше времени, чтобы отсоединиться. При необходимости инкубируют клетки при 37 °C. - Инактивировать трипсин с 20 мл полного DMEM; тщательно повторно суспендировать ячейки путем пипетки вверх и вниз и перенести их в центрифужную трубку объемом 50 мл.
- Центрифугируйте ячейки при 800 х г в течение 5 мин при комнатной температуре и выбросьте супернатант.
- Промыть ячейки 10 мл PBS при комнатной температуре, чтобы удалить остаточную среду.
- Центрифугируйте ячейки при 800 х г в течение 5 мин при комнатной температуре и выбросьте супернатант.
- Переложите гранулу ячейки в микроцентрифужную трубку объемом 1,5 мл.
- Встраивайте клетки в агарозные нити.
- Растопить одну аликвоту затвердевшей агарозы при 85 °С на водяной бане и впоследствии сохранить ее в растворе при 37 °С в блок-нагревателе.
- Пипеткой Пастера заполните дно проточной ямР-трубки 60-70 мкл 1,5% агарозного геля и поместите его в лед. Это создаст нижнюю заглушку высотой ~5 мм, которая позволит поместить образец ячейки в активный объем катушки ЯМР 1H.
- Нагревают гранулы ячеек, полученных на стадии 3.1.8 при 37 °С в течение 15−20 с в термоблоке.
- Повторное суспендирование клеток в 450 мкл раствора агарозы. Будьте осторожны, чтобы избежать образования пузырьков.
- Аспирировать клеточно-агарозную суспензию в хроматографическую трубку PEEK длиной ~30 см (т.д. = 0,75 мм), соединенную со шприцем объемом 1 мл.
ПРИМЕЧАНИЕ: Перед аспирацией трубка и мертвый объем шприца должны быть предварительно заполнены PBS при комнатной температуре, чтобы избежать образования пузырьков. Длина трубки не критична. - Дайте трубке остыть при комнатной температуре в течение 2 мин.
- Предварительно залейте проточную трубку ЯМР 100 мкл PBS при комнатной температуре.
- Литые нити ячеек, встроенных в агарозу, в проточную установку ЯМР-трубки путем осторожного нажатия шприца.
ПРИМЕЧАНИЕ: Чтобы заполнить ЯМР-трубку однородно, начните с размещения конца трубки PEEK в нижней части трубки ЯМР и продолжайте двигаться к вершине, медленно раскачиваясь влево-вправо. - Повторяйте шаги 3.2.5, 3.2.6 и 3.2.8 до тех пор, пока не будет отлита вся суспензия клеточной агарозы.
- Вставьте клетки в биореактор.
- Извлеките пустую ЯМР-трубку из проточного блока и увеличьте скорость потока до 2 мл/мин в течение нескольких минут, чтобы удалить остаточные пузырьки газа во входной трубке.
- Установите скорость потока на 0,2 мл/мин и вставьте ЯМР-трубку, содержащую ячейки, медленно, но неуклонно подталкивая ее вверх.
ПРИМЕЧАНИЕ: Активный поток среды позволяет избежать обратного потока содержимого трубки через входное отверстие, которое в противном случае произошло бы во время введения.
4. Эксплуатация и очистка биореактора
- Работа биореактора во время эксперимента ЯМР.
- Установите температуру в ЯМР-спектрометре на уровне 310 К.
- Вставьте блок потока в спектрометр.
- Подавайте биореакторную среду со скоростью потока 0,1 мл/мин в течение всего времени экспериментов ямР в клетке.
- В нужное время во время эксперимента вводят концентрированный раствор внешней молекулы в бутылку со средним резервуаром, прокалывая силиконовую трубку стерильным длинноигольным шприцем.
ПРИМЕЧАНИЕ: Окончательная концентрация молекулы в среде должна быть выбрана на основе предыдущих знаний о клеточной токсичности и, при наличии, на основе прогнозируемой/предполагаемой скорости диффузии через клеточную мембрану. - В конце эксперимента С ЯМР замените трубку, содержащую ячейки, пустой трубкой и промойте проточный блок водой.
- Биореактор очищается на месте.
- Очистите блок потока, протекая следующие растворы со скоростью 1 мл/мин: 0,2 М гидроксида натрия (NaOH); 3 М лимонной кислоты; 0,2 М NaOH, в течение не менее 30 мин каждый, а затем стерильно-фильтрованная сверхчистая вода в течение >2 ч.
- Очищайте и автоклавируйте резервуар бутылки и трубки в сборе после каждого прогона.
5. ЯМР-эксперименты
- Настройка ЯМР-экспериментов.
ПРИМЕЧАНИЕ: Выполните эти шаги заранее, до подготовки внутриклеточного образца ЯМР, чтобы избежать каких-либо задержек между сбором клеток и сбором данных.- Создайте новый набор данных на ЯМР-спектрометре и задайте параметры для нужных ЯМР-экспериментов.
- Задайте параметры для ЯМР-экспериментов 1D 1H.
- Центрируйте несущую частоту 1H на уровне 4,7 ppm на сигнале воды.
- Выберите импульсную программу zgesgp, установите спектральную ширину на 20 ppm и квадратный импульс 1000 мкс 180° для подавления воды. Установите задержку между сканированием 1 с. Получите спектр с помощью 32 сканирований.
- Для клеток, экспрессирующих немаркированный CA II: выберите импульсную программу p3919gp, установите спектральную ширину 30 ppm для покрытия области имино спектра и отрегулируйте задержку для подавления биномиальной воды таким образом, чтобы максимальное возбуждение было сосредоточено на химических сдвигах интересующих сигналов (d7 = 20 мкс при 950 МГц). Установите задержку между сканированием ≥1 с. Получение с помощью 512 сканов.
- Для ячеек, экспрессирующих 15N-меченый SOD1: выберите импульсную программу sfhmqf3gpph, установите спектральную ширину 1H и 15N на 16 и 50 ppm соответственно, ширину смещения и возбуждения фигурного импульса на 8,5 и 6 ppm соответственно и импульс 350 мкс для схемы разъединения (garp4 или другая в зависимости от прибора). Установите задержку между сканированием 0,3 с. Приобретайте с помощью 16 сканирований и 128 приращений в измерении 15N.
- Получение ЯМР-спектров в режиме реального времени.
- После того, как биореактор вставлен в ЯМР-спектрометр, подождите несколько минут, чтобы обеспечить обмен среды.
ПРИМЕЧАНИЕ: Этот процесс легко контролируется с момента появления сигнала блокировки, поскольку PBS заменяется средой, содержащей 2% D2O. - Отрегулируйте согласование и настройку канала 1H, нажмите на магнит и рассчитайте длину жесткого импульса 1H 90°.
- Отрегулируйте уровни мощности 1H в каждой последовательности импульсов в соответствии с жестким импульсом 1H.
- Запишите первый спектр zgesgp 1H, чтобы проверить содержание образца и однородность поля.
- Скопируйте эксперименты zgesgp и p3919gp/sfhmqcf3gpph на нужное число и поставьте их в очередь в диспетчере очереди получения.
ПРИМЕЧАНИЕ: Спектры zgesgp используются только для управления состоянием образца и однородностью поля; поэтому их можно пропускать или записывать реже. - Для ячеек, экспрессирующих немаркированный CA II: обработайте спектры p3919gp, применив нулевое заполнение и экспоненциальную функцию окна расширения линии (LB = 20 Гц).
- Для ячеек, экспрессирующих 15N-меченый SOD1: обработайте спектры sfhmqcf3gpph, применяя нулевое заполнение и квадратную функцию синусоидального окна (SSB = 2) в обоих измерениях.
ПРИМЕЧАНИЕ: Размер обрабатываемых спектров может быть дополнительно уменьшен путем удаления областей, свободных от сигналов (в Topspin это делается путем установки желаемых значений STSR и STSI).
- После того, как биореактор вставлен в ЯМР-спектрометр, подождите несколько минут, чтобы обеспечить обмен среды.
6. Анализ MCR-ALS
- Для анализа спектров CA II импортируйте 1D спектральные области в MATLAB R2019b.
- В программном обеспечении создайте список экспериментов для экспорта в меню Список наборов данных процесса .
- Используя модифицированную версию программы au convbin2asc, экспортируйте интересующую спектральную область в формате ASCII для каждого спектра.
ПРИМЕЧАНИЕ: При этом создается текстовый файл с именем ascii-spec.txt в каждом подкаталоге спектра. - В MATLAB импортируйте спектральные области с помощью пользовательского скрипта Load_ascii_spectra.
ПРИМЕЧАНИЕ: Этот скрипт требует каталог набора данных в качестве входных данных и создает спектры 2D-массива, содержащие стекированные 1D-спектры, и 1D-массив cs, содержащий химические сдвиги. - Запустите сценарий Load_acqus, чтобы извлечь метки времени из 1D-спектров.
ПРИМЕЧАНИЕ: Этот скрипт создает 1D-массив times_hours, содержащий приращение времени для каждого спектра, выраженного в часах, с начальным спектром во времени = 0.
- Для анализа спектров SOD1 импортируйте 2D спектры в MATLAB R2020b.
- В Topspin создайте список экспериментов для экспорта в меню Список наборов данных процесса .
- В MATLAB импортируйте 2D-спектры с помощью пользовательского скрипта Load_2D_spectra.
ПРИМЕЧАНИЕ: Этот скрипт требует каталог набора данных в качестве входных данных и создает 3D-массив Spectra, содержащий стекированные 2D-спектры, и 1D-массив cs, содержащий химические сдвиги. - Запустите сценарий Load_acqus, чтобы извлечь метки времени из 2D-спектров.
- Укажите спектральные области, представляющие интерес, в пользовательском скрипте Cut_2D_spectra и запустите скрипт для вырезания 3D-подмассивов [(1H x 15N) спектральных интенсивностей) x времени]; измените их форму как 2D-массивы (временные точки x спектральные интенсивности) и соедините их вместе.
ПРИМЕЧАНИЕ: Это создает 2D-массив JoinSpec_flat, содержащий измененные и объединенные спектральные области.
- Запустите MCR-ALS 2.0 в режиме графического интерфейса.
- Откройте графический интерфейс MCR-ALS 2.0, выполнив сценарий mcr_main.
- На вкладке Выбор данных загрузите спектры или матрицу JoinSpec_flat. Данные могут быть построены для проверки.
- Оцените количество компонентов либо с помощью разложения сингулярных значений (SVD), либо вручную.
ПРИМЕЧАНИЕ: Количество компонентов должно соответствовать количеству отдельных видов, присутствующих в эксперименте. В этом случае n = 2, соответствующее свободному и связанному белку. - Выберите метод начальной оценки чистых спектров. Можно использовать либо чистейшее обнаружение переменных, либо эволюционирующий факторный анализ (EFA).
- В окне Выбор набора данных нажмите кнопку Продолжить.
- Задайте ограничения для концентраций в окне Ограничения: режим строки . Примените ограничение неотрицательности, выберите fnnls (Быстрые неотрицательные наименьшие квадраты) как «реализация и 2 вида». Примените 1 ограничение закрытия, установите ограничение на 1, условие закрытия как «равное» и примените ко всем видам.
ПРИМЕЧАНИЕ: Это заставляет сумму концентраций каждого вида быть равной 1, так что полученные профили каждого вида нормализуются относительно общей концентрации белка. - Задайте ограничения для спектров в окне Ограничения: Режим столбца . Примените ограничение неотрицательности, выберите fnnls как «реализация и 2 вида».
ПРИМЕЧАНИЕ: Это ограничение не должно применяться, если отрицательные сигналы присутствуют в спектрах ЯМР. - В последнем окне задайте 50 итераций и критерий сходимости 0,01. Укажите выходные имена для значений Концентрации, Спектры и Std. отклонения. Нажмите «Продолжить», чтобы запустить фитинг MCR-ALS.
ПРИМЕЧАНИЕ: Графическое окно покажет результат подгонки с графиками профилей концентрации и спектров чистых компонентов. - Для набора данных SOD1: используйте пользовательский скрипт Rebuild_2D_spectra для реконструкции 2D-спектральных областей из 1D-выхода MCR-ALS и их построения.
7. Тест трипана синего
- Восстановите содержание ЯМР-трубки с помощью пипетки Пастера и переложите нити агарозы в трубку с крышкой 1,5 мл.
- Удалить остаточную среду, промыв нити агарозы 600 мкл PBS и центрифугировать их при 4000 х г в течение 1 мин при комнатной температуре. Выбросьте супернатант.
- Добавьте 250 мкл PBS и 50 мкл 0,4% раствора трипана синего цвета.
- Инкубировать в течение 2 мин с непрерывным пипетированием.
- Дважды промыть 600 мкл PBS, выбрасывая супернатант.
- Поместите несколько нитей агарозы на предметное стекло микроскопа и нарежьте их лезвиями бритвы, чтобы создать небольшие кусочки геля. Для анализа выберите самые тонкие срезы (толщина < 0,4 мм, в идеале ~0,2 мм).
- Переложите кусочки геля в самодельную ячейку счетной камеры, состоящую из двух стеклянных слайдов, разделенных тремя слоями парафиновой пленки (~ 0,4 мм общей толщины) с каждой стороны.
ПРИМЕЧАНИЕ: Можно также использовать затвор камеры; однако срезы геля толще высоты камеры (0,1 мм) будут сжиматься, разрывая встроенные ячейки. - Получайте изображения клеток внутри агарозы и подсчитывайте белые и синие клетки.
- Вычисление жизнеспособности клеток как (всего ячеек - синие ячейки) / всего ячеек.
Результаты
Вышеуказанный протокол позволяет инкапсуляцию клеток в нити гидрогеля для максимизации жизнеспособности клеток в течение длительных периодов времени, необходимых для исследования внутриклеточных процессов в режиме реального времени. В биореакторе клетки поддерживаются живыми и метаболически активными до 72 ч, что подтверждается синим тестом Трипана (рисунок 2a-c). В принципе, этот протокол может быть применен для наблюдения за внутриклеточным интересующим белком, претерпевающим какие-либо конформационные или химические изменения. В первой заявке, описанной выше, биореактор применяют для мониторинга в режиме реального времени связывания двух ингибиторов, AAZ и MZA, с CA II, сверхэкспрессированным в цитозоле клеток HEK293T. Первый зарегистрированный спектр скульптуры возбуждения 1Н (zgesgp) используется для оценки общей интенсивности сигнала (которая пропорциональна количеству клеток), наличия сигналов от сверхэкспрессированного белка и однородности поля (рисунок 2d). В случае CA II внутриклеточное связывание двух ингибиторов можно контролировать с помощью 1D 1H ЯМР-спектров WATERGATE 3-9-1935 1D 1H (p3919gp), наблюдая сигналы 1H в области между 11 и 16 ppm. Эти сигналы возникают из цинк-координационных гистидинов и других ароматических остатков CA II36 и нарушаются при связывании лигандов14,15. Концентрации лигандов могут быть выбраны на основе скорости диффузии или, при наличии, из ранее определенных значений проницаемости14. Успешное связывание подтверждается визуально появлением дополнительного набора сигналов в интересующей спектральной области, который постепенно заменяет исходные сигналы (рисунок 3). Зависящие от времени кривые связывания получены методом анализа MCR-ALS, который разделяет два набора сигналов ЯМР, возникающих из свободного и связанного СА II (рисунок 4a), и одновременно обеспечивает относительные профили концентрации двух видов (рисунок 4b). Во втором применении биореактор применяют для мониторинга образования связанной с цинком внутримолекулярной дисульфидной связи SOD1, продвигаемой эбселеном, миметиком глутатионпероксидазы, в клетках человека. Этот процесс контролируется путем наблюдения за изменениями в спектрах 1H-15N 2D SOFAST-HMQC37 (которые обеспечивают отпечаток конформации белковой основы), вызванными возмущениями структуры белка, вызванными образованием дисульфидной связи. Дополнительные сигналы, возникающие в результате дисульфид-окисленного SOD1, появляются в спектре 1H-15N и постепенно заменяют сигналы дисульфид-восстановленного SOD1. Анализ MCR-ALS на отдельных областях 2D-спектра разделяет сигналы, возникающие от двух видов (рисунок 5a), и дает их относительные профили концентрации (рисунок 5b). Полученные кривые концентрации могут быть дополнительно проанализированы методом нелинейной примерки для получения информации о кинетике исследуемых процессов25.
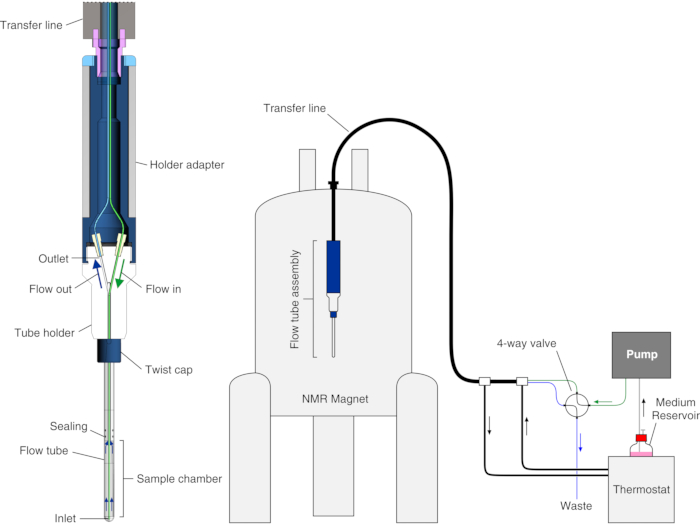
Рисунок 1: Схема биореактора. Слева: вид поперечного сечения блока пустого потока. Справа: схема установки биореактора. Впускные трубки PEEK показаны зеленым цветом; выпускная трубка из PTFE показана синим цветом. Левая панель воспроизводится с разрешения Luchinat et al.25. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
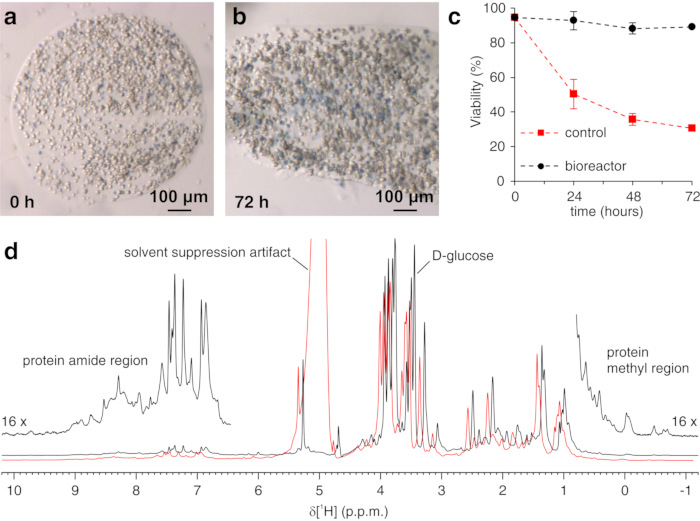
Рисунок 2: Тест Trypan Blue на инкапсулированных клетках и проверка образцов с помощью 1H ЯМР. Репрезентативные срезы агарозы, содержащие внедренные клетки и окрашенные трипановым синим цветом, (а) сразу после отливки и (б) через 72 ч в биореакторе; (c) жизнеспособность клеток в зависимости от времени в биореакторе ЯМР при активном потоке (черный) и в статических условиях (красный), измеренная с помощью теста Трипана Блю. (d) спектры ЯМР zgesgp 1H, зарегистрированные на встроенных в агарозу клетках, сверхэкспрессирующих CA II в отсутствие (черный) и в присутствии (красный) пузырьков газа в биореакторе. В последнем случае снижение однородности поля вызывает расширение линий и появление артефактов подавления растворителей. Обозначены интересные спектральные особенности. Панели (a-c) воспроизводятся с разрешения Luchinat et al.25. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
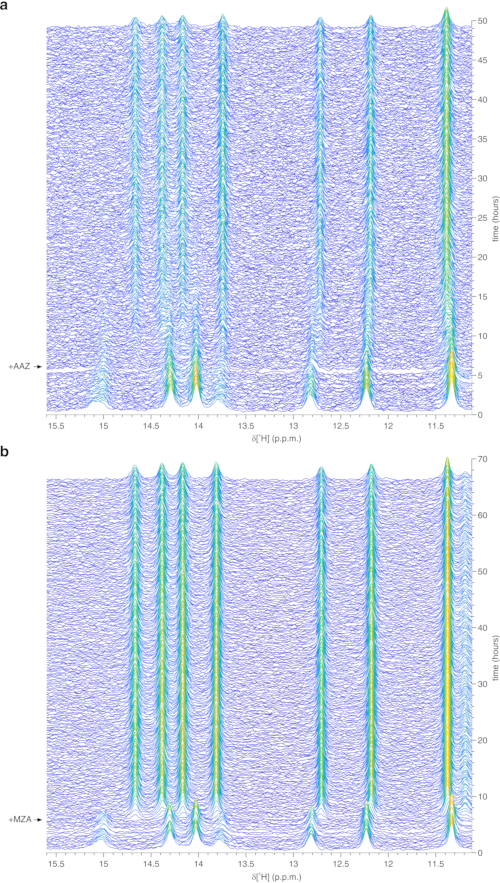
Рисунок 3: Репрезентативные внутриклеточные данные ЯМР 1H в реальном времени, полученные на инкапсулированных агарозой клетках в биореакторе. Каскадные графики 1D 1H ЯМР-спектров (область между 15,6 и 11,1 ppm) клеток HEK293T, сверхэкспрессирующих CA II и впоследствии обработанных (a) 25 мкм AAZ и (b) 10 мкМ MZA, зарегистрированных как функция времени в биореакторе ЯМР. Время обработки лигандами показано стрелкой. Спектральная интенсивность (a.u.) имеет цветовую кодировку от синего (самый низкий) до желтого (самый высокий). Эта цифра воспроизводится с разрешения Luchinat et al.25. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
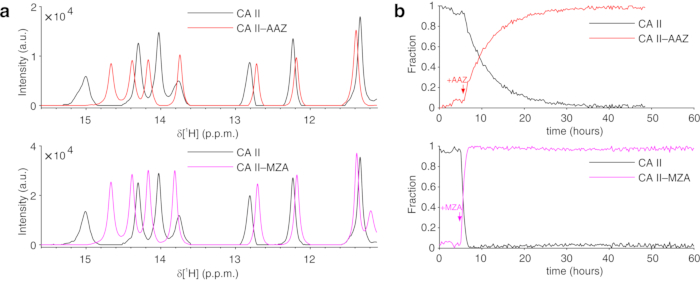
Рисунок 4: Репрезентативный выход MCR-ALS из спектров 1D ЯМР. (a) 1H ЯМР спектров чистых компонентов, реконструированных MCR-ALS: CA II в отсутствие лигандов (черный) и в комплексе с AAZ (красный) или MZA (пурпурный); (b) относительные профили концентрации свободного (черного) и связанного CA II в зависимости от времени при добавлении AAZ (красный) или MZA (пурпурный), полученные MCR-ALS. Время обработки лигандами обозначено стрелками. Эта цифра воспроизводится с разрешения Luchinat et al.25. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
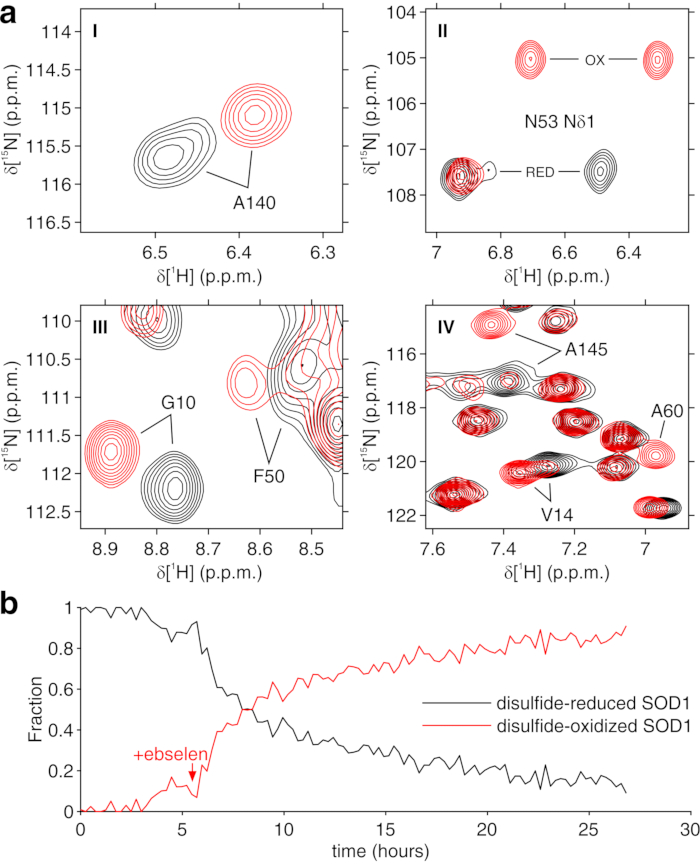
Рисунок 5: Репрезентативный выход MCR-ALS из спектров 2D ЯМР. (a) спектральные области 1H-15N (обозначенные I-IV) чистых компонентов, реконструированных MCR-ALS: дисульфид-восстановленный SOD1 (черный) и дисульфид-окисленный SOD1 (красный); b) профиль относительной концентрации чистых компонентов в зависимости от времени при добавлении эбселена (отмеченного стрелкой), полученного MCR-ALS. Эта цифра воспроизводится с разрешения Luchinat et al.25. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Обсуждение
Целью использования биореактора для эксперимента с внутриклеточным ЯМР является поддержание жизни и метаболической активности клеток в течение длительного периода времени. Для достижения этой цели необходимо учитывать ряд важнейших аспектов. Во-первых, крайне важно избегать бактериального загрязнения при подготовке образца клеток и во время сбора данных ЯМР. Если штаммы E. coli или других бактерий, обычно используемых для клонирования генов и экспрессии рекомбинантного белка, используются в лаборатории, они могут загрязнять клетки во время подготовки образца. Попав в биореактор, бактерии будут быстро расти, используя свежую питательную среду, и будут вызывать гибель клеток из-за производства эндотоксинов. Бактериальное загрязнение обнаруживается только на запущенной стадии, когда оно превращает среду роста в желтый и мутный. Кроме того, неполная очистка биореактора может привести к загрязнению насоса или трубки бактериями, дрожжами или обычными плесенями.
Обязательным условием успеха эксперимента является недопущение образования газовых пузырьков. Пузырьки газа, захваченные между нитями агарозы в активном объеме катушки ЯМР, внесут большие неоднородности магнитного поля, вызывая неполное подавление сигнала H2O и серьезную потерю спектрального качества (рисунок 2d). Пузырьки могут быть вызваны воздухом, захваченным в системе, или образованием газообразного CO2. Первого можно легко избежать, промыв систему средой перед введением образца клетки, в то время как во избежание последнего рекомендуется уменьшить концентрацию NaHCO3 в питательной среде и поддерживать все части системы при постоянной температуре, чтобы свести к минимуму различия в растворимости CO2 . Клеточный аэробный метаболизм также может вызывать образование газообразного CO2, который можно предотвратить, увеличив скорость потока.
Жизнеспособность клеток должна проверяться после каждого запуска Trypan Blue Test. Однако это не дает представления о метаболической активности. Для получения более полной картины метаболического состояния клеток во время работы биореактора можно выполнить ЯМР-спектры 31P для оценки продукции АТФ в зависимости от времени23,25. Однако для этого измерения часто необходим специальный зонд, который может позволить одновременную запись с 1H ЯМР.
В случае CA II наличие хорошо разрешенных репортерных сигналов в необычной области спектра 1H облегчает анализ из простых спектров 1D ЯМР и не требует обогащения изотопами во время экспрессии белка. В целом, другие белки могут давать сигналы 1H, полезные для мониторинга спектральных изменений в других областях, таких как типичное для гидрофобного ядра белка от 0 до -1 ppm11; однако эти области, как правило, переполнены для свернутых белков размером более ~ 10 кДа. В этом случае, как показано для SOD1, предпочтительно обогащать белок 15N, обеспечивая равномерно обогащенную 15N питательную среду во время экспрессии белка, и контролировать изменения в 2D 1H-15N ЯМР-спектрах 2D 1H-15N. 2D-спектры импортируются в виде 2D-массивов в MATLAB, перестраиваются в 1D-массивы и складываются перед анализом MCR-ALS. Последний подход в целом применим к любому внутриклеточному белку, который порождает обнаруживаемые сигналы, и предоставляет информацию о конформационных изменениях белка на уровне одного остатка. В принципе, последний подход может быть обобщен на спектры nD и на другие схемы маркировки изотопов.
Что касается применения к различным типам клеток, протокол должен быть легко адаптирован к различным клеточным линиям и не требует, чтобы интересующий белок непосредственно экспрессировался в клетках. Поэтому другие подходы к внутриклеточному ЯМР могут быть объединены с этим протоколом, в котором макромолекула, представляющая интерес, производится рекомбинантно или синтезируется, а затем вводится в ячейки электропорацией или другими способами доставки1,9,38. При работе с различными клеточными линиями или протоколами пробоподготовки такие параметры, как концентрация агарозы, толщина резьбы и конечная плотность ячеек в нитях агарозы, возможно, потребуется оптимизировать эмпирически. Кроме того, применимость протокола, описанного здесь, ограничена клетками, которые переносят инкапсуляцию агарозы. Другие типы клеток могут требовать различных составов гидрогелей, тогда как другая установка рекомендуется при анализе клеток, которые изначально растут в суспензии, например, с использованием коаксиальной микродиализной мембраны для обеспечения диффузии питательных веществ при сохранении взвешенных клеток, ограниченных в трубке ЯМР23.
По сравнению с другими конструкциями биореакторов ЯМР19,20,21,22, устройство, описанное здесь, опирается на коммерчески доступный блок потока, адаптированный с незначительными изменениями. Поэтому устройство можно легко тиражировать в разных лабораториях с высокой воспроизводимостью. Кроме того, он обеспечивает стандартизированную работу и полное соблюдение строгих лабораторных правил безопасности, если это необходимо. В целом, гибкость и простота работы биореактора должны позволить использовать многие другие применения раствора ЯМР, как в клетках, так и in vitro, в дополнение к тем, о которых уже сообщалось23,25. В конце концов, та же конструкция биореактора может быть применена к образцам, которые больше напоминают физиологическую среду ткани, такие как сфероиды или органоиды, при условии, что будут найдены соответствующие каркасы для поддержания таких образцов живыми или даже поддержания их роста в ЯМР-спектрометре.
Раскрытие информации
Авторы заявляют, что конфликта интересов нет.
Благодарности
Эта работа была поддержана iNEXT-Discovery, номером гранта 871037, финансируемым программой Horizon 2020 Европейской комиссии, Instruct-ULTRA, номером гранта 731005, проектом ЕС H2020 для дальнейшего развития услуг Instruct-ERIC, и грантом Ministero dell'Istruzione, dell'Università e della Ricerca PRIN 20177XJCHX. Авторы признают поддержку Instruct-ERIC, знакового проекта ESFRI, посредством присуждения премии JRA No 815 и использования ресурсов Итальянского центра CERM/CIRMMP. Мы благодарим Маттео Пеннестри (Bruker, Великобритания) за поддержку работы блоки потока InsightMR.
Материалы
| Name | Company | Catalog Number | Comments |
| Materials | |||
| Citric acid | Sigma-Aldrich | 251275 | |
| D2O | Sigma-Aldrich | 453366 | |
| DMEM, high glucose | Life Technologies | 10313-021 | |
| DMEM, high glucose, powder | Sigma-Aldrich | D5648 | |
| FBS | Life Technologies | 10270 | |
| HCl | Sigma-Aldrich | 30721 | |
| L-glutamine (200 mM) | Life Technologies | 25030 | |
| Low-gelling agarose, powder | Sigma-Aldrich | A4018 | |
| NaHCO3, powder | Carlo Erba | 478537 | |
| PBS | Life Technologies | 10010 | |
| Penicillin–streptomycin (10,000 U/ml) | Life Technologies | 15140-122 | |
| NaOH, pellets | Sigma-Aldrich | 30620 | |
| Trypan Blue solution (0.4% (wt/vol) | Sigma-Aldrich | T8154 | Hazard statement(s): H350 may cause cancer. |
| Trypsin–EDTA (0.05% (wt/vol)) | Life Technologies | 25300-054 | |
| Equipment | |||
| Avance III Spectrometer equipped with a 5 mm CryoProbe | Bruker | n/a | All modern spectrometers and narrow-bore magnets equipped with 5 mm probes are compatible. |
| InsightMR flow unit | Bruker | n/a | |
| P-920 pump module from ÄKTA FPLC | GE Healthcare | n/a | Any FPLC, HPLC peristaltic or syringe pump should be compatible with the flow unit. |
Ссылки
- Inomata, K., et al. High-resolution multi-dimensional NMR spectroscopy of proteins in human cells. Nature. 458 (7234), 106-109 (2009).
- Luchinat, E., Banci, L. In-cell NMR: a topical review. IUCrJ. 4, 108-118 (2017).
- Dzatko, S., et al. Evaluation of the stability of DNA i-motifs in the nuclei of living mammalian cells. Angewandte Chemie (International Ed. in English). 57 (8), 2165-2169 (2018).
- Luchinat, E., Banci, L. In-cell NMR in human cells: direct protein expression allows structural studies of protein folding and maturation. Accounts of Chemical Research. 51 (6), 1550-1557 (2018).
- Tanaka, T., et al. High-resolution protein 3D structure determination in living eukaryotic cells. Angewandte Chemie (International Ed. in English). 58 (22), 7284-7288 (2019).
- Siegal, G., Selenko, P. Cells, drugs and NMR. Journal of Magnetic Resonance. 306, 202-212 (1997).
- Banci, L., et al. Atomic-resolution monitoring of protein maturation in live human cells by NMR. Nature Chemical Biology. 9 (5), 297-299 (2013).
- Luchinat, E., et al. In-cell NMR reveals potential precursor of toxic species from SOD1 fALS mutants. Nature Communications. 5, 5502 (2014).
- Theillet, F. -. X., et al. Structural disorder of monomeric α-synuclein persists in mammalian cells. Nature. 530 (7588), 45-50 (2016).
- Barbieri, L., Luchinat, E., Banci, L. Intracellular metal binding and redox behavior of human DJ-1. Journal of biological inorganic chemistry: JBIC: A Publication of the Society of Biological Inorganic Chemistry. 23 (1), 61-69 (2018).
- Banci, L., Barbieri, L., Luchinat, E., Secci, E. Visualization of redox-controlled protein fold in living cells. Chemistry & Biology. 20 (6), 747-752 (2013).
- Mercatelli, E., Barbieri, L., Luchinat, E., Banci, L. Direct structural evidence of protein redox regulation obtained by in-cell NMR. Biochimica Et Biophysica Acta. 1863 (2), 198-204 (2016).
- Barbieri, L., Luchinat, E., Banci, L. Protein interaction patterns in different cellular environments are revealed by in-cell NMR. Scientific Reports. 5, 14456 (2015).
- Luchinat, E., et al. Drug screening in human cells by NMR spectroscopy allows the early assessment of drug potency. Angewandte Chemie (International Ed. in English). 59 (16), 6535-6539 (2020).
- Luchinat, E., et al. Intracellular binding/unbinding kinetics of approved drugs to carbonic anhydrase II observed by in-cell NMR. ACS Chemical Biology. 15 (10), 2792-2800 (2020).
- DeMott, C. M., et al. Potent inhibitors of mycobacterium tuberculosis growth identified by using in-cell NMR-based screening. ACS Chemical Biology. 13 (3), 733-741 (2018).
- Krafcikova, M., et al. Monitoring DNA-ligand interactions in living human cells using NMR spectroscopy. Journal of the American Chemical Society. 141 (34), 13281-13285 (2019).
- Broft, P., et al. In-cell NMR of functional riboswitch aptamers in eukaryotic cells. Angewandte Chemie (International Ed. in English). , (2020).
- Sharaf, N. G., Barnes, C. O., Charlton, L. M., Young, G. B., Pielak, G. J. A bioreactor for in-cell protein NMR. Journal of magnetic resonance. 202 (2), 140-146 (2010).
- Kubo, S., et al. A gel-encapsulated bioreactor system for NMR studies of protein-protein interactions in living mammalian cells. Angewandte Chemie (International Ed. in English). 52 (4), 1208-1211 (2013).
- Inomata, K., Kamoshida, H., Ikari, M., Ito, Y., Kigawa, T. Impact of cellular health conditions on the protein folding state in mammalian cells. Chemical Communications. 53 (81), 11245-11248 (2017).
- Breindel, L., DeMott, C., Burz, D. S., Shekhtman, A. Real-time in-cell nuclear magnetic resonance: ribosome-targeted antibiotics modulate quinary protein interactions. Biochemistry. 57 (5), 540-546 (2018).
- Cerofolini, L., et al. Real-time insights into biological events: in-cell processes and protein-ligand interactions. Biophysical Journal. 116 (2), 239-247 (2019).
- Breindel, L., Burz, D. S., Shekhtman, A. Active metabolism unmasks functional protein-protein interactions in real time in-cell NMR. Communications Biology. 3, (2020).
- Luchinat, E., Barbieri, L., Campbell, T. F., Banci, L. Real-time quantitative in-cell NMR: ligand binding and protein oxidation monitored in human cells using multivariate curve resolution. Analytical Chemistry. 92 (14), 9997-10006 (2020).
- Koczula, K. M., et al. Metabolic plasticity in CLL: adaptation to the hypoxic niche. Leukemia. 30 (1), 65-73 (2016).
- Alshamleh, I., et al. Real-time NMR spectroscopy for studying metabolism. Angewandte Chemie (International Ed. in English). 59 (6), 2304-2308 (2020).
- Supuran, C. T. Carbonic anhydrases: novel therapeutic applications for inhibitors and activators. Nature Reviews. Drug Discovery. 7 (2), 168-181 (2008).
- Neri, D., Supuran, C. T. Interfering with pH regulation in tumours as a therapeutic strategy. Nature Reviews. Drug Discovery. 10 (10), 767-777 (2011).
- Alterio, V., Di Fiore, A., D'Ambrosio, K., Supuran, C. T., De Simone, G. Multiple binding modes of inhibitors to carbonic anhydrases: how to design specific drugs targeting 15 different isoforms. Chemical Reviews. 112 (8), 4421-4468 (2012).
- Capper, M. J., et al. The cysteine-reactive small molecule ebselen facilitates effective SOD1 maturation. Nature Communications. 9 (1), 1693 (2018).
- Trist, B., Hilton, J. B., Crouch, P. J., Hare, D. J., Double, K. L. Superoxide dismutase 1 in health and disease: How a front-line antioxidant becomes neurotoxic. Angewandte Chemie (International Ed. in English). , (2020).
- Tauler, R. Multivariate curve resolution applied to second order data. Chemometrics and Intelligent Laboratory Systems. 30 (1), 133-146 (1995).
- Barbieri, L., Luchinat, E., Banci, L. Characterization of proteins by in-cell NMR spectroscopy in cultured mammalian cells. Nature Protocols. 11 (6), 1101-1111 (2016).
- Piotto, M., Saudek, V., Sklenár, V. Gradient-tailored excitation for single-quantum NMR spectroscopy of aqueous solutions. Journal of biomolecular NMR. 2 (6), 661-665 (1992).
- Vasa, S. K., Singh, H., Grohe, K., Linser, R. Assessment of a large enzyme-drug complex by proton-detected solid-state NMR spectroscopy without deuteration. Angewandte Chemie (International Ed. in English). 58 (17), 5758-5762 (2019).
- Schanda, P., Brutscher, B. Very fast two-dimensional NMR spectroscopy for real-time investigation of dynamic events in proteins on the time scale of seconds. Journal of the American Chemical Society. 127 (22), 8014-8015 (2005).
- Ogino, S., et al. Observation of NMR signals from proteins introduced into living mammalian cells by reversible membrane permeabilization using a pore-forming toxin, streptolysin O. Journal of the American Chemical Society. 131 (31), 10834-10835 (2009).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены