Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Улучшение оценки расположения электродов при кохлеарной имплантации с помощью слияния изображений компьютерной томографии
В этой статье
Резюме
Этот протокол демонстрирует метод совмещения изображений предоперационной и послеоперационной компьютерной томографии для пользователей кохлеарных имплантатов. Такой подход может повысить точность измерения глубины вставки и центральной частоты контактов электродной матрицы. Кроме того, этот метод имеет потенциальное применение в подгонке на основе анатомии, новой области в области кохлеарных имплантатов.
Аннотация
Это исследование было направлено на то, чтобы определить, может ли совмещение изображений до и после операции компьютерной томографии (КТ) помочь в оценке размещения электродов и центральной частоты (ЦВ) у пользователей кохлеарного имплантата (КИ). Вторичной целью было сравнение автоматического слияния с ручными методами измерения параметров улитки. В исследование были включены двадцать ушей с КИ, которым была проведена компьютерная томография как до, так и после операции. Ручные измерения параметров улитки первоначально проводились по послеоперационным КТ-изображениям, за которыми последовало автоматическое обнаружение с помощью объединенных пред- и послеоперационных КТ-изображений с отологическим программным обеспечением (OTOPLAN). С помощью обоих методов рассчитывали глубину углового введения (AID) и CF каждого контакта электрода, а также оценивали разницу в ошибках. Анализ показал значительные различия между двумя методами по ширине улитки (B-значению) и длине кохлеарного протока (CDL); Однако эти различия не были клинически значимыми. Кроме того, не было статистически значимой разницы в диаметре улитки (A-значение). Средние различия составили 0,04 мм для значения А, 0,21 мм для значения В и 0,73 мм для CDL. Сравнение AID и CF выявило несущественные различия между ручным и автоматическим методами сварки по всем контактам электродов, за исключением электрода No пять. Согласно этому исследованию, пред- и послеоперационные КТ-изображения с фьюзингом могут быть использованы для определения положения электродов у реципиентов КИ. Автоматическое совмещение изображений потенциально может измерять параметры улитки, AID и CF с меньшим вмешательством человека. Таким образом, этот метод может послужить еще одной основой для создания аппроксимации на основе анатомии.
Введение
Операция с кохлеарным имплантатом (КИ) — это преобразующий метод лечения людей с тяжелой и глубокой сенсоневральной тугоухостью, обеспечивающий существенное улучшение слуховой функции и качества жизни1. Решающим фактором для успеха хирургии КИ является точное размещение электродной решетки в правильном кохлеарном компартменте, в частности, в барабанной мышце, поскольку оптимальное расположение электродов неизменно связано с превосходными результатами слуха2. Таким образом, тщательное предоперационное планирование и оценка анатомии улитки имеют важное значение для обеспечения правильного расположения электродной решетки. Обеспечение того, чтобы электродная решетка была полностью вставлена в барабанную перепонку, имеет решающее значение для максимизации пользы для пациента и достижения оптимальных клинических результатов3.
Предоперационная оценка угла глубины введения матриц электродов CI считается важной для эффективного хирургического планирования. Эта оценка в значительной степени зависит от получения точных измерений ключевых параметров улитки, таких как длина кохлеарного протока (CDL), с помощью предоперационной компьютерной томографии (КТ)4. Эти измерения позволяют сделать важные прогнозы относительно покрытия улитки и глубины углового введения во время операции КИ, когда длина электрода известна. Основным предиктором CDL является A-значение, определяемое как расстояние между круглым окном и самой дальней точкой на базальном повороте. Предыдущие исследования подчеркнули решающую роль предоперационной визуализации и планирования в принятии хирургических решений и оптимизации результатов для пациентов с КИ5.
Предоперационная компьютерная томография является стандартной практикой во многих клиниках КИ для оценки анатомии внутреннего уха и параметров улитки перед операцией. Предоперационная компьютерная томография обеспечивает четкие изображения без артефактов, что способствует эффективному планированию и оптимизации хирургических процедур6. Тем не менее, предоперационный анализ КТ сам по себе имеет ограничения в точном прогнозировании фактической угловой глубины введения (AID) и центральной частоты (CF) электродных контактов вдоль электродной матрицы CI. Следовательно, послеоперационная визуализация остается необходимой для подтверждения положения электродной решетки, оценки любого смещения или транслокации, а также определения истинной AIDкаждого контакта.
Послеоперационная визуализация подтверждает точность установки электродов и помогает создавать индивидуальные карты подгонки, адаптированные к уникальной анатомии улитки каждого пациента. Эти карты подгонки необходимы для оптимизации слуховой производительности, обеспечивая точную стимуляцию волокон слухового нерва. Недавние исследования показали, что индивидуализированные карты подгонки, или анатомические карты (ABF), улучшают понимание речи как в тихой, так и в шумной обстановке по сравнению со стандартными или клиническими картамиподгонки 8,9,10,11,12,13. Кроме того, реципиенты, как правило, отдают предпочтение картам ABF, когда их электродная решетка достигает адекватной стимуляции апикальной области улитки8. Несоответствие частоты и места — это расхождение между CF электродных контактов, основанным на их физическом расположении в улитке, и настройками по умолчанию4. Mertens et al. сообщили, что влияние рассогласования частоты и местоположения уменьшается при длительном использовании устройства14. Другие исследования показали, что уменьшение несоответствия частоты и места с ABF у пациентов с КИ улучшает восприятие речи в шумной обстановке, не влияя на понимание в тихой обстановке11,13.
Для оценки реципиентов КИ использовались различные методы визуализации, в том числе рентген15,16, конусно-лучевая КТ17 и магнитно-резонансная томография (МРТ)18,19. Тем не менее, компьютерная томография остается предпочтительным методом из-за ее высокого пространственного разрешения и способности захватывать подробную анатомию улитки. Компьютерная томография позволяет точно оценить структуры внутреннего уха, такие как барабанная кость и вестибули скала, что способствует точной установке электродов.
Несмотря на множество преимуществ компьютерной томографии, определенные проблемы сохраняются, особенно при послеоперационном сканировании с низким разрешением. Контакты с металлическими электродами могут образовывать артефакты изображения, которые скрывают соседние структуры, что затрудняет точное измерение критических параметров, таких как AID и CF. Недавние исследования показали, что совмещение до- и послеоперационной компьютерной томографии повышает четкость изображения по сравнению со стандартными сканированиями, обеспечивая более точную оценку и улучшая расположение электродов за счет предоставления дополнительной информации как до, так и после операционногоизображения.
В настоящее время послеоперационный анализ изображений КТ часто включает в себя ручные измерения с использованием программных инструментов, которые требуют существенного обучения, требуют много времени и могут быть подвержены вариабельности и ошибкам, что ограничивает их эффективность и более широкое применение. Существует ограниченное количество литературы о возможностях автоматических измерений по совлещенным изображениям для устранения этих ограничений и обеспечения надежных измерений AID для электродных контактов. Это исследование направлено на то, чтобы оценить, может ли слияние до- и послеоперационных изображений КТ эффективно оценить характеристики улитки и размещение электродов у реципиентов КИ. Кроме того, в исследовании исследуется, как объединение изображений может улучшить подгонку на основе анатомии (ABF) и повысить точность измерений как для угловой глубины введения (AID), так и для центральной частоты (CF).
протокол
Это исследование получило одобрение главного институционального наблюдательного совета (E-21-5737) и проводилось в соответствии с этическими принципами, изложенными в Хельсинкской декларации. Данные были ретроспективно собраны из медицинских карт в нашем третичном центре КИ. Из-за анонимного характера анализа данных информированное согласие не требовалось. В исследование было включено 20 ушных раковин от пациентов разных возрастных групп.
Критерии включения были следующими: пациенты с нормальной анатомией внутреннего уха, получавшие КИ в период с 2020 по 2023 год, перенесшие как до, так и послеоперационное компьютерное сканирование, и им были имплантированы устройства КИ того же производителя, совместимые с используемым программным обеспечением для планирования хирургических операций. Компьютерная томография височной кости обычно проводится в рамках предоперационной оценки пациентов с кохлеарными имплантатами в нашем центре, в то время как послеоперационная компьютерная томография проводится только в случае медицинской необходимости для минимизации лучевой нагрузки. Критерии исключения включали пациентов с КИ, перенесших ревизионные операции или имевших кохлеарное окостенение, кохлеарный отосклероз или переломы височной кости с вовлечением глазной капсулы. Подробная информация об оборудовании и программном обеспечении представлена в Таблице материалов.
1. Загрузка и измерение параметров улитки
ПРИМЕЧАНИЕ: Протокол измерения, использованный в этом исследовании, включал в себя ряд последовательных шагов, разработанных для оценки эффективности метода слияния изображений КТ до и после операции при оценке расположения электродов у реципиентов КИ (Рисунок 1).
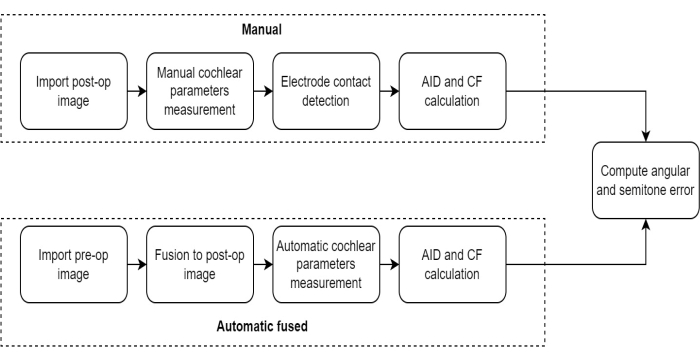
Рисунок 1: Сравнение протоколов измерений. На этом рисунке показан протокол измерения параметров улитки методом автоматического слияния по сравнению с ручным методом. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
- Нажмите кнопку «Импорт » в программном модуле «Управление данными », чтобы загрузить послеоперационные и предоперационные снимки компьютерной томографии, и выберите файлы DICOM .
- Вручную определите центр модиолуса, круглого окна и метрики улитки, включая A-значение (диаметр улитки), B-значение (ширина улитки) и H-значение (высота улитки)в модуле 4 3D Ear-Cochlea (рис. 2).
- Рассчитайте длину кохлеарного канала (CDL) с использованием значений A и B, применяя метод Алексиадеса к эллиптически круговой аппроксимации (ECA)2,4.
ПРИМЕЧАНИЕ: Подробные этапы послеоперационного анализа описаны в работе Canfarotta et al.21. Эти измерения обеспечивают анатомические ориентиры для оценки CDL.
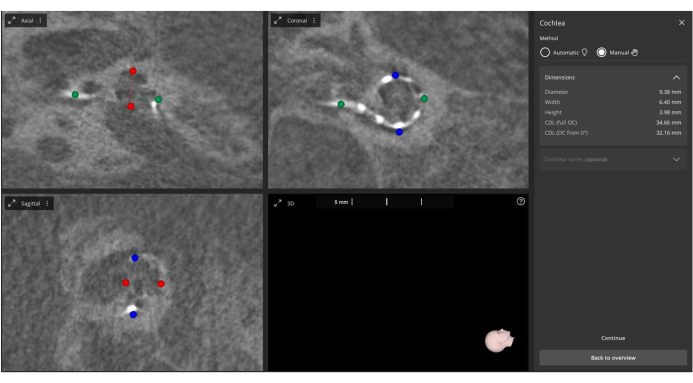
Рисунок 2: Ручное измерение послеоперационных значений A, B и H. Послеоперационные изображения импортируются в программное обеспечение, а значение A (отмечено зеленым цветом), значение B (отмечено синим) и значение H (отмечено красным) измеряется вручную. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
2. Идентификация контактов электродов и расчет AID/CF
- Откройте модуль «Оценка имплантатов ». Программное обеспечение автоматически определит двенадцать точек контакта электродов на послеоперационных КТ-изображениях.
- При необходимости вручную отрегулируйте обнаруженные точки контакта перед подтверждением их положения.
- Позвольте программному обеспечению использовать эти точки, наряду с предварительно определенными кохлеарными метриками, для автоматического расчета глубины углового ввода (на основе Escude et al.22) и характеристической частоты (на основе Greenwood et al.23) для каждого контакта (см. рисунок 3).
ПРИМЕЧАНИЕ: Этот ручной подход считается стандартным методом измерения AID и CF и в данном исследовании называется «ручным».
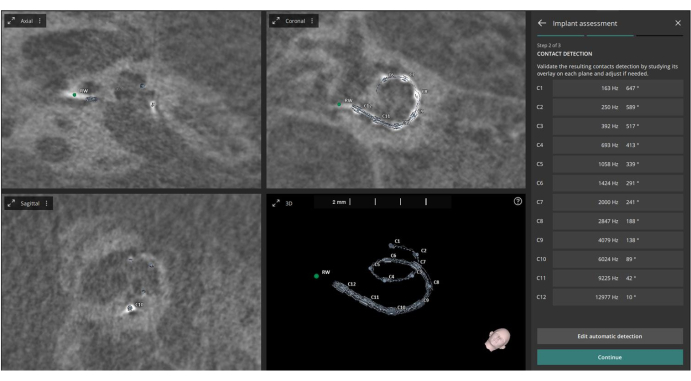
Рисунок 3: Идентификация контактов электродов. На этом рисунке показана идентификация двенадцати электродных контактов по послеоперационным изображениям КТ. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
3. Слияние изображений
- Нажмите значок «Добавить » в пользовательском интерфейсе, чтобы импортировать предоперационные изображения компьютерной томографии на панель «Слияние изображений».
- Позвольте программному обеспечению автоматически начать регистрацию предоперационных КТ-изображений с предварительно загруженными послеоперационными КТ-изображениями с помощью функции автоматического объединения, которая применяет алгоритм взаимной информации.
- Воспользуйтесь функцией «Ручное выравнивание » в меню предоперационного изображения, если требуется ручная настройка склейки. Этот процесс слияния улучшает визуализацию и позволяет более полно оценить анатомию улитки и размещение электродов с меньшим количеством артефактов. Слияние направлено на улучшение визуализации для лучшей оценки (см. рис. 4).
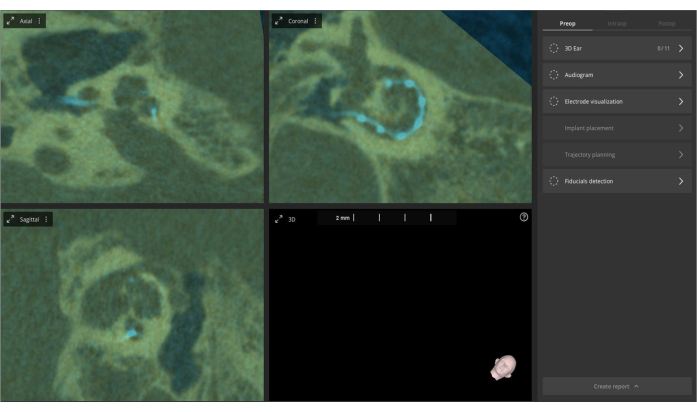
Рисунок 4: Слияние до- и послеоперационных изображений компьютерной томографии. Предоперационные КТ-изображения импортируются в программное обеспечение и объединяются с послеоперационными КТ-изображениями. Накладка отображается в оливковом цвете, а электроды выделены ярко-синим цветом. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
4. Автоматическое измерение параметров улитки на предоперационном изображении
- Повторное измерение параметров улитки на только что импортированном предоперационном изображении в модуле 3D - Cochlia.
- Выберите опцию «Автоматически» в меню модуля для выполнения автоматических измерений параметров улитки. Эта функция доступна только для предоперационных изображений без электродов имплантата, так как металлические артефакты отсутствуют.
- Используйте автоматический алгоритм для реконструкции анатомии внутреннего уха в 3D. 3D-модель будет служить основой для автоматических измерений параметров улитки, как описано в Abari et al.24.
ПРИМЕЧАНИЕ: 3D-реконструкция помогает точно измерить параметры улитки (см. Рисунок 5).
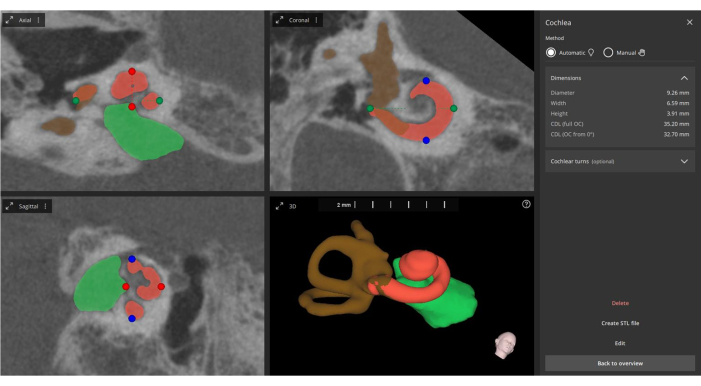
Рисунок 5: Автоматизированное измерение параметров улитки. По совпадающим изображениям программа автоматически измеряет основные параметры улитки (обозначены зелеными, синими и красными точками), выполняет 3D-реконструкцию (улитка — оранжевым, внутренний слуховой проход — зеленым, полукружные каналы — коричневым) и обновляет информацию о контактах электродов. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
5. Обновление точек контакта электродов с новыми параметрами улитки
- Подтвердите новые измерения длины кохлеарного протока (CDL), полученные на основе предоперационных изображений.
- Позвольте ранее идентифицированным точкам контакта электродов на послеоперационных изображениях автоматически обновляться с учетом новой информации о параметрах улитки, определяя подход «Автоматическое слияние».
- Выполните расчеты на основе слитых изображений (до и после операции) для глубины углового введения (AID) и характеристической частоты (CF), которые важны для подтверждения размещения электродной матрицы, покрытия улитки и построения карты подгонки на основе анатомии (ABF) (см. рисунок 5).
ПРИМЕЧАНИЕ: AID и CF имеют решающее значение для подтверждения положения электродов и покрытия улитки в практике кохлеарного импланта (КИ) (см. Рисунок 6).
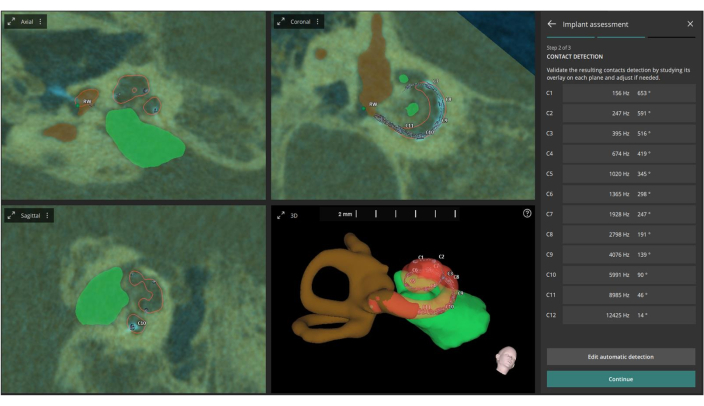
Рисунок 6: Автоматическое определение AID и CF. На этом рисунке показано автоматическое определение AID (распределение акустического импеданса) и CF (центральная частота) для каждого отдельного контакта электрода на основе расплавленных изображений. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
6. Расчет средней угловой ошибки и частотной ошибки
- Рассчитайте среднюю угловую ошибку между ручным и автоматическим методами сварки для каждого электродного контакта.
- Рассчитайте частотную погрешность в полутонах между обоими методами (ручным и автоматическим сплавлением) для каждого контакта электрода.
- Используйте эти расчеты для получения количественных показателей разницы и точности между двумя методами. Обратите внимание, что полутона — это наименьшие музыкальные интервалы, обычно используемые в западной музыке25.
7. Статистический анализ
- Подавайте рассчитанные вручную параметры улитки, глубину углового введения (AID) и характеристическую частоту (CF) из послеоперационной компьютерной томографии, а также автоматически объединенные расчетные данные, полученные в технике объединения изображений КТ до и после операции для каждого контакта электрода, в программное обеспечение для статистического анализа (программное обеспечение R).
- Используйте средние значения и стандартные отклонения для описательной статистики количественных переменных, в то время как для категориальных переменных применяйте подсчеты и проценты.
- Проведите сравнительный анализ между измеренным вручную AID и частотами и автоматически объединенными измерениями с использованием парного t-критерия с поправкой на Бонферрони или рангового теста со знаком Вилкоксона, в зависимости от предположения о нормальности, проверенного с помощью теста Шапиро-Уилка.
Примечание: Предположим, что все сравнения имеют клинически значимые стандартизированные величины эффектов (d) Коэна). Предположим, что статистически значимое значение P меньше 0,05.
Результаты
В это исследование было включено 20 ушей от пользователей КИ, с 11 имплантатами с левой стороны и девятью с правой. Средний возраст участников составил 13,3 года, из них 55% женщин и 45% мужчин. В таблице 1 представлен сравнительный анализ ручных и автоматических мето...
Обсуждение
Результаты настоящего исследования показали сопоставимые измерения между ручным и автоматическим методами слияния для большинства параметров и частот улитки. В то время как ручные измерения показали незначительно более высокие значения для определенных параметро...
Раскрытие информации
Ясин Абдельсамад и Тахир Шариф работают в MED-EL только на научных должностях. Авторы не имеют финансовых интересов в продуктах, описанных в данной рукописи, и им больше нечего раскрывать.
Благодарности
Авторы хотели бы поблагодарить доктора Николу Ивановича за ознакомление с протоколом и Рахму Свиди за проведение статистического анализа.
Материалы
| Name | Company | Catalog Number | Comments |
| CI devices | MED-EL, Innsbruck, Austria | ||
| OTOPLAN software | CASCINATION, MED-EL, Innsbruck, Austria | version 4 (3.0.0) | Otology Planning Software |
| R software | R Foundation for Statistical Computing, Vienna, Austria | version 4.2.2 | Language and Environment for Statistical Computing |
Ссылки
- Dazert, S., Thomas, J. P., Loth, A., Zahnert, T., Stover, T. Cochlear Implantation. Dtsch Arztebl Int. 117 (41), 690-700 (2020).
- Jwair, S., Versnel, H., Stokroos, R. J., Thomeer, H. The effect of the surgical approach and cochlear implant electrode on the structural integrity of the cochlea in human temporal bones. Sci Rep. 12 (1), 17068 (2022).
- O'Connell, B. P., Hunter, J. B., Wanna, G. B. The importance of electrode location in cochlear implantation. Laryngoscope Investig Otolaryngol. 1 (6), 169-174 (2016).
- Aljazeeri, I., et al. Anatomy-based frequency allocation in cochlear implantation: The importance of cochlear coverage. Laryngoscope. 132 (11), 2224-2231 (2021).
- Oh, J., et al. Cochlear duct length and cochlear distance on pre-operative CT: imaging markers for estimating insertion depth angle of cochlear implant electrode. Eur Radiol. 31 (3), 1260-1267 (2021).
- Yoshimura, H., Watanabe, K., Nishio, S. Y., Takumi, Y., Usami, S. I. Determining optimal cochlear implant electrode array with OTOPLAN. Acta Otolaryngol. 143 (9), 748-752 (2023).
- Farnsworth, P. J., et al. Improved cochlear implant electrode localization using coregistration of pre-and post-operative CT. J Neuroimaging. 33 (3), 387-392 (2023).
- Kurz, A., Herrmann, D., Hagen, R., Rak, K. Using anatomy-based fitting to reduce frequency-to-place mismatch in experienced bilateral cochlear implant users: A promising concept. J Pers Med. 13 (7), 1109 (2023).
- Dillon, M. T., et al. Influence of the frequency-to-place function on recognition with place-based cochlear implant maps. The Laryngoscope. 133 (12), 3540-3547 (2023).
- Dillon, M. T., O'Connell, B. P., Canfarotta, M. W., Buss, E., Hopfinger, J. Effect of place-based versus default mapping procedures on masked speech recognition: Simulations of cochlear implant alone and electric-acoustic stimulation. Am J Audiology. 31 (2), 322-337 (2022).
- Creff, G., et al. Comparison of tonotopic and default frequency fitting for speech understanding in noise in new cochlear implantees: A prospective, randomized, double-blind, cross-over study. Ear Hearing. 45 (1), 35-52 (2024).
- Lassaletta, L., Calvino, M., Sanchez-Cuadrado, I., Gavilán, J. Does it make any sense to fit cochlear implants according to the anatomy-based fitting? Our experience with the first series of patients. Front Audiol Otol. 1, (2023).
- Kurz, A., Müller-Graff, F. -. T., Hagen, R., Rak, K. One click is not enough: Anatomy-based fitting in experienced cochlear implant users. Otol Neurotol. 43 (10), 1176-1180 (2022).
- Mertens, G., Van de Heyning, P., Vanderveken, O., Topsakal, V., Van Rompaey, V. The smaller the frequency-to-place mismatch the better the hearing outcomes in cochlear implant recipients. Eur Arch Otorhinolaryngol. 279 (4), 1875-1883 (2022).
- Liu, G. S., Cooperman, S. P., Neves, C. A., Blevins, N. H. Estimation of cochlear implant insertion depth using 2D-3D registration of post-operative X-ray and pre-operative CT images. Otol Neurotol. 45 (3), e156-e161 (2024).
- Alahmadi, A., et al. Advancing cochlear implant programming: X-ray guided anatomy-based fitting. Otol Neurotol. 45 (2), 107-113 (2024).
- Helal, R. A., et al. Cone-beam CT versus Multidetector CT in post-operative cochlear implant imaging: Evaluation of image quality and radiation dose. AJNR Am J Neuroradiol. 42 (2), 362-367 (2021).
- George-Jones, N. A., Tolisano, A. M., Kutz, J. W., Isaacson, B., Hunter, J. B. Comparing cochlear duct lengths between CT and MR images using an otological surgical planning software. Otol Neurotol. 41 (9), e1118-e1121 (2020).
- Swarup, A., et al. Comparing accuracy of cochlear measurements on magnetic resonance imaging and computed tomography: A step towards radiation-free cochlear implantation. J Otol. 18 (4), 208-213 (2023).
- Benson, J. C., Nassiri, A. M., Saoji, A. A., Carlson, M. L., Lane, J. I. Co-registration of pre- and post-operative images after cochlear implantation: A proposed technique to improve cochlear visualization and localization of cochlear electrodes. Neuroradiol J. 36 (2), 194-197 (2023).
- Canfarotta, M. W., Dillon, M. T., Buss, E., Pillsbury, H. C., Brown, K. D., O'Connell, B. P. Validating a new tablet-based tool in the determination of cochlear implant angular insertion depth. Otol Neurotol. 40 (8), 1006-1010 (2019).
- Escudé, B., et al. The size of the cochlea and predictions of insertion depth angles for cochlear implant electrodes. Audiol Neurotol. 11 (SUPPL. 1), 27-33 (2006).
- Greenwood, D. D. A cochlear frequency-position function for several species-29 years later. J Acoust Soc Am. 87 (6), 2592-2605 (1990).
- Abari, J., Heuninck, E., Topsakal, V. Entirely robotic cochlear implant surgery. Am J Otolaryngol. 45 (5), 104360 (2024).
- Bell, A., Jedrzejczak, W. W. The 1.06 frequency ratio in the cochlea: Evidence and outlook for a natural musical semitone. Peer J. 5, e4192 (2017).
- Cohen, J. . Statistical Power Analysis for the Behavioral Sciences. , (2013).
- Mertens, G., Van Rompaey, V., Van de Heyning, P., Gorris, E., Topsakal, V. Prediction of the cochlear implant electrode insertion depth: Clinical applicability of two analytical cochlear models. Sci Rep. 10 (1), 3340 (2020).
- Paouris, D., Kunzo, S., Goljerova, I. Validation of automatic cochlear measurements using OTOPLAN(R) software. J Pers Med. 13 (5), 805 (2023).
- IbraheemAl-Dhamari Rania Helal, T. A. S. W., Paulus, D. Automatic cochlear multimodal 3D image segmentation and analysis using atlas-model-based method. Cochlear Implants Int. 25 (1), 46-58 (2024).
- Rivas, A., et al. Automatic cochlear duct length estimation for selection of cochlear implant electrode arrays. Otol Neurotol. 38 (3), 339-346 (2017).
- Breitsprecher, T., et al. CT imaging-based approaches to cochlear duct length estimation human temporal bone study. Eur Radiol. 32 (2), 1014-1023 (2022).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены