Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Un análisis de espectroscopia de fluorescencia fluctuación de interacciones de proteínas en los contactos célula-célula
En este artículo
Resumen
Este protocolo describe un enfoque basado en la espectroscopia de la fluorescencia fluctuación para investigar las interacciones entre las proteínas median las interacciones célula-célula, es decir, proteínas localizadas en las ensambladuras de la célula, directamente en las células vivas. Ofrecemos directrices detalladas sobre la calibración del instrumento, adquisición de datos y análisis, incluyendo las correcciones a las fuentes de posible artefacto.
Resumen
Una variedad de procesos biológicos implica las interacciones célula-célula, generalmente mediadas por las proteínas que interactúan en la interfaz entre células vecinas. De interés, sólo algunos ensayos son capaces de sondear específicamente tales interacciones directamente en las células vivas. Aquí, presentamos un ensayo para medir la Unión de las proteínas expresadas en las superficies de las células vecinas, en los contactos célula-célula. Este análisis consisten de dos pasos: mezcla de células que expresan las proteínas de interés unida a diversas proteínas fluorescentes, seguido por las medidas de espectroscopia de fluorescencia fluctuación en los contactos de la célula usando un láser confocal de barrido microscopio. Demostramos la factibilidad de este ensayo en un contexto biológico pertinente mediante la medición de las interacciones de la proteína amiloidea del precursor-como 1 (APLP1) a través de las ensambladuras de la célula. Ofrecemos protocolos detallados en la adquisición de datos usando técnicas basadas en fluorescencia (análisis de espectroscopia de correlación cruzada de fluorescencia, número de la correlación cruzada y análisis de brillo) y las calibraciones del instrumento requerido. Además, discutimos los pasos críticos en el análisis de datos y cómo identificar y corregir las variaciones de la señal externa, falsas, tales como debido al movimiento de fotoblanqueo o celular.
En general, el análisis presentado es aplicable a cualquier homo - o heterotípicos proteínas interacción en los contactos de la célula, las células de las misma o diferentes tipos y pueden implementarse en un comercial láser confocal de barrido microscopio. Un requisito importante es la estabilidad del sistema, que debe ser suficiente para sondear la dinámica de difusión de las proteínas de interés durante varios minutos.
Introducción
Muchos procesos biológicos ocurren en los sitios de las interacciones célula-célula, por ejemplo, célula adhesión1,2,3, célula fusion4 y reconocimiento celular5. Estos eventos son particularmente importantes durante el desarrollo de los organismos multicelulares y para la comunicación de la célula, por ejemplo, durante la respuesta inmune. Estos procesos son típicamente mediados por las proteínas que se localizan en la superficie, es decir, en la membrana plasmática (PM) de los vecinos de las células y sufren interacciones en el contacto de la célula que son precisamente regulado en espacio y tiempo. En muchos casos, estas interacciones son directo homo - o heterotípicos proteínas trans interacciones, pero pueden también implicar iones o ligandos actuando como enlazadores extracelulares1. Aunque de fundamental importancia, hay una falta de análisis de sondeo estas interacciones proteína-proteína específica directamente en el ambiente natural de las células vivas. Muchos métodos requieren o interrupción de la célula (por ejemplo, ensayos bioquímicos tales como co-inmunoprecipitación6), fijación (por ejemplo, algunas de las técnicas de súper-resolución de microscopía óptica y microscopia electrónica de la célula contacto con7), o son no específicos, por ejemplo, la agregación / ensayos de adherencia8,9. Para resolver este problema, se han implementado técnicas de fluorescencia basada en fluorescencia de resonancia energética transferencia (traste)10 o fluorescencia complementación11. Sin embargo, para lograr distancias suficientemente pequeñas entre fluoróforos, estos métodos requieren etiquetas fluorescentes en el lado extracelular de las proteínas10, potencialmente interferir con las interacciones trans .
Aquí, presentamos un ensayo alternativo basado en la fluorescencia para las interacciones proteína-proteína en los contactos célula-célula. Este enfoque combina enfoques de cross-correlación de fluorescencia (análisis espectroscopia de correlación cruzada de fluorescencia (sFCCS), número de la correlación cruzada y brillo (ccN & B)) y la mezcla de células que expresan un concepto de fusión de la proteína de interés, por ejemplo, un receptor de adhesión. Los receptores investigados en las dos células interactuantes están marcados con dos proteínas fluorescentes separadas espectralmente (FPs), desde el intracelular lado (ver figura 1A).
Los métodos empleados se basan en el análisis estadístico de las fluctuaciones de la fluorescencia inducida por el movimiento difusivo de las proteínas fluorescentes de fusión a través del volumen focal de un láser confocal de barrido microscopio. Más detalladamente, el análisis de sondas la difusión conjunta de las proteínas de interés en ambos vecinos PMs en los contactos célula-célula. Si las proteínas se someten a las interacciones trans , estos complejos trans llevará a proteínas fluorescentes emiten en dos canales espectrales, causando fluorescencia correlacionada fluctuaciones de ambos emisores. Por otro lado, si se produce no vinculante, las fluctuaciones del número de proteínas frente a PMs será independientes, no causando fluctuaciones correlacionadas. La adquisición puede realizarse de dos maneras: 1) sFCCS se basa en un análisis en forma de línea a través del contacto célula-célula y efectiva puntas de prueba de las interacciones en un lugar situado en la región de contacto. A través de un análisis temporal de las fluctuaciones de la fluorescencia, sFCCS proporciona también información dinámica, es decir, los coeficientes de difusión de complejos de proteína; 2) ccN & B se basa en un análisis pixel-wise de una secuencia de imágenes adquiridas en las regiones de contacto célula-célula. Tiene capacidad para sondear y mapa interacciones a lo largo de toda la región (en un plano focal) de contacto, pero no proporciona información sobre la dinámica. Ambos métodos pueden combinarse con un análisis de la luminosidad molecular, es decir, la señal de fluorescencia promedio emitida en la unidad de tiempo por solo difunde complejos de proteína y, así, proporcionar estimaciones de la estequiometría de los complejos de proteína en contactos de la célula.
En este artículo, le ofrecemos protocolos detallados para la preparación de la muestra, calibración del instrumento, adquisición de datos y análisis realizar el ensayo presentado en un comercial láser confocal de barrido microscopio. Los experimentos pueden realizarse en cualquier instrumento equipado con conteo de fotones o detectores analógicos y un objetivo con alta apertura numérica. Además discutir pasos críticos del protocolo y proporcionar esquemas de corrección para varios procesos causando fluctuaciones de señal artefactual, p. ej., detector ruido, movimiento fotoblanqueo o celular. Originalmente desarrollado para probar las interacciones entre las células adherentes, el ensayo puede ser modificado para que las células de suspensión, o adaptados a los sistemas modelo de membranas, por ejemplo, propiedades gigantes vesículas (2.fino) o plasma gigante vesículas de membrana (GPMVs), que permite la cuantificación de las interacciones en entornos diferentes lípidos o en la ausencia de un citoesqueleto organizado12,13.
Análisis de espectroscopia de fluorescencia de la correlación cruzada es una versión modificada de la espectroscopia de correlación cruzada de fluorescencia14 y fue diseñado específicamente para sonda lenta dinámica difusión en membranas de lípidos15. Se basa en una adquisición de exploración de línea perpendicular a la PM que contiene las proteínas fluorescentes de interés. Para probar las interacciones de dos especies de proteínas diferentemente etiquetadas, la adquisición se realiza en dos canales espectrales usando dos líneas láser y dos ventanas de detección de fluoróforos espectralmente separados. Debido a la dinámica de la difusión lenta de las proteínas en el PM (D≤ ~ 1 μm2/s), puede realizarse una medición libre de charla Cruz alternando el esquema de excitación de la línea a la línea15. El análisis comienza con: 1) un algoritmo de alineamiento corregir para el movimiento lateral de la célula basado en block-wise con un promedio de ~ 1000 líneas, 2) determinación de la posición con fluorescencia máxima señales decir, el PM posición, en cada bloque y cambio de 3) de todos los bloques a un común origen12,15, por separado en cada canal. A continuación, una selección automática de píxeles correspondiente a la PM se realiza seleccionando la región central de un ajuste gaussiano de la suma de todas las líneas alineadas (es decir, centro ± 2.5σ). Integración de la señal en cada línea produce la membrana fluorescencia serie f (t) en cada canal (g = green canal, r = canal rojo). Nota que el tamaño del pixel ha de ser pequeño, por ejemplo, < 200 nm, para reconstruir la forma del punto de difundir la función y encontrar su centro, correspondiente a la posición de la PM. En presencia de fotoblanqueo substancial, la serie de tiempo de fluorescencia en cada canal puede modelada con una función doble exponencial y luego corregir con la fórmula siguiente:16
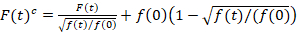 . (1)
. (1)
Es importante tener en cuenta que esta fórmula corrige eficazmente las amplitudes y tiempos de difusión obtenidos del análisis de correlación de f (t)c, en comparación con las estimaciones del parámetro que se obtendría de la no corregida f (t). Entonces, las funciones de auto - y la correlación cruzada (ACFs / CCFs) de la fluorescencia señales se calculan:
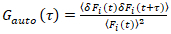 , (2).
, (2).
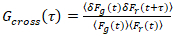 , (3).
, (3).
donde δF = F(t) - 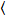 F(t)
F(t)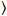 y = g, r.
y = g, r.
Un modelo de difusión bidimensional entonces se acopla a todas las funciones de correlación (SFC):
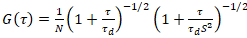 . (4)
. (4)
Aquí N denota el número de proteínas fluorescentes en el volumen de observación y τd el tiempo de difusión para cada canal. Este modelo toma en cuenta que en la configuración experimental descrita, difusión de proteínas en la PM se presenta en el plano x-z, en contraste con la configuración de uso general de correlación de fluorescencia espectroscopia (FCS) experimentos en las membranas de sondeo difusión en el plano x-y del confocal volumen17. La cintura w0 y el factor de estructura S, describiendo la elongación wz del volumen focal en z, S = wz/w0, se obtienen de una medida de calibración punto de FCS realizada con tintes espectral similares y misma configuración óptica utilizando valores ya están disponibles para el coeficiente de difusión Dtinte:
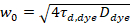 , (5).
, (5).
donde τd, tinte es el tiempo medido medio difusión de las moléculas de colorante, de un modelo de difusión tridimensional de los datos, teniendo en las transiciones de la cuenta de una fracción T de todas las moléculas de N a una Estado triplete con una constante de tiempo ττ:
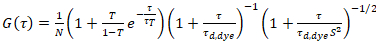 . (6)
. (6)
Por último, coeficientes de difusión (D), los valores de brillo molecular (ε) y la relativa correlación cruzada de datos sFCCS (rel.cc.) se calculan como sigue:
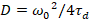 , (7).
, (7).
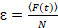 , (8).
, (8).
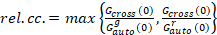 , (9).
, (9).
donde GCruz(0) es la amplitud de la función de correlación cruzada y 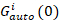 es la amplitud de la función de autocorrelación en el -ésimo canal.
es la amplitud de la función de autocorrelación en el -ésimo canal.
Esta definición de la relativa correlación cruzada, es decir, utilizando máximo en lugar de decir en la ecuación 9, toma en cuenta que el número máximo de conjuntos de dos especies de proteínas presentes en diferentes concentraciones se ve limitado por la especies presentes en un número inferior.
Brillo y el número de la correlación cruzada se basa en un análisis del momento de la intensidad de fluorescencia para cada píxel de una pila de imagen adquirida con el tiempo en una posición fija en la muestra, por lo general consisten en ~ 100-200 marcos, con dos espectral canales () g = green canal, r = canal rojo). De la media temporal 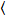 I
I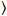 i y varianza
i y varianza 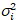 , el brillo molecular εi y número n se calculan en cada pixel y canal espectral ( = g, r)18:
, el brillo molecular εi y número n se calculan en cada pixel y canal espectral ( = g, r)18:
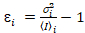 , (10).
, (10).
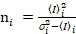 . (11)
. (11)
Es importante tener en cuenta que las ecuaciones dadas se aplican al caso ideal de un verdadero detector de recuento de fotones. Las ecuaciones siguientes aplican para sistemas de detección analógico,19,20:
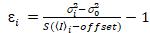 , (12).
, (12).
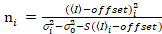 . (13)
. (13)
Aquí, S es el factor de conversión entre fotones detectados y las cuentas de digitales grabadas, 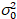 es el ruido de lectura y offset se refiere a la compensación de la intensidad de detector. Por lo general, estas cantidades se deberán calibrar, para cualquier tipo de detector, basado en la medición de la variación del detector en función de la intensidad de iluminación constante19, p. ej., una superficie metálica reflectora o solución colorante seco. El offset puede determinarse midiendo la tasa de conteo para una muestra sin luz de excitación. Realizando una regresión lineal de la varianza asociados detector
es el ruido de lectura y offset se refiere a la compensación de la intensidad de detector. Por lo general, estas cantidades se deberán calibrar, para cualquier tipo de detector, basado en la medición de la variación del detector en función de la intensidad de iluminación constante19, p. ej., una superficie metálica reflectora o solución colorante seco. El offset puede determinarse midiendo la tasa de conteo para una muestra sin luz de excitación. Realizando una regresión lineal de la varianza asociados detector 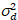 contra la trama de la intensidad (), S y
contra la trama de la intensidad (), S y 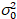 puede ser resuelto19:
puede ser resuelto19:
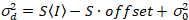 . (14)
. (14)
Por último, el brillo de la correlación cruzada se calcula en cada pixel y se define en general como21
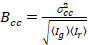 , (15).
, (15).
donde 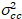 es la varianza de la Cruz
es la varianza de la Cruz 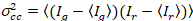 .
.
Para filtrar las fluctuaciones de larga duración, todos ccN y cálculos de B se realizan siguiendo un furgón filtrado, independientemente para cada pixel22. En Resumen, ni, ε ( = g, r) y Bcc se calculan en desplazamiento de segmentos de p. ej., 8-15 marcos. Los valores así obtenidos pueden ser promediados entonces para obtener el pixel final valores de número y brillo.
Análisis de la estequiometría
Para estimar la estequiometría de los complejos de la proteína en los contactos célula-célula, el brillo molecular puede analizarse por separado en cada canal espectral para la sFCCS o ccN y B los datos. En sFCCS, un valor de brillo se obtiene por medición de cada canal. En ccN y B, se obtiene un histograma de brillo de los píxeles correspondientes al contacto célula-célula y el valor promedio (o mediano) puede utilizarse como brillo representativo para la medición. Por realizar el mismo análisis en referencia monomérica, todos los valores de brillo pueden ser normalizados para obtener directamente el estado oligomérico promedio de los complejos de proteína detectado. En este punto, es importante corregir la presencia de FPs no fluorescente que puede resultar en una subestimación del estado oligomérico. Normalmente esto se realiza midiendo el brillo de un homo dimérico referencia proteína23,24 con sFCS un color o número y el brillo (N & B).
Protocolo
1. Preparación: Célula mezcla ensayo
Nota: El siguiente protocolo describe el procedimiento de mezcla para células adherentes. Puede ser modificada para que las células cultivadas en suspensión.
- Un número apropiado de células en una placa de 6 pozos, por ejemplo, 800.000 células HEK 293T (cuentan con una cámara de recuento de Neubauer), un día antes de la transfección de la semilla. El número puede ser modificado dependiendo del tiempo entre siembra y transfección y ajustado para otros tipos de células. Para realizar un experimento básico (es decir, proteínas de interés y control negativo), prepare por lo menos 4 pocillos. Células en cultivo a 37 ° C, 5% CO2 en medio de Dulbecco modificado Eagle Medium (DMEM) suplementado con suero fetal bovino (10%) y L-glutamina (1%).
- Transfectar las células según las instrucciones del fabricante (véase la Tabla de materiales).
- Para realizar un experimento básico, transfectar, en pozos separados, plásmidos para la proteína de interés unida a un 'verde' (p. ej., monoméricas mayor proteína verde fluorescente (mEGFP), o proteína amarilla fluorescente (mEYFP)) o 'rojo' (por ejemplo, mCherry, o mCardinal) proteína fluorescente.
Nota: En este protocolo, nos centramos en mEYFP APLP1 y APLP1-mCardinal12y el correspondiente control negativo, por ejemplo, myristoylated-palmitoylated-mEYFP (myr-Palma-mEYFP) y - mCardinal (myr-palm-mCardinal)12. Por lo general, 200 ng - 1 μg de ADN plásmido son suficientes. Eficiencia de transfección alta aumenta la probabilidad de encontrar células 'rojas' y 'verdes' en contacto. Modificar la cantidad de plásmido y transfección reactivos para optimizar la eficiencia de transfección. Crítica: Confluencia de células debe ser alrededor 70% cuando transfectar las células. Si las células son demasiado confluente, disminuirá la eficiencia de transfección. Si las células no son confluente, transfección y mezcla puede inducir estrés y evitar que muchas células del accesorio apropiado después de la mezcla.
- Para realizar un experimento básico, transfectar, en pozos separados, plásmidos para la proteína de interés unida a un 'verde' (p. ej., monoméricas mayor proteína verde fluorescente (mEGFP), o proteína amarilla fluorescente (mEYFP)) o 'rojo' (por ejemplo, mCherry, o mCardinal) proteína fluorescente.
- Realizar mezcla de ~4 ± 2 h después de la transfección de la célula.
- Retire el medio de cultivo y lave cada bien suavemente con 1 mL de PBS suplementado con Mg2 + y Ca2 +. Luego, retire el PBS. (Crítica) Gota de PBS en borde bien para evitar el desprendimiento de las células durante el lavado.
- Añadir 50 μl tripsina etilendiaminotetracético (EDTA) solución mediante goteo a cada bien para facilitar el desprendimiento de las células. Incubar a 37 ° C por 2 min luego, lentamente agitar la placa de la pozo 6 lateralmente para separar las células.
Nota: Tiempos de incubación prolongado pueden ser necesarios para algunos tipos de células. - Agregar 950 μl de medio de crecimiento para cada pozo y resuspender las células mediante pipeteo unas veces arriba y abajo de, tal modo separar todas las células desde bien abajo. (Crítica) Asegúrese de que las células se resuspendió correctamente y separadas entre sí por controlar visualmente la ausencia de agregados de células grande después resuspension. De lo contrario muchos contactos 'verdes'-'rojos' o 'verdes'-'rojos' se obtiene después de mezclar.
- Transferir la solución de la célula de un pozo (proteína de interés o control negativo) a la correspondiente, es decir, 'rojo' (por ejemplo, transfectada APLP1-mCardinal) 'verde' (p. ej., transfectada APLP1-mEYFP) las células. Mezclar mediante pipeteo suavemente unas cuantas veces hacia arriba y hacia abajo. Entonces, semilla de las células mixtas en platos de fondo de cristal de 35 mm (1 mL de solución de mezclado de la célula por plato), más 1 mL de medio de cultivo y cultura había sembrado células para otro día a 37 ° C, 5% CO2.

Figura 1 . Flujo de trabajo experimental y representación esquemática de análisis espectroscopia de correlación cruzada de fluorescencia y análisis de número y brillo de correlación cruzada en los contactos célula-célula. (A) esquema de preparación de la muestra: dos poblaciones de células transfectadas con la proteína del interés (e.g., APLP1) fusionada a dos proteínas fluorescentes espectralmente distintas (por ejemplo, mEYFP y mCardinal) se mezclan después de transfección. Contactos de células transfected diferentemente son seleccionados en los experimentos de microscopía. Para evitar interferencias con dominios de Unión extracelular, la proteína fluorescente debe ser fusionada a la terminal intracelular de la proteína de interés. (B) exploración FCCS (sFCCS) las medidas son realizada perpendicularmente hasta el contacto de la célula en dos canales espectrales (canal 1, verde y canal 2, rojo). Líneas de exploración (representadas como kymographs) se alinean y suman píxeles de membrana. Luego, se calcula ACFs y MCP de los rastros de intensidad F(t). ACFs se representan en rojo y verde. CCF se representa en azul. Adquisición de (C) correlación cruzada N & B (ccN & B) da como resultado una pila de imagen tridimensional (x-y-tiempo). Un ROI es seleccionado por el contacto célula-célula. Y luego brillo canal y correlación cruzada (ε1, ε2y Bcc) los valores se calculan en cada pixel contacto célula-célula. Los resultados entonces se visualizan como histogramas, agrupación de los píxeles seleccionados. Haga clic aquí para ver una versión más grande de esta figura.
2. Preparación: Control positivo para los experimentos de correlación cruzada y construcción Homo-Dimer para análisis de brillo
- 600.000 células HEK 293T, cuentan con un celular con cámara, en los platos de fondo de cristal de 35 mm un día antes de la transfección de la semilla. Cultura de las células a 37 ° C, 5% CO2 en medio DMEM completo (véase el paso 1.1) para otro día.
- Transfectar las células con ~ 250 ng de plásmido de DNA según las instrucciones del fabricante. Para el control positivo de la correlación cruzada, utilizar un plásmido de codificación un hetero dímero anclado en la membrana de la proteína fluorescente, por ejemplo, myr-Palma-mCherry-mEGFP o myr-Palma-mCardinal-mEYFP12 correspondiente a los FPs de la proteína de interés. Para la calibración de brillo, utilizar plásmidos codifican tanto una anclada a la membrana monómero FP y homo-dimer correspondiente a los FPs fusionado a la proteína de interés, por ejemplo, myr-Palma-mEYFP y myr-Palma-mEYFP-mEYFP para calibrar el análisis de brillo de MEYFP APLP112.
- Cultura de las células a 37 ° C, 5% CO2 en medio DMEM completo (véase el paso 1.1) para otro día.
3. confocal láser microscopía: Instalación y calibración de volumen Focal
Nota: El siguiente protocolo es escrito para los experimentos realizados con mEGFP/mEYFP y mCherry/mCardinal en el láser confocal microscopio utilizado en este estudio. La configuración óptica, la configuración de software (líneas láser, espejos dicroicos, filtros) y la elección de tintes de calibración pueden ser modificadas para otras configuraciones de FPs y microscopio.
- Encienda el microscopio y láser por lo menos una hora antes del experimento para asegurar la estabilidad del láser y conseguir el equilibrio de la temperatura.
- Preparar 100-200 μL de soluciones adecuado tinte fluorescente soluble en agua (véase la Tabla de materiales por ejemplo) en el agua o PBS para calibrar el volumen focal, con concentraciones entre 10-50 nm.
- Coloque las soluciones de tinte en un plato de fondo de la limpieza de 35 mm cristal #1.5, es decir, con un grosor de 0.16-0.19 mm.
Nota: Lo ideal es utilizar platos con vidrio de cubierta de alto rendimiento con una tolerancia de poco espesor, por ejemplo, 0.170 ± 0.005 mm, permitiendo una corrección óptima cuello de anillo (paso 3.6). Es importante utilizar el mismo tipo de plato ya utilizado más adelante para los siguientes experimentos. - Coloque el plato que contiene la solución de tinte directamente sobre el objetivo (preferiblemente, inmersión en agua, con NA 1.2) para asegurar el enfoque en la solución. Como alternativa, coloque el plato en el portamuestras y el enfoque en la muestra (por ejemplo, 10-20 μm por encima del fondo del plato).
Nota: No recomendamos usar objetivos de aceite debido a la mala señal obtenida al enfoque profundo en las muestras acuosas. - Configurar la ruta de excitación y emisión, por ejemplo, elegir el láser de 488 nm, espejo dicroico 488/561 nm, detección ventana 499-552 nm y un tamaño de agujero de alfiler de 1 unidad de Airy (AU). Asegúrese de que el tamaño del agujero de alfiler es el mismo que se utilizará en las medidas de correlación cruzada.
- Ajuste la posición del agujero de alfiler (ajuste del agujero de alfiler) y el anillo de cuello objetivo para maximizar la tasa de conteo. Para ello, gire el anillo de cuello hasta que se detecta la tasa de conteo máximo.
Nota: La corrección de anillo collar representa el grosor específico del cubierta de vidrio. Maximizar la tasa de conteo, es decir., que recoge tantos fotones por molécula como sea posible, es fundamental para maximizar la relación señal a ruido (SNR) de las mediciones. - Realizar una serie de mediciones de punto FCS (p. ej., 6 medidas en diferentes lugares, cada uno con 15 repeticiones de 10 s, es decir, 2,5 min tiempo total, muestra con tiempo de permanencia de 1 μs o menos) en el mismo poder de láser utilizado en la correlación cruzada mediciones (típicamente ~ 1%, es decir, ~ 1-2 MW).
- Ajustar un modelo de difusión tridimensional incluyendo una contribución de trío (ecuación 6) a los datos.
Nota: Normalmente, los tiempos de difusión obtenidos son alrededor de 30 μs y el factor de estructura es alrededor de 4-8. - Calcular la cintura w0 del tiempo de difusión promedio medido y publicado los valores para el coeficiente de difusión del colorante usado en temperatura ambiente25 según la ecuación 5. Los valores típicos son 200-250 nm.
- Repita la rutina de calibración (pasos 3.4 3.9) con un colorante fluorescente diferente para un segundo canal de detección si es necesario (por ejemplo, 561 nm de excitación y detección entre 570 nm y 695 nm). Mantener la posición del agujero de alfiler y el tamaño como lo fue el primer canal de detección.
- Calcular el brillo molecular (ecuación 8) de las mediciones de calibración y almacenar los valores obtenidos.
Nota: Los valores típicos para la configuración usada son ~8-10 kHz/1,8 μW 488 nm energía de excitación en la molécula (MOL). Inferiores a valores generalmente podrían indicar suciedad en el objetivo, desalineamiento de la instalación o una salida reducida laser. Comprobar y almacenar energías de salida de láser en el objetivo regularmente usando un medidor de potencia. Para la comparación de diferentes configuraciones, brillo molecular normalizada por la potencia del láser de excitación es el parámetro más significativo para evaluar el desempeño del microscopio.
4. Análisis de espectroscopia de correlación cruzada de fluorescencia: adquisición
Nota: El siguiente protocolo es escrito para los experimentos realizados con mEGFP/mEYFP ('verde') y mCherry/mCardinal ('rojo') en el microscopio confocal láser utilizado en este estudio. La configuración óptica y la configuración de software (líneas láser, espejos dicroicos, filtros) puede ser diferente para otros montajes FPs o microscopio.
- Establecer la trayectoria óptica, por ejemplo, 488 nm y 561 de nm de excitación y un espejo dicroico 488/561 nm, agujero de alfiler en 1 AU para la excitación de nm 488. Para evitar interferencia espectral, seleccione dos pistas separadas para excitar y detectar mEGFP/mEYFP (488 nm excitación, canal verde) y mCherry / mCardinal (561 nm excitación, canal rojo) secuencialmente y seleccione el interruptor de pistas de cada línea. Para la detección, utilizar filtros adecuados para ambos canales, por ejemplo, 499-552 nm en el canal verde y 570-695 nm en el canal rojo.
- Si alterna de excitación no es posible, utilice configuración de filtro apropiado para el canal rojo para minimizar la interferencia espectral (es decir, detectar fluorescencia mCherry/mCardinal no por debajo de 600 nm). Esto puede reducir la cantidad de fotones detectados en el canal rojo y así reducir el SNR.
- Coloque el plato que contiene las células mezcladas en el portamuestras. Espere al menos 10 minutos para conseguir el equilibrio de temperatura y reducir la deriva de enfoque.
- Se centran en las células mediante la transmisión de luz en el menú de localización .
- La búsqueda de un par de 'rojo' y una 'verde' de la célula en contacto entre sí. Para el cross-correlación positiva o homo-dimer control de brillo (ver sección 2), buscar una celda aislada emitiendo fluorescencia en canales o la señal respectiva homo-dimer en la PM.
Nota: (Crítica) minimice muestra la exposición mientras buscaba las células evitar la decoloración, que puede reducir la correlación cruzada26. Por lo tanto, la exploración de la velocidad de escaneo más rápida y potencias de láser de baja. Para evitar la saturación del detector mientras que expresaban fuertemente las células de la proyección de imagen, búsqueda en el modo de integración. Sin embargo, para minimizar la exposición, análisis en menores potencias de láser es posible en modo de conteo de fotones . - Seleccione un perpendicular del camino de exploración contacto célula-célula (o a horas de una sola célula para el control de brillo positivo correlación cruzada o homo-dimer) utilizando el botón de cultivo como se muestra en las figuras 1B y 2A.
Nota: Algunos microscopios antiguos no permiten direcciones de exploración arbitraria. En este caso, contactos de la célula con una orientación perpendicular a la dirección de análisis debe estar situado. -
Zoom para lograr un tamaño de pixel de 50-200 nm y selecta línea de en el Modo Scan. Establecer tamaño del marco 128 pixeles del × 1.
Nota: Tamaño de píxel típico es de 160 nm, correspondiente a una longitud de la exploración de alrededor de 20 μm. - Establecer velocidad de exploración en el máximo valor permitido, por ejemplo, 472,73 μs por línea.
Nota: Para un esquema alternativo de excitación, esto corresponde a 954,45 μs tiempo de la exploración, es decir, ~ 1000 exploraciones/s en el programa de instalación utilizado. La velocidad de exploración puede ajustarse según el coeficiente de difusión de la proteína de interés. Para las proteínas ancladas a membrana, tiempos de difusión típicos son alrededor de 10-20 Sra. el tiempo de exploración debe ser por lo menos diez veces menor que los tiempos de difusión. Velocidades de exploración más bajas pueden inducir mayor photobleaching y requerir menores potencias de iluminación. Alternativamente, se puede imponer una pausa, por ejemplo, 5 ms, entre cada exploración muy lentamente difunde complejos utilizando el intervalo en el submenú de Series de tiempo . - Elegir el láser adecuado poderes, por ejemplo, ~ 1-2 MW para 488 nm y ~ 5-10 MW para la excitación de nm 561.
Nota: Potencias de láser mayores mejoran la SNR, pero aumentan el fotoblanqueo. Por lo tanto, deben ser elegidos potencias de láser que photobleaching es menos del 50% de la tasa de conteo inicial. - Establecer ciclos de 100.000-500, 000.
Nota: El número de exploraciones, es decir, duración de la medición, puede variar: tiempo de medición mejorará SNR y puede ser más apropiado para difundir lentamente las moléculas, sin embargo, el movimiento de las células y el fotoblanqueo limitan la máxima medida hora. Los datos presentados aquí fueron adquiridos habitualmente ~ 3-6 min, es decir, 200.000-400.000 línea explora. - Establecer detectores en modo de conteo de fotones . Pulse Inicio experimento para empezar la adquisición. Repita los pasos 4,5-4.11 medir otra célula.
Nota: Se recomienda medir 10-15 células por muestra a nivel de expresión diferente. (Crítica) Evitar la saturación del detector en niveles de alta expresión. La tasa de conteo máximo no debe exceder ~ 1 MHz. - Si se realizan análisis de brillo para determinar los Estados, realizar mediciones de calibración de brillo homo-dimer según pasos modificadas 4.1-4.11: medir cada homo-dimer de la proteína fluorescente por separado (en células aisladas, con Protocolo artículo 2) y realizar mediciones en un canal espectral.
5. Análisis de espectroscopia de correlación cruzada fluorescencia: Análisis de los datos
Nota: El siguiente protocolo sigue una implementación del procedimiento de análisis que se describe detalladamente en anteriores artículos12,15. El código del software está disponible a petición a los autores.
- Exportar los archivos de datos (por ejemplo, CZI) a una imagen RGB TIFF en formato de datos raw. Este archivo contendrá un kymograph con el verde y los datos de canal rojo, en el canal llaman G y R de la imagen, respectivamente.
- Importar el archivo TIFF con el software de análisis apropiado y proceda a realizar el análisis.
Nota: Los siguientes pasos (pasos 5.3-5.7) se aplican por separado para cada canal: - Alinee las líneas realizando un promedio de tiempo segment-wise o mover bloques de líneas 500-1000. Determinar la posición de la membrana, es decir, la posición del pixel con la tasa de conteo máximo, en cada bloque. Cambiar todos los bloques en la misma posición lateral. Este procedimiento corrige el desplazamiento lateral del contacto célula-célula, por ejemplo, debido al movimiento de la célula.
- En definitiva todas las líneas alineadas a lo largo el eje del tiempo y el perfil de intensidad media usando una función Gaussiana. En presencia de fondo intracelular importante, utilizar un Gaussian más una función sigmoide. Definir los píxeles correspondientes a la membrana como todos los píxeles dentro de ±2.5σ de la posición de la membrana y suma la intensidad de los píxeles de cada línea, obteniendo un valor de señal de fluorescencia individual para cada punto del tiempo (es decir, para cada línea de exploración).
- Si es necesario (por ejemplo, fondo > 10% de la señal de la membrana), aplicar una corrección de fondo restando la intensidad promedio de píxeles en el citoplasma multiplicado por 2.5σ (en unidades de píxel) de la fluorescencia de membrana, en bloques de 1000 líneas. Evitar brillantes vesículas intracelulares al seleccionar píxeles del fondo.
- Si se observa el fotoblanqueo, aplicar una corrección de decoloración. Por lo tanto, montar la serie de tiempo de fluorescencia de membrana con una función doble exponencial y aplicar la corrección adecuada fórmula, ecuación 116.
Nota: Alternativamente, Fourier espectro basado en esquemas de corrección pueden ser aplicada27. (Crítica) Si fotoblanqueo está presente pero no corregida para, el CSA puede distorsionarse severamente y parámetros estimados pueden estar sesgados fuertemente (e.g., vea la figura 5E). - Calcule la ACFs y MCP según las ecuaciones 2 y 3 utilizando, por ejemplo, un algoritmo de múltiples-tau28. Para mejorar la fiabilidad de los análisis y evitar artefactos, realizar los cálculos de segmentos iguales de 10-20 de la medición total. Inspeccione la serie de tiempo de fluorescencia y CFs en cada segmento y segmentos claramente distorsionados (ver ejemplos en la Figura 4A- 4D). Promedio de todos los segmentos no-torcido.
Nota: Este procedimiento puede ser automatizado para evitar un sesgo subjetivo a la información29. Para mediciones muy inestables puede ser útil tener muchos segmentos cortos. Sin embargo, la longitud de un segmento debe ser al menos tres órdenes de magnitud por encima del tiempo de difusión para evitar estadística undersampling errores29,30,17. - Ajustar un modelo de difusión bidimensional, ecuación 4, para el CFs obtenidos. Por lo tanto, fijar el factor de estructura para el valor obtenido en la medida de calibración (Protocolo, artículo 3). La precisión del ajuste puede mejorarse realizando un ajuste ponderado utilizando los pesos estadísticos de cada punto de datos obtenidos del algoritmo de tau múltiples.
- Calcular el coeficiente de difusión con la cintura calibrada según la ecuación 7.
- Calcular el brillo molecular dividiendo la intensidad de fluorescencia media en cada canal por el número de partículas, ecuación 8. Normalizar el valor de brillo determinado en cada canal por el brillo promedio de la referencia monomérica correspondiente para obtener el estado oligomérico, teniendo en cuenta no fluorescente FPs23. Para ello, determine los valores de brillo medio homo-dimer de análisis de un solo color para calcular la fracción de no fluorescente FPs23.
- Calcular la correlación cruzada relativa según la ecuación 9.
6. correlación cruzada número y brillo: calibración del Detector
Nota: El siguiente protocolo provee una guía general acerca de cómo calibrar el sistema de detección. Este procedimiento es obligatorio para sistemas de detección analógicos, pero no es estrictamente necesario cuando se usan detectores cuenta del fotón real.
- Seco soluciones adecuado tinte soluble en agua (véase Tabla de materiales por ejemplo) en un plato de fondo de cristal de 35 mm. Establecer la ruta óptica en consecuencia, es decir, 488 o 561 nm de excitación y detección en 499-552 nm o 570-695 nm, respectivamente.
Nota: Alternativamente, una superficie metálica reflectora puede utilizarse en lugar de soluciones de tinte seca mediante la colocación de la pieza de metal directamente sobre el objetivo. - Realizar mediciones de N & B de un solo color en regiones con concentraciones diferentes de tinte o en potencias de láser diferentes. Por lo tanto, utilizar el Zoom para lograr un tamaño de pixel de 300 nm, escaneo velocidad tiempo de permanencia del píxel apropiado, por ejemplo, 25 μs y ciclos a 100-200 marcos.
- Detectores de recuento de fotones (o modo analógico si las mediciones se realizan con detección analógica) y pulse Inicio experimento para empezar la adquisición. Realizar la medida a cero potencia de excitación para determinar el offset de intensidad.
- Trama de la varianza de píxeles en función de la intensidad de píxel píxeles medidos todos y realizar un ajuste lineal de estos datos. Determinar S como la pendiente del ajuste lineal. Calcular el ruido de lectura de la intersección, con S y el offset de intensidad determinada según la ecuación 14.
7. correlación cruzada número y brillo: adquisición
- Siga los pasos 4.1-4.4 del Protocolo de adquisición de sFCCS.
- Usar cultivos para seleccionar un marco de 512 × 128 pixeles alrededor de un contacto de célula (o el PM aislado para el control de brillo de homo-dimer) y Zoom para lograr un tamaño de pixel de 50-100 nm.
- Utilice Scan velocidad para establecer tiempo de permanencia del píxel apropiado, por ejemplo, 6,3 μs.
Nota: En N & B, el tiempo de permanencia del pixel debe ser mucho menor que el tiempo de difusión de la proteína de interés. Si se elige un esquema alternativo de excitación, por ejemplo, cambiar pistas de cada línea, el tiempo entre las dos vías debe ser menor que el tiempo de difusión de la proteína de interés. De lo contrario se reduce la correlación cruzada detectable. - Establecer ciclos en 100-200 marcos.
Nota: Un número mayor de marco mejorará la SNR, sin embargo, movimiento celular puede limitar el tiempo de medición total. El tiempo de exploración por el marco debe ser mucho mayor que el tiempo de difusión de la proteína de interés. De lo contrario se reduce el brillo aparente, es decir, las partículas parecen estar inmóviles. Para complejos de difusión muy lentamente, imponer una pausa, por ejemplo, 2 s, entre marcos con el intervalo en el submenú de Series de tiempo . - Set láser poderes a valores adecuados (los valores típicos son ~ 1-2 MW de 488 nm y ~ 5-10 MW para la excitación de nm 561).
Nota: Mayor potencia láser conduce a un mayor brillo y mejor SNR, pero también mayor photobleaching. Potencias de láser deben ser lo suficientemente altos para lograr un brillo detectado de menos ~ 1 kHz/MOL pero mantenerse lo suficientemente bajo como para evitar más de fotoblanqueo de 10-20%. Para fotoblanqueo mEGFP/mEYFP o mCherry/mCardinal, a menos de 10% se obtienen generalmente. - Establecer detectores en conteo de fotones (o modo analógico si las mediciones se realizan con detección analógica). Pulse Inicio experimento para empezar la adquisición.
- Evaluar la tasa de conteo de fotones. Si las tasas de conteo de pixeles contacto célula-célula exceden 1 MHz, reducir la potencia del láser o seleccionadas células con bajos niveles de expresión. Repita los pasos 7.2 7.7. para medir el par siguiente de células. Se recomienda medir 10-15 células por experimento en niveles de expresión diferentes.
- Si se realizaron un análisis de brillo para cuantificar la Oligomerización, mida la homo-dimer brillo calibración según pasos modificados 7.7 7.1: medir cada homo-dimer de la proteína fluorescente por separado (en células aisladas, con Protocolo artículo 2) y realizar mediciones en un canal espectral.
8. correlación cruzada número y brillo: Análisis de datos
Nota: El siguiente protocolo sigue un procedimiento de análisis anteriormente descritas12,31. El código del software está disponible de los autores a petición.
- Importar los datos en bruto (por ejemplo, CZI archivos pueden ser importados usando el paquete de32 Bioformats). Promedio de todos los fotogramas y seleccione una región de interés (ROI) en el contacto célula-célula.
- Realizar una imagen alineación algoritmo33, por ejemplo, maximizando la correlación espacial entre ROIs en los marcos posteriores traducciones lateral arbitraria, promediada sobre ambos canales. Este procedimiento corrige para movimiento lateral de las células.
- Aplicar un filtro boxcar del22 para reducir fluctuaciones de larga vida extrañas, provenientes de, por ejemplo, movimiento de celular residual o blanqueo de fondo. Como alternativa, puede aplicarse un método robustos para corregir por photobleaching34.
Nota: Si no hay análisis segment-wise o robustos se aplicación, el brillo evidente puede ser sobreestimado en gran medida.- Definir segmentos deslizantes de, por ejemplo, 8 a 15 fotogramas (por ejemplo, marcos de 1 a 8, 2 a 9 y así sucesivamente) y calcular los valores de brillo de canal y correlación cruzada según las ecuaciones 10, 11 y 15 pixel-wise en cada segmento. Si los detectores no son fotón verdadero contar detectores, considerar los parámetros de detector calibrado en el cálculo de la luminosidad, es decir, utilice las ecuaciones 12 y 13 en su lugar.
Nota: Calcular los valores de brillo en segmentos de 8 a 15 marcos conduce a una subestimación de 10-20% de la luminosidad absoluta y una sobreestimación de 10-20% de los números de la partícula. Sin embargo, cocientes de luminosidad (por ejemplo, dimer para brillo de monómero) no se ven afectadas, como la longitud del segmento se mantiene constante a lo largo del análisis (datos no mostrados). El error estadístico para una longitud del segmento determinado puede ser determinado a través de simulaciones y así corregido para. - Promedio los valores obtenidos de brillo pixel-wise en todos los segmentos. En este paso, uno puede quitar el 5% más alto y más bajo de los valores de brillo de segmento de la media o excluir segmentos que muestran una clara distorsión de la intensidad, debido a, por ejemplo, una vesícula intracelular o agregado transitorio presente en estos píxeles.
- Definir segmentos deslizantes de, por ejemplo, 8 a 15 fotogramas (por ejemplo, marcos de 1 a 8, 2 a 9 y así sucesivamente) y calcular los valores de brillo de canal y correlación cruzada según las ecuaciones 10, 11 y 15 pixel-wise en cada segmento. Si los detectores no son fotón verdadero contar detectores, considerar los parámetros de detector calibrado en el cálculo de la luminosidad, es decir, utilice las ecuaciones 12 y 13 en su lugar.
- Trazar los valores de brillo del píxel en función de la intensidad del pixel y seleccionar la población de píxeles que se corresponde con el contacto de la célula. Píxeles del fondo tendrán valores de muy baja intensidad. En este punto, volver a evaluar la tasa de conteo máximo. Excluir los píxeles con tasas de conteo por encima de 1 MHz para evitar que se acumulen.
- Crear histogramas de brillo de canal y correlación cruzada de las célula píxeles contacto y obtener los valores de brillo de un promedio de retorno de la inversión. Normalizar el valor de brillo del canal promedio por el brillo promedio de la referencia monomérica correspondiente para obtener el estado oligomérico, teniendo en cuenta no fluorescente FPs23. Por lo tanto, determine los valores de brillo medio homo-dimer de análisis de un solo color para calcular la fracción de no fluorescente FPs23.
- Para Ilustración, trazar mapas de brillo del canal y correlación cruzada.
Resultados
Una primera prueba para el análisis de interacción de proteínas, es decir, mezcla de células que expresan proteínas fluorescentes espectralmente distintas seguidas por sFCCS/ccN y las mediciones de B (figura 1), debe realizarse en las proteínas que no se esperan que interactuar en el contacto célula-célula (es decir, un control negativo). Por lo tanto, se mezclaron células HEK 293T expresando myristoylated-palmitoylated-mEYFP (myr-P...
Discusión
El procedimiento experimental que se describe aquí permite la investigación de proteínas trans interacciones en los contactos célula-célula, empleando técnicas de espectroscopia fluctuación de fluorescencia, a saber sFCCS y ccN & B. Estos métodos implican un análisis estadístico de las fluctuaciones de la fluorescencia emitida por dos separados espectralmente FPs fusionado a la proteína de interés en un contacto de dos células vecinas, cada una expresando uno o la otra proteína de fusión. La prese...
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Este trabajo fue parcialmente financiado por la Deutsche Forschungsgemeinschaft (DFG) conceder 254850309. Los autores agradecen Madlen Luckner para lectura crítica del manuscrito.
Materiales
| Name | Company | Catalog Number | Comments |
| DMEM growth medium | PAN-Biotech | P04-01548 | |
| DPBS w/o: Ca2+ and Mg2+ | PAN-Biotech | P04-36500 | |
| DPBS w: Ca2+ and Mg2+ | PAN-Biotech | P04-35500 | |
| Trypsin EDTA | PAN-Biotech | P10-023100 | |
| TurboFect Transfection Reagent | Thermo Fisher Scientific | R0531 | |
| HEK 293T cells | DSMZ | ACC 635 | |
| Alexa Fluor 488 NHS Ester | Thermo Fisher Scientific | A20000 | |
| Rhodamine B | Sigma-Alderich | 83689-1G | |
| Plasmid DNA | Addgene | NA | See reference 12 (Dunsing et. al., MBoC 2017),for a detailed description of all plasmids |
| 6-well plate | Starlab | CC7672-7506 | |
| 35-mm glass bottom dishes | CellVis | D35-14-1.5-N | |
| Zeiss LSM780 confocal | Carl Zeiss | NA | |
| MATLAB software package | MathWorks | 2015b | |
| Neubauer cell counting chamber | Marienfeld | 640110 |
Referencias
- Alberts, B., Johnson, A., Lewis, J., Raff, M., Roberts, K., Walter, P. . Molecular biology of the cell. , (2002).
- Tepass, U., Truong, K., Godt, D., Ikura, M., Peifer, M. Cadherins in embryonic and neural morphogenesis. Nature Reviews Molecular Cell Biology. 1 (2), 91-100 (2000).
- Harris, T. J. C., Tepass, U. Adherens junctions: from molecules to morphogenesis. Nature Reviews Molecular Cell Biology. 11 (7), 502-514 (2010).
- Hernández, J. M., Podbilewicz, B. The hallmarks of cell-cell fusion. Development. 144 (24), 4481-4495 (2017).
- Huppa, J. B., Davis, M. M. T-cell-antigen recognition and the immunological synapse. Nature Reviews Immunology. 3 (12), 973-983 (2003).
- Kaden, D., Voigt, P., Munter, L. -. M., Bobowski, K. D., Schaefer, M., Multhaup, G. Subcellular localization and dimerization of APLP1 are strikingly different from APP and APLP2. Journal of cell science. 122, 368-377 (2009).
- Yap, A. S., Michael, M., Parton, R. G. Seeing and believing: recent advances in imaging cell-cell interactions. F1000Research. 4, 273 (2015).
- Kashef, J., Franz, C. M. Quantitative methods for analyzing cell-cell adhesion in development. Developmental Biology. 401 (1), 165-174 (2015).
- Soba, P., et al. Homo- and heterodimerization of APP family members promotes intercellular adhesion. The EMBO Journal. 24 (20), 3624-3634 (2005).
- Kim, S. A., Tai, C. -. Y., Mok, L. -. P., Mosser, E. A., Schuman, E. M. Calcium-dependent dynamics of cadherin interactions at cell-cell junctions. Proceedings of the National Academy of Sciences of the United States of America. 108 (24), 9857-9862 (2011).
- Feinberg, E. H., et al. GFP Reconstitution Across Synaptic Partners (GRASP) Defines Cell Contacts and Synapses in Living Nervous Systems. Neuron. 57 (3), 353-363 (2008).
- Dunsing, V., Mayer, M., Liebsch, F., Multhaup, G., Chiantia, S. Direct evidence of amyloid precursor-like protein 1 trans interactions in cell-cell adhesion platforms investigated via fluorescence fluctuation spectroscopy. Molecular biology of the cell. 28 (25), 3609-3620 (2017).
- Schneider, F., et al. Diffusion of lipids and GPI-anchored proteins in actin-free plasma membrane vesicles measured by STED-FCS. Molecular Biology of the Cell. 28 (11), 1507-1518 (2017).
- Bacia, K., Kim, S. A., Schwille, P. Fluorescence cross-correlation spectroscopy in living cells. Nature methods. 3 (2), 83-89 (2006).
- Ries, J., Schwille, P. Studying Slow Membrane Dynamics with Continuous Wave Scanning Fluorescence Correlation Spectroscopy. Biophysical Journal. 91 (5), 1915-1924 (2006).
- Ries, J., Chiantia, S., Schwille, P. Accurate Determination of Membrane Dynamics with Line-Scan FCS. Biophysical Journal. 96 (5), 1999-2008 (2009).
- Chiantia, S., Ries, J., Schwille, P. Fluorescence correlation spectroscopy in membrane structure elucidation. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1788 (1), 225-233 (2009).
- Digman, M. A., Dalal, R., Horwitz, A. F., Gratton, E. Mapping the number of molecules and brightness in the laser scanning microscope. Biophysical journal. 94 (6), 2320-2332 (2008).
- Dalal, R. B., Digman, M. A., Horwitz, A. F., Vetri, V., Gratton, E. Determination of particle number and brightness using a laser scanning confocal microscope operating in the analog mode. Microscopy research and technique. 71 (1), 69-81 (2008).
- Unruh, J. R., Gratton, E. Analysis of Molecular Concentration and Brightness from Fluorescence Fluctuation Data with an Electron Multiplied CCD Camera. Biophysical Journal. 95 (11), 5385-5398 (2008).
- Digman, M. A., Wiseman, P. W., Choi, C., Horwitz, A. R., Gratton, E. Stoichiometry of molecular complexes at adhesions in living cells. Proceedings of the National Academy of Sciences of the United States of America. 106 (7), 2170-2175 (2009).
- Hellriegel, C., Caiolfa, V. R., Corti, V., Sidenius, N., Zamai, M. Number and brightness image analysis reveals ATF-induced dimerization kinetics of uPAR in the cell membrane. The FASEB journal official publication of the Federation of American Societies for Experimental Biology. 25 (9), 2883-2897 (2011).
- Dunsing, V., Luckner, M., Zühlke, B., Petazzi, R. A., Herrmann, A., Chiantia, S. Optimal fluorescent protein tags for quantifying protein oligomerization in living cells. Scientific Reports. 8 (1), 10634 (2018).
- Chen, Y., Johnson, J., Macdonald, P., Wu, B., Mueller, J. D. Observing Protein Interactions and Their Stoichiometry in Living Cells by Brightness Analysis of Fluorescence Fluctuation Experiments. Methods in enzymology. 472, 345-363 (2010).
- . Absolute Diffusion Coefficients: Compilation of Reference Data for FCS Calibration Available from: https://www.picoquant.com/images/uploads/page/files/7353/appnote_diffusioncoeffients.pdf (2010)
- Foo, Y. H., Naredi-Rainer, N., Lamb, D. C., Ahmed, S., Wohland, T. Factors affecting the quantification of biomolecular interactions by fluorescence cross-correlation spectroscopy. Biophysical journal. 102 (5), 1174-1183 (2012).
- Baum, M., Erdel, F., Wachsmuth, M., Rippe, K. Retrieving the intracellular topology from multi-scale protein mobility mapping in living cells. Nature Communications. 5, 4494 (2014).
- Wohland, T., Rigler, R., Vogel, H. The standard deviation in fluorescence correlation spectroscopy. Biophysical journal. 80 (6), 2987-2999 (2001).
- Ries, J., et al. Automated suppression of sample-related artifacts in Fluorescence Correlation Spectroscopy. Optics Express. 18 (11), 11073 (2010).
- Ries, J., Schwille, P. New concepts for fluorescence correlation spectroscopy on membranes. Physical Chemistry Chemical Physics. 10 (24), 3487 (2008).
- Mayer, M. C., et al. Amyloid precursor-like protein 1 (APLP1) exhibits stronger zinc-dependent neuronal adhesion than amyloid precursor protein and APLP2. Journal of Neurochemistry. 137 (2), 266-276 (2016).
- Linkert, M., et al. Metadata matters: access to image data in the real world. The Journal of Cell Biology. 189 (5), 777-782 (2010).
- Trullo, A., Corti, V., Arza, E., Caiolfa, V. R., Zamai, M. Application limits and data correction in number of molecules and brightness analysis. Microscopy Research and Technique. 76 (11), 1135-1146 (2013).
- Nolan, R., et al. nandb-number and brightness in R with a novel automatic detrending algorithm. Bioinformatics. 33 (21), 3508-3510 (2017).
- Hammond, G. R. V., Sim, Y., Lagnado, L., Irvine, R. F. Reversible binding and rapid diffusion of proteins in complex with inositol lipids serves to coordinate free movement with spatial information. The Journal of cell biology. 184 (2), 297-308 (2009).
- Hendrix, J., Dekens, T., Schrimpf, W., Lamb, D. C. Arbitrary-Region Raster Image Correlation Spectroscopy. Biophysical journal. 111 (8), 1785-1796 (2016).
- Hendrix, J., et al. Live-cell observation of cytosolic HIV-1 assembly onset reveals RNA-interacting Gag oligomers. The Journal of cell biology. 210 (4), 629-646 (2015).
- Hendrix, J., Schrimpf, W., Höller, M., Lamb, D. C. Pulsed Interleaved Excitation Fluctuation Imaging. Biophysical Journal. 105 (4), 848-861 (2013).
- Honigmann, A., et al. Scanning STED-FCS reveals spatiotemporal heterogeneity of lipid interaction in the plasma membrane of living cells. Nature Communications. 5 (1), 5412 (2014).
- Chojnacki, J., et al. Envelope glycoprotein mobility on HIV-1 particles depends on the virus maturation state. Nature Communications. 8 (1), 545 (2017).
- Godin, A. G., et al. Revealing protein oligomerization and densities in situ using spatial intensity distribution analysis. Proceedings of the National Academy of Sciences of the United States of America. 108 (17), 7010-7015 (2011).
- Müller, J. D., Chen, Y., Gratton, E. Resolving Heterogeneity on the Single Molecular Level with the Photon-Counting Histogram. Biophysical Journal. 78 (1), 474-486 (2000).
- Kim, S. A., Heinze, K. G., Bacia, K., Waxham, M. N., Schwille, P. Two-Photon Cross-Correlation Analysis of Intracellular Reactions with Variable Stoichiometry. Biophysical Journal. 88 (6), 4319-4336 (2005).
- Jenkins, E., et al. Reconstitution of immune cell interactions in free-standing membranes. Journal of cell science. 132 (4), (2018).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados