Method Article
Un'esofagectomia Ivor Lewis progettata per ridurre al minimo le complicanze anastomotiche e ottimizzare la funzione Conduit
In questo articolo
Riepilogo
Descriviamo una nuova tecnica anastomonica esofagogia intratocida progettata per creare un'anastomosi di grande diametro, mantenendo contemporaneamente l'afflusso di sangue di condotti per ridurre al minimo l'incidenza di perdite e stenosi anatomotiche. Viene descritta anche la costruzione e l'orientamento del condotto dello stomaco progettato per ottimizzare la funzione del tratto gastrointestinale superiore.
Abstract
Descriviamo una nuova tecnica anastomatica esofagogatrica ("side-to-side: linea di pinzatura", STS) per anastomosi intratociche progettate per creare un'anastomosi di grande diametro, mantenendo contemporaneamente l'afflusso di sangue conduito. Questa tecnica mira a ridurre al minimo l'incidenza di perdite anastomotiche e stenosi, che è una frequente fonte di morbilità e mortalità occasionale dopo l'esofagectomia. Anatomosi esofagogiche analizzano i risultati di questa tecnica STS su 368 pazienti e confrontamo i risultati con 112 pazienti sottoposti ad anastomosi esofagogastri utilizzando un cucitore end-to-end (EEA) per un intervallo di tempo di 8 anni presso il nostro istituto.
La tecnica STS prevede l'allineamento dell'esofago intratoracico rimanente sulla punta della linea di pinzatura curva inferiore di un tubo dello stomaco, creato come condotto sostitutivo per l'esofago. Un dispositivo di pinzatura lineare taglia e ristaples la linea di pinzatura del condotto alla parete laterale dell'esofago in modo laterale. Il lume comune aperto viene quindi chiuso in due strati di suture.
Il totale è stato di 12 (3,8%) perdite anastomiche in pazienti sottoposti ad anastomosis esofagogastrica STS. Due pazienti su otto (25%) ha avuto perdite anastomotiche dopo l'esofagectomia per l'achalasia allo stadio finale rispetto a un tasso di perdita del 2,8% (10/336) dopo l'esofagectomia per altre condizioni. Diciotto (5,2%) pazienti hanno richiesto una mediana di 2 dilatazioni per la stenosi anastomotica dopo l'anastomosi STS. L'alimentazione egiunostomia supplementare è stata richiesta solo nell'11,1% dei pazienti sottoposti ad anastomosi STS dopo la dimissione ospedaliera. Al contrario, i pazienti sottoposti a anastomosi del SEA hanno dimostrato tassi di perdite e stenosi anastomotiche rispettivamente del 16,1% e del 14,3% (p<0,01). L'analisi del tempo degli studi di contrasto postoperatorio che seguono la tecnica STS ha in genere dimostrato un condotto di diametro dritto/uniforme con un contrasto essenzialmente completo svuotamento nell'intestino piccolo entro 3 minuti nell'88,4% dei pazienti.
L'incidenza di perdite erigidi anastomatiche esofagogiche esofagogiche era estremamente bassa utilizzando questa nuova tecnica anastomotica. Inoltre crediamo che sulla base di tempo e analisi qualitative di studi di contrasto postoperatorio, questa tecnica sembra ottimizzare la funzione del tratto gastrointestinale superiore postoperatorio; tuttavia, sono necessari ulteriori studi comparativi.
Introduzione
Le perdite anastomotiche esofagogastriche rappresentano una complicazione non rara dopo l'esofageomia1. Inoltre, una perdita anatomotica è stata associata a risultati sfavorevoli a lungo termine tra cui riammissione ospedaliera, mortalità precoce, e occasionalmente scarsa qualità della vita2,3,4. Una stenosi anastomotica rappresenta una complicazione a lungo termine, che può anche essere una conseguenza di una perdita anastomotica5. Le stenosi anastomotiche hanno un impatto negativo sulla qualità della vita, sia aumentano il costo dell'assistenza.
Poiché i pazienti affetti da carcinoma esofageo vivono più a lungo a causa della rilevazione endoscopica dell'adenocarcinoma in fase iniziale e della terapia per la chemioradio di induzione per i tumori più avanzati localmente, diventa importante anche ottimizzare la funzione del condotto dello stomaco. La "funzione" del condotto gastrico si basa principalmente sulla gravità per il drenaggio. La costruzione e l'orientamento del condotto gastrico possono influenzare la funzione del tratto gastrointestinale superiore e quindi la scarsa "funzione" del condotto può essere il risultato di problemi tecnici.
Dal 2009 abbiamo utilizzato una nuova tecnica STS (side-to-side: staple line-on-staple line" (STS) per anastomosi esofagogastri intratoracici. Questa tecnica è progettata per creare un'anastomosi di diametro maggiore rispetto alle anastomosi fatte con cucitrici end-to-end (EEA), mantenendo contemporaneamente l'afflusso di conduttura di conduita per ridurre l'incidenza di perdite e stenole anastomotiche. Descriviamo questa nuova tecnica anastomotica e inoltre descritto la costruzione e l'orientamento del condotto gastrico per ottimizzare la funzione. Abbiamo confrontato i risultati di questa tecnica STS con le anastomosi eseguite con le cucitrici del SEA nell'arco di 8 anni presso la nostra istituzione.
Protocollo
Questo studio è stato approvato dall'Università dell'Indiana-Purdue University nel comitato di revisione istituzionale di Indianapolis (1109006832). Questa procedura è stata eseguita su tutti i pazienti che necessitano di resezione e resezione dell'esofago intraporacico distale per malattie maligne o benigne dal 2009 presso l'Indiana University Hospital.
1. Fase pre-anestesia
- Posizionare un catetere epidurale.
- Ottenere l'accesso arterioso centrale standard.
- Anestetizzare e intubare utilizzando un doppio tubo endobronchiale sinistro per la ventilazione polmonare selettiva durante la fase toracica dell'operazione.
2. Fase di laparotomia iniziale
- Eseguire una laparotomia mediana superiore compresa l'escissione del processo zyfoide con elettrocauterio. Posizionare un retrattore a parete addominale autosufficiente per l'esposizione alla cavità peritoneale.
- Eseguire un'ampia manovra Kocher, che mobilita l'intero duodenum dal retroperitoneum. Questa manovra non solo raddrizza il condotto gastrico, ma permette anche porzioni ben vascolarizzate del condotto dello stomaco per essere avanzate sopra l'arco azygos.
- Posizionare temporaneamente una spugna di laparotomia di dimensioni standard sotto il duodenum per elevare il condotto, che viene rimosso nella fase finale di laparotomia.
- Dividere il legamento gastrocolico cauterizzando e dividendo i vasi sanguigni omentali con un dispositivo energetico standard. Evitare la manipolazione dei vasi gastroepiploici giusti posizionando un tubo nasogastrico lungo la curvatura maggiore, che viene utilizzato come una "maniglia" che ritrae lo stomaco verso l'alto.
- Segnare il peritoneo circonferenzialmente intorno ai crus diaframmatici con elettrocauterio e posizionare temporaneamente uno scarico Penrose intorno all'esofago intraabdominale.
- Ligate i vasi gastroeploici e corti lasciati con una combinazione di sutura e clip chirurgiche. Allora dividi.
- In caso di malignità, mobilitare la linfa celiaca che porta i tessuti dall'aspetto superiore del pancreas, che include la legatura e la divisione sia dell'arteria gastrica sinistra che della vena.
- Eliminare la curva gastrica minore di grasso e vasi sanguigni in genere da 3 a 5 cm distale alla giunzione gastroesofagea con endostapleri vascolari. In caso di malignità, pianificare le operazioni per ottenere tumore libero 3 a 5 cm distale stomaco e 5 a 7 cm margini chirurgici esinfali prossimali. Poiché le posizioni dei tumori vanno dal mid-esofago alla cardia gastrica, ottenendo adeguati margini di stomaco distale e disinfascopici prossimali si traducono in condotti di lunghezza variabile e associati anatomosi esofagogamitri inferiori o superiori. Il sito specifico della compensazione della curva minore è quindi in qualche modo variabile e dipendente dalla posizione esatta del tumore.
- Tagliare il fondo gastrico superiore e il cardia dal resto dello stomaco in genere utilizzando ovunque da 3 a 5 60 mm cucitrici endoscopiche a partire dalla maggiore curva gastrica nell'area cancellata sulla curva gastrica minore.
- Creazione di condotti gastrici
- Debulk meno grasso omentale intorno ai vasi gastrici giusti, che permette il condotto di essere raddrizzato e allungato. La divisione dei recipienti gastrici giusti che si inseriscono sulla curva minore all'incisura fornirà un ulteriore allungamento.
- Fissare lo stomaco a tre punti e fornire la retrazione verso l'esterno (Figura 1).
- Creare un condotto di diametro uniforme stretto (media 7-8 cm) con un fuoco iniziale della pinzatrice da 100 mm, che fornisce due file di graffette da 4,8 mm che puntano appena sotto la precedente linea di pinzatura. Il completamento della costruzione del condotto richiede solitamente 2 o 3 incendi aggiuntivi del tri-stapler endoscopico da 60 mm nell'area sgombrata sulla curva gastrica minore. In caso di malignità, inviare il difetto dello stomaco come "margine di stomaco distale" per l'analisi patologica della sezione congelata.
- Ispezionare la punta del condotto. Entro 3-5 min, il sanguinamento rosso brillante da puntualità è di solito visto attraverso la linea di fiocco curva minore che rappresenta una buona perfusione del condotto. Se non è presente una foratura rosso brillante, tagliare leggermente la punta del condotto con un altro cucitore 100 mm fino a quando non si vede il sanguinamento forato. I tri-pinzatori non sono utilizzati per il taglio dei condotti in quanto il taglio e il riposo della punta del condotto durante l'anastomosi intratoracica possono essere difficili.
- Eseguire una pyloroplasta Standard Heineke-Mikulicz al fine di assicurare un buon svuotamento del condotto.
- Inizialmente stimare quanto in alto nel petto il condotto raggiungerà allungando comodamente il condotto verso il collo senza tensioni indebite.
- Aprire la pleura destra attraverso i crus diaframmatici. Posizionare la punta del condotto nel petto destro mantenendo la linea di fiocco della curva minore rivolta verso destra.
- Chiudere temporaneamente l'addome con alcune suture facciali interrotte e graffette della pelle.
3. Fase toracica
- Posizionare il paziente nella posizione decubito laterale sinistra.
- Eseguire un muscolo serratus risparmiando toracotomia destra attraverso il 5esimo spazio intercostale. Dividere il muscolo intercostale sotto l'incisione entro 3-5 cm del corpo vertebrale posteriormente e lo sterno anteriormente, consentendo un movimento aggiuntivo delle costole 5th e 6th con il minimo rischio di frattura o lividi.
- Accisa l'arco della vena azygos e divide il legamento polmonare inferiore. In caso di malignità, eseguire en block dissezione mobilitando i due terzi distale dell'esofago intratoracico con tutti i tessuti molli circostanti dal pericardio anteriormente ai vasi sanguigni aorta posteriormente esofageal. Occlude linfatici con clip chirurgiche prima della divisione durante questa dissezione.
- Consegnare il condotto nel torace destro fino a quando non vi è ridondanza, limitando la tensione sui pedicoli vascolari gastroeploici giusti e gastroeploici per determinare l'estensione superiore della dissezione esofagea necessaria.
- A livello della carina tracheale, sezionare la parete esofagea dai tessuti molli mediastici circostanti superiore ad un livello in cui la punta del condotto raggiunge senza tensione, che di solito è da 3 a 5 cm superiore alla carina. Ancora una volta, date diverse posizioni di tumori e la lunghezza dei condotti dello stomaco creati durante la fase addominale, stabilire anastomosi più in basso vicino alla carina per tumori di cardia gastrica e più alto presso l'inserizia toracica per i tumori che coinvolgono l'esofago intratoracico medio.
- Creazione dell'anastomosi esofagogaste
- Allineare l'aspetto laterale medio-sinistro del terzo superiore dell'esofago intratocico sulla linea di pinzatura della curva minore.
- Posizionare quattro suture di virata distanti da 2 a 3 cm per mantenere l'allineamento (Figura 2).
- Transettale l'esofago 1 cm distale al set inferiore di suture di virata. In caso di malignità, inviare un anello di esofago a questo livello come "margine esofageo prossimale" per l'esame patologico della sezione congelata prima di procedere.
- Creare un'apertura corrispondente da 1 a 2 cm nel condotto attraverso la linea di pinzatura curva minore.
- Posizionare suture interrotte all'interno del lume comune, incorporando il condotto adiacente e le pareti esofagee che iniziano nel mezzo attraverso la linea di pinzatura curva minore e procedendo su entrambi i lati(Figura 3).
- Posizionare l'incudine stretta di una cucitrice endoscopica da 45 mm con un'altezza di base di 4,1 mm nel lume esofageo e l'incudine grande nel condotto. Per ottimizzare la lunghezza della comunicazione laterale tra l'esofago e il condotto, tagliare 5 mm dalla punta di plastica disal della cartuccia di cucitrice con una sega oscillante.
- Sparare la cucitrice, che taglia e ristaples la linea di pinzatura curva minore (Figura 4). La lunghezza dell'estremità tagliata dell'esofago è di solito un po 'più lunga del bordo del condotto gastrico, quindi rimuovi un'ellisse del condotto sulla linea di fiocco curva minore piuttosto che estendere l'affitto lateralmente, preservando l'afflusso di sangue collaterale (Figura 4 inset).
- Chiudere il lume comune aperto in due strati di suture che iniziano con uno strato interno di sutura di poliglactina 3-0 interrotta invertita seguita da un secondo strato di seta 3-0 interrotto utilizzando una tecnica Lembert (Figura 5).
- Segua l'aspetto superiore della linea di base del condotto della curva inferiore con suture di seta 3-0 interrotte in modo Lembert che si estendono in modo inferiore, fino a quando non si incontrano i vasi gastrici giusti.
- Chiedi all'anestesista di inserire un tubo nasogastrico nel condotto fino al livello dei crus per palpazione.
- Per le anastomosi create vicino all'insediazione toracica, utilizzare un lembo pleero per sigillare gli anastomosi nel mediastino posteriore. Per le anastomosi nell'aspetto centrale del mediastinum posteriore, mobilitare una pacca di grasso pericardiodale da mediastinum anteriore e vagamente avvolto per coprire anastomosi esofagogastrica (Figura 6 e Figura 7).
- Inserire e posizionare due tubi pettorali 28-francese all'interno dell'emitorace destro, uno anteriore e l'altro posteriore, accanto, ma non confinante con il condotto. Chiudere l'incisione della toracotomia.
4. Re-laparotomy: fase "doppio capovolgimento"
- Riportare il paziente in posizione supina e riaprire l'incisione della laparotomia mediana.
- Ispezionare il grasso gastroepiploico destro e spingere con attenzione qualsiasi grasso in eccesso verso l'alto attraverso il diaframma destro crus nel petto.
- Fissare il grasso gastroepiploico giusto e condotto ai cru sofragmatici con interruzione 2-0 suture di seta (Figura 8). Posizionare un tubo di ejejunostomia di alimentazione in pazienti selezionati, principalmente in pazienti anziani o pazienti con deficit nutrizionali preoperatori.
- Chiudere formalmente l'incisione della laparotomia mediana.
- Mantenere i pazienti intubati la sera dell'intervento chirurgico con estubazione pianificata la mattina seguente.
- Fornire il controllo del dolore con cateteri epidurali posizionati appena prima dell'induzione anestetica per i primi 3 o 4 giorni, che viene completato da narcotici per via endovenosa.
- Ottenere contrasto superiore serie gastrointestinale 5 a 7 giorni postoperatorio per valutare l'integrità anastomotica.
- Se non viene identificata alcuna perdita anatomotica, rimuovere il tubo nasogastrico.
- Istruire i pazienti ad avanzare a una dieta regolare in 2 O 3 settimane dopo la dimissione come tollerato.
Risultati
Dal 2009 al 2017 sono stati identificati in totale 368 pazienti sottoposti a un anastogastico esofagogastico esofagogastico STS e di questi 12 (3,8%) avuto fughe di perdite anatomotiche. Cinque di questi pazienti hanno dimostrato perdite di grado I/II e non hanno richiesto alcun intervento. Sei pazienti e un paziente hanno sperimentato rispettivamente perdite di grado III e di grado IV che richiedono stenting e/o intervento chirurgico endoscopico2. Un tasso di perdita del 25% (2/8) è stato osservato dopo l'esofagectomia per l'achalasia allo stadio finale rispetto a un tasso di perdita del 2,8% (10/336) in cui l'esofagectomia è stata eseguita per altre condizioni. Erano 4 (1,1%) paziente che è morto postoperatorio, nessuno dei quali ha avuto una complicazione antomotica. Di pazienti affetti da STS, 18 (5,0%) ha richiesto una mediana di 2 dilatazioni per sintomatiche stenosi di stenosi di stenosi. L'alimentazione egiunostomia supplementare è stata richiesta solo nell'11,1% di questi pazienti dopo la dimissione ospedaliera. Al contrario, dei 112 pazienti identificati che hanno subito anastomosi meccanica end-to-end (EEA) toracscopica (EEA) anastomosis nello stesso intervallo di tempo, 16,1% e 14,3% hanno dimostrato perdite anastomotiche e stenologie sintomatiche (p<0,01) nonostante tutto (100%) di questi pazienti mantenuti con una dieta limitata con poppate supplementari con tubi di jejunostomia per almeno un mese dopo l'intervento chirurgico (Tabella 1). Le differenze demografiche e di comorbilità dei gruppi STS e EEA erano statisticamente simili; tuttavia, c'è stata una tendenza verso una maggiore malattia cardiaca nella coorte STS(tabella 2). L'analisi del tempo degli studi di contrasto postoperatorio nei primi 208 pazienti che hanno subito un'anastomosi STS ha in genere dimostrato un condotto di diametro dritto/uniforme con essenzialmente completo (>95%) contrasto svuotamento nell'intestino piccolo entro 3 min nel 184 (88,4%) Pazienti. Il restante 11,6% dei pazienti studiati era quasi completo (>95%) contrasto svuotamento nel piccolo intestino entro 5 minuti. Nessun paziente studiato aveva un tempo di transito di contrasto superiore a 5 minuti.

Figura 1: Creazione del condotto dello stomaco. Lo stomaco è fissato in tre punti, che vengono retratti verso l'esterno. Viene creato un condotto di diametro relativamente uniforme con cucitrici che puntano appena inferiore alla linea di pinzatura precedente sulla curva minore. (Preso da con permesso11.) Fare clic qui per visualizzare una versione più grande di questa figura.
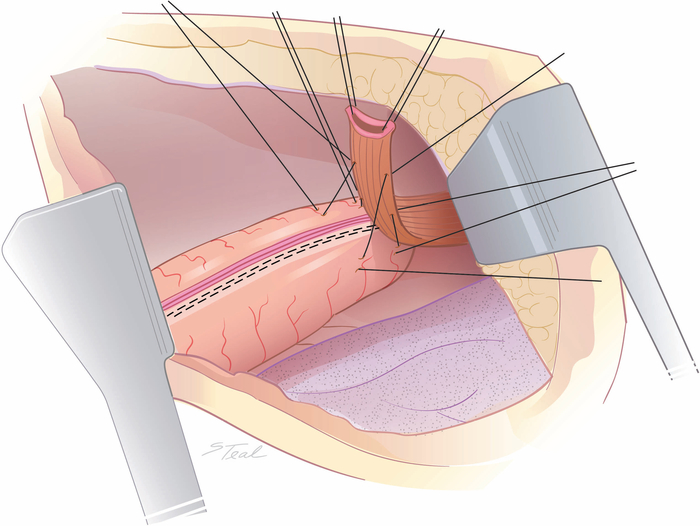
Figura 2: Allineamento dell'esofago sul condotto dello stomaco. L'aspetto laterale medio-sinistro del terzo superiore dell'esofago intratocico è allineato sulla linea di base della curva minore sulla punta del condotto con 4 suture di virata iniziali distanti circa 2-3 cm di distanza. (Preso da con permesso11.) Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 3: Preparazione per una comunicazione laterale tra l'esofago e il condotto dello stomaco. Un affitto da 1 a 2 cm è fatto nel condotto dello stomaco attraverso la linea di fiocco curva minore. Le suture di taccatura sono posizionate tra il condotto adiacente e le pareti esofagee che iniziano nel mezzo attraverso la linea di fiocco della curva minore, quindi due suture su entrambi i lati. (Preso da con permesso11.) Fare clic qui per visualizzare una versione più grande di questa figura.
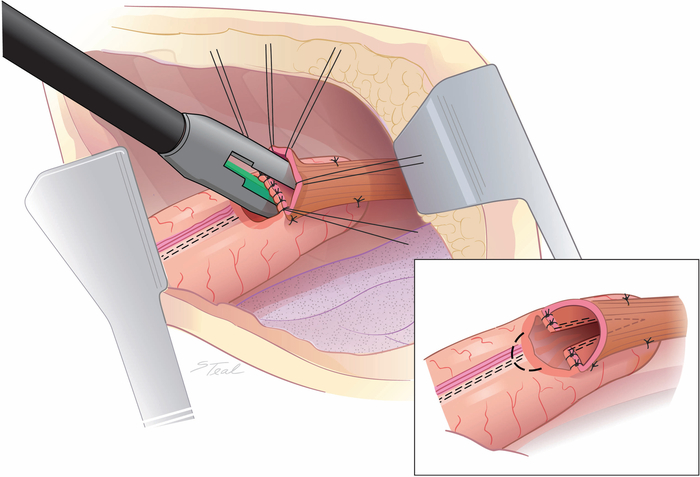
Figura 4: Creazione di una comunicazione laterale tra l'esofago e il condotto dello stomaco. Una cucitrice endoscopica da 45 mm viene sparata tagliando e riposando la linea di pinzatura della curva minore. In genere vengono utilizzati solo 2/3 della lunghezza della pinzatrice. Un'ellisse di condotto viene rimossa sopra la linea di pinzatura curva minore (linea punteggiata) piuttosto che estendere l'affitto lateralmente per eguagliare la lunghezza dell'estremità tagliata dell'esofago e della gastrotomia. (insetto) (Preso da con permesso11.) Fare clic qui per visualizzare una versione più grande di questa figura.

Figura 5: Chiusura del lume comune aperto. Il lume comune aperto è chiuso a mano in due strati di suture che iniziano con suture assorbenti interrotte invertite. Il primo strato di sutura è assorbito da un secondo strato di suture di seta Lembert che posizionano la sutura dello stomaco di qualche mm inferiore al primo strato di suture. (insetto) (Preso da con permesso11.) Fare clic qui per visualizzare una versione più grande di questa figura.
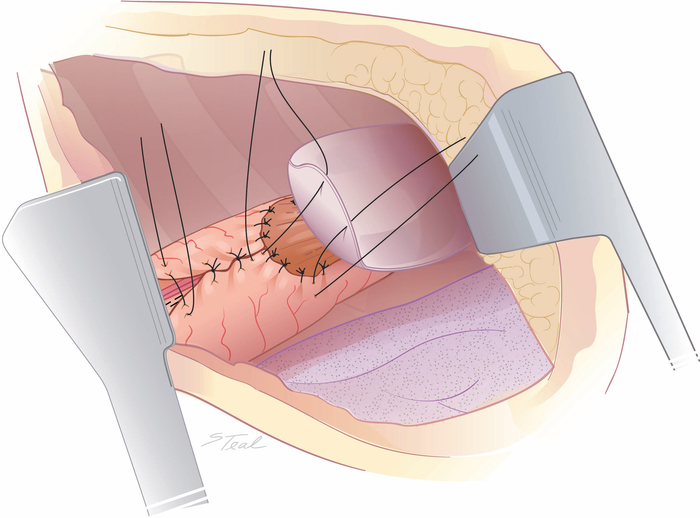
Figura 6: Sovrazzare la linea di pinzatura della curva minore e il contrafforte plerica dell'anastomosi. L'aspetto superiore della linea di pinzatura del condotto di curva inferiore può essere sovracucita a questo punto con suture di seta interrotte in modo inferiore fino a quando non si incontrano i vasi gastrici giusti. Per le anastomosi stabilite nei pressi dell'inserie toracico, un lembo di pleura mobilitato viene attaccato al condotto dello stomaco per contenere piccole perdite anastomotiche. (Preso da con permesso11.) Fare clic qui per visualizzare una versione più grande di questa figura.
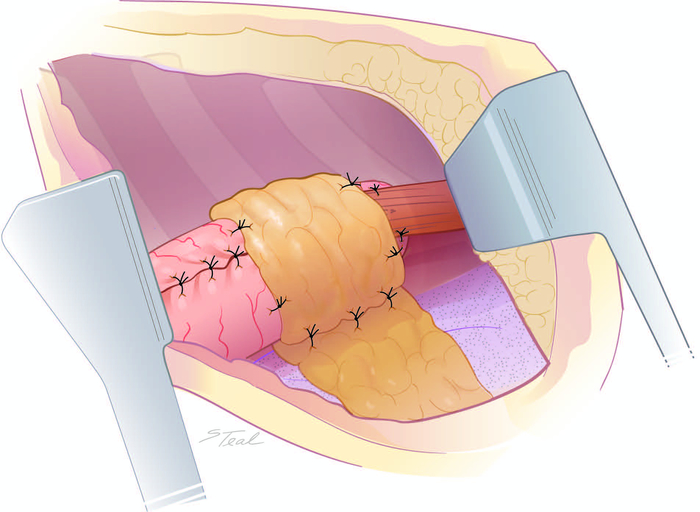
Figura 7: contrafforte vascolarizzato dei tessuti molli dell'anastomosi. Il grasso pericardioè è vagamente avvolto intorno ad anastomosi create nell'aspetto centrale del mediastino posteriore per contenere piccole aree di dehiscenza anatomotica. Fare clic qui per visualizzare una versione più grande di questa figura.
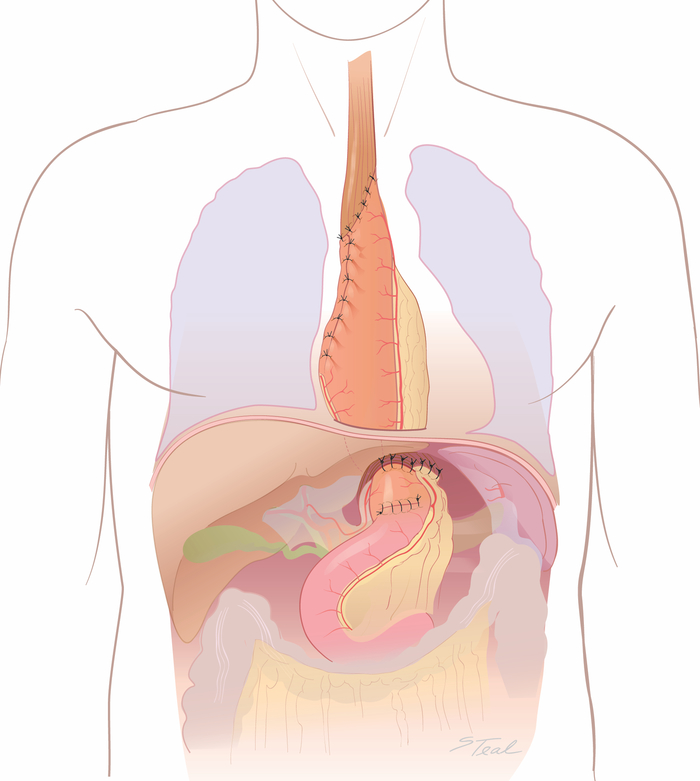
Figura 8: Fase di laparotomia finale ("doppio capovolgimento"). L'incisione della laparotomia viene riaperta. Il grasso gastroepiploico giusto e condotto con cura virata ai crus con suture di seta 2-0. (Preso da con permesso11.) Fare clic qui per visualizzare una versione più grande di questa figura.
| StS (N. 368) | EEA (N. 112) | |
| Perdite anastomiche | 3.8%* | 16.1% |
| Rigorosa anastomotica | 5.2%* | 14.3% |
| Post Op J-Tube Utilizzo | 11.0%* | 100.0% |
Tabella 1. Perdite anastomiotiche/restrizioni e uso di jejunostomia di alimentazione postoperatoria (Post Op J-Tube Usage) a seguito di dimissione ospedaliera confrontando i pazienti sottoposti a STS aperto e anasofagogastri dell'EEA toracica utilizzando un approccio Ivor Lewis eseguito presso l'Indiana University Simon Cancer Center dal 2009 al 2017. (valore p < 0,01, chi-quadrato)
| Servizio token di sicurezza (n.278) | E-AEA (n. 82) | Valore P | |
| Età alla diagnosi (anni) | 60,3 x 11,4 (23-84) | 60,6 x 9,0 (38-80) | 0.80 |
| Genere | |||
| Uomo | 228 (82.0%) | 69 (84.1%) | 0.66 |
| Donna | 50 (18.0%) | 13 (15.9%) | |
| Cormorbidità | |||
| Cardiaca | 114 (41.0%) | 24 (29.3%) | 0.06 |
| Diabete Mellito | 70 (25.2%) | 19 (23.2%) | 0.71 |
| Bpco | 32 (11.5%) | 12 (14.6% | 0.45 |
| Istologia | |||
| Adenocarcinoma | 237 (85.3%) | 74 (90.2%) | 0.25 |
| Altre diagnosi | 41 (14.7%) | 8 (9.8%) | |
| Terapia Neoadjuvant | 200 (71.9%) | 59 (71.9%) | 0.99 |
Tabella 2: Confronto demografico e comorbilità aperto STS e anastomosi toracoscopici EA utilizzando un approccio Ivor Lewis eseguito presso l'Indiana University Simon Cancer Center dal 2009 al 2015. Deviazione media e standard con intervallo assegnato per le variabili continue. Valori P per le variabili continue generate dal test t di Student e il chi quadrato per le variabili discrete.
Discussione
L'esofagectomia rappresenta una procedura chirurgica molto estesa. La qualità avversa della vita a lungo termine è stata collegata a pazienti che hanno avuto complicazioni postoperatorie tra cui perdite anastomiche3. I fattori di rischio per una perdita antomotica includono principalmente la creazione di un anastomosi con scarso apporto di sangue. Una perdita anastomotica non solo rappresenta una fonte significativa di morbilità postoperatoria, ma può anche comunemente provocare severità. Una stenosi può anche essere il risultato di problemi tecnici tra cui l'esecuzione di un anastomosi di piccolo diametro. Oltre a influire sulla qualità della vita, le restrizioni si aggiungono ai costi medici complessivi quando è necessaria la dilatazione5. Eseguire accuratamente diversi passaggi è della massima importanza per ridurre al minimo le complicazioni, nonché raggiungere buoni risultati funzionali oncologici e del tratto gastrointestinale superiore.
L'anastomosis esofagogastrica può essere realizzata con diversi metodi, tra cui cucito a mano, EEA e tecniche di cucitrice lineare che rappresentano la maggior parte. Un rapporto della Società di Chirurghi Toracici General Thoracic Database ha citato un tasso complessivo di perdita del 9,3% in pazienti sottoposti ad anastomosi esofagogiche intratociche6. Mentre la mortalità postoperatoria a causa di perdite anastomotiche sembra diminuire, i tassi di stenosi successivi rimangono elevati, che vanno tra il 10 e il 56%7. Collard e Orringer hanno descritto una tecnica di cucitrice lineare per creare un esofagogaste cervicale laterale8,9. L'apertura triangolata posteriore formata dalla cucitrice lineare è stata dimostrata per provocare un basso tasso di perdita e resistenza alla stesia. Uno studio retrospettivo della Mayo Clinic ha riportato un incidente del 5,6% di perdita anastomiotica intratocistica in 177 pazienti in cui è stata utilizzata una tecnica di pinzatura lineare rispetto a un tasso di perdita dell'8,3% in 48 pazienti sottoposti a un'anastomosis graffetta e del EEA. Sebbene questa differenza non abbia raggiunto la differenza statistica, la probabilità di un anno per la stenosi era del 32% dopo l'anastomosi del CEE rispetto a solo l'8,6% con tecniche lineari pinzate, che era significativa5. Wang e colleghi hanno effettuato uno studio clinico prospettico che ha coinvolto 155 pazienti che sono stati randomizzati in uno dei tre metodi anastomotici esofagogici10. Impressionante, nessuna stenosura postoperatoria sviluppata in pazienti sottoposti a una tecnica di cucitrice lineare rispetto al 9,6% e 19,1% nei casi cuciti a mano e pinzati circolari, che era statisticamente significativa. Studi precedenti che hanno coinvolto anastomosi di cucitore lineare hanno utilizzato la parete anteriore del condotto dello stomaco per il sito anastomotico. Questo approccio può portare a una striscia ischemica di condotto tra la linea di fiocco della curva minore e l'anastomosi predisponendo alla fuoriuscita. Nuovo alla nostra tecnica, l'afflusso di sangue collaterale alla punta del condotto dello stomaco viene preservato tagliando e riposando la linea di fiocco della curva minore.
Ci sono limitazioni allo studio. In primo luogo, si tratta di un'analisi retrospettiva. Nonostante la natura retrospettiva, tuttavia, abbiamo utilizzato questo approccio STS uniformemente in tutti i pazienti sottoposti a chirurgia per la patologia media-esofagea allo stomaco prossima durante l'intervallo di studio come un "intento di trattare" compresi i pazienti stabili che hanno sostenuto perforazioni esofagei durante la dilatazione per la stesura in cui la riparazione non era possibile. Comune a qualsiasi tecnica anastomotica intratoracica laterale è la necessità di sezionare un ulteriore 3 a 4 cm di esofago prossimale, potenzialmente diminuendo la lunghezza del margine esofageo chirurgico nei casi di malignità e anche potenzialmente con conseguente certo grado di devascolizzazione esofagea. Per evitare la depurazione, un punto critico non è quello di sezionare l'esofago intratocico più in modo superiore verso il collo di quanto la punta del condotto dello stomaco raggiungerà senza tensione. Ipotizziamo che il più alto tasso di perdita osservato utilizzando questa tecnica per i pazienti con achalasia allo stadio finale può essere correlato a un'ulteriore devascolizzazione di una parete esofagea addensante dopo la mobilitazione per eseguire un anastomosi STS dove l'afflusso di sangue preesistente può essere scarso. La dilatazione esofagea frequentemente osservata nei casi di achelasia rende molto difficile cucire a mano il lume comune aperto, che può anche essere un fattore. Sulla base di questa esperienza, ora crediamo che l'achalasia sia una controindicazione per eseguire anastomosi intraritmici STS. Da notare, per i tumori lunghi o più centrali in cui un'anastomosi esofagogica deve essere creata vicino all'ingresso toracico per ottenere un adeguato margine esofageo prossimale, abbiamo utilizzato una comunicazione iniziale un po 'più breve da quella a lato che non utilizza l'intera lunghezza del GIA da 45 mm, che tuttavia ha il potenziale per essere più incline alla formazione restrittiva.
A differenza dell'esofago, lo stomaco è un condotto passivo, dipendente dalla gravità per il drenaggio. Diverse variabili tra cui il diametro del condotto e la lunghezza, nonché l'orientamento del condotto possono, quindi, avere un impatto significativo sulla funzione del tratto gastrointestinale superiore. Il cibo ingerito ha il potenziale per riagganciare in tre posizioni: l'anastomosi esofagogica, il corpo dello stomaco e lo sbocco gastrico. Scarsa funzione condotto può essere il risultato di problemi tecnici in uno qualsiasi di questi tre settori. Scarso svuotamento del condotto paradossalmente può causare più "reflusso", non solo influenzando negativamente la qualità della vita, ma anche occasionalmente con conseguente aspirazione. Gli approcci "minimo invasivo" (laparoscopico/toracoscopico), che utilizzano una cucitrice dell'AEA per anastomosi esofagogastri, anche se rappresentano ancora la minoranza di casi di esofagectomia eseguiti, sono diventati sempre più popolari. Riteniamo tuttavia che la nostra tecnica aperta come descritta non solo consenta la creazione di un'anastomossi STS precisa per ridurre i tassi di stenosi, ma ottimizza inoltre la costruzione e l'orientamento dei condotti con un condotto destro dello stomaco non ridondante, tra cui la pyloroplastica con una tendenza minima per i materiali alimentari ingeriti a riagganciare in queste aree rispetto agli approcci thcooraci. I tempi di transito misurati dalla bocca all'intestino piccolo su studi postoperatori di routine supporterebbero l'eccellente funzione del condotto con la nostra tecnica, tuttavia sono necessari studi comparativi utilizzando altre tecniche. Le nostre osservazioni sosterrebbero sintomi minimi e autolimitanti di "dumping" nella stragrande maggioranza dei pazienti affetti da STS, tuttavia sono attualmente in corso specifiche valutazioni della qualità della vita. Infine, con l'approccio della toracotomia descritto, abbiamo osservato poche differenze rispetto al disagio postoperatorio acuto e a lungo termine rispetto ai pazienti sottoposti a un approccio toracoscopico presso la nostra istituzione.
Riassumendo, crediamo che questa nuova tecnica STS possa ridurre significativamente la morbilità e la mortalità occasionale delle complicazioni anastomotiche esofagogiche a seguito dell'esofagectomia. Condutto costruzione e orientamento come descritto inoltre ottimizza la funzione del tratto gastrointestinale superiore. Infine, questa tecnica è facilmente adattabile e riproducibile.
Divulgazioni
Gli autori non hanno divulgazioni.
Riconoscimenti
Nessuno.
Materiali
| Name | Company | Catalog Number | Comments |
| 100 mm Linear Stapler (ILA Autosuture, “green” cartridge, 4.8 mm staple height) | Covidien | 3973 | Surgical Stapler |
| 3-0 silk (Perma hand black, 8x18", SH needle, 1/2 circle 26 mm, C013) | Ethicon | C013D | Suture Material |
| 3-0 silk (Perma hand black, 8x30", SH needle, 1/2 circle 26 mm, C017) | Ethicon | C017D | Suture Material |
| 3-0 vicryl (Coated vicryl violet, 8x18", SH needle, 1/2 circle 26 mm, J774) | Ethicon | VCP774D | Suture Material |
| 3-0 vicryl (Coated vicryl violet, 8x27", SH needle, 1/2 circle 26 mm, J784) | Ethicon | VCP784D | Suture Material |
| 45 mm Endoscopic Stapler (Flex “green” cartridge, 4.1 mm staple height) | Ethicon | SC45A | Surgical Stapler |
| 60 mm Endoscopic Tristapler | Ethicon | SC60A | Surgical Stapler |
| Flex “green” cartridge, 4.1 mm staple height | Ethicon | GST45G | Surgical Stapler |
| Flex 60, “black” cartridge (for 60 mm Endoscopic Tristapler) | Ethicon | GST60T | Surgical Stapler |
| Foceps Debakey 7.75 inch | Jarit | 320-101 | Surgical Instrument |
| Forceps Debakey 12 inch | Jarit | 320-103 | Surgical Instrument |
| Forceps Debakey 9.5 inch | Jarit | 320-102 | Surgical Instrument |
| Needle Holder Mayo-Hegar 10 inch | Codman | 36-2019 | Surgical Instrument |
| Needle Holder Mayo-Hegar 7 inch | Codman | 36-2017 | Surgical Instrument |
| Needle Holder Mayo-Hegar 8 inch | Codman | 36-2018 | Surgical Instrument |
| Needle Holder Ryder 10 inch | Codman | 36-3005 | Surgical Instrument |
| Needle Holder Ryder 9 inch | Jarit | 121-164 | Surgical Instrument |
Riferimenti
- Cassivi, S. D. Leaks, strictures, and necrosis: a review of anastomotic complications following esophagectomy. Seminars in Thoracic and Cardiovascular Surgery. 16, 124-132 (2004).
- Low, D. E., et al. International consensus on standardization of data collection for complications associated with esophagectomy: Esophagectomy complication consensus group (ECCG). Annals of Surgery. 262, 286-294 (2015).
- Derogar, M., Orsini, N., Sadr-Azodi, O., Langergren, P. Influence of major postoperative complications on health-related quality of life among long-term survivors of esophageal cancer surgery. Journal of Clinical Oncology. 30, 1615-1619 (2012).
- Kofoed, S. C., et al. Intrathoracic anastomotic leakage after gastroesophageal cancer resection is associated with increased risk of recurrence. Journal of Thoracic and Cardiovascular Surgery. 150, 42-48 (2015).
- Price, T. N., et al. A comprehensive review of anastomotic technique in 432 Esophagectomies. Annals of Thoracic Surgery. 95, 1154-1160 (2013).
- Kassis, E. S., et al. Predictors of anastomotic leak after esophagectomy: an analysis of the Society of Thoracic Surgeons General Thoracic Database. Annals of Thoracic Surgery. 96, 1919-1926 (2013).
- Yuan, Y., Wang, K. N., Chen, L. Q. Esophageal anastomosis. Diseases of the Esophagus. 28, 127-137 (2015).
- Collard, J. M., Romagnoli, R., Goncette, L., Otte, J. B., Kestens, P. J. Terminalized semimechanical side-to-side suture technique for cervical esophagogastrostomy. Annals of Thoracic Surgery. 65, 814-817 (1998).
- Orringer, M. B., Marshall, B., Iannectoni, M. D. Eliminated the cervical esophagogastric anastomotic leak with a side-to-side stapled anastomosis. Journal of Thoracic and Cardiovascular Surgery. 119, 277-288 (2000).
- Wang, W. P., Gao, Q., Wang, K. N., Shi, H., Chen, L. Q. A prospective randomized controlled trial of semi-mechanical versus hand-sewn or circular stapled esophagogastrostomy for prevention of anastomotic stricture. World Journal of Surgery. 37, 1043-1050 (2013).
- Kesler, K. A. Outcomes of a novel intrathoracic esophagogastric anastomotic technique. The Journal of Thoracic and Cardiovascular Surgery. 156 (4), 1739-1745 (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon