Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Hücre Kültüründe ve Civciv Embriyosunda Akson Kılavuz Reseptörlerinin Dinamiklerini Değerlendirmek için pHluorin Kullanımı
* Bu yazarlar eşit katkıda bulunmuştur
Bu Makalede
Özet
Hücre yüzeyindeki akson kılavuz reseptörlerinin mekansal-zamansal dinamiklerini incelemek için pH'a duyarlı yeşil floresan protein varyantı pHluorin'in kullanımını burada açıklıyoruz. pHluorin etiketli reseptör hem hücre kültüründe hem de in vivoolarak ifade edilir Civciv embriyosunun elektroporasyonunu kullanarak.
Özet
Geliştirme sırasında, akson kılavuz reseptörleri, aksonların hem çekici hem de itici ipuçlarına duyarlılığını düzenlemede çok önemli bir rol oynar. Gerçekten de, kılavuz reseptörlerinin aktivasyonu, akson uçlarının, büyüme konilerinin ligandlara yanıt vermesine izin veren sinyal mekanizmalarının ilk adımıdır. Bu nedenle, hücre yüzeyindeki kullanılabilirliklerinin modülasyonu, büyüme konisi duyarlılığının ayarlanmasına katılan mekanizmalardan biridir. Burada, gelişmekte olan civciv omurilikte hem in vitro hem de in vivo bir akson kılavuz reseptörün mekansal-zamansal hücre yüzey dinamiklerini tam olarak görselleştirmek için bir yöntem açıklıyoruz. Plazma zarına hitap eden akson kılavuz reseptörünün fraksiyonunu özellikle tespit etmek için yeşil floresan protein (GFP) varyantının pH'a bağımlı floresan özelliğinden yararlandık. İlk olarak bu tür pH'a bağımlı yapıların in vitro doğrulamasını açıklıyoruz ve akson kılavuz reseptörün mekansal-zamansal dinamiklerini değerlendirmek için in vivo, civciv omurilik akorunda kullanımlarını daha ayrıntılı olarak açıklıyoruz.
Giriş
Navigasyonları sırasında, aksonlar onları hedeflerine yönlendiren birden fazla çevresel ipucu entegre eder. Bu ipuçları, axon terminallerinin yüzeyindeki kılavuz reseptörlerini, büyüme konilerini aktive eder ve bu da uygun bir sinyal yolu başlatır. Bu nedenle, reseptörlerin hücre yüzey dağılımının zamansal ve mekansal regülasyonu, büyüme konisinin hassasiyetini ayarlamak için kritik öneme sahiptir1. Bu bağlamda, kommissural aksonlar tarafından orta çizgi geçişi, reseptör hücre yüzey seviyelerinin düzenlenmesini araştırmak için mükemmel bir modeldir. Gelişen omurilikte, kommissural aksonlar başlangıçta orta çizgiyi geçtikleri ventral zemin plakasına doğru çekilir. Geçtikten sonra, zemin plakası çekicilerine yanıtlarını kaybederler ve zemin plakası kovuculara yanıt kazanırlar, böylece zemin plakasından çıkabilirler ve sinir sisteminin karşıt tarafında son hedeflerine doğru gidebilirler2,3. Büyüme konisi yüzeyinde reseptör kullanılabilirliğinin düzenlenmesi, yanıt vermenin orta hat ipuçlarına geçişinin altında kalan mekanizmalardan biridir4,5. Bu nedenle, büyüme konilerinin plazma zarında bulunan reseptörlerin seçici izlenmesi birincil öneme sahiptir. Burada, gelişmekte olan civciv omuriliğinde plazma zarı in vitro ve in vivoyahitap eden akson kılavuz reseptörlerini özellikle görselleştirmek için yeşil bir floresan protein (GFP) varyantının pH'a bağımlı floresan özelliğine dayanan bir yöntemi açıklıyoruz.
Rothman ve meslektaşları, ekliptik pHluorin 6 da dahil olmak üzere GFP'nin nokta mutasyonları pH'a duyarlı varyantları tarafındantasarlanmıştır. Ekliptik pHluorin, asidik pH'a (<6) maruz kaldığında, nötr pH'da floresan iken, nonfluorescent olma özelliğine sahiptir. Bu, hücre içi asidik bölmelerde lokalize olan nonfluoresan reseptörlerin(yani endozomlar, kaçakçılık veziklinleri) plazma membranına dahil edilen floresan reseptörlerden ayırt etmesine ve böylece hücre dışı nötr pH7'yemaruz kalmalarına izin verir. Orta hat kovucu semaforin 3B5'e (Şekil 1A)büyüme konisi tepkisine aracılık eden bir akson kılavuz reseptörü olan pleksinA1'in plazma membran lokalizasyonunu izlemek için bundan yararlandık. Burada, gelişmekte olan civciv omuriliğinde bu yapının8-10 no'luk ovo elektroporasyonunun yanı sıra bir pHluorin-pleksinA1 yapının in vitro karakterizasyonunu ve ardından hem mekansal hem de zamansal çözünürlüklerle akson kılavuz reseptör dinamiklerini in vivo olarak takip etmeyi sağlayan kriyoseksiyonların mikroskobik analizini açıklıyoruz.
Access restricted. Please log in or start a trial to view this content.
Protokol
1. PleksinA1 Reseptörü pHluorin ile Etiketlemek için Klonlama Stratejisi
- Omurga olarak uygun bir ifade vektörü seçin(örneğin, fare reseptör pleksistiA1 ifade vektörü, Dr. Andreas Puschel11'inbir tür hediyesi).
Not: Bu pleksinA1 vektörü, plazma membranında verimli HA veya VSV etiketli reseptör yerleştirmesi elde etmek için tasarlanmıştır. - PCR tarafından, şablon olarak yeterli plazmid kullanarak ekliptik pHluorin kodlama dizisini güçlendirin(örneğin pHluorin etiketli GABA A reseptörü, Dr. Jacob2'ninbir tür hediyesi). Gerekirse, omurgadaki klonlama adımını kolaylaştırmak için astarın 5' ucuna bir kısıtlama bölgesi ekleyin.
- pHluorin dizisini, kısıtlama sitelerini kullanarak sinyal peptidi ile reseptör kodlama sırası arasına çerçeveye ekleyin(örneğin, Şekil 1B'deaçıklandığı gibi NruI/Kpn2I kısıtlama siteleri).
Not: Reseptörlerin doğru hedeflanmasını sağlayan sinyal peptidi bölündüğünden, pHluorin bunun üzerine yerleştirilmelidir. Bu, sinyal peptidinin tanınmasını garanti eder ve pHluorin'in ilgi çekiciden bölünmesini önler. - PCR tarafından herhangi bir mutasyona uğramamasını sağlamak için elde edilen yapıları sıralayın.
2. COS7 Hücrelerinde pHluorin Etiketli Reseptör In vitro karakterizasyonu
Füzyon proteininin plazma zarı ilebilme yeteneği ve pH düşürüldükçe geri dönüşümlü floresan kaybı aşağıdaki prosedür kullanılarak doğrulanabilir.
- 1. Gün. Plaka 1.5 x 105 COS7 hücreleri cam tabanlı 35 mm'lik bir tabakta 2 ml tam Dulbecco Modifiye Kartal Orta (DMEM - % 10 Fetal Sığır Serumu - 1 mM sodyum piruvat - 25 U/ml penisilin/stretomisin - 2,5 μg/ml Amfoterisin B - pH 7,4).
- 2. Gün. Hücreleri transfect:
Not: Hücreler %70-80 bir arada olmalıdır.- 200 μl NaCl 150 mM hazırlayın ve 3 μg DNA ekleyin, yani vektör kodlama pHluorin etiketli reseptör. Yavaşça girdap ve kısa bir süre aşağı döndürün.
Not: Bu deneylerde kullanılan pHluorin-pleksinA1 vektörün haritası Şekil 1B'de gösterilmiştir. - 10 μl transfeksiyon reaktifi (veya kullanılan reaktifin uygun miktarını) ekleyin. Vortex hemen.
- RT'de 10 dakika kuluçkaya yaslanın.
- Hücrelere 200 μl transfeksiyon reaktifi/DNA karışımı ekleyin.
- Karışımın yeniden bölümlenmesini sağlamak için plakayı hafifçe hareket ettinin ve hücreleri 37 °C inkübatöre geri yerleştirin.
- 200 μl NaCl 150 mM hazırlayın ve 3 μg DNA ekleyin, yani vektör kodlama pHluorin etiketli reseptör. Yavaşça girdap ve kısa bir süre aşağı döndürün.
- 3. gün. Transfeksiyon ortamını çıkarın ve 2 ml taze komple DMEM ile değiştirin.
- 4. gün. COS7 pHluorin-pleksinA1 transfected hücrelerinin canlı hücre görüntülemesini gerçekleştirin:
- İki aliquots DMEM komple orta hazırlayın ve pH'ı sırasıyla 3,5 ve 9,5'e ayarlayın.
Not: Bir 35 mm plaka için, deneyi gerçekleştirmek için her çözeltinin 1,5 ml'si gereklidir. - Hücre ortamını çıkarın ve 1 ml DMEM komple orta pH 7.4 ile değiştirin.
- Mikroskop odasını açmadan çeşitli bileşenleri doğrudan hücre kültürü ortamına enjekte etmek için uygun bir boru tipine sahip 5 ml'lik bir şırınga hazırlayın.
- 37 °C, %5 CO2 nemli çalışma atmosferinin bakımına izin veren bir modül kullanın.
Not: CO2 odasının kullanımına alternatif bir yaklaşım HEPES tamponlu ortam kullanmaktır (genellikle hücre tipine göre 10-25 mM aralığında). - Hücreleri odaya yerleştirin ve boruyu ve şırınnayı ayarlayın.
Not: Kayıt sırasında mekanik sürüklenmeyi önlemeye başlamadan önce mikroskop dengelenmelidir. - Görüntüleme yazılımını açın ve çok boyutlu alım programını seçin.
- 40X hedefine sahip transfected COS7 hücrelerini bulun ve her biri için yazılımdaki konumunu işaretleyin.
- Z yığınını 15 μm derinlik alımına sahip olacak şekilde yapılandırın (plakaya ortam eklerken odak değişebilir).
- GFP filtresi ve Faz için pozlamayı ayarlayın.
- Edinme zamanlamasını yapılandırın.
Not: 5 ilgi alanı olan tüm deney için, 10 dakika boyunca her 20 saniyede bir alım yeterli olmalıdır. - Satın almaya başlayın ve DMEM pH 7.4 ortamında 5 kontrol görüntüsü alın.
- Satın almayı duraklatın, kültür ortamında 5,5 pH elde etmek için 1,25 ml pH 3,5 komple DMEM enjekte edin, yazılımda olayı işaretleyin ve 5 daha fazla zaman puanı için edinimi sürdürin.
Not: Yeşil floresan giderek kaybolmalıdır. - Satın almayı duraklatın, kültür ortamında bir pH 7.4 elde etmek için 1.2 ml pH 9.5 komple DMEM enjekte edin, yazılımda olayı işaretleyin ve 5 zaman puanı daha almaya devam edin.
Not: Yeşil floresan plazma zarında tekrar ortayalanmalıdır. - Görüntüleri analiz edin.
Şekil 2, pHluorin-pleksinA1 yapısı ile böyle bir protokolle elde edilen temsili görüntüleri göstermektedir.
- İki aliquots DMEM komple orta hazırlayın ve pH'ı sırasıyla 3,5 ve 9,5'e ayarlayın.
3. pHluorin-pleksinA1 Yapısı ovo Elektroporasyon içinde
- Elektroporasyondan önce yumurtaların işlenmesi:
- Döllenmiş yumurtaları kuluçkadan bir hafta öncesine kadar 14 °C'de bir buzdolabında saklayın.
- Embriyolar HH14 12 aşamasına ulaşana kadar 50-52 saat doymuş neme sahip bir inkübatörde 38,5 °C'de(101,3°F) yumurta kuluçkaya yatırın.
Not: Yumurtalar kuluçka sırasında yatay olarak yerleştirilmelidir, böylece embriyo elektroporasyon için uygun şekilde konumlandırılmalı ve sarısının üstünde yüzmelidir. HH14 evresi, omurilikteki farklılaşmış nöronlarda ve dorsal kök ganglionunda plazmidlerin uygun sağkalım oranı ile ekspresyonunun ifadesini elde etmek için uygundur.
- Elektroporat embriyoları8-10:
- Elektroporasyon hazırlayın:
- İstenilen konsantrasyon olarak seyreltebilmek için 2 μg/μl'den daha yüksek konsantrasyona sahip endotoksin içermeyen DNA plazmidleri hazırlayın.
- Farklı DNA çözeltilerini enjekte etmek için yeterli cam kılcal damarı çekin.
- Steril PBS (-Ca2+; -Mg2+) - 100 U/ml penisilin/streptomisinin hazırlayın ve 38,5 °C'de dengeyi sağla.
- Kaputu, kavisli makası ve ince asaları sterilize edin.
- Elektrot aralığını kontrol edin.
Not: Elektrotlar arasında genellikle 4 mm'lik bir boşluk kullanılır.
- Pencere yumurta13 (Şekil 3A):
- Yumurtanın kör tarafındaki kabuğu delmek için kavisli makas kullanın.
- 0,9 mm x 25 mm iğne ve 5 ml şırınga kullanarak 2 ml albümen çıkarın. Yumurta sarısı kesesine zarar vermemek için iğneyi dikey olarak yönlendirin.
- Kabuğun bütünlüğünü korumak için yumurtanın üstünü bantla örtün.
- Kavisli makas kullanarak, yumurtadan 2 ml albümen çıkarırken basıncı eşitlemek için bandın ortasındaki kabuğu delin. Daha sonra, embriyoyu görselleştirecek ve üzerinde çalışabilecek kadar büyük bir pencere kesin.
- Embriyonun susuz kalmamasını önlemek ve manipülatör için daha erişilebilir hale getirmek için~2ml steril sıcak PBS (-Ca 2+ ; -Mg2+) - 100 U/ml penisilin/streptomisilin ekleyin.
- DNA enjekte edin ve embriyoyu elektroporat edin
- PBS'de plazmid (-Ca2+; -Mg2+) 0,5-2 μg/μl arasında bir konsantrasyonda seyreltin ve son % 0,025 konsantrasyona ulaşmak için Hızlı yeşil boya ekleyin. DNA karışımını kılcal damara yükleyin. Bir enjektör kullanılması önerilir.
Not: Kılcal damar direncinin ne çok büyük (embriyo enjekte ederken zorluklar olabileceği anlamına gelir) ne de çok küçük (kılcal damarın çok büyük olabileceği ve embriyoya zarar verebileceği anlamına gelir) olduğunu kontrol edin. Ayrıca, 2 μg/μl'den yüksek nükleik asitlerin konsantrasyonu spesifik olmayan etkilere neden olabilir ve kontrol edilmesi gerekir. - Sarnıç kesesini ve kaudal taraftaki sinir tüpünü yüklü kılcal damarla delin. Sinir tüpünü sığ bir açıyla girin ve lümeni kuyruktan başa DNA karışımı ile doldurun (Şekil 3B).
Not: Hızlı yeşil, enjeksiyonun doğruluğunu kontrol etmeyi sağlar. - 4 mm platin elektrotları sinir tüpünün her iki tarafına elektroporat vermek istediğiniz seviyeye hızla yerleştirin ve 50 msec aralıklarla 50 msec için 31 V'ta 3 darbe uygulayın (Şekil 3C).
Not: Gelişmekte olan embriyoya zarar vermemek için elektrotları kalbe veya büyük ekstra embriyonik damarlara yerleştirmekten kaçının. Elektrotlarda kabarcıklar oluşmalıdır. - İğne ile kabuktaki seviyeyi azaltmak için 2 ml albümen çıkarın.
- Pencereyi ve künt tarafı bantla hermetik olarak kapatın.
- Yumurtaları istenen aşamaya gelene kadar inkübatöre 38,5 °C'de geri koyun.
- PBS'de plazmid (-Ca2+; -Mg2+) 0,5-2 μg/μl arasında bir konsantrasyonda seyreltin ve son % 0,025 konsantrasyona ulaşmak için Hızlı yeşil boya ekleyin. DNA karışımını kılcal damara yükleyin. Bir enjektör kullanılması önerilir.
- Elektroporasyon hazırlayın:
4. Embriyoların Gömülmesi ve Kriyoseksiyon
- Elektroporasyondan 48 saat sonra, elektroporlu embriyoları dikkatlice hasat edin (HH24 aşaması). Bandı ve koryovantoid zarın yarısını kesin. Embriyoların yumurta sarısına batmasını önlemek için embriyonun altına bir kevgir yerleştirin ve koryallantoid zarın ikinci yarısını kesin.
- Embriyoyu buz gibi PBS ile dolu bir diseksiyon kabına aktarın.
- Floresan stereo mikroskop ile nöral tüpte floresan arayarak elektroporasyon verimliliğini kontrol edin.
Not: RFP'yi kodlayan bir kontrol plazmidinin koelektroporasyonu elektroporlu alanın görselleştirilmesine yardımcı olabilir. - Omuriliğin elektropore bölgesini seçmek için embriyoları bir mikroskalpel kullanarak parçalara ayrıştırın.
- Parçalanmış embriyoları 24 kuyulu bir tabağa aktarın ve pH%7,4 4 Paraformaldehit (PFA) - Fosfat Tampon Salin (PBS), 4 °C'de O/N'de sabitlenin.
Not: Fiksasyon adımı, pHluorin'in "canlı" konformasyonunda stabilizasyonuna izin vermek ve böylece sabit /permeabilize dokuda pHluorin kullanabilmek için çok önemlidir. Fiksasyon, floresanların pH'a bağlı değişimini büyük ölçüde yavaşlatsa da, fiksasyondan sonra konformasyon/protonasyon değişikliklerinin hala gerçekleşebileceğini dikkate almak gerekir. Bu nedenle, aşağıdaki protokol (gömme, kriyoseksiyon ve gözlem) sabitleme adımından sonraki 3 gün içinde, tüm tamponlar pH 7'de olacak şekilde yapılmalıdır. Fiksasyon gerekli değilse, canlı doku bölümlerinde gözlem yapılması önerilir. - %4 PFA'yı çıkarın ve embriyoları pH 7.4 PBS'de yıkayın.
- PBS-% 15 sakkarozda embriyoları kuluçkaya yatırın ve embriyolar batana kadar 4 °C'de tutun.
- Sabit embriyoları pH 7.4%7.5 jelatin- %15 sakkarozda 37 °C'de 45 dakika kuluçkaya yatırarak embriyolar tamamen gömülür.
- Yerleştirme kalıplarını buza yerleştirin ve sağlam bir 2 mm taban elde etmek için 400 μl pH 7.4% 7.5 jelatin -% 15 sakkaroz ekleyin.
- Gömülü embriyoyu kesik uçla aspire edin ve embriyoyu katı jelatin tabanına yerleştirin.
- pH 7.4% 7.5 jelatin - % 15 sakkaroz ile örtün ve jelatin katılaştırılmadan önce embriyoyups ile konumlandırın.
- Jelatin katılaştıktan sonra, -40 °C izopropanol banyosu hazırlayın (kuru buz veya sıvı azot kullanın) ve jelatin bloğunu 5 dakika dondurun.
- Donmuş blokları -80 °C'de tutun.
- Donmuş bloğu 1 saat boyunca -20 °C'ye yerleştirin.
- Kalıbı çıkarın ve bloğu polietilen glikol ortamına sahip bir aynaya sabitleyin.
- Blok sıkıca sabitlendikten sonra, mandreni kriyostat sistemine yerleştirin.
Not: Boyama sırasında doku kaybını önlemek için kaplamalı kaydıraklar kullanın. - Seri kriyoseksiyonlar gerçekleştirin (genellikle 20 μm kriyoseksiyonlar gerçekleştirilir).
- Rt'de kriyoseksiyonların 15 dakika kurumasına izin verin.
Not: GFP floresanının ağartılmasını önlemek için kriyoseksiyonlar gereksiz ışığa maruz kalmaktan korunmalıdır.
5. Kriyoseksiyonların Mikroskobik Analizi
- RT'de pH 7.4 PBS'de kriyoseksiyonları 10 dakika boyunca yeniden sulatır.
Not: Gerekirse, çekirdek Hoechst ile boyanabilir. - PBS'de 0,5 μg/ml Hoechst çözeltisi kullanın ve kriyoseksiyonları 15 dakika kuluçkaya yatır.
- Slaytları 5 dakika boyunca pH 7,4 PBS ile 3x durulayın.
- Slayt montajına devam edin. O/N'yi sertleyen bir pH 7.4 (veya daha temel) polivinil alkol montaj çözeltisi kullanılabilir: slayt ve kapak arasında hava kabarcıkları oluşumunu önlemek için kapak kapağını dikkatlice yerleştirin.
- Montaj ortamının karanlıkta 4 °C'de O/N sertleşmesine izin verin.
- pHluorin-pleksinA1 füzyon proteinini hassas bir şekilde görselleştirmek için ters konfokal mikroskop kullanın: en uygun iğne deliği ve optik çözünürlükte z-stack gerçekleştirin ve 20X (NA 0.75) veya 40X (NA 1.3) lens kullanın.
Not: pHluorin, GFP'yi (yani 509 nm'deki emisyon zirvesini) tespit etmek için kullanılan parametrelerle tespitedilebilir. Dalga boyu ekscitasyon ve algılama filtresi ayarları görüntüleme yazılımı tarafından en iyi şekilde tanımlanır. Hoechst 425-460 nm (ekscitasyon 405 nm'de), GFP veya pHluorin 485-54 arasında tespit edilir 5 nm (ekscitasyon 473 nm'de) ve RFP 575-675 nm arasında saptanır (heyecan 559 nm'dedir).
Civciv embriyosu omuriliğinde pHluorin-pleksinA1 ve eGFP ekspresyonunun temsili görüntüleri Şekil 4'tegösterilmiştir.
Access restricted. Please log in or start a trial to view this content.
Sonuçlar
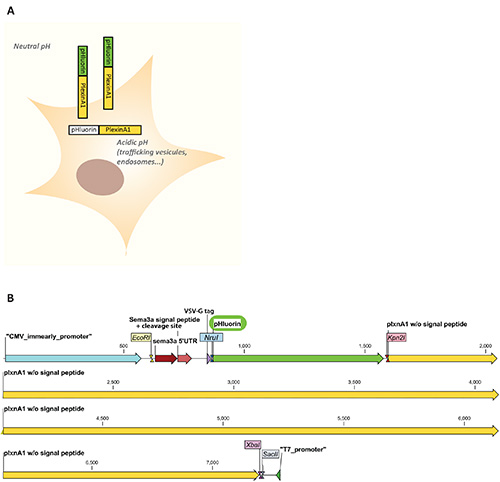
Şekil 1. A. Hücresel bağlamda pHluorin-pleksinA1 floresan özelliklerinin şeması. PHluorin, pH'ın kaçakçılık veziküllerinde veya endozomlarda olduğu gibi asidik (<6) olduğu hücre içi bölmelerde ve pH'ın nötr olduğu hücre dışı ortama maruz kaldığında floresan değildir. Bu, pHluorin-...
Access restricted. Please log in or start a trial to view this content.
Tartışmalar
Bu protokol, hem hücre kültüründe hem de civciv embriyo omuriliğinin gelişimsel bağlamında bir akson kılavuz reseptörü dinamiklerini takip etmek için adım adım bir prosedür sağlar.
Bir de novo pHluorin etiketli protein tasarlamak için klonlama stratejisi ile ilgili iki noktanın göz önünde bulundurulması gerekir. İlk olarak, pHluorin etiketi, plazma membran reseptör havuzunu görselleştirmek için asidik endozomların lümenine ve dolayısıyla hücre dışı b...
Access restricted. Please log in or start a trial to view this content.
Açıklamalar
Yazarların açıklayacak bir şeyi yok.
Teşekkürler
Yardımları için Homaira Nawabi, Frederic Moret ve Isabelle Sanyas'a teşekkür ederiz. Bu çalışma CNRS, Association Francaise contre les Myopathies (AFM), ANR YADDLE, Labex DevWeCan, Labex Cortex, ERC YODA to V.C. C.D-B ve A.J, sırasıyla La Ligue contre le cancer ve Labex DevWeCan bursları tarafından desteklenmektedir.
Access restricted. Please log in or start a trial to view this content.
Malzemeler
| Name | Company | Catalog Number | Comments |
| COS7 cells | ATCC | CRL-1651 | |
| DMEM GlutaMAX | GIBCO | 61965-026 | |
| Sodium pyruvate | GIBCO | 11360-039 | |
| Amphotericin B | Sigma | A2942 | |
| Fetal bovine serum | GIBCO | 10270-106 | |
| Penicillin/Streptomycin | GIBCO | 15140-122 | |
| Exgen500 reagent | Euromedex Fermentas | ET0250 | |
| PBS -Ca2+ -Mg2+ | GIBCO | 14190-094 | |
| Fast green dye | Sigma | F7252 | |
| 32% Paraformaldehyde aqueous solution | Electron Microscopy | 15714-S | Dilute extemporaneously in PBS to achieve a 4% solution |
| Gelatin from cold water fish skin | Sigma | G7041 | |
| Sucrose | Sigma | S0389 | |
| Cryomount | Histolab | 00890 | |
| Hoechst 34580 | Invitrogen | H21486 | |
| Mowiol 4-88 | Fluka | 81381 | |
| Consumables | |||
| Bottom-glass 35 mm dish | MatTek | P35G-1.5-14-C | |
| 5 ml Syringe | Terumo | SS-05S | |
| Needles 0.9 mm x 25 mm | Terumo | NN-2025R | |
| Capillaries | CML | PP230PO | capillaries are stretched manually in the flame |
| Superfrost Plus Slides | Thermo Scientific | 4951PLUS | |
| Material | |||
| Curved scissors | FST | 129-10 | |
| Microscalpel | FST | 10316-14 | |
| Forceps | FST | Dumont #5 REF#11254 | |
| Equipment/software | |||
| Time lapse microscope | Zeiss | Observer 1 | |
| Temp module S | PECON for Zeiss | ||
| CO2 module S | PECON for Zeiss | ||
| Metamorph software | Metamorph | ||
| Eggs incubator | Sanyo | MIR154 | |
| Electroporator apparatus | Nepa Gene CO., LTD | CUY21 | |
| Electrodes | Nepa Gene CO., LTD | CUY611P7-4 | 4 mm platinum electrodes |
| Fluorescence stereomicroscope | LEICA | MZ10F | |
| Cryostat | MICROM | HM550 | |
| Confocal microscope | Olympus | FV1000, X81 | |
| Fluoview software | Olympus | ||
| CLC Main Workbench software | CLC Bio |
Referanslar
- Winckler, B., Mellman, I. Trafficking guidance receptors. Cold Spring Harb. Perspect. Biol. 2, (2010).
- Jacob, T. C., et al. J. Neurosci. 25, 10469-10478 (2005).
- Nawabi, H., Castellani, V. Axonal commissures in the central nervous system: how to cross the midline. Cell Mol. Life Sci. 68, 2539-2553 (2011).
- Keleman, K., Ribeiro, C., Dickson, B. J. Comm function in commissural axon guidance: cell-autonomous sorting of Robo in vivo. Nat. Neurosci. 8, 156-163 (2005).
- Nawabi, H., et al. A midline switch of receptor processing regulates commissural axon guidance in vertebrates. Genes Dev. 24, 396-410 (2010).
- Miesenbock, G., De Angelis, D. A., Rothman, J. E. Visualizing secretion and synaptic transmission with pH-sensitive green fluorescent proteins. Nature. 394, 192-195 (1998).
- Miesenbock, G. Synapto-pHluorins: genetically encoded reporters of synaptic transmission. Cold Spring Harb. Protoc.. 2012, 213-217 (2012).
- Avraham, O., Zisman, S., Hadas, Y., Vald, L., Klar, A. Deciphering axonal pathways of genetically defined groups of neurons in the chick neural tube utilizing in ovo electroporation. J. Vis. Exp. (39), 1792-17 (2010).
- Blank, M. C., Chizhikov, V., Millen, K. J. In ovo electroporations of HH stage 10 chicken embryos. J. Vis. Exp. (9), (2007).
- Wilson, N. H., Stoeckli, E. T. In ovo electroporation of miRNA-based plasmids in the developing neural tube and assessment of phenotypes by DiI injection in open-book preparations. J. Vis. Exp. (68), (2012).
- Rohm, B., Ottemeyer, A., Lohrum, M., Puschel, A. W. Plexin/neuropilin complexes mediate repulsion by the axonal guidance signal semaphorin 3A. Mech. Dev. 93, 95-104 (2000).
- Hamburger, V., Hamilton, H. L. A series of normal stages in the development of the chick embryo. 1951. Dev. Dyn.. 195, 231-272 (1992).
- Korn, M. J., Cramer, K. S. Windowing chicken eggs for developmental studies. J. Vis. Exp. (8), (2007).
- Alberts, P., et al. Cdc42 and actin control polarized expression of TI-VAMP vesicles to neuronal growth cones and their fusion with the plasma membrane. Mol. Biol. Cell. 17, 1194-1203 (2006).
- Perret, E., Lakkaraju, A., Deborde, S., Schreiner, R., Rodriguez-Boulan, E. Evolving endosomes: how many varieties and why. Curr. Opin. Cell Biol. 17, 423-434 (2005).
- Li, Y., et al. Imaging pHluorin-tagged receptor insertion to the plasma membrane in primary cultured mouse neurons. J. Vis. Exp. (69), (2012).
- Tojima, T., Itofusa, R., Kamiguchi, H. Asymmetric clathrin-mediated endocytosis drives repulsive growth cone guidance. Neuron. 66, 370-377 (2010).
- Matsui, A., Yoshida, A. C., Kubota, M., Ogawa, M., Shimogori, T. Mouse in utero electroporation: controlled spatiotemporal gene transfection. J. Vis. Exp. (54), 3024-30 (2011).
- Falk, J., et al. Electroporation of cDNA/Morpholinos to targeted areas of embryonic CNS in Xenopus. BMC Dev. Biol. 7 (107), (2007).
- Holzhausen, L. C., Lewis, A. A., Cheong, K. K., Brockerhoff, S. E. Differential role for synaptojanin 1 in rod and cone photoreceptors. J. Comp. Neurol. 517, 633-644 (2009).
- Shang, Y., Claridge-Chang, A., Sjulson, L., Pypaert, M., Miesenbock, G. Excitatory local circuits and their implications for olfactory processing in the fly antennal lobe. Cell. 128, 601-612 (2007).
- Dittman, J. S., Kaplan, J. M. Factors regulating the abundance and localization of synaptobrevin in the plasma membrane. Proc. Natl. Acad. Sci. U.S.A. 103, 11399-11404 (2006).
- Bozza, T., McGann, J. P., Mombaerts, P., Wachowiak, M. In vivo imaging of neuronal activity by targeted expression of a genetically encoded probe in the mouse. Neuron. 42, 9-21 (2004).
- Sankaranarayanan, S., Ryan, T. A. Real-time measurements of vesicle-SNARE recycling in synapses of the central nervous system. Nat. Cell. Biol. 2, 197-204 (2000).
- Stark, D. A., Kasemeier-Kulesa, J. C., Kulesa, P. M. Photoactivation cell labeling for cell tracing in avian development. CSH Protoc.. 2008, (2008).
- Hildick, K. L., Gonzalez-Gonzalez, I. M., Jaskolski, F., Henley, J. M. Lateral diffusion and exocytosis of membrane proteins in cultured neurons assessed using fluorescence recovery and fluorescence-loss photobleaching. J. Vis. Exp. (60), (2012).
- Hanson, G. T., et al. Green fluorescent protein variants as ratiometric dual emission pH sensors. 1. Structural characterization and preliminary application. Biochemistry. 41, 15477-15488 (2002).
- Rose, T., Schoenenberger, P., Jezek, K., Oertner, T. G. Developmental refinement of vesicle cycling at schaffer collateral synapses. Neuron. 77, 1109-1121 (2013).
- Li, Y., Tsien, R. W. pHTomato, a red, genetically encoded indicator that enables multiplex interrogation of synaptic activity. Nat. Neurosci. 15, 1047-1053 (2012).
- de Wit, J., Toonen, R. F., Verhage, M. Matrix-dependent local retention of secretory vesicle cargo in cortical neurons. J. Neurosci. 29, 23-37 (2009).
Access restricted. Please log in or start a trial to view this content.
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır