Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Bir Membran Reaktöründe Hidrojen Üretimi ve Kullanımı
* Bu yazarlar eşit katkıda bulunmuştur
Bu Makalede
Özet
Membran reaktörleri, doğrudanH2 girişi olmadan ortam koşullarında hidrojenasyon sağlar. Bu sistemlerdeki hidrojen üretimini ve kullanımını atmosferik kütle spektrometresi (atm-MS) ve gaz kromatografisi kütle spektrometresi (GC-MS) kullanarak takip edebiliriz.
Özet
Endüstriyel hidrojenasyon yılda ~ 11 Mt fosil kaynaklıH2 gazı tüketir. Grubumuz, hidrojenasyon kimyası içinH2 gazı kullanma ihtiyacını atlamak için bir membran reaktörü icat etti. Membran reaktörü hidrojeni sudan alır ve yenilenebilir elektrik kullanarak reaksiyonları yönlendirir. Bu reaktörde, ince bir Pd parçası, bir elektrokimyasal hidrojen üretim bölmesini kimyasal hidrojenasyon bölmesinden ayırır. Membran reaktöründeki Pd, (i) hidrojen seçici bir membran, (ii) bir katot ve (iii) hidrojenasyon için bir katalizör görevi görür. Burada, bir Pd membran boyunca uygulanan elektrokimyasal önyargının, bir membran reaktöründe doğrudanH2 girişi olmadan verimli hidrojenasyon sağladığını göstermek için atmosferik kütle spektrometresi (atm-MS) ve gaz kromatografisi kütle spektrometresi (GC-MS) kullanımını bildiriyoruz. ATM-MS ile, GC-MS ile ölçüldüğü gibi, propiofenonun propilbenzene% 100 seçicilikle hidrojenlenmesini sağlayan% 73'lük bir hidrojen geçirgenliği ölçtük. Protik elektrolit içinde çözünmüş başlangıç malzemesinin düşük konsantrasyonlarıyla sınırlı olan geleneksel elektrokimyasal hidrojenasyonun aksine, hidrojen üretiminin membran reaktöründe kullanımdan fiziksel olarak ayrılması, herhangi bir çözücüde veya herhangi bir konsantrasyonda hidrojenasyona olanak tanır. Yüksek konsantrasyonların ve çok çeşitli çözücülerin kullanılması, reaktörün ölçeklenebilirliği ve gelecekteki ticarileştirme için özellikle önemlidir.
Giriş
Termokimyasal hidrojenasyon reaksiyonları, tüm kimyasal sentezlerin ~% 20'sinde kullanılır1. Bu reaksiyonlar, genellikle fosil yakıtlardan, 150 ° C ile 600 ° C arasındaki sıcaklıklardan ve 200atm 2'ye kadar basınçlardan türetilen büyük miktarlardaH2 gazı gerektirir. Elektrokimyasal hidrojenasyon, bu gereksinimleri atlamak ve su ve yenilenebilir elektrik kullanarak hidrojenasyon reaksiyonlarını sürdürmek için çekici bir yoldur3. Geleneksel elektrokimyasal hidrojenasyon için, doymamış bir hammadde, bir elektrokimyasal hücredeki protik bir elektrolit içinde çözülür. Hücreye bir potansiyel uygulandığında, anotta su oksidasyonu meydana gelirken, katotta hidrojenasyon meydana gelir. Bu reaksiyon kurulumunda, hem elektrokimyasal su oksidasyonu hem de kimyasal hidrojenasyon aynı reaksiyon ortamında gerçekleşir. Organik substrat, hem elektrokimyasal suyun ayrılmasını hem de hammaddenin hidrojenasyonunu sağlamak için protik bir elektrolit içinde çözülür. Bu reaksiyonların yakınlığı, reaktan nükleofilik saldırıya duyarlı olduğunda veya reaktans konsantrasyonu çok yüksek olduğunda (>0,25 M)4 yan ürün oluşumuna ve elektrot kirlenmesine neden olabilir.
Bu zorluklar grubumuzu hidrojenasyon reaksiyonlarını elektrokimyasal olarak yönlendirmenin alternatif yollarını araştırmaya yöneltti 5,6,7. Bu araştırma, geleneksel olarak hidrojen gazı ayırma8'de kullanılan bir Pd membranının kullanılmasıyla sonuçlandı. Elektrokimyasal reaktör tarafında su elektrolizi için bir elektrot olarak kullanıyoruz. Bir paladyum membranının bu yeni uygulaması, elektrokimyasal su oksidasyon bölgesinin kimyasal hidrojenasyon bölgesinden fiziksel olarak ayrılmasını sağlar. Ortaya çıkan reaktör konfigürasyonunun iki bölmesi vardır: 1) hidrojen üretimi için bir elektrokimyasal bölme; ve 2) hidrojenasyon için kimyasal bir bölme (Şekil 1). Protonlar, elektrokimyasal bölmede, Pt anot ve aynı zamanda katot görevi gören Pd membranı boyunca bir potansiyel uygulanarak üretilir. Bu protonlar daha sonra Pd membranına göç eder ve burada yüzey adsorbe edilmiş hidrojen atomlarına indirgenirler. Elektrokimyasal bölme, bu proton göçünü kolaylaştırmak için isteğe bağlı bir katyon değişim zarı içerecek şekilde alt bölümlere ayrılabilir. Yüzey adsorbe edilmiş hidrojen atomları, Pd fcc kafes9'un interstisyel oktahedral bölgelerine nüfuz eder ve hidrojenasyon bölmesindeki zarın karşı yüzünde ortaya çıkar ve burada hidrojene ürünler oluşturmak için belirli bir hammaddenin doymamış bağları ile reaksiyona girerler 7,10,11,12,13,14,15,16. Bu nedenle, membran reaktöründeki Pd, (i) hidrojen seçici bir membran, (ii) bir katot ve (iii) hidrojenasyon için bir katalizör görevi görür.
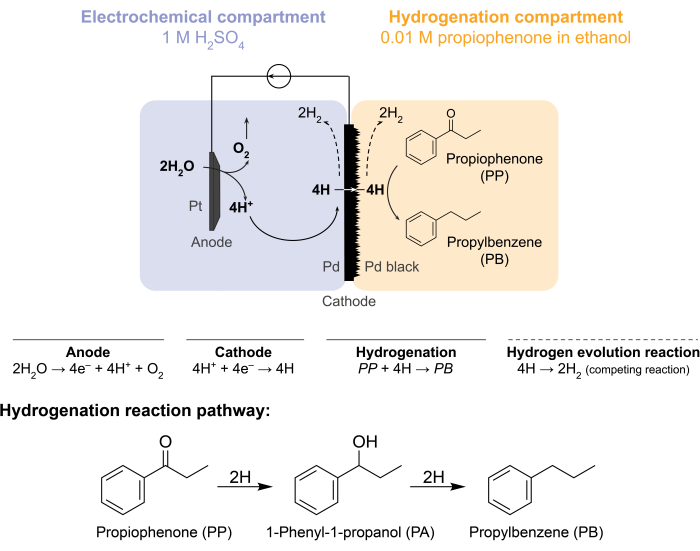
Resim 1: Bir membran reaktöründe hidrojenasyon. Anottaki su oksidasyonu, paladyum katotu üzerinde indirgenen protonlar üretir. H, Pd membranından nüfuz eder ve propilbenzen oluşturmak için propiofenon ile reaksiyona girer. Hidrojen evrimi, paladyum zarının her iki tarafında da meydana gelebilecek rakip bir reaksiyondur. Atmosferik kütle spektrometresi için, H'nin reaktörü elektrokimyasal veya hidrojenasyon bölmelerindeH2 gazı şeklinde bırakmasını gerektiren hiçbir kimyasal hammadde kullanılmaz. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
Membran reaktörü, bir elektrokimyasal H hücresi12'nin anot ve katot bölmeleri arasına bir Pd membranı sandviç ile monte edilir. Kimyasal maddelere dayanıklı O-ringler, membranı yerine sabitlemek ve sızdırmaz bir sızdırmazlık sağlamak için kullanılır. Membran reaktörünün elektrokimyasal bölmesi, hidrojen bakımından zengin bir sulu çözelti içerir. Bu çalışmada 1 M H2SO4 ve 5cm2 parça platin ağ içine sarılmış bir Pt telinden oluşan bir anot kullanılmıştır. Anot, elektrokimyasal bölmenin üstündeki bir delikten elektrolit çözeltisine batırılır. Kimyasal hidrojenasyon bölmesi bir çözücü ve hidrojenasyon hammaddesi 7,10,11,12,16,17 içerir. H hücresi bölmesinin üstündeki delik, örnekleme için kullanılır. Burada gösterilen deneyler, hidrojenasyon yemi olarak etanolde 0.01 M propiofenon kullanmaktadır. Bununla birlikte, başlangıç materyali (ve konsantrasyonu) deneysel ihtiyaçlara uyacak şekilde değiştirilebilir. Örneğin, uzun bir hidrokarbon zinciri ve bir alkin fonksiyonel grubu içeren bir başlangıç malzemesi, çözünürlüğü artırmak için pentan içinde çözülebilir11. Reaksiyon için uygulanan akım 5 mA/cm2 ile 300 mA/cm2 arasında olabilir. Tüm reaksiyonlar ortam sıcaklığı ve basıncı altında gerçekleştirilir.
Atmosferik kütle spektrometresi (atm-MS), hidrojenasyon bölmesi11,12'ye nüfuz eden elektrokimyasal bölmedeki hidrojen yüzdesini ölçmek için kullanılır. Bu ölçüm, membran reaktörü için gerekli enerji girdilerini anlamak için önemlidir, çünkü mümkün olan maksimum hidrojen kullanımını (yani, üretilen hidrojenin ne kadarının aslında hidrojenasyon reaksiyonları için kullanılabileceğini) ortaya koymaktadır. Pd membranından hidrojen geçirgenliği, hem elektrokimyasal hem de hidrojenasyon bölmelerinden11,12 gelişenH2 miktarı ölçülerek hesaplanır. % 100'lük bir geçirgenlik değeri, elektrokimyasal bölmede üretilen tüm hidrojenin Pd membranından hidrojenasyon bölmesine taşındığı ve daha sonra hidrojen gazı oluşturmak üzere birleştiği anlamına gelir. % <100'lük bir geçirgenlik değeri, membrandan nüfuz etmeden önce elektrokimyasal bölmede hidrojen evriminin meydana geldiği anlamına gelir. H2, elektrokimyasal veya hidrojenasyon bölmesinden üretildiğinden, cihaza girer veH2+'ya iyonize edilir. Kuadrupol, m / z = +2 parçalarını seçer ve karşılık gelen yük dedektör tarafından ölçülür. Bu teknikle elde edilen arsa, zaman içindeki iyonik yüktür. İyonik yük önce hidrojenasyon bölmesi için ölçülür ve sinyal stabilize olduğunda, elektrokimyasal bölmeyi ölçmek için kanallar değiştirilir. Hidrojen geçirgenliği, hidrojenasyon bölmesindeki ortalama iyonik yükün, reaktörde ölçülen toplam iyonik yüke bölünmesiyle hesaplanır (Denklem 1)11,12. Hidrojen geçirgenliğini hesaplamak için, hidrojenasyon ve elektrokimyasal bölmelerden gelenH2, atm-MS kullanılarak ayrı ayrı ölçülür.
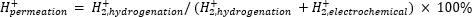 (Ek. 1)
(Ek. 1)
Gaz kromatografisi kütle spektrometresi (GC-MS), hidrojenasyon reaksiyonunun ilerlemesini izlemek için kullanılır12,14,15,16. Örneğin veri toplamak için, reaktörün hidrojenasyon bölmesi etanol içinde 0.01 M propiofenon ile doldurulur. Pt anot ve Pd katot boyunca bir potansiyel uygulanarak, hidrojenasyon bölmesine reaktif hidrojen verilir. Reaktif hidrojen atomları daha sonra doymamış hammaddeyi hidrojene eder ve ürünler, numunenin parçalandığı ve iyonize edildiği GC-MS kullanılarak nicelleştirilir. Bu parçaların kütlesini analiz ederek, hidrojenasyon çözeltisinin bileşimi belirlenebilir ve reaksiyon hızları 12,14,15,16 hesaplanabilir.
Protokol
1. Pd haddeleme
- Pd gofret çubuğunu pamuklu bir bez kullanarak altıgen karışımıyla temizleyin.
DİKKAT: Hekzan yanıcıdır, sağlık açısından tehlikelidir, tahriş edicidir ve çevreye zarar verir. Uygun havalandırma altında çalışın (yani, şnorkel veya duman davlumbazı). - Pd gofreti manuel bir silindir kullanarak dijital bir mikrometre tarafından belirlenen ≤150 μm kalınlığa ulaşana kadar yuvarlayın.
- Pd'yi otomatik bir silindir kullanarak dijital bir mikrometre tarafından belirlenen 25 μm kalınlığa kadar yuvarlayın. Ardından, elde edilen Pd'yi istenen boyutlara kesin (örneğin, 3,5 cm x 3,5 cm).
2. Pd tavlama
- Haddelenmiş Pd folyolarıN2 atmosferine sahip bir kalıp fırınına yükleyin.
- Pd folyoları 25 °C'den başlayarak ısıtın ve sıcaklığı 60 °C / s hızında 850 °C'ye yükseltin. Sıcaklığı 1,5 saat boyunca 850 ° C'de tutun ve ardından fırını 60 ° C / s hızında oda sıcaklığına soğutun.
3. Pd temizleme
- 10 mL nitrik asit, 20 mL %30 (v/v) hidrojen peroksit ve 10 mL deiyonize suyu birleştirerek bir temizleme çözeltisi hazırlayın.
DİKKAT: Nitrik asit aşındırıcı, oksidan ve toksiktir. Hidrojen peroksit aşındırıcı, oksidan ve zararlıdır. - Tavlanmış Pd folyolarını, kuvvetli köpürme azalıncaya veya çözelti sararana kadar (20-30 dakika) temizleme çözeltisine batırın.
- Pd folyoları iki kez DI su ve bir kez izopropil alkol ile durulayın ve ardından hava ile kurulayın.
4. Reaktör tertibatı (Şekil 2, soldan sağa)
- Pd membranını elektrokimyasal bir H hücresinin iki yarısı arasına sıkıştırarak reaktörü monte edin.
- Hücrenin sol tarafı ile Pd membranı arasına kimyasallara dayanıklı bir conta yerleştirin.
- Pd membran ile elektrokimyasal hücrenin sağ tarafı arasına kimyasal maddelere dayanıklı ek bir conta yerleştirin.
- Elde edilen hücre yapılandırmasını bir klipsle kapatın.
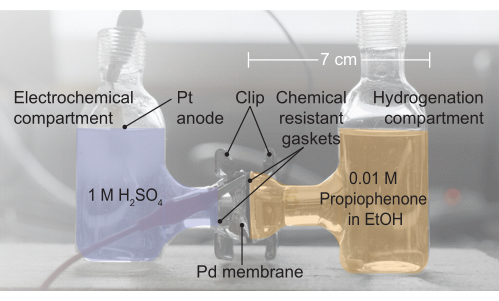
Resim 2: H hücresi tertibatının bir görüntüsü. Elektrokimyasal bölme 1 M H2SO4 elektrolit içerir; Su oksidasyonunun meydana geldiği yer burasıdır. Paladyum membran, H hücresinin iki yarısını ayırır ve contalar sızdırmaz bir sızdırmazlık sağlar. Hidrojenasyon bölmesi etanol (EtOH) içinde 0.01 M propiofenon içerir. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
5. Pd elektrodepozisyon
- 15,9 mM'lik bir konsantrasyona ulaşmak için PdCl2'yi 1 M HCl'ye çözerek bir elektrokaplama çözeltisi hazırlayın.
DİKKAT: PdCl2 zararlı ve aşındırıcıdır. HCl aşındırıcı ve tahriş edicidir. - Reaktörü adım 3'ten itibaren temiz bir Pd folyo kullanarak monte edin.
- Reaktörün elektrokimyasal bölmesini hazırlanan elektrokaplama çözeltisinin 24 mL'si ile doldurun ve hidrojenasyon bölmesini boş bırakın.
- Elektrokimyasal bölmedeki çözeltiye bir Pt örgü anot ve bir Ag/AgCl referans elektrodu yerleştirin.
- Elektrotları bir potansiyostata bağlayın ve 15 C'lik bir yük geçene kadar Pd folyoya Ag / AgCl'ye karşı -0.2 V'luk bir potansiyel uygulayın.
- Reaktörü sökün, elde edilen Pd membranını iki kez deiyonize suyla ve bir kez izopropil alkolle durulayın ve ardından membranı bir hava akımı veyaN2 altında kurutun. Pd membran artık elektrokaplama çözeltisine maruz kalan yüzeyde görünür bir Pd siyah birikimine sahip olacaktır.
6. Atm-MS reaktör kurulumu
- Reaktörü adım 4'te belirtildiği gibi monte edin. Elektrokimyasal bölmeyi 1 M H2SO4 ile doldurun ve hidrojenasyon bölmesini etanol ile doldurun. Hidrojenasyon hammaddesi eklemeyin.
DİKKAT:H2 S04zararlı ve aşındırıcıdır. Etanol yanıcı, zararlı ve sağlık açısından tehlikelidir. - Bir Pt sayaç elektrodunu elektrolitin içine batırın. Pt sayaç elektrodunu ve Pd membranını timsah klipsleri kullanarak bir güç kaynağına bağlayın. Pt sayaç elektrodunu pozitif elektrot olarak ve Pd membranını negatif elektrot olarak bağlayın.
- 25 mA'lık sabit bir akım uygulayın.
7. Atm-MS cihaz kurulumu
- ATM-MS ünitesinin arkasında, güç kablosunun hemen altındaki güç düğmesini açın.
- Pompayı açmak için öndeki pompa düğmesine basın (açıldığında mavi yanar). Ardından, fırın ceketini açın (yeşil yuvarlak anahtar, ışık yanacaktır).
- Kullanılacak kılcal kanalı açın (kanalların yanındaki kırmızı yuvarlak anahtarlar, ışık yanacaktır). Tüpün ısıtıldığını hissederek kullanılan kanalın açık olup olmadığını kontrol edin.
NOT: "vac ok" ifadesinin yanındaki yeşil LED, pompayı açtıktan sonra birkaç dakika içinde yanacaktır. Denemeleri tamamladıktan sonra sistemi kapatmak için, açık olan tüm anahtarları kapatın. - Hidrojenasyon hücresi çıkışını atm-MS kılcal damarlarına bağlayın. Bu bağlantı hava geçirmez olmalıdır.
8. Atm-MS yazılım kurulumu
- Servis masaüstü kısayoluna tıklayın. Kurulum'a gidin | SEM / Emisyon Kontrolü ve hem SEM hem de emisyonlar için kutuları işaretleyin. Tamam'a basın. Servis penceresini kapatın.
- Hesaplama kısayoluna tıklayın ve Sıralama | Yürütün.
- Aşağıdaki parametreleri doldurun: Ölçümler = 30, Temizleme süresi = 30 sn. Dosya Yöneticisi'ne basın ve çıktı verilerini kaydetmek için bir klasör oluşturun. Bu ayarlar, her ölçüm seti arasında 30 s'lik bir temizleme süresiyle 30 ölçüm alacaktır; Gerekirse bu değiştirilebilir.
- Ardından MID ölçümleri dosyası açılır. Dosya Yönetimi'ni seçin ve m/z = 2 için kütle spektrometresi sinyalini ölçmek üzere bir program açın. Bu sinyal, hidrojen gazının iyonize formu olanH2+'dan gelen iyonik akıma karşılık gelir.
- Programı başlatmak için Tamam'a basın. Ölçüm penceresini kapatmayın, çünkü bu cihazın çalışmasını durduracaktır.
- Sinyal stabilize olduktan sonra (1-3 saat), atm-MS kılcal damarını hidrojenasyon bölmesinden ayırın ve elektrokimyasal bölmeye bağlayın.
- Verileri kaydedin ve elektrokimyasal bölmenin sinyali stabilize olduğunda (yaklaşık 30 dakika) deneyi sonlandırın.
- Denklem 1'i kullanarak Pd membranından hidrojen geçirgenliğinin yüzdesini hesaplayın.
9. Elektrokimyasal hidrojenasyon
- Reaktörü adım 4'e göre monte edin.
- Elektrokimyasal bölmeyi 24 mL 1 M H2SO4 ile doldurun.
- Sayaç elektrot açıklığından elektrokimyasal bölmeye bir Pt sayaç elektrodu yerleştirin. Pt sayaç elektrodunu bir güç kaynağının pozitif terminaline bağlayın ve Pd membranını Cu bandı aracılığıyla negatif terminale bağlayın.
- 15 dakika boyunca hücre boyunca 25 mA'lık (40 mA /cm2'ye karşılık gelir) bir galvanostatik akım uygulayın. Voltaj 3 V ile 5 V arasında okuyacaktır.
- 15 dakika geçtikten sonra, kimyasal bölmeyi 24 mL reaksiyon çözeltisi ile doldurun (örneğin, etanolde 0.01 M propiofenon). Reaktant ilavesi sırasında galvanostatik akımı koruyun.
NOT: Reaktöre eklenmeden önce ilk reaksiyon çözeltisini örnekleyin. Bkz. adım 9.6.
DİKKAT: Propiofenon zararlıdır. - Bir mikropipet kullanarak kimyasal bölmeden 30 μL reaksiyon çözeltisi alarak ve numuneyi 1 mL diklorometan içinde çözerek kimyasal bölmeyi periyodik olarak (örneğin her 15 dakikada bir) örnekleyin. Numuneleri, reaksiyon tamamlanana kadar GC-MS şişelerinde saklayın.
DİKKAT: Diklorometan zararlıdır ve sağlık açısından tehlikelidir.
10. Gaz kromatografisi-kütle spektrometresi
- Numune şişelerini otomatik numune alma tepsisine yükleyin.
- Yeşil Masshunter simgesine tıklayarak GC-MS yazılımını başlatın.
- Diziye tıklayın | Dizi düzenleme penceresini açmak için Sırayı Düzenle. İstediğiniz örnek adlarını, flakonu (otomatik örnekleme tepsisindeki konum), yöntem yolunu, yöntem dosyasını, veri yolunu ve veri dosyasını grafiğe doldurun. Örnek türünü "örnek" ve seyreltmeyi 1 olarak ayarlayın ve veri dosyasının örnek adıyla eşleştiğinden emin olun.
- Yöntem'e tıklayarak yöntemi ayarlayın | Tüm yöntemi düzenleyin.
- Hem Yöntem bilgilerinin hem de Cihaz alımının kontrol edildiğinden emin olun. Tamam'a tıklayın. Yöntem yorumları ekleyin (istenirse).
- Veri Toplama ve Veri analizinin kontrol edildiğinden emin olun. Diğer tüm alanları boş bırakın. Tamam'a tıklayın.
- Numune girişinin GC olarak ayarlandığından ve enjeksiyon kaynağının GC ALS olarak ayarlandığından emin olun. MS Kullan kutusunu işaretleyin. Giriş konumunun Ön olarak ayarlandığından ve MS'nin Ön'e bağlı olduğundan emin olun. Tamam'a tıklayın.
- Giriş sekmesi altında, ısıtıcı sıcaklığının 250 ° C'ye ayarlandığından emin olun. Basıncı 7,2 psi'ye ve He akışını 23,1 mL/dak'ya ayarlayın.
- Fırın sekmesinin altında, başlangıç sıcaklığını 50 °C'ye ayarlayın ve 1 dakika bekleyin. Ardından, rampa hızını 25 ° C / dak ve sıcaklığı 200 ° C'ye ayarlayın ve 0 dakika bekleyin. Tamam'a tıklayın.
- Ekran sinyallerinin hiçbirinin kontrol edilmediğinden emin olun. Tamam'a tıklayın.
- Solvent gecikmesini 2,50 dakikaya ayarlayın. Tamam'a tıklayın.
- Seçilen monitörlerin aşağıdakileri içerdiğinden emin olun: GC fırın sıcaklığı, GC giriş F sıcaklığı, GC giriş F basıncı, GC sütun 2 akış hesaplaması, MS EM volt, MS MS kaynağı, MS MS dörtlü. Tamam'a tıklayın.
- Yöntemi istediğiniz yöntem adı altına kaydedin.
- Dizi'ye tıklayarak diziyi başlatın | Başlangıç Sırası | Sırayı Çalıştır.
- Dizi tamamlandığında, Masshunter yazılımını açıp adım 10.3'te programlanan dosya adına tıklayarak verileri görüntüleyin.
- Spectrum'a tıklayarak ürün zirvelerini belirleyin | Elde edilen kütle spektrumlarını NIST veritabanıyla karşılaştırmak için kütüphane arama raporu.
- Başlangıç malzemelerinin ve ürünlerin nispi bileşimini Denklem 2'yi kullanarak hesaplayın.
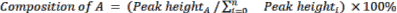 (Ek. 2)
(Ek. 2)
burada A , ilgilenilen kimyasal bileşendir ve n , GC-MS tarafından ölçülen bileşenlerin sayısıdır. Örnek olarak aşağıdaki gibidir: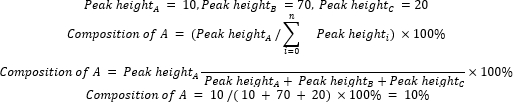
Sonuçlar
Atm-MS, membran reaktöründe üretilen hidrojenin iyonik akımını ölçmek için kullanılır. Bu ölçümleri, elektroliz sırasında Pd membranından ne kadar hidrojenin nüfuz ettiğini ölçmek için kullanabiliriz. İlk olarak, hidrojenasyon bölmesinden evrimleşen hidrojen ölçülür (Şekil 3, noktalı çizgilerin solunda). Sinyal sabit bir duruma ulaştığında, kanal elektrokimyasal bölmeye geçirilir. Elektrokimyasal bölmeden evrimleşenH2 gazı daha sonra sinyal...
Tartışmalar
Pd membran hidrojen geçirgenliği ve kimyasal hidrojenasyon sağlar. Bu nedenle, bu membranın hazırlanması, membran reaktörünün etkinliği için önemlidir. Pd membran boyutu, kristalografisi ve yüzeyi, deneysel sonuçları iyileştirmek için ayarlanmıştır. Pd metali hidrojeni herhangi bir kalınlıkta evrimleştirebilse de, Pd membranları 25 μm'ye kadar yuvarlanır. Membran kalınlığının bu standardizasyonu, hidrojenin membrandan nüfuz etmesi için gereken sürenin tüm deneyler için sabit olmasını...
Açıklamalar
Bu çalışmada açıklanan teknolojiye dayanan patent başvuruları yapılmış ve yayınlanmıştır: Berlinguette, C. P.; Sherbo, RS "Kimyasal ve Elektrokimyasal Reaksiyonları Gerçekleştirmek için Yöntemler ve Aparatlar" ABD Patent Başvurusu No. 16964944 (PCT Ocak 2019, ulusal giriş Temmuz 2020), Yayın No. US20210040017A1 (Şubat 2021'de yayınlandı). Kanada Patent Başvurusu No. 3089508 (PCT Ocak 2019, ulusal giriş Temmuz 2020), Yayın No. CA3089508 (Ağustos 2019'da yayınlanmıştır). Öncelikli veriler: ABD Geçici Patent Başvurusu No. 62/622,305 (Ocak 2018'de dosyalandı).
Teşekkürler
Kanada Doğa Bilimleri ve Mühendisliği Araştırma Konseyi'ne (RGPIN-2018-06748), Kanada İnovasyon Vakfı'na (229288), Kanada İleri Araştırma Enstitüsü'ne (BSE-BERL-162173) ve Kanada Araştırma Başkanlarına finansal destek için minnettarız. Bu araştırma kısmen Kanada İlk Araştırma Mükemmellik Fonu, Kuantum Malzemeleri ve Gelecek Teknolojileri Programı'nın finansmanı sayesinde gerçekleştirildi. UBC Paylaşımlı Enstrüman Tesisi'nden Ben Herring'e GC-MS enstrümanı ve yöntem geliştirme konusundaki yardımları için teşekkür ederiz. Bu yazının geliştirilmesine ve düzenlenmesine katkılarından dolayı Dr. Monika Stolar'a teşekkür ederiz. Son olarak, British Columbia Üniversitesi'ndeki tüm Berlinguette Grubu'na, membran reaktörünün incelenmesinde devam eden destekleri ve işbirlikleri için teşekkür ederiz.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Ag/AgCl Reference Electrode | BASi research products | MW-2021 | Reference electrode |
| Analytical Balance | Cole-Parmer | RK-11219-03 | Instrument |
| Atmospheric Mass Spectrometer | ESS CatalySys | NA | Instrument |
| Bench Power Supply | Newark | 1550 | Instrument |
| Conductive Copper Foil Electrical Tape | McMaster Carr | 76555A711 | Electrochemical cell assembly |
| Dichloromethane | Sigma Aldrich | 270997 | Reagent |
| Electric Rolling Press with Dual Micrometer | MTI Corporation | MR100A | Equipment |
| Electrochemical glass H-cell | University of British Columbia glass blowing | NA | Electrochemical cell assembly |
| ESS catalysis QUADSTAR | ESS CatalySys | NA | Software |
| Ethanol | Sigma Aldrich | 493511 | Reagent |
| Flat Rolling Mill | Pepetolls | 18700A | Equipment |
| Gas Chromatography Mass Spectrometer | Agilent | NA | Instrument |
| GC-MS vial | Agilent | 5067-0205 | Vial for GC-MS |
| Hexanes | Sigma Aldrich | 1.0706 | Reagent |
| Hydrochloric Acid | Sigma Aldrich | 258148 | Reagent |
| Hydrogen peroxide solution (30% v/v) | Sigma Aldrich | H1009 | Reagent |
| Isopropyl Alcohol | Sigma Aldrich | W292907 | Reagent |
| Masshunter Aquisition Software | Agilent | G1617FA | Software |
| Micropipette (100 µL - 1000 µL) | Gilson | F123602 | instrument |
| Micropipette (20 µL - 200 µL) | Gilson | F123601 | Instrument |
| Mitutoyo Digital Micrometer | Uline | H-2780 | Instrument |
| Muffle Furnace | MTI Corporation | KSL-1100X | Equipment |
| Nitric acid | Sigma Aldrich | 438073 | Reagent |
| Nitrogen gas | Sigma Aldrich | 608661 | Reagent |
| Palladium (II) Chloride | Sigma Aldrich | 520659 | Reagent |
| Pd wafer bar, 1 oz, 99.95% | Silver Gold Bull. | NA | Reagent |
| Platinum Auxiliary Electrode | BASi research products | MW-1032 | Anode |
| Potentiostat | Metrohm | PGSTAT302N | Instrument |
| Propiophenone | Sigma Aldrich | P51605 | Reagent |
| Proton Exchange Membrane, Nafion 212 | Fuel cell store | NA | Electrochemical cell assembly |
| Sulfuric acid | Sigma Aldrich | 258105 | Reagent |
Referanslar
- Rytter, E., Hillestad, M., Austbø, B., Lamb, J. J., Sarker, S., Lamb, J. J., Pollet, B. G. Chapter six - Thermochemical production of fuels. Hydrogen, Biomass and Bioenergy. , 89-117 (2020).
- Arpe, H. -. J. . Industrial Organic Chemistry. , (2017).
- Orella, M. J., Román-Leshkov, Y., Brushett, F. R. Emerging opportunities for electrochemical processing to enable sustainable chemical manufacturing. Current Opinion in Chemical Engineering. 20, 159-167 (2018).
- May, A. S., Biddinger, E. J. Strategies to control electrochemical hydrogenation and hydrogenolysis of furfural and minimize undesired side reactions. ACS Catalysis. 10 (5), 3212-3221 (2020).
- Tang, B. Y., Bisbey, R. P., Lodaya, K. M., Toh, W. L., Surendranath, Y. Reaction environment impacts charge transfer but not chemical reaction steps in hydrogen evolution catalysis. ChemRxiv. , (2022).
- Iwakura, C., Yoshida, Y., Inoue, H. A new hydrogenation system of 4-methylstyrene using a palladinized palladium sheet electrode. Journal of Electroanalytical Chemistry. 431 (1), 43-45 (1997).
- Inoue, H., Abe, T., Iwakura, C. Successive hydrogenation of styrene at a palladium sheet electrode combined with electrochemical supply of hydrogen. Chemical Communications. , 55-56 (1996).
- Conde, J. J., Maroño, M., Sánchez-Hervás, J. M. Pd-based membranes for hydrogen separation: Review of alloying elements and their influence on membrane properties. Separation and Purification Reviews. 46 (2), 152-177 (2017).
- Wicke, E., Brodowsky, H., Züchner, H., Alefeld, G., VÖlkl, J. Hydrogen in palladium and palladium alloys. Hydrogen in Metals II. Topics in Applied Physics., edited by Alefeld, G., Völkl, J. 29, (1978).
- Sato, T., Sato, S., Itoh, N. Using a hydrogen-permeable palladium membrane electrode to produce hydrogen from water and hydrogenate toluene. International Journal Hydrogen Energy. 41 (12), 5419-5427 (2016).
- Sherbo, R. S., Delima, R. S., Chiykowski, V. A., MacLeod, B. P., Berlinguette, C. P. Complete electron economy by pairing electrolysis with hydrogenation. Nature Catalysis. 1, 501-507 (2018).
- Sherbo, R. S., Kurimoto, A., Brown, C. M., Berlinguette, C. P. Efficient electrocatalytic hydrogenation with a palladium membrane reactor. Journal of American Chemical Society. 141 (19), 7815-7821 (2019).
- Kurimoto, A., Sherbo, R. S., Cao, Y., Loo, N. W. X., Berlinguette, C. P. Electrolytic deuteration of unsaturated bonds without using D2. Nature Catalysis. 3, 719-726 (2020).
- Jansonius, R. P., et al. Hydrogenation without H2 using a palladium membrane flow cell. Cell Reports Physical Science. 1 (7), 100105 (2020).
- Huang, A., et al. Electrolysis can be used to resolve hydrogenation pathways at palladium surfaces in a membrane reactor. Journal of American Chemical Society Au. 1 (3), 336-343 (2021).
- Delima, R. S., et al. Selective hydrogenation of furfural using a membrane reactor. Energy and Environmental Science. 15 (1), 215-224 (2021).
- Sato, T., Takada, A., Itoh, N. Low-temperature hydrogenation of toluene by electrolysis of water with hydrogen permeable palladium membrane electrode. Chemistry Letters. 46 (4), 477-480 (2017).
- Maoka, T., Enyo, M. Overpotential decay transients and the reaction mechanism on the Pd-H2 electrode. Surface Technology. 8 (5), 441-450 (1979).
- Kurimoto, A., et al. Physical separation of H2 activation from hydrogenation chemistry reveals the specific role of secondary metal catalysts. Angewandte Chemie International Edition. 60 (21), 11937-11942 (2021).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır