Method Article
Gümüş Nanopartiküller Kullanarak Farelerde Osteoartritin İyileştirilmesi
Bu Makalede
Özet
Burada, sinovyal inflamasyon, sinovyal hiperplazi, vasküler hiperplazi vb. dahil olmak üzere tip II kollajenaz kaynaklı osteoartrit farelerinin akut semptomlarını etkili bir şekilde iyileştirmek için gümüş nanopartiküllerin kullanılması için bir protokol sunulmaktadır.
Özet
Diz osteoartriti (KOA), 45 yaş üstü kişilerde eklemlerin en sık görülen dejeneratif hastalıklarından biridir. Şu anda, KOA için etkili bir terapötik yoktur ve tek son nokta stratejisi total diz artroplastisidir (TDA); bu nedenle KOA, ekonomik yükler ve toplumsal maliyetlerle ilişkilidir. İmmün inflamatuar yanıt, KOA'nın oluşumunda ve gelişiminde rol oynar. Daha önce tip II kollajen kullanarak bir fare KOA modeli oluşturmuştuk. Modelde çok sayıda infiltre inflamatuar hücrenin yanı sıra sinovyal dokunun hiperplazisi mevcuttu. Gümüş nanopartiküllerin önemli anti-enflamatuar etkileri vardır ve tümör tedavisinde ve cerrahi ilaç dağıtımında yaygın olarak kullanılmaktadır. Bu nedenle, gümüş nanopartiküllerin terapötik etkilerini kollajenaz II ile indüklenen bir KOA modelinde değerlendirdik. Deneysel sonuçlar, gümüş nanopartiküllerin sinovyal hiperplaziyi ve sinovyal dokudaki nötrofillerin infiltrasyonunu önemli ölçüde azalttığını gösterdi. Bu nedenle, bu çalışma AE için yeni bir stratejinin tanımlandığını göstermekte ve KOA'nın ilerlemesini önlemek için teorik bir temel sağlamaktadır.
Giriş
Diz osteoartriti (KOA), osteoartritin en sık görülen formlarından biridir ve tüm sinovyal eklemde karmaşık bir hastalık sürecini içerir1. Dünya nüfusu giderek yaşlandıkça, KOA insidansı önemli ölçüde artmaktadır. Diz eklemindeki sürekli ağrı genellikle KOA'lı hastaları tıbbi tedavi aramaya sevk eder. KOA'da ağrının etiyolojisi inflamatuar yanıt, sinovyal hiperplazi ve kıkırdak dejenerasyonuile ilişkili olabilir 2. Sinovyum dokuları iki tip hücreden oluşur: sinovyal fibroblastlar ve makrofajlar 3,4,5. Sinovyal fibroblastlar sinovyal sıvı üretir. Sinovyal makrofajlar normalde uykudadır ve inflamatuar yanıt ile aktive edilir. Sinovyumun ilk iltihabı diz eklemi ağrısına neden olur6.
Sinovyum dokusu inflamatuar immün yanıtı, KOA patogenezinde çok önemli bir rol oynar. Önceki çalışmalar, KOA'da sinovit olarak bilinen sinovyum dokularında inflamatuar yanıtlar olduğunu ve KOA'nın sinovit derecesinin sinovyum dokularının inflamatuar hücre infiltrasyonu ile yakından ilişkili olduğunu doğrulamıştır 7,8,9. Sinovit, sinovyumun enflamatuar bir reaksiyonudur ve patolojik özellikleri sinovyal hücrelerin çoğalması, yeni damar oluşumu ve inflamatuar hücrelerin infiltrasyonudur 5,10,11.
KOA tedavisinin amacı, sinovyumun enflamatuar reaksiyonunu hafifletmek ve hastalığın ilerlemesini geciktirmektir. Şu anda, KOA'yı tedavi etmek için başlıca klinik ilaçlar steroid olmayan antienflamatuar ilaçlardır (NSAID'ler); Bununla birlikte, nefrotoksisite12,13 gibi önemli yan etkiler sergilerler. Eklem içi glukokortikoid enjeksiyonları, KOA'yı tedavi etmek için başka bir seçenektir; Bununla birlikte, glukokortikoid hızla yayılır ve eklem efüzyonu ile hızla metabolize edilebilir. Bu arada, altta yatan hiperglisemisi olan diyabetik hastalar, devam eden steroid enjeksiyonları konusunda dikkatli olmalıdır14. Özetle, KOA için mevcut bir ilaç terapötik stratejisi yoktur. Bu nedenle, KOA'yı tedavi etmek için yeni ilaçların araştırılması son derece acildir.
Gümüş nanopartiküllerin boyutu 100 nm'den azdır. Belirgin anti-inflamatuar, antibakteriyel ve antioksidan etkileri nedeniyle, yara iyileşmesi ve yanık yaralanması gibi sağlık ve tıbbın çeşitli yönlerinde yaygın olarak kullanılmaktadırlar15,16. Ayrıca hedefe yönelik ilaç dağıtımı, tıbbi görüntüleme ve moleküler tanıda da kullanılırlar17. Gümüş (Ag), bakır (Cu), çinko (Zn) ve demir (Fe) gibi diğer metal nanopartiküllerden daha fazla anti-inflamatuar ve anti-bakteriyel etkiye sahiptir15. Yeni bir nanomalzeme türü olan gümüş nanopartiküller, geniş spektrumlu ve güçlü antimikrobiyal özelliklere sahiptir. Önceki bir çalışma, yanık yaralanması ve peritonit fare modellerinde 18,19, gümüş nanopartiküllerin enflamatuar faktörlerin üretimini etkili bir şekilde engelleyebileceğini ve yara iyileşmesini destekleyebileceğini buldu. Daha önceki bir çalışma, gümüş nanopartiküllerin, büyüme faktörlerinin ve kollajen birikiminin sentezini teşvik ederek diyabetik yaraların iyileşmesini iyileştirdiğini göstermiştir20.
Gümüş nanopartiküllerin anti-enflamatuar etkilerine dayanarak, farelerde tip II kollajen kaynaklı KOA'yı tedavi etmek için gümüş nanopartikülleri kullanmayı amaçladık. Sonuçlar, farelerde sinovyal eklemin enflamatuar infiltrasyon hücrelerinin sayısının bu tedavi ile önemli ölçüde azaldığını göstermiştir. Sonuçlar ayrıca gümüş nanopartiküllerin farelerde KOA semptomlarını önemli ölçüde hafifletebileceğini öne sürdü. Bu nedenle, gümüş nanopartiküllerin uygulanması, klinik KOA için yeni tedavi seçeneklerinin geliştirilmesini destekleyebilir.
Protokol
Tüm hayvan çalışmaları, Guangzhou Forevergen Tıbbi Laboratuvar Hayvan Merkezi'nin Hayvan Etik ve Refah Komitesi (AEWC) tarafından onaylanmıştır (2018-0186).
1. KOA fare modelinin kurulması
- BALB/c farelerini (18-24 g; 12-14 haftalık) %70 nemli bir ortamda ve 12 saatlik bir aydınlık/karanlık döngüsüyle 26 °C'de tutun. Bu deney için hayvanlar Guangzhou Forevergen Tıbbi Laboratuvar Hayvan Merkezi'nde tutuldu.
- Daha önce açıklandığı gibi bir KOA fare modeli oluşturmak için tip II kollajen kullanın21. Eklem içi enjeksiyonu aşağıda anlatıldığı gibi gerçekleştirin.
- Anestezi için% 2 sodyum pentobarbital (40 mg / kg) ve analjezi için buprenorfin (0.05 mg / kg, deri altı enjeksiyon) uygulayın. Ardından, fare uzuvlarını bantla sabitleyin, tüyleri usturayla çıkarın ve üç kez% 0.1 iyodofor ve alkolden oluşan alternatif bir fırçalama ile dezenfekte edin.
- Steril eldiven giyin ve cildi, deri altı dokusunu ve infrapatellar bağı sırayla ortaya çıkarmak için steril makas kullanın. Kesi bölgesini 0,5 cm'nin altında tutun.
NOT: Operasyon sırasında farelerin vücut ısısını korumak için bir ısıtma battaniyesi kullanılmıştır. - Eklem boşluğuna (infrapatellar ligamanın altına) 10 U 30 mg / kg (0.4 mg / mL) tip II kollajenaz enjekte etmek için 1 mL'lik bir insülin şırıngası kullanın22.
NOT: İğne ile cilt arasındaki açı yaklaşık 15° olmalıdır; Daha sonra iğnenin yönü değiştirilmeli ve iğne tamamen geri çekilmelidir. - Enjeksiyondan sonra önce deri altı dokusunu, sonra cildi dikin. Dikiş bölgesini %0,1 iyodofor ile sterilize edin. Fareleri anesteziden uyandıktan sonra ayrı ayrı havalandırılan kafeslere (IVC'ler) yerleştirin.
2. Gümüş nanopartiküllerin sentezi
NOT: Gümüş nanopartiküllerin hazırlanması daha önce ayrıntılıolarak açıklanmıştır 19. Tüm formülasyon işlemi buz üzerinde gerçekleştirilir. Hazırlandıktan sonra karışım 4 °C'de saklanır; Aksi takdirde, karışım oda sıcaklığında kolayca katılaşır.
- 1.5 mL'lik bir mikrosantrifüj tüpüne toplam 400 μL kollajen tip I (4 mg / mL) ekleyin ve buz üzerine yerleştirin.
- Yukarıdaki kolajene toplam 200 μL fosfat tamponlu salin (PBS) ekleyin, çözeltiyi iyice karıştırın ve buzun üzerine yerleştirin.
- Son olarak, yukarıdaki çözeltiye 400 μL gümüş nanopartikül ekleyin ve ardından yeterince karıştırın. Nanopartikül çözeltisinin son konsantrasyonu 1 mM'dir.
NOT: Gümüş nanopartiküllerin ortalama çapı 5 nm ila 15 nm23 arasında değişmektedir. Bu elektron mikroskobu ile doğrulandı.
3. Tip II kollajenaz kaynaklı KOA farelerinin gümüş nanopartikül tedavisi
- Tip II kollajenaz kaynaklı KOA farelerini 1 hafta sonra kafeslerinden çıkarın ve onlara gümüş nanopartiküller enjekte edin. Gümüş nanopartikülleri haftada bir kez enjekte edin ve örnekleri 30 gün sonra toplayın.
- İntraperitoneal enjeksiyon yoluyla anestezi için toplam% 2 sodyum pentobarbital (doz: 2 mL / kg) enjekte edin ve ardından cildi sabitleyin, hazırlayın ve adım 1.2'de açıklandığı gibi sterilize edin.
- Steril eldiven giyin ve cildi, deri altı dokusunu ve diz bağlarını sırayla ortaya çıkarmak için steril makas kullanın.
- 1 mL'lik bir insülin şırıngası kullanın ve iğne ile eklem boşluğuna 15°'lik bir açıyla girin. Gümüş nanopartikül kollajen karışımından yaklaşık 20 μL'yi yavaşça enjekte edin ve iğneyiyavaşça çekin 24.
- Deri altı dokusunu ve cildi sırayla dikin ve sterilize edin. Fareleri anesteziden uyandıktan sonra ayrı ayrı havalandırılan kafeslere (IVC) yerleştirin.
- Gümüş nanopartikül kollajen karışımının (20 μL) bu enjeksiyonunu haftada bir sıklıkta dört kez gerçekleştirin.
NOT: Gümüş nanopartikül kollajen karışımı ile tedavi edilen fareler ayrı kafeslerde tutulmalıdır. Fareler birlikte tutulduklarında kavga edebilirler ve bu deneysel sonuçları etkiler. Enjeksiyon sırasında iğne eklem boşluğuna ulaştığında gerginlik hissi olacaktır ve enjeksiyon sonrası diz ekleminde şişlik oluşur. Bu iki yöntemin kombinasyonu, araştırmacının ilacın diz eklemine başarılı bir şekilde enjekte edildiğinden emin olmasını sağlar.
4. Diz eklemi ve sinovyal dokunun toplanması
- Fareleri karbondioksit asfiksiasyonu veya ilgili hayvan etik kurulu tarafından onaylanan başka bir protokol ile kurban edin.
- Cildi ve deri altı dokusunu sırayla sterilize edin ve inceleyin ve diz eklemini tamamen ortaya çıkarın.
- Femur ve tibia dahil olmak üzere diz eklemlerini toplayın ve kas dokularını çıkarın.
- Femur, tibia ve çevresindeki yumuşak dokular (bağ ve kapsula) dahil olmak üzere diz eklemi dokularını koruma ve sabitleme için% 10 formalin içinde toplayın.
5. Hematoksilen-eozin boyama
- Gece boyunca fiksasyondan sonra, bölümleri parafine gömün ve parafine gömülü dokuyu 0.4 μm kalınlığa kesmek için bir mikrotom kullanın. Daha fazla boyama için hazırlanan bölümleri kullanın (hematoksilen-eozin boyama, Safranin O / Fast Green ve immünohistokimyasal (IHC) boyama).
- Bölümleri iki kez ksilen ile deparafinize edin, her biri 5 dakika boyunca sırayla %100, %95, %80 ve %70 etanole batırın ve yeniden sulandırın.
- Bölümleri 5 dakika boyunca hematoksilen (0.1 g / 100 mL) ile boyayın ve ardından 10 saniye boyunca doğrudan% 1 HCl ve 1 dakika boyunca eozin (0.5 g / 100 mL) yerleştirin.
- Mikroskop altında sinovyumun histopatolojik değişikliklerini gözlemleyin.
6. Safranin O / Hızlı Yeşil
- Dokuyu parafine gömün ve adım 5.1'de açıklandığı gibi histolojik bölümleri hazırlayın.
- Bölümleri iki kez ksilen ile deparafinize edin ve bunları bir etanol serisiyle (her biri 5 dakika boyunca damıtılmış suda %100, %95, %80 ve %70 etanol gibi) yeniden sulandırın.
- Hazırlanan bölümleri hematoksilen ile boyayın ve her biri 2 dakika boyunca üç kez PBS ile yıkayın.
- Bölümleri hidroklorik asit alkolle ayırt edin ve her biri 2 dakika boyunca PBS ile üç kez yıkayın.
- Bölümleri 5-10 dakika boyunca %0,02 Hızlı Yeşil boyama solüsyonuna, ardından 1-2 dakika %0,1 Safranin O boyamaya daldırın.
- Bölümleri% 1 asetik asit ile ayırt edin, ardından PBS yıkama yapın.
- Kesitlerde fibrokartilaj oluşumunu tespit ve analiz edin.
7. İmmünohistokimyasal (IHC) boyama
- Dokuyu parafine gömün ve adım 5.1'de açıklandığı gibi histolojik bölümleri hazırlayın.
- Bölümleri iki kez ksilen ile deparafinize edin ve bunları bir etanol serisiyle (her biri 5 dakika boyunca damıtılmış suda %100, %95, %80 ve %70 etanol gibi) yeniden sulandırın. Bölümleri Tris-EDTA tamponuna (10 mM Tris bazı, 1 mM EDTA çözeltisi; pH 9.0) daldırın ve antijen alımını gerçekleştirmek için 95 °C'de bir mikrodalga fırında 10 dakika ısıtın.
- Endojen peroksidazı çıkarmak için bölümleri 10 dakika boyunca% 3 hidrojen peroksit çözeltisine maruz bırakın.
- Spesifik olmayan bağlanmayı engellemek için bölümlere %5 keçi serumu uygulayın.
- CD177'ye karşı seyreltilmiş primer antikorları (1: 1.000 seyreltme) ekleyin ve gece boyunca 4 ° C'de inkübe edin. Ardından, bölümleri PBS ile üç kez yıkayın.
- Bölümleri PBS ile ıslatın ve bölümleri uygun ikincil antikor (HRP konjuge polimer anti-tavşan sistemi) ile oda sıcaklığında 30 dakika inkübe edin.
- Kromojen olarak 3,3'-diaminobenzidin (DAB) kullanarak IHC boyamanın görselleştirilmesini gerçekleştirin.
- Kesitleri mikroskop altında görüntüleyin ve elde edilen görüntüleri analiz edin.
Sonuçlar
KOA fare modeli, tip II kollajenaz kullanılarak indüklendi. Model indüksiyonundan 1 hafta sonra başlayarak, hazırlanan gümüş nanopartikül kollajen karışımı 4 hafta boyunca haftada bir kez eklem boşluğuna enjekte edildi (Şekil 1). Her gruptaki farelerin ağırlıkları günlük olarak gözlemlendi ve kaydedildi. Sonuçlar, KOA farelerinin ortalama vücut ağırlığının normal kontrol grubundaki farelerinkinden önemli ölçüde daha düşük olduğunu gösterdi. Bununla birlikte, tip II kollajenaz + AgNPs grubundaki farelerin ortalama vücut ağırlığı, KOA farelerine kıyasla daha yüksekti, ancak bu fark istatistiksel olarak anlamlı değildi (Şekil 2). 30 gün sonra diz eklemlerinin sinovyal dokuları farelerden toplandı ve patolojik incelemeye tabi tutuldu. Hiperplazi, vasküler proliferasyon, sinovyumun inflamatuar infiltrasyonu ve kıkırdak hasarı analiz edildi 5,10,11. Sonuçlar, KOA grubundaki farelerin sinovyal kalınlığının normal kontrol grubuna göre anlamlı derecede yüksek olduğunu gösterdi. Gümüş nanopartikül kollajen karışımı ile muamele edilen grupta, KOA grubuna kıyasla sinovyal membran kalınlığı azalmıştır (Şekil 3). KOA farelerinin sinovyumunda normal kontrol grubuna kıyasla vasküler hiperplazi vardı ve gümüş nanopartikül kollajen karışımı ile tedavi edilen farelerin sinovyumunda vasküler hiperplazi önemli ölçüde azaldı (Şekil 4). Safranin-O boyamanın sonuçları, KOA farelerinin kıkırdak matrisinin tahrip olduğunu, gümüş nanopartikül kollajen karışımı ile tedavi edilen farelerin ise önemli ölçüde daha iyi bir kıkırdak matrisi gösterdiğini gösterdi (Şekil 5). Her gruptaki morfolojik özellik skorları daha önce tarif edildiği gibideğerlendirildi 22. Sonuçlar şöyleydi: salin grubu için 0 ± 0, tip II kollajen grubu için 7 ± 0.63 ve tip II kollajenaz + AgNPs grubu için 4.2 ± 1.17 (Şekil 6). CD177 önemli bir nötrofil belirtecidir25. CD177, normal koşullar altında nötrofillerin %40-60'ında eksprese edilir. Bununla birlikte, nötrofillerde CD177 ekspresyonu akut inflamasyon sırasında önemli ölçüde artar. IHC boyamanın sonuçları, sinovyal bölgedeki infiltre nötrofillerin, AgNP'lerle tedavi edilen grupta KOA grubuna kıyasla önemli ölçüde azaldığını göstermiştir (Şekil 7), bu da AgNP'lerle tedavinin KOA semptomlarını iyileştirebileceğini düşündürmektedir.
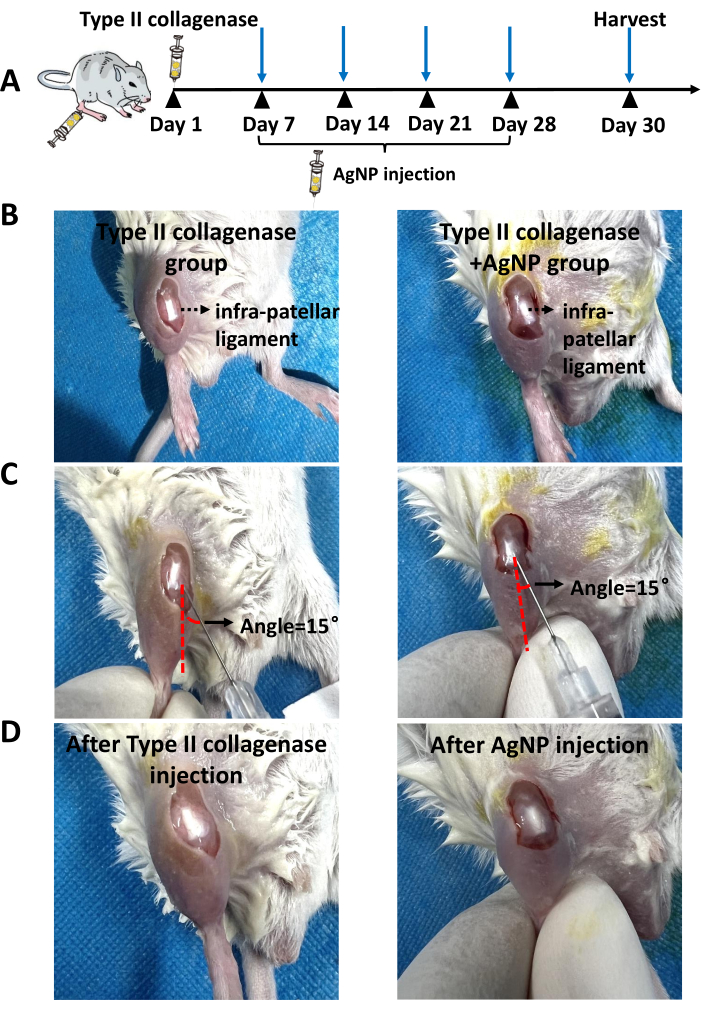
Şekil 1: Enjeksiyon yeri. (A) Tip II kollajenaz enjeksiyonunun temsili görüntüleri. (B) Tip II kollajenaz enjeksiyonundan sonra temsili görüntüler. (C) KOA fare modelinde gümüş nanopartikül kollajen karışımı enjeksiyonunun temsili görüntüleri. (D) KOA model farelerde gümüş nanopartikül kollajen karışımı enjeksiyonundan sonra temsili görüntüler. Kırmızı noktalı çizgi, fare diz bağlarına paralel çizgiyi temsil eder. Siyah ok, insülin şırınga iğnesi ile cilt arasındaki açıyı temsil eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 2: Her gruptaki farelerin vücut ağırlığı değişiklikleri. Bu panel, her gruptaki farelerin farklı zaman noktalarındaki ortalama ağırlığını gösterir; x ekseni, tip II kollajenaz enjeksiyonundan sonraki gün sayısını gösterir ve y ekseni, vücut ağırlığındaki kat değişimini gösterir. Tuzlu su grubu (n=7), tip II kollajenaz grubu (n=5), tip II kollajenaz + AgNPs grubu (n=5). *p < 0,05. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 3: Sinovyal hiperplaziyi temsil eden hematoksilen-eozin (H&E) boyama. Her fare grubundaki sinovyal dokular toplandı, sabitlendi, kesitlere ayrıldı ve ameliyattan 30 gün sonra H & E ile boyandı. Çift oklar, tespit edilen sinovyal kalınlığı temsil eder. Ölçek çubuğu = 0,1 mm. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 4: Perisinovyal vasküler hiperplazinin temsili görüntüsü. Oklar gemileri gösterir. Ölçek çubuğu = 0,05 mm. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 5: Her fare grubunda diz ekleminin Safranin-O boyaması. Ölçek çubuğu = 0,2 mm. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 6: Her gruptaki morfolojik özellik puanları. Her gruptaki fareler için morfolojik özellik skorunu ölçmek için sinovyal doku kullanıldı. Sinovyal astar hücre tabakasının hiperplazi / genişleme derecesini, sinovyal dokudaki nötrofil infiltrasyon derecesini ve sinovyal stromanın aktivasyon derecesini analiz etmek için her grupta beş doku kesiti seçildi (Tablo 1). Nihai puan olarak ortalama değer kullanıldı. **p < 0.01 ve ***p < 0.001, tedavi edilmeyen KOA grubuna kıyasla her kohort için bir Öğrenci t-testi ile. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 7: Her fare grubunda sinovyal dokuda bir nötrofil belirteci için immünohistokimyasal boyama. Her gruptaki farelerin sinovyal dokusunda nötrofil belirteci CD177'nin ekspresyonunu saptamak için immünohistokimyasal boyama kullanıldı. Oklar nötrofilleri gösterir. Ölçek çubuğu = 100 μm. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Tablo 1: Skorlama morfolojik özellikleri. Bu Tabloyu indirmek için lütfen buraya tıklayın.
Tartışmalar
Gümüş nanopartiküller anti-enflamatuar, antibakteriyel, antioksidan ve immünomodülatör etkiler sergiler, yani reaktif oksijen türlerinin üretimini azaltarak hücreleri ve dokuları hasardan koruyabilirler26. Bazı araştırmacılar gümüş nanopartiküllerin toksisitesi konusunda endişelidir27. Gümüş nanopartiküllerin toksisitesi, serbest gümüş iyonlarının varlığı ile doğrudan ilişkilidir. Gümüş nanopartiküllerin nano ölçekli boyutu nedeniyle, biyomoleküllere, hücrelere ve insan organlarına kolayca müdahale edebilirler 15,28,29. Birkaç çalışma, gümüş nanopartiküllerin oksidatif strese neden olabileceğini ve insan hücrelerinde mitokondriyal fonksiyonu bozabileceğini bildirmiştir30. Ek olarak, Ag, büyük miktarlarda gümüş nanopartiküllerin kullanılmasından sonra insan organlarında, özellikle karaciğer ve dalakta tespit edilebilir. Araştırmacılar ayrıca gümüş nanopartiküllerin transsinaptik taşıma yoluyla kan-beyin bariyerini geçme ve beyinde birikme yeteneğine sahip olduğunu bildirmişlerdir31. Gümüş nanopartiküllerin biyotoksisitesine ilişkin sistematik bir rapor hazırlanmamıştır, ancak bazı araştırmacılar gümüş nanopartiküllerin güvenliğini kabul etmektedir32.
Bu çalışmada gümüş nanopartiküllü kollajen karışımı hazırladık. Gerçekten de, gümüş nanopartiküllerin insan dokularındaki süresi kısadır, ancak gümüş nanopartiküllerin süresi bir kollajen karışımı ile uygulandığında uzayabilir; Bu sadece travmayı azaltmakla kalmaz, aynı zamanda ilaçların dozunu da azaltır. Gümüş nanopartiküllerin toksisitesi göz önüne alındığında, bu çalışmada uygulanan gümüş nanopartiküllerin dozu, önceki araştırmalara paralel olarak 30 mg / kg idi33.
Deneysel operasyonun birkaç hayati hususu aşağıdaki gibidir. Tip II kollajenaz, enzimatik bölünme nedeniyle bozulmayı önlemek için hazırlandıktan sonra −20 °C'de saklanmalıdır. Gümüş nanopartikül kollajen karışımının hazırlanması, oda sıcaklığında sürekli olarak buz üzerinde yapılmalıdır, çünkü gümüş nanopartikül kollajen karışımı hızla yarı katı bir jel haline gelir ve daha sonra enjeksiyon için kullanılamaz. Çözelti hazırlandıktan sonra 4 °C'de saklanmalıdır. Eklem içi uygulama için daha küçük iğneli 1 mL'lik bir insülin şırıngası seçilmelidir ve bu, enjekte edilen ilaçların sızmasını etkili bir şekilde önleyebilir. Gümüş nanopartikül kollajen karışımını enjekte etmek için iğne 15 ° 'lik bir açıyla yerleştirilmelidir. İğnenin dirençsiz olması, iğnenin diz eklemi boşluğuna ulaştığını gösterir. Enjekte edildikten sonra, enjeksiyonun açısı değiştirilmeli ve enjekte edilen ilacın sızmasını önlemek için iğne yavaşça geri çekilmelidir.
Bu çalışmada, gümüş nanopartiküller, farelerde tip II kollajenaz kaynaklı KOA semptomlarını etkili bir şekilde iyileştirdi ve gümüş nanopartiküllerin anti-enflamatuar etkisini gösterdi. Birkaç çalışma, gümüş nanopartiküller ile in vitro inkübe edilen hücrelerde apoptoz varlığını bildirmiştir 34,35,36. Sinovyal hiperplazideki azalma, mitokondriyal fonksiyonun bozulmasına karışmalarından dolayı gümüş nanopartiküllerden kaynaklanmış olabilir veya bu sonuçlara reaktif oksijen türleri aracılık etmiş olabilir. KOA model grubundaki farelerin sinovyumunda vasküler hiperplazi gözlendi. Bu işlem sırasında kemokinlerin nötrofilleri kan damarlarından sinovyal dokuya sürmesi ve iltihap patlamasının hücrelerin daha fazla oksijen tüketmesine neden olması ve böylece vasküler hiperplaziye yol açması mümkündü. Bu nedenle, bu hipotezin güvenilirliğini kanıtlamak için daha fazla deney yapılması gerekmektedir. Bu çalışma, klinik KOA tedavisine yönelik araştırmalar için teorik faydalar sağlamaktadır. Gelecekteki çalışmalarda, gümüş nanopartiküllerin etkisini gözlemlemek için ön çapraz bağ (ÖÇB) yöntemini kimyasal olarak indüklenen KOA model yöntemi ile birleştirmeyi amaçlıyoruz. Deneysel sonuçlar, gümüş nanopartiküllerin KOA farelerinde sinovyumdaki enflamatuar hücrelerin infiltrasyonunu önemli ölçüde azaltabildiğini göstermektedir, ancak bu etkinin mekanizmaları, KOA'nın patogenezini çözebilecek daha fazla çalışmaya ihtiyaç duymaktadır.
Açıklamalar
Yazarların ifşa edecek herhangi bir çıkar çatışması yoktur.
Teşekkürler
Bu çalışma, Guangdong Eyaleti Doğa Bilimleri Vakfı (Sayı: 2019A1515010209) ve Çin'in Guangzhou Şehri Bilim ve Teknoloji Projesi (Sayı: 202102010164) tarafından finanse edilmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 1 mL insulin syringe | BD | 305932 | None |
| CD177 Polyclonal Antibody | ThermoFisher Scientific | PA5-98759 | None |
| Chloral hydrate | Sigma-Aldrich | 302-17-0 | None |
| DAB | MCE | HY-15912 | None |
| Eosin | Beyotime Biotechnology | C0109 | None |
| Formalin | Sigma-Aldrich | HT501128 | None |
| Hematoxylin | Beyotime Biotechnology | C0107 | None |
| Light Microscopy | Leica | DM500 | None |
| Silver nanoparticle | Wolcacvi | S-10-20 | Store product in the dark at 4°C |
| Safranine O-Fast Green FCF Cartilage Stain Kit | Solarbio | 90-15-3 | None |
| Type II collagen | Sigma-Aldrich | C6885-500mg | None |
Referanslar
- Kuyinu, E. L., Narayanan, G., Nair, L. S., Laurencin, C. T. Animal models of osteoarthritis: Classification, update, and measurement of outcomes. Journal of Orthopaedic Surgery and Research. 11, 19(2016).
- Kraus, V. B., Blanco, F. J., Englund, M., Karsdal, M. A., Lohmander, L. S. Call for standardized definitions of osteoarthritis and risk stratification for clinical trials and clinical use. Osteoarthritis and Cartilage. 23 (8), 1233-1241 (2015).
- Smith, M. D. The normal synovium. Open Rheumatology Journal. 5, 100-106 (2011).
- de Sousa, E. B., Casado, P. L., Moura, N. V., Duarte, M. E., Aguiar, D. P. Synovial fluid and synovial membrane mesenchymal stem cells: Latest discoveries and therapeutic perspectives. Stem Cell Research and Therapy. 5 (5), 112(2014).
- Scanzello, C. R., Goldring, S. R. The role of synovitis in osteoarthritis pathogenesis. Bone. 51 (2), 249-257 (2012).
- Glyn-Jones, S., et al. Osteoarthritis. Lancet. 386 (9991), 376-387 (2015).
- Roemer, F. W., et al. Presence of MRI-detected joint effusion and synovitis increases the risk of cartilage loss in knees without osteoarthritis at 30-month follow-up: The MOST study. Annals of Rheumatic Diseases. 70 (10), 1804-1809 (2011).
- Furman, B. D., et al. Articular ankle fracture results in increased synovitis, synovial macrophage infiltration, and synovial fluid concentrations of inflammatory cytokines and chemokines. Arthritis and Rheumatology. 67 (5), 1234-1239 (2015).
- Ayral, X., Pickering, E. H., Woodworth, T. G., Mackillop, N., Dougados, M. Synovitis: A potential predictive factor of structural progression of medial tibiofemoral knee osteoarthritis -- Results of a 1 year longitudinal arthroscopic study in 422 patients. Osteoarthritis and Cartilage. 13 (5), 361-367 (2005).
- Henrotin, Y., Lambert, C., Richette, P. Importance of synovitis in osteoarthritis: Evidence for the use of glycosaminoglycans against synovial inflammation. Seminars in Arthritis and Rheumatism. 43 (5), 579-587 (2014).
- Liu-Bryan, R. Synovium and the innate inflammatory network in osteoarthritis progression. Current Rheumatology Reports. 15 (5), 323(2013).
- Towheed, T., Shea, B., Wells, G., Hochberg, M. Analgesia and non-aspirin, non-steroidal anti-inflammatory drugs for osteoarthritis of the hip. Cochrane Database of Systematic Reviews. (2), (2000).
- Co, C. M., et al. Click chemistry-based pre-targeting cell delivery for cartilage regeneration. Regenerative Biomaterials. 8 (3), (2021).
- Oo, W. M., Liu, X., Hunter, D. J. Pharmacodynamics, efficacy, safety and administration of intra-articular therapies for knee osteoarthritis. Expert Opinion on Drug Metabolism and Toxicology. 15 (12), 1021-1032 (2019).
- Morozova, O. V. Silver nanostructures: Limited sensitivity of detection, toxicity and anti-inflammation effects. International Journal of Molecular Sciences. 22 (18), 9928(2021).
- He, M., et al. A pH-responsive mesoporous silica nanoparticles-based drug delivery system with controlled release of andrographolide for OA treatment. Regenerative Biomaterials. 8 (4), (2021).
- Samuel, M. S., Jose, S., Selvarajan, E., Mathimani, T., Pugazhendhi, A. Biosynthesized silver nanoparticles using Bacillus amyloliquefaciens; Application for cytotoxicity effect on A549 cell line and photocatalytic degradation of p-nitrophenol. Journal of Photochemistry and Photobiology B. 202, 111642(2020).
- Liu, X., et al. Silver nanoparticles mediate differential responses in keratinocytes and fibroblasts during skin wound healing. ChemMedChem. 5 (3), 468-475 (2010).
- Tian, J., et al. Topical delivery of silver nanoparticles promotes wound healing. ChemMedChem. 2 (1), 129-136 (2007).
- Vendidandala, N. R., et al. Gallocatechin-silver nanoparticle impregnated cotton gauze patches enhance wound healing in diabetic rats by suppressing oxidative stress and inflammation via modulating the Nrf2/HO-1 and TLR4/NF-kappaB pathways. Life Sciences. 286, 120019(2021).
- Kikuchi, T., Sakuta, T., Yamaguchi, T. Intra-articular injection of collagenase induces experimental osteoarthritis in mature rabbits. Osteoarthritis and Cartilage. 6 (3), 177-186 (1998).
- Lorenz, J., Grässel, S. Experimental osteoarthritis models in mice. Methods in Molecular Biology. 1194, 401-419 (2014).
- Zhao, Z., et al. Design and synthesis of Ag NPs/chitosan-starch nano-biocomposite as a modern anti-human malignant melanoma drug. International Journal of Biological Macromolecules. 236, 123823(2023).
- Ahmed, E., et al. Decellularized extracellular matrix-rich hydrogel-silver nanoparticle mixture as a potential treatment for acute liver failure model. Journal of Biomedical Materials Research Part A. 108 (12), 2351-2367 (2020).
- Bai, M., et al. CD177 modulates human neutrophil migration through activation-mediated integrin and chemoreceptor regulation. Blood. 130 (19), 2092-2100 (2017).
- Singh, D., Chaudhary, D., Kumar, V., Verma, A. Amelioration of diethylnitrosamine (DEN) induced renal oxidative stress and inflammation by Carissa carandas embedded silver nanoparticles in rodents. Toxicology Reports. 8, 636-645 (2021).
- Singh, N., et al. NanoGenotoxicology: The DNA damaging potential of engineered nanomaterials. Biomaterials. 30 (23-24), 3891-3914 (2009).
- Noronha, V. T., et al. Silver nanoparticles in dentistry. Dental Materials. 33 (10), 1110-1126 (2017).
- Ahamed, M., Alsalhi, M. S., Siddiqui, M. K. Silver nanoparticle applications and human health. Clinica Chimica Acta. 411 (23-24), 1841-1848 (2010).
- Palacios-Hernandez, T., et al. cellular uptake and apoptotic responses in human coronary artery endothelial cells exposed to ultrasmall superparamagnetic iron oxide nanoparticles. Journal of Applied Toxicology. 40 (7), 918-930 (2020).
- Lebda, M. A., et al. Potential role of alpha-lipoic acid and Ginkgo biloba against silver nanoparticles-induced neuronal apoptosis and blood-brain barrier impairments in rats. Life Sciences. 212, 251-260 (2018).
- Yin, I. X., et al. The antibacterial mechanism of silver nanoparticles and its application in dentistry. International Journal of Nanomedicine. 15, 2555-2562 (2020).
- Kim, Y. S., et al. Subchronic oral toxicity of silver nanoparticles. Particle and Fibre Toxicology. 7, 20(2010).
- Pascarelli, N. A., et al. Effects of gold and silver nanoparticles in cultured human osteoarthritic chondrocytes. Journal of Applied Toxicology. 33 (12), 1506-1513 (2013).
- Braydich-Stolle, L. K., et al. Silver nanoparticles disrupt GDNF/Fyn kinase signaling in spermatogonial stem cells. Toxicological Sciences. 116 (2), 577-589 (2010).
- Eom, H. J., Choi, J. p38 MAPK activation, DNA damage, cell cycle arrest and apoptosis as mechanisms of toxicity of silver nanoparticles in Jurkat T cells. Environmental Science and Technology. 44 (21), 8337-8342 (2010).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır