Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Longitudinal MicroPET/MicroCT Görüntüleri Kullanılarak Kardiyovasküler Kalsifikasyon İlerlemesi için Yeni Kantifikasyon Protokolü
Bu Makalede
Özet
Bu yeni protokol, küçük araştırma hayvanlarında seri mikro pozitron emisyon tomografisi (PET)/mikro bilgisayarlı tomografi (BT) görüntülerinden kardiyovasküler kalsifikasyon ilerlemesinin ölçülmesini gerektirir.
Özet
Mikro pozitron emisyon tomografisi (PET) ve mikro bilgisayarlı tomografi (BT) görüntüleme, kardiyovasküler kalsifikasyonun ilerlemesini takip etmek için güçlü ve ideal araştırma araçlarıdır. İnvaziv olmayan doğaları nedeniyle, küçük araştırma hayvanları birden fazla zaman noktasında görüntülenebilir. Buradaki zorluk, kardiyovasküler kalsifikasyonun doğru bir şekilde ölçülmesinde yatmaktadır. Burada, uzunlamasına çalışmalarda kardiyovasküler kalsifikasyonun ilerlemesini doğru bir şekilde ölçmek için daha sonraki hastalık evrelerinden görüntüleri şablon olarak kullanan bir protokol sunuyoruz. Protokol, 1) ilk adım olarak uzunlamasına bir çalışma sırasında aynı hayvandan alınan birden fazla görüntüde göğüs bölgesinin hizalanmasını, 2) daha sonraki görüntülerde belirginleşen daha büyük kalsiyum birikintilerinin bulunduğu yerde kalp ve aort içinde yer alan bir ilgi bölgesinin (ROI) tanımlanmasını ve 3) uzunlamasına çalışma sırasında elde edilen tüm görüntülerde kalsiyum birikintilerinin eşzamanlı segmentasyonunu ve nicelleştirilmesini içerir. Bu kolaylaştırılmış yöntem, ROI tanımının hassasiyetini artırarak ve bireysel taramaları bağımsız olarak analiz eden önceki tekniklerle ilişkili değişkenliği azaltarak kardiyovasküler kalsifikasyonun ilerlemesini takip etmede görüntü analizinin doğruluğunu artırır.
Giriş
Kardiyovasküler hastalıklar, morbidite ve mortalitenin önde gelen küresel bir nedenidir ve mekanizmalarını ortaya çıkarmak ve etkili önleyici ve terapötik stratejiler geliştirmek için titiz araştırmalar gerektirir. Koroner arter kalsifikasyonu (KAK), kardiyovasküler hastalık için prediktif bir faktör olarak alandaki uzmanlar tarafından yaygın olarak kabul edilmekte ve kardiyovasküler mortalite riskini önemli ölçüde artırmaktadır 1,2,3,4,5. Mikroskobik kalsifikasyonlar, kalsifik aterosklerozun en erken aşamaları olarak kabul edilir ve "mikrokalsifikasyonlar" terimi, çapı 0,5 ila 50 μm 6,7,8,9 arasındaki kalsiyum birikintilerini ifade etmek için kullanılmıştır. Bu küçük kalsifikasyonların, kalsifik plaklarınilerlemesini hızlandırarak daha büyük kalsiyum birikintileri oluşturmak üzere birleştiğine inanılmaktadır 6,7.
Pozitron emisyon tomografisi (PET) ve bilgisayarlı tomografi (BT), in vivo kardiyovasküler kalsifikasyonun non-invaziv değerlendirmesi için sıklıkla kullanılan değerli araştırma araçları olarak hizmet eder 5,10,11,12,13,14,15,16,17,18,19. Bu görüntüleme yöntemleri, küçük araştırma hayvanlarını içeren uzunlamasına çalışmalarda vasküler kalsifikasyon ilerlemesini izlemek için özellikle avantajlıdır 11,12,13,19. MikroBT görüntüleme, nispeten büyük kalsiyum birikintilerinin anatomik görüntülerini sağlamada etkinlik göstermiştir 11,12,13,19,20.Bununla birlikte, canlı hayvanlarda küçük kalsiyum birikintilerini görüntülemedeki faydası, ~100 μm'lik 8,14 uzamsal çözünürlüğü ile sınırlıdır ve bu da ilk aşamalarında kalsifikasyonun araştırılmasını zorlaştırır.
Kayda değer bir gelişme, mineral yüzey alanına bağlanmasına dayalı olarak kalsifikasyonun tespiti için standart yöntem olarak PET izleyici, florür-18 etiketli sodyum florür (18F-NaF) ile kombine mikroPET/mikroCT görüntülemenin benimsenmesidir. Bu yaklaşım, florür iyonları kalsiyum hidroksiapatite kovalent olarak bağlanırken kalsiyum mineral yüzeyini10,13 tanımlamak için gösterilen radyoaktif işaretli 18F-NaF kullanır ve floroapatit21 oluşturmak üzere hidroksil gruplarının yerini alır. 18 F'nin (yarı ömür ~ 110dakika) radyoaktif bozunmasına ve izleyicinin böbrekler22 yoluyla temizlenmesine göre daha yavaş değişim oranı ile tutarlı olarak, Irkle ve meslektaşları13, kalsifiye karotis örneklerine 18F-NaF bağlanmasının tespit sırasında yüzeyle sınırlı olduğunu buldular. Bu nedenle, izleyici alımı, belirli bir miktarda mineral birden fazla küçük odakta veya gözenekli formda meydana geldiğinde, az, büyük, katı tortularda mevcut olduğundan daha büyük olan mineral yüzey alanı ile doğrudan ilişkili olmalıdır. 18F-NaF PET görüntüleme, mineralizasyonun en erken aşamalarını yüksek hassasiyetle vurgulayarak, hastalığın erken evreleri hakkında değerli bilgiler sağlayabilir ve bu da onu hem önleyici hem de terapötik stratejilerin incelenmesinde özellikle yararlı hale getirir 13,14,15.
Vasküler kalsifikasyonun kombine microPET/microCT görüntülemesindeki son gelişmelerle bile, uzunlamasına, kardiyovasküler kalsifikasyon çalışmalarında görüntü analizinin doğruluğunu artırmak için fırsatlar vardır. Konvansiyonel yaklaşımlar, boylamsal çalışma boyunca her bir zaman noktasında her bir farede her bir görünür kalsifiye bölgenin etrafındaki ilgi bölgelerinin (ROI) emek yoğun, manuel olarak tanımlanmasını kullanır. Bu yöntem, özellikle kalsiyum birikintilerinin boyutlarının tarayıcıların tespit sınırlarına yaklaştığı erken hastalık aşamalarında hassasiyeti azaltır ve düşük yoğunlukta düzenlenmiş küçük birikintilere sahip bazı alanları potansiyel olarak görünmez hale getirir.
Görüntüleme alanında, hizalama genellikle bir dizi görüntünün uzamsal hizalamasını ifade eder. Hizalamayı mevcut zorluklara yeni bir çözüm olarak tanıtan önerilen yöntemimiz, araştırmacıların uzunlamasına bir çalışma boyunca bireysel deneklerden alınan seri görüntülerde kalsifikasyonun ilerlemesini takip etmek için tutarlı bir konum kullanmalarına olanak tanır. Doku kalsifikasyonunun, mikroskobik, daha sonra makroskopik hidroksiapatitminerali 23 oluşturmak üzere birleşen nano boyutlu matriks veziküllerinden (50-150 nm) kaynaklandığı bilindiğinden, mikrokalsifikasyonların fark edilmeden önce erken görüntülerde nerede bulunacağı geriye dönük olarak belirlenebilir.
Görüntü hizalama ile mümkün kılınan zaman içinde aynı konumu takip etmek, bu yöntemin temelidir. ROI, mineralizasyonun kolayca tanımlandığı en son aşamalara göre atandığından, en erken kalsifikasyon aşamalarını doğrudan belirleme ihtiyacını ortadan kaldırır. Bu protokolde, uzunlamasına, birleşik, microPET/microCT görüntüleme çalışmalarında kalsiyum birikiminin doğru kantitasyonunu geliştiren, hayati bir adım olarak bir zaman serisi görüntünün hizalanmasını içeren geliştirilmiş, kolaylaştırılmış bir veri analizi yöntemi sunuyoruz (Şekil 1). Örnek olarak PET/CT veri analizini kullansak da, bu yöntem tek foton emisyonlu bilgisayarlı tomografi (SPECT), manyetik rezonans görüntüleme (MRI) ve optik görüntüleme dahil olmak üzere diğer boylamsal görüntüleme verilerinin analizlerine uygulanabilir24.
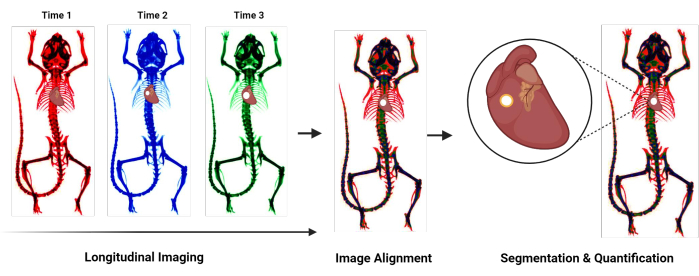
Şekil 1: Protokole genel bakış akış şeması. Kardiyovasküler kalsifikasyonu ölçmek için yeni protokolü özetleyen akış şeması. Genel adımlar, uzunlamasına görüntülemeyi, farklı zaman noktalarında elde edilen görüntülerin hizalanmasını ve kalsifiye bölgenin segmentasyonunu ve nicelleştirilmesini içerir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Protokol
Temsili görüntüler, dişi bir apolipoprotein-E-eksikliği olan (Apoe-/-) fareyi göstermektedir. Deneysel protokoller, Los Angeles Kaliforniya Üniversitesi Kurumsal Hayvan Bakımı ve Kullanımı Komitesi tarafından gözden geçirildi ve onaylandı.
1. Hayvan taraması
- İki görüntü alımı arasında, fareyi herhangi bir müdahale olmadan standart bir diyetle besleyin. Bununla birlikte, 15 aylıkken ilk görüntüden önce, başlangıç aort kalsifikasyonunu indüklemek için 12 ila 14 aylıkken bir Batı diyetine (% 21 yağ,% 0.2 kolesterol) geçin.
- Optimum PET veri toplama ve CT ortak kaydı için microPET/CT tarayıcısının rutin olarak kalibre edildiğinden emin olun. Kalibrasyonları üreticinin talimatlarına göre gerçekleştirin.
- Görüntülemeden önce fareyi 10 dakika boyunca bir odada% 2 izofluran gazı kullanarak uyuşturun. Hayvanın ayak parmağını yanıt vermeden sıkıştırarak anesteziyi onaylayın.
- 3.7 MBq 18F-NaF intravenöz enjeksiyonundan 60 dakika sonra kombine bir mikroPET/CT tarayıcıda mikroPET (350-650 keV, 10 dakika tarama süresi) ve 100 μm mikroCT (80 kVp, 150 μA, 720 projeksiyon, 1 dakika tarama süresi) görüntüleri elde edin. MikroPET taramalarının hemen ardından mikroCT taramalarını edinin.
NOT: Tarayıcı yatağı, hayvan anestezi altında ve aynı pozisyonda kalırken hayvanı PET modelinden CT modeline taşıdı. - Rastgele, zayıflama ve bozulma düzeltmesi ile 3B sıralı bir alt küme beklenti maksimizasyon algoritması (24 alt küme ve 3 yineleme) kullanarak microPET görüntülerini yeniden oluşturun. Değiştirilmiş bir Feldkamp Algoritması kullanarak CT görüntülerini yeniden oluşturun.
NOT: Görüntülemeden sonra, fare sternal yaslanmayı sürdürmek için yeterli bilinci yeniden kazanana kadar izlendi. Boylamsal çalışmanın sonunda, tüm farelere ötenazi yapıldı.
2. DICOM dosyalarını DICOM görüntüleyici yazılımına aktarın
NOT: Bu temsili protokol, ticari olmayan bir lisans altında ORS Dragonfly yazılımını kullanırken, esnekliği diğer DICOM görüntüleyici yazılım seçeneklerine kadar uzanır.
- Uygulamaya çift tıklayarak DICOM görüntüleyici yazılımını başlatın.
- Sol üst köşedeki Dosya'ya gidin. Açılır menüde, Manage DICOM Images (DICOM Görüntülerini Yönet) penceresinin görüntülenmesini istemek için DICOM Görüntülerini İçe Aktar...'ı seçin (Ek Dosya 1- Ek Şekil S1A).
- Manage DICOM Images (DICOM Görüntülerini Yönet) penceresinde Folder Contents (Klasör İçeriği) sekmesine tıklayın. Sağ tarafta, boylamsal bir etütte ilgilenilen DICOM dosyalarını içeren klasörleri seçmek için Klasörü Aç...'ı seçin (Ek Dosya 1- Ek Şekil S1B).
- DICOM dosyalarını içeren klasörleri tanımlayın. İlk klasörü Manage DICOM Images (DICOM Görüntülerini Yönet) penceresine aktarmak için Select Folder (Dosya Seç) seçeneğini tıklatın (Ek Dosya 1- Ek Şekil S1C).
- Manage DICOM Images (DICOM Görüntülerini Yönet) penceresinde hem PET ("PT") hem de CT ("CT") DICOM dosyalarını seçin. Ardından, içe aktarılan tüm DICOM görüntülerini açmak için sağ taraftaki Etüdü Görüntüle'ye tıklayın (Ek Dosya 1- Ek Şekil S1D).
- Boylamsal etüddeki aynı tek konu ile ilgili DICOM görüntülerini içeren her klasör için 2.4 ve 2.5 adımlarını tekrarlayın.
3. Görüntü görselleştirmeyi optimize etmek için DICOM görüntüleyici ayarlarını yapın
- Düzeni, Ek Dosya 1- Ek Şekil S2'de gösterildiği gibi dört görünümü (3B, enine, koronal, sagittal) görüntüleyecek şekilde değiştirin. Sol taraftaki Düzen açılır menüsünde Görünümler'i (seçili sahnede) bulun ve dört görünüm görüntüleyen bir düzen seçin.
- Görüntüleri, zaman noktalarını ve PET veya CT görüntüleri olup olmadıklarını gösterecek şekilde yeniden adlandırın. Görüntü adını seçin ve her görüntüyü yeniden adlandırmak için çift tıklayın .
- Sağ taraftaki Veri Özellikleri ve Ayarları açılır menüsüne erişerek bir görüntüyü açın. Görünürlüğü değiştirmek için her görüntü adının solundaki göz simgesini tıklayın (Ek Dosya 1- Ek Şekil S2)
- Her CT görüntüsünün parlaklığını ve kontrastını ayrı ayrı ayarlayın.
NOT: Optimum BT parlaklığı ve kontrast aralığı konuya, görüntüleme protokolüne, tarayıcıya ve rekonstrüksiyon parametrelerine bağlı olarak değişebilir25,26; Bununla birlikte, tüm ayarlamalar, boylamsal bir çalışmada tek bir denek için tutarlı olmalıdır.- Veri Özellikleri ve Ayarları (Ek Dosya 1- Ek Şekil S2) altındaki görüntü adına tıklayarak bir CT görüntüsü seçin ve açın.
- Görüntü ekranının sol tarafındaki Ana sekmesinde bulunan Pencere Seviyelendirme açılır menüsünde histogramı bulun. Histogramın üzerinde LogY'yi etkinleştirin; ardından, histogramdaki ikinci tepe noktasını tamamen kapsayacak şekilde sarı aralık göstergelerini tıklayıp kaydırmaya devam edin (Ek Dosya 1- Ek Şekil S3A). Optimum parlaklık/kontrasta ulaşılana kadar küçük ayarlamalar yapın; parlaklık/kontrast ayarlı CT görüntüsü örneği için Şekil 2B'ye bakın.
- Pencere Seviyelendirme histogramının altındaki Seçili Aralık kutusunu bulun (Ek Dosya 1- Ek Şekil S3B). Sonraki adımlarda kullanmak için Seçili Aralık değerlerini not edin.
- İkinci bir CT görüntüsü seçin ve açın (Ek Dosya 1- Ek Şekil S3C). İlk CT görüntüsünden seçilen aralık değerlerini, ikinci CT görüntüsü için Seçilen Aralık kutusuna girin (Ek Dosya 1- Ek Şekil S3B-S3D). Ardışık tüm görüntüler için bu işlemi tekrarlayın.
- Arama Tablosu filtresini ayrı ayrı ayarlayarak her PET görüntüsünü iyileştirin.
NOT: En uygun PET renk skalası aralığı konuya, görüntüleme protokolüne, tarayıcıya ve rekonstrüksiyon parametrelerine27 bağlı olarak değişebilir; Bununla birlikte, tüm ayarlamalar, boylamsal bir çalışmada tek bir denek için tutarlı olmalıdır.- Veri Özellikleri ve Ayarları (Ek Dosya 1- Ek Şekil S2) altındaki görüntü adına tıklayarak bir PET görüntüsü seçin ve açın.
- Ana sekmedeki Pencere Dengeleme açılır menüsünün altında, Arama Tablosu'nu (LUT) bulun ve LUT açılır menüsü altında PET'i bulmak için kaydırın ve PET filtresini seçin (Ek Dosya 1- Ek Şekil S4A).
- En iyi görselleştirmeyi elde etmek için Pencere Dengeleme açılır menüsünün altındaki histogramı kullanarak seçilen aralığa ince ayar yapın. Histogramın üzerinde LogY'yi etkinleştirin; daha sonra, tıklamaya devam edin ve sarı aralık göstergelerini Ek Şekil S4B'de (Ek Dosya 1) gösterilen konuma doğru kaydırın. PET görüntü görselleştirme için en uygun seçilen aralığa ulaşılana kadar küçük ayarlamalar yapın; Optimum seçilen aralık için ayarlanmış bir PET/CT görüntüsü örneği için Şekil 2D'ye bakın.
- Pencere Seviyelendirme histogramının altındaki Seçili Aralık açılır menüsünü bulun (Ek Dosya 1- Ek Şekil S4B). Sonraki adımlarda kullanmak için seçilen aralık değerlerini not edin.
- İkinci bir PET görüntüsü seçin ve açın (Ek Dosya 1- Şekil S4C). İkinci görüntü için 3.5.2 adımını tekrarlayın.
- İlk PET görüntüsünden seçilen aralık değerlerini, ikinci PET görüntüsü için Seçilen Aralık kutusuna girin (Ek Dosya 1- Şekil S4B-S4D). Ardışık tüm görüntüler için bu işlemi tekrarlayın.
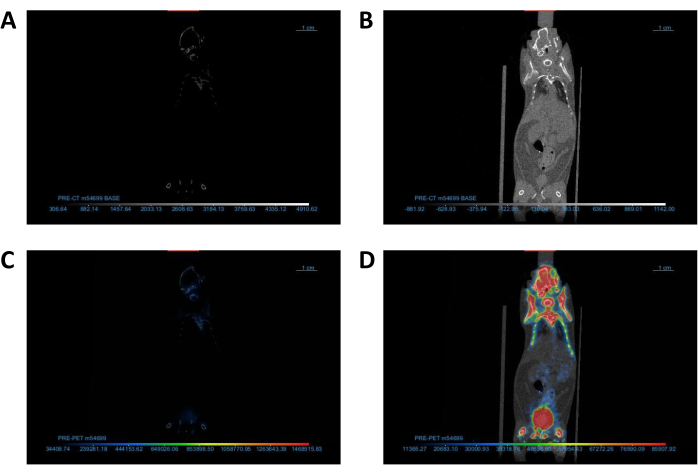
Şekil 2: Görüntü görselleştirmeyi optimize etmek için DICOM görüntüleyici ayarlarının yapılması. (A,B) CT görüntülerinin koronal görünümü (A) kontrast/parlaklık ayarından önce ve (B) sonra. (C,D) PET/CT görüntülerinin koronal görünümü (C) Arama Tablosu ayarından önce ve (D) sonrası. Kısaltmalar: CT = bilgisayarlı tomografi; PET = pozitron emisyon tomografisi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
4. BT görüntülerinde göğüs bölgesini hizalayın
NOT: Kolaylık olması açısından, bir CT görüntüsü "temel" görüntü görevi görecek ve çevrilmeyecek veya döndürülmeyecektir. İkinci CT görüntüsü (ve nihayetinde sonraki seri görüntüler) temel görüntüyle hizalanacak şekilde çevrilecek ve/veya döndürülecektir; Bu, gösterim amacıyla "bindirme" görüntüsü olarak adlandırılacaktır. Hizalama boyunca, temel görüntü ile diğer tüm kaplama görüntüleri arasında ayrım yapmak önemlidir.
- Veri Özellikleri ve Ayarları açılır menüsü altındaki her görüntü adının solundaki göz simgesini tıklayarak tüm PET görüntülerini kapatın ve temel CT görüntüsünü açın.
- CT görüntüsünün opaklığını ~%50 olarak değiştirin. 2D görünümlerden birine tıklayın. Pencere Dengeleme kutusunun altında, Opaklık Eşleme açılır menüsünü bulun ve Opaklık ölçeğini merkeze kaydırın (Ek Dosya 1- Şekil S5).
- Bindirme CT görüntüsünü açın ve adım 4.2'yi tekrarlayın.
- Temel CT görüntüsü ile bindirmeli CT görüntüsü arasında ayrım yapmak için bindirme CT görüntüsünün filtresini değiştirin. Ana sekmedeki Pencere Seviyelendirme açılan listesinin altında Arama Tablosu (LUT) öğesini bulun. LUT açılır menüsünün altında kaydırın ve kırmızı filtreye tıklayın.
NOT: Ek Şekil S5'te (Ek Dosya 1) gösterildiği gibi her görünümde artık iki CT görüntüsü olmalıdır. - Kaplama görüntüsündeki göğüs bölgesini temel görüntüdeki bölgeye mümkün olduğunca yakın hizalamak için 2B görünümlerde Çevir/Döndür araçlarını kullanın. BT görüntüsünde göğüs hizalama göstergeleri olarak göğüs kafesi, üst omurga ve sternuma bakın.
NOT: Aşağıdaki eylemler yalnızca 2B görünümlerde (Enine, Koronal veya Sagital) yürütülebilir (Ek Dosya 1- Ek Şekil S1). En iyi sonucu elde etmek için, üç 2B görünümün tümü arasında geçiş yapın ve her görünümde göğüs bölgesini hizalamak için çevirme/döndürme araçlarını kullanın.- Veri Özellikleri ve Ayarları açılır menüsünde kaplama görüntüsünü seçin ve 2D görünümlerden birini seçmek için bir kez tıklatın.
- Ana sekmenin altındaki Çevir/Döndür açılır menüsünü bulun ve Yer Değiştir simgesini tıklayın (Ek Dosya 1- Şekil S6A).
- Sol alt köşedeki çeviri kutusuna tıklayıp sürükleyin ve bindirme görüntüsünü temel görüntüyle kabaca hizalanacak şekilde hareket ettirmek için seçilen 2D görünümün ortasındaki pivot noktasını döndürün (Ek Dosya 1 - Ek Şekil S6B). Hizalama referansı için kemik yapılarına bakın.
- Manipüle Et açılır menüsünün altında İzleme aracını bulun ve eksenin merkezini tıklayıp sürükleyerek ekseni göğüs bölgesine taşıyın. Bilgisayar faresindeki orta kaydırma düğmesine tıklayarak ve fareyi ekrandan dışarı doğru sürükleyerek göğüs bölgesini yakınlaştırın (Ek Dosya 1 - Ek Şekil S6C).
- Daha fazla öteleme ve döndürme ayarlaması ile göğüs kafesi, üst omurga ve sternum gibi göğüs yapılarıyla hassas konumlandırma için hizalamada ince ayar yapın. 2D görünümler arasında geçiş yapın ve iki görüntü Şekil 3'e benzeyecek şekilde hizalanana kadar 4.5.3-4.5.4 adımlarını tekrarlayın.
- Temel ve ilk bindirme CT görüntüleri hizalandıktan sonra, bindirme CT görüntüsünün filtresini LUT açılır menüsü altında tekrar gri tonlamalı olarak değiştirin. Sabit bir temel görüntü kullanarak aynı hayvandan alınan tüm bindirmeli BT görüntüleri için bölüm 4'ü tekrarlayın.
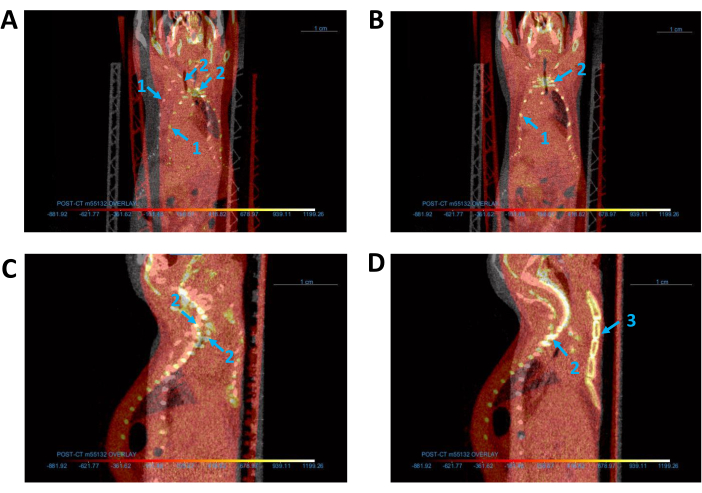
Şekil 3: Tüm CT görüntülerinin hizalanması. (A,B) Baz (gri) ve bindirme (kırmızı) BT görüntülerinin koronal görünümü (A) hizalamadan önce ve (B) sonra. (C,D) BT görüntülerinin sagital görünümü (C) hizalamadan önce ve (D) sonra. Mavi oklar farenin (1) göğüs kafesini, (2) omurgasını ve (3) sternumunu gösterir. Kısaltma: CT = bilgisayarlı tomografi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
5. PET görüntülerini karşılık gelen CT görüntüleriyle birlikte kaydedin
NOT: Bindirme CT görüntüsünün ve temel CT görüntüsünün hizalanması, başlangıçta bindirme CT görüntüsünün Şekil 4'te görülen ilgili PET görüntüsüyle yanlış hizalanmasına neden olacaktır. PET görüntüsünün, karşılık gelen CT görüntüsüyle bir kez daha birlikte kaydedilmesi gerekir.
- Her görüntü adının solundaki göz simgesini tıklayarak bindirme CT görüntüsünü ve ilgili PET görüntüsünü açın.
- PET ve CT görüntülerinin opaklığını ~%50 olarak değiştirin. Pencere Dengeleme açılır menüsünün altında, Opaklık Eşleme açılır menüsünü bulun ve Opaklık ölçeğini merkeze kaydırın (Ek Dosya 1 - Ek Şekil S5).
- CT görüntüsündeki kemik yapısına ve PET görüntüsündeki 18F-NaF kemik yüzeyine bağlı olarak PET görüntüsünü karşılık gelen CT görüntüsüyle hizalamak için 2D görünümlerde Çevir/Döndür araçlarını kullanın.
- Veri Özellikleri ve Ayarları açılır menüsünde bindirme CT görüntüsüne karşılık gelen PET görüntüsünü seçin ve 2D görünümlerden birini seçmek için bir kez tıklayın.
- Ana sekmenin altındaki Çevir/Döndür açılır menüsünü bulun ve Yer Değiştir simgesini tıklayın (Ek Dosya 1 - Ek Şekil S6A).
- PET görüntüsünü CT görüntüsüyle birlikte kaydetmek üzere taşımak için sol alt köşedeki çeviri kutusuna tıklayın ve sürükleyin ve seçilen 2D görünümün ortasındaki pivot noktasını döndürün (Ek Dosya 1 - Ek Şekil S6B).
- CT görüntüleriyle birlikte kayıtlı olmayan tüm bindirmeli PET ve CT görüntüleri için bölüm 5'i tekrarlayın.
NOT: Ortak kayıt tamamlandıysa, ilgili PET/CT görüntüleri, Şekil 4'te gösterildiği gibi vücudun tüm uzunluğu boyunca hizalanmalıdır.
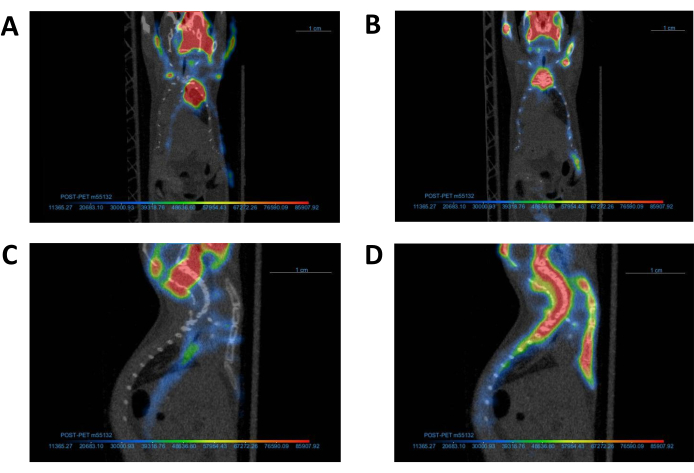
Şekil 4: PET görüntülerinin karşılık gelen CT görüntüsü ile hizalanması. Temsili bir PET görüntüsü ve buna karşılık gelen BT görüntüsü (A, C) ortak kayıttan önce ve (B, D) sonra. Ortak kaydın tamamlanmasını takiben, PET ve CT görüntüleri Panel B'de gösterildiği gibi hizalanmalıdır. Kısaltmalar: CT = bilgisayarlı tomografi; PET = pozitron emisyon tomografisi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
6. Kardiyovasküler kalsifikasyonu tanımlayın
- Boylamsal çalışmada tahmin edilen en büyük kalsifiye bölgelere sahip zaman noktasını belirleyin (yani, geç kalsifikasyon zaman noktası veya önceden tedavi edilmiş denekler). "Referans" görüntü olarak hizmet etmek için bu zaman noktasına karşılık gelen görüntüyü seçin ve en belirgin şekilde görünür kalsifikasyonu vurgulayın. Seçilen bu görüntü daha sonra farklı zaman noktalarında daha küçük kalsifikasyon alanları içeren diğer tüm görüntülerle karşılaştırma için bir şablon işlevi görecektir.
- Görüntünün solundaki göz simgesine tıklayarak referans CT görüntüsünü açın. Manipüle Et açılır menüsünün altında İzleme aracını seçin ve eksen merkezini kardiyak bölgenin etrafında hareket ettirin.
- Göğüs kafesi, sternum ve omurga arasındaki kardiyak siluet üzerine bindirilmiş kalsifiye bölgeleri (küçük, parlak yoğun bölgeler) bulmak için yakınlaştırın (Şekil 5). Kireçlenmiş bölgeler hemen görünmüyorsa, bir 2B görünüm seçip fareyle kaydırarak her görüntünün katmanları arasında gezinin.
- Kireçlenmiş bölgenin üzerine gelmek için İzleme eksenini hareket ettirin ve tüm 2B görünümlerde görünürlüğünü sağlayın. Bir fare BT görüntüsündeki kalsifikasyon bölgelerinin görsel bir referansı için Şekil 5'e bakın.
- Kalsifikasyonun varlığını doğrulamak için ilgili PET görüntüsünü açın.
NOT: PET görüntü ayarları ve ortak kayıt uygun şekilde ayarlandıysa, PET görüntüsü, Şekil 5D'de örneklendiği gibi kalsifiye bölge çevresinde aktivite göstermelidir.
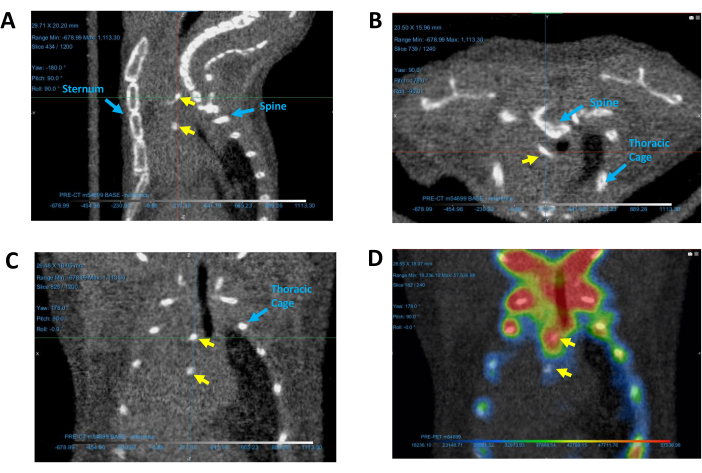
Şekil 5: Kalpteki kalsifiye bölgelerin belirlenmesi. Temsili (A) sagital, (B) transvers ve (C) koronal BT görüntülerinde ve (D) koronal PET/BT görüntülerinde gösterilen kalsifikasyon bölgeleri. Sarı oklar kalsiyum birikintilerini gösterir. Mavi oklar, kalsifikasyonun yerini belirlemek için kullanılan referans yapıları tanımlar. Kısaltmalar: CT = bilgisayarlı tomografi; PET = pozitron emisyon tomografisi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
7. Kireçlenmiş bölgelerin etrafına ROI'ler çizin
- PET referans görüntüsünü kapatın. Görüntünün solundaki göz simgesini tıklayarak yalnızca CT referans görüntüsünü açın.
- Şekiller açılır menüsünü bulun ve Küre şeklini seçin (Ek Dosya 1 - Ek Şekil S7). Boyutu değiştirmek için kürenin kenarlarını tıklayıp sürükleyerek kürenin boyutlarını ayarlayın. Ortadaki kareyi tıklatıp sürükleyerek küreyi yeniden konumlandırın.
- Küreyi dikkatli bir şekilde konumlandırmak için 2B görünümler arasında gezinin. Küre, tanımlanan tüm kalsifikasyon bölgesini ve çevresindeki bazı alanları kapsamalı, ancak çevredeki kemiklerden kaçınmalıdır. Optimum küre çizimi hakkında görsel bir kılavuz için, kürenin uygun şekilde yerleştirilmesi için Ek Şekil S7'ye (Ek Dosya 1) bakın.
- Veri Özellikleri ve Ayarları açılır menüsünde, küre adına sağ tıklayın ve ROI'ye Ekle...'yi seçin. (Ek Dosya 1 - Ek Şekil S8A), ardından Yeni ROI (Ek Dosya 1 - Ek Şekil S8B) seçilir.
- Yeni oluşturulan yatırım getirisine uygun bir ad atayın. Geometri altında, ROI'nin oluşturulacağı CT görüntüsünü seçin (Ek Dosya 1 - Ek Şekil S8C).
- ROI adının solundaki göz simgesine tıklayarak ROI'yi açın ve Ek Şekil S8D'de (Ek Dosya 1) gösterildiği gibi, daha önce çizilmiş kürenin boyutuna karşılık gelen renkli bir ROI'yi gözlemleyin.
- Görüntü ekranının solunda, ana sekmenin yanında yer alan Segment sekmesini bulun (Şekil 6A). Segment sekmesi, ROI'lerin oluşturulmasına ve düzenlenmesine olanak tanır.
NOT: Aşağıdaki üç adım, belirlenen küre içindeki kalsifiye alanları özel olarak vurgulayan bir hassasiyetle bir ROI oluşturulmasına yöneliktir.- Veri Özellikleri ve Ayarları'nda referans yatırım getirisini seçin ve Segment sekmesinin altındaki Aralık açılır menüsünü bulun. Aralık tanımla'yı kontrol etmek için tıklayın (Şekil 6A).
- Seçili Aralık kutusunu kullanarak tanımlanan aralığı değiştirin (Şekil 6A). Tanımlanan aralığın, kalsiyum eşiğinin altındaki Hounsfield birimi (HU) değerlerine sahip tüm kalsifiye edilmemiş pikselleri kapsüllediğinden emin olun. Bu gösteri, kalsiyum için 300 HU'luk bir eşik kullanır ve bu görüntüdeki en düşük yoğunluklu piksel -2,626'dır; bu nedenle, seçilen aralık -2.626-300 HU'dur.
- Seçilen aralık yapılandırıldıktan sonra, belirtilen eşiğin altındaki tüm pikselleri küre ROI'sinden çıkarmak için Kaldır'a (Şekil 6A) tıklayın.
NOT: Bu eylem, küre içindeki kalsifiye bölgeleri özel olarak vurgulayan ve daha fazla analiz için odaklanmayı kolaylaştıran yeni bir ROI ile sonuçlanır. Tamamlanan ROI'ler, Şekil 6B'de gösterilen ROI'ye benzer olmalıdır.
- Ortak bir referans küresi kullanarak benzersiz yeni ROI'ler oluşturmak için tüm ardışık CT görüntüleri için 7.3-7.4 adımlarını tekrarlayın. Her bir ROI'yi, belirli CT görüntüsünün kimliğine karşılık gelecek şekilde adlandırın, kısa ve düzenli bir analiz sağlayın.
NOT: Her görüntünün ROI analizi için yeni bir küre oluşturmak GEREKLİ OLMAMALIDIR, çünkü referans küresi, hizalamanın doğru olduğu varsayılarak, tüm görüntülerin en büyük kalsifiye bölgesini kapsamalıdır.
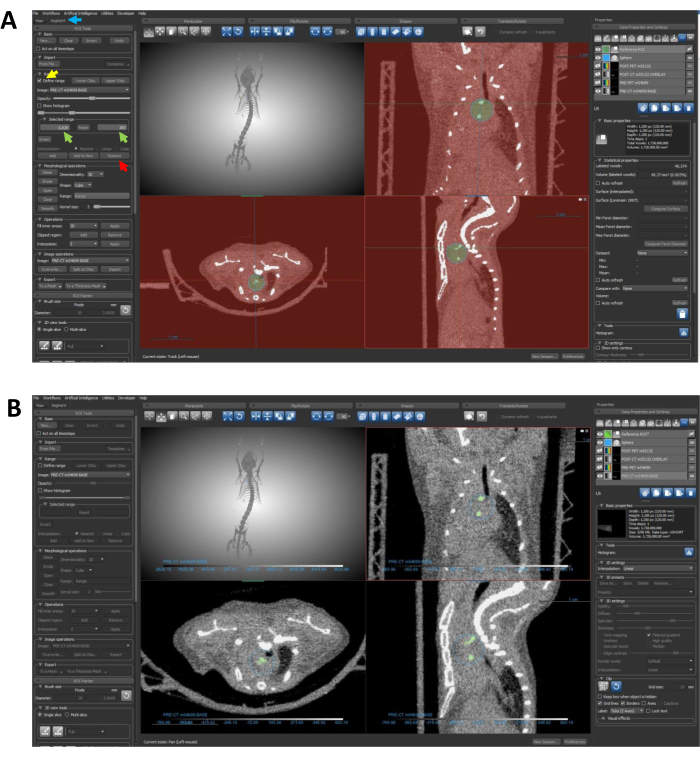
Şekil 6: ROI'yi kalsifiye bölgelerle sınırlamak için segmentasyonu kullanma. (A) Oklar, istenmeyen yoğunluk verilerini ROI'den çıkarmak için gereken adımlarda yol gösterir. Mavi ok, Segment sekmesini gösterir; sarı ok, Aralık Tanımla özelliğini vurgular; yeşil oklar seçilen aralık girişlerini gösterir; ve kırmızı ok Kaldır düğmesini gösterir. (B) 7.4-7.4.3 protokol adımlarının tamamlanmasını takiben, ROI, bu panelde gösterildiği gibi kalsifiye bölgeleri özel olarak tanımlamalıdır. Kısaltma: ROI = ilgi alanı. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
8. Her görüntü için yatırım getirisini ölçün
- Veri Özellikleri ve Ayarları açılır menüsü altında ölçülecek yatırım getirisini seçin.
- Temel Özellikler açılır menüsünün altında sağ tarafta bulunan İstatistiksel özellikler açılır menüsünü bulun (Şekil 7).
- İstatistiksel Özellikler altında Veri Kümesi tablosunu bulun. Sağdaki açılır menüyü kullanarak, ölçülecek yatırım getirisi ile ilişkili olan uygun görüntüleme veri kümesini seçin (Şekil 7).
- ROI içindeki CT verilerini ölçerken, ROI ile ilişkili CT görüntü adını seçin.
- ROI içindeki PET verilerini ölçerken, ROI'ye karşılık gelen PET görüntü adını seçin.
- Seçili kireçlenmiş bölgenin niceliksel değerlerini almak için Yenile'ye tıklayın. Veri kümesi tablosuna göre Min, Max ve Average değerlerini not edin. Niceleme için Ortalama değerleri kullanın (Şekil 7).
- İstatistiksel Özellikler kutusunun üst kısmında hacim hesaplamasını bulun. Miktar tayini için bu hacmi kullanın (Şekil 7).
- CT veri kümeleri için değerler HU cinsinden rapor edilir. Ortalama ROI değeri (HU) ve ROI hacminin (mm3) çarpımını kullanarak hacimsel kalsiyum içeriğini (vHU) hesaplayın12.
- PET veri kümeleri için değerler, bozunma/saniye ile karşılık gelen Becquerels (Bq) cinsinden rapor edilir. İzleyici alım konsantrasyonu için ortalama ROI değerini (Bq) ROI hacmine (mm 3) bölerek Bq/mm3'e dönüştürün.

Şekil 7: ROI ölçümü. Seçili bir ROI için İstatistiksel Özellikler sekmesi. Kırmızı oklar, yatırım getirisine dayalı bir veri kümesi için istatistiksel bilgi elde etmek için gereken adımları gösterir. Kırmızı kutular, daha fazla analiz hesaplaması için gerekli olan hacmi ve ortalama Hounsfield birim değerini tanımlar. Kısaltma: ROI = ilgi alanı. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Sonuçlar
Analiz yöntemleri
Bu bölüm, temsili sonuçlar aracılığıyla başarılı kullanımı göstermektedir. Burada, 12 ila 14 aylık bir Batı diyetine (% 21 yağ,% 0.2 kolesterol) tabi tutulduktan sonra 15 ve 18 aylıkken taranan tek bir farenin birleşik mikroPET / mikroCT görüntüsünü sergiliyoruz. Kalsifikasyon miktar tayini için protokol bölümleri 2-8'i takiben, dört bağımsız araştırmacı, 15 ve 18aylık zaman noktalarında elde edilen ayn?...
Tartışmalar
Bu yeni protokol, kardiyovasküler kalsifikasyonun miktar tayini için geliştirilmiş bir yaklaşımdır. Görüntülemenin non-invaziv doğası nedeniyle, küçük hayvanlarda kardiyovasküler kalsifikasyonun ilerlemesini takip etmek için uzunlamasına mikroBT görüntüleri elde edilebilir. MikroCT görüntüleri tek başına kalsiyum içeriğinin ilerlemesini gösterebilse de, mikroPET görüntüleri, mevcut olduğunda, özellikle yüzey alanına izleyici bağlanması nedeniyle kü?...
Açıklamalar
Yazarların beyan edebilecekleri herhangi bir çıkar çatışması yoktur.
Teşekkürler
UCLA Crump Klinik Öncesi Görüntüleme Teknolojisi Merkezi'nin tüm üyelerine, veri toplama ve işlemenin yanı sıra ekipman ve altyapı bakımı konusundaki yardımları için teşekkür ederiz. Jeffrey Collins'e siklotron çalışması ve 18F-NaF sentezi konusundaki yardımları için teşekkür ederiz. UCLA İstatistiksel Danışmanlık Grubu'na istatistiksel analiz konusundaki yardımları için teşekkür ederiz. Bu çalışma, NIH Kanser Merkezi Destek Hibesi (MT'ye 2 P30 CA016042-44) ve Ulusal Sağlık, Kalp, Akciğer ve Kan Enstitüsü (HL137647 ve YT ve LLD'ye HL151391) tarafından desteklenmektedir. GNEXT PET/CT tarayıcısı, NIH S10 Hayvan Araştırmaları için Paylaşılan Enstrümantasyon Hibesi (1S10OD026917-01A1'den Arion Chatziioannou'ya) tarafından finanse edildi.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 0.5 cc Sterile Insulin Syringes | Exel International | #26028 | Used for IV injection of 18F-NaF PET Tracer |
| 18F-NaF PET Tracer | CNSI Cyclotron | ||
| Biorender | Biorender | Used for figure 1 | |
| Female Apoe-/- mouse | Jackson Laboratories | #002052 | B6.129P2-Apoetm1Unc/J |
| GNEXT PET/CT | Sofie Biosciences, Dulles, Virginia | ||
| Isoflurane | Piramal Critical Care | Used as anesthesia for mouse imaging | |
| ORS Dragonfly | Comet Technologies Canada Inc. | ||
| SPSS Statistics | IBM | ||
| Western diet for mice | Envigo | #TD88139 | 21% fat, 0.2% cholesterol |
Referanslar
- Rennenberg, R. J. M. W., et al. Vascular calcifications as a marker of increased cardiovascular risk: A meta-analysis. Vasc Health Risk Man. 5, 185-197 (2009).
- Budoff, M. J., et al. Long-term prognosis associated with coronary calcification - observations from a registry of 25,253 patients. J Am Coll Cardiol. 49 (18), 1860-1870 (2007).
- Polonsky, T. S., et al. Coronary artery calcium score and risk classification for coronary heart disease prediction. JAMA. 303 (16), 1610-1616 (2010).
- Gepner, A. D., et al. Comparison of coronary artery calcium presence, carotid plaque presence, and carotid intima-media thickness for cardiovascular disease prediction in the multi-ethnic study of atherosclerosis. Circ Cardiovasc Imaging. 8 (1), e002262 (2015).
- Pillai, I. C. L., et al. Cardiac fibroblasts adopt osteogenic fates and can be targeted to attenuate pathological heart calcification. Cell Stem Cell. 20 (2), 218-232.e5 (2017).
- Mori, H., et al. Coronary artery calcification and its progression: What does it really mean. JACC Cardiovasc Imaging. 11 (1), 127-142 (2018).
- Mohan, J., Bhatti, K., Tawney, A., Zeltser, R. . StatPearls [Internet]. , (2023).
- Wang, Y., Osborne, M. T., Tung, B., Li, M., Li, Y. Imaging cardiovascular calcification. J Am Heart Assoc. 7 (13), e008564 (2018).
- Fletcher, A. J., et al. Quantifying microcalcification activity in the thoracic aorta. J Nucl Cardiol. 29 (3), 1372-1385 (2022).
- Derlin, T., et al. Feasibility of 18F-sodium fluoride PET/CT for imaging of atherosclerotic plaque. J Nucl Med. 51 (6), 862-865 (2010).
- Hsu, J. J., et al. Changes in microarchitecture of atherosclerotic calcification assessed by 18F-NaF PET and CT after a progressive exercise regimen in hyperlipidemic mice. J Nucl Cardiol. 28 (5), 2207-2214 (2021).
- Hsu, J. J., et al. Effects of teriparatide on morphology of aortic calcification in aged hyperlipidemic mice. Am J Physiol Heart Circ Physiol. 314 (6), H1203-H1213 (2018).
- Irkle, A., et al. Identifying active vascular microcalcification by 18F-sodium fluoride positron emission tomography. Nat Commun. 6, 7495 (2015).
- Syed, M. B. J., Doris, M., Dweck, M., Forsythe, R., Newby, D. E. Chapter 9 - Imaging vascular calcification: Where are we headed. Coronary Calcium: A Comprehensive Understanding of Its Biology, Use in Screening, and Interventional Management. , (2019).
- Joshi, N. V., et al. 18F-fluoride positron emission tomography for identification of ruptured and high-risk coronary atherosclerotic plaques: A prospective clinical trial. Lancet. 383 (9918), 705-713 (2014).
- Fiz, F., et al. 18F-NaF uptake by atherosclerotic plaque on PET/CT imaging: Inverse correlation between calcification density and mineral metabolic activity. J Nucl Med. 56 (7), 1019-1023 (2015).
- Kruithof, B. P., et al. An in vivo map of bone morphogenetic protein 2 post-transcriptional repression in the heart. Genesis. 49 (11), 841-850 (2011).
- Sheen, C. R., et al. Pathophysiological role of vascular smooth muscle alkaline phosphatase in medial artery calcification. J Bone Miner Res. 30 (5), 824-836 (2015).
- Tsai, M. T., Chen, Y. Y., Chang, W. J., Li, S. Y. Warfarin accelerated vascular calcification and worsened cardiac dysfunction in remnant kidney mice. J Chin Med Assoc. 81 (4), 324-330 (2018).
- Wait, J. M., et al. Detection of aortic arch calcification in apolipoprotein e-null mice using carbon nanotube-based micro-ct system. J Am Heart Assoc. 2 (1), e003358 (2013).
- White, D. J., et al. 19F MAS-NMR and solution chemical characterization of the reactions of fluoride with hydroxyapatite and powdered enamel. Acta Odontol Scand. 46 (6), 375-389 (1988).
- Czernin, J., Satyamurthy, N., Schiepers, C. Molecular mechanisms of bone 18F-NaF deposition. J Nucl Med. 51 (12), 1826-1829 (2010).
- Chen, N. X., O'neill, K. D., Dominguez, J. M., Moe, S. M. Regulation of reactive oxygen species in the pathogenesis of matrix vesicles induced calcification of recipient vascular smooth muscle cells. Vasc Med. 26 (6), 585-594 (2021).
- Klose, A. D., Paragas, N. Automated quantification of bioluminescence images. Nat Commun. 9 (1), 4262 (2018).
- Chen-Mayer, H. H., et al. Standardizing ct lung density measure across scanner manufacturers. Med Phys. 44 (3), 974-985 (2017).
- Coxson, H. O. Sources of variation in quantitative computed tomography of the lung. J Thorac Imaging. 28 (5), 272-279 (2013).
- Rogasch, J. M. M., et al. Influences on pet quantification and interpretation. Diagnostics (Basel). 12 (2), 451 (2022).
- Liljequist, D., Elfving, B., Skavberg Roaldsen, K. Intraclass correlation - a discussion and demonstration of basic features. PLoS One. 14 (7), e0219854 (2019).
- Koo, T. K., Li, M. Y. A guideline of selecting and reporting intraclass correlation coefficients for reliability research. J Chiropr Med. 15 (2), 155-163 (2016).
- Moss, A. J., et al. Molecular coronary plaque imaging using (18)f-fluoride. Circ Cardiovasc Imaging. 12 (18), e008574 (2019).
- Moss, A., et al. Coronary atherosclerotic plaque activity and future coronary events. JAMA Cardiol. 8 (8), 755-764 (2023).
- Badea, C., Hedlund, L. W., Johnson, G. A. Micro-ct with respiratory and cardiac gating. Med Phys. 31 (12), 3324-3329 (2004).
- Yang, Y., Rendig, S., Siegel, S., Newport, D. F., Cherry, S. R. Cardiac pet imaging in mice with simultaneous cardiac and respiratory gating. Phys Med Biol. 50 (13), 2979-2989 (2005).
- Liao, W., Deserno, T. M., Spitzer, K. Evaluation of free non-diagnostic dicom software tools. Proc Spie. 6919, (2008).
- Haak, D., Page, C. E., Deserno, T. M. A survey of dicom viewer software to integrate clinical research and medical imaging. J Digit Imaging. 29 (2), 206-215 (2016).
- Aiello, M., et al. How does dicom support big data management? Investigating its use in medical imaging community. Insights Imaging. 12 (1), 164 (2021).
- Kristanto, W., Van Ooijen, P. M., Groen, J. M., Vliegenthart, R., Oudkerk, M. Small calcified coronary atherosclerotic plaque simulation model: Minimal size and attenuation detectable by 64-MDCT and microCT. Int J Cardiovasc Imaging. 28 (4), 843-853 (2012).
- Dehmeshki, J., et al. Volumetric quantification of atherosclerotic plaque in ct considering partial volume effect. IEEE Trans Med Imaging. 26 (3), 273-282 (2007).
- Demer, L. L., Tintut, Y., Nguyen, K. L., Hsiai, T., Lee, J. T. Rigor and reproducibility in analysis of vascular calcification. Circ Res. 120 (8), 1240-1242 (2017).
- Alluri, K., et al. Scoring of coronary artery calcium scans: History, assumptions, current limitations, and future directions. Atherosclerosis. 239 (1), 109-117 (2015).
- Zhang, L., et al. Advances in CT techniques in vascular calcification. Front Cardiovasc Med. 8, 716822 (2021).
- Achenbach, S., Raggi, P. Imaging of coronary atherosclerosis by computed tomography. Eur Heart J. 31 (12), 1442-1448 (2010).
- Agatston, A. S., et al. Quantification of coronary artery calcium using ultrafast computed tomography. J Am Coll Cardiol. 15 (4), 827-832 (1990).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır