Method Article
Centrosomes التصوير في يطير الخصية
In This Article
Summary
التصوير من البروتينات centrosomal خلال ذبابة الفاكهة الحيوانات المنوية هو وسيلة قوية لتحديد بروتينات جديدة الحرجة للبيولوجيا الجسيم المركزي وكذلك لتوضيح وظيفة معينة من اللاعبين المعروفين في هذه العملية.
Abstract
يتم حفظها Centrosomes العضيات القائم على أنيبيب هيكلها وتغير بشكل كبير في جميع أنحاء دورة الخلية وتمايز الخلايا وظيفة. Centrosomes ضرورية لتحديد محور انقسام الخلايا أثناء الانقسام ول nucleate أهداب أثناء الطور البيني. تبقى هوية من البروتينات التي تتوسط هذه التغيرات الدينامية الوحيدة المعروفة جزئيا، وظيفة العديد من البروتينات التي قد تورطت في هذه العمليات لا تزال بدائية. وقد أظهرت الأعمال الأخيرة التي ذبابة الفاكهة الحيوانات المنوية يوفر نظام قوي لتحديد بروتينات جديدة حاسمة من أجل وظيفة الجسيم المركزي وتشكيل وكذلك لاكتساب نظرة ثاقبة على وظيفة معينة من اللاعبين المعروفين في العمليات المتعلقة الجسيم المركزي. ذبابة الفاكهة هو إنشاء نموذج الوراثية الحي حيث المسوخ في الجينات centrosomal يمكن الحصول بسهولة وتحليلها بسهولة. علاوة على ذلك، التطورات الحديثة في الحساسية والقرار من المجهر الضوئي وتطوير علامات centrosomal الموسومة راثيا قوية حولت القدرة على استخدام الخصيتين ذبابة الفاكهة كنظام نموذج بسيط ويمكن الوصول إليها لدراسة centrosomes. توضح هذه الورقة استخدام علامات centrosomal الموسومة راثيا لأداء شاشات الوراثية للطفرات centrosomal جديدة واكتساب نظرة ثاقبة وظيفة محددة من الجينات التي تم تشخيصها حديثا.
Introduction
الخصيتين ذبابة الفاكهة هي نظام الجهاز مناسبة لدراسة مجموعة متنوعة من العمليات الخلوية والتنموية وتم استعراض نطاق واسع على مدى السنوات 1-9. يركز هذا المخطوط على استخدام الخصيتين ذبابة الفاكهة لدراسة الجسيم المركزي، وهي عضية الخلوية الحفظ. كما هو الحال في الأنظمة الأخرى، والجسيم المركزي وظيفة الخصيتين ذبابة الفاكهة في الانقسام، الانقسام الاختزالي، وتكون الأهداب 10. وتتكون Centrosomes من زوج من الهياكل القائمة على أنيبيب المعروفة باسم centrioles تحيط بها شبكة معقدة من البروتين المواد المشار إليها محيط بالمريكز باسم (PCM). ويتألف الزوج مريكز من مريكز الأم الأكبر سنا والأصغر سنا ابنة مريكز. كما تقدم الخلية نحو الانقسام، سواء centrioles فصل، مكررة، والحصول على كمية كبيرة من PCM لتشكيل نهاية المطاف اثنين centrosomes متميزة. يشار إلى الجسيم المركزي الذي يحتوي على مريكز الأم الأصلي باسم الجسيم المركزي الأم والمركيشار osome تحتوي على ابنة مريكز الأصلي على أنها ابنة الجسيم المركزي.
الخصيتين ذبابة الفاكهة مثالية لدراسة الأساس الجزيئي للبيولوجيا الجسيم المركزي بواسطة المجهر الفلورسنت لمجموعة متنوعة من الأسباب.
- يتم حفظها معظم البروتينات ذبابة الفاكهة التي مطلوبة من أجل البيولوجيا الجسيم المركزي في الخصيتين بين حقيقيات النوى، مما يوحي بأن البصيرة ذات الصلة لعلم الأحياء الجسيم المركزي في البشر والأنواع الأخرى يمكن الحصول عليها من خلال دراسة الجسيم المركزي في ذبابة الفاكهة الخصيتين 1،11-14.
- تحليل أداء متحولة في ذبابة الفاكهة يوفر ميزة كبيرة منذ ذلك الحين، على عكس العديد من النماذج الأخرى، والطفرات centrosomal في ذبابة الفاكهة ليست قاتلة الجنينية، مما يسمح للتحليل الجيني الكلاسيكية وظيفة الجسيم المركزي. هذه الميزة الفريدة لذبابة الفاكهة بسبب وجود مساهمة الأمهات التي استمرت خلال المراحل الحرجة من develo الجنينيةpment. 1،11-14. وبالتالي، يمكن للمرء أ) الطفرات الدراسة أن القضاء نهائيا على تشكيل الجسيم المركزي وب) دراسة مصير الجسيم المركزي العادية التي تشكلت في الجنين في وقت مبكر عن طريق مساهمة الأمهات في سياق متحولة بعد أن تم استنفاد مساهمة الأمهات (مبدأ الأسلوب الموضح في 11).
- تتوفر الجينات المحورة وظيفية مع العلامات الفلورية المرمزة وراثيا أن تسمية الجسيم المركزي. العديد من هذه الخطوط تستخدم المروج البروتين نفسه لدفع النسخ من التحوير من أجل منع من overexpression قوية. هذا مهم بشكل خاص لأن overexpression من البروتينات غالبا ما يؤدي إلى القطع الأثرية التي تتداخل مع وظيفة تحليل الجسيم المركزي 1،11.
- ومريكز والجسيم المركزي طويلة فريد طوال ذبابة الفاكهة الحيوانات المنوية، وبالتالي السماح للتحليل السريع والسهل من الجسيم المركزي قبل التصوير.
- خطوات متتالية في الحيوانات المنوية والجسيم المركزي بويتم تنظيم iology زمنيا على طول الخصيتين، بدءا من طرف الخصية مع centrosomes الخلايا الجذعية الحيوانات المنوية وتنتهي في أسفل الخصيتين مع انخفاض حجم الجسيم المركزي والنشاط في خلايا الحيوانات المنوية الناضجة (الشكلان 1 و 2). وهذا يسمح لسهولة تحديد وتحليل وظيفة الجسيم المركزي خلال مراحل مختلفة من التنمية الحيوانات المنوية.
- يتم تشريح الخصيتين بسهولة من يرقات الذكور، الشرانق، والكبار 27.
- خلال الحيوانات المنوية، والجسيم المركزي وcentrioles في المضي قدما من خلال التركيبية متعددة والهيكلية والوظيفية الدول لتعمل في الانقسام، الانقسام الاختزالي، وتشكيل هدب. خلال هذه العمليات، وتجميع الجسيم المركزي، التكرارات، يهاجر، والمراسي لأجزاء معينة من الخلايا، وينضج، والقسمة، ويخلق هدب. وعلاوة على ذلك، فإن مريكز من أرومة النطفة الناضجة يثير تمهيدا مريكزي يدعى PCL 1. أيضا في أرومة النطفة ناضجة، والجسيم المركزي يخضع لعملية جalled الحد الجسيم المركزي حيث أنه يفقد العديد من العناصر من PCM ومريكز (الشكلان 1 و 2). وبالتالي، دراسات في الخصيتين تسمح لأحد لمعالجة جوانب متعددة من الحياة الجسيم المركزي مثل الاحتفاظ الجسيم المركزي في الخلايا الجذعية، والازدواجية مريكز والاستقرار مريكز، واستطالة مريكز، والفصل مريكز والفصل العنصري، PCM التوظيف، وتكون الأهداب، وتشكيل PCL، والحد من الجسيم المركزي، و التنوي أنيبيب نجمي من بين آخرين.
- أخيرا، وبمساعدة دراسات البيولوجيا الجسيم المركزي قبل غيرها من الخصائص المعروفة من ذبابة الفاكهة التي جعلت من كائن النموذج المفضل للدراسات البيولوجية. وتشمل هذه فترة قصيرة جيل، وسهولة علم الوراثة، وكذلك الطفرات العشوائية وتوجه الموقع.
معا، وخصائص ذكر أعلاه من ذبابة الفاكهة الخصيتين يقدم نموذجا حيث الجسيم المركزي يمكن دراستها عن طريق سهلة وسريعة ومفصلة التصوير. التقنيات الموضحةفي هذه الورقة تم تطبيقها على تحقيق العديد من جوانب علم الأحياء الجسيم المركزي بما في ذلك تشكيل مريكز 11، الازدواجية مريكز 15، PCM تجنيد 16، وتنظيم الجسيم المركزي 17، وتكون الأهداب 18. كما تم تطبيق هذه التقنيات لدراسة الجسيم المركزي في مناطق أخرى من الأحياء مثل تنظيم الانتصافي 19، والتجمع المغزل 20، والنشاط الجسيم المركزي في انقسام الخلايا الجذعية غير المتكافئة 21 ضمن أشياء أخرى كثيرة.
التصوير من الخصيتين في بدايات الجسيم المركزي مع الحصول على الذباب التي تعبر عن البروتينات centrosomal راثيا الموسومة وعزل الخصيتين من يرقات الذكور، الشرانق، أو الذباب الكبار. تتوفر العديد من المجموعات البحثية هذه الذباب 1،11،15،22-25. الخصيتين اليرقات تحتوي على جميع مراحل تكوين الحيوانات المنوية قبل الانقسام الاختزالي ومفيدة عند تحليل الطفرات التي هي قاتلة في خادرة أو الكبار. ومع ذلك، في وقت متأخر أو العذراء أدو الشبابالخصيتين لتر هي الأكثر قوة وتحتوي على جميع مراحل ما قبل وما بعد الانتصافي من الحيوانات المنوية، مما يجعلها الأفضل للتحليل. لأن عدد الخلايا المنوية تتناقص مع العصور ذبابة، واستخدام الخصيتين الكبار هو أيضا مناسبة لدراسة الجسيم المركزي في سياق الشيخوخة 26. وهناك طريقة للخصية بمعزل عن الذباب الكبار وقد وصفت سابقا 27.
لا يمكن أن يتحقق من التصوير centrosomes وظيفتها في الخصيتين ذبابة الفاكهة عبر ثلاثة مسارات ذات الصلة التي يتم تقديمها هنا (الشكل 3). اختيار المسار الذي هو الأنسب يعتمد على طبيعة المسألة المحقق تعالج.
المسار A ينطوي على التصوير من الخصيتين الحية. هو أسرع من المسارات الثلاثة ولكن يمكن تطبيقها فقط عندما لا تحتاج العينات ليتم الحفاظ عليها وعندما المناعية غير مطلوب. في المسار A، هي التي شنت الخصيتين (سليمة، مثقوب أو قطع) على الشرائحوممرود بعناية تحت ساترة لتشكيل طبقة واحدة من الخلايا يسهل التعرف عليها. ثم يتم تصور الخلايا باستخدام المجهر على حد سواء وعلى النقيض من المرحلة المجهر الفلورسنت. استخدام على النقيض من المرحلة أهمية خاصة لتحليل الخصيتين ذبابة الفاكهة لأنه يكشف عن معلومات الخلوية التي هي غير مرئية مع أشكال أخرى من الإضاءة المنقولة وبالتالي يسمح لتحديد سريع لمراحل مختلفة من التطوير الحيوانات المنوية 28،29. ومع ذلك، المسار واثنين من العيوب الرئيسية. الأولى، في كثير من الأحيان للخطر سلامة المورفولوجية للخلايا مرة واحدة وتمزق الخصيتين. الثانية، والخلايا غير المثبتة التحرك في بعض الأحيان داخل العينة، مما يجعل التصوير من طبقات متعددة متحد البؤر داخل المنطقة المحددة صعبة. لتعزيز تحليل أنواع معينة من الخلايا، الخصيتين قد اخترقت أو قطع من أجل توجيه الطريقة التي تمزق الخصية أن مثل سحق تحت الحد الأدنى ساترة يؤثر على التشكل من نوع من الخلايا في المصالح.
المسار B ينطوي التثبيت الكيميائية من الخصيتين. هذا المسار يتطلب مبلغ وسيطة من الوقت لإعداد العينات وديه ميزة أن العينات ثابتة يمكن حفظها لتحليلها لاحقا. علاوة على ذلك، تثبيت يعمل على جعل الهياكل الخلوية أكثر جمودا، والتقليل من حركة العينة أثناء التصوير. ومع ذلك، يصبح على النقيض من المرحلة المجهري أقل بكثير بالمعلومات بعد التثبيت الكيميائية، مما يجعل بعض مراحل التنمية الحيوانات المنوية من الصعب التعرف عليها.
المسار C هي الأكثر كثافة من الوقت، ولكن له فائدة أضاف أن الهياكل الخلوية والثابتة وimmunostained، والسماح لتصور من البروتينات التي لا تتوفر مع علم الوراثة به المناسبة. هناك العديد من الأجسام المضادة المتاحة سواء تجاريا ومجموعات بحثية من مختلف المناعية للcentrosomes والهياكل ذات الصلة الجسيم المركزي في الخصيتين ذبابة الفاكهة.
Protocol
1. المسار A. إعداد الخصية لايف
- إعداد برنامج تلفزيوني عن طريق إذابة 8.0 جم كلوريد الصوديوم، 0.2 غرام بوكل، 1.44 ز نا 2 هبو 4، 0.24 غ KH 2 PO 4 في 800 مل من الماء المقطر وضبط درجة الحموضة إلى 7.4. تبرزي حجم إلى 1 L وتعقيم بواسطة التعقيم.
- عزل الخصيتين كما هو موضح سابقا 27.
- إعداد العازلة تلطيخ دابي عن طريق تمييع 1 ملغ / مل الأسهم إلى 1 ميكروغرام / مل في برنامج تلفزيوني. استخدام رقائق الألومنيوم لحماية أنبوب من الضوء وتخزينها في -20 درجة مئوية.
- بعد عزل الخصيتين، تزج العينة في 6 ميكرولتر من العازلة تلطيخ دابي على رأس شريحة المجهر والزجاج موجبة الشحنة لمدة 10 دقيقة. الخصيتين تلتزم بشكل جيد لمتاحة تجاريا الشرائح موجبة الشحنة، مما يسمح للتلاعب السهل للعينة. يتم تعديل الشرائح موجبة الشحنة تساهميا لنقل شحنة موجبة ثابتة على سطح الزجاج. مماثلة لطلاء متعدد الليزين، وهذا يشجع على التفاعل بين واي الخصيتينال سطح الشريحة.
- يغسل دابي الزائدة عن طريق استبدال العازلة تلطيخ مرتين مع 6 ميكرولتر من برنامج تلفزيوني. استخدام قطعة من ورق الترشيح لالفتيل بعيدا المخزن المؤقت بعد كل خطوة الغسيل. توخي الحذر حتى لا قصد إزالة الخصيتين جنبا إلى جنب مع المخزن المؤقت أثناء كل غسل.
- إضافة 6 ميكرولتر من برنامج تلفزيوني لعينة. ينبغي تعديل كمية من العازلة المستخدمة لحجم ساترة. وحدات التخزين المنصوص عليها في هذا البروتوكول هي ل18 × 18 مم ساترة. اختياري: ومن المستحسن أن يخترق الخصيتين بالقرب من الموقع النسبي لنوع من الخلايا في المصالح. وهذا يضمن أن هناك ضغوطا على الحد الأدنى من هذه الخلايا خلال الخطوة سحق، وبالتالي الحفاظ على سلامة الهيكلية. ثقب الخصيتين يمكن القيام بها باستخدام حاد، مشرط نظيفة.
- وضع بعناية ساترة على أعلى من العينة.
- ختم حواف ساترة باستخدام طلاء الأظافر واضحة لضمان أن المخزن المؤقت لا تتبخر من العينة الحية أثناء الدردشةالشيخوخة.
- استخدام علامة للدلالة على موقف الخصيتين لسهولة في تحديد مكان العينة على الشريحة، والشروع في التصوير.
- غسل الزائدة دابي العازلة تلطيخ عن طريق استبدال العازلة مرتين مع 6 ميكرولتر من برنامج تلفزيوني. استخدام قطعة من ورق الترشيح لالفتيل بعيدا المخزن المؤقت بعد كل خطوة الغسيل. نكون حذرين حتى لا إزالة بطريق الخطأ عينة جنبا إلى جنب مع المخزن المؤقت أثناء كل غسل.
2. المسار B. إعداد الخصية الثابتة
- إعداد العازلة فيكس عن طريق تمييع الحل الأسهم 37٪ الفورمالديهايد في برنامج تلفزيوني إلى تركيز النهائي من 3.7٪ الفورمالديهايد في برنامج تلفزيوني 1X
- إعداد العازلة تلطيخ دابي عن طريق تمييع الأسهم 1 ملغ / مل دابي إلى 1 ميكروغرام / مل في برنامج تلفزيوني.
- تزج الخصيتين في قطرة ميكرولتر من برنامج تلفزيوني 6 على رأس موجبة الشحنة شريحة المجهر والزجاج.
- توجيه الخصيتين بطريقة خطية أو كما يفضل خلاف ذلك يدويا.
- استخدام قطعة من ورق الترشيح لالفتيل بعيدا PBS واستبدالها 6 ميكرولتر من فيكسالعازلة لمدة 5 دقائق.
- استخدام قطعة من ورق الترشيح لالفتيل بعيدا المخزن المؤقت فيكس وتزج العينة في 6 ميكرولتر من العازلة تلطيخ دابي لمدة 10 دقيقة.
- وضع بعناية على 18 × 18 مم ساترة على أعلى من العينة.
- ختم حواف ساترة باستخدام طلاء الأظافر واضحة لضمان أن المخزن المؤقت لا تتبخر من العينة في حين التصوير.
- استخدام علامة للدلالة على موقف الخصيتين لسهولة في تحديد مكان العينة على الشريحة، والشروع في التصوير.
3. المسار C. إعداد Immunostained الخصية
siliconization ساترة: تزج متعددة 18 × 18 مم coverslips في علبة صغيرة تحتوي على محلول siliconizing واحتضان لمدة 1 دقيقة في درجة حرارة الغرفة تحت غطاء الدخان. تأكد من أن لل coverslips يتعرضون بشكل كامل وغير مكدسة فوق بعضها البعض.
- وضع العينة في قطرة ميكرولتر من برنامج تلفزيوني على 5 ساترة siliconized. توجيه والخصيتين كما تريد ويخترق الخصيتين باستخدام مشرط حاد. وضع بلطف موجبة الشحنة شريحة المجهر والزجاج على ساترة، والسماح للبرنامج تلفزيوني لتصبح فرقت بالتساوي بين ساترة والشريحة. استخدام قطعة صغيرة من ورق الترشيح لالفتيل بعيدا المخزن المؤقت الزائدة بين ساترة والشريحة. كما تتم إزالة المنطقة العازلة التي كتبها ورقة الترشيح، فإن الزيادة في ضغط الاسكواش الخصيتين. وينبغي إعداد العديد من العينات في وقت واحد، كما أن البعض قد يكون المفقودة أو التالفة على مدار البروتوكول. A حفارة الزجاج يمكن استخدامها لتسمية الشرائح إذا كان سيتم إعداد أنواع مختلفة من العينات في وقت واحد.
- غسل coverslips 3X لمدة 1 دقيقة في كل من المياه، تليها 3X لمدة 1 دقيقة في كل من 70٪ من الإيثانول، وغسل النهائي لمدة 1 دقيقة في الماء. السماح لل coverslips siliconized إلى الهواء الجاف تحت غطاء الدخان.
- إسقاط الشرائح في النيتروجين السائل وتسمح العينة لتجميد لمدة 5-10 دقيقة.
- إزالة الشرائح من لiquid النيتروجين باستخدام ملقط كبير. استخدام مشرط لإزالة بسرعة ساترة. يجب أن تبقى العينة على الشريحة. يجب الحرص على عدم تشويه العينة أثناء هذه العملية عن طريق تحريك ساترة على طول الشريحة.
- احتضان الشرائح في الميثانول prechilled في كوب Coplin جرة تلطيخ في -20 درجة مئوية لمدة 15 دقيقة.
- نقل الشرائح إلى الزجاج جرة تحتوي على Coplin تلطيخ الأسيتون prechilled في -20 درجة مئوية لمدة 30 ثانية.
- تغسل الشرائح لمدة 1 دقيقة في برنامج تلفزيوني في درجة حرارة الغرفة باستخدام الزجاج جرة Coplin تلطيخ.
- إعداد PBST-B من خلال استكمال برنامج تلفزيوني مع 0.1٪ تريتون-X100 و 1٪ مصل بقري البياض (BSA). 5٪ مصل طبيعي من الأنواع المضيفة نفس الأجسام المضادة الثانوية (من الخطوة 3.14) يمكن أن تستخدم بدلا من BSA للحد من الضوضاء في الخلفية غير محددة تنتج من الأجسام المضادة الثانوية ملزمة.
- احتضان الشرائح لمدة 10 دقيقة في PBST-B في تلطيخ عاء زجاجي Coplin للحجب المواقع غير محددة.
- ملء آبارغرفة الرطوبة بالماء. سوف الرطوبة داخل غرفة تقليل التبخر من الحلول الضد من العينة خلال الخطوات الحضانة.
- إعداد PBST-BR من خلال استكمال PBST-B مع 100 ميكروغرام / مل ريبونوكلياز ريبونوكلياز A. A يحط الحمض النووي الريبي في العينة وأيضا بمثابة وكيل حجب إضافية من خلال استيعاب بقوة على سطح الزجاج.
- وضع قطعة 1X1 سم تقريبا من parafilm على رأس العينة لنشر الحل الضد بالتساوي وحماية حل الضد من التبخر. إغلاق غرفة الرطوبة واحتضان العينة في الأجسام المضادة الأولية لمدة 1 ساعة في درجة حرارة الغرفة.
- إزالة الشرائح من PBST-B. استخدام قطعة من ورق الترشيح لتجفيف المنطقة من الشريحة حول العينة، باستخدام الحذر لا تجف العينة نفسها. أخيرا، ضع الشريحة في غرفة الرطوبة مع العينة مواجهة
- بلطف إضافة 100 ميكرولتر من الأجسام المضادة الأولية مخففة في PBST-BR على أعلى المواصفاتإيمان (1:200 عموما هو تركيز الأجسام المضادة انطلاق جيدة لuncharacterized).
- تغطية العينة مع ما يقرب من 1 × 1 سم قطعة من parafilm وإغلاق غرفة الرطوبة. احتضان العينة في الضد الثانوية لمدة 1 ساعة في درجة حرارة الغرفة.
- فتح غرفة الرطوبة واستخدام الملقط لإزالة بلطف Parafilm من الشريحة. احتضان الشرائح لمدة 5 دقائق في PBST في تلطيخ عاء زجاجي Coplin في درجة حرارة الغرفة لغسل. كرر هذه العملية ما مجموعه ثلاثة يغسل.
- إزالة الشرائح من PBST-B ووضعها في غرفة الرطوبة مع العينة مواجهة. بلطف إضافة 100 ميكرولتر من الأجسام المضادة الثانوية مخففة في PBST-BR على أعلى من العينة.
- فتح غرفة الرطوبة واستخدام الملقط لإزالة بلطف Parafilm من الشريحة. مرة أخرى، وغسل 3X العينة لمدة 5 دقائق في كل من PBST في تلطيخ عاء زجاجي Coplin تليها 3X لمدة 5 دقائق كل في برنامج تلفزيوني.
- استخدام Kimwipe ورقة الترشيح ل تجف بعناية سطح الشريحة، والحرص على تجنب لمس أو تجفيف العينة.
- إضافة 6 ميكرولتر من تركيب وسائل الإعلام لعينة، مع تغطية ساترة نظيفة (غير المغلفة مع السيليكون)، وختم حواف مع طلاء الأظافر.
- استخدام علامة للدلالة على موقف الخصيتين لسهولة في تحديد مكان العينة على الشريحة، والشروع في التصوير.
4. التصوير ملاحظات
لا يمكن أن يتحقق التصوير باستخدام مجهر الضوء العادي تستقيم أو مقلوب أو المجهر متحد البؤر. من المهم أن تكون مجهزة المجهر مع مرحلة النقيض من ذلك، خاصة بالنسبة للتصوير الخصيتين الحية العينات (المسار A). أصبحت هذه الميزة متوفرة في الآونة الأخيرة المجاهر متحد البؤر.
عندما كسر الخصيتين بشكل عفوي (المسار A)، الطرف (الجذعية المنطقة الخلية) وعادة ما يتم الحفاظ عليه ويسهل التعرف عليها، وتوفير علامة جيدة لتحديد مكان واستخدامها في التوجه في البداية.
_content "> Centrioles هي هياكل صغيرة إلى حد ما، وبالتالي ينبغي أن تؤخذ الصور باستخدام 63X أو 100X أهداف، وهو عامل التكبير من 4 6X، والقرار 512 على الأقل 512 بكسل العاشر عندما يكون ذلك ممكنا.النتائج
Centrosomes الخضوع متعددة التحولات المورفولوجية والوظيفية على مدار الحيوانات المنوية. هذه الخاصية يجعل الحيوانات المنوية الخصيتين نظام مفيد لدراسة مختلف جوانب علم الأحياء الجسيم المركزي. واحدة من هذه العملية بسهولة لاحظ هو استطالة الجسيم المركزي. في أمهات المني، علامة مريكزي Ana1-GFP يصادف (4A الشكل) 0.6 ميكرون مريكز طويلة. هذا مريكز يستطيل خلال الحيوانات المنوية ويبلغ طولها 2.5 ميكرومتر في طلائع منوية ناضجة تقريبا. منذ centrioles في ذبابة الفاكهة الحيوانات المنوية هي طويلة بشكل فريد، والتصوير يمكن أن تستخدم لجعل البيانات الكمية المتعلقة استطالة الجسيم المركزي (الشكل 4B). ويمكن أيضا تحليل طول مريكز أن يؤديها في خلفية متحولة وتم تحديدها مختلف المسوخ التي تغير النمو مريكز (الشكل 5). الأمثلة هي دائما في وقت مبكر (ALY) وتسديدة صاروخية (يمكن)، والطفرات التي عراسر الحيوانات المنوية قبل بدء الانقسام الاختزالي 30 ولكن لا تحجب مريكز استطالة. في هذه المسوخ، centrioles منوية ناضجة من النمو إلى حوالي 2.4 ميكرومتر ~ مقارنة centrioles من الخلايا السيطرة التي تصل بحد أقصى 1.8 ميكرون.
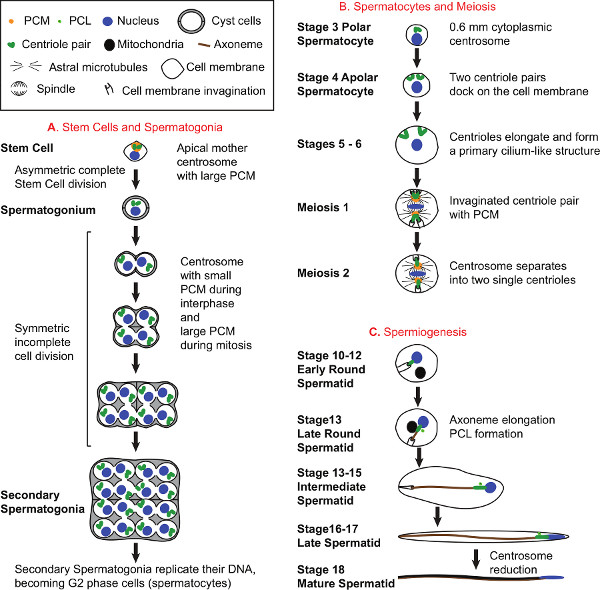
الشكل 1. الحيوانات المنوية والبيولوجيا الجسيم المركزي. أ) تطوير الخلايا الجذعية وأمهات المني. جميع الخلايا المنوية تنشأ من الخلايا الجذعية الموجودة في الطرف القمي من الخصيتين. يقسم كل الخلايا الجذعية غير متماثلة لتشكيل الخلايا الجذعية أن يرث الجسيم المركزي أم وspermatogonium السلف يرث ابنة الجسيم المركزي 31. كما شكل أمهات المني، فإنها تصبح محاطة 2 خلايا الكيس، التي لا تزال تحيط الخلايا المنوية والحيوانات المنوية في جميع أنحاء طلائع منوية. أمهات المني الفجوة 4 مرات لإنتاج 16 أمهات المني، كل منها يحتوي على اثنين centrioles. ب) تطوير الخلايا المنوية والانقسام الاختزالي. أثناء تطوير منوية، centrioles تكرار مرة أخرى لتوليد أربعة centrioles تنظيمها في اثنين من أزواج لكل خلية و 64 centrioles في الكيس. في وقت مبكر خلال تطوير منوية، كل مريكز ينتقل إلى غشاء البلازما، والاحواض لذلك، ويستطيل لتشكيل هيكل يشبه هدب الأولية 18،32-34. في الخلايا المنوية الناضجة، وطول يصل مريكز ~ 1.8 ميكرون. وcentrosomes تلعب دورا أساسيا في الانقسام الاختزالي. أثناء الانقسام الاختزالي الأول، أزواج مريكز التي لا تزال تعلق على غشاء البلازما الخطوة نحو مركز الخلية، وخلق خلية غشاء invaginations في تلميح بهم القاصي. وPCM حول centrioles ينمو، nucleates الأنابيب الدقيقة نجمي، وcolocalizes مع قطب المغزل. أثناء الانتقال إلى الانقسام الاختزالي الثاني، الزوج مريكز يفصل بحيث يتم حاضرا سوى مريكز واحدر في كل قطب المغزل. C) تكون النطاف. في نهاية الانقسام الاختزالي الثاني، وأرومة النطفة جولة في وقت مبكر لديها مريكز واحدة تعلق على غشاء البلازما invaginated. تم العثور على المشتقة الميتوكوندريا جولة كبيرة بالقرب من النواة ويبدأ في وقت لاحق إلى استطال على طول الخيط المحوري المتزايد في وقت لاحق طلائع منوية جولة. خلال الحيوانات المنوية، وأشكال الخيط المحوري ويستطيل داخل السيتوبلازم. بالإضافة يظهر هيكل مريكزي الجديدة المعروفة باسم PCL (الدانية مريكز مثل) بالقرب من مريكز قبل الإيجاد 1. في نهاية الحيوانات المنوية، والخلايا تقاسم كيس مشتركة منفصلة عن بعضها البعض لتصبح الحيوانات المنوية متحركة ناضجة تماما. المخططات التنمية منوية (B) وتكون النطاف (C) تصور خلية واحدة فقط من أصل 16 المنوية وطلائع منوية 64، على التوالي في الكيس، وليس لتصوير الخلايا الكيس. اضغط هنا لمشاهدة كبيرة الرقم ص.
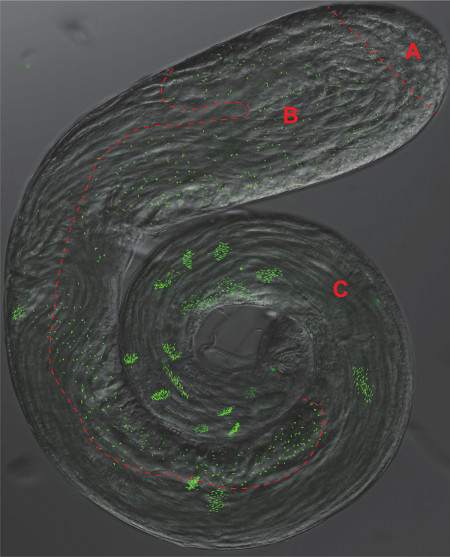
الشكل 2. ذبابة الفاكهة الخصية. تراكب من مرحلة التباين وGFP مضان صورة مجهرية من الخصية كله جبل معربا عن علامة عموم مريكزي آنا-1-GFP. يتم فصل منطقة متميزة المقابلة لوحات 1-3 من الشكل 1 بواسطة خط أحمر متقطع A) الخلايا الجذعية وأمهات المني، B) والخلايا المنوية الانقسام الاختزالي، C) تكون النطاف.
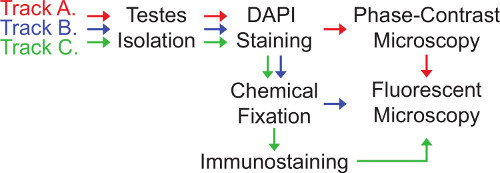
الرقم 3. يتابع نحو التصوير Centrosomes في ذبابة الفاكهة الخصية.
: together.within المحافظة على صفحة = "دائما"> 
الشكل 4. الجسيم المركزي الاستطالة خلال الحيوانات المنوية. A) يظهر كل مرحلة صورة على النقيض من المرحلة (يسار)، وصورة مضان (وسط)، وصورة مكبرة من الجسيم المركزي (يمين). يوضح الصورة على النقيض من المرحلة مرحلة خلية معينة استنادا إلى موقف ومورفولوجية الخلية، النواة، نوية، والميتوكوندريا. يظهر صورة مضان الحمض النووي ملطخة دابي (الأزرق). يظهر الصورة الجسيم المركزي centrosomes صفت من قبل Asterless-GFP (الاصل، وأعلى صور) وAna1-GFP (Ana1، الصورة أسفل). دائرة بيضاء يسلط الضوء على غشاء الخلية في كل مرحلة التباين ومضان الصور. الدوائر البيضاء متقطع والدائرة الرمادية في الصورة مضان تسليط الضوء على موقف نواة ونوية، على التوالي. يشير السهم الأصفر إلى الصبغي Y-بعض الحلقات. أحمر متقطع الدوائر بمناسبة الميتوكوندريا. المراحل 1-6 يشير إلى 29 ومراحل 13-17 يشير إلى وصف مراحل خلية في 32. المرحلة 1: منوية الابتدائية. التعرف على خلية صغيرة غيض من الخصية. المرحلة 2A: القطبية منوية. التي حددتها وجود غطاء الميتوكوندريا على جانب واحد من النواة. المرحلة 3: عديم الأقطاب منوية. النسبية التي حددها لها حجم أكبر من منوية الأولية وعدم وجود غطاء الميتوكوندريا. المرحلة 4: منوية الابتدائية. التي حددها ظهور جميع: كل 3 حلقات Y كروموسوم. المرحلة 5: منوية ناضجة الابتدائية. أكبر منوية أنتجت في الحيوانات المنوية التي تحمل لزيادة أخرى في حجم النووية. المرحلة 6: منوية السابق للانتصاف الابتدائية. الحلقات Y كروموسوم تتفكك وتختفي النواة. المرحلة 13: البصل المرحلة أرومة النطفة. خلية تحتوي على نواة مستديرة متساوية الحجم والميتوكوندريا. المرحلة 17: أرومة النطفة في وقت متأخر. حددت باعتبارها أرومة النطفة ممدود التي لا تزال جزءا من bundl(ه) من 64 طلائع منوية مع نوى وجدت بالقرب من قاعدة الخصيتين.، نواة أوسع قليلا من طلائع منوية ناضجة وجدت في الحويصلة المنوية. أشرطة النطاق، 10 ميكرومتر و 1 ميكرومتر. B) رسم بياني يصور المتوسط والانحراف المعياري لكل مرحلة مقاسا Asterless-GFP (الازرق) وAna1-GFP (الخضراء). في المرحلة 6، Asterless-GFP (الازرق) وAna1-GFP (الخضراء) المتوسطات والانحرافات المعيارية وتتداخل فقط Asterless-GFP (الأزرق) هو واضح. ابتداء من الساعة 13 مرحلة، Asterless-GFP لا تزيين مريكز كله ولم يحدد القياسات (ND).
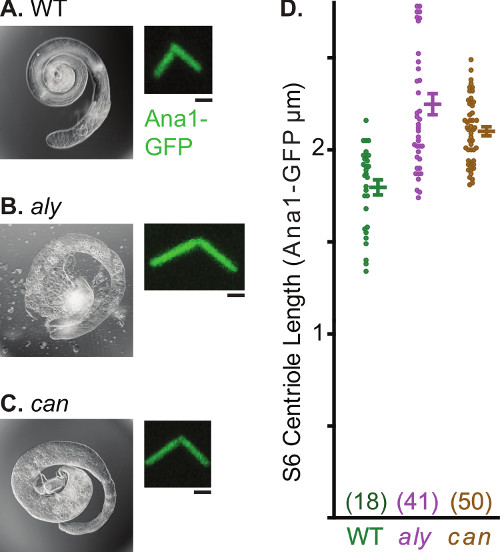
الرقم 5. Centrioles طويلة بشكل غير طبيعي في المرحلة 6 من الخلايا المنوية على وسعها المسوخ. AC) صورة مجهرية ضوء الخصيتين كله ولوحة الفلورسنت من ممثل الجسيم المركزي لاbeled بواسطة Ana1-GFP. لاحظ شكل غير طبيعي في الخصيتين في وسعها على المسوخ، والذي ينتج من نقص طلائع منوية نتيجة لاعتقال الانتصافي. D) رسم بياني يصور المتوسط، الانحراف المعياري، وتوزيع البيانات من طول مريكز في البرية من نوع، ويمكن على . عدد العينة لكل نقطة بيانات في أقواس. شريط النطاق، 1 ميكرون.
Discussion
دراسة البيولوجيا الجسيم المركزي في الخصيتين الطاير باستخدام علامات centrosomal الموسومة راثيا هو طريقة مفيدة لتقييم وظيفة الجسيم المركزي والنشاط في كل من النوع البري ومتحولة السياق. على وجه الخصوص، والمسار هو مناسبة لفحص السريع للشذوذ centrosomal مثل تشوه، misegregation، وعدم الاستقرار، أو طول غير طبيعي في محاولة لتحديد طفرات جديدة. علاوة على ذلك، أهداب أرومة النطفة في الأعمال التحضيرية الحية تبقى متحركة لحوالي 15 دقيقة بعد تشريح واستخدام الخصيتين يعيش في المسار A كما يسمح للالحيوانات المنوية على الحركة أن تعالج بسهولة. منذ نشاط الحيوانات المنوية أهداب متحركة يرتبط مباشرة إلى وظيفة الجسيم المركزي، لا يمكن أن يؤديها المقايسات لتحديد آثار الطفرات المختلفة centrosomal على وظيفة الهدبية. المسار B يمكن استخدامها لملاحظات أكثر تحديدا وخاصة عندما يكون مطلوبا البيانات الإحصائية مثل لإحصاء عدد centrioles لكل خلية وأو عدد الخلايا في الكيس. المسار C هو الأكثر usefuلتر بالنسبة للملاحظات التفصيلية التي تتطلب تلطيخ مع الأجسام المضادة. وتشمل الأمثلة وضع العلامات من نوع خلية معينة مثل الخلايا الجذعية، وتلطيخ من البروتين الذي ليس لديه علامة المتاحة مثل تويولين الأسيتيل، أو للتحقق من عدم وجود أو mislocalization من البروتين في متحولة.
عند التصوير centrosomes والهياكل ذات الصلة الجسيم المركزي، وذلك باستخدام علامات وراثيا الموسومة بدلا من الأجسام المضادة ليست فقط أسهل تجريبيا، ولكن أيضا يوفر نتائج أكثر قوة واستنساخه. ولذا، فإن استخدام البروتينات centrosomal الموسومة راثيا هو نهج يمكن الاعتماد عليها لتحليل الآلية والكمية التي تتطلب مجموعة البيانات الكبيرة. على سبيل المثال، فقد تم استخدام علامات centrosomal الموسومة راثيا ذات قيمة خاصة لتقدير حجم طول مريكز. وقد كشف هذا التحليل أن مختلف الطفرات يمكن تصنيفها إلى فئتين استنادا إلى التباين في طول مريكز. وتشمل فئة واحدة الطفرات التي تشانجنرال الكتريك طول مريكز ولكن لا تؤثر على الانحراف المعياري 1 والفئة الأخرى تشمل الطفرات التي تؤثر على كل من طول مريكز والانحراف المعياري في الطول 11. يمكن لمثل هذه البيانات الكمية توفر نظرة متعمقة مفيدة في وظيفة معينة الجينات centrosomal. قد يكون راجعا إلى زعزعة استقرار هيكل مريكزي المسوخ Centrosomal الذي يحمل عيب طول مريكز مع زيادة في الانحراف المعياري. ومع ذلك، معيبة طول مريكز مع الخطأ المعياري العادي قد يشير إلى أن الطفرات لا هيكليا في زعزعة استقرار مريكز وعلى الأرجح أن ذلك يعود إلى تغير في آلية تنظيمية السيطرة على طول مريكز. بسبب التضارب في المناعية، التحليلات الكمية هي صعبة مع استخدام علامات الأجسام المضادة وحدها.
والجسيم المركزي هو كبير وبناء البروتينية المعقدة والكثير من البروتينات التي لا توجد إلا في باطنها. باستخدام centrosomal راثيا الموسومةعلامات بدلا من الأجسام المضادة يسمح احد لتسمية باستمرار المكونات الداخلية للالجسيم المركزي الذي لا يمكن الوصول إليها إلا قد يكون لعلامات الضد الحواتم. على سبيل المثال، ودراسات توطين BLD10 باستخدام الأجسام المضادة يجد البروتين لتخصيبه في نهايات القاصي والداني من مريكز 13، في حين يظهر BLD10-GFP توزيع أكثر اتساقا 1. ومع ذلك، فمن المهم أيضا النظر في مستوى التعبير عن بروتين معين وراثيا الموسومة، وهذا يمكن أن يؤثر على توزيع البروتين. أعرب توطين ساس-4-GFP وSAS-6-GFP تحت الوطنية لديها يقتصر على الغايات القريبة من مريكز 1،16،35 ومن ناحية أخرى، أعرب ساس-4-GFP وSAS-6-GFP تحت يتم ترجمة المروج اليوبيكويتين قوية على طول من مريكز 12،14. هناك اعتبار آخر مهم هو تأثير العلامة الجينية على وظيفة البروتين. يمكن تحليل البروتينات الموسومة إذا وراثيا وظيفية تكون الاحصائيينتيد عن طريق إدخال البروتين المعدلة وراثيا الى خلفية متحولة ودراسة ما إذا كان البروتين المعدلة وراثيا النمط الظاهري ينقذ متحولة.
تثبيت الخصيتين من ذبابة الفاكهة يمكن القيام بها باستخدام مجموعة متنوعة من مثبتات كيميائية. هنا، نحن تصف التثبيت مع كل من الفورمالديهايد (المسار B) والميثانول، الأسيتون (المسار C). ومع ذلك، إما تثبيتي يمكن استخدامها بالتبادل، ومنذ عدة مثبتات قد يعطل كيميائيا الحواتم الأجسام المضادة الأم، يجب تحديد اختيار المناسب لتثبيتي المناعية تجريبيا. ومثبتات التالية وشروط الحضانة وتستخدم عادة: 3.7٪ الفورمالديهايد، 5 دقائق في درجة حرارة الغرفة؛ الميثانول، 15 دقيقة عند درجة حرارة -20 درجة مئوية، الأسيتون، 10 دقيقة عند درجة حرارة -20 درجة مئوية، والميثانول، و15 دقيقة في -20 درجة مئوية. تليها الأسيتون، 30 ثانية عند درجة حرارة -20 درجة مئوية؛ الإيثانول، 20 دقيقة عند درجة حرارة -20 درجة مئوية. على الرغم من أن التثبيت مع الأسيتون، والميثانول، والإيثانول لا تتطلب خطوة permeabilization الموسعة لالمناعية، واي التثبيتوينبغي اتباع ال الفورمالديهايد قبل 1 ساعة حضانة في PBST-B في درجة حرارة الغرفة لpermeabilize أغشية الخلايا وتسمح بالوصول إلى الضد الحواتم داخل الخلايا. وعلاوة على ذلك، فإن بعض مثبتات هي أكثر ملاءمة لمستضدات معينة. على سبيل المثال، وظائف الفورمالديهايد جيدا لتثبيت البروتينات الصغيرة، في حين الميثانول والأسيتون هي مناسبة تماما للتثبيت من المجمعات الجزيئية كبيرة 36.
وقد المناعية من ذبابة الفاكهة الخصيتين سابقا صفها لمراقبة الهياكل ونين وأنيبيب الهيكل الخلوي 29،37. هنا (المسار C)، وقد تم تحسين الإجراء لتحليل الهياكل التي تحتوي على البروتينات الموسومة centrosomal وراثيا. نحن نقدم وصفا مفصلا لهذا الإجراء لتوجيه الأفراد الذين يفتقرون إلى الخبرة في العمل في الخصيتين ذبابة الفاكهة. ويشمل هذا الإجراء أيضا تعديلات لتحسين الحفظ والتشكل من الخصيتين، مثل باستخدام قiliconized coverslips وموجبة الشحنة شرائح المجهر الزجاجية.
Disclosures
وأيد حرية الوصول إلى هذا المنشور من قبل لايكا مايكروسيستمز.
Acknowledgements
وأيد هذا العمل من خلال منحة (R01GM098394) من المعاهد الوطنية للصحة والمعهد الوطني للعلوم الطبية العامة وكذلك منحة 1121176 من المؤسسة الوطنية للعلوم.
Materials
| Name | Company | Catalog Number | Comments |
| DAPI | Invitrogen | D1306 | |
| Positively Charged Slides | AZER Scientific | EMS200A+ | |
| Feather Microscalpel | Electron Microscopy Sciences | 72045-30 | |
| 37% Formaldehyde or Paraformaldehyde | Fisher Scientific | BP531-500 | |
| Phosphate Buffered Saline (PBS) | Boston Bioproducts | BM-220 | |
| 18x18 mm coverslips number 1.5 | VWR | 48366 205 | |
| Nail Polish | Electron Microscopy Sciences | 72180 | |
| Sigmacote | Sigma-Aldrich | SL2-100 ml | |
| Methanol | Fisher Scientific | A412-4 | |
| Acetone | Fisher Scientific | A949-1 | |
| Triton-X100 | Sigma-Aldrich | T9284-100ML | |
| BSA | Jackson ImmunoResearch | 001-000-162 | |
| RNAse A | 5 prime | 2900142 | |
| Filter paper | Whatman | 1001-055 | |
| Glass engraver | Dremel | 290-01 | |
| TCS SP5 confocal microscope | Leica | ||
| Mounting Media | Electron Microscopy Sciences | 17985-10 | |
| Immuno Stain Moisture Chamber, Black | Electron Microscopy Sciences | 62010-37 | |
| Glass Coplin Staining Jar, Screw Cap | Electron Microscopy Sciences | 70315 |
References
- Blachon, S., et al. A proximal centriole-like structure is present in Drosophila spermatids and can serve as a model to study centriole duplication. Genetics. 182, 133-144 (2009).
- Hennig, W. Spermatogenesis in Drosophila. The International journal of developmental biology. 40, 167-176 (1996).
- Fabian, L., Brill, J. A. Drosophila spermiogenesis: Big things come from little packages. Spermatogenesis. 2, 197-212 (2012).
- White-Cooper, H. Molecular mechanisms of gene regulation during Drosophila spermatogenesis. Reproduction. 139, 11-21 (2010).
- Davies, E. L., Fuller, M. T. Regulation of self-renewal and differentiation in adult stem cell lineages: lessons from the Drosophila male germ line. Cold Spring Harb Symp Quant Biol. 73, 137-145 (2008).
- Belote, J. M., Zhong, L. Duplicated proteasome subunit genes in Drosophila and their roles in spermatogenesis. Heredity. 103, 23-31 (2009).
- Xiao, X., Yang, W. X. Actin-based dynamics during spermatogenesis and its significance. Journal of Zhejiang University. Science. B. 8, 498-506 (2007).
- Hennig, W. Chromosomal proteins in the spermatogenesis of Drosophila. Chromosoma. 111, 489-494 (2003).
- Wakimoto, B. T. Doubling the rewards: testis ESTs for Drosophila gene discovery and spermatogenesis expression profile analysis. Genome research. 10, 1841-1842 (2000).
- Avidor-Reiss, T., Gopalakrishnan, J. Building a centriole. Curr Opin Cell Biol. , (2012).
- Blachon, S., et al. Drosophila asterless and vertebrate Cep152 Are orthologs essential for centriole duplication. Genetics. 180, 2081-2094 (2008).
- Basto, R., et al. Flies without Centrioles. Cell. 125, 1375-1386 (2006).
- Mottier-Pavie, V., Megraw, T. L. Drosophila bld10 is a centriolar protein that regulates centriole, basal body, and motile cilium assembly. Mol Biol Cell. 20, 2605-2614 (2009).
- Rodrigues-Martins, A., et al. DSAS-6 Organizes a Tube-like Centriole Precursor, and Its Absence Suggests Modularity in Centriole Assembly. Curr Biol. 17, 1465-1472 (2007).
- Stevens, N. R., Dobbelaere, J., Brunk, K., Franz, A., Raff, J. W. Drosophila Ana2 is a conserved centriole duplication factor. J Cell Biol. 188, 313-323 (2010).
- Gopalakrishnan, J., et al. Sas-4 provides a scaffold for cytoplasmic complexes and tethers them in a centrosome. Nat Commun. 2, 359 (2011).
- Gopalakrishnan, J., et al. Tubulin nucleotide status controls Sas-4-dependent pericentriolar material recruitment. Nat Cell Biol. 14, 865-873 (2012).
- Riparbelli, M. G., Callaini, G., Megraw, T. L. Assembly and persistence of primary cilia in dividing Drosophila spermatocytes. Dev Cell. 23, 425-432 (2012).
- Maines, J. Z., Wasserman, S. A. Post-transcriptional regulation of the meiotic Cdc25 protein Twine by the Dazl orthologue Boule. Nat Cell Biol. 1, 171-174 (1999).
- Herrmann, S., Amorim, I., Sunkel, C. E. The POLO kinase is required at multiple stages during spermatogenesis in Drosophila melanogaster. Chromosoma. 107, 440-451 (1998).
- Yamashita, Y. M., Jones, D. L., Fuller, M. T. Orientation of asymmetric stem cell division by the APC tumor suppressor and centrosome. Science. 301, 1547-1550 (2003).
- Dix, C. I., Raff, J. W. Drosophila Spd-2 Recruits PCM to the Sperm Centriole, but Is Dispensable for Centriole Duplication. Curr Biol. , (2007).
- Stevens, N. R., Dobbelaere, J., Wainman, A., Gergely, F., Raff, J. W. Ana3 is a conserved protein required for the structural integrity of centrioles and basal bodies. J Cell Biol. 187, 355-363 (2009).
- Giansanti, M. G., Bucciarelli, E., Bonaccorsi, S., Gatti, M. Drosophila SPD-2 Is an Essential Centriole Component Required for PCM Recruitment and Astral-Microtubule Nucleation. Curr Biol. , (2008).
- Januschke, J., Llamazares, S., Reina, J., Gonzalez, C. Drosophila neuroblasts retain the daughter centrosome. Nat Commun. 2, 243 (2011).
- Cheng, J., et al. Centrosome misorientation reduces stem cell division during ageing. Nature. 456, 599-604 (2008).
- Zamore, P. D., Ma, S. Isolation of Drosophila melanogaster testes. J. Vis. Exp. , e2641 (2011).
- Fuller, M. T., Bate, M., Martinez-Arias, A. . The Development of Drosophila melanogaster. , 71-174 (1993).
- Cenci, G., Bonaccorsi, S., Pisano, C., Verni, F., Gatti, M. Chromatin and microtubule organization during premeiotic, meiotic and early postmeiotic stages of Drosophila melanogaster spermatogenesis. J Cell Sci. . 107 (Pt. 12), 3521-3534 (1994).
- White-Cooper, H., Schafer, M. A., Alphey, L. S., Fuller, M. T. Transcriptional and post-transcriptional control mechanisms coordinate the onset of spermatid differentiation with meiosis I in Drosophila. Development. 125, 125-134 (1998).
- Yamashita, Y. M., Mahowald, A. P., Perlin, J. R., Fuller, M. T. Asymmetric inheritance of mother versus daughter centrosome in stem cell division. Science. 315, 518-521 (2007).
- Tates, A. D. . Cytodifferentiation during Spermatogenesis in Drosophila melanogaster: An Electron Microscope Study. , (1971).
- Baker, J. D., Adhikarakunnathu, S., Kernan, M. J. Mechanosensory-defective, male-sterile unc mutants identify a novel basal body protein required for ciliogenesis in Drosophila. Development. 131, 3411-3422 (2004).
- Avidor-Reiss, T., Gopalakrishnan, J., Blachon, S., Polyanovsky, A., Schatten, H. . The Centrosome: Cell and Molecular Mechanisms of Functions and Dysfunctions in Disease. , (2012).
- Gopalakrishnan, J., et al. Self-assembling SAS-6 multimer is a core centriole building block. J Biol Chem. 285, 8759-8770 (2010).
- Hassell, J., Hand, A. R. Tissue fixation with diimidoesters as an alternative to aldehydes. I. Comparison of cross-linking and ultrastructure obtained with dimethylsuberimidate and glutaraldehyde. The journal of histochemistry and cytochemistry : official journal of the Histochemistry Society. 22, 223-229 (1974).
- Pisano, C., Bonaccorsi, S., Gatti, M. The kl-3 loop of the Y chromosome of Drosophila melanogaster binds a tektin-like protein. Genetics. 133, 569-579 (1993).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved