A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
فصل كبريتات التي كتبها الانتقائية تبلور مع يجند مكرر iminoguanidinium
In This Article
Summary
ويرد بروتوكول لفي تركيب مائي الموقعي ل(iminoguanidinium) يجند مكررا، واستخدامه في فصل الانتقائي للكبريتات.
Abstract
A simple and effective method for selective sulfate separation from aqueous solutions by crystallization with a bis-guanidinium ligand, 1,4-benzene-bis(iminoguanidinium) (BBIG), is demonstrated. The ligand is synthesized as the chloride salt (BBIG-Cl) by in situ imine condensation of terephthalaldehyde with aminoguanidinium chloride in water, followed by crystallization as the sulfate salt (BBIG-SO4). Alternatively, BBIG-Cl is synthesized ex situ in larger scale from ethanol. The sulfate separation ability of the BBIG ligand is demonstrated by selective and quantitative crystallization of sulfate from seawater. The ligand can be recycled by neutralization of BBIG-SO4 with aqueous NaOH and crystallization of the neutral bis-iminoguanidine, which can be converted back into BBIG-Cl with aqueous HCl and reused in another separation cycle. Finally, 35S-labeled sulfate and β liquid scintillation counting are employed for monitoring the sulfate concentration in solution. Overall, this protocol will instruct the user in the necessary skills to synthesize a ligand, employ it in the selective crystallization of sulfate from aqueous solutions, and quantify the separation efficiency.
Introduction
يمثل فصل الانتقائي للoxoanions محبة للماء (على سبيل المثال، كبريتات، الكروم والفوسفات) من المحاليل المائية تنافسية تحديا أساسيا مع أهميتها لإصلاح البيئة وإنتاج الطاقة، وصحة الإنسان. 1،2 كبرت على وجه الخصوص يصعب استخراجها من المياه نظرا ل تردد جوهري لتسليط مجال الماء وتهاجر إلى البيئات القطبية أقل. 3 جعل استخراج كبريتات مائي أكثر كفاءة وعادة ما يتطلب مستقبلات المعقدة التي يصعب ومملة لتجميع وتنقية، وغالبا ما تنطوي الكواشف السامة والمذيبات. 4،5
تقدم بلورة الانتقائية بديل بسيطة لكنها فعالة لكبريتات فصل من الماء 6-9 على الرغم من بعض الكاتيونات المعدنية مثل با 2+، والرصاص 2+، أو را 2+ شكل أملاح الكبريتات غير قابلة للذوبان جدا، واستعمالها في فصل كبريتات ليس عمليا دائما بسبب TOXI العاليةالمدينة ومنخفضة أحيانا الانتقائية. توظيف بروابط العضوية ومسببات الكبريتات يستفيد من التنوع الهيكلي وقابليته لتصميم مميزة لجزيئات عضوية. ينبغي أن يكون يجند العضوية المثالي لبلورة كبريتات المائية القابلة للذوبان في الماء، وبعد تشكل الملح كبريتات غير قابلة للذوبان أو معقدة في وقت قصير نسبيا وفي وجود تركيزات عالية من الأيونات المتنافسة. بالإضافة إلى ذلك، يجب أن يكون من السهل تجميع وإعادة التدوير. واحدة من هذه ليجند، 1،4-البنزين مكرر (iminoguanidinium) (BBIG)، في الموقع من اثنين السلائف المتاحة تجاريا، terephthalaldehyde وكلوريد aminoguanidinium الذاتي تجميعها، وقد عثر عليها مؤخرا لتكون فعالة للغاية في فصل كبريتات مائي. 10 يجند في شكل كلوريد للذوبان في الماء، ويبلور بشكل انتقائي مع كبريتات إلى الملح غير قابلة للذوبان للغاية التي يمكن إزالتها بسهولة من الحل عن طريق الترشيح بسيط. يجند BBIG ومن ثم يمكن استردادها عن طريق نزع بروتون معqueous هيدروكسيد الصوديوم وتبلور محايدة مكرر iminoguanidine، والتي يمكن تحويلها مرة أخرى إلى شكل كلوريد مع مائي حمض الهيدروكلوريك، وإعادة استخدامها في دورة فصل آخر. فعالية هذا يجند في إزالة كبريتات من المياه هو من الضخامة بحيث أن رصد تركيز كبريتات المتبقية في الحل لم يعد بالأمر الهين، وتتطلب تقنية أكثر تقدما التي تسمح بقياس دقيق لكميات ضئيلة من أنيون. لهذا الغرض، كان يعمل رديولبلد 35 S التتبع سلفات بالتزامن مع بيتا عد التلألؤ السائل، تستخدم تقنية عادة في فصل الاستخراجية بين السوائل، ومؤخرا أظهرت أن تكون فعالة في بلورة مراقبة كبريتات 8
يوضح هذا البروتوكول في وعاء واحد في التوليف الموقع من يجند BBIG وتبلور بوصفه الملح كبريتات من المحاليل المائية. وتقدم أيضا تركيب خارج الموقع ليجند 11 بوصفه مشاركاطريقة nvenient لإنتاج كميات أكبر من BBIG-CL، والتي يمكن تخزينها في شكل بلوري حتى جاهزة للاستخدام. ثم يتجلى إزالة الكبريت من مياه البحر باستخدام معدة مسبقا BBIG-CL يجند. وأخيرا، أظهر استخدام 35 المسمى S-كبريتات وبيتا عد التلألؤ السائل لقياس تركيز كبريتات في مياه البحر. ويهدف هذا البروتوكول إلى توفير برنامج تعليمي للمهتمين على نطاق واسع في استكشاف واستخدام بلورة الانتقائية لفصل أنيون مائي.
Protocol
1. تجميع 1،4-بنزين مكرر (iminoguanidinium) كلوريد (BBIG-CL)
- في الموقع التجميعي من 1،4-بنزين مكرر (iminoguanidinium) كلوريد يجند (BBIG-CL) وتبلور لها مع كبريتات
- إضافة 0.067 غرام من terephthalaldehyde و 2.2 مل من محلول 0.5 M مائي من كلوريد aminoguanidinium إلى 10 مل من الماء منزوع الأيونات في 25 مل قارورة أسفل جولة مزودة بقضيب مغناطيسي.
- تحريك حل مغناطيسيا لمدة أربع ساعات عند 20 درجة مئوية. هذا وسوف تسفر عن حل أصفر قليلا من BBIG-الكلورين.
- إضافة 0.5 مل من محلول 1 M مائي من كبريتات الصوديوم. وهذا يؤدي إلى هطول الأمطار لحظة من BBIG-SO 4 كما بلورية بيضاء صلبة.
- تصفية الصلبة باستخدام الترشيح فراغ لاسترداد BBIG-SO 4. غسل الصلبة على ورقة الترشيح خمس مرات مع 5 مل aliquots من المياه من أجل الحصول على الملح كبريتات النقي.
- تحقق نقاء مرحلة من مراحل البلورية BBIG-SO 4 التي حصلت عليها مسحوق حيود الأشعة السينية 12. مقارنة مع النمط هو مبين في الشكل 1.
- خارج الموقع توليف 1،4-بنزين مكرر (iminoguanidinium) كلوريد 11
- إضافة 4 غرام من terephthalaldehyde و7.26 غرام من كلوريد aminoguanidinium إلى 20 مل من الايثانول في 50 مل قارورة أسفل جولة مزودة بقضيب مغناطيسي.
- الحرارة الحل إلى 60 درجة مئوية باستخدام موقد، واثارة مع شريط مغناطيسي لمدة 2 ساعة. تبريد الحل إلى 20 درجة مئوية، والسماح لها الجلوس لمدة 3 ساعات، ثم جمع الصلبة عن طريق الترشيح فراغ من خلال قمع بوشنر مرشح ورقة مجهزة.
- تعليق حصلت الصلبة في 20 مل من الايثانول والحرارة على موقد حتى الغليان. إذا كانت صلبة لا يذهب تماما في حل في هذه المرحلة، إضافة قسامات الصغيرة (1 مل) من الإيثانول، مما يسمح في كل مرة الحل للوصول إلى درجة حرارة الغليان، حتى يتم حل جميع الصلبة.
- السماح للقارورة لتبريد لمن درجات الحرارة الغرفةإعادة، ثم وضع في 0 درجة مئوية الثلاجة بين عشية وضحاها. جمع الصلبة عن طريق الترشيح من خلال ورقة فلتر مجهزة قمع بوشنر باستخدام فراغ الترشيح.
- تأكيد الهوية ونقاء BBIG-الكلورين بنسبة 1 H NMR الطيفي 13. مقارنة مع الطيف هو مبين في الشكل 2.
2. فصل كبريتات من مياه البحر
- تبلور الكبريتات كما BBIG-SO 4
ملاحظة: مقدار BBIG-الكلور اللازم لإزالة كبريتات يعتمد على المبلغ المحدد للكبريتات في مياه البحر. وقد وجد أن استخدام 1.5 في حكمه من BBIG-CL بالنسبة إلى النتائج الكبريتات في إزالة 99٪ من كبريتات. مياه البحر المستخدمة في هذا البروتوكول لديه تركيز 30 ملم كبريتات، على النحو الذي يحدده المعايرة مع بووتون 2.- تصفية مياه البحر مع فلتر حقنة 0.22 ميكرون أو غشاء الترشيح مع حجم المسام الصغيرة لإزالة الجسيمات العالقة والكائنات الحيوية.
- جعل 30حل ملي من BBIG-الكلور باستخدام الماء منزوع الأيونات والصلبة BBIG-CL أعد كما هو موضح في المقطع السابق.
- إضافة الحل BBIG-الكلور إلى مياه البحر في 1.5: (/ ت ت) نسبة 1.
- يحرك الخليط لبضع ساعات للتأكد من كمية (> 99٪) إزالة كبريتات.
- جمع الصلبة عن طريق الترشيح من خلال ورقة فلتر مجهزة قمع بوشنر باستخدام فراغ الترشيح. غسل الصلبة على ورقة الترشيح خمس مرات مع 5 مل aliquots من المياه.
- تجفيف معزولة صلبة تحت فراغ وتزن عليه لتحديد العائد.
- يجند الانتعاش
- إضافة 53.1 ملغ من BBIG-SO 4 إلى حل 2 مل من هيدروكسيد الصوديوم (10٪) في قارورة 20 مل التلألؤ مزودة بقضيب مغناطيسي.
- يحرك الخليط لمدة ساعتين عند 20 درجة مئوية. وهناك راسب أصفر قليلا النموذج.
- تصفية الصلبة من خلال ورقة فلتر مجهزة قمع بوشنر باستخدام فراغ الترشيح. غسل الصلبة على ورقة الترشيح مع 0.2مل من الماء، ويجف تحت فراغ.
- تميز تعافى الصلبة التي كتبها NMR 13 لتأكيد هويتها باعتبارها مكرر (غوانيدين) قاعدة الحرة. مقارنة مع طيف الرنين النووي المغناطيسي هو مبين في الشكل (3).
- تحديد كمية سلفات إزالتها من مياه البحر بواسطة بيتا السائل التلألؤ العد
تنبيه: هذه التقنية تنطوي على استخدام النظائر المشعة، التي تشكل فئة مختلفة من المخاطر مما واجه عادة في معظم المختبرات. عادة ما كان مطلوبا معدات الحماية من الإشعاع خاصة عند التعامل مع النويدات المشعة. وبالتالي، فمن الضروري أن الإجراء يتبع بعناية وأن ضابط أمن واستشارة للحصول على المشورة والتوجيه.- حساب حجم محلول المخزون من النظائر المشعة الكبريت 35 (5 زارة التجارة والصناعة / مل) المستخدمة لضمان وجود أكثر من 5 ملايين التهم لكل دقيقة (CPM) لكل مليلتر من محلول ماء البحر، وذلك باستخدام المعادلات التالية (CPM وكوري (تسى ) على حد سواء وحدات القياس وأو النشاط الإشعاعي):
- ارتفاع 25 مل من ماء البحر مع 0.0112 مل من 5.0 MCI حل / مل من 35 S رديولبلد محلول كبريتات الصوديوم.
- إعداد 0، 15، 30، 33، 45، و 60 ملي حلول من BBIG-الكلورين في الماء منزوع الأيونات والجمع بين 0.750 مل من هذه الحلول مع حجم مساو من كبريتات 35 S-رديولبلد ارتفعت مياه البحر في أنبوب الطرد المركزي 2 مل.
- يحرك الخليط عن طريق عجلة دوارة أو دوامة في / الهواء مربع حاضنة الحفاظ على درجة حرارة ثابتة من 25 ± 0.2 درجة مئوية لمدة 24 ساعة.
- أجهزة الطرد المركزي الحلول في 1500 x ج لمدة 10 دقيقة في درجة حرارة 25 درجة مئوية.
- بعد الطرد المركزي، وإزالة 1.2 مل من كل حل باستخدام حقنة، ثم تصفية من خلال مرشح حقنة 0.22 ميكرون لإزالة الموقوف يعجل. ماصة 1.0 مل من كل من هذه الحلول إلى 20 مل من كوكتيل التلألؤ في قوارير البولي بروبلين التلألؤ. الحل لا تحتوي على BBIG-CL (الحل السيطرة) يجب تخفيفه عشرة أضعاف مع الماء منزوع الأيونات قبل بالإضافة إلى كوكتيل التلألؤ.
- ضع قارورة التلألؤ التي تحتوي على عينات وكوكتيل التلألؤ على عداد التلألؤ السائل والسماح لها الجلوس لمدة 1 ساعة قبل عد للسماح للعينات إلى dark-التكيف.
ملاحظة: قبل عد العينات، معايرة أجهزة القياس ويسمح لكل عينة لحساب لمدة 30 دقيقة. عدد قارورة إضافية تحتوي على التلألؤ كوكتيل الوحيد من أجل السماح لتصحيح الخلفية التي يتم استخدامها عند تحديد تركيزات من كبريتات في الحل. - تحديد كمية سلفات إزالتها، وذلك باستخدام المعادلات التالية:
54411 / 54411eq5.jpg "/>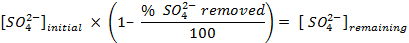
- حساب حجم محلول المخزون من النظائر المشعة الكبريت 35 (5 زارة التجارة والصناعة / مل) المستخدمة لضمان وجود أكثر من 5 ملايين التهم لكل دقيقة (CPM) لكل مليلتر من محلول ماء البحر، وذلك باستخدام المعادلات التالية (CPM وكوري (تسى ) على حد سواء وحدات القياس وأو النشاط الإشعاعي):
النتائج
الأشعة السينية نمط الحيود مسحوق من BBIG-SO 4 (الشكل 1) يسمح للتأكيد واضح للهوية تبلور الصلبة. وبمقارنة نمط الحصول عليها مقابل إشارة واحدة، ذروة كثافة مسائل أقل من ذروة المواقع. وينبغي لجميع القمم قوية هو مبين في إشارة تكون موجودة في العينة...
Discussion
هذا الأسلوب هو متسامح وليس لكثير من الانحرافات عن إجراءات مكتوبة، مما يجعله قويا جدا. ولكن هناك اثنين من الخطوات الحاسمة التي يجب اتباعها. أولا، يجند BBIG-الكلورين يجب أن يكون نقيا بقدر الإمكان. سوف الشوائب لا تؤثر فقط على بلورة وذوبان الملح كبريتات الناتجة عن ذلك، بل و...
Disclosures
The authors have nothing to disclose.
Acknowledgements
This work was supported by the U.S. Department of Energy, Office of Science, Basic Energy Sciences, Chemical Sciences, Geosciences, and Biosciences Division. We thank the University of North Carolina Wilmington for providing the seawater.
Materials
| Name | Company | Catalog Number | Comments |
| Terephthalaldehyde | Sigma | T2207 | |
| Aminoguanidinium Chloride | Sigma | #396494 | |
| Sodium Sulfate | Sigma | #239313 | |
| Barium Chloride | Sigma | #342920 | Highly Toxic |
| Ethanol | Any | Reagent Grade (190 proof) | |
| Sodium Hydroxide | EMD | SX0590-1 | |
| Hydrochloric Acid | Sigma | #258148 | |
| Filter Paper | Any | - | Any qualitative or analytical filter paper will work |
| Syringe Filter (0.22 μm) | Any | - | Nylon filter |
| 35S Labeled Sulfate | Perkin Elmer | NEX041005MC | |
| Ultima Gold Scintillation Cocktail | Perkin Elmer | #6013329 | |
| Polypropylene Vials | Any | - | |
| Disposable Syringe (2-3 ml) | Any | - | Any disposable plastic syringe works |
References
- Langton, M. L., Serpell, C. J., Beer, P. D. Anion Recognition in Water: Recent Advances from Supramolecular and Macromolecular Perspective. Angew. Chem. Int. Ed. 55, 1974-1987 (2016).
- Busschaert, N., Caltagirone, C., Van Rossom, W., Gale, P. A. Applications of Supramolecular Anion Recognition. Chem. Rev. 115, 8038-8155 (2015).
- Moyer, B. A., Custelcean, R., Hay, B. P., Sessler, J. L., Bowman-James, K., Day, V. W., Sung-Ok, K. A Case for Molecular Recognition in Nuclear Separations: Sulfate Separation from Nuclear Wastes. Inorg. Chem. 52, 3473-3490 (2013).
- Kim, S. K., Lee, J., Williams, N. J., Lynch, V. M., Hay, B. P., Moyer, B. A., Sessler, J. L. Bipyrrole-Strapped Calix[4]pyrroles: Strong Anion Receptors That Extract the Sulfate Anion. J. Am. Chem. Soc. 136, 15079-15085 (2014).
- Jia, C., Wu, B., Li, S., Huang, X., Zhao, Q., Li, Q., Yang, X. Highly Efficient Extraction of Sulfate Ions with a Tripodal Hexaurea Receptor. Angew. Chem. Int. Ed. 50, 486-490 (2011).
- Rajbanshi, A., Moyer, B. A., Custelcean, R. Sulfate Separation from Aqueous Alkaline Solutions by Selective Crystallization of Alkali Metal Coordination Capsules. Cryst. Growth Des. 11, 2702-2706 (2011).
- Custelcean, R. Urea-Functionalized Crystalline Capsules for Recognition and Separation of Tetrahedral Oxoanions. Chem. Commun. 49, 2173-2182 (2013).
- Custelcean, R., Sloop, F. V., Rajbanshi, A., Wan, S., Moyer, B. A. Sodium Sulfate Separation from Aqueous Alkaline Solutions via Crystalline Urea-Functionalized Capsules: Thermodynamics and Kinetics of Crystallization. Cryst. Growth Des. 15, 517-522 (2015).
- Custelcean, R., Williams, N. J., Seipp, C. A. Aqueous Sulfate Separation by Crystallization of Sulfate-Water Clusters. Angew. Chem. Int. Ed. 54, 10525-10529 (2015).
- Custelcean, R., Williams, N. J., Seipp, C. A., Ivanov, A. S., Bryantsev, V. S. Aqueous Sulfate Separation by Sequestration of [(SO4)(H2O)4]4- Clusters within Highly Insoluble Imine-Linked Bis-Guanidinium Crystals. Chem. Eur. J. 22, 1997-2003 (2016).
- Khownium, K., Wood, S. J., Miller, K. A., Balakrishna, R., Nguyen, T. B., Kimbrell, M. R., Georg, G. I., David, S. A. Novel Endotoxin-Sequestering Compounds with Terephthaldehyde-bis-guanylhydrazone Scaffolds. Bioorg. Med. Chem. Lett. 16, 1305-1308 (2006).
- Pecharsky, V. K., Zavalij, P. Y. . Fundamentals of Powder Diffraction and Structural Characterization of Materials. , (2005).
- Goldenberg, D. P. . Principles of NMR Spectroscopy: An Illustrated Guide. , (2016).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved