このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
ビスiminoguanidiniumリガンドと選択的結晶化により硫酸の分離
要約
ビス(iminoguanidinium)リガンドおよび硫酸の選択的分離におけるその利用をその場水系合成のためのプロトコルが提示されています。
要約
A simple and effective method for selective sulfate separation from aqueous solutions by crystallization with a bis-guanidinium ligand, 1,4-benzene-bis(iminoguanidinium) (BBIG), is demonstrated. The ligand is synthesized as the chloride salt (BBIG-Cl) by in situ imine condensation of terephthalaldehyde with aminoguanidinium chloride in water, followed by crystallization as the sulfate salt (BBIG-SO4). Alternatively, BBIG-Cl is synthesized ex situ in larger scale from ethanol. The sulfate separation ability of the BBIG ligand is demonstrated by selective and quantitative crystallization of sulfate from seawater. The ligand can be recycled by neutralization of BBIG-SO4 with aqueous NaOH and crystallization of the neutral bis-iminoguanidine, which can be converted back into BBIG-Cl with aqueous HCl and reused in another separation cycle. Finally, 35S-labeled sulfate and β liquid scintillation counting are employed for monitoring the sulfate concentration in solution. Overall, this protocol will instruct the user in the necessary skills to synthesize a ligand, employ it in the selective crystallization of sulfate from aqueous solutions, and quantify the separation efficiency.
概要
競争力のある水溶液から親水性オキソアニオンを選択的に分離( 例えば 、硫酸、クロム酸塩、リン酸塩)は環境改善、エネルギー生産、およびヒトの健康との関連での基本的な課題である。特に1,2硫酸塩は、そのように水から抽出することが困難ですその水和球を当てると極性の低い環境に移行するための固有不本意。3、より効率的な水性硫酸抽出の作成 は、典型的には、しばしば毒性試薬および溶媒を含む、合成および精製が困難と退屈な複雑な受容体を必要とします。4,5
選択的結晶化は、水からの分離を硫酸するシンプルで効果的な代替手段を提供しています。6-9などのBa 2+、Pbの2+、またはRaが2+形非常に不溶性の硫酸塩のようないくつかの金属陽イオンは、硫酸塩分離におけるそれらの使用は必ずしも実用的ではありませんがその高いtoxiへ都市と時々-低い選択。硫酸塩沈殿剤として有機配位子を採用することにより、有機分子に特徴的なデザインする構造の多様性と従順を利用しています。水性硫酸塩結晶化のための理想的な有機配位子は、水に可溶で、まだ比較的短時間でかつ競合するイオンの高濃度の存在下で不溶性の硫酸塩または錯体を形成すべきです。さらに、合成とリサイクルが容易であるべきです。そのようなリガンド、1,4-ベンゼンビス(iminoguanidinium)(BBIG)、自己集合し、その場に 2つの市販の前駆体、テレフタルアルデヒド及びaminoguanidiniumクロリドから、最近、水性硫酸分離において非常に有効であることが見出された。10リガンド水溶性の塩化物の形態であり、選択的に簡単な濾過によって溶液から除去することができる非常に不溶性の塩に硫酸結晶化します。 BBIGリガンドは次いで、脱プロトン化することによって回収することができますqueous NaOHおよびHCl水溶液でバック塩化物形態に変換され、別の分離サイクルで再利用することができる中性ビスiminoguanidineの結晶。水から硫酸塩を除去する際に、このリガンドの有効性は、溶液中に残存する硫酸濃度を監視する陰イオンの微量の正確な測定を可能にし、より高度な技術を必要とする、もはや単純な作業であることがとても素晴らしいです。この目的のために、β液体シンチレーション計数と一緒に35 S放射性標識硫酸トレーサーは、一般に、液-液抽出分離に利用技術を用いて、最近硫酸塩の結晶化をモニタリングするのに有効であることが実証された。8
このプロトコルは、水溶液から硫酸塩としてBBIGリガンドおよびその結晶のその場合成にワンポットを示しています。リガンド11の域外合成はまた、共同として提示されています使用する準備ができるまで結晶形で保存することができるBBIG-Clを、より多量の生産のためのnvenient方法。先に調製したBBIG-Clをリガンドを使用して、海水からの硫酸除去がその後実証されています。最後に、35 Sで標識された硫酸塩と海水中の硫酸濃度を測定するβ液体シンチレーションカウンターの使用が実証されます。このプロトコルは、水性陰イオン分離のための選択的結晶化の使用を模索中で広く興味のある人のためのチュートリアルを提供することを意図しています。
プロトコル
1.合成1,4-ベンゼンビス(iminoguanidinium)塩化物(BBIG-CL)
- その場 1,4-ベンゼンビス(iminoguanidinium)塩化物リガンド(BBIG-CL)の合成と硫酸とのその結晶化で
- 磁気撹拌棒を備えた25ml丸底フラスコに0.067テレフタルアルデヒドのグラムおよび脱イオン水10mlにaminoguanidinium塩化0.5 M水溶液2.2 mLを加え。
- 20℃で4時間磁気溶液を攪拌します。これはBBIG-Clをわずかに黄色の溶液が得られます。
- 硫酸ナトリウムの1 M水溶液0.5ミリリットルを追加します。これは、結晶性の白色固体としてBBIG-SO 4の瞬間降水量になります。
- BBIG-SO 4を回復するための固体使用して真空ろ過をフィルタリングします。純粋な硫酸塩を得るために、水5mlアリコートで濾紙上の固体を5回洗浄します。
- 結晶BBIG-SOの相純度をチェック図4は、粉末X線回折12によって得られました。 図1に示すパターンと比較してください。
- 1,4-ベンゼンビスの域外合成(iminoguanidinium)塩化11
- 磁気撹拌棒を備えた50mlの丸底フラスコ中のエタノール20mlにテレフタルアルデヒドを4gとaminoguanidiniumクロライド7.26グラム加えます。
- ホットプレートを用いて60℃に溶液を加熱し、そして2時間、磁気撹拌棒で撹拌しました。 20°Cにソリューションを冷却し、それが濾紙装備したブフナー漏斗を通して真空濾過により固体を収集した後、3時間放置します。
- 沸騰するまでホットプレート上でエタノールと熱の20ミリリットルで得られた固体を一時停止します。固体は、この時点で溶液中に完全に入らない場合、すべての固体が溶解するまで、溶液を沸騰温度に到達するたびに、許可、エタノールの少量のアリコート(1 ml)を加えます。
- フラスコを室温temperatuに冷却することを許可します再、一晩0℃の冷凍庫に入れます。真空濾過を用いてブフナー漏斗装備濾紙を通して濾過することにより固体を収集します。
- 1 H NMR分光法13によってBBIG-Clでのアイデンティティおよび純度を確認してください。 図2に示されるスペクトルと比較してください。
海水から2硫酸の分離
- BBIG-SO 4などの硫酸塩の結晶化
注:硫酸を除去するために必要なBBIG-Clでの量は、海水中の硫酸の正確な量に依存します。これは、硫酸の99%の除去中の硫酸結果にBBIG-Clでの相対的な1.5当量を使用していることがわかりました。 BaCl 2を用いた滴定により決定されるように、このプロトコルで使用される海水は、30 mMの硫酸濃度を有します。- 浮遊粒子とバイオ生物を除去するための小孔径が0.22μmのシリンジフィルターや濾過膜で海水をフィルタリングします。
- 30を作ります前のセクションで説明したように調製し、脱イオン水と固体BBIG-Clで使用BBIG-ClをmM溶液。
- 1(v / v)の割合:1.5で海水にBBIG-Cl溶液を追加します。
- 硫酸の定量的(> 99%)除去を確実にするために数時間のために、混合液を撹拌しました。
- 真空濾過を用いてブフナー漏斗装備濾紙を通して濾過することにより固体を収集します。水5mlアリコートで濾紙上の固体を5回洗浄します。
- 真空下で単離された固体を乾燥し、収量を決定するために、それを量ります。
- リガンド回復
- 磁気撹拌棒を備えた20ミリリットルのシンチレーションバイアル中のNaOH(10%)の2ミリリットルの溶液にBBIG-SO 4の53.1 mgを追加します。
- 20℃で2時間混合物を撹拌しました。わずかに黄色の沈殿物が形成されます。
- 真空濾過を使用して濾紙装備したブフナー漏斗を通して固体をフィルタリングします。 0.2を用いて濾紙上の固体を洗浄mlの水、そして真空下で乾燥しました。
- ビス(グアニジン)、遊離塩基としての同一性を確認するために、NMR 13で回収した固体を特徴づけます。 図3に示すNMRスペクトルと比較してください。
- 液体シンチレーション計数をβによって海水から削除硫酸塩の量の決意
注意:この手法は、通常、ほとんどの研究室で発生したものよりも危険性の異なるクラスをもたらす放射性同位元素の使用を含みます。放射性核種を取り扱う場合には、特別な放射線防護装置が通常必要とされます。したがって、手順に従って慎重に作業していること、および安全管理者が助言・指導のために参照されることが不可欠です。- 硫黄-35放射性同位元素(5 mCiの/ミリリットル)のストック溶液の量は、以下の式(CPMとキュリー(Ciのを使用して、海水溶液1ミリリットル当たり毎分500万人以上のカウント(CPM)が存在することを確認するために使用される計算)メジャーfの両方の単位であり、または放射能):
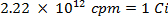
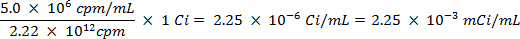
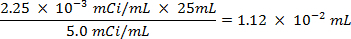
- 35 S放射性標識された硫酸ナトリウム溶液の5.0 mCiの/ ml溶液の0.0112 mlの海水25mlのスパイク。
- 調製0、15、30、33、45、及び脱イオン水中BBIG-Clを60mMの溶液と35 S-放射標識硫酸等量のこれらの溶液の0.750ミリリットル組み合わせを2mlの遠心管に海水をスパイクしました。
- 24時間25±0.2℃の一定温度に維持したインキュベーター/エアボックス内の回転ホイールまたは渦を経由して、混合液を撹拌しました。
- 25℃で10分間、1500×gでソリューションを遠心。
- 遠心分離後、シリンジを用いて各溶液を1.2mlのを削除し、懸濁除去するために0.22μmのシリンジフィルターを介してフィルター沈殿します。ピペットポリプロピレンシンチレーションバイアル中のシンチレーションカクテル20ml中にこれらの溶液をそれぞれ1.0 mlです。何BBIG-Clで(対照溶液)を含有しない溶液は、従来のシンチレーションカクテルに添加し、脱イオン水で10倍に希釈されるべきです。
- サンプルおよび液体シンチレーションカウンターでのシンチレーションカクテルを含むシンチレーションバイアルを置き、前暗適応にサンプルを可能にするために、カウントに1時間放置します。
注:サンプルをカウントする前に、機器を較正し、各試料を30分間カウントすることを可能にします。溶液中の硫酸の濃度を決定する際に使用されるバックグラウンド補正を可能にするために、唯一のシンチレーションカクテルを含む追加のバイアルを数えます。 - 以下の式を使用して、削除硫酸塩の量を決定します。
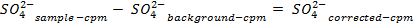
54411 / 54411eq5.jpg "/>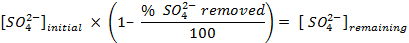
- 硫黄-35放射性同位元素(5 mCiの/ミリリットル)のストック溶液の量は、以下の式(CPMとキュリー(Ciのを使用して、海水溶液1ミリリットル当たり毎分500万人以上のカウント(CPM)が存在することを確認するために使用される計算)メジャーfの両方の単位であり、または放射能):
結果
BBIG-SO 4( 図1)の粉末X線回折パターンは、結晶化固体の同一性の明確な確認を可能にします。参照1対得られたパターンを比較することで、ピーク強度は、以下のピークの位置よりも重要。基準に示されているすべての強いピークが得られた試料中に存在しなければなりません。基準パターンには存在しないサンプル中の強いピークの出現は?...
ディスカッション
この技術は、非常に堅牢に書かれた手順から多くの逸脱にかなり寛容です。従わなければならないしかし、2つの重要なステップがあります。まず、BBIG-Clでリガンドは、できるだけ純粋である必要があります。不純物は結晶化し、得られた硫酸塩の溶解性には影響しませんが、またそれが困難な溶液からの定量的な硫酸塩の除去に必要な量を計算することになります。この技術は微妙な変化?...
開示事項
The authors have nothing to disclose.
謝辞
This work was supported by the U.S. Department of Energy, Office of Science, Basic Energy Sciences, Chemical Sciences, Geosciences, and Biosciences Division. We thank the University of North Carolina Wilmington for providing the seawater.
資料
| Name | Company | Catalog Number | Comments |
| Terephthalaldehyde | Sigma | T2207 | |
| Aminoguanidinium Chloride | Sigma | #396494 | |
| Sodium Sulfate | Sigma | #239313 | |
| Barium Chloride | Sigma | #342920 | Highly Toxic |
| Ethanol | Any | Reagent Grade (190 proof) | |
| Sodium Hydroxide | EMD | SX0590-1 | |
| Hydrochloric Acid | Sigma | #258148 | |
| Filter Paper | Any | - | Any qualitative or analytical filter paper will work |
| Syringe Filter (0.22 μm) | Any | - | Nylon filter |
| 35S Labeled Sulfate | Perkin Elmer | NEX041005MC | |
| Ultima Gold Scintillation Cocktail | Perkin Elmer | #6013329 | |
| Polypropylene Vials | Any | - | |
| Disposable Syringe (2-3 ml) | Any | - | Any disposable plastic syringe works |
参考文献
- Langton, M. L., Serpell, C. J., Beer, P. D. Anion Recognition in Water: Recent Advances from Supramolecular and Macromolecular Perspective. Angew. Chem. Int. Ed. 55, 1974-1987 (2016).
- Busschaert, N., Caltagirone, C., Van Rossom, W., Gale, P. A. Applications of Supramolecular Anion Recognition. Chem. Rev. 115, 8038-8155 (2015).
- Moyer, B. A., Custelcean, R., Hay, B. P., Sessler, J. L., Bowman-James, K., Day, V. W., Sung-Ok, K. A Case for Molecular Recognition in Nuclear Separations: Sulfate Separation from Nuclear Wastes. Inorg. Chem. 52, 3473-3490 (2013).
- Kim, S. K., Lee, J., Williams, N. J., Lynch, V. M., Hay, B. P., Moyer, B. A., Sessler, J. L. Bipyrrole-Strapped Calix[4]pyrroles: Strong Anion Receptors That Extract the Sulfate Anion. J. Am. Chem. Soc. 136, 15079-15085 (2014).
- Jia, C., Wu, B., Li, S., Huang, X., Zhao, Q., Li, Q., Yang, X. Highly Efficient Extraction of Sulfate Ions with a Tripodal Hexaurea Receptor. Angew. Chem. Int. Ed. 50, 486-490 (2011).
- Rajbanshi, A., Moyer, B. A., Custelcean, R. Sulfate Separation from Aqueous Alkaline Solutions by Selective Crystallization of Alkali Metal Coordination Capsules. Cryst. Growth Des. 11, 2702-2706 (2011).
- Custelcean, R. Urea-Functionalized Crystalline Capsules for Recognition and Separation of Tetrahedral Oxoanions. Chem. Commun. 49, 2173-2182 (2013).
- Custelcean, R., Sloop, F. V., Rajbanshi, A., Wan, S., Moyer, B. A. Sodium Sulfate Separation from Aqueous Alkaline Solutions via Crystalline Urea-Functionalized Capsules: Thermodynamics and Kinetics of Crystallization. Cryst. Growth Des. 15, 517-522 (2015).
- Custelcean, R., Williams, N. J., Seipp, C. A. Aqueous Sulfate Separation by Crystallization of Sulfate-Water Clusters. Angew. Chem. Int. Ed. 54, 10525-10529 (2015).
- Custelcean, R., Williams, N. J., Seipp, C. A., Ivanov, A. S., Bryantsev, V. S. Aqueous Sulfate Separation by Sequestration of [(SO4)(H2O)4]4- Clusters within Highly Insoluble Imine-Linked Bis-Guanidinium Crystals. Chem. Eur. J. 22, 1997-2003 (2016).
- Khownium, K., Wood, S. J., Miller, K. A., Balakrishna, R., Nguyen, T. B., Kimbrell, M. R., Georg, G. I., David, S. A. Novel Endotoxin-Sequestering Compounds with Terephthaldehyde-bis-guanylhydrazone Scaffolds. Bioorg. Med. Chem. Lett. 16, 1305-1308 (2006).
- Pecharsky, V. K., Zavalij, P. Y. . Fundamentals of Powder Diffraction and Structural Characterization of Materials. , (2005).
- Goldenberg, D. P. . Principles of NMR Spectroscopy: An Illustrated Guide. , (2016).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved