Method Article
ترميز الوراثية الأحماض الأمينية غير المقبول لتوليد الأجسام المضادة-المخدرات يرتبط من خلال رد فعل سريع بيورثوجونال
In This Article
Summary
دمج سيكلوبروبيني مشتق ليسين في أجسام يتيح الربط الخاصة بالموقع، وسرعة وكفاءة لجزيئات تيترازيني الحاملة لتوليد الأجسام المضادة-المخدرات يصرف.
Abstract
جسم مضاد-المخدرات يصرف (ADCs) يستخدم في الوقت الحاضر في الممارسة السريرية خليط جزيئات الأجسام المضادة ترتبط بعدد متباين من السموم في مواقف مختلفة. وقد أظهرت الدراسات السريرية أن المؤشر العلاجي لهذه ADCs التقليدية يمكن أن تتحسن بالربط الخاصة بالموقع من السموم. بيد أن النهج الحالي لإنتاج ADCs متجانسة العديد من القيود، مثل تعبير البروتين المنخفض وبطء الاستجابة الحركية. في هذا البروتوكول ونحن تصف كيفية إعداد نظام لتعبير لإدماج سيكلوبروبيني مشتق ليسين (سيبك) التوسع في الشفرة الجينية باستخدام الأجسام المضادة. يسمح هذا المؤشر بيورثوجونال الحد الأدنى التصريف السريع من مشتقات تيترازيني من خلال سيكلواديشن ديلز-الدر معكوس-طلب. يتيح نظام التعبير هنا ذكرت سهلة الإنتاج وتنقية تراستوزوماب واضعة سيبك في كل من سلاسل ثقيلة. نشرح كيفية ربطها الجسم أوريستاتين مونوميثيل السم ه وتميز إيمونوكونجوجاتي مسعور التفاعل اللوني والطيف الكتلي. وأخيراً، يمكننا وصف فحوصات لتقييم الاستقرار في مصل الدم البشري للربط ديهيدروبيريدازيني الناجمة عن التصريف واختبار سيتوتوكسيسيتي انتقائية من ADC لخلايا سرطان الثدي مع مستويات عالية من مستقبلات HER2.
Introduction
يصرف جسم-المخدرات (ADCs) الجمع بين القدرة الانتقائية بيوثيرابيوتيكس وفاعلية الجزيئات السامة للخلايا الصغيرة. وتهدف معظم ADCs لتقليل الآثار الجانبية للعلاج الكيميائي التقليدي باستهداف الأدوية التي تؤثر على بلمرة الحمض النووي أو microtubule ل خلايا السرطان1. ADCs الجيل الأول أقر بأن الغذاء والدواء (FDA) تعتمد على تعديل ليسينيس وسيستينيس، الذي يولد خليط جزيئات تعديل في مواقف مختلفة مع خصائص الحرائك الدوائية انخفاض2. على النقيض من ذلك، يمكن أن تولد التصريف الخاصة بالموقع من المخدرات للأجسام المضادة المركبات مع تحسين العلاجية إينديسيس3،4. تسعى إلى التصدي للتحدي المتمثل في إنتاج ADCs متجانسة، كانت عدة تعديلات المواد الكيميائية والانزيميه انتقائية عنها1،5. بيد الأساليب الحالية يمكن أن تستهدف فقط موقف معين على الجسم يعانون من التعبير البروتين المنخفض، تزويد linkers الاستقرار منخفضة أو الاعتماد على ردود الفعل بطيئة ومنخفضة الغلة.
إدماج أحماض الأمينية غير المقبول (نكا) من خلال التوسع في الشفرة الجينية تمكن التثبيت الخاصة بالموقع لعدد كبير جماعات بيورثوجونال رد الفعل في البروتينات، ويحتمل أن التغلب على أوجه قصور الأساليب الأخرى لتوليد ADCs. ترميز ncAAs ردا على كودون مستهدفة (إيقاف) يعتمد على أمينواسيل-الحمض الريبي النووي النقال سينثاتيز/الحمض الريبي النووي النقال أزواج هي متعامد على أزواج الذاتية التي تتضمن6من الأحماض الأمينية المتعارف عليه. أدرجت عدة ncAAs في أجسام مضادة لتوليد ADCs. ومع ذلك، الأكثر يعانون من الالتزامات المختلفة للتطبيقات في تصريف العقاقير العلاجية. فأسيتيلفينيلالانيني (pAcF)،من78 لا تماما بيورثوجونال، يتطلب انخفاض الأس الهيدروجيني (4.5) وأوقات رد الفعل الطويل (> ح 60)، بينما أزيدات مثل p-أزيدوفينيلالانيني (بازف)7،،من910، قد يتم تخفيض فأزيدوميثيلفينيلالانيني (بامف)11، ومشتق أزيد من يسين (أزك)،من1213 في الخلية14، ويمكن حمل النحاس المستخدمة لتحفيز سيكلواديتيونس هويزن الضرر التأكسدي 15.
على الرغم من أن ncAAs بديلة استناداً إلى ترانس-سيكلوكتيني (TCO)، سيكلوكتيني (اسكتلندا) ونونيني بيسيكلو [6.1.0] (BCN) قد مؤخرا تم ترميزه في جسم مضاد لأغراض التصوير الحيوي، نظام التعبير يعاني من الغلات منخفضة جداً (0.5 مغ/لتر)16. وعلاوة على ذلك، سيكلوكتينيس وسيكلوكتينيس الكبيرة ومقابض مسعور التي قد تزيد من قابلية ADC للتجميع-ADC حمولات مسعور تقليديا والخصائص الفيزيائية للرابط ثبت إلى حد كبير أثر مؤشر العلاجية والدوائية17. على النقيض من ذلك، سيكلوبروبينيس 1، 3-ديسوبستيتويد هي مجموعات صغيرة رد الفعل الذي ينبغي أن يؤدي تغيير الحد الأدنى بالبروتين الهيكل وفيسيتشوتشيميكال خصائص18. سيكلوبروبينيس بشكل انتقائي وسرعة تتفاعل مع تيترازينيس عن طريق سيكلواديتيون ديلز-الدر معكوس إلكترون-طلب19. في هذا البروتوكول نحرز استخدام مشتق تأثير يسين (سيبك، الشكل 1b) سيكلوبروبيني الميثيل أقل المتأثرين بعائق الفراغية من دورات غير المشبعة توتر أكبر وقد ثابت معدل رد فعل حسب ترتيب 1-30 متر-1s -1 في وسائل الإعلام مائي18،20.
نحن أبلغ مؤخرا عن كيفية إدماج سيبك في أجسام مضادة لتوليد ADCs برد الفعل هذا المؤشر بيورثوجونال الحد الأدنى مع جزيئات تحمل تيترازيني21. هنا يمكننا وصف الإجراء إعداد ADC بمزيد من التفصيل مع التركيز على الخطوات الأكثر تحديا. إدراج سيبك موجه بيروليسيل-الحمض الريبي النووي النقال سينثاتيز (بيلرس) باستخدام/زوج الحمض الريبي النووي النقالكوا(بيلت) ردا على كودون العنبر وعرض في سلسلة جسم ثقيل (HC)22. هنا نستخدم والبلازميدات اثنين تعداء عابرة (الشكل 1a)، ترميز سلسلة ثقيلة الجسم واحد والآخر ترميز السلسلة الخفيفة (LC)، كلاهما يحتوي على كاسيت بيلرس/بيلت. وبدلاً من ذلك، يمكن إنشاء خط خلية مستقرة تمكن غلات جسم من خلال إجراءات أكثر شاقة21.
نظم التعبير المذكورة أعلاه يمكن أن تنتج الغلوبولين المناعي العلاجية المضادة-HER2 1 (IgG1) تراستوزوماب مع سيبك في مستويات مماثلة للأجسام المضادة نوع البرية. علينا تحديد المركز الأول في المجال CH1 على السلسلة الثقيلة لترميز نكا (HC-118TAG). هذا هو موقع تم التعديل الأكثر شيوعاً في ADCs23 ويعرف باسم المفوض السامي-118 (الاتحاد الأوروبي الترقيم) لكن يشار إليها ك HC-121 (تسلسل الموقف) و HC-114 (كابات الترقيم)24. نظراً لهذا الموقف هو المحافظة عليها طوال جميع IgG1s، ينبغي أن تكون هذه النظم التعبير قابلة للأجسام المضادة الأكثر العلاجية.
وتظهر لنا trastuzumab(CypK)2 يمكن أن تكون بسهولة تنقيته بالبروتين اتباعها بالبروتين سريعة اللوني السائل مع عمود تفاعل مسعور (فبلك-التحالف الدولي للموئل). بعد ذلك يرتبط الجسم تساهمي داخل 3 (ح) microtubule البلمرة مثبط مونوميثيل أوريستاتين ه (ما)، الذي يستخدم في أدسيتريس ADC وافقت إدارة الأغذية والعقاقير. هنا نستخدم مشتق البنزيل تيترازيني لما (تيترازيني-فكماي) مع رابط يضم فاصل جلوتاراتي ومكون حوزتي مجا فالين-citrulline تليها وحدة فسيلفيمولاتيفي-أمينوبينزيلالكوهول؛ هذا الرابط هو المشقوق بكاثيبسين في يحلول عند تدخيل ADC أسفر عن إطلاق سراح تراسيليس السمية25. من أجل إظهار نطاق واسع من رد فعل، الجسم يرتبط أيضا تيتراميثيلرهوداميني فلوروفوري (تمرا). نشرح كيفية التحقق من هوية حساب المرافق له اللوني السائل بالإضافة إلى الطيف الكتلي (LC-MS) وحساب نسبة المخدرات إلى جسم (دار) باستخدام كروماتوغرافيا سائلة عالية الأداء مع عمود تفاعل مسعور ([هبلك]-التحالف الدولي للموئل) .
كجزء من وصف أداء الأجسام المضادة، ونحن تصف كيفية اختبار استقرار الروابط ديهيدروبيريدازيني في مصل الدم البشري. يتم تقييم هذه المعلمة بسهولة أكبر في طمره تراستوزوماب نظراً لأنه يمكن قياسها كمياً أليسا بسيطة وتفسير النتائج هي ليست معقدة بحوزتي المكون مجا trastuzumab(MMAE)2. وأخيراً، يتم تقييم الانتقائية وفاعلية من trastuzumab(MMAE)2 بمقارنة سيتوكسيسيتي ADC عبر خطوط الخلايا معربا عن مستويات مختلفة من HER2. كما يوفر هذا التحليل وظيفية دليلاً على استقرار ADC عند إجراء بعد حضانة إيمونوكونجوجاتي في مصل الدم البشري.
Protocol
1-إنتاج وتميز جسم
- التعبير عن الأجسام المضادة
- ذوبان الجليد قنينة من HEK تعليق الخلايا في قارورة 250 مل التي تحتوي على 50 مل من التعبير المتوسطة وتستكمل مع 100 وحدة/مل البنسلين و 100 ميكروغرام/مل ستربتوميسين 250 نانوغرام/مليلتر الامفوتريسين باء إبقاء الخلايا في 37 درجة مئوية مع نسبة 8% CO2 في هوميديفيد حاضنات مجهزة مع شاكر 125 لفة في الدقيقة. تقسيم الخلايا إلى 0.3-0.5 × 106 خلايا/مل (كل 2-3 أيام) على الأقل مرتين قبل ترانسفيكتينج.
- عند كثافة 2.5 × 106 خلايا/مل هو بلغ (2-3 أيام بعد تقسيم)، تعد حلاً جديدة من 100 ملم سيبك. لهذا الغرض، تزن 64 ملغ سيبك، إضافة 2.5 مل من هيدروكسيد الصوديوم 0.1، ودوامه، وتدور إلى أسفل استرداد الجسيمات أونديسولفيد جميعا و sonicate.
- إضافة 2.5 مل سيبك (100 ملم في 0.1 M هيدروكسيد الصوديوم) إلى 42.5 مل من التعبير المتوسطة وتستكمل مع المضادات الحيوية. يخلط جيدا وإضافة 250 ميليلتر من 0.1 M HCl، وتعقيمها باستخدام عامل تصفية 0.22 ميكرومتر.
- تمييع 50 ميكروغرام من المفوض السامي و LC pKym1 والبلازميدات21 إلى 2.5 مل مع انخفاض مصل المتوسطة. في أنبوب منفصل، تمييع 135 ميليلتر من تعداء الكاشف إلى 2.5 مل مع انخفاض مصل المتوسطة.
- خمس دقائق بعد إعداد الحلول، تخلط البلازميدات والحل كاشف تعداء واحتضان لمدة 20 دقيقة للسماح بتشكيل مجمعات بين الحمض النووي والكاشف تعداء.
- وفي الوقت نفسه، الطرد المركزي خلايا 125 مليون في كثافة المستهدفة لمدة 5 دقائق في 500 x ز، ريسوسبيند مع وسيلة التعبير التي تحتوي على سيبك وإضافة خليط كاشف الحمض النووي – تعداء. سيبك يمكن شراؤها أو تصنيعه كما ذكرت سابقا18.
- بعد حضانة الخلايا ح 20، إضافة 250 ميليلتر من تعداء كاشف معززات في الطقم.
- حصاد الأجسام المضادة من طافية 6-7 الأيام بعد إضافة سيبك (أي تغيير في المتوسط مطلوب خلال التعبير).
* بدلاً من ذلك، للحصول على عائدات أعلى وأكثر اتساقا، خط خلية مستقرة يمكن إنشاء كما هو موضح في سالفا Oller et al. 21من عام 2018. وفي هذه الحالة، يتم التعبير عن trastuzumab(CypK)2 ببساطة عن طريق إضافة سيبك 5 ملم في الأجلين المتوسط والتعبير.
- تنقية جسم
- الطرد المركزي الخلايا لمدة 15 دقيقة في 3000 x ز.
- تصفية المادة طافية مع 0.45 أو عامل تصفية 0.22 ميكرومتر. إذا كان عامل التصفية يصبح تغطي، تحل محلها واحدة جديدة ومواصلة تصفية. إذا كان هذا يحدث بعد سوى بضع ملليلتر، الطرد المركزي المادة طافية 15 دقيقة إضافية في 7000 x ز.
- إضافة الراتنج بالبروتين (2 مل/100 مل من المادة طافية) في عمود كروماتوغرافيا البوليبروبيلين فارغة وحجته الراتنج مع وحدات التخزين على الأقل 5 حبة يغسل المخزن المؤقت (فوسفات الصوديوم 0.1 M، 150 مم كلوريد الصوديوم).
- تقسيم المادة طافية إلى اثنين من أنابيب مخروطية 50 مل وإضافة 5 × حبة غسل العازلة (فوسفات الصوديوم 0.5 م، 150 مم كلوريد الصوديوم) تليها الراتنج بالبروتين قبل متوازن. ضع الأنبوبة المخروطية على اسطوانة على ح 3 في درجة حرارة الغرفة لهدم الجسم في المادة طافية.
وبدلاً من ذلك: إضافة المادة طافية على العمود الذي يتضمن على الأقل ضعف حجم الموصى بها من الراتنج والسماح بالتدفق من خلال. تأكد من أن ليست هناك كمية كبيرة من الأجسام المضادة التي تركت في المادة طافية بالحزب الديمقراطي الصربي صفحة. إذا لم يكن هناك، الوتي المادة طافية عن طريق الراتنج مرة أخرى. - نقل الراتنج البروتين A مع المادة طافية في عمود وتسمح للسائل بالتدفق من خلال.
- إضافة 25 مل أغسل المخزن المؤقت (أو الراتنج على الأقل 10 وحدات التخزين)، والسماح بالتدفق من خلال.
- الوتي الجسم مع 4 مل سترات الصوديوم 0.1 M، الأس الهيدروجيني 3، في 1 مل من 1 متر العازلة الفوسفات، 150 مم كلوريد الصوديوم.
- تضعف الجسم مع 10 مل من برنامج تلفزيوني، والتركيز على 0.5-1 مل بالترشيح الطرد المركزي، وتبادل المخزن المؤقت ثلاث مرات مع برنامج تلفزيوني.
- تنقية العينات التي فبلك باستخدام عمود الائتلاف بوتيل مع تدفق 0.5 مل/دقيقة، ومن 0-100% التدرج في 30 دقيقة منخفضة الملح المخزن المؤقت (pH فوسفات الصوديوم 50 مم 7.0، 20% الايزوبروبانول) في المخزن المؤقت للملح عالية (1.5 متر (NH4)2هكذا4، 50 مم فوسفات الصوديوم درجة الحموضة 7.0 ، 5% الايزوبروبانول). جمع كافة الكسور ورصد شطف في 280 نانومتر. يمكن تنقية كميات صغيرة (< 1 ملغ) مع [هبلك]-التحالف الدولي للموئل حسب الشروط الموضحة في 2.4 لتعظيم العائد والنقاء.
- تجمع الكسور التي تحتوي على الأجسام المضادة، وتمييع لهم على الأقل 4 مل مع برنامج تلفزيوني، والتركيز عليها بالمخزن الترشيح وتبادل الطرد المركزي ثلاث مرات مع برنامج تلفزيوني.
- التحديد الكمي جسم
- الحصول على بتركيز تقريبية عن طريق قياس امتصاص في 280 nm استخدام جهاز المطياف الضوئي الصغير الحجم.
- إذا كان مطلوباً قياس دقيق، استخدم مجموعة أليسا لقياس إيجس البشرية. لتقدير تقريبي، استخدم الحزب الديمقراطي الصربي صفحة مع وصمة عار على أساس أخذ كما يلي:
- إعداد المعايير بتمييع ست مرات من شقين هما معيار تراستوزوماب كمياً بإليزا في 1 ملغ/مل.
- يغلي بالمعايير والعينات في حوالي 0.25 مغ/مل في تقليل تحميل المخزن المؤقت.
- تشغيلها في الحزب الديمقراطي الصربي مكررا-تريس-الصفحة 4-12 ٪ باستخدام المخزن المؤقت مس-الحزب الديمقراطي الصربي ووصمة عار مع صبغة المستندة إلى أخذ. وأخيراً قياس كثافة اللون للفرقة المقابلة للضوء أو السلسلة الثقيلة باستخدام إيماجيج واقحم الإشارة من العينات في المنحنى القياسي.
- مخزن الجسم في 4 درجات مئوية.
2-مترافق الجسم وتميز ADC
- مترافق الضد مع جزيء تيترازيني الحاملة
- تمييع مكافئات مولى 10 من تيترازيني-فكماي (4 ميليلتر، ملم 3.4 في ثنائي ميثيل سلفوكسيد ([دمس])) مع 20 ميليلتر من الاسيتو الانيتريل وميليلتر 76 من برنامج تلفزيوني في أنبوب مخروطي صغير (مثلأنبوب PCR).
- إضافة ما يعادل المولى 1 trastuzumab(CypK)2 (100 ميليلتر، 2 ملغ/مل في برنامج تلفزيوني)، ومزيج دقيق، والسماح للرد على ح 3 في درجة حرارة الغرفة (25 درجة مئوية) لتشكيل trastuzumab(MMAE)2.
ملاحظة: يمكن ربط الجزيئات الأخرى مثل تيترازيني-5-طمره بجسم بدلاً من تيترازيني-فكماي باستخدام هذا البروتوكول.
- تنقية ADC
- قبل حجته عمود دوران استبعاد حجم مع برنامج تلفزيوني اتباع إرشادات الشركة المصنعة.
- إضافة حجم كل من رد فعل على عمود الدوران وأجهزة الطرد المركزي في 1500 غ س ل 1 دقيقة.
- التحديد الكمي ADC وتحليل المتقارن من الحزب الديمقراطي الصربي صفحة
- التحديد الكمي ADC كما هو موضح في 1.3.2. بقياس كثافة اللون سلسلة الضوء على صفحة الحزب الديمقراطي الصربي باستخدام الجسم غير المعدلة للمنحنى المعياري.
- وينبغي أن تحول سلسلة ثقيلة قليلاً تظهر زيادة في الوزن الجزيئي بناء على تصريف.
ملاحظة: إذا تم تعديل الجسم مع فلوروفوري كما هو الحال في trastuzumab(TAMRA)2، يجب إظهار فقط الفرقة المقابلة للسلسلة الثقيلة fluorescence في جل قبل التلوين.
- تحليل المتقارن من [هبلك]-التحالف الدولي للموئل
- حجته العمود [هبلك]-الائتلاف مع المخزن المؤقت 100% ألف (1.5 متر (NH4)2هكذا4، 50 مم فوسفات الصوديوم درجة الحموضة 7.0، 5% الايزوبروبانول) لمدة 5 دقائق.
- ميكس 15 ميليلتر (بمول 67) من حل 1 ملغ/مل من تراستوزوماب (سيبك) 2 مع 15 ميليلتر من 2 x المخزن المؤقت في قنينة. ثم برنامج حقنه 10 ميليلتر في [هبلك].
- الوت في تدفق 1 مل/دقيقة isocratic مع العازلة 100% A لمدة 1 دقيقة تليها تدرج 15 دقيقة من 100 إلى 0% من المخزن المؤقت أ في ب (pH فوسفات الصوديوم 50 مم 7.0 أو الأيسوبروبانول 20%). رصد شطف في 280 نانومتر.
- حساب في دار بإدماج ذروة المقابلة لكل نوع من الأنواع واستخدام المناطق الناتجة عن ذلك في المعادلة التالية:
دار = (1 x trastuzumab(MMAE) + 2 x trastuzumab(MMAE)2)
/(trastuzumab(MMAE)0 trastuzumab(MMAE)1 + trastuzumab(MMAE)2)
حان وقت الاحتفاظ المتوقعة trastuzumab(CypK)2 دقيقة 7.5-8.0، تراستوزوماب (سيبك، ما) 9.1-9.6 دقيقة، و trastuzumab(MMAE)2 دقيقة 10.5-11.0.
- تحليل المتقارن من LC-مرض التصلب العصبي المتعدد
- ديجليكوسيلاتي 30 ميليلتر من 1 ملغ/مل ADC وجسم غير معدلة في الحد من غير شروط استخدام وحدات بنغازي و 250 على الأقل 6 ح عند 37 درجة مئوية.
- الوت الجسم في مطياف كتلة في الخلية C4 1-5 ميكرون 1.0 × 100 مم عمود باستخدام تدرج 20 دقيقة من الاسيتو الانيتريل 2% إلى 80% في المياه. الحصول على البيانات عبر مجموعة m/z من 350-4000 في وضع أيون إيجابية مع جهد مخروط من 150v.
- ديكونفولوتي البيانات الخام باستخدام البرمجيات المناسبة. حساب الفرق في الكتلة بين تعديل وأجسام غير معدلة.
3-تحليل الاستقرار الربط ديهيدروبيريدازيني في Trastuzumab(TAMRA)2 في مصل الدم
- تصفية المصل باستخدام عامل تصفية 0.22 ميكرومتر تحت ظروف معقمة. يمكنك إضافة 100 وحدة/مل البنسلين، و 100 ميكروغرام/مل والستربتوميسين.
- سد الآبار الخارجية للوحة 96-جيدا مع الماء. في الآبار المركزية، خلط في ثلاث ميليلتر 90 من المصل الذي تم تصفيته مع 10 ميليلتر من 1 ملغ/مل trastuzumab(TAMRA)2 في برنامج تلفزيوني بتركيز 0.1 مغ/مل نهائي. ضع اللوحة في حاضنة المشبعة بالرطوبة في 37 درجة مئوية و 4-5% CO2.
- كل 24 ساعة طوال 5 أيام، بيبيت كل جيدا جيدا للمزيج، تتخذ من ميليلتر 5 الكوة، فلاش-التجميد بالنيتروجين السائل، وتخزينها في-80 درجة مئوية.
- مرة واحدة وقد جمعت جميع العينات، ذوبان الجليد في مختبرين وتحليلها باستخدام أليسا غير مباشرة كما ذكر سابقا12 مع بعض التعديلات:
- معطف صفيحة 96-جيدا بين عشية وضحاها مع 0.25 ميكروغرام/مل HER2 عند 4 درجة مئوية. يتم تنفيذ كافة الخطوات الأخرى في درجة حرارة الغرفة.
- اليوم التالي، يغسل 5 مرات مع برنامج تلفزيوني 0.05% توين (برنامج تلفزيوني-T) وكتلة مع ألبومين المصل البقري 1% ح 1.
- أغسل واحتضان هذه العينات في إضعاف 1:10000 في برنامج تلفزيوني عن ح 2.
- أغسل واحتضان جسم طمره المضادة المثارة في الماوس في إضعاف 1:2000 في برنامج تلفزيوني-T مع جيش صرب البوسنة 0.5% ح 1.
- أغسل واحتضانها ماوس المضادة HRP المتقارنة 1: 1000 في برنامج تلفزيوني-T مع جيش صرب البوسنة 0.5% ح 1.
- إضافة TMB والسماح للرد 5-10 دقيقة.
- وقف رد الفعل مع 50 ميليلتر ح2حتى4 م 1 وقياس امتصاص 450 نانومتر. طرح الخلفية التي تقاس في 570 نانومتر.
- تناسب منحنى انحدار اللوجستي 4-معلمة لتخفيف القياسية واقحم القياسات من العينات.
ملاحظة: يمكن تقييم استقرار trastuzumab(MMAE)2 استخدام البروتوكول نفسه عن طريق تغيير المقايسة الموصوفة في 3.3 لمجموعه أليسا تجارية لقياس تركيز ADC.
4-تقييم سيتوتوكسيسيتي ADC
ملاحظة: هذا البروتوكول على أساس فحوصات سبق الإبلاغ عنها23،26 مع بعض التعديلات.
- ذوبان الجليد كورونا-BR-3 وخلايا mcf-7 والسماح لهم بالاستيطان في قوارير p25 تتضمن المتوسطة كاملة، أي إبطال دميم وتستكمل مع الحرارة 10% مصل بقرى الجنين و 100 وحدة/مل البنسلين 100 ميكروغرام/مل والستربتوميسين.
- تقسيم الخلايا في التقاء 80-90% (كل 3-4 أيام) على الأقل مرتين قبل المقايسة.
- يومين قبل الفحص، سد الآبار الخارجي من صفيحة 96-جيدا مع الماء. ثم رفع الخلايا مع التربسين 0.05% في 0.5 مم يدتا، الطرد المركزي 3 دقيقة على 250 x ز، ريسوسبيند في الوسيلة الجديدة والبذور الخلايا 3000 في 100 ميليلتر كل بئر (فارغة) في لوحات 96-جيدا.
- يومين بعد زرع الخلايا، وإعداد 10 تخفيف المسلسل من جميع العينات في ثلاث نسخ مع [دمس] 0.1% في المتوسط كاملة. النظر في النماذج وعناصر التحكم التالية: trastuzumab(MMAE)2، trastuzumab(CypK)2، ونوع البرية تراستوزوماب، تيترازيني-فكمماي وما.
- إضافة 100 ميليلتر من كل عينة في كل بئر واحتضان لمدة 5 أيام في شركة 37 درجة مئوية و 4-5%2.
- في يوم 5، قياس بقاء الخلية. وتحقيقا لهذه الغاية، استخدام أدوات تجارية الخلايا وقياس ATP إصدارها. رسم النسبة المئوية للإشارة فيما يتعلق بمراقبة الخلايا تعامل مع [دمس] 0.1%.
ملاحظة: يمكن المحتضنة لمدة 5 أيام في مصل الدم ADCs وجزيئي سيتوتوكسيسيتي أن يثبت الاستقرار الوظيفي.
تنبيه: ما شديد السمية. لذلك استخدام قفازات ونظارات واقية عند التعامل مع المشتقات ما. إذا كنت تستخدم ما غير معدلة كعنصر تحكم في التجربة، عند إعداد الحل الأسهم في [دمس]، التعامل مع المنتج الصلبة داخل غطاء دخان.
النتائج
نظام التعبير عنها عابرة (الشكل 1a) غلة 22 ± 2 مغ من trastuzumab(CypK)2 لتر من الثقافة المتوسطة، التي تمثل 2/3 جسم نوع البرية تنتج بموجب نفس الشروط (الشكل 1 ج). خط الخلية مستقرة يمكن زيادة هذا المحصول يصل إلى 2 مغ/لتر ± 3121.
Trastuzumab(CypK)2 يمكن أن يكون مترافق مع تيترازيني-فكماي، التي تعطي trastuzumab(MMAE) متجانسة أو شبه2 ضمن ح 3 عند 25 درجة مئوية (الشكل 2). هيدروفوبيسيتي عالية من هذا سيتوتوكسين يتطلب إضافة 10% الاسيتو الانيتريل عند 5 أو تستخدم مكافئات المولى المزيد من السمية الواحدة سيبك. بدلاً من ذلك، سيكلواديتيون اكتمال أيضا ضمن ح 20 باستخدام معادلات 2 من تيترازيني-فكمماي دون الاسيتو الانيتريل (الشكل 2 (ج)). Trastuzumab(CypK)2 يتفاعل مع تيترازيني-طمره ضمن ح 2 عند 25 درجة مئوية وح 3-6 مطلوبة عندما انخفضت درجة الحرارة إلى 4 درجات مئوية (الشكل 3 ج).
دار المتوقعة ل trastuzumab(MMAE)2 يقاس [هبلك]-التحالف الدولي للموئل هو 1.9 (الشكل 2). الذروة في البداية لاحظت في chromatogram في دقيقة 8.0 يمثل جسم أونكونجوجاتيد (دار 0) وأن اختفت تماما عندما يتم الانتهاء من رد فعل. الأنواع مع دار 1 التيس في 9.1-9.6 دقيقة وينبغي أن يكون منطقة < 10% بعد 3 ح؛ والمنتج المستهدف مع 2 دار له فترة استبقاء من 10.5-11.0 مع منطقة المتوقعة > 90%. ويؤكد تحول التنقل والأسفار في الحزب الديمقراطي الصربي صفحة المواد الهلامية إدراج تمارا (الشكل 3b) وهوية إيمونوكونجوجاتيس يمكن التحقق منه ب MS LC (الشكل 2d-ه و 3d الشكل).
حضانة trastuzumab(TAMRA)2 لمدة 5 أيام في مصل الدم البشري والتحليل اللاحق بإليزا يؤكد أن الحمولة لا تزال متمسكة بالجسم (الشكل 4 باء). فيما يتعلق بالفحص سيتوتوكسيسيتي، trastuzumab(MMAE)2 يوضح فاعلية عالية في الثدي كورونا-BR-3 (HER2 عالية) الخلايا السرطانية، مع تركيز فعالية قصوى نصف (المفوضية الأوروبية50) من 55 ± 10:00 م (الشكل 4 د). وتحتفظ Trastuzumab(MMAE)2 سيتوتوكسيسيتي بعد 5 أيام حضانة في مصل الدم البشري (الشكل 4 ج). على العكس من ذلك، عندما ADC هو جزيئي في MCF-7 (HER2 منخفض) من المفوضية الأوروبية50 200-fold السفلي (الشكل 4 د). جسم نوع البرية و trastuzumab(CypK)2 وتيترازيني-فكماي إظهار سمية منخفضة للغاية (د 4 أرقام و 4e)، بينما يعرض ما سيتوتوكسيسيتي غير انتقائية عالية في كلا خطوط الخلايا (4e الشكل).
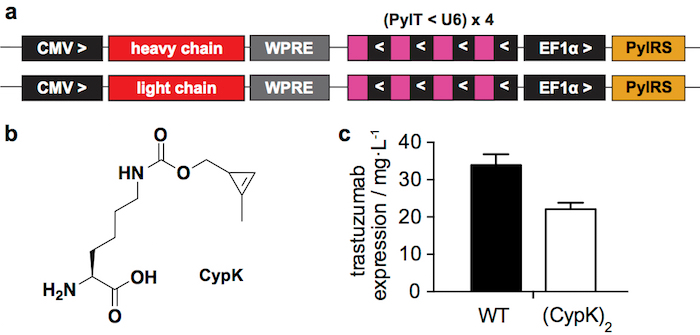
رقم 1: نظام تعبير عابر. ألف المناطق ذات الصلة من البلازميدات المستخدمة تعداء عابر في الخلايا HEK293. CMV: الفيروس المضخم للخلايا المروج، وبر: وودكوك الالتهاب الكبدي فيروس بوسترانسكريبشونال العنصر التنظيمي، بيلت: بيروليسيل الحمض الريبي النووي النقال، U6: محددة المروج، بيلرس: بيروليسيل الحمض الريبي النووي النقال سينثاتيز، > و <: الاتجاه للنسخ. ب Nاليورو--[((2-methylcycloprop-2-en-1-yl)methoxy)carbonyl]-L-lysine (سيبك). (ج) التعبير غلة من نوع البرية (WT) تراستوزوماب ولطخة trastuzumab(CypK)2 التي تقاس بالغربية بعد البروتين على تنقية. أشرطة الخطأ يمثل الانحراف المعياري تريبليكاتيس البيولوجية. تم تعديل هذا الرقم مع إذن من سالفيا Oller et al. 21من عام 2018. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
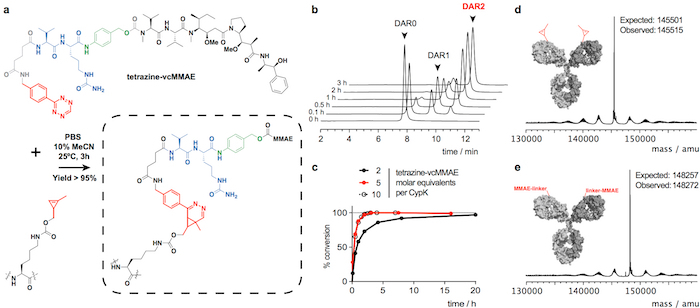
الشكل 2: تصريف trastuzumab(CypK)2 مع تيترازيني-فكمماي. ألف سيكلواديشن ديلز-الدر الطلب إلكترون معكوس بين بقايا سيبك في الجسم ومشتقة تيترازيني ما. ويسلط الضوء على هذه الجماعات في رد الفعل باللون الأحمر، وهو يصور فأمينوبينزيلالكوهول في dipeptide citrulline فالين باللون الأزرق والأخضر. باء [هبلك]-التحالف الدولي للموئل تشروماتوجرامس عرض التقدم المحرز في تصريف الأجسام المضادة. جيم درجة التحويل فيما يتعلق بدار الأقصى من 1.9 استخدام تركيزات كاشف مختلفة. د-هاء ديكونفولوتيد أطياف الشامل لجسم كامل طول قبل وبعد التصريف. وحصل Trastuzumab(CypK)2 باستخدام خط الخلية مستقرة. تم تعديل هذا الرقم مع إذن من سالفيا Oller et al. 21من عام 2018. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
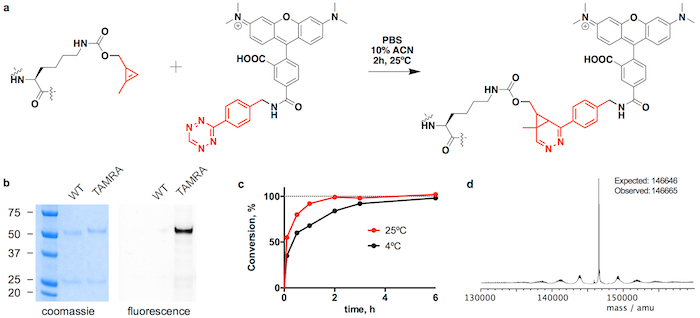
الشكل 3: تصريف trastuzumab(CypK)2 مع تيترازيني-طمره. ألف سيكلواديشن ديلز-الدر الطلب إلكترون معكوس بين بقايا سيبك في الجسم ومشتقة تيترازيني طمره. باء الهلام الحزب الديمقراطي الصربي صفحة عرض التحول التنقل والأسفار في جل نشأت عن طريق تصريف طمره. جيم حركية التصريف في درجات حرارة مختلفة اثنين. دال ديكونفولوتيد الطيف الشامل من trastuzumab(TAMRA)2- وحصل Trastuzumab(CypK)2 باستخدام خط الخلية مستقرة. تم تعديل هذا الرقم مع إذن من سالفيا Oller et al. 21من عام 2018. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
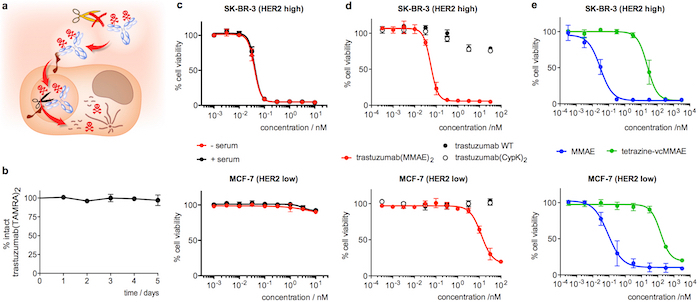
الشكل 4: الاستقرار في مصل الدم وسيتوتوكسيسيتي من يصرف تراستوزوماب. ألف الكرتون تسليط الضوء على الميزات التي رغبت في استبطان ADC. ب الاستقرار في trastuzumab(TAMRA)2 في مصل الدم البشري الذي يقاس في أليسا. جيم خلية مقايسة البقاء مع trastuzumab(MMAE)2 بعد 5 أيام في مصل الدم البشري (+ المصل، أسود). نموذج تحكم المحتضنة في برنامج تلفزيوني بدلاً من المصل (-المصل، أحمر) أدرج في التحليل نفسه. دال خلية مقايسة البقاء مع عينات جسم الطازج المخفف. هاء خلية مقايسة البقاء مع الطازج المخفف ما المشتقات. أشرطة الخطأ تمثل الخطأ القياسي لمتوسط 3 تجارب مستقلة. تم تعديل هذا الرقم مع إذن من سالفيا Oller et al. 21من عام 2018. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
Discussion
الإجراء تعبير عابر لإنتاج trastuzumab(CypK)2 الموصوفة في هذا البروتوكول بسيطة ويسمح لنمطية عالية. الغلات داخل تلك المتوقعة في إعداد أكاديمي27 ويمكن إنشاء خطوط الخلايا مستقرة لمواصلة تعزيز غلة الإنتاج21. أثناء التعبير، تركيزات سيبك أقل من 5 مم قد يؤدي إلى انخفاض نكا التأسيس، ومبالغ أعلى قد يؤثر على نمو الخلايا وانخفاض غلة الأجسام المضادة. سيبك الأحماض الأمينية حرة الذوبان في الماء منخفضة، وبالتالي ينبغي أن يحل أولاً في 100 ملم في 0.1 M هيدروكسيد الصوديوم وثم أضيف إلى متوسط الثقافة. بعد تمييع سيبك في الأجل المتوسط وقبل إضافتها إلى الخلايا، من المهم لتحييد المتوسطة مع HCl وتصفية وتعقيم. وفي وقت لاحق، استخدام الكواشف تعداء المحددة في هذا البروتوكول وبعد أوقات الاحتضان الذي أوصت به الشركة المصنعة مهم لتعبير عالية الغلة. لمزيد من التفاصيل عن التعبير عابرة من الأجسام المضادة البشرية، يحال القارئ إلى أخرى البروتوكولات المنشورة31،32.
عندما يتم تنقيتها الضد، مطلوب فائض عالية من الراتنج البروتين A كما هو مبين لضمان سحب جسم كامل أسفل من المادة طافية. من أجل منع هطول الأمطار تراستوزوماب أثناء شطف، من يوصي باستخدام حل مع التخزين المؤقت عالية القدرة، وتمييع فورا مع برنامج تلفزيوني وتبادل في المخزن المؤقت لتجنب الإفراط في تركيز. دائماً الحفاظ الجسم < 5 ملغ/مل.
تصريف trastuzumab(CypK)2 مع تيترازيني-فكماي أسرع من معظم ردود الفعل ذكرت مع مقابض بيورثوجونال أخرى ل ADCs. وعلاوة على ذلك، يحدث هذا سيكلاديتيون تحت ظروف خفيف جداً: درجة حرارة الغرفة أو الأس الهيدروجيني أقل والفسيولوجية. من المهم أن تمييع الحلول [دمس] الأسهم من كواشف مختبر مع الاسيتو الانيتريل قبل إضافة برنامج تلفزيوني والأجسام المضادة؛ وإلا سوف يعجل بمشتقات تيترازيني. الاسيتو الانيتريل مطلوب فقط بسبب هيدروفوبيسيتي العالية ما وطمره، ولكن أقل من جزيئات الماء قد لا تحتاج إلى إضافة مادة مذيبة المشارك. بدلاً من ذلك، يمكن أن يكون مترافق تيترازيني-فكماي دون الاسيتو الانيتريل ومكافئات المولى 2 فقط من تيترازيني-فكماي ضمن ح 20. يمكن أن يشمل هذا المبلغ قليلاً من السمية حدوث انخفاض كبير في تكلفة التصنيع ADC بالمقارنة مع التكنولوجيات الحالية المستندة إلى نكا. Trastuzumab(CypK)2 رد الفعل تماما لمدة 4 أشهر على الأقل عند الحفاظ عليها عند 4 درجة مئوية.
[هبلك]-التحالف الدولي للموئل يمكن تحديد دقيق لدار منذ ما هو مسعور جداً ويوفر حل ممتاز لقمم المقابلة لجسم يصرف مع السموم 0، 1 و 2. تيترازيني-فكمماي الممتص الوتيس حوالي 13.7 دقيقة ويتم الكشف عن في 280 نانومتر. ويتطلب هذا الأسلوب مادة بدءاً بدرجة نقاء عالية. وعلاوة على ذلك، لا يوصي لإخماد التفاعل مع الجزيئات المتفاعلة تيترازيني الأخرى مثل أوه BCN نظراً لأنها يمكن أن تغير الأوقات الاحتفاظ وشكل القمم. فمن الضروري أن تركيز الملح من العينات يطابق أحد في المرحلة المتنقلة في بداية التدرج بغية الحصول على فصل جيدة، خاصة إذا كان يتم حقن أكثر من 10-20 ميليلتر.
فيما يتعلق بالتحليل LC-مرض التصلب العصبي المتعدد، وديجليكوسيليشن عينات جسم المطلوبة للحصول على ذروة واحدة عند deconvolution الطيف الخام. قد تختلف دقة جسم الكلية، والجماهير ADC كاليبريشن الصك. ومن ثم، من أجل حساب الكتلة للتعديل، طرح كتلة الحصول على أجسام غير معدلة عن تلك التي تم الحصول عليها ADC. ينبغي أن توفر مطيافات أسلحة ذات الدقة العالية الحديثة خطأ نسبي أقل 1:10000. على الرغم من أن يمكن أيضا استخدام LC-مرض التصلب العصبي المتعدد لحساب النسبة بين الأنواع المختلفة، هذه القيمة هي عادة ما تكون المبالغة في تقدير نظراً لأن التعديل قد تؤثر على قدرة التأين للأنواع التي تم إنشاؤها، وقد لا يتم الكشف عن كميات قليلة من الشوائب.
استقرار الرابط في ADCs حرج لأنه سابق لأوانه الإفراج عن المخدرات ينتج سمية أعلى وأدنى من الفعالية؛ سيتوتوكسين الحرة أضرار الأنسجة السليمة وجسم عارية تتنافس مع أحد المسلحين لمواقع الربط المستهدف على الخلايا المريضة. إصدار أقل من 5%، وضمن مدى تغير الإنزيم الاستقرار، ينبغي أن يتوقع.
وأخيراً، انتقائية ADC استهداف HER2 مثل trastuzumab(MMAE)2 يمكن تقييمها عن طريق مقارنة سيتوتوكسيسيتي في خلايا كورونا-BR-3 (HER2 عالية) وخلايا mcf-7 (HER2 منخفض) منذ الأخير أعرب عن 15-fold مستقبلات HER2 أقل من السابق28 . من المتوقع أن يؤدي إلى بقاء خلية الأقل 2 أوامر من حجم أقل في كورونا-BR-3 بالمقارنة مع MCF 7 إيمونوكونجوجاتي. المفوضية الأوروبية50 كورونا-BR-3 ينبغي أن تكون في نطاق nanomolar رقمين مما يعكس ارتفاع فاعلية هذه ADC29،30. جسم غير معدلة، trastuzumab(MMAE)2 أو تراستوزوماب، ينبغي أن تظهر لا سمية في هذا التحليل. يجب أن يكون تيترازيني-فكماي تأثير 3 أوامر من حجم أقل من ADC حيث يزيل الرابط نشاط السم بيبتيدوميميتيك. على العكس من ذلك، نظراً لما يمكن أن تتخلل غشاء الخلية30، فإنه ينبغي أن سمية مماثلة إلى ADC ولكنها عرض أي تمييز بين HER2 عالية وخطوط الخلايا منخفض HER2. وعلاوة على ذلك، إذا كان يتم إجراء هذا الفحص بعد حضانة 5 أيام من ADC في مصل الدم، يمكن استخدامه لتوفير دليل فنية لاستقرار الرابط: الإفراج عن السم من شأنه أن يؤدي إلى أما انخفاضا في كفاءة ADC في كورونا-BR-3 إذا ما أفرج عنه مع ف فن الرابط أو نقصانا في انتقاء إذا كان المشقوق الرابط بطريقة تراسلس.
وتسمح هذه التقنية ADC الموضحة هنا إدماج سيكلوبروبيني مشتق ليسين كفاءة والمعينة للموقع في IgG1s. بعد تنقية سهلة، يمكن أن الأجسام المضادة مترافق سريعاً مع الجزيئات التي تحتوي على تيترازيني، مما أسفر عن منتجات متجانسة. نظراً لصغر حجمها وتفاعلية عالية للتعامل مع الحد الأدنى سيكلوبروبيني، ينبغي أن تمكن هذا الأسلوب على تصريف حمولات أعاقت ستيريكالي. إيمونوكونجوجاتيس الناتجة هي مستقرة في مصل الدم وقوية للغاية وانتقائية. وعموما، تمكن سيبك ربط بيورثوجونال الخاصة بالموقع ومستقر وسريع للأجسام المضادة وغيرها يصرف البروتين لاستخدامها في العلاج أو التشخيص.
Disclosures
الكتاب ليس لها علاقة بالكشف عن.
Acknowledgements
وأيد هذا العمل "مجلس البحوث الطبية"، المملكة المتحدة. B.O.-س. حاصل زمالة التطريز (أتلف 158-2016)، وتشعر بالامتنان بيلهام H. والذقن فولفجانج للدعم وليم غ.، مورغان الأميركي جيم وسين بيريسيتش للمساعدة والمشورة.
Materials
| Name | Company | Catalog Number | Comments |
| Expi293F | ThermoFisher Scientific | A14527 | HEK suspension cells |
| Expi293 Expression Medium | ThermoFisher Scientific | A1435101 | Expression medium |
| Antibiotic-antimycotic | ThermoFisher Scientific | 15240062 | Penicillin-streptomycin-amphotericin B |
| 125mL Polycarbonate Erlenmeyer Flask with Vent Cap | Corning | 431143 | Shake flasks |
| Brunswick S41i incubator | Eppendorf | S41I230011 | CO2 incubator with a shaker |
| Sodium hydroxide 4 mol/l (4 N) in aqueous solution | VWR | 191373M | |
| Cyclopropene lysine | Sichem | SC-8017 | In this study it was synthesized as described by Elliot et al. 2014 |
| Steriflip-GP, 0.22 µm, polyethersulfone, gamma irradiated | Merck Millipore | SCGP00525 | |
| Opti-MEM, Reduced Serum Medium | ThermoFisher Scientific | 31985070 | Reduced serum medium |
| ExpiFectamine 293 Transfection Kit | ThermoFisher Scientific | A14525 | Transfection reagent |
| 5810 R centrifuge | Eppendorf | 5811000460 | |
| Millex-GP Syringe Filter Unit, 0.22 µm, polyethersulfone, 33 mm, gamma sterilized | Merck Millipore | SLGP033RS | |
| Protein A resin | Sino Biological | 10600-P07E-RN-25 | |
| Poly-Prep Chromatography Columns, Pkg of 50 | Bio-Rad | 7311550 | Polypropylene chromatography column |
| Econo-Column Funnel | Bio-Rad | 7310003 | |
| Sodium citrate | Fluka | 71635 | |
| ÄKTA explorer FPLC | GE Healthcare | ||
| HiTrap HIC Selection Kit | GE Healthcare | 28-4110-07 | Includes HiTrap 1 mL Butyl HP |
| Ammonium sulfate | VWR | 2133.296 | |
| Isopropanol | Honywell | 34863-2.5L | |
| Dymethyl sulfoxide | Sigma-Aldrich | D8418-50ML | |
| Tetrazine-vcMMAE | ChemPartner | - | Costum synthesized |
| Tetrazine-5-TAMRA | Jena Bioscience | CLK-017-05 | |
| NuPAGE 4-12% Bis-Tris Gel 1.0mm x 10 well | ThermoFisherScientific | NP0321BOX | |
| Xcell SureLock Mini-Cell | ThermoFisherScientific | EI0001 | |
| UltiMate 3000 HPLC | ThermoFisherScientific | ||
| Thermo Scientific MAbPac, HIC-20, 4.6 x 100 mm, 5 µm | ThermoFisherScientific | 088553 | |
| PNGase F | New England BioLabs | P0704S | |
| NanoAcquity | Waters | ||
| C4 BEH 1-5 µm 1.0 x 100 mm UPLC column | Waters | ||
| 96-well microplates for cell culture | ThermoFisherScientific | 156545 | |
| Human serum | Sigma-Aldrich | H4522-20mL | |
| CO2 incubator | Panasonic | ||
| HER2 ECD | Sino Biological | 10004-HCCH | |
| Anti-TAMRA | Abcam | an171120 | |
| Anti-mouse HRP | Santa Cruz | sc-2005 | |
| TMB | BioLengend | 421101 | |
| Sulfuric acid | Sigma-Aldrich | 84727-500ML | |
| PHERAstar FS | BMG Labtech | Plate reader | |
| DMEM | Sigma-Aldrich | D5671-500ML | |
| SK-BR-3 | ATCC | HTB-30 | |
| MCF-7 | ATCC | HTB-22 | |
| CellTiterGlo 2.0 Assay | Promega | G9242 | Cell viability assay based on the measurement of ATP released after cell lysis. The output signal is luminscence. |
| Monomethyl Auristatin E | Cayman Chemical | 16267 | |
| NanoDrop 2000 | ThermoFisherScientific | Microvolume spectrophotometer | |
| Human IgG ELISA Quantificaiton Set | Bethyl | E80-104 | |
| MaxEnt1 in MassLynx | Waters | Software application for mass spectrum deconvolution | |
| IntantBlue | Expedeon | ISB1L | Coomassie-based stain |
| Intact MMAE-ADC ELISA Kit (Sandwich Assay) | Epitope Diagnostics, Inc. | KTR 782 | |
| Tube 50 mL, 114x28mm, PP | Sarstedt | 62.547.254 | Conical tube |
| Amicon Ultra-15 Centrifugal Filter Units 50,000 NMWL | Merck | UFC905024 | Centrifugal filtration concentrator (after protein A pull down) |
| Amicon Ultra-4 Centrifugal Filter Units 50,000 NMWL | Merck | UFC805024 | Centrifugal filtration concentrators (after FPLC or HPLC purification) |
| Zeba Spin Desalting Columns, 7K MWCO, 0.5 mL | ThermoFisherScientific | 89882 | Size exclusion spin columns |
| Tube PCR 0.2ml Flat Cap | Thistle Scientific Ltd | AX-PCR-02-C-CS | PCR tubes |
| Nunc MaxiSorpª flat-bottom | ThermoFisherScientific | 44-2404-21 | Plates for ELISA |
References
- Beck, A., Goetsch, L., Dumontet, C., Corvaia, N. Strategies and challenges for the next generation of antibody-drug conjugates. Nature Reviews Drug Discovery. 16 (5), 315-337 (2017).
- Wakankar, A. A., et al. Physicochemical Stability of the Antibody−Drug Conjugate Trastuzumab-DM1: Changes due to Modification and Conjugation Processes. Bioconjugate Chemistry. 21 (9), 1588-1595 (2010).
- Stan, A. C., Radu, D. L., Casares, S., Bona, C. A., Brumeanu, T. -. D. Antineoplastic Efficacy of Doxorubicin Enzymatically Assembled on Galactose Residues of a Monoclonal Antibody Specific for the Carcinoembryonic Antigen. Cancer Research. 59 (1), 115-121 (1999).
- Hamblett, K. J., et al. Effects of Drug Loading on the Antitumor Activity of a Monoclonal Antibody Drug Conjugate. Clinical Cancer Research. 10 (20), 7063-7070 (2004).
- Chari, R. V. J., Miller, M. L., Widdison, W. C. Antibody-Drug Conjugates: An Emerging Concept in Cancer Therapy. Angewandte Chemie International Edition. 53 (15), 3796-3827 (2014).
- Chin, J. W. Expanding and Reprogramming the Genetic Code. Nature. 550 (7674), 53-60 (2017).
- Axup, J. Y., et al. Synthesis of Site-Specific Antibody-Drug Conjugates Using Unnatural Amino Acids. Proceedings of the National Academy of Sciences of the United States of America. 109 (40), 16101-16106 (2012).
- Hallam, T. J., Wold, E., Wahl, A., Smider, V. V. Antibody Conjugates with Unnatural Amino Acids. Molecular Pharmaceutics. 12 (6), 1848-1862 (2015).
- Tian, F., et al. A General Approach to Site-Specific Antibody Drug Conjugates. Proceedings of the National Academy of Sciences of the United States of America. 111 (5), 1766-1771 (2014).
- Kern, J. C., et al. Discovery of Pyrophosphate Diesters as Tunable, Soluble, and Bioorthogonal Linkers for Site-Specific Antibody-Drug Conjugates. Journal of the American Chemical Society. 138 (4), 1430-1445 (2016).
- Zimmerman, E. S., et al. Production of Site-Specific Antibody-Drug Conjugates Using Optimized Non-Natural Amino Acids in a Cell-Free Expression System. Bioconjugate Chemistry. 25 (2), 351-361 (2014).
- VanBrunt, M. P., et al. Genetically Encoded Azide Containing Amino Acid in Mammalian Cells Enables Site-Specific Antibody-Drug Conjugates Using Click Cycloaddition Chemistry. Bioconjugate Chemistry. 26 (11), 2249-2260 (2015).
- Xiao, H., et al. Genetic Incorporation of Multiple Unnatural Amino Acids into Proteins in Mammalian Cells. Angewandte Chemie International Edition. 52 (52), 14080-14083 (2013).
- Milles, S., et al. Click Strategies for Single-Molecule Protein Fluorescence. Journal of the American Chemical Society. 134 (11), 5187-5195 (2012).
- Lallana, E., Riguera, R., Fernandez-Megia, E. Reliable and Efficient Procedures for the Conjugation of Biomolecules through Huisgen Azide-Alkyne Cycloadditions. Angewandte Chemie International Edition. 50 (38), 8794-8804 (2011).
- Koehler, C., et al. Genetic Code Expansion for Multiprotein Complex Engineering. Nature Methods. 13 (12), 997-1000 (2016).
- Lyon, R. P., et al. Reducing Hydrophobicity of Homogeneous Antibody-Drug Conjugates Improves Pharmacokinetics and Therapeutic Index. Nature Biotechnology. 33 (7), 733-735 (2015).
- Elliott, T. S., et al. Proteome Labeling and Protein Identification in Specific Tissues and at Specific Developmental Stages in an Animal. Nature Biotechnology. 32, 465-472 (2014).
- Ravasco, J. M. J. M., Monteiro, C. M., Trindade, A. F. Cyclopropenes: A New Tool for the Study of Biological Systems. Organic Chemistry Frontiers. 4 (6), 1167-1198 (2017).
- Yang, J., Šečkutė, J., Cole, C. M., Devaraj, N. K. Live-Cell Imaging of Cyclopropene Tags with Fluorogenic Tetrazine Cycloadditions. Angewandte Chemie International Edition. 124 (30), 7594-7597 (2012).
- Oller-Salvia, B., Kym, G., Chin, J. W. Rapid and Efficient Generation of Stable Antibody-Drug Conjugates via an Encoded Cyclopropene and an Inverse-Electron-Demand Diels-Alder Reaction. Angewandte Chemie International Edition. 57, 2831-2834 (2018).
- Schmied, W. H., Elsässer, S. J., Uttamapinant, C., Chin, J. W. Efficient Multisite Unnatural Amino Acid Incorporation in Mammalian Cells via Optimized Pyrrolysyl tRNA Synthetase/tRNA Expression and Engineered eRF1. Journal of the American Chemical Society. 136 (44), 15577-15583 (2014).
- Junutula, J. R., et al. Site-Specific Conjugation of a Cytotoxic Drug to an Antibody Improves the Therapeutic Index. Nature Biotechnology. 26 (8), 925-932 (2008).
- Junutula, J. R., et al. Rapid Identification of Reactive Cysteine Residues for Site-Specific Labeling of Antibody-Fabs. Journal of Immunological Methods. 332 (1), 41-52 (2008).
- Doronina, S. O., et al. Development of potent monoclonal antibody auristatin conjugates for cancer therapy. Nature Biotechnology. 21 (7), 778-784 (2003).
- Shiraishi, Y., et al. Identification of Highly Reactive Cysteine Residues at Less Exposed Positions in the Fab Constant Region for Site-Specific Conjugation. Bioconjugate Chemistry. 26 (6), 1032-1040 (2015).
- Sabourin, M., et al. Increasing Antibody Yield and Modulating Final Product Quality using the Freedom(TM). CHO-S(TM) Production Platform. BMC Proceedings. 5 (8), 102 (2011).
- Xiao, Y., Gao, X., Maragh, S., Telford, W. G., Tona, A. Cell Lines as Candidate Reference Materials for Quality Control of ERBB2 Amplification and Expression Assays in Breast Cancer. Clinical Chemistry. 55 (7), 1307-1315 (2009).
- Shinmi, D., et al. One-Step Conjugation Method for Site-Specific Antibody-Drug Conjugates through Reactive Cysteine-Engineered Antibodies. Bioconjugate Chemistry. 27 (5), 1324-1331 (2016).
- Badescu, G., et al. Bridging Disulfides for Stable and Defined Antibody Drug Conjugates. Bioconjugate Chemistry. 25 (6), 1124-1136 (2014).
- Vazquez-Lombardi, R., et al. Transient expression of human antibodies in mammalian cells. Nature Protocols. 13 (1), 99-117 (2018).
- Baldi, L., Hacker, D. L., Meerschman, C., Wurm, F. M., Hartley, J. L. . Protein Expression in Mammalian Cells: Methods and Protocols. , 13-26 (2012).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved