A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
تحديد حركية التشغيل في المختبر والخلوية لأبتامير الحمض النووي الريبي الفلوري
In This Article
Summary
يقدم البروتوكول طريقتين لتحديد حركية أبتامير الحمض النووي الريبي الفلوري السبانخ2 والبروكلي. تصف الطريقة الأولى كيفية قياس حركية الأبتامير الفلورية في المختبر باستخدام قارئ الألواح ، بينما توضح الطريقة الثانية قياس حركية الأبتامير الفلورية في الخلايا عن طريق قياس التدفق الخلوي.
Abstract
تم تطبيق أبتامير الحمض النووي الريبي الفلوري في الخلايا الحية لوضع علامة على الحمض النووي الريبي وتصوره ، والإبلاغ عن التعبير الجيني ، وتنشيط المستشعرات الحيوية الفلورية التي تكتشف مستويات المستقلبات وجزيئات الإشارة. من أجل دراسة التغيرات الديناميكية في كل من هذه الأنظمة ، من المستحسن الحصول على قياسات في الوقت الفعلي ، لكن دقة القياسات تعتمد على حركية التفاعل الفلوري أسرع من تردد أخذ العينات. هنا ، نصف طرق تحديد حركية التشغيل في المختبر والخلوية لأبتامير الحمض النووي الريبي الفلوري باستخدام قارئ لوحة مجهز بحاقن عينة ومقياس تدفق خلوي ، على التوالي. لقد أظهرنا أن الحركية في المختبر لتنشيط التألق ل Spinach2 و Broccoli aptamers يمكن نمذجتها على أنها تفاعلات ارتباط ثنائية الطور ولها ثوابت معدل طور سريع مختلفة تبلغ 0.56 s−1 و 0.35 s−1 ، على التوالي. بالإضافة إلى ذلك ، نظهر أن الحركية الخلوية لتنشيط التألق للسبانخ2 في الإشريكية القولونية ، والتي يتم تقييدها بشكل أكبر بسبب انتشار الصبغة في البكتيريا سالبة الجرام ، لا تزال سريعة بما يكفي لتمكين تردد أخذ العينات بدقة على مقياس زمني دقيق. تنطبق هذه الطرق لتحليل حركية تنشيط التألق على أبتامات الحمض النووي الريبي الفلورية الأخرى التي تم تطويرها.
Introduction
التفاعلات الفلورية هي تفاعلات كيميائية تولد إشارة مضان. عادة ما تؤدي أبتامير الحمض النووي الريبي الفلوري هذه الوظيفة عن طريق ربط صبغة جزيء صغيرة لتعزيز عائدها الكمي الفلوري (الشكل 1 أ)1. تم تطوير أنظمة أبتامير RNA مختلفة الفلوروجين وتتكون من تسلسلات محددة من الحمض النووي الريبي أبتامير وروابط الصبغة المقابلة1. تم إلحاق أبتامير الحمض النووي الريبي الفلوري بنسخ الحمض النووي الريبي كعلامات فلورية تمكن من تصوير الخلايا الحية ل mRNAs و RNAs غير المشفرة2،3،4. كما تم وضعها بعد تسلسل المروج كمراسلين فلورسنت للتعبير الجيني ، على غرار استخدام بروتين الفلورسنت الأخضر (GFP) كمراسل ، باستثناء وظيفة الإبلاغ عند مستوى الحمض النووي الريبي 5,6. أخيرا ، تم دمج أبتامير الحمض النووي الريبي الفلوري في أجهزة الاستشعار الحيوية الفلورية القائمة على الحمض النووي الريبي ، والتي تم تصميمها لتحفيز التفاعل الفلوري استجابة لجزيء صغير معين. تم تطوير أجهزة الاستشعار الحيوية الفلورية القائمة على الحمض النووي الريبي لتصوير الخلايا الحية لمختلف المستقلبات غير الفلورية وجزيئات الإشارة7،8،9،10،11.
هناك اهتمام متزايد بتطوير أبتامير الحمض النووي الريبي الفلوري لتصور التغيرات الديناميكية في توطين الحمض النووي الريبي ، والتعبير الجيني ، وإشارات الجزيئات الصغيرة. لكل من هذه التطبيقات ، من المستحسن الحصول على قياسات في الوقت الفعلي ، لكن دقة القياسات تعتمد على حركية التفاعل الفلوري أسرع من تردد أخذ العينات. هنا ، نصف طرق تحديد حركية المختبر لأبتامير الحمض النووي الريبي الفلوري السبانخ212 والبروكلي13 باستخدام قارئ لوحة مجهز بحاقن عينة ولتحديد حركية التشغيل الخلوي للسبانخ2 المعبر عنها في الإشريكية القولونية باستخدام مقياس التدفق الخلوي. تم اختيار هذين الأبتامير RNA لأنه تم تطبيقهما لدراسة توطين الحمض النووي الريبي2،3،4 ، وقد تم استخدامهما في المراسلين5،6 وأجهزة الاستشعار الحيوية7،8،9،10،11 ، وروابط الصبغة المقابلة (DFHBI أو DFHBI-1T) متاحة تجاريا. ويرد ملخص لخصائصها في المختبر المحددة في الأدبيات في الجدول 14،13،14 ، والذي أبلغ تطوير البروتوكول (على سبيل المثال ، الأطوال الموجية وتركيزات الصبغة المستخدمة). توضح هذه النتائج أن التفاعلات الفلورية المتأثرة بأبتامير الحمض النووي الريبي سريعة ويجب ألا تعيق القياسات الدقيقة للتطبيقات البيولوجية الخلوية المطلوبة.
Protocol
1. تجربة الحركية في المختبر
- إعداد قوالب الحمض النووي بواسطة PCR
- إعداد تفاعل (تفاعلات) تفاعل البوليميراز المتسلسل: لتحضير تفاعلات تفاعل البوليميراز المتسلسل ، ادمج الكواشف التالية في أنبوب PCR رقيق الجدران:
33 ميكرولتر من الماء المقطر المزدوج (ddH2O)
10 ميكرولتر من المخزن المؤقت 5x لبوليميراز الحمض النووي عالي الدقة
5 ميكرولتر من 2 مللي متر لكل ديوكسي ريبونوكليوزيد ثلاثي الفوسفات (dNTP)
0.5 ميكرولتر من 40 ميكرومتر التمهيدي الأمامي
0.5 ميكرولتر من 40 ميكرومتر التمهيدي العكسي
0.5 ميكرولتر (10-100 نانوغرام) من قالب الحمض النووي (ل Spinach2 PCR فقط ؛ تتداخل مواد البروكلي التمهيدية)
0.5 ميكرولتر من بوليميراز الحمض النووي عالي الدقة (أضف الأخير)
ملاحظة: غالبا ما يتم شحن قليل النيوكليوتيدات الاصطناعية جافة. لتحضير محاليل المخزون ، أضف حجما معروفا (يوصى ب 100 ميكرولتر) من ddH2O ، وقم بقياس A260 لهذا المحلول لتحديد التركيز بواسطة قانون بير ، حيث يمكن حساب معامل الانقراض بواسطة قواعد أقرب جار عبر الإنترنت. يمكن بعد ذلك استخدام محلول المخزون هذا لجعل التخفيفات مناسبة للاستخدام في تفاعل البوليميراز المتسلسل. - قم بتشغيل بروتوكول العجلة الحرارية.
- استخدم بروتوكول العجلة الحرارية التالي لتضخيم قوالب الحمض النووي الكاملة للسبانخ2 والبروكلي:
تمسخ الأولي: 98 °C لمدة 2 دقيقة
35 دورة:
تمسخ: 98 °C تمسخ لمدة 15 ثانية
التلدين: 72 °C لمدة 30 ثانية
التمديد: 72 °C لمدة 30 ثانية
التمديد النهائي: 72 درجة مئوية لمدة 5 دقائق. - بعد التفاعل ، قم بتحليل حصة صغيرة من المنتج بنسبة 2٪ هلام الأغاروز جنبا إلى جنب مع سلم منخفض الوزن الجزيئي (نطاق الحجم: 25-766 نيوكليوتيدات) لتأكيد وجود منتج الحمض النووي المطلوب.
- قم بتنقية المنتج عن طريق استخراج الجل المتاح تجاريا أو مجموعات تنظيف PCR وقم بالتخلص من ddH2O أو المخزن المؤقت الذي توفره الشركة المصنعة.
ملاحظة: تأكد عند اختيار مجموعة تنظيف PCR من أن قطع الوزن الجزيئي للعمود منخفض بما يكفي للاحتفاظ ب T7-Broccoli (81 نيوكليوتيدات) ، وإلا فقد منتج PCR.
ملاحظة: نقطة توقف اختيارية: قم بتخزين الحمض النووي عند -20 درجة مئوية.
- استخدم بروتوكول العجلة الحرارية التالي لتضخيم قوالب الحمض النووي الكاملة للسبانخ2 والبروكلي:
- إعداد تفاعل (تفاعلات) تفاعل البوليميراز المتسلسل: لتحضير تفاعلات تفاعل البوليميراز المتسلسل ، ادمج الكواشف التالية في أنبوب PCR رقيق الجدران:
- تحضير السبانخ2 والحمض النووي الريبي البروكلي عن طريق النسخ في المختبر (IVT)
- قم بإعداد تفاعل (تفاعلات) النسخ.
- لتحضير تفاعل نسخ 100 ميكرولتر ، ادمج الكواشف التالية في أنبوب طرد مركزي دقيق سعة 1.5 مل: 10 ميكرولتر من مخزن النسخ المؤقت 10x + 20 ميكرولتر من ثلاثي فوسفات ريبونوكليوزيد 10 مللي متر (rNTPs) + 1-64 ميكرولتر من قالب الحمض النووي (إجمالي 1 ميكروغرام) + 2 ميكرولتر من بيروفوسفاتيز غير العضوي + ddH 2 O إلى 98 ميكرولتر +2ميكرولتر من بوليميراز T7 RNA (أضف الأخير).
- احتضان هذا التفاعل لمدة 4 ساعات عند 37 درجة مئوية. قم بإخماد التفاعل بإضافة 100 ميكرولتر من 2x محلول تحميل هلام اليوريا (2x ULB) ، المكون من 20٪ سكروز ، 0.1٪ كبريتات دوديسيل الصوديوم (SDS) ، 1x Tris-Borate-EDTA (1x TBE) العازلة ، و ~ 18 M اليوريا.
ملاحظة: نقطة توقف اختيارية: قم بتخزين التفاعل المروي عند -20 درجة مئوية.
- قم بإعداد تفاعل (تفاعلات) النسخ.
- بولي أكريلاميد هلام الكهربائي (PAGE) تنقية الحمض النووي الريبي
- صفحة تنقية السبانخ2 والحمض النووي الريبي البروكلي
تنبيه: مادة الأكريلاميد غير المبلمرة (سائلة أو مسحوقة) شديدة السمية. إذا كنت تزن مسحوق الأكريلاميد ، فافعل ذلك في غطاء الدخان. احرص دائما على ارتداء معدات الحماية المناسبة وإزالة القفازات الملوثة بمسحوق أو محلول الأكريلاميد على الفور ، وغسل اليدين جيدا. إذا لامست مادة الأكريلاميد الجلد مباشرة ، اغسل المنطقة المكشوفة لمدة 15 دقيقة على الأقل بالماء والصابون. إذا لامست مادة الأكريلاميد العينين مباشرة ، اغسلهما بالماء لمدة 15 دقيقة.- تحضير جل PAGE: لإزالة النصوص المجهضة غير المرغوب فيها و rNTPs غير المتفاعلة من المنتج الكامل ، قم بإعداد جل اليوريا بولي أكريلاميد بنسبة 6٪. بشكل عام ، يمكن استخدام المواد الهلامية 28 سم × 16.5 سم × 1.5 مم مع مشط 8 جيدا. قم بإعداد معدات الجل والرحلان الكهربائي ، باستخدام 1x TBE buffer لملء الخزانات.
- قم بتحميل عينة (عينات) الحمض النووي الريبي في هلام PAGE: قم بتحميل الجل بتفاعل واحد مروي 200 ميكرولتر لكل حارة. في حارة منفصلة ، قم بتحميل 2x ULB مع أصباغ تعقب زيلين سيانول وبروموفينول الأزرق ، والتي تهاجر في الجل عند 106 نيوكليوتيدات و 26 نيوكليوتيدات ، على التوالي15. اترك حارة فارغة بين كل عينة لتجنب التلوث المحتمل في الخطوات التالية.
- قم بتشغيل جل PAGE: لفصل 95-nt Spinach2 و 49-nt Broccoli عن المنتجات المقطوعة الخاصة بكل منهما ، قم بتشغيل الجل لمدة 1.5-2 ساعة عند 25 W ، وعند هذه النقطة ستكون صبغة البروموفينول الزرقاء قد هاجرت ~ 5/6 من طول الجل.
- تصور عينة (عينات) الحمض النووي الريبي في هلام PAGE: قم بتفكيك الألواح الزجاجية حول الجل وقم بتغطية الجل في غلاف بلاستيكي على كلا الجانبين ، مع وضع علامات على الممرات الموجودة على الغلاف. تصور نطاقات الحمض النووي الريبي في غرفة مظلمة عن طريق التظليل بالأشعة فوق البنفسجية عن طريق وضع الجل الملفوف على لوحة TLC الفلورية تحت ضوء الأشعة فوق البنفسجية. حدد بسرعة حافة نطاقات الحمض النووي الريبي المقابلة للمنتج بقلم تحديد وأطفئ مصباح الأشعة فوق البنفسجية لتقليل الضرر الناتج عن التعرض للأشعة فوق البنفسجية.
- قم باستئصال واستخراج عينة (عينات) الحمض النووي الريبي من هلام PAGE: باستخدام شفرة حلاقة جديدة لكل عينة ، قم باستئصال نطاقات المنتج المطلوبة ، ونرد إلى مكعبات ~ 1 مم ، وأضف قطع الجل إلى أنبوب طرد مركزي دقيق سعة 2 مل مع 500 ميكرولتر من محلول نقع السحق لاستخراج الحمض النووي الريبي على دوار لمدة 2 ساعة في درجة حرارة الغرفة (RT) أو طوال الليل عند 4 درجات مئوية.
ملاحظة: نقطة توقف اختيارية: يمكن تخزين العينة عند -20 درجة مئوية. - ترسب الحمض النووي الريبي
- لفصل قطع الهلام عن الحمض النووي الريبي المستخرج في المخزن المؤقت ، قم بالطرد المركزي للعينة عند 13000 × جم لمدة 20 دقيقة عند 4 درجات مئوية ، ثم استخدم ماصة ضيقة الطرف لاستخراج المادة الطافية وتحميلها في أنبوب طرد مركزي دقيق جديد سعة 2 مل.
- لترسيب الحمض النووي الريبي ، أضف 1.5 مل من الإيثانول المثلج و 1 ميكرولتر من 20 مجم / مل من الجليكوجين ، الدوامة ، وقم بتخزينه لمدة ساعة واحدة على الأقل عند -20 درجة مئوية أو -80 درجة مئوية.
ملاحظة: نقطة توقف اختيارية: يمكن تخزين الحمض النووي الريبي عند -20 درجة مئوية لبضعة أشهر.
- جمع راسب الحمض النووي الريبي: حبيبات الحمض النووي الريبي المترسب عن طريق الطرد المركزي عند 13000 × جم لمدة 20 دقيقة عند 4 درجات مئوية. قم بإزالة المادة الطافية واترك الإيثانول المتبقي يتبخر تحت الهواء الطلق (~ 1 ساعة) قبل إعادة تعليق الحبيبات في 30 ميكرولتر من ddH2O أو 1x TE buffer.
ملاحظة: ينتج عن هذه العملية عادة تركيز نهائي للحمض النووي الريبي يبلغ ~ 10 ميكرومتر.
ملاحظة: نقطة توقف اختيارية: يمكن تخزين عينة الحمض النووي الريبي عند -20 درجة مئوية لبضعة أشهر.
- تحديد تركيزات مخزون الحمض النووي الريبي.
- تحضير حصة الحمض النووي الريبوزي (RNA) لتفاعل التحلل المائي.
- لإجراء هذا الفحص ، أولا ، استخدم مقياس الطيف الضوئي النانوي للأشعة فوق البنفسجية / المرئية لتحديد A260 من عينة الحمض النووي الريبي للمخزون وعمل حصة مخففة للعينة إلى ~ 10 وحدات امتصاص (AU) في ddH2O.
- تحضير التفاعل التالي في أنبوب PCR 0.5 مل: 16 ميكرولتر من ddH 2 O + 2 μL من 10x Na 2 CO3 buffer +2μL من حصص الحمض النووي الريبي المخفف إلى ~ 10 AU. احتضان التفاعل لمدة 90 دقيقة عند 95 درجة مئوية ، ثم اتركه يبرد إلى RT.
- تحديد تركيز الحمض النووي الريبي باستخدام امتصاص النيوكليوتيدات: قم بقياس A260 من هذه العينة باستخدام مقياس الطيف الضوئي النانوي للأشعة المرئية وفوق البنفسجية واحسب تركيز الحمض النووي الريبي باستخدام الصيغة التالية:

حيث c هو تركيز الحمض النووي الريبي ، b هو طول المسار ، i هو النوكليوتيدات المحددة (A ، C ، G ، أو U) ، n i هو تردد النوكليوتيدات i في تسلسل الحمض النووي الريبي ، و ε i هو معامل الانقراض المولي للنيوكليوتيد i. لتحديد تركيز الحمض النووي الريبي الأصلي للمخزون ، اضرب c في عامل التخفيف.
ملاحظة: نقطة توقف اختيارية: قد يتم تخزين الحمض النووي الريبي في -20 درجة مئوية لبضعة أشهر.
- تحضير حصة الحمض النووي الريبوزي (RNA) لتفاعل التحلل المائي.
- صفحة تنقية السبانخ2 والحمض النووي الريبي البروكلي
- إجراء in vitro فحص حركية قارئ اللوحة
- قم بإعداد برنامج إعادة تشكيل الحمض النووي الريبي: قم بإنشاء بروتوكول العجلة الحرارية التالي عن طريق تحديد إنشاء برنامج جديد > إضافة مرحلة جديدة > إضافة خطوة جديدة عدة مرات لإضافة كل خطوة من الخطوات التالية قبل الضغط على حفظ:
70 درجة مئوية لمدة 3 دقائق
65 درجة مئوية لمدة 45 ثانية
60 درجة مئوية لمدة 45 ثانية
55 درجة مئوية لمدة 45 ثانية
50 درجة مئوية لمدة 45 ثانية
45 درجة مئوية لمدة 45 ثانية
40 درجة مئوية لمدة 45 ثانية
35 درجة مئوية لمدة 45 ثانية
30 درجة مئوية لمدة 45 ثانية - إعادة طبيعة الحمض النووي الريبي: لإعادة طبيعة السبانخ 2 والحمض النووي الريبي البروكلي ، قم بإعداد مخزون 2 ميكرومتر من كل حمض نووي ريبوزي (RNA)في ddH 2 O في أنبوب PCR رقيق الجدران سعة 0.5 مل ، ثم أضف حجما متساويا من محلول إعادة التشكيل 2x (80 mM HEPES ، درجة الحموضة 7.5 [KOH] ، 250 mM KCl ، 6 mM MgCl2) لعمل محاليل 1 ميكرومتر من الحمض النووي الريبي. أضف الأنابيب إلى العجلة الحرارية ، وافتح برنامج إعادة التدوير المحفوظ ، واضغط على تشغيل.
ملاحظة: في حالة عدم توفر جهاز حراري ، يمكن بدلا من ذلك تحضين الحمض النووي الريبي على كتلة حرارية 70 درجة مئوية لمدة 3 دقائق ثم السماح لها بالتبريد ببطء إلى RT على الطاولة. - تحضير المخزن المؤقت لتفاعل الربط: لتحضير المخزن المؤقت لتفاعل ربط صبغة أبتامير واحد ، قم بعمل مزيج رئيسي يحتوي على مكونات عازلة (69.5 ميكرولتر من ddH 2O + 4 ميكرولتر من 1 M HEPES ، درجة الحموضة 7.5 [KOH] + 6.2 ميكرولتر من 2 M KCl + 0.3 ميكرولتر من 1 M MgCl2). بناء على عدد العينات والنسخ المتماثلة المطلوبة ، اضرب هذه القيم في عدد العينات زائد واحد. بشكل عام ، ثلاثة مكررات لكل عينة RNA مرضية.
- تحضير قارئ اللوحة.
- قم بإعداد برنامج حاقن قارئ اللوحة: في قارئ لوحة التألق ، حدد درجة الحرارة واضبط درجة الحرارة المطلوبة على 37 درجة مئوية ، مع التأكد من توازن درجة الحرارة مع هذه القيمة جيدا قبل بدء تجارب الحركية. افتح برنامج قارئ اللوحة ، وحدد الإعدادات > عرض الاستحواذ ، وأدخل البرنامج التالي لقياسات الحركة:
حلقة: لكل بئر
إعداد خط الأساس: 60 قراءة أساسية
إعدادات SmartInject: حقن 10 ميكرولتر (والذي سيحدث بعد قراءة خط الأساس)
يقرأ التألق (أو FL):
الإثارة: 448 نانومتر (عرض النطاق الترددي: 9 نانومتر)
الانبعاثات: 506 نانومتر (عرض النطاق الترددي: 15 نانومتر)
خرطوشة: أحادي (ق / ن 3297)
توقيت:
إجمالي وقت القراءة: 10 دقائق
الفاصل الزمني للقراءة: 0.5 ثانية
PMT والبصريات: 6 ومضات لكل قراءة
حلقة: البئر التالي - تحضير الحاقن
- اغسل الحاقن واستنشقه: لتحضير حاقن قارئ اللوحة ، حدد أولا حقن على قارئ اللوحة ، وقم بتزويد لوحة تجميع النفايات لقارئ اللوحة عند توجيهه ، ثم حدد غسل ، وقم بتنظيف أنبوب الحقن باتباع الإرشادات الموجودة على قارئ اللوحة بأحجام 1 مل من ddH 2 O ، 75٪ إيثانول في ddH2O ، ثم ddH2O. بعد ذلك ، حدد نضح ، مما يسمح للحاقن بإخراج السائل الزائد.
- رئيس الحاقن: بعد الخروج إلى الشاشة السابقة ، حدد Prime لتجهيز الحاقن بمجلدين 260 ميكرولتر من الربيطة المراد حقنها لضمان إضافة ليجند نقي ومركز إلى العينات أثناء التجارب - في هذه الحالة ، أولي مع 100 ميكرومتر DFHBI في ddH2O.
- قم بإعداد برنامج حاقن قارئ اللوحة: في قارئ لوحة التألق ، حدد درجة الحرارة واضبط درجة الحرارة المطلوبة على 37 درجة مئوية ، مع التأكد من توازن درجة الحرارة مع هذه القيمة جيدا قبل بدء تجارب الحركية. افتح برنامج قارئ اللوحة ، وحدد الإعدادات > عرض الاستحواذ ، وأدخل البرنامج التالي لقياسات الحركة:
- إجراء تجارب الحركية في المختبر : لإجراء تجربة حركية واحدة ، أضف أولا 80 ميكرولتر من مزيج المخزن المؤقت المعد مسبقا إلى بئر واحد من صفيحة ذات قاع صاف 96 بئرا ، متبوعا ب 10 ميكرولتر من الحمض النووي الريبي المعاد تشكيله. اترك هذه اللوحة ومحلول DFHBI في الحاقن يتوازنان إلى 37 درجة مئوية لمدة 15 دقيقة في قارئ اللوحة.
- في إعدادات برنامج قارئ اللوحة ضمن منطقة القراءة ، حدد البئر المراد تحليله ، ثم ، ضمن علامة التبويب الصفحة الرئيسية ، حدد تشغيل لتنفيذ برنامج الحركية الموضح سابقا. كرر هذه العملية حتى تكتمل جميع التجارب.
ملاحظة: بشكل حاسم ، يجب إجراء تجارب الحركية بئرا واحدا تلو الآخر لضمان قياس حركية الحمض النووي الريبي في ظل ظروف متطابقة بين النسخ المتماثلة والعينات. - اغسل الحاقن: لإزالة محلول DFHBI المتبقي من أنبوب الحقن ، اغسل أنبوب الحقن كما هو موضح في الخطوة 1.4.4.2.1 بأحجام 1 مل من ddH 2 O ، و 75٪إيثانول في ddH 2 O ، ثم ddH2O.
ملاحظة: نقطة توقف مؤقتة.
- قم بإعداد برنامج إعادة تشكيل الحمض النووي الريبي: قم بإنشاء بروتوكول العجلة الحرارية التالي عن طريق تحديد إنشاء برنامج جديد > إضافة مرحلة جديدة > إضافة خطوة جديدة عدة مرات لإضافة كل خطوة من الخطوات التالية قبل الضغط على حفظ:
- تحليل الحركية في المختبر لأبتامير الحمض النووي الريبي الفلوروجيني.
- إدخال البيانات في برنامج التحليل: تصدير البيانات التجريبية كجدول بيانات لنسخ البيانات بسهولة للمعالجة. في برنامج التحليل ، قم بإنشاء جدول بيانات جديد بتنسيق XY. في العمود X ، أدخل كل نقطة زمنية للقراءة ، مع t = 0 هو وقت حقن DFHBI. في العمود Y ، أدخل متوسط قيم التألق بين النسخ المتماثلة في تلك النقطة الزمنية المعنية بدءا من t = 0.
- تطبيع البيانات ورسمها بيانيا: لتطبيع قيم التألق ، انقر فوق تحليل معالجة البيانات > > تطبيع ، ثم انقر فوق موافق. اختر استخدام أصغر وأكبر قيم مجموعة البيانات للتسوية، وتقديم النتائج ككسر، ورسم النتائج بيانيا، ثم النقر فوق موافق. لإنشاء رسم بياني لمتوسط التألق الطبيعي بمرور الوقت، انقر فوق أيقونة تطبيع [اسم مجموعة البيانات] وحدد عائلة الرسم البياني: XY مع النقاط فقط.
ملاحظة: يمكن أن يكون من المفيد رؤية أشرطة الخطأ في الحالات التي يتم فيها رسم عدد صغير من النقاط الزمنية بيانيا. إذا كانت هذه مطلوبة ، عند اختيار جدول بيانات بتنسيق XY ، حدد الخيار الموجود أسفل "Y" لإدخال قيم النسخ المتماثل في أعمدة جنبا إلى جنب. سيؤدي رسم الجدول الناتج مع تحديد الخيارات الافتراضية إلى إنتاج رسم بياني بأشرطة خطأ. - قم بإجراء تركيب المنحنى للحصول على المعلمات الحركية: لملاءمة منحنى لبيانات الحركية ، انقر فوق تحليل > تحليل البيانات وحدد الانحدار غير الخطي (ملاءمة المنحنى) ضمن علامة التبويب تحليلات XY . ضمن علامة التبويب النموذج ، انقر فوق الارتباط الأسي > ثنائي الطور لملاءمة بيانات الحركية مع معادلة الارتباط ذات المرحلتين التالية:
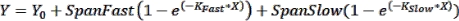
حيث Y هو التألق في الوقت X ، Y 0 هو التألق عند t = 0 ، K Fast و KSlow هما ثوابت معدل سريع وبطيء ، على التوالي ، و SpanFast و SpanSlow هما نطاقات تشغيل التألق التي تمثلها المعدلات السريعة والبطيئة ، على التوالي (انظر النتائج التمثيلية ، الشكل 1). انقر فوق علامة التبويب Nonlin Fit لعرض ثوابت المعدل وقيم t1/2 وقيم PercentFast.
ملاحظة: للحصول على انحراف معياري لجميع هذه القيم ، يمكن معالجة تكرارات تجربة قارئ اللوحة الفردية بنفس الطريقة الموضحة أعلاه.
2. تجربة الحركية الخلوية
- تحضير سلالات الإشريكية القولونية
- قم بتحويل خلايا الإشريكية القولونية BL21 Star (DE3) باستخدام ~ 100 نانوغرام من pET31b tRNA-Spinach2 وفقا لبروتوكول الشركة المصنعة.
ملاحظة: بناء البلازميد متاح تجاريا (Plasmid # 79783). - ضعي الخلايا على ألواح LB agar المحتوية على كاربينيسيلين (الكربوهيدرات: 50 مجم / مل) واحتضانها عند 37 درجة مئوية لمدة 12-16 ساعة. تنمو الخلايا التي تحتوي على البلازميدات كمستعمرات على اللوحة.
ملاحظة: نقطة توقف اختيارية: يمكن تخزين خلايا BL21 Star المحولة على الألواح عند 4 °C ملفوفة في بارافيلم لمدة أسبوع واحد.
- قم بتحويل خلايا الإشريكية القولونية BL21 Star (DE3) باستخدام ~ 100 نانوغرام من pET31b tRNA-Spinach2 وفقا لبروتوكول الشركة المصنعة.
- نمو الخلايا وتحفيز التعبير عن أبتامير الحمض النووي الريبي الفلوري
- تلقيح مزرعة 2 مل من الوسائط غير المحفزة (NI) التي تحتوي على كاربينيسيلين (الكربوهيدرات: 50 مجم / مل) مع مستعمرة واحدة من خلايا BL21 Star المحولة. كرر هذا لثلاث نسخ بيولوجية على الأقل. احتضان المزارع عند 37 درجة مئوية في حاضنة / شاكر عند 250 دورة في الدقيقة لمدة 22-24 ساعة.
ملاحظة: نقطة توقف اختيارية: تحتفظ الخلايا المزروعة في وسائط NI بالبلازميد ويمكن تخزينها عند 4 °C لمدة 1 أسبوع. - بعد النمو في وسائط NI ، قم بتخفيف المزرعة 100x إلى 3 مل جديدة من وسائط الحث الذاتي ZYP-5052 (الذكاء الاصطناعي) التي تحتوي على كاربينيسيلين (الكربوهيدرات: 50 مجم / مل). تنمو الخلايا عند 37 درجة مئوية في حاضنة / شاكر عند 250 دورة في الدقيقة لمدة 16-18 ساعة للحث على التعبير.
ملاحظة: سيتراوح OD600 النموذجي للمزارع من 2.0-3.3 بعد 18 ساعة من النمو. يتراوح نطاق كثافة الخلايا الأمثل بين 2.5-3.0.
- تلقيح مزرعة 2 مل من الوسائط غير المحفزة (NI) التي تحتوي على كاربينيسيلين (الكربوهيدرات: 50 مجم / مل) مع مستعمرة واحدة من خلايا BL21 Star المحولة. كرر هذا لثلاث نسخ بيولوجية على الأقل. احتضان المزارع عند 37 درجة مئوية في حاضنة / شاكر عند 250 دورة في الدقيقة لمدة 22-24 ساعة.
- إجراء تجربة الحركية الخلوية
- قم بإعداد مقياس التدفق الخلوي.
- قم بتشغيل مقياس التدفق الخلوي والكمبيوتر المتصل بالجهاز. بمجرد تسجيل الدخول إلى البرنامج الخاص بمقياس التدفق الخلوي ، ضمن علامة التبويب Instrument ، انقر فوق رمز بدء التشغيل . اتبع الخطوات الموضحة على شاشة البرنامج لضمان تهيئة الأجهزة بشكل صحيح.
ملاحظة: تسمي بعض مقاييس التدفق الخلوي تسلسل بدء تشغيل الجهاز Priming. تأكد من اتباع بروتوكول الشركة المصنعة لمقياس التدفق الخلوي الذي سيتم استخدامه للتجربة. - قم بإجراء اختبار أداء (إن أمكن). ضمن علامة التبويب القائمة الرئيسية ، انقر فوق اختبار الأداء. في أنبوب المزرعة ، أضف ثلاث قطرات من حبات تتبع أداء الشركة المصنعة إلى 3 مل من سائل التركيز.
- ضع أنبوب الاستزراع في رافع أنبوب العينة وارفع الرافع. قبل النقر فوق تشغيل اختبار الأداء ، تأكد من أن Lot # لأنبوب حبات التتبع هو نفسه المشار إليه في شاشة إعداد اختبار الأداء . انقر فوق اختبار الأداء لتشغيل الاختبار.
- قم بإعداد برنامج مقياس التدفق الخلوي لهذه التجربة باستخدام معلمات الاكتساب التالية للتألق أحادي الخلية:
ليزر الإثارة: 488 نانومتر
قناة الانبعاثات: GFP (وتسمى أيضا FITC)
حجم الاستحواذ: 40 ميكرولتر (بإجمالي حجم سحب 90 ميكرولتر)
معدل التدفق: 200 ميكرولتر / دقيقة
عدد الخلايا لكل قياس: 30000
إعدادات الأداة:
ضغط:
FSC: 480 فولت
SSC: 400 فولت
BL1: 540 فولت
BL2: 392 فولت
BL3: 422 فولت
- قم بتشغيل مقياس التدفق الخلوي والكمبيوتر المتصل بالجهاز. بمجرد تسجيل الدخول إلى البرنامج الخاص بمقياس التدفق الخلوي ، ضمن علامة التبويب Instrument ، انقر فوق رمز بدء التشغيل . اتبع الخطوات الموضحة على شاشة البرنامج لضمان تهيئة الأجهزة بشكل صحيح.
- قم بإعداد الملفات التجريبية.
- أنشئ ملف تجربة جديدا ضمن علامة التبويب مستكشف التجارب بالنقر بزر الماوس الأيمن فوق اسم مستخدم مقياس التدفق الخلوي. حدد تجربة جديدة في النافذة المنسدلة. عندما تنبثق نافذة جديدة على شاشة الكمبيوتر، حدد موافق.
- في ملف التجربة الجديد ، انقر بزر الماوس الأيمن فوق مجلد "المجموعة" وحدد إضافة أنبوب عينة جديد. قم بتسمية أنابيب العينة لكل نقطة زمنية محددة وقم بتكرارها بالنقر بزر الماوس الأيمن فوق عينة وتحديد إعادة تسمية في القائمة المنسدلة. كرر هذه الخطوة للحصول على العدد الإجمالي للنسخ المكررة والنقاط الزمنية للدورة الزمنية المقصودة للدراسة.
- تحضير محلول خلية مخففة: في أنبوب مزرعة جديد ، أضف 1.5 مل من محلول 1x PBS. بعد ذلك ، أضف 3 ميكرولتر من الخلايا المستحثة في وسائط الذكاء الاصطناعي إلى محلول 1x PBS لعمل محلول خلية مخفف. كرر هذه الخطوة لكل تكاثر بيولوجي في أنابيب استزراع مختلفة.
- قياس مضان الخلفية للخلايا: قبل إضافة الصبغة ، خذ قراءات لكل أنبوب ثقافة بيولوجي مكرر يحتوي على خلايا في محلول 1x PBS. هذا بحيث يتم قياس الخلفية الفلورية للخلايا لمراقبة تشغيل الطية بمرور الوقت بمجرد إضافة الصبغة.
- لأخذ قراءة ، ضع أنبوب الثقافة في رافع أنبوب العينة ، وارفع الرافع يدويا إلى إبرة حقن العينة. حدد نموذج الملف المناسب ضمن صفحة لوحة المجموعة ، وانقر تسجيل.
- عند اكتمال التشغيل ، قم بخفض رافع أنبوب العينة باستخدام أنبوب الثقافة يدويا. سيؤدي ذلك إلى بدء خطوة الشطف التي من شأنها شطف نظام السوائل وتقليل الترحيل بين كل عينة بيولوجية مكررة. سيتم حفظ البيانات تلقائيا على الكمبيوتر بعد اكتمال التشغيل.
- كرر الخطوات في غضون 2.3.4 لقياس الخلفية الفلورية الخلوية لثلاث نسخ بيولوجية على الأقل. للانتقال إلى نموذج الملف التالي، حدد نموذج الملف التالي بالنقر فوق رمز السهم لليمين بالقرب من اسم الأنبوب النموذجي أسفل أيقونة التسجيل .
- قياس مضان في نقاط زمنية للخلايا مع صبغة.
- أضف 1.4 ميكرولتر من مخزون الصبغة المركزة (50 mM DFHBI-1T في DMSO) إلى محلول PBS واحد مع الخلايا لإعطاء تركيز نهائي قدره 50 ميكرومتر DFBHI-1T. بعد ذلك ، قم بتأمين غطاء أنبوب الاستزراع ، ثم اقلب أنابيب الاستزراع 3x-5x لخلط المحلول بالتساوي قبل أخذ قراءة النقطة لأول مرة.
ملاحظة: يجب ألا تتجاوز النسبة المئوية الإجمالية ل DMSO داخل أنابيب الاستزراع للإشريكية القولونية 10٪ ، حيث يمكن أن يؤثر ذلك على صلاحية الخلية16. - قم بإزالة الغطاء ووضع أنبوب الثقافة في رافع أنبوب العينة. ارفع الحامل يدويا إلى إبرة حقن العينة ، وتحت ملف العينة المناسب ، انقر فوق رمز التسجيل . بالإضافة إلى ذلك ، ابدأ مؤقتا بالضغط على ابدأ للتجربة.
- اخفض رافع الأنبوب يدويا بعد اكتمال التشغيل ، وكرر الخطوات 2.3.5.1-2.3.5.2. (مع تشغيل المؤقت) عن طريق إضافة 1.4 ميكرولتر من DFHBI-1T المركز ، وعكس أنابيب الاستزراع ، وأخذ قراءات لجميع التكرارات البيولوجية المتبقية. ستكون هذه التسجيلات الأولى هي القراءات التي تم الحصول عليها في 0 دقيقة لجميع التكرارات البيولوجية. افعل ذلك واحدا تلو الآخر لكل تكرار بيولوجي.
ملاحظة: قم بتدوين الوقت الذي يتم فيه الضغط على الحصول على قياس التدفق الخلوي للسجل. التزم بهذا الوقت المذهل للنقاط الزمنية على مدار التجربة. - استمر في أخذ القراءات عن طريق رفع أنابيب الاستزراع في رافع أنبوب العينة إلى إبرة حقن العينة ، وتحديد ملف العينة المناسب ، والنقر فوق تسجيل ، وخفض الرافع يدويا بعد اكتمال كل تشغيل. افعل ذلك لجميع النقاط الزمنية الإضافية والتكرارات البيولوجية التي يتم اختبارها. كرر الخطوات حتى تكتمل التجربة.
ملاحظة: احتفظ بالعينات بعيدا عن الضوء لتجنب التبييض الضوئي ل DFHBI-1T في المحلول عن طريق تغطية العينات بورق الألمنيوم.
- أضف 1.4 ميكرولتر من مخزون الصبغة المركزة (50 mM DFHBI-1T في DMSO) إلى محلول PBS واحد مع الخلايا لإعطاء تركيز نهائي قدره 50 ميكرومتر DFBHI-1T. بعد ذلك ، قم بتأمين غطاء أنبوب الاستزراع ، ثم اقلب أنابيب الاستزراع 3x-5x لخلط المحلول بالتساوي قبل أخذ قراءة النقطة لأول مرة.
- قياس التألق في نقاط زمنية للخلايا بدون صبغة (التحكم).
- قم بتشغيل بروتوكولات التنظيف المناسبة لمقياس التدفق الخلوي قبل تكرار التجربة مرة أخرى مع عناصر تحكم سلبية تتبع بروتوكول الشركة المصنعة. يتم ذلك لتقليل أي ترحيل من التجربة السابقة إلى تجربة تحليل نقطة التحكم الزمنية. فيما يلي الخطوات المتبعة لمقياس التدفق الخلوي بين التجارب:
- ضع أنبوبا فارغا في رافع الأنبوب يدويا ، وارفع حامل الأنبوب ، وانقر على أيقونة Unclog في علامة التبويب Instrument . سيؤدي ذلك إلى تشغيل تدفق عكسي في نظام الموائع لتنظيف أي عينات لاصقة. اخفض حامل الأنبوب يدويا وقم بإزالة الأنبوب بمجرد الانتهاء من تسلسل Uncplug .
- باستخدام أنبوب استزراع جديد ، أضف 3 مل من محلول التبييض بنسبة 10٪ ، ضع أنبوب الاستزراع في حامل الأنبوب ، وارفع الحامل يدويا إلى إبرة حقن العينة. بالإضافة إلى ذلك ، ضع لوحة نظيفة من 96 بئرا في أخذ العينات الأوتوماتيكي إذا كان ذلك ينطبق على مقياس التدفق الخلوي.
- انقر على أيقونة تعقيم SIP / تعقيم أخذ العينات الأوتوماتيكية SIP لتشغيل تسلسل تنظيف بنسبة 10٪ مبيض في جميع أنحاء نظام السوائل. اخفض حامل الأنبوب لإكمال تسلسل التنظيف.
- قم بتعيين ملفات النماذج لتحليل نقطة وقت التحكم الذي يتم تشغيله باتباع الإرشادات الواردة في الخطوة 2.3.3.
- في أنبوب ثقافة جديد ، قم بإعداد محلول خلية مخفف في 1.5 مل من محلول 1x PBS. أضف 3 ميكرولتر من الخلايا المستحثة في وسائط الذكاء الاصطناعي إلى محلول 1x PBS لعمل محلول خلية مخفف. كرر هذه الخطوة لكل نسخة بيولوجية.
- أضف 1.4 ميكرولتر من DMSO إلى أنبوب الاستزراع واحدا تلو الآخر إلى محلول 1x PBS مع الخلايا واختبر نفس النقاط الزمنية. قم بتأمين غطاء أنبوب الاستزراع ، ثم اقلب أنابيب الاستزراع 3x-5x لخلط المحلول بالتساوي قبل أخذ قراءة النقطة لأول مرة. افعل ذلك واحدا تلو الآخر لكل تكرار بيولوجي.
- اتبع نفس البروتوكول لتحليل خلايا التحكم كما هو الحال بالنسبة للخلايا ذات الصبغة ، باستخدام الخطوات 2.3.5.2-2.3.5.4.
- قم بتشغيل بروتوكولات التنظيف المناسبة لمقياس التدفق الخلوي قبل تكرار التجربة مرة أخرى مع عناصر تحكم سلبية تتبع بروتوكول الشركة المصنعة. يتم ذلك لتقليل أي ترحيل من التجربة السابقة إلى تجربة تحليل نقطة التحكم الزمنية. فيما يلي الخطوات المتبعة لمقياس التدفق الخلوي بين التجارب:
- إيقاف تشغيل مقياس التدفق الخلوي: اتبع بروتوكول الشركة المصنعة للإغلاق المناسب للأجهزة. بالنسبة لمقياس التدفق الخلوي ، يتم إعداد الأداة للإغلاق بالطريقة التالية:
- قم بتنفيذ بروتوكول التنظيف الأولي لمقياس التدفق الخلوي باتباع الخطوات 2.3.6.1.1-2.3.6.1.3.
- استبدل أنبوب الاستزراع بمحلول مبيض بنسبة 10٪ بأنبوب استزراع به 3 مل من سائل التركيز. ارفع حامل الأنبوب يدويا ، وتحت رمز إيقاف التشغيل ، انقر فوق القائمة المنسدلة وحدد Thorough.
ملاحظة: نقطة توقف مؤقتة.
- قم بإعداد مقياس التدفق الخلوي.
- تحليل بيانات قياس التدفق الخلوي
- تصدير جميع ملفات FCS للتحليل. افتح ملفات FCS باستخدام برنامج تحليل قياس التدفق الخلوي.
- باستخدام أحد ملفات FCS للخلية فقط ، قم بإنشاء بوابة من مخطط نقطة التشتت الأمامي (FSC) والتشتت الجانبي (SSC) (FSC-Area / SSC-Area) ، باستخدام كلا محوري السجل لاستبعاد أي إشارات من الحطام. لإنشاء هذه البوابة ، انقر فوق رمز AutoGate في برنامج تحليل قياس التدفق الخلوي وقم بتسميته Gate 1. قم بتطبيق هذه البوابة نفسها على جميع العينات التي تم اختبارها ضمن علامة التبويب كافة العينات في مساحة عمل معالجة البيانات. سيؤدي ذلك إلى البوابة 1 أسفل جميع ملفات FCS التي تتم معالجتها.
- قم بإنشاء ملف مجموعة فرعية جديد باستخدام ملف الخلية FCS فقط المستخدم في الخطوة 2.4.2 بالنقر المزدوج فوقه. قم بتغيير إعدادات المحور إلى FSC-Area / FSC-Height، مع استخدام كلاهما محاور السجل. انقر على أيقونة AutoGate في برنامج تحليل قياس التدفق الخلوي لإنشاء بوابة بيضاوية ، وتسميتها البوابة 2. قم بتطبيق هذه البوابة كمجموعة فرعية أسفل البوابة المحددة في الخطوة 2.4.2 على جميع العينات التي تم اختبارها. سيؤدي ذلك إلى جميع العينات التي تحتوي على البوابة 1 > البوابة 2 المرتبطة بكل ملف FCS.
- قم بإنشاء ملف مجموعة فرعية أخرى مع تعيين كلا البوابتين في الخطوة 2.4.2 والخطوة 2.4.3 المطبقة بالنقر المزدوج فوق البوابة 2. قم بتغيير إعدادات المحور إلى FSC-Area/الرسم البياني. قم بتطبيق بوابة الرسم البياني هذه كمجموعة فرعية على جميع العينات التي تم اختبارها ، مما أدى إلى أن تحتوي جميع العينات على البوابة 1 > البوابة 2 > البوابة 2 المرتبطة بكل ملف FCS.
ملاحظة: يمكن إعادة تسمية الرسوم البيانية من البوابة 2 إلى الرسم البياني للمساعدة في نقل الرسوم البيانية إلى نافذة التخطيط ، وكذلك لإنشاء المزيد من التنظيم مع معالجة البيانات. - لتحليل قيم متوسط كثافة التألق (MFI)، افتح نافذة التخطيط. انقر واسحب بوابات الرسم البياني لكل نقطة زمنية إلى نافذة التخطيط.
- قم بإجراء تحليل إحصائي ل "∑ المتوسط: BL1-A" (GFP) لكل عينة تم اختبارها لعرض نتائج MFI في نافذة التخطيط.
- احسب الانحراف المعياري لقيم MFI لكل تحليل نقطة زمنية لثلاث نسخ بيولوجية مستقلة على الأقل.
- احفظ المدرج التكراري وقيم MFI لكل نقطة زمنية عن طريق تصدير نافذة التخطيط كملف PDF.
ملاحظة: نقطة توقف مؤقتة.
- بيانات قياس التدفق الخلوي للرسم البياني
- افتح ملف PDF الذي يحتوي على الرسوم البيانية وقيم MFI لكل نقطة زمنية. سيتم نسخ قيم MFI إلى برنامج تحليل البيانات. في برنامج الرسوم البيانية للبيانات، قم بإنشاء جدول بيانات جديد بتنسيق XY.
- حدد لإنشاء جدول XY مع تحديد ما يلي:
جدول البيانات: إدخال البيانات أو استيرادها إلى جدول جديد
خيارات:
X: الأوقات المنقضية
Y: أدخل (من ثلاثة إلى أربعة) قيم النسخ المتماثل في أعمدة فرعية جنبا إلى جنب - قم بالتسمية على المحور X جميع النقاط الزمنية لتشغيل التجربة والتحكم.
- في المجموعة أ ، أدخل قيم MFI لجميع التكرارات البيولوجية في كل نقطة زمنية لتحليل مضان الخلايا مع إضافة الصبغة.
- في المجموعة ب ، أدخل قيم MFI لجميع التكرارات البيولوجية في كل نقطة زمنية لتحليل الخلايا بدون إضافة صبغة (DMSO).
- لمراقبة النتائج ، انقر فوق [إدراج اسم مجموعة البيانات] ضمن علامة التبويب الرسوم البيانية . سيعرض هذا نقاط البيانات كوسائل ، مع أشرطة خطأ تمثل الانحراف المعياري (s.d.) في كل نقطة زمنية. يمثل المحور X الوقت المنقضي ، ويمثل المحور Y قيم MFI.
- حدد لإنشاء جدول XY مع تحديد ما يلي:
- افتح ملف PDF الذي يحتوي على الرسوم البيانية وقيم MFI لكل نقطة زمنية. سيتم نسخ قيم MFI إلى برنامج تحليل البيانات. في برنامج الرسوم البيانية للبيانات، قم بإنشاء جدول بيانات جديد بتنسيق XY.
النتائج
الحركية في المختبر
يتم عرض تسلسل قوالب الحمض النووي والبادئات ، التي يتم شراؤها على شكل قليل النيوكليوتيدات الاصطناعية ، في الجدول 2 ، ويتم عرض وصفات الكاشف في الملف التكميلي 1. يستخدم تضخيم تفاعل البوليميراز المتسلسل لزيادة كمية قالب الحمض الن?...
Discussion
بالنسبة لتجربة الحركية في المختبر ، يمكن تعديل نفس البروتوكول العام لقياس الحركية في المختبر لجهاز استشعار حيوي فلوري قائم على الحمض النووي الريبي يحتوي على كل من مجال ربط الليجند وربط الفلوروفور8. في هذه الحالة ، يجب تحضين الحمض النووي الريبي مع الفلوروفور قبل الق?...
Disclosures
يعلن المؤلفون عدم وجود تضارب في المصالح.
Acknowledgements
تم دعم هذا العمل من خلال المنح التالية لصحة الأم والطفل: NSF-BSF 1815508 و NIH R01 GM124589. تم دعم MRM جزئيا من خلال منحة التدريب NIH T32 GM122740.
Materials
| Name | Company | Catalog Number | Comments |
| Agarose | Thermo Fischer Scientific | BP160500 | |
| Agarose gel electrophoresis equipment | Thermo Fischer Scientific | B1A-BP | |
| Alpha D-(+)-lactose monohydrate | Thermo Fischer Scientific | 18-600-440 | |
| Amber 1.5 mL microcentrifuge tubes | Thermo Fischer Scientific | 22431021 | |
| Ammonium persulfate (APS) | Sigma-Aldrich | A3678 | |
| Ammonium sulfate ((NH4)2SO4) | Sigma-Aldrich | A4418 | |
| Attune NxT Flow cytometer | Thermo Fischer Scientific | A24861 | |
| Attune 1x Focusing Fluid | Thermo Fischer Scientific | A24904 | |
| Attune Shutdown Solution | Thermo Fischer Scientific | A24975 | |
| Attune Performance Tracking Beads | Thermo Fischer Scientific | 4449754 | |
| Attune Wash Solution | Thermo Fischer Scientific | J24974 | |
| Boric acid | Sigma-Aldrich | B6768 | |
| Bromophenol blue | Sigma-Aldrich | B0126 | |
| Carbenicillin disodium salt | Sigma-Aldrich | C3416 | |
| Chlorine Bleach | Amazon | B07J6FJR8D | |
| Corning Costar 96-well plate | Daigger Scientific | EF86610A | |
| Culture Tubes, 12 mm x 75 mm, 5 mL with attached dual position cap | Globe Scientific | 05-402-31 | |
| DFHBI | Sigma-Aldrich | SML1627 | |
| DFHBI-1T | Sigma-Aldrich | SML2697 | |
| D-Glucose (anhydrous) | Acros Organics | AC410955000 | |
| Dimethyl sulfoxide (DMSO) | Sigma-Aldrich | D8418 | |
| Dithiothreitol (DTT) | Sigma-Aldrich | DTT-RO | |
| DNA loading dye | New England Biolabs | B7025S | |
| DNA LoBind Tubes (2.0 mL) | Eppendorf | 22431048 | |
| dNTPs: dATP, dCTP, dGTP, dTTP | New England Biolabs | N0446S | |
| EDTA, pH 8.0 | Gibco, Life Technologies | AM9260G | |
| Ethanol (EtOH) | Sigma-Aldrich | E7023 | |
| Filter-tip micropipettor tips | Thermo Fischer Scientific | AM12635, AM12648, AM12655, AM12665 | |
| FlowJo Software | BD Biosciences | N/A | FlowJo v10 Software |
| Fluorescent plate reader with heating control | VWR | 10014-924 | |
| Gel electrophoresis power supply | Thermo Fischer Scientific | EC3000XL2 | |
| Glycerol | Sigma-Aldrich | G5516 | |
| Glycogen AM95010 | Thermo Fischer Scientific | AM95010 | |
| GraphPad Prism | Dotmatics | N/A | Analysis software from Academic Group License |
| Heat block | Thomas Scientific | 1159Z11 | |
| HEPES | Sigma-Aldrich | H-4034 | |
| Inorganic pyrophosphatase | Sigma-Aldrich | I1643-500UN | |
| Low Molecular Weight DNA Ladder | New England Biolabs | N3233L | Supplied with free vial of Gel Loading Dye, Purple (6x), no SDS (NEB #B7025). |
| Magnesium chloride hexahydrate (MgCl2) | Sigma-Aldrich | M2670 | |
| Magnesium sulfate (MgSO4) | Fisher Scientific | MFCD00011110 | |
| Microcentrifuge tubes (1.5 mL) | Eppendorf | 22363204 | |
| Microcentrifuge with temperature control | Marshall Scientific | EP-5415R | |
| Micropipettors | Gilson | FA10001M, FA10003M, FA10005M, FA10006M | |
| Micropipettor tips | Sigma-Aldrich | Z369004, AXYT200CR, AXYT1000CR | |
| Millipore water filter with BioPak unit | Sigma-Aldrich | CDUFBI001, ZRQSVR3WW | |
| Narrow micropipettor pipette tips | DOT Scientific | RN005R-LRS | |
| PBS, 10x | Thermo Fischer Scientific | BP39920 | |
| PCR clean-up kit | Qiagen | 28181 | |
| PCR primers and templates | Integrated DNA technologies | ||
| PCR thermocycler for thin-walled PCR tubes | Bio-Rad | 1851148 | |
| PCR thermocycler for 0.5 mL tubes | Techne | 5PRIME/C | |
| pET31b-T7-Spinach2 Plasmid | Addgene | Plasmid #79783 | |
| Phusion High-Fidelity DNA polymerase | New England Biolabs | M0530L | Purchase of Phusion High-Fideldity Enzyme is supplied with 5x Phusion HF Buffer, 5x Phusion GC Buffer, and MgCl2 and DMSO solutions. |
| Polyacrylamide gel electrophoresis gel comb, C.B.S. Scientific | C.B.S. Scientific | VGC-1508 | |
| Polyacrylamide gel electrophoresis equipment | C.B.S. Scientific | ASG-250 | |
| Potassium chloride (KCl) | Sigma-Aldrich | P9333 | |
| Potassium phosphate monobasic | Sigma-Aldrich | P5655 | |
| Razor blades | Genesee Scientific | 38-101 | |
| rNTPs: ATP, CTP, GTP, UTP | New England Biolabs | N0450L | |
| SDS | Sigma-Aldrich | L3771 | |
| Short wave UV light source | Thermo Fischer Scientific | 11758221 | |
| Sodium carbonate (Na2CO3) | Sigma-Aldrich | S7795 | |
| Sodium chloride (NaCl) | Sigma-Aldrich | S7653 | |
| Sodium hydroxide (NaOH) | Sigma-Aldrich | S8045 | |
| Sodium phosphate dibasic, anhydrous | Thermo Fischer Scientific | S375-500 | |
| SoftMax Pro | Molecular Devices | N/A | SoftMax Pro 6.5.1 (platereader software) obtained through Academic Group License |
| Sterile filter units | Thermo Fischer Scientific | 09-741-88 | |
| Sucrose | Sigma-Aldrich | S0389 | |
| SYBR Safe DNA gel stain | Thermo Fischer Scientific | S33102 | |
| TAE buffer for agarose gel electrophoresis | Thermo Fischer Scientific | AM9869 | |
| Tetramethylethylenediamine (TEMED) | Sigma-Aldrich | T9281 | |
| Tris base | Sigma-Aldrich | TRIS-RO | |
| Tryptone (granulated) | Thermo Fischer Scientific | M0251S | |
| T7 RNA polymerase | New England Biolabs | M0251S | |
| Urea-PAGE Gel system | National Diagnostics | EC-833 | |
| UV fluorescent TLC plate | Sigma-Aldrich | 1.05789.0001 | |
| UV/Vis spectrophotometer | Thermo Fischer Scientific | ND-8000-GL | |
| Vortex mixer | Thermo Fischer Scientific | 2215415 | |
| Xylene cyanol | Sigma-Aldrich | X4126 | |
| Yeast Extract (Granulated) | Thermo Fischer Scientific | BP9727-2 |
References
- Su, Y., Hammond, M. C. RNA-based fluorescent biosensors for live cell imaging of small molecules and RNAs. Current Opinion in Biotechnology. 63, 157-166 (2020).
- Zhang, J., et al. Tandem spinach array for mRNA Imaging in living bacterial cells. Scientific Reports. 5, 17295 (2015).
- Wang, Z., et al. In spatial complementation of aptamer-mediated recognition enables live-cell imaging of native RNA transcripts in real time. Angewandte Chemie. 57 (4), 972-976 (2018).
- Strack, R. L., Disney, M. D., Jaffrey, S. R. A superfolding Spinach2 reveals the dynamic nature of trinucleotide repeat-containing RNA. Nature Methods. 10 (12), 1219-1224 (2013).
- Thavarajah, W., et al. Point-of-use detection of environmental fluoride via a cell-free riboswitch-based biosensor. ACS Synthetic Biology. 9 (1), 10-18 (2020).
- You, M., Litke, J. L., Jaffrey, S. R. Imaging metabolite dynamics in living cells using a Spinach-based riboswitch. Proceedings of the National Academy of Sciences of the United States of America. 112 (21), 2756-2765 (2015).
- Kellenberger, C. A., Wilson, S. C., Sales-Lee, J., Hammond, M. C. RNA-based fluorescent biosensors for live cell imaging of second messengers cyclic di-GMP and cyclic AMP-GMP. Journal of the American Chemical Society. 135 (13), 4906-4909 (2013).
- Manna, S., Truong, J., Hammond, M. C. Guanidine biosensors enable comparison of cellular turn-on kinetics of riboswitch-based biosensor and reporter. ACS Synthetic Biology. 10 (3), 566-578 (2021).
- Bose, D., Su, Y., Marcus, A., Raulet, D. H., Hammond, M. C. An RNA-based fluorescent biosensor for high-throughput analysis of the cGAS-cGAMP-STING pathway. Cell Chemical Biology. 23 (12), 1539-1549 (2016).
- Wang, X. C., Wilson, S. C., Hammond, M. C. Next-generation RNA-based fluorescent biosensors enable anaerobic detection of cyclic di-GMP. Nucleic Acids Research. 44 (17), 139 (2016).
- Paige, J. S., Thinh, N. -. D., Wenjiao, S., Jaffrey, S. R. Fluorescence imaging of cellular metabolites with RNA. Science. 335 (6073), 1194 (2012).
- Paige, J. S., Wu, K. Y., Jaffrey, S. R. RNA mimics of green fluorescent protein. Science. 333 (6042), 642-646 (2011).
- Filonov, G. S., Moon, J. D., Svensen, N., Jaffrey, S. R. Broccoli: Rapid selection of an RNA mimic of green fluorescent protein by fluorescence-based selection and directed evolution. Journal of the American Chemical Society. 136 (46), 16299-16308 (2014).
- Song, W., Strack, R. L., Svensen, N., Jaffrey, S. R. Plug-and-play fluorophores extend the spectral properties of spinach. Journal of the American Chemical Society. 136 (4), 1198-1201 (2014).
- Sambrook, J., Fritsch, E., Maniatis, T. . Molecular Cloning: A Laboratory Manual. , (1989).
- Basch, H., Gadebusch, H. H. In vitro antimicrobial activity of dimethylsulfoxide. Applied Microbiology. 16 (12), 1953-1954 (1968).
- Kallansrud, G., Ward, B. A comparison of measured and calculated single- and double-stranded oligodeoxynucleotide extinction coefficients. Analytical Biochemistry. 236 (1), 134-138 (1996).
- Wilson, S. C., Cohen, D. T., Wang, X. C., Hammond, M. C. A neutral pH thermal hydrolysis method for quantification of structured RNAs. RNA. 20 (7), 1153-1160 (2014).
- Szatmári, D., et al. Intracellular ion concentrations and cation-dependent remodelling of bacterial MreB assemblies. Scientific Reports. 10, 12002 (2020).
- Boulos, L., Prévost, M., Barbeau, B., Coallier, J., Desjardins, R. LIVE/DEAD® BacLightTM: Application of a new rapid staining method for direct enumeration of viable and total bacteria in drinking water. Journal of Microbiological Methods. 37 (1), 77-86 (1999).
- Huang, H., et al. A G-quadruplex-containing RNA activates fluorescence in a GFP-like fluorophore. Nature Chemical Biology. 10 (8), 686-691 (2014).
- Jeng, S. C. Y., Chan, H. H. Y., Booy, E. P., McKenna, S. A., Unrau, P. J. Fluorophore ligand binding and complex stabilization of the RNA Mango and RNA Spinach aptamers. RNA. 22 (12), 1884-1892 (2016).
- Han, K. Y., Leslie, B. J., Fei, J., Zhang, J., Ha, T. Understanding the photophysics of the Spinach-DFHBI RNA aptamer-fluorogen complex to improve live-cell RNA imaging. Journal of the American Chemical Society. 135 (50), 19033-19038 (2013).
- Wang, P., et al. Photochemical properties of Spinach and its use in selective imaging. Chemical Science. 4 (7), 2865-2873 (2013).
- Dao, N. T., et al. Photophysics of DFHBI bound to RNA aptamer Baby Spinach. Scientific Reports. 11, 7356 (2021).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved