需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
两种异核体的形成方法,发现丙型肝炎病毒的制约因素
摘要
我们描述有条件的两种方法反丙型肝炎病毒(HCV)的组装和完成的全病毒的生命周期,这对异核体的形成依靠的互补。这些技术是合适的细胞系表达占主导地位的制约因素,其中排除感染丙型肝炎病毒的后代生产的屏幕。
摘要
丙型肝炎病毒(HCV)是一种嗜肝病毒与宿主范围只限于人类和黑猩猩。虽然已在人类非肝和小鼠细胞株观察丙型肝炎病毒RNA复制,效率非常低,需要长期的选拔程序,用丙型肝炎病毒复制子构建表达占主导地位的抗生素选择标记1-5。因此,丙型肝炎病毒在体外的研究仅限于人类肝癌细胞株病毒进入和完成病毒生命周期的宽容。由于医疗券计划狭窄的物种的取向,有没有免疫的小动物模型,维持完整的丙型肝炎病毒复制周期6-8。低效的丙型肝炎病毒复制非人类细胞如鼠标起源的可能是由于缺乏主机依赖基本因素和/或制约因素表达的遗传不相容。
我们调查是否抑制丙型肝炎病毒的传播是由占主导地位的限制,发无论是从非肝组织或在小鼠肝细胞株人类细胞系的构造函数中。为此,我们制定了两个独立的条件反式互补的方法,依靠体细胞融合。在这两种情况下,完成病毒的复制周期是唯一可能在heterokaryons的。因此,成功的反式互补,这是通过测量从头传染性病毒后代的生产决定,表示没有占主导地位的限制。
具体来说,亚基携带丙型肝炎病毒复制子的荧光素酶基因转染非常宽容的人肝癌细胞(Huh-7.5细胞)。随后,这些细胞共培养和融合各种人类和小鼠细胞表达丙型肝炎病毒结构蛋白的核心,信封1和2(素E1,E2)和辅助蛋白P7和NS2。提供治疗与聚乙二醇(PEG)发起,细胞融合,文化释放病毒PA工艺品的感染,其中幼稚细胞在受体依赖的方式。
评估完整的病毒生命周期的主导限制,包括进入细胞,RNA的翻译,复制和病毒装配的影响,我们采取了一个人的肝细胞株(HuH-7 Lunet N细胞)缺乏CD81的内源性表达的优势,丙型肝炎病毒的基本项因素。在异位表达CD81的情况下,这些细胞基本上是难治性丙型肝炎病毒感染10。重要的是,当共同培养和融合细胞表达人CD81,但缺乏起码的另一个关键进入细胞因子(即SR-BI的CLDN1,OCLN),只有heterokaryons的显示一整套进入丙型肝炎病毒感染的必要因素。因此,分析优势制约因素,如果抑制丙型肝炎病毒复制周期完成,我们融合Lunet N细胞与人类和小鼠的起源的各种细胞履行上述暴ERIA。当共同培养的细胞转染高度膜融合病毒包膜蛋白突变体的原型泡沫病毒(PFV 11),并随后与感染丙型肝炎病毒颗粒(HCVcc)的挑战, 从头传染性病毒的生产进行了观察。这表明,丙型肝炎病毒成功地完成其复制周期,从而排除了在这些细胞株的主导限制因子的表达heterokaryons的。这些新的条件反式互补的方法将是有益的筛选丙型肝炎病毒的特定优势制约因素表达的细胞株和原代细胞的大面板。
研究方案
用PEG细胞融合
1。细胞培养
- 咦,7.5 HeLa和Hep56.1D的天真或包装细胞株15厘米的完整的DMEM培养液(DMEM培养液cplt)中型细胞培养皿12文化,培养液补充2毫米L-谷氨酰胺,1个非必需氨基酸,100 U / L mL青霉素,100μg/ mL链霉素,10%胎牛血清。运用适当的选择如表1所示的稳定细胞线。
2。丙型肝炎病毒RNA的转染
- 洗两次了7.5细胞(1合流15厘米盘子)用磷酸盐缓冲液(PBS),trypsinize,在1.5×10 7细胞/ ml在Cytomix浓度(120毫米氯化钾, 氯化钙 0.15毫米,10毫米ķ悬浮2 HPO 4 pH值7.6 - 25毫米的HEPES,EGTA 2毫米,5毫米MgCl 2的 ,调整到7.6 pH值与氢氧化钾和过滤消毒),其中包含2毫米ATP和5 mM的谷胱甘肽。
- 转染通过electroporat离子400μL细胞悬液,10微克,丙型肝炎病毒RNA(pFKi389Luc-EI/NS3-3“_JFH1_dg 13)使用一个0.4厘米的缝隙宽度和一个基因脉冲Xcell系统(Biorad公司)设置为975试管(6X10 6个细胞) μF和270 V的描述以前14。
- 立即转了7.5细胞转移至10毫升培养液cplt介质和种子成一个直径10厘米的单培养皿整个悬挂。为培养24 h的细胞在37°C间和5%的CO 2。
3。经PEG诱导融合
- 2.1收获细胞悬浮在培养液cplt中等和稀释到5×10 5细胞/ ml。
- 生成咦-7.5的单细胞悬液,HeLa细胞,并包装细胞Hep56.1D,并稀释至5×10 5细胞/ mL,2×10 5细胞/毫升,2×10 5细胞/ ml,分别。需要注意的是包装细胞异位两个明确的丙型肝炎病毒蛋白的核心,素E1,E2,P7,NS2的后转依赖慢病毒载体转导的C-E1和E2-P7,NS2的表达盒,分别为13,15。
- 准备用2-3每口井的无菌玻璃盖的融合效率的进一步分析单6孔培养板。
- 结合1毫升转了1毫升的包装细胞,种子7.5窝藏亚基因组复制子细胞到6孔板,在37°C和5%的CO 2孵育24小时。
- 在这个时间点,细胞密度应介于60-80%汇合诱导细胞融合前,以便在靠近细胞膜的融合细胞。
- 吸共培养细胞的培养基,用1 mL PBS洗一次,然后小心加入500μL预热的40%PEG-1500或PBS作为控制和孵化,在37°C诱导异核体的形成,为5分钟。
- 吸聚乙二醇,并仔细清洗3-5次为1分钟(分钟)2毫升PBS,每洗,以去除多余的PEG和最后加2毫升培养液cplt中每口井,并于37°C和5%的CO 2。
- 四十八小时后融合,收集各上清通过0.45微米的过滤器的过滤器。
- 测量生产在融合heterokaryons的传染性颗粒天真了7.5细胞(8x10的4个细胞/孔接种在12孔板,24小时前接种)接种500μL细胞培养液和随后测定荧光素酶活动14。
4。免疫测定融合效率
- 后收集细胞培养上清液(3.8节),洗井含玻璃盖单,一次1分钟1毫升的PBS。在室温(RT),应执行以下所有步骤和应用1 mL PBS洗涤每洗1分钟。
- 修复细胞600μL3%多聚甲醛(PFA)的PBS 15分钟,然后用PBS洗3倍。仔细转让盖玻片到24孔板使用镊子。
- 通透细胞500μL0.5%Triton的PBS中X-100的5分钟,随后用PBS洗3倍。
- 准备辅以5%山羊血清抗体在PBS溶液。在浓度为6.4毫微克/毫升的浓度在0.5微克/毫升和人类单克隆抗E2抗体(CBH-23)使用反病毒NS5A抗体(9E10)。适用于250μL,每口井,并在室温下孵育45分钟。
- 用PBS洗3倍和250μL,中学的羊抗鼠或羊抗人IgG特异性抗体结合Alexa的氟546或网站,福陆公司488约束的主要抗体检测浓度2微克/毫升的PBS,辅以5%山羊血清。在室温30分钟,在黑暗中培养。
- 然后,用PBS洗1X和随后用250微升的DAPI(4',6'-diamidino-2-苯基二胺)在PBS稀释1:3,000,在室温下为1分钟,在黑暗中孵育染色细胞核。
- 洗净用PBS和1X 4X与H 2 澳,然后装入盖玻片,在显微镜幻灯片Fluoromount下降到倒挂,让在黑暗和评估的样品干燥的间接免疫荧光显微镜。
瞬时转染的原型泡沫病毒(PFV)糖蛋白的融合
5。病毒接种的制备
- HuH-7.5细胞在体外转录丙型肝炎病毒RNA转染和收获后48 h和72 h细胞培养上清中所述先前14产生高滴度病毒的股票。限制稀释法(TCID 50)13,确定病毒滴度。
6。细胞培养,细胞融合的膜融合PFV糖蛋白的转染
- 文化Lunet氮,HeLa细胞,并Hep56.1D hCD81细胞根据表1说明,在培养液cplt介质中包含适当的选择。
- 分离细胞,如2.1中所述,准备在培养液cplt米的单细胞悬液edium,并共同培养Lunet列印与HeLa或Hep56.1D hCD81细胞株的细胞产生的总细胞密度1.5×10 5细胞每在适当的比例(如HeLa细胞Hep56.1D hCD81或1:1 1:2) 12孵育24小时在37°C和5%的CO 2。
- 第二天,瞬时转染用脂质体2000根据制造商的指示的高度膜融合的PFV包膜蛋白(pczHFVenvEM066 16)的细胞。
7。感染试验
- 接种heterokaryons的病毒库存为12Ĥ一夜之间350μL(内政部〜2.3)的转染30小时后,用PBS洗一次,添加1毫升培养液cplt每口井的媒介。 48小时在37°C和5%的CO 2。
- 收获上清异核文化,通过0.45微米的过滤器和接种了7.5细胞,接种于96孔板(1×10 4细胞/孔)的前一天,在限制稀释法,过滤器 13。
- 72小时后,感染了7.5细胞染色与丙型肝炎病毒特异性抗体(NS5A的; 9E10)量化传染性后代颗粒生产。
8。细胞融合的可视化
- 可视化的融合事件,准备在DMEM培养基的5至10μM的解决方案CellTracker染料无添加剂和前完成共培养6小时以下的步骤(6.2和6.3节中所述)。
- 一次用5毫升的PBS洗涤贴壁细胞,然后孵育细胞4毫升45分钟,每10厘米的菜37染色解决方案°C和5%CO 2(染色Lunetñ与CellTracker橙CMTMR HeLa或Hep56.1D的细胞hCD81细胞CellTracker绿色CMFDA,分别)。
- 1分钟,5毫升的PBS洗涤细胞一次和添加培养液cplt介质,为6小时37°C和5%CO 2孵育。
- 如上所述,在节6.2,然而,加盖玻片的准备播种染细胞和转染播种前的细胞培养皿。
- 转染后30小时,洗涤细胞1毫升的PBS精心为1分钟,然后用250微升3%的煤灰修复细胞在室温为15分钟。用1 mL PBS洗涤细胞1分钟后,用DAPI染色1分钟,如4.6节所述,1分钟1毫升PBS洗一次,重复清洗与H 2 O和安装盖玻片,载玻片上(见4.7节)。用荧光显微镜分析细胞。
| 种类 | 细胞株 | 起源 | 生长介质与选择 |
| 人的 | 呵呵7.5 | 亚克隆的HuH-7肝癌细胞株17 | DMEM培养液cplt |
| 呵呵-7.5 [CE1的] [E2p7NS2] | 稳定表达病毒蛋白的核心,E1,E2,P7,NS2的,转由慢病毒基因T转让(BOT)的两个独立的基因盒 | DMEM培养液cplt +稻瘟5微克/毫升 | |
| HuH-7 Lunet列印 | 亚克隆的HuH-7肝癌细胞株9 | DMEM培养液cplt | |
| HeLa细胞 | 宫颈腺癌细胞株(ATCC编号:CCL-2) | DMEM培养液cplt | |
| HeLa细胞[CE1的[E2p7NS2] | 稳定表达病毒蛋白的核心,E1,E2,P7,NS2的,转由两个独立的基因盒的慢病毒基因转移 | DMEM培养液cplt + G418的750微克/毫升;稻瘟5微克/毫升 | |
| 鼠标 | Hep56.1D | 原发性肝癌(研究恩克样的礼物) 成年C57BL/6J小鼠 | DMEM培养液cplt |
| Hep56.1D [CE1的[E2p7NS2] | 稳定前按病毒核心蛋白,E1,E2,P7,NS2的,转由两个独立的基因盒的慢病毒基因转移 | DMEM培养液cplt + G418的750微克/毫升;稻瘟5微克/毫升 | |
| Hep56.1D hCD81 | 稳定表达人CD81转慢病毒基因转移 | DMEM培养液cplt +稻瘟5微克/毫升 |
完成后,G418的:,H geneticin: 人类起源和文化用细胞系Cplt条件表1规格。
9。代表结果
在这项研究中,我们采用了两种体细胞融合,使我们专门调查heterokaryons的丙型肝炎病毒复制周期完成的制约因素的影响,不同的方法。值得注意的是,两个不同类型的细胞融合后的反式互补的条件设计,确保了(方法2)只有在人类肝细胞和非允许细胞株,病毒大会(方法1)或病毒进入和充分的丙型肝炎病毒复制周期之间的真正heterokaryons的完成。
在第一种方法,咦-7.5,高度宽松的丙型肝炎病毒,细胞转染与亚基因组复制子表达支持亚基丙型肝炎病毒RNA的复制(咦-7.5复制子细胞)的荧光素酶基因和丙型肝炎病毒非结构蛋白。这些细胞共同培养和融合细胞系中表达丙型肝炎病毒核心结构蛋白,E1,E2以及配件蛋白质P7和NS2。 Figure1A显示了实验过程的概述。重要的是,粒子装配所需的所有蛋白质的PEG融合后,应该在形成异核体,可以通过对个别病毒蛋白的免疫证实。图1B描绘了一个模范的融合事件,在双方的NS5A的信号在HuH-7.5复制子细胞和E2表示在Huh-7.5 [CE1的表达[E2p7NS2]包装细胞检测PEG诱导异核体形成后,在相同的细胞质。当共同培养的细胞,而不是用PBS治疗,诱导无融合,因此,只有单阳性细胞和无信号的共定位观察。此外,为了控制转基因表达,我们进行了酶联免疫吸附具体的核心和E2(以前15详细报道)。咦7.5除了控制包装细胞系[CE1的[E2p7NS2,我们产生的HeLa和人类非肝小鼠肝细胞的代表,分别Hep56.1D包装细胞。在这些后者细胞丙型肝炎病毒RNA的复制效率低和丙型肝炎病毒的组装和释放并没有被证明。图1C所示的融合实验的结果。收集上清共培养48小时后融合感应和用于随后的荧光素酶检测天真了7.5细胞接种。值得注意的是,当了7.5复制子细胞融合,要么天真的细胞株或用PBS作为对照治疗,没有传染性的培养液中检测到。然而,经PEG诱导之间咦-7.5复制子和包装细胞系的细胞融合时,复制子和结构蛋白组成型表达之间的跨互补救出病毒造成heterokaryons的生产和传染性病毒颗粒释放到培养液。因此,我们得出的结论是病毒生产所需的细胞融合,并在包装细胞株的病毒蛋白的表达。引人注目的是,不仅咦-7.5肝癌细胞的heterokaryons的,但也与人类非肝(CE1的HeLa细胞[] [E2p7NS2])和小鼠肝(Hep56.1D [CE1的[E2p7NS2)细胞允许病毒释放heterokaryons的,表明,组装和释放不显性抑制由这些细胞类型中的制约因素。在弗伦岑在包装细胞系和地道入口进入靶细胞的结构蛋白的表达等15。
利用细胞融合的一个替代方法,以分析可能影响进入细胞,RNA翻译和RNA复制的复制周期阶段的限制,并排除高转咦7.5复制子细胞中的病毒的负担会妨碍饱和制约因素检测。为此,我们开发了一个基于HCVcc和检测新病毒在这些细胞生产heterokaryons的接种独立检测。正如图2A中所述,诱导体细胞融合后的细胞共培养膜融合糖蛋白的表达。这种方法被选中,因为敏感性增加可能是由于提高融合效率。 heterokaryons的是由不同的细胞系与前共同培育的CellTracker染料染色的可视化。一个异核体与细胞质内的染料均匀分布表明,两种类型的细胞融合作为表明D图2B。只有在的Lunet列印HeLa细胞或Hep56.1D hCD81细胞与细胞heterokaryons的所有丙型肝炎病毒进入的因素,从而选择性地表达渲染heterokaryons的易患丙型肝炎病毒进入细胞。与HCVcc的挑战,这是显而易见的, 从头生产的约10倍以上的检测(图2C)的背景病毒感染后代heterokaryons的完整的丙型肝炎病毒的复制。作为对照,Lunet N细胞Lunet N细胞融合。重要的是,只有非常低的水平感染丙型肝炎病毒接近检出限进行了观察。当Lunet N细胞与天真Hep56.1D细胞的融合获得了类似的结果。在这两种情况下,人类CD81的缺席,使HCV富有成效感染heterokaryons的,。这后者在这两个案件中发现的传染性是非常低的可能由于Lunet N细胞和/或残留的接种传染性病毒输入的低水平感染水平低。在对比HeLa细胞和他p56.1D hCD81细胞表达人CD81,从而补充缺乏的细胞中的异核项因素,并允许丙型肝炎病毒进入细胞。因此,增加10倍的水平感染丙型肝炎病毒,在涉及这两个细胞系heterokaryons的媒介检测可能反映从头 heterokaryons的传染性颗粒的生产。因此,我们认为,丙型肝炎病毒复制周期的完成,并不限于不含主导HCV制约因素,在这些细胞株中的表达。
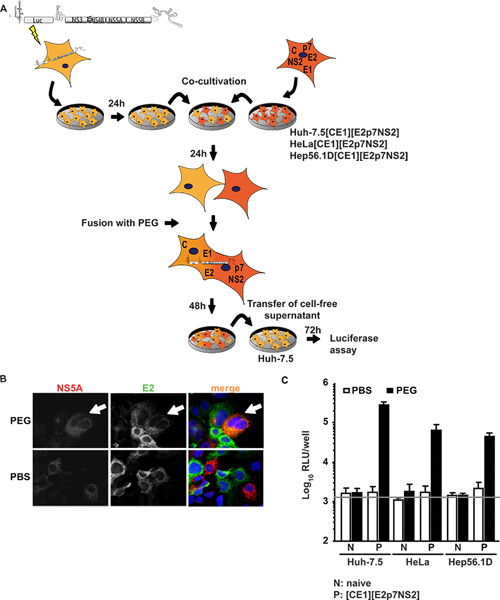
图1。 跨互补丙型肝炎病毒在heterokaryons的组装和释放。(一)PEG介导的细胞融合的实验过程纲要。天真了7.5细胞转染荧光素酶的JFH1记者复制子吕克-NS3蛋白-5B电第二天,细胞分离和共培养幼稚细胞或包装细胞表达HCV核心,E1和E2,P7和NS2。 24小时后共同培育,异核体形成的诱导治疗,40%的PEG作为阴性对照PBS。 48小时后收获,无细胞上清液接种天真了7.5细胞。测定荧光素酶活性的传染性。 (二)检测的异核细胞,免疫组化染色对E2和NS5A单克隆抗体。同时表达这两种蛋白在细胞内,细胞融合。 (三)荧光素酶的测量进行量化病毒传染性从heterokaryons的产生。三个独立的实验和手段的标准偏差的平均值。单杠代表背景的RLU在未受感染了7.5细胞决定的。 点击这里查看大图 。
9/4029fig2.jpg“/>
图2。完成后丙型肝炎病毒复制周期接种的heterokaryons的。(一)实验过程中的总体示意图。 HuH-7 Lunet的N细胞缺乏CD81的指示细胞株缺乏或表达人CD81共同培养。重要的是,这些后者细胞缺乏至少有一个丙型肝炎病毒进入的因素,因此不能进行富有成效的感染。第二天,发起的膜融合PFV病毒包膜蛋白转染融合。 30小时后,细胞与感染丙型肝炎病毒颗粒的挑战。来衡量进入细胞,RNA复制及病毒生产由这些heterokaryons的持续,释放在细胞培养液的传染性被确定接种后48小时。为此,天真了7.5细胞作为靶细胞在限制稀释法(TCID 50)。 (乙)检测的异核细胞染色,与CellTracker绿色或6小时CellTracker橙合作,cultiv前ATION和转染。 30小时后,细胞被固定,并用DAPI染色。 (三)Lunet N细胞进行融合,HeLa细胞,的天真Hep56.1D或Hep56.1D细胞表达人CD81。这些文化与HCVcc(2.3 MOI),接种。 48 h后收集培养液和新从heterokaryons的粒子释放TCID 50测定,用天真了7.5靶细胞。 3次独立实验的平均值。单杠检测的检测限。 点击这里查看大图 。
讨论
我们提出了两种方法在培养细胞诱导异核分析显性负的限制,排除丙肝病毒的复制形成。使用这些程序时,我们排除了存在的一个组成明示或病毒引起的各种人类非肝小鼠肝细胞株的主导因素。第一法主要分析制约因素,防止传染性后代的丙型肝炎病毒的组装和释放。因为在这种情况下包装细胞融合丙型肝炎病毒复制子细胞,包装细胞中表达的因素可能限制只获取的细胞,已经有一个高负荷的病?...
披露声明
总磷收到Biotest咨询费。
致谢
我们是鹰二胁田和延Bukh JFH1和J6CF株,分别表示感谢。此外,我们感谢查尔斯·赖斯HuH-7.5细胞和9E10的抗体,史蒂芬Foung为E2特定的抗体CBH-23,实验病毒学,有益的建议和讨论Twincore部的所有成员。
材料
| Name | Company | Catalog Number | Comments |
| 试剂名称 | 公司 | 目录编号 | |
| DMEM培养液 | Invitrogen公司,卡尔斯鲁厄,德国 | 41965-039 | |
| L-谷氨酰胺 | Invitrogen公司,卡尔斯鲁厄,德国 | 25030-024 | |
| 非必需氨基酸 | Invitrogen公司,卡尔斯鲁厄,德国 | 11140-035 | |
| 青霉素/ | Invitrogen公司,卡尔斯鲁厄,德国 | 15140-122 | |
| 胎牛血清 | 临时机场管理局,科尔贝,德国 | A15151 | |
| α-E2(CBH23的) | 慷慨地提供由史蒂芬Foung 10 | ||
| 三磷酸腺苷 | Steinheim,德国西格玛, | A2833-106 | |
| 谷胱甘肽 | Steinheim,德国西格玛, | G4251-1G | |
| 稻瘟 | invivo根,圣地亚哥,美国 | ANT-BL-1 | |
| G418(geneticin) | Invitrogen公司,卡尔斯鲁厄,德国 | 11811-064 | |
| 聚乙二醇-1500 | 罗氏,德国曼海姆 | 10783641001 | |
| 多聚甲醛 | 罗斯,卡尔斯鲁厄,德国 | 0335.3 | |
| 的Triton X-100 | 罗斯,卡尔斯鲁厄,德国 | 3051.2 | |
| 山羊血清 | Steinheim,德国西格玛, | G9023-5ML | |
| α-NS5A的(9E10) | 请提供由查尔斯·赖斯7 | ||
| 的DAPI(4',6'-diamidino-2-苯基盐酸盐) | Invitrogen公司 | D1306 | |
| Alexa的氟546 - 羊抗人IgG | Invitrogen公司,卡尔斯鲁厄,德国 | A21089 | |
| Alexa的氟488 - 羊抗鼠IgG | Invitrogen公司,卡尔斯鲁厄,德国 | A10680 | |
| 脂质体2000 | Invitrogen公司,卡尔斯鲁厄,德国 | 11668-019 | |
| CellTracker CMTMR | Invitrogen公司,卡尔斯鲁厄,德国 | C2927 | |
| CellTracker CMFDA | Invitrogen公司,卡尔斯鲁厄,德国 | C2925 | |
| fluoromount | Steinheim,德国西格玛, | F4680-25ML | |
| 所有其他化学品 | 罗斯,卡尔斯鲁厄,德国 | ||
| 细胞培养材料 | 萨尔斯塔特,Nümbrecht,德国 |
参考文献
- Zhu, Q., Guo, J. T., Seeger, C. Replication of hepatitis C virus subgenomes in nonhepatic epithelial and mouse hepatoma cells. J. Virol. 77, 9204-9210 (2003).
- Kato, T. Nonhepatic cell lines HeLa and 293 support efficient replication of the hepatitis C virus genotype 2a subgenomic replicon. J. Virol. 79, 592-596 (2005).
- Ali, S., Pellerin, C., Lamarre, D., Kukolj, G. Hepatitis C virus subgenomic replicons in the human embryonic kidney 293 cell line. J. Virol. 78, 491-501 (2004).
- Date, T. Genotype 2a hepatitis C virus subgenomic replicon can replicate in HepG2 and IMY-N9 cells. J. Biol. Chem. 279, 22371-22376 (2004).
- Chang, K. S. Replication of hepatitis C virus (HCV) RNA in mouse embryonic fibroblasts: protein kinase R (PKR)-dependent and PKR-independent mechanisms for controlling HCV RNA replication and mediating interferon activities. J. Virol. 80, 7364-7374 (2006).
- Zhong, J. Robust hepatitis C virus infection in vitro. Proc. Natl. Acad. Sci. U.S.A. 102, 9294-9299 (2005).
- Lindenbach, B. D. Complete replication of hepatitis C virus in cell culture. Science. 309, 623-626 (2005).
- Wakita, T. Production of infectious hepatitis C virus in tissue culture from a cloned viral genome. Nat. Med. 11, 791-796 (2005).
- Witteveldt, J. CD81 is dispensable for hepatitis C virus cell-to-cell transmission in hepatoma cells. J. Gen. Virol. 90, 48-58 (2009).
- Bitzegeio, J. Adaptation of hepatitis C virus to mouse CD81 permits infection of mouse cells in the absence of human entry factors. PLoS Pathog. 6, e1000978 (2010).
- Lindemann, D., Goepfert, P. A. The foamy virus envelope glycoproteins. Curr Top Microbiol Immunol. 277, 111-129 (2003).
- Brohm, C. Characterization of determinants important for hepatitis C virus p7 function in morphogenesis by using trans-complementation. J. Virol. 83, 11682-11693 (2009).
- Steinmann, E., Brohm, C., Kallis, S., Bartenschlager, R., Pietschmann, T. Efficient trans-encapsidation of hepatitis C virus RNAs into infectious virus-like particles. J. Virol. 82, 7034-7046 (2008).
- Koutsoudakis, G. Characterization of the early steps of hepatitis C virus infection by using luciferase reporter viruses. J. Virol. 80, 5308-5320 (2006).
- Frentzen, A. Completion of hepatitis C virus replication cycle in heterokaryons excludes dominant restrictions in human non-liver and mouse liver cell lines. PLoS Pathog. 7, e1002029 (2011).
- Lindemann, D. A particle-associated glycoprotein signal peptide essential for virus maturation and infectivity. J. Virol. 75, 5762-5771 (2001).
- Blight, K. J., McKeating, J. A., Rice, C. M. Highly permissive cell lines for subgenomic and genomic hepatitis C virus RNA replication. J. Virol. 76, 13001-13014 (2002).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。