Method Article
基于分子印迹的电容生物传感器超灵敏检测生物标志物
摘要
在这里, 我们提出了一个协议, 以检测和定量的低丰度分子在复杂的解决方案使用分子印迹结合电容生物传感器。
摘要
在自然科学中, 在复杂溶液中检测和定量生物分子的能力一直被高度追求;用于检测生物标志物、污染物和其他感兴趣的分子。一种常用的技术为这个目的是酶联免疫吸附试验 (ELISA), 其中往往一个抗体是针对一个特定的靶分子, 和第二个标记抗体用于检测的主要抗体, 允许研究中分子的绝对量化。然而, 抗体作为识别元素的使用限制了该方法的鲁棒性;也需要使用标记分子。为了克服这些局限性, 分子印迹已经实现, 创建了与模板分子互补的人工识别站点, 并 obsoleting 了使用抗体进行初始绑定的必要性。此外, 对于更高的灵敏度, 二次标记抗体可由依赖于电容的生物传感器代替靶分子的量化。在本协议中, 我们描述了一种快速、无标签检测和定量复杂样本中的低丰度生物分子 (蛋白质和病毒) 的方法, 其灵敏度明显优于常用的检测系统, 如 ELISA。这是所有介导的分子印迹结合电容生物传感器。
引言
生物分子的量化被用于科学中的许多不同的研究领域, 采用了放射免疫 (RIA) 或 ELISA1等方法。其中一些方法需要有标记的试剂, 如放射性同位素或标记为抗体/抗原的酶, 这使得它们耗费劳力, 并且耗时复杂的程序2。此外, 这些方法的鲁棒性、选择性和灵敏度对所有分析都不够;特别是, 当需要分析 attogram 数量而不是象形文字数量3时, 它们是不够的。为此, 生物传感器获得了相当大的兴趣4,5, 特别是与分子印迹, 以提高鲁棒性。
分子印迹依赖于通过在模板6周围聚合功能单体来创建空穴, 从而创建完全类似于模板7的人工识别站点。这项技术已用于几个应用, 包括药物传递系统和分析分离, 但也作为 biorecognition 元素的生物传感器8,9,10。然而, 在分子印迹聚合物 (MIPs) 的设计中仍然有一些困难的大分子模板, 如蛋白质和细胞11,12。由于这一点, 许多研究人员专注于将模板蛋白直接印迹到基板上, 从而创建了一个将被目标蛋白12识别的曲面。这种表面涂层技术用于为大型分子和组件 (包括蛋白质)使用识别腔, 称为微接触印迹 13, 14.该方法的一般过程取决于两个表面之间的聚合--模板图章和聚合物支持--模板在一个表面上吸附在15、16上, 并使其与单体处理表面。通过这种方法, 通过紫外聚合, 形成了一种薄聚合物薄膜。最后, 模板被删除, 留下模板特定的空洞在表面的印迹电极。该方法具有一些优点, 包括减少了印迹分子的活动损耗, 以及需要很小数量的模板分子来进行印迹处理16,17。因此, 可以在传感器表面创建这些经济高效、稳定、敏感和选择性的曲面, 以此作为用户选择的任何模板的目标。
该生物传感器可用于检测单蛋白和更大的大分子, 包括病毒。一个特定的病毒组获得最近的兴趣是噬菌体, 这是一种病毒感染细菌。对噬菌体进行快速和灵敏的检测, 在生物技术和制药过程中非常重要, 以便用噬菌体18确定细菌培养的感染。噬菌体检测最常用的生物检验方法是双层琼脂法19, 费时费力, 使用时间长。曾多次尝试开发新的病毒诊断工具 (包括噬菌体), 如原子力显微镜 (AFM)20, 干涉测量21, 电化学22, 传感器系统23,24. 由于生物传感器具有操作方便、灵敏度高、可实时测量1525等优点, 许多工作一直集中在生物传感系统上。一种特定类型的生物传感器是基于电容的变化。这些电容式生物传感器是一种电化学传感器, 用于测量当分析物与传感器表面上的 biorecognition 元素相互作用时介电特性的变化, 导致电容的减少2,4.电容式生物传感器用于检测各种分析方法, 如抗原、抗体、蛋白质和重金属离子6,26,27,28。这些类型的生物传感器具有固有的快速性、高灵敏度、简单、低成本、易于操作和实时测量的优点, 不加标签29。
本文所描述的方法旨在使高复杂样本中低丰度生物分子的检测和量化, 而不需要使用任何标记。特别是, 这种技术在生物分子阿托微量范围内最有用, 因为其他商业现有仪器未能准确定量其目标。
研究方案
1. 玻璃盖板的修改 (模板邮票)
- 要清洁玻璃盖板, 在室温下超声波清洗机的每一个步骤中依次浸泡10毫升1.0 米 HCl、去离子水和1.0 米的氢氧化钠。
- 用氮气将玻璃罩滑干。
注: 在气态氮的流下, 盖板会被蒸发干燥。
- 用氮气将玻璃罩滑干。
- 将清洁干燥的盖板浸入 10% (v/v), 10 毫升溶液中的 3-氨基丙基 triethoxysilane (APTES) 在乙醇中 1 h, 以在室温下在盖子玻璃表面上引入氨基基团。
- 用去离子水冲洗盖子。
- 用氮气把盖子滑干。
- 浸泡在 5% (v/v), 10 毫升的戊二醛溶液在10毫米磷酸盐缓冲 (pH 7.4) 为 2 h, 以激活在表面上的氨基组, 在室温下6,15的 APTES。
- 用10毫米磷酸缓冲液 (pH 7.4) 冲洗盖子, 以去除表面多余的戊二醛。
- 用氮气把盖子滑干。
- 1.0 毫升的模板 (蛋白质/噬菌体) 溶液在10毫米磷酸盐缓冲 (pH 7.4) 的0.1 毫克/毫升浓度。
注: 在1.0 毫升磷酸盐缓冲液中溶解0.1 毫克蛋白质 (10 毫米, pH 值 7.4)。如有需要, 可使用分光光度计 (280 nm) 测定蛋白质浓度。- 将此模板解决方案的200µL 放到修改后的封面上, 一夜之间孵化4摄氏度。
注: 过剩模板解决方案可用于准备 1-2 更多的模板邮票用于表征研究。 - 用10毫米磷酸缓冲液 (pH 7.4) 冲洗盖子, 以便从表面去除未绑定模板。
注: 冲洗电极, 三十年代用磷酸盐缓冲剂 (10 毫米, pH 7.4) 冲洗。 - 用氮气把盖子滑干。
注: 在聚合步骤中使用时, 盖板应保存在4摄氏度。
- 将此模板解决方案的200µL 放到修改后的封面上, 一夜之间孵化4摄氏度。
2. 电容式金电极的改性
- 为了清洁电极, 将电极浸入一个小烧杯中, 依次包含5毫升乙醇 (70%)、去离子水、丙酮、去离子水、酸性食人鱼溶液 (3:1、h2, 因此4: h2O2, v/v) 和去离子水, 每个步骤分别为10分钟, 在室温下的超声波清洗器。
- 用氮气干燥电极。
- 为了执行酪胺的聚合, 准备8毫升的10毫米酪胺溶液在10毫米磷酸盐缓冲 (pH 7.4) 含乙醇 (2 毫升)15。
注: 酪胺溶液总容积必须为8毫升, 包括2毫升乙醇。- 使用恒电位仪覆盖 0-1.5 V (Ag/AgCl) 的潜在范围, 并扫描速率为 50 mV/秒30, 执行此解决方案中的循环伏安扫描 (15 个周期)。
- 用去离子水冲洗电极。
- 用氮气干燥电极。
- 将电极浸入含有30毫米丙烯酰基氯和30毫米三甲胺的溶液中, 在室温下一夜 6, 15, 30, 在甲苯 (V 总 = 5 毫升) 中.
- 用去离子水冲洗电极。
注: 为了确保更好地去除反应丙烯酰基氯化物和三甲胺残留物, 还可以在去离子水后用氢氧化钠冲洗表面。 - 用氮气干燥电极。
- 用去离子水冲洗电极。
3. 模板印迹电容式金电极的制备
-
噬菌体印迹电容金电极的制备
- 在聚合之前, 准备一个单体溶液, 其中含有单体 (n-羟甲基丙烯酰胺) 和交联剂 (聚乙烯 glycol-400-dimethacrylate) 的比例为 1:5 (摩尔/摩尔) 在1毫升10毫米磷酸盐缓冲 (pH 7.4)。
注: 含有单体和交联剂的单体溶液可在不同配比下使用, 或者单体和交联器的类型可以根据模板优化特定的相互作用而改变。 - 将1毫克的照片启动器添加到此解决方案中。
注: 如果聚合是在 UV 光下进行的, 则必须使用光引发剂来启动聚合。如果聚合是由自由基聚合进行的, 则必须改变引发剂的类型。 - 吸管1.5 µL 这个溶液到金表面的修饰金电极。
注意: 电极的金表面在图 1中以示意图显示。 - 将模板图章与金电极表面顶部的单体溶液接触。
- 启动 UV 聚合 (365 nm, 400 W), 并继续15分钟31。
注: UV 聚合是在冷却柜内进行, 在开始聚合之前设置为-25 摄氏度。然后, uv 光固化系统开启, 在关闭 uv 光固化系统前, 聚合持续15分钟。 - 使用镊子从表面删除模板戳。
注: 从表面去除模板戳时, 表面上的聚合物薄膜可能损坏。因此, 应该在不使用武力的情况下, 小心而缓慢地将邮票从表面移走。 - 用去离子水冲洗电极表面, 用氮气将其烘干。
- 将电极浸泡在1毫升的10毫米 1-dodecanethiol 乙醇中制备20分钟, 以覆盖电极表面的针孔。
- 用去离子水冲洗电极, 用氮气干燥电极。
- 在聚合之前, 准备一个单体溶液, 其中含有单体 (n-羟甲基丙烯酰胺) 和交联剂 (聚乙烯 glycol-400-dimethacrylate) 的比例为 1:5 (摩尔/摩尔) 在1毫升10毫米磷酸盐缓冲 (pH 7.4)。
-
蛋白质印迹电容金电极的制备
- 聚合前, 制备含有单体的单体溶液 (丙烯酰胺:54 毫克;n-hydroxymethylacrylamide: 140 µL;n-丙烯酰胺: 85.6 毫克) 和交叉链接器 (methylenebisacrylamide: 9.5 毫克) 在820µL 的超纯水30, 32.
- 在超纯水中制备 5% (v/v) n、n、n、n '-tetramethylethyldiamine (TEMED)。
- 将 TEMED 溶液的20µL 加入单体溶液中, 用氮气净化5分钟。
- 在超纯水中制备 10% (w/v) 硫酸钾铵 (APS)。
- 将 APS 溶液的20µL 加入单体溶液中。
- 将单体溶液的1.5 µL 移到修饰金电极表面。
- 将模板戳与单体处理表面接触。
- 在室温下开始聚合, 持续5小时。
注: 为制备蛋白印迹金电极而非 UV 聚合, 室温下自由基聚合 (25 °c) 是以 APS-TEMED 为引发剂催化剂进行的。 - 使用镊子小心地从表面删除模板戳。
- 用去离子水冲洗电极, 用氮气干燥。
- 将电极浸泡在1毫升的10毫米 1-dodecanethiol 乙醇中制备20分钟, 以覆盖电极表面的针孔。
- 用去离子水冲洗电极, 用氮气干燥电极。
4. 电极表面的扫描电镜表征 (SEM)
- 用粘碳胶带将试样安装在铝持纸上。
- 涂层电极与10毫微米钯或金子。
- 用 SEM 检查电极。
5. 模板印迹电容式金电极实时电容测量
- 将印迹电容金电极插入到与电容式生物传感器集成的电化学流电池中。
- 准备100毫升再生缓冲器 (25 毫米甘氨酸盐酸盐, pH 2.5, 包括50毫米 Tween-20) 和 1 L 运行缓冲器 (为噬菌体印迹系统:10 毫米磷酸, ph 7.4; 蛋白质印迹系统:50 毫米三盐酸, ph 7.4)。
- 通过注入再生缓冲器进行分析, 重新生成系统和运行缓冲器, 使系统平衡25分钟。
- 在运行缓冲区中的所需浓度范围内准备标准模板解决方案。
注: 首先通过溶解0.1 毫克蛋白质, 或大约 108 pfu 噬菌体, 在1.0 毫升磷酸盐缓冲 (10 毫米磷酸盐, pH 7.4) 中, 先准备一个模板溶液的存货。然后, 通过将十序10倍稀释从库存溶液中制备出校准曲线的标准解。这些解决方案将在步骤5.5 中与电容式生物传感器进行分析。蛋白质浓度可以用分光光度计 (280 nm) 来测量。为了测量噬菌体浓度, 可以使用双层琼脂法, 详细描述了以前的19。 - 在最佳条件下依次向系统注入这些标准溶液的250µL (流量: 100 µL/分钟, 温度:25 °c)。
注: 在这个应用中, 标准蛋白质溶液是在 1.0 x 10-4 -1.0 x 10-14的浓度范围内制备的, 而噬菌体浓度在范围 1.0 x 101 -1.0 x 105 pfu/毫升。解决方案放在注射阀中, 并按顺序注入系统, 通过单注射器泵和多端口阀在 triplicates 中注入样品。该仪器的软件自动监测由模板绑定到印迹腔所产生的标准溶液后电容的减少。
结果
按照该协议, 根据图 1中的示意图, 裸金电极将被印上模板, 表示大分子的结构。该电极可应用于电容式生物传感器 (图 2), 允许将模板稳定地应用到电极上, 以及在模板绑定时测量电容的变化。
电容式生物传感器的示意图表示形式显示在图 2中。螯针泵, 负责连续注射的运行缓冲 (10 毫米磷酸盐, pH 值 7.4) 和再生缓冲 (25 毫米甘氨酸盐酸, ph 2.5) 在再生进入流动细胞, 可以清楚地看到在图中。流单元由工作、参考和计数器电极组成。注射阀由标准蛋白/噬菌体溶液组成, 通过 degasser, 然后依次注入系统。当解决方案到达工作电极插入到流单元中时, 实时监测结果。电容值可以按照计算机屏幕上的 sensorgrams 进行注册。
图 3和图 4描述了裸和印迹金电极表面之间的差异。这个特征步骤是重要的, 以确保有聚合物腔, 被视为粗糙的表面上的电极印迹后。除了 SEM, 还有其他的表征方法, 包括 AFM, 接触角测量, 椭偏等, 可以用来表征的表面后印记。通过这种方法, 可以保证印迹过程是成功的, 模板腔是在表面形成的。在这些腔内, 模板可以结合高特异性和亲和力。
将标准溶液注入电容系统后, 软件自动计算了最后五读数的平均值, 并通过绘制电容的变化与分析.注册电容的减少源于模板的绑定。与金电极表面结合的分子越多, 总电容的还原量越高, 根据电容测量的一般原理。图 5和图 6表明, 随着分析物浓度的增加, ΔC 会随预期的增长而增加。动态范围 (介于这两者之间是系统用于检测特定目标的浓度范围) 和检测极限 (LOD) 可以通过分析这些图来评估。根据图 6, 噬菌体印迹电容式生物传感器可以检测 101 -105 pfu/毫升浓度范围内的噬菌体, 该研究中的 LOD 值为 10 pfu/毫升。图 5和图 6也强调了在模板集中所需的相同间隔内测量校准曲线的必要性, 因为回归的线性度可能因浓度而异 (图 5), 或具有不同的斜率 (图 6)。还应指出, 由于使用的浓度低, 系统对波动非常敏感 (样品中的浊度、空气草稿、等), 因此建议至少运行 triplicates 以减少包括异常值的可能性。.出于同样的原因, 标准偏差对于高度稀释的样本可能非常重要, 如图 6所示。
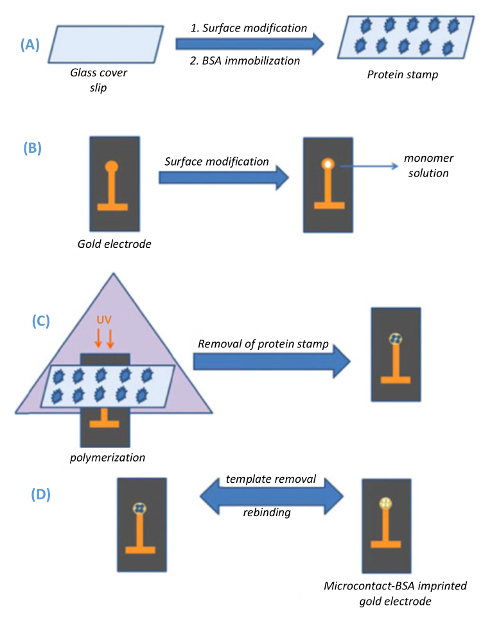
图 1.微接触印迹方法的示意图表示法。(A) 准备玻璃盖板 (模板戳), (B) 制备电容性金电极, (C) 通过 UV 聚合将模板微接触印迹到金电极表面, (D)从电极表面去除模板 (从 Ertürk et) 复制, 生物技术报告 2014 (3):65-72 以允许)。请单击此处查看此图的较大版本.
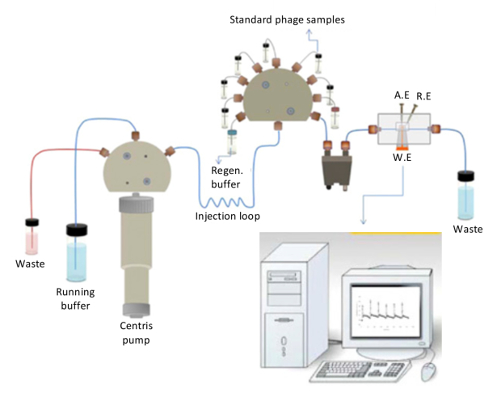
图 2。电容式生物传感器的示意图表示形式.本研究中使用的电容式生物传感器的总体布局 (从 Ertürk et) 复制, 生物技术报告 2014 (3):65-72 以允许)。请单击此处查看此图的较大版本.

图 3。扫描电子显微镜的蛋白质印迹电极.SEM 图像 (A) 裸金电极 (鳞片棒 = 20 µm) 和 (B) 蛋白质印迹电容金电极 (鳞片棒 = 10 µm)。请单击此处查看此图的较大版本.

图 4。噬菌体印迹电极的扫描电子显微镜.电镜图像的裸金电极 (鳞片杆 = 20 µm) (a) 和噬菌体印迹电容金电极在不同的放大 (6600x, 缩放条 = 10 µm) (B) 和 11,500X, 缩放条 = 5 µm) (C);箭头表示粘附噬菌体)。请单击此处查看此图的较大版本.
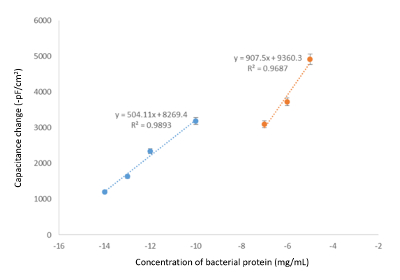
图 5。校准图的缓冲区组合的效果.校准图显示电容与蛋白质浓度在最佳条件下的变化 (运行缓冲器:50 毫米三盐酸, pH 值 7.4;再生缓冲器:25 毫米甘氨酸-HCl, pH 2.5 包括50毫米 Tween-20;流量: 100 µL/分, 样品容积: 250 µL;T:25 °c)。请单击此处查看此图的较大版本.

图 6。用于大型大分子的典型校准曲线.在最佳条件下显示电容与噬菌体浓度变化的标定图 (运行缓冲器:10 毫米磷酸盐, pH 值 7.4;再生缓冲器:25 毫米甘氨酸-HCl, pH 2.5 包括50毫米 Tween-20;流量: 100 µL/分, 样品容积: 250 µL;T:25 °c)请单击此处查看此图的较大版本.
讨论
当执行此方法时, 在遵循该协议时必须考虑一些关键步骤。一个关键步骤是清洁步骤与酸性食人鱼解决方案。步骤2.1 不能超过10分钟。步骤1.4 的模板解决方案不能超过0.1 毫克/毫升, 因为这些值以前已经过优化。为了获得最佳厚度, 循环伏安扫描不能超过15个周期。对于步骤 3.1.3, 1.5 µL 是一个优化值。对于此特定类型的电极, 此值必须不高。如果 UV 固化系统的功率为 400 W, 则聚合必须进行最大 10-15 分钟。一旦 ap (启动器) 在 TEMED 后添加到解决方案中, 则必须快速执行后续步骤以避免立即聚合 (步骤 3.2.5)。
最关键的步骤之一是在 UV 聚合后从表面去除模板戳。如果此步骤未正确执行, 则可能存在电极表面上的聚合物薄膜与图章一起移除的风险。因此, 建议在聚合后水溶液中将电极和蛋白印浸入顶部, 然后从表面 (步 3.1.6) 非常缓慢和小心地去除图章。
根据所使用的模板, 对所用单体 (功能单体和交联器) 的类型和比例的修改可以评估产生更高的灵敏度。这必须经验主义地确定。此外, 模板分子的亲和结合通常同时涉及几种不同的相互作用。因此, 这可能会导致在再生步骤中出现问题。如果绑定模板没有正确地从表面释放, 这可能会影响电极的可重用性, 以便进一步分析。这些多点亲缘关系也可能是通过较弱的交互绑定导致的。在这种系统中, 可能发生非特定绑定, 这会对系统16的选择性产生负面影响。这些是方法的常见和一般的限制。
除了这些特定的限制外, 讨论的方法在现有方法上有许多显著的优点。虽然区域一体化、ELISAs 和荧光测量非常敏感, 但它们需要使用标记材料 (无论是模板还是探测器), 而生物传感器完全没有标签。这些方法也更加昂贵和耗时。生物传感器的方法允许快速, 并行合成的 MIPs 在不同的组合在同一时间16。由于制备的单体溶液只有少数微升, 所以使用昂贵或其他有限的单体时, 该方法是方便的。此外, 单一的 MIP 电极可以用于大约80分析, 而不显著降低性能, 这比其他现有方法30显著高。现有的方法在不同程度上也受到低灵敏度和选择性的影响, 而所描述的方法允许在 pM 范围内检测和定量具有高选择性的分子。
由于该仪器的成本效益高、操作方便, 而且在短时间内实时敏感检测与现有方法相比, 在野外条件下, 生物传感器是非常有前途的注意点检测系统;例如, 用于环境监测和发展中国家的应用。在诊断疾病的许多应用中, 对复杂混合物 (如血清) 中的生物标志物进行实时、敏感、选择性和快速检测是必需的15,25。在这里, 生物传感器优于现有的方法, 特别是由于其鲁棒性和灵敏度。特别是为检测感染性药物, 噬菌体最近被认为是替代 biorecognition 元素的生物传感器由于其宿主细菌特异性33,34,35。用噬菌体替代抗体是非常有希望的, 以降低成本和增加稳定性, 甚至进一步36。这种系统还将允许在环境和临床样本中检测和量化特定的噬菌体。由于噬菌体的盛行, 以及它们用抗生素耐药性基因传感器细菌的能力37,38, 这种方法可能对研究耐药性细菌的传播有很高的价值。
披露声明
作者没有什么可透露的。
致谢
玛丽亚鲍姆嘉通 (智商生物技术平台, 传染医学, 隆德大学) 被认可为执行和提供扫描电子显微照片。这项工作得到了瑞典研究理事会 Formas (2017-00100) 的赠款的支持, 作为欧洲第三次关于抗菌素耐药性的联合规划倡议 (JPIAMR) 称为 "传输动力学" 的一部分。出资人在研究设计、口译、写作、撰写手稿、决定提交或决定发表作品方面没有任何作用。
材料
| Name | Company | Catalog Number | Comments |
| Glass Cover slips | ThermoFisher | 102222 | protein stamp |
| HCl | Sigma-Aldrich | H1758-500ML | cleaning |
| NaOH | Sigma-Aldrich | 72068-100ML | cleaning |
| Ultrasonic cleaner | Branson Ultrasonic | BRANSONIC M1800- E | cleaning |
| 3-amino-propyl-triethoxysilane (APTES) | Sigma-Aldrich | A3648-100ML | modification |
| EtOH | Sigma-Aldrich | 1009836010 | rinsing/cleaning |
| glutaraldehyde | Sigma-Aldrich | G5882-100ML | cross-linker |
| acetone | Sigma-Aldrich | 34850-1L-M | cleaning |
| H2SO4 | Sigma-Aldrich | 339741-100ML | piranha solution |
| H2O2 | Sigma-Aldrich | H1009-500ML | piranha solution |
| tyramine | Sigma-Aldrich | T90344-5G | modification |
| CompactStat | Ivium Technologies | CompactStat.h: 30mA@10V/3MHz | potentiostat |
| Platinum Counter Electrode Kit | Equilabrium | AFCTR5 | potentiostat |
| Reference Electrode | Equilabrium | RREF0021 | potentiostat |
| acryloyl chloride | EMD Millipore | 8.00826.0100 | modification |
| triethylamine | EMD Millipore | 8.08352.0100 | modification |
| toluene | Sigma-Aldrich | 244511-100ML | modification |
| N-hydroxymethyl acrylamide | Sigma-Aldrich | 245801-100G | functional monomer |
| poly ethylene glycol-400-dimethacrylate | Sigma-Aldrich | 409510-250ML | cross-linker |
| 2-Hydroxy-4′-(2-hydroxyethoxy)-2-methylpropiophenone | Sigma-Aldrich | 410896-50G | functional monomer |
| UV polymerizator | Dymax | Dymax 5000ECE | UV-polymerization |
| forceps | Sigma-Aldrich | Z168777-1EA | consumable |
| 1-dodecanethiol | Sigma-Aldrich | 471364-100ML | blocking agent |
| acrylamide | Sigma-Aldrich | A3553-100G | functional monomer |
| N-hydroxymethylacrylamide | Sigma-Aldrich | 245801-100G | functional monomer |
| N-isopropylacrylamide | Sigma-Aldrich | 415324-50G | functional monomer |
| methylenebisacrylamide | Sigma-Aldrich | 146072-500G | cross-linking monomer |
| N,N,N',N'-tetrametyhlethyldiamine (TEMED) | Sigma-Aldrich | T9281-25ML | catalyst |
| ammonium persulphate | Sigma-Aldrich | A3678-25G | initiator |
| Capacitive biosensor | CapSenze | Equipment | |
| Glycine | Merck | 1042011000 | regeneration buffer |
| Tween-20 | Sigma-Aldrich | P9416-50ML | regeneration buffer |
| Trizma base | Sigma-Aldrich | 93352-1KG | running buffer |
| Na2HPO4 • 2H2O | Calbiochem | 567547-1KG | running buffer |
| NaH2PO4 • 2H2O | Calbiochem | 567549-1KG | running buffer |
| DELPHI correlative light and electron microscope | Phenom-World | equipment | |
| Capacitive gold electrodes | CapSenze Biosystems | consumables | |
| 2,2'-azobis(2-methypropionitrile) | Sigma-Aldrich | 441090-25G | photo-initiator |
| CapSenze Smart Software | CapSenze Biosystems | software program |
参考文献
- Lin, T. Y., Hu, C. H., Chou, T. C. Determination of albumin concentration by MIP-QCM sensor. Biosensors and Bioelectronics. 20 (1), 75-81 (2004).
- Berggren, C., Bjarnason, B., Johansson, G. Capacitive Biosensors. Electroanalysis. 13 (3), 173-180 (2001).
- Zhang, S., Garcia-D'Angeli, A., Brennan, J. P., Huo, Q. Predicting detection limits of enzyme-linked immunosorbent assay (ELISA) and bioanalytical techniques in general. The Analyst. 139 (2), 439-445 (2014).
- Mattiasson, B., Teeparuksapun, K., Hedström, M. Immunochemical binding assays for detection and quantification of trace impurities in biotechnological production. Trends in Biotechnology. 28 (1), 20-27 (2010).
- Limbut, W., Hedström, M., Thavarungkul, P., Kanatharana, P., Mattiasson, B. Capacitive biosensor for detection of endotoxin. Analytical and Bioanalytical Chemistry. 389 (2), 517-525 (2007).
- Ertürk, G., Berillo, D., Hedström, M., Mattiasson, B. Microcontact-BSA imprinted capacitive biosensor for real-time, sensitive and selective detection of BSA. Biotechnology Reports. 3, 65-72 (2014).
- Arshady, R., Mosbach, K. Synthesis of substrate-selective polymers by host-guest polymerization. Macromolecular Chemistry and Physics. 182 (2), 687-692 (1981).
- Andersson, L. I. Molecular imprinting: developments and applications in the analytical chemistry field. Journal of chromatography. B, Biomedical sciences and applications. 745 (1), 3-13 (2000).
- Li, X., Husson, S. M. Two-dimensional molecular imprinting approach to produce optical biosensor recognition elements. Langmuir: the ACS Journal of Surfaces and Colloids. 22 (23), 9658-9663 (2006).
- Alexander, C., Davidson, L., Hayes, W. Imprinted polymers: artificial molecular recognition materials with applications in synthesis and catalysis. Tetrahedron. 59 (12), 2025-2057 (2003).
- Kryscio, D. R., Peppas, N. A. Surface imprinted thin polymer film systems with selective recognition for bovine serum albumin. Analytica Chimica Acta. 718, 109-115 (2012).
- Inerowicz, H. D., Howell, S., Regnier, F. E., Reifenberger, R. Multiprotein immunoassay arrays fabricated by microcontact printing. Langmuir. 18 (13), 5263-5268 (2002).
- Lin, H. Y., Hsu, C. Y., Thomas, J. L., Wang, S. E., Chen, H. C., Chou, T. C. The microcontact imprinting of proteins: The effect of cross-linking monomers for lysozyme, ribonuclease A and myoglobin. Biosensors and Bioelectronics. 22 (4), 534-543 (2006).
- Liao, P. C., Tyan, Y. C., Wang, C. Y., Hsu, J. F., Chou, T. C., Lin, H. Y. Assessing the binding selectivity of molecularly imprinted polymer artificial antibodies by mass spectrometry-based profiling system. Journal of Biomedical Materials Research Part A. 91 (2), 597-604 (2009).
- Ertürk, G., Hedström, M., Tümer, M. A., Denizli, A., Mattiasson, B. Real-time prostate-specific antigen detection with prostate-specific antigen imprinted capacitive biosensors. Analytica Chimica Acta. 891, 120-129 (2015).
- Ertürk, G., Mattiasson, B. From imprinting to microcontact imprinting-A new tool to increase selectivity in analytical devices. Journal of Chromatography. B, Analytical Technologies in the Biomedical and Life Sciences. 1021, 30-44 (2016).
- Ertürk, G., Mattiasson, B. Molecular Imprinting: The Creation of Biorecognition Imprints on Biosensor Surfaces. Advanced Molecularly Imprinting Materials. , 523-560 (2017).
- Janczuk-Richter, M., et al. Long-period fiber grating sensor for detection of viruses. Sensors and Actuators B: Chemical. 250, 32-38 (2017).
- Kropinski, A. M., Mazzocco, A., Waddell, T. E., Lingohr, E., Johnson, R. P. Enumeration of bacteriophages by double agar overlay plaque assay. Methods in Molecular Biology. 501, 69-76 (2009).
- Meillan, M., et al. Self-assembled monolayer for AFM measurements of Tobacco Mosaic Virus (TMV) at the atomic level. RSC Adv. 4 (23), 11927 (2014).
- Ymeti, A., et al. Fast, ultrasensitive virus detection using a Young interferometer sensor. Nano Letters. 7 (2), 394-397 (2007).
- Wei, Y., Wong, L. P., Toh, C. -. S. Fuel cell virus sensor using virus capture within antibody-coated nanochannels. Analytical Chemistry. 85 (3), 1350-1357 (2013).
- Guliy, O. I., et al. Immunodetection of bacteriophages by a piezoelectric resonator with lateral electric field. Applied biochemistry and microbiology. 52 (4), 457-463 (2016).
- Reta, N., Michelmore, A., Saint, C., Prieto-Simón, B., Voelcker, N. H. Porous silicon membrane-modified electrodes for label-free voltammetric detection of MS2 bacteriophage. Biosensors & Bioelectronics. 80, 47-53 (2016).
- Ertürk, G., Özen, H., Tümer, M. A., Mattiasson, B., Denizli, A. Microcontact imprinting based surface plasmon resonance (SPR) biosensor for real-time and ultrasensitive detection of prostate specific antigen (PSA) from clinical samples. Sensors and Actuators B: Chemical. 224, 823-832 (2016).
- Lebogang, L., Mattiasson, B., Hedström, M. Capacitive sensing of microcystin variants of Microcystis aeruginosa using a gold immunoelectrode modified with antibodies, gold nanoparticles and polytyramine. Microchimica Acta. 181 (9-10), 1009-1017 (2014).
- Loyprasert, S., Hedström, M., Thavarungkul, P., Kanatharana, P., Mattiasson, B. Sub-attomolar detection of cholera toxin using a label-free capacitive immunosensor. Biosensors & Bioelectronics. 25 (8), 1977-1983 (2010).
- Teeparuksapun, K., Hedström, M., Wong, E. Y., Tang, S., Hewlett, I. K., Mattiasson, B. Ultrasensitive detection of HIV-1 p24 antigen using nanofunctionalized surfaces in a capacitive immunosensor. Analytical Chemistry. 82 (20), 8406-8411 (2010).
- Labib, M., Hedström, M., Amin, M., Mattiasson, B. A capacitive biosensor for detection of staphylococcal enterotoxin B. Analytical and Bioanalytical Chemistry. 393 (5), 1539-1544 (2009).
- Ertürk, G., Hedström, M., Mattiasson, B. A sensitive and real-time assay of trypsin by using molecular imprinting-based capacitive biosensor. Biosensors & Bioelectronics. 86, 557-565 (2016).
- Ertürk, G., Uzun, L., Tümer, M. A., Say, R., Denizli, A. Fab fragments imprinted SPR biosensor for real-time human immunoglobulin G detection. Biosensors & Bioelectronics. 28 (1), 97-104 (2011).
- El-Sharif, H. F., Phan, Q. T., Reddy, S. M. Enhanced selectivity of hydrogel-based molecularly imprinted polymers (HydroMIPs) following buffer conditioning. Analytica Chimica Acta. 809, 155-161 (2014).
- Wang, F., et al. Detection of Salmonella Typhimurium on Spinach Using Phage-Based Magnetoelastic Biosensors. Sensors (Basel, Switzerland). 17 (2), (2017).
- Chin, B. A., et al. Rapid detection of small quantities of specific bacteria using phage-based wireless biosensors. 2016 10th International Conference on Sensing Technology (ICST). , 1-5 (2016).
- Park, M. -. K., Chin, B. A. Novel Approach of a Phage-Based Magnetoelastic Biosensor for the Detection of Salmonella enterica serovar Typhimurium in Soil. Journal of Microbiology and Biotechnology. 26 (12), 2051-2059 (2016).
- Mack, J. D., Yehualaeshet, T., Park, M. -. K., Tameru, B., Samuel, T., Chin, B. A. Phage-Based Biosensor and Optimization of Surface Blocking Agents to Detect Salmonella typhimurium on Romaine Lettuce. Journal of food safety. 37 (2), 12299 (2017).
- Colomer-Lluch, M., Jofre, J., Muniesa, M. Antibiotic resistance genes in the bacteriophage DNA fraction of environmental samples. Plos One. 6 (3), 17549 (2011).
- Lood, R., Ertürk, G., Mattiasson, B. Revisiting antibiotic resistance spreading in wastewater treatment plants - bacteriophages as a much neglected potential transmission vehicle. Frontiers in microbiology. 8, (2017).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。