Method Article
使用电子地图的光映射数据的高通量分析
摘要
该协议描述了 ElectroMap 的设置和使用,这是一个基于 MATLAB 的开源软件平台,用于分析心脏光学映射数据。ElectroMap 提供了一个多功能的高通量工具,用于分析各种心脏实验模型的光学映射电压和钙数据集。
摘要
光学映射是多细胞制剂中心脏电生理学高时空分辨率研究的既定技术。在这里,我们在分步指南中介绍使用 ElectroMap 分析、量化和映射通过光学映射获得的高分辨率电压和钙数据集。ElectroMap 分析选项涵盖各种关键电生理参数,图形用户界面允许直接修改预处理和参数定义,使 ElectroMap 适用于各种实验模型。我们展示了内置的起搏频率检测和信号分割如何允许对整个实验记录、急性响应和单拍变数进行高通量分析。此外,ElectroMap 还集成了自动多拍平均法,以提高噪声数据集的信号质量,在这里,我们演示了此功能如何帮助阐明在使用单个数据集时可能无法检测到的电生理变化节拍分析。软件中包含自定义模块,用于对传导、单文件分析和变数进行详细调查,如下所示。该软件平台可用于实现和加速复杂心脏电生理学的处理、分析和映射。
引言
光学映射利用电压和/或钙浓度的荧光报告机来询问多细胞制剂中的心脏电生理学 (EP) 和钙处理,其空间分辨率比传统的要高技术1,2,3。因此,光学映射已成为一项重要和日益被利用的技术,为心脏3、4、5的生理和病理生理电行为提供了关键见解。,6,7,8.光学映射实验获得的数据的有效处理和分析,由于多种因素而变得复杂。光学映射数据集的高时空分辨率特性导致由数千个图像帧组成的原始视频文件,每个帧由多个单个像素组成,从而产生需要高吞吐量和自动化的大型数据文件处理9.像素小、染料载荷差和不均匀以及荧光小小小变化导致光信号信号信号低,信噪比(SNR)较低,需要预处理才能实现有效分析。使用光遗传学起搏协议来启动活化,可能会扭曲荧光传感器11、12的记录信号,从而进一步复杂化处理和分析。此外,一旦数据处理,可以应用几种不一致的技术和定义来测量感兴趣的参数,最适用的技术因实验设置、模型和问题2而异。 10,13.这些限制阻碍了技术的进一步采用,并阻碍了真正客观的分析。
为了克服这些限制,几个研究小组设计了定制加工管道,以适应他们的实验模型,问题和硬件7,14,15,16。另一些则利用商业专有软件,其中底层算法可能难以访问4,17。因此,显然需要一个免费的开源软件平台来处理和分析光学映射数据。重要的是,该软件是开源的,易于使用,灵活的参数调整,适用于一系列具有不同EP特性的实验模型,并关键允许直接和可调的定量心脏范围参数,可以使用光学映射来研究。
我们最近发布并发布了一个全面的软件平台,ElectroMap,用于高全、半自动化处理、分析和映射心脏光学映射数据集13。在这里,我们提供了一个利用 ElectroMap 的视频手册,并演示了如何使用它来处理、分析和映射多个光学映射数据集。我们专注于使用 ElectroMap 量化标准 EP 和钙处理变量,并演示使用独立传导速度、单文件分析和变数模块。
研究方案
1. 光学映射数据收集
- 使用广泛的实验模型之一执行心脏光学映射,包括完整和孤立的整个心脏6,18,隔离的 atria14,19,心室楔20, 心脏切片21,22,和细胞单层23。请参阅实验设计的相关参考,以便从这些制剂中收集原始光学映射数据。前提是获得的数据可以转换为 tiff 堆栈或保存在 中。MAT 文件,它应该可以使用电子地图进行分析。这包括不同尺寸(方形/矩形)和分辨率(当前测试的最大尺寸为 2048 像素 x 2048 像素)的数据。
2. 软件安装和启动
注:下面详细介绍了安装和运行 ElectroMap 的两种方法 - 在 MATLAB 中从源 (.m) 代码运行,或者作为独立可执行文件 (.exe 用于窗口)。最终软件及其功能在两个设置选项之间是不变的(除了目录导航中的一些差异)。因此,选择要安装的版本的主要考虑因素是访问 MATLAB 和所需的工具箱,以及是否需要访问源代码。在可能的情况下,建议使用 MATLAB 版本,以加快启动时间、缩短处理时间并更轻松地报告错误。
-
设置 1:在 MATLAB 内运行电图
- 安装 MATLAB。ElectroMap 在 MATLAB 2017a 中设计,但是,软件已经过测试,可用于 MATLAB 的所有后续版本(截至撰写本文时为 2018b)。需要以下工具箱:图像处理、信号处理、统计和机器学习以及曲线拟合。
- 从 GitHub 存储库 (https://github.com/CXO531/ElectroMap) 下载/克隆 ElectroMap 的最新"源代码"版本中的所有文件。将下载的内容解压缩到所需位置。
- 打开 MATLAB 并导航到承载 ElectroMap 源代码的文件夹位置。然后,打开文件ElectroMap.m并在编辑器中按"运行",或者在命令窗口中键入ElectroMap,然后按RETURN。这将启动 ElectroMap 用户界面,图 1A。
-
设置 2:独立 .exe 文件
- 下载安装程序文件:https://drive.google.com/open?id=1nJyI07w9WIt5zWcit0aEyIbtg31tANxI。
- 按照安装程序中的说明进行操作,安装程序将从 Web 上下载所需的 MATLAB 运行时以及 ElectroMap 软件。
- 运行ElectroMap.exe.
注: 独立版本的启动时间可以是几分钟。
3. 图像加载和预处理
- 按"选择文件夹"并导航到要分析的数据文件的位置。这将使用该目录中具有正确文件类型 (.tif 或 ) 的所有文件填充左侧列表框。垫子)。.MAT 文件必须仅包含映像堆栈变量。
注:当您在目录选择器中导航时,只会显示文件夹,而不是单个文件。 - 选择要从接口内加载的文件,然后按"加载图像"。
- 加载后,将显示第一帧,红色轮廓将指示图像的自动阈值。如果需要,通过选择"保存/加载ROI"重新加载以前使用过的 ROI。在这种情况下,跳过步骤 3.3。
- 默认情况下,阈值基于第一帧中的像素强度。如果需要,请通过更改"图像"中阈值下拉菜单中的选项,将此修改为基于信号时间过程振幅的阈值。请注意,选择阈值后,将应用于整个映像堆栈。
- 如果需要,将阈值选项更改为手动,这将激活滑块以手动调整图像阈值。此外,裁剪图像 (裁剪图像) 和/或绘制一个自定义感兴趣的区域 (自定义 ROI) 通过选择低于阈值选项的相应勾选框进行分析。请注意,感兴趣的区域选择的高级选项(如区域数)可从顶部菜单中的ROI 选择中获得。
- 应用适当的阈值后,按"过程图像"进行应用处理。下面详细介绍了处理设置(步骤 3.4.1-3.4.5)。此时,请确保输入了正确的摄像机设置。这些是像素大小(重要:这是图像像素大小,而不是构成芯片或成像设备中等效硬件的像素大小)和帧速率(以 kHz 为单位)。
- 对于信号反转,请勾选"反转数据"复选框以启用。如果报告的荧光信号与兴趣参数成反比(与常用的电位染料一样),则信号可以反转。
- 对于空间筛选,从内核菜单中选择高斯或平均值。空间平均区域的大小由内核下拉菜单旁边的Size输入控制(即3 导致 3 像素 x 3 像素的筛选器内核)。应用高斯滤波器时,也可以从西格玛输入设置标准差。
- 对于基线校正,请从基线菜单中选择顶帽24或多项式(4度或 11 度)校正25。校正可以单独应用于每个像素(长时间处理),也可以作为整个图像的平均值(更快但假定同质基线更改)。也可以通过将"顶帽长度"设置为毫秒(以毫秒为单位)来修改顶帽校正,该长度与基线选择下拉菜单相邻。Top-Hat 内核的长度应大于单个动作电位/钙瞬变的时间尺度。
- 对于时间筛选,从筛选菜单中选择"萨维茨基-目标"或无限脉冲 (IIR) 筛选。
注:除了出现在左下角的组织平均信号外,在从集合平均图像范围进行参数量化时,将分别对每个像素应用时间滤波。通过在需要时筛选少量数据而不是整个文件,可以缩短处理时间。 - 对于帧删除,请注意,如果选择了"删除帧"选项,则可以从图像集中删除振幅大于目标信号的大峰。这在光学节奏的数据集中可能有用,例如光遗传学步调,其中去极化是由光激活蛋白酶(如通道性多普辛 211,12) 引起的。
注: 由于帧移除可能会在图像信号中引入非生理步骤更改,因此时间滤波可能会将伪影引入数据,因此此处不建议这样做。
- 请注意,一旦根据"分割"选项下的选项选择"过程图像",信号将被分割,但是无需重新处理整个数据集即可快速更改信号(请参阅第 4 节)。
4. 数据分割和集合平均
注:处理完文件后,组织平均信号(右下角轨迹,图1A)的峰值将被检测到,并贴上红色圆圈的标签。只计算高于设定阈值的峰值(由峰值阈值设置的跟踪上的蓝线)。此外,峰值仅在与由最小峰值距离输入设置的先前峰值相比充分延迟时才计算。然后根据检测到的峰值对信号进行分割。首先,通过测量每个峰值与下一个峰值之间的时间来计算每个峰值的有效周期长度 (CL)。如果一些峰值(由最小峰值数输入设置)具有类似的 CL(阈值由最小边界输入设置),则对它们进行分组,并计算这些峰值的平均 CL。
- 要进一步分割数据,请按段信号。子分段选项为:无= 具有相同 CL 的所有峰值组合在一起;所有= 在常量 CL 时间内 n个峰值的段(n峰值由段大小输入设置);如果输入,则标识 n 个峰值的段数;最后一个 = 在确定和分组 CL 更改之前的最终 n个峰值,并且不分析所有其他峰值;和单节拍– 这相当于应用具有 n个峰值= 1的所有分段,因此不应用任何分组或集合平均(参见 4.5)。这可以通过选择"单节拍"按钮来应用。
- 通过放大感兴趣的时间并选择分段信号来应用信号的自定义分割。这将向节列表框添加一个名为"缩放节"的附加选项,该选项对应于所选的时间点。
- 分割的结果将显示在组织平均信号旁边的列表框中,并显示节号和估计的CL。所有分段时间节均用不同颜色表示。从列表框中选择一个段以红色突出显示该部分。这也将自动触发此部分的分析,就像选择了"生成地图"按钮一样(请参阅第 5 节)。
- 将基于"平均"数据对分组峰值进行分析。这包括一起平均段中的峰值,参考时间为步骤 4.2 中标识的峰值。通过修改输入前后的时间窗口并按下段信号来更新为平均值。
5. 作用电位/钙瞬态持续时间和传导速度分析
- 处理图像后,"生成地图"按钮将变为活动状态。按"生成地图"应用操作电位持续时间 (APD)、激活时间、传导速度和 SNR 分析。默认情况下,分析将应用于第一个信号段。从列表框中选择其他线段会将分析应用于所选段。
注:分析结果显示在结果表中,包括平均值、标准偏差、标准误差、方差和第 5 至 95 百分位分析。持续时间图称为"APD"地图,但是,使用相同的设置处理的钙信号将测量钙瞬态持续时间。 - 选择"获取像素信息"以查看图像内任何像素的信号的详细显示,并比较像素以同时绘制来自最多 6 个位置的信号。
- 使用"信号处理"面板调整持续时间分析的设置。它们是:持续时间= 从峰值测量的百分比再极化/衰减时间;"APD"基线– 定义为振幅测量参考基线的信号时间段;和"APD"开始时间= 持续时间测量的开始时间。这些是决定等时图激活时间的相同选项(下文讨论),并称为:开始(d2F/dt2最大值)、上冲程(dF/dt最大值)、去极化中点(50% 振幅的时间),峰值(最大振幅的时间)。这些定义应用于小鼠和豚鼠行动电位如图2A所示。
注: 更改任何这些选项将自动更新持续时间图和结果表。地图比例和异常值删除选项也可用。
- 使用"信号处理"面板调整持续时间分析的设置。它们是:持续时间= 从峰值测量的百分比再极化/衰减时间;"APD"基线– 定义为振幅测量参考基线的信号时间段;和"APD"开始时间= 持续时间测量的开始时间。这些是决定等时图激活时间的相同选项(下文讨论),并称为:开始(d2F/dt2最大值)、上冲程(dF/dt最大值)、去极化中点(50% 振幅的时间),峰值(最大振幅的时间)。这些定义应用于小鼠和豚鼠行动电位如图2A所示。
- 传导速度也在主软件接口内自动测量。这是使用 Bayly 等人26的多矢量方法从所选激活措施定义的等时距图中实现的(步骤 5.4 中已讨论)。按激活点渲染激活图的 3D 表示形式。
- 多矢量传导速度测量方法在空间上将等时图分割成n x n像素的区域。使用"本地窗口大小"输入设置n的值,并设置激活时间范围,以便使用"拟合激活时间"输入将分析应用于。
注: 对于每个局部区域,拟合一个多项式曲面f,最能描述激活时间和空间位置之间的关系(x,y)。然后,此曲面的渐变矢量 CV局部值计算为: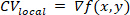 ⑴
⑴
其中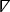 表示二维单数空间差分运算符26。
表示二维单数空间差分运算符26。 - 对于等时图中的每个像素,将计算表示传导速度和方向的局部矢量。从显示下拉菜单中选择具有矢量的等时贴贴图以查看此分析。
- SNR 计算为与基线信号的标准偏差相比的最大振幅比率。此分析在所有处理步骤后执行。按顶部菜单中的SNR 计算编辑定义为基线的信号周期的设置。
6. 传导分析模块
- 按传导以访问传导速度的更详细分析。这将打开一个单独的模块,其中传导可以使用 Bayly 多矢量方法进行量化,如在主接口、单矢量方法中,以及作为激活曲线。
- 按"单矢量"分析使用单矢量方法的传导,其中 CV 是根据两点之间的激活时间的延迟计算的。这可以使用"自动"或"手动"方法完成,可在"单矢量"按钮下方选择。
- 对于自动单矢量方法,选择测量传导的距离和起始点。然后,软件将从所选点执行 360 度扫描,测量时间延迟,并沿所有方向以 1 度增量计算相关的传导速度。此分析的结果显示在地图旁边的图形中,最慢的传导方向以红色显示。
- 对于手动单矢量方法,从等时图中选择起点和终点以计算传导速度。要选择新的起点,请按"清除起始点"。
- 按"局部矢量"以应用多矢量方法,其设置与主界面中的设置匹配。在传导模块中,可以显示传导速度的分布,以及计算矢量的角度分布和传导速度的角依赖性。
- 按激活曲线绘制作为时间函数激活的组织百分比。自动显示 100% 激活时间,同时也可以选择最小(蓝色)和最大(红色)激活百分比的自定义值。
7. 其他分析和模块
- 除了自动执行持续时间和传导速度分析外,还可以使用 ElectroMap 对其他几个参数进行量化。这些分析可以从显示地图上方的下拉菜单中选择。选择这些选项之一以执行分析,结果将显示在结果表的第4 行中:1)舒张间隔= 从 90% 重极到下一个操作电位的激活时间;2)主导频率– 每个像素的频谱使用快速傅立叶变换计算,功率最大的频率被定义为主导频率。通过选择频率映射,可提供用于主导频率分析的高级范围和窗口设置。3)峰值时间= 两个用户选择的百分比之间的上升时间(默认为 10 到 90%)作用电位或钙的脱极化相。可以通过选择"TTP设置"来更改百分比值 ;4)放松常数(*) = 放松常数是通过拟合形式形式的单指数衰减来计算的:
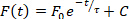 (2)
(2)
其中时间t的荧光水平取决于峰值荧光,F 0,和随后衰减(C是常数)27。拟拟方程 2 的值在主 ElectroMap 用户界面中可供选择,以及基于 r2值的拟合排除条件优。 - 按"单文件分析"打开一个专用模块,用于高吞吐量持续时间,并传导文件中每个标识段的分析。可以对整个图像(持续时间、传导和激活时间)或选定区域或感兴趣点(当前仅持续时间)执行分析。结果将输出到 .csv 文件。
注: 对于整个图像中的 APD 值,.csv 文件中的第一列是平均值,而第二列是标准偏差。 - 按Alternans启动独立模块,用于专门分析和映射节拍可变性。有关变子处理和分析选项的详细信息,请参阅 O'Shea 等人 201913。具体来说,该模块旨在识别两个周期振荡,称为变数。计算和输出持续时间和振幅变数。
注: 持续时间变数是通过比较从一个峰值到下一个峰值的持续时间测量来测量的;即,如果峰值 1 和 2 以及 APD1和 APD2分别,则持续时间变数 ([APD)]计算为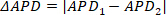 (3)
(3)
使用主界面中的设置执行持续时间测量。同时,振幅变化可以量化和映射跨多细胞准备作为绝对变化(定义为百分比其中0%= 相同的振幅之间的一个节拍和下一个)。此外,钙负荷等现象的影响可以通过测量和比较负荷和释放变数进一步研究,正如先前报道的28。如果L定义为大节拍的峰值振幅(即振幅大于前一个节拍),S 小节拍的振幅,D 小节拍的舒张负载,则释放变数 (
小节拍的舒张负载,则释放变数 (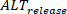 ) 定义为:
) 定义为: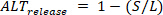 (4)
(4)
相反,负载变数 (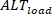 ) 定义为:
) 定义为: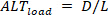 (5)
(5)
可以在整个组织中进行 Alternans 测量,分析结果显示在模块的右下角。首次使用模块时,将对整个实验文件执行分析,显示的结果是整个文件的平均节拍差。但是,通过取消选择"保持缩放"、放大特定时间段以及选择"分析缩放截面",可以将分析限制为文件中的特定时间。这将更新结果面板以显示所选时间段的分析。- 选择"播放"以显示变数分析的节拍视频。此外,选择"创建平均贴图"以导出从选择时间点平均的"更改"行为的地图,这些时间点在使用此功能时在弹出式菜单中设置。
- 按相位图启动相位映射模块。执行 Hilbert 变换以计算每个时间点的瞬时相位(介于 -+ 和 + 之间)。按播放或拖动滑块可显示一段时间内的相位行为,然后单击像素以呈现相图。
8. 导出数据
- 数据以各种形式从 ElectroMap 导出。按"导出值"以保存主使用的界面中当前显示的地图的值。测量值可以保存为地图(保留像素位置)或压缩到单个列表中,并可以保存为 .csv、.txt 或 。MAT 文件。
- 按"导出地图"可弹出包含当前显示的地图的弹出窗口,然后可以以各种图像格式保存该地图。地图的显示选项通过选择"地图设置"进行控制,但也可以在选择导出地图后进行编辑。例如,可以通过从顶部菜单中选择此图标来添加颜色栏,也可以通过选择"编辑>颜色映射"来设置比例。
- 按激活视频渲染激活序列的动画,该动画可以保存为动画 .gif 文件。
- 按分段视频保存每个已识别段当前显示的参数的 .avi 视频文件。
结果
作为这项研究的一部分进行的所有工作都是根据1986年《英国动物(科学程序)法》和欧洲议会关于保护用于科学目的的动物的第2010/63/EU号指令所规定的伦理准则进行的。实验得到了内政部的批准(鼠标:PPL 30/2967和PFDAAF77F,豚鼠:PPL PF75E5F7F)和伯明翰大学(小鼠)和伦敦国王学院(豚鼠)的机构审查委员会批准。在这里分析的原始数据收集的详细方法可以在我们以前的出版物5,6,14,19中找到。
控制 ElectroMap 的主接口如图1A所示。分析数据集的必要步骤主要由加载图像、进程图像和生成地图按钮控制,并在图 1A中分别以绿色、蓝色和红色突出显示。图 1B-D显示了选择每个按钮时执行的操作。加载图像应用用户选择的图像阈值选项(图1B),而进程图像(图1C)应用过滤和基线校正。最后,生成地图将首先根据时间窗口和分段设置(除非选择单节拍分割)平均数据,然后执行上述分析。
ElectroMap 的一个关键方面是它在摄像机类型和实验模型方面的灵活性。由于广泛使用的模型之间存在独特的心脏 EP 和解剖特征,因此这对光学映射软件的效用至关重要。图2A例如显示了与豚鼠心室相比,鼠耳的力势形态,使用电压敏感染料记录,如先前报道的6,14。尽管操作潜力的形状不同,并且使用了两个具有不同帧速率和像素大小的独立光学映射摄像机,但 ElectroMap 仍可用于成功分析这两个数据集。但是,这需要修改用户界面中的某些参数 (图 2B)。请注意,长时间的豚鼠行动潜力需要更大的时间窗口。此外,为了防止顶帽基线校正不生理地修改光学记录的信号,必须增加其时间长度,使其大于行动电位的时间过程。
ElectroMap 提供了多种处理选项,可帮助改进光学记录信号的 SNR,这些信号可能需要有效地恢复 EP 参数。例如,数据分段后的峰值的自动集合平均。图 3A-C演示了使用集合平均代替其他方法如何从孤立的鼠位(n = 13)中改进 SNR。这降低了测量异质性和分析失败的可能性 (图 3D)。例如,从 3 Hz 到 10 Hz 的起搏频率变化并没有改变 APD50,当没有进行集合平均时,但从集合平均数据测量时,在 10 Hz 起搏时 APD50的预期减少29次(图 3E.
图 4演示了 ElectroMap 提供的自动起搏频率检测和分段的有效性和效用。在这里,鼠标左 atria (n = 5) 以 120 ms 的周期长度和周期长度递增缩短 10 毫秒,直到达到 50 ms. ElectroMap 自动识别起搏周期长度和分组组织平均峰值(图 4A).这是在所有数据集中高精度实现的 (图 4B)。自动分割数据,通过增加起搏频率/缩短的周期长度,对传导速度的减慢进行直接、高通量分析(图4C,D)。同时,APD50 (图 4E) 和舒张间隔 (图 4F) 缩短.光学测量的峰值的振幅减小,而峰值时间增加(图4G,H)。这些再次成为心脏组织29,30的预期恢复反应,使用ElectroMap可以帮助阐明在存在药理剂、基因改造、作用下对起搏频率的反应变化,或疾病状态。
在使用电子地图等软件时,一个重要的考虑因素是基础数据中是否存在工件。图5,例如,表明运动伪影(通过组织运动对光记录的信号的失真)可以阻止对激活的精确测量,特别是在ElectroMap中重新极化。有关进一步考虑,请参阅讨论。
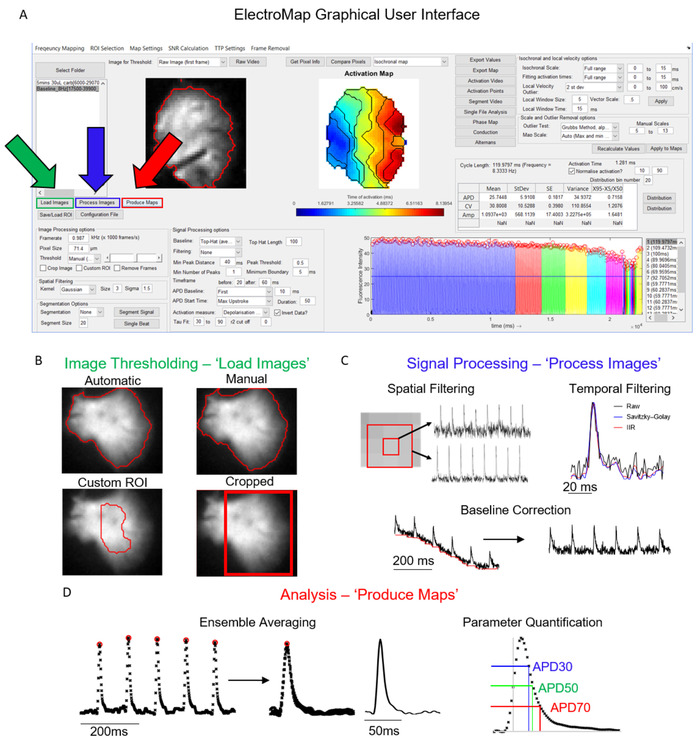
图1:电图主要处理步骤。(A) ElectroMap 的图形用户界面,突出显示加载图像(绿色)、过程图像(蓝色)和生成地图(红色)按钮。(B) 可在选择加载图像时应用的图像阈值选项。(C) 用户可用的信号处理选项包括空间和时间滤波和基线校正,可通过按"进程图像"应用于图像堆栈。(D) 通过选择"生成地图"激活的集合平均和参数量化(所示 APD 测量)。图改编自奥谢等人,201913。请点击此处查看此图的较大版本。
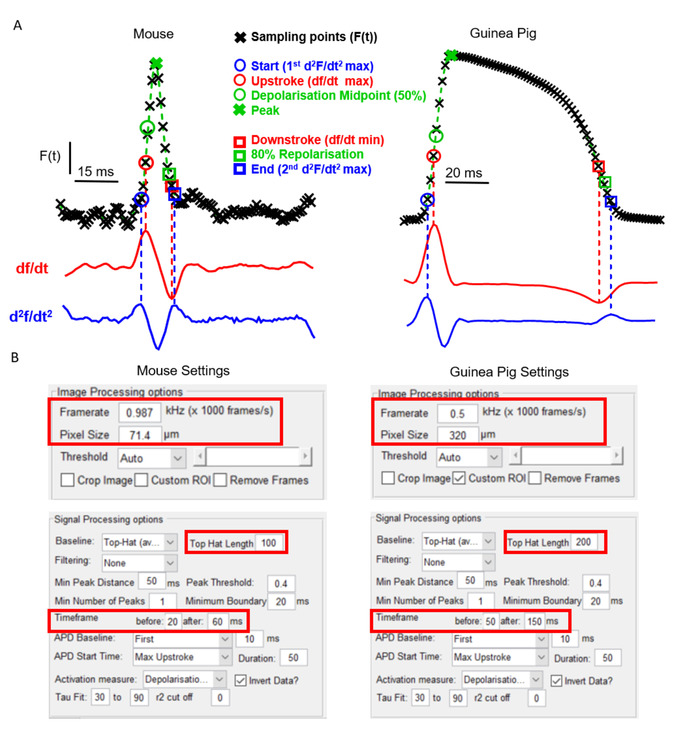
图2:使用ElectroMap分析小鼠和豚鼠数据。a) 从小鼠心室和豚鼠心室,以及这些信号的第一个(df/dt)和第二(d2f/dt2)衍生物的光学记录作用电位。在 ElectroMap 中可采用的激活和再极化时间的各种定义将突出显示。(B) 在 ElectroMaps 界面中使用的图像和信号处理设置的屏幕截图。红色框突出显示需要在分析小鼠和豚鼠数据之间进行修改的设置。图改编自奥谢等人,201913。请点击此处查看此图的较大版本。
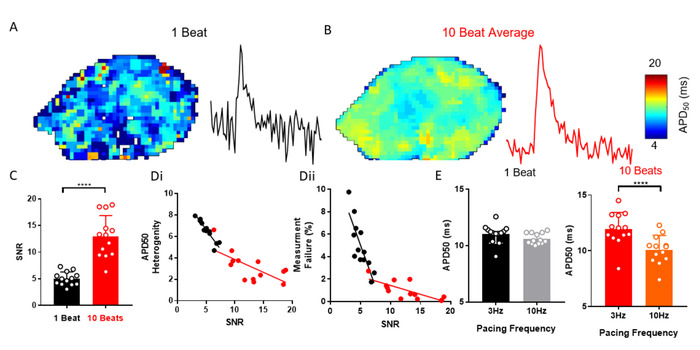
图3:集合平均解决APD更改。(A) APD50地图和单拍光学动作电位的单像素信号示例。(B) APD50映射和示例单像素信号,来自光学动作电位,由 10 个连续节拍(峰值方法)的一组平均产生。(C) 单节拍的 SNR 与 10 节拍平均信号相比.(D ) APD50异质性 (i) 和测量失败数 (ii) 作为单节拍的 SNR 函数和 10 拍的平均 APD50地图。(E) APD50在 3 和 10 Hz 起搏频率下,以单节拍和 10 个节拍图测量。(数据显示为均值 = 标准误差,n = 13 左 atria,=p < 0.001 通过学生的成对t-测试)。请点击此处查看此图的较大版本。
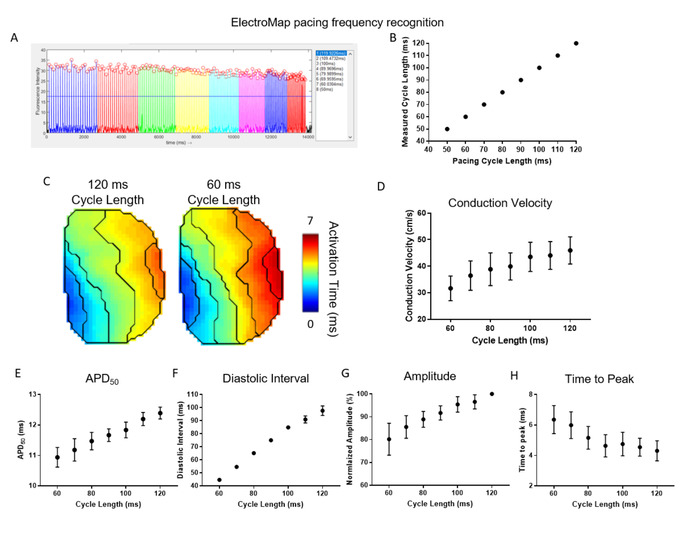
图4:使用ElectroMap研究心脏组织起搏频率反应。(A) 起搏频率识别和分割的电图屏幕截图示例。(B) 已知和电图测量的起搏周期长度的比较。(C) 120 ms 和 60 ms 起搏周期长度的激活映射。(D-H)传导速度 (D)、 APD50 (E)、舒张间隔 (F)、 振幅 (G) 和峰值时间 (H) 的分组数据,作为起搏周期长度的函数,以 10 ms 的增量从 120 ms 减小到 60 ms。(数据显示为平均值 = 标准误差,n = 5 左 atria) 请点击此处查看此图的较大版本。
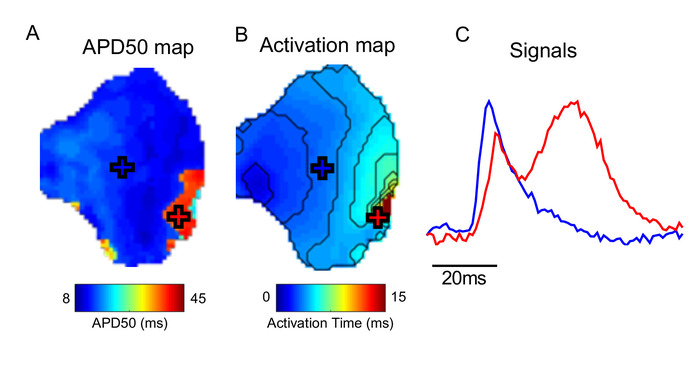
图5:运动伪影的效果。(A) APD50地图.(B) 激活映射.(C) 来自 APD 和激活地图上标记(交叉)位置的示例信号。在标有红十字的组织中,收缩未成功分离,从而扭曲了测量的光学信号。请点击此处查看此图的较大版本。
讨论
在这里,我们提供了一个分步指南,用于利用开源软件ElectroMap对心脏光学映射数据集进行灵活和多变量的分析。为了成功使用 ElectroMap,成像数据必须位于 .tif 或 中。MAT 格式。Electro 包含多个可修改的用户设置。如图2A所示,由于实验模型和成像硬件之间存在广泛的异质性,这是必要的。但是,这意味着软件中的默认设置并不总是最佳的,因此使用该软件的关键步骤是用户调整其特定实验设置的设置。其中包括摄像机设置和时间刻度,如图2B所示。找到最佳设置后,可以通过选择"配置文件"来保存这些设置,并在以后重新加载这些设置。
结合自动CL测量和信号分割是该软件的主要优势。这些功能允许分析实验录音中的急性反应,并扩大分析,从专注于孤立的单次节拍。实现所需的分段后,单文件分析模块允许自动分析每个单独的片段(包括单节拍),实现跨记录输出的多个变量的高吞吐量分析。单个 .csv 文件。同时,分组峰值的合奏平均是提高在 ElectroMap 中自动执行的噪声信号质量的有效方法。然而,集合平均并不普遍有益,例如在节拍可变性的研究中。因此,ElectroMap 集成了单节拍分割,以避免集合平均、替代处理选项,以改善 SNR(空间和时间滤波),并包括Alternans分析模块,以进一步调查和映射节拍的可变性。
光学映射数据集通常显示伪影,如基线漂移和运动伪影。同样,由于像素大小小、曝光时间短、荧光变化小2,生成的信号质量可能较低。这些因素会妨碍对基础 EP 行为进行有效和准确的分析。如上所述,ElectroMap 有几个处理策略来解决这些问题。但是,将这些算法应用于从根本上较差质量/失真的数据仍将阻止有效的分析。因此,SNR 是在 ElectroMap 中测量和显示的参数之一。同样,用户可以使用Pixel Info和比较模块选择和比较来自样本中特定区域的信号,从而能够识别现象,如图 5所示的运动伪影,并适当排除数据。
目前,ElectroMap 不支持以与基线校正相同的方式从原始数据中删除运动伪影。因此,该软件未来的可能发展是纳入运动物删除的计算方法,如已报道31,32。此外,ElectroMap 目前仅限于研究一个光信号。然而,对于比例染料和同时使用电压和钙染料27,需要同时处理两个波长通道。因此,双信号分析的集成是该软件未来的重要补充。扩展适用于心律失常数据集的分析选项,如相位奇点跟踪,同样会扩大软件33、34的范围。最后,所述几种分析选项在分析电极映射数据时也很有用。事实上,尽管电图波形对比为20、35,但ElectroMap已经用于分析电极映射数据,进一步优化将扩大其在这种模式上的应用。
披露声明
P.K.从几家活跃在心房颤动的药物和设备公司获得研究支持,并获得了几家此类公司的酬金。L.F.获得了欧盟、BHF、MRC、DFG和Gilead的机构研究资助。P.K.和L.F.被列为伯明翰大学持有的两项专利的发明者(心房颤动治疗WO 2015140571,心房颤动标志物WO 2016012783)。
所有其他作者均声明不存在潜在的利益冲突。
致谢
这项工作由EPSRC学生服务(科学-Phy-4-健康中心,博士培训L016346)资助, K.R.和L.F.,韦康信托种子奖授予(109604/Z/15/Z)给D.P.,英国心脏基金会赠款(PG/17/55/33087,RG/17/15/33106)给D.P.,欧洲联盟(授予P.K.和L.F.的第633196号[CATCH ME])英国心脏基金会(FS/13/43/30324至P.K.和L.F.) 的赠款协议;PG/17/30/32961 到 P.K.和 A.H.,以及莱杜克基金会到 P.K.。J.W. 由英国心脏基金会(FS/16/35/311952)支持。
材料
| Name | Company | Catalog Number | Comments |
| MATLAB and Simulink R2018a | Mathworks, Inc, Natick, MA | MATLAB software |
参考文献
- Efimov, I. R., Nikolski, V. P., Salama, G. Optical Imaging of the Heart. Circulation Research. 94, 21-33 (2004).
- Herron, T. J., Lee, P., Jalife, J. Optical imaging of voltage and calcium in cardiac cells & tissues. Circulation Research. 110, 609-623 (2012).
- Boukens, B. J., Efimov, I. R. A century of optocardiography. IEEE Reviews in Biomedical Engineering. 7, 115-125 (2014).
- Myles, R. C., Wang, L., Kang, C., Bers, D. M., Ripplinger, C. M. Local β-adrenergic stimulation overcomes source-sink mismatch to generate focal arrhythmia. Circulation Research. 110, 1454-1464 (2012).
- Syeda, F., et al. PITX2 Modulates Atrial Membrane Potential and the Antiarrhythmic Effects of Sodium-Channel Blockers. Journal of the American College of Cardiology. 68, 1881-1894 (2016).
- Winter, J., et al. Sympathetic nervous regulation of cardiac alternans in the intact heart. Frontiers in Physiology. 9, 1-12 (2018).
- Faggioni, M., et al. Suppression of spontaneous ca elevations prevents atrial fibrillation in calsequestrin 2-null hearts. Circulation: Arrhythmia and Electrophysiology. 7, 313-320 (2014).
- Sato, P. Y., et al. Loss of Plakophilin-2 Expression Leads to Decreased Sodium Current and Slower Conduction Velocity in Cultured Cardiac Myocytes. Circulation Research. 105, 523-526 (2009).
- Yu, T. Y., et al. Optical mapping design for murine atrial electrophysiology. Computer Methods in Biomechanics and Biomedical Engineering: Imaging & Visualization. 5, 368-378 (2017).
- Laughner, J. I., Ng, F. S., Sulkin, M. S., Arthur, R. M., Efimov, I. R. Processing and analysis of cardiac optical mapping data obtained with potentiometric dyes. American Journal of Physiology. Heart and Circulatory Physiology. 303, H753-H765 (2012).
- Crocini, C., Ferrantini, C., Pavone, F. S., Sacconi, L. Optogenetics gets to the heart: A guiding light beyond defibrillation. Progress in Biophysics and Molecular Biology. 130, 132-139 (2017).
- Entcheva, E., Bub, G. All-optical control of cardiac excitation: Combined high-resolution optogenetic actuation and optical mapping. The Journal of Physiology. 9, 2503-2510 (2016).
- O’Shea, C., et al. ElectroMap: High-throughput open-source software for analysis and mapping of cardiac electrophysiology. Scientific Reports. 9, 1-13 (2019).
- Yu, T. Y., et al. An automated system using spatial oversampling for optical mapping in murine atria. Development and validation with monophasic and transmembrane action potentials. Progress in Biophysics and Molecular Biology. 115, 340-348 (2014).
- Jaimes, R., et al. Functional response of the isolated, perfused normoxic heart to pyruvate dehydrogenase activation by dichloroacetate and pyruvate. Pflugers Archiv. 468, 131-142 (2016).
- Wang, K., et al. Cardiac tissue slices: preparation, handling, and successful optical mapping. American Journal of Physiology. Heart and Circulatory Physiology. 308, H1112-H1125 (2015).
- Parrish, D. C., et al. Transient denervation of viable myocardium after myocardial infarction does not alter arrhythmia susceptibility. American Journal of Physiology. Heart and Circulatory. , (2017).
- Ihara, K., et al. Electrophysiological Assessment of Murine Atria with High-Resolution Optical Mapping. Journal of Visualized Experiments. (132), e56478 (2018).
- Holmes, A. P., et al. A Regional Reduction in Ito and IKACh in the Murine Posterior Left Atrial Myocardium Is Associated with Action Potential Prolongation and Increased Ectopic Activity. Plos One. 11, e0154077 (2016).
- Lang, D., et al. Arrhythmogenic remodeling of β2 versus β1 adrenergic signaling in the human failing heart. Circulation: Arrhythmia and Electrophysiology. 8, 409-419 (2015).
- Kang, C., et al. Human Organotypic Cultured Cardiac Slices: New Platform For High Throughput Preclinical Human Trials. Scientific Reports. 6, 1-13 (2016).
- Wen, Q., et al. Transverse cardiac slicing and optical imaging for analysis of transmural gradients in membrane potential and Ca2+ transients in murine heart. The Journal of Physiology. 596, 3951-3965 (2018).
- Houston, C., et al. Characterisation of re-entrant circuit (or rotational activity) in vitro using the HL1-6 myocyte cell line. Journal of Molecular and Cellular Cardiology. 119, 155-164 (2018).
- Yu, T. Y., et al. Optical mapping design for murine atrial electrophysiology. Computer Methods in Biomechanics and Biomedical Engineering: Imaging and Visualization. 5, 368-376 (2017).
- Laughner, J. I., Ng, F. S., Sulkin, M. S., Arthur, R. M., Efimov, I. R. Processing and analysis of cardiac optical mapping data obtained with potentiometric dyes. AJP: Heart and Circulatory Physiology. 303, H753-H765 (2012).
- Bayly, P. V., et al. Estimation of Conduction Velocity Vector Fields from Epicardial Mapping Data. IEEE Transactions on Bio-Medical Engineering. 45, 563-571 (1998).
- Jaimes, R., et al. A technical review of optical mapping of intracellular calcium within myocardial tissue. American Journal of Physiology. Heart and Circulatory Physiology. 310, H1388-H1401 (2016).
- Wang, L., et al. Optical mapping of sarcoplasmic reticulum Ca2+ in the intact heart: Ryanodine receptor refractoriness during alternans and fibrillation. Circulation Research. 114, 1410-1421 (2014).
- Winter, J., Shattock, M. J. Geometrical considerations in cardiac electrophysiology and arrhythmogenesis. Europace. , (2016).
- Mironov, S., Jalife, J., Tolkacheva, E. G. Role of conduction velocity restitution and short-term memory in the development of action potential duration alternans in isolated rabbit hearts. Circulation. 118, 17-25 (2008).
- Khwaounjoo, P., et al. Image-Based Motion Correction for Optical Mapping of Cardiac Electrical Activity. Annals of Biomedical Engineering. 43, 1235-1246 (2014).
- Christoph, J., Luther, S. Marker-Free Tracking for Motion Artifact Compensation and Deformation Measurements in Optical Mapping Videos of Contracting Hearts. Frontiers in Physiology. 9, (2018).
- Umapathy, K., et al. Phase Mapping of Cardiac Fibrillation. Circulation: Arrhythmia and Electrophysiology. 3, 105-114 (2010).
- Tomii, N., et al. Detection Algorithm of Phase Singularity Using Phase Variance Analysis for Epicardial Optical Mapping Data. IEEE Transactions on Biomedical Engineering. 63, 1795-1803 (2016).
- Cantwell, C. D., et al. Techniques for automated local activation time annotation and conduction velocity estimation in cardiac mapping. Computers in Biology and Medicine. 65, (2015).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。