Method Article
基于核磁共振的片段筛选,样品最少,自动化程度最高
摘要
核磁共振基于片段的筛选是快速鉴定生物大分子(DNA、RNA或蛋白质)的小分子结合剂的可靠方法。介绍了描述基于自动化的样品制备、NMR 实验和采集条件以及分析工作流程的协议。该技术允许对 1H和 19F NMR活性细胞核进行最佳利用以进行检测。
摘要
基于片段的筛选(FBS)在学术界和工业界的药物发现过程中都是一个经过充分验证和接受的概念。基于核磁共振的片段筛选的最大优势在于它不仅能够检测超过7-8个数量级亲和力的结合剂,而且还能够监测片段的纯度和化学质量,从而产生高质量的命中率和最小的假阳性或假阴性。FBS的先决条件是对片段库进行初始和定期质量控制,确定片段在相关缓冲液中的溶解度和化学完整性,并建立多个文库以覆盖不同的支架以适应各种大分子靶标类别(蛋白质/RNA/DNA)。此外,需要在生物构建/片段空间、条件空间(缓冲液、添加剂、离子、pH 和温度)和配体空间(配体类似物、配体浓度)水平上对样品数量、采集和分析速度进行广泛的基于 NMR 的筛选方案优化。至少在学术界,到目前为止,这些筛选工作是以非常有限的方式手动进行的,导致筛选基础设施的可用性有限,不仅在药物开发过程中,而且在化学探针开发的背景下。为了经济地满足要求,提出了先进的工作流程。它们利用最新的先进硬件,通过这些硬件,液体样品收集可以以温控方式自动填充到NMR管中。 1然后在给定温度下收集基于H / 19F NMR配体的光谱。高通量自动进样器(HT 自动进样器)可在温控块中处理 500 多个样品。这与先进的软件工具相结合,加快了数据采集和分析的速度。此外,还描述了在蛋白质和RNA样品上应用筛选程序,以了解生物大分子研究中广泛用户群的既定方案。
引言
基于片段的筛选现在是一种常用的方法,用于鉴定相当简单和低分子量的分子(MW <250 Da),这些分子与包括蛋白质,DNA和RNA在内的大分子靶标的结合较弱。来自主筛选的初始命中作为对市售的较大命中类似物进行二次筛选的基础,然后利用基于化学的片段生长或连接策略。对于成功的基于片段的药物发现(FBDD)平台,通常需要一种强大的生物物理方法来检测和表征弱命中,片段库,生物分子靶标和后续化学策略。药物发现活动中常用的四种生物物理方法是热位移测定、表面等离子体共振(SPR)、晶体学和核磁共振波谱(NMR)。
核磁共振波谱在FBDD的不同阶段显示出不同的作用。除了确保溶解在优化缓冲液系统中的片段库中片段的化学纯度和溶解度外,配体观察的NMR实验还可以检测片段与低亲和力靶标的结合,并且靶标观察到的NMR实验可以描绘片段的结合表位,从而实现详细的构效关系研究。在表位作图中,基于NMR的化学位移变化不仅可以识别正位结合位点,还可以识别可能神秘的变构位点,并且只能在生物分子靶标的所谓激发构象状态下才能访问。如果生物分子靶标已经结合内源性配体,则通过执行基于NMR的竞争实验,可以很容易地将鉴定的片段命中分为变构或正位。确定配体-靶点相互作用的解离常数(KD)是FBDD过程中的一个重要方面。基于NMR的化学位移滴定,无论是配体还是靶标,都可以很容易地进行,以确定 KD。核磁共振的一个主要优点是相互作用研究是在溶液中和接近生理条件进行的。因此,可以探测用于分析配体/片段与其靶标相互作用的所有构象状态。此外,基于核磁共振的方法不仅仅限于筛选折叠良好的可溶性蛋白质,而且还被用于适应更大的靶标空间,包括DNA、RNA、膜结合和固有无序蛋白质1。
片段库是 FBDD 流程中不可或缺的一部分。通常,片段充当初始前体,最终成为为生物靶标开发的新抑制剂的一部分(亚结构)。据报道,几种药物(维奈托克2,维莫非尼3,艾达非替尼4,Pexidartnib5)已以片段形式开始,现已成功用于临床。通常,片段是具有高水溶性和稳定性的低分子量(<250Da)有机分子。一个精心制作的片段库通常包含几百个片段,已经可以保证对化学空间的有效探索。片段库的一般组成随着时间的推移而发展,通常是通过将已知药物解剖成更小的片段或计算设计得出的。这些不同的片段库主要包含扁平芳烃或杂原子,并遵循Lipinski规则5 6或当前商业趋势规则 3 7,但避免反应性基团。一些片段库也衍生或由高度可溶的代谢物、天然产物和/或其衍生物组成8。大多数片段库带来的一个普遍挑战是易于下游化学。
法兰克福歌德大学生物分子磁共振中心(BMRZ)是iNEXT-Discovery(用于转化研究发现的核磁共振,EM和X射线基础设施)的合作伙伴,iNEXT-Discovery是一个为来自所有生物化学和生物医学研究领域的所有欧洲研究人员提供结构研究基础设施的联盟。在iNEXT于2019年结束的先前计划中,制作了一个由768个片段组成的片段库,旨在覆盖广阔的化学空间,以实现"最小片段和最大多样性"。此外,与任何其他片段库不同,iNEXT片段库也是基于"准备片段"的概念设计的,旨在简化复杂、高亲和力配体的下游合成,此后称为内部文库(Diamond、Structural Genomic Consortium和iNEXT)。
通过核磁共振建立FBDD需要人力、知识和仪器。在BMRZ,已经开发了优化的工作流程,以支持通过NMR进行片段筛选的技术援助。这些包括片段库 9的质量控制和溶解度评估,所选靶标的缓冲液优化,基于 1H或19 F-观察的 1D配体筛选,区分正位和变构结合的竞争实验,基于2D的靶标观察NMR实验用于表位定位,以及表征与初始片段命中的二级衍生物集的相互作用。BMRZ已经建立了用于分析小分子-蛋白质相互作用的自动化程序,正如之前在文献 10,11中所讨论的那样,并为基于NMR的片段筛选提供了所有必要的自动化基础设施。它已经实施了饱和转移差核磁共振(STD-NMR),通过梯度光谱(waterLOGSY)观察的水配体,以及基于Carr-Purcell-Meiboom-Gill(基于CPMG)的弛豫实验,以鉴定各种亲和力范围内的片段,以及最先进的自动化核磁共振仪器和用于药物发现的软件。虽然基于NMR的片段筛选已经很好地用于蛋白质,但这种方法不太常用于寻找与RNA和DNA相互作用的新配体。BMRZ已经为能够识别小分子RNA/DNA相互作用的新方案建立了概念验证。在本贡献的以下部分中,报告了蛋白质和RNA样品筛选程序的应用,以了解生物大分子研究中广泛用户群的既定方案。
研究方案
1. 片段库
- 内部片段库
注:在iNEXT的一项联合研究活动的框架内,开发了一个强大的下游化学友好型第一代片段库12 ,随后与Enamine合作组建了第二代文库,被称为DSI(Diamond-SGC-iNEXT)-准备片段库(从现在开始称为"内部图书馆")。该库可在BMRZ提供,用于筛选目的。- 使用先前报道的基于 NMR 的方案评估片段库的完整性和溶解度9.
注意:内部库由 768 个具有非常高化学多样性的片段组成(>200 个单例)。在片段混合物中进行筛选可以显着加快筛选活动;然而,由于 1H-NMR波谱中的信号重叠,混合物中的片段数量受到限制。内部库提供的更高化学多样性允许制备包含12个不同片段的混合物,在 1H观察到的NMR波谱中没有任何明显的化学位移重叠。 - 768个片段中的103个片段具有氟原子。对于 19F 筛选目的,根据最小 19F 化学位移重叠,将所有具有氟基团的 103 个片段分成 5 个混合物。为了最大限度地减少 19F 筛选中的信号重叠,请使用来自单个化合物测量的化学位移信息来设计具有最大片段数和最小信号重叠的混合物。每种混合物都有 20-21 个片段,具有不同的 19F 化学位移,允许明确分配片段。
- 使用先前报道的基于 NMR 的方案评估片段库的完整性和溶解度9.
- 用户定义/提供的片段库
- 使用用户定义或提供的片段库执行筛选活动;但是,在筛查活动之前需要执行以下步骤。
- 如果用户事先未指定,则对片段进行基于NMR的质量控制(在BMRZ,为此使用先进的软件工具;9,第6.1.1章)。
- 使用前检查片段在所选缓冲液中的溶解度,了解生物分子靶标、结构完整性和片段浓度。
- 设计混合物以减少 NMR 波谱中的信号重叠和测量时间。
- 按照步骤4.2设计混合物。
- 筛选单个片段或混合物的子集,而不是整个库。
2. 样品制备
注意:核磁共振高通量筛选利用移液机器人进行样品制备。核磁共振波谱以及蛋白质、RNA和DNA信号采集数天的稳定性对温度波动极为敏感,因此温控自动化系统将极大地促进移液样品的稳定性。为此,一个额外的附加装置在4至40°C之间工作,与移液机器人耦合,用于在温度受控的环境中处理NMR样品的液体。
- 配体混合物制备
- 使用样品制备机器人制备用于 NMR 测量的筛选样品。机器人的灵活配置允许广泛的应用(例如,将样品从核磁共振管中回收回储存容器或一般液体处理任务)。可以使用不同直径(1.7、2.0、2.5、3.0 和 5.0 mm)的 NMR 管。自动取样系统与先进的控制软件一起读取为每种容器类型分配的条形码,并以最佳方式执行液体灌装方案。
- 为了制备内部图书馆配体混合物,请使用条形码小瓶。带条形码的小瓶保证了样品的最高可靠性和最佳的可追溯性。
- 将 768 种化合物分配到 8 个 96 孔格式的板中。每个单独片段的储备浓度在d 6-DMSO/D2O(9:1)中为50 mM。总共制备 64 个混合物,每个混合物包含 12 个片段。混合物中每个片段的最终浓度为4.2 mM。
注意:移液机器人可以容纳具有不同几何形状的各种容器类型(冷冻或自动进样器样品瓶、圆形或方形深的 96 孔板、条形码标准样品瓶、微量离心管),并有助于有效地将液体转移到各种 NMR 管和架子上。

图 1:(A) 安装在 BMRZ 的高通量 NMR 样品制备和 NMR 管灌装机器人。(B) 高通量自动进样器,在 BMRZ 设施的 600 MHz 光谱仪上安装了单独的温控架。 请点击此处查看此图的大图。
- 筛选样品制备空白(参考配体谱图)和靶标(存在靶标的配体)
- 为了制备核磁共振筛选样品,在目标生物分子(蛋白质/RNA/DNA)和配体混合物存在的情况下,使用从布鲁克核磁共振标准核磁共振管产品组合中选择的3 mm NMR HT进样管。
- 手动或使用移液机器人将生物分子靶标(例如, 1小时筛选:10 μM RNA或蛋白质)在定义的筛选缓冲液中转移到3 mm NMR管(最终体积为200 μL)中。
- 在下一步中使用机器人系统将 10 μL(例如, 1小时筛选)配体混合物转移到包含目标生物分子的条形码 3 mm NMR 管中,并使用控制软件的内置协议进行混合。
注意:核磁共振管的条形码编号可方便、自动地整合到采集的核磁共振数据集中,从而确保以ID为导向的工作流程,而不会造成任何混淆。移液机器人温度控制附件允许将制备的样品保持在恒定温度下的NMR管中。
- 内部定义的条件和参数
- 建立最佳缓冲液条件,以针对内部片段库进行RNA和蛋白质筛选。以下样品条件用于BMRZ处的RNA:25 mM KPi,50 mM KCl,pH 6.2。镁2+ 是可选的。
- 蛋白质对溶液条件极其敏感;使用最适合所选靶标的缓冲液。对于这些缓冲液中的每一个,获取配体的额外参考光谱以作为分析的空白。
- 用户指定的条件
注意:如果内部确定的条件不适合从潜在用户中筛选目标,则应执行以下步骤。- 单独对缓冲液进行 1H-NMR,以确保在执行和分析配体观察到的筛选实验时,缓冲液成分的干扰最小。干扰成分可以适当地用氘代当量代替。
- 样品生产(目标数量)/条件和可用性的限制
注意:在某些情况下,某些生物大分子的分离或重组生产可能具有挑战性,并导致靶标的可用性有限,无法进行成功的药物筛选活动。在靶标可用性有限或无限的情况下,可以使用以下替代方案进行成功的基于NMR的片段筛选。- 如果限制,请使用 基于19个F-NMR的筛选。典型的氟化配体具有单个 19F信号;因此,使用具有25-30个片段的鸡尾酒,没有任何信号重叠。需要分析的信号更少,缓冲器组件没有信号干扰,命中识别所依赖的信号也更少。
- 如果无限制,请使用更大的屏幕,如 1H-NMR。可以筛选较大的片段库。通常,片段由多个质子组成,这意味着分析所依赖的信号更多。
3. 核磁共振获取条件
- 内部一般定义的条件
- 配备HT自动进样器的光谱仪(自动化)
- 对于高通量筛选,请使用只能使用 HT 自动进样器测量的 96 孔板。HT 自动进样器还可以单独回火每个样品架。
- 为了获得最佳信噪比,请使用带有氦气或氮气冷却的低温探头的光谱仪。自动化需要自动调谐和匹配模块 (ATM)。
- 参数设置和脉冲序列
注意:许多NMR实验可以表征结合事件。命中标识因实验设置而异。以下实验通常用于BMRZ筛查活动。但是,可以根据用户规范对用户定义的筛选活动进行更改。- 如果使用TopSpin软件,请包括基于配体的实验的参数集:SCREEN_STD,SCREEN_T1R,SCREEN_T2 SCREEN_WLOGSY。参数集包括所有必要的参数和脉冲序列:STD:stddiffesgp.3;T1ρ: t1rho_esgp2d;T2: cpmg_esgp2d;和水日志:ephogsygpno.2。
- 对于所有列出的实验,使用激发雕刻13 作为水抑制。作为参考,请使用 1D 激发雕刻 (zgesgp)。扫描次数取决于系统的灵敏度(磁场强度和探头)、样品浓度和实验选择。建议是:NS=64的1D,NS=128的T1ρ 和T2 ,NS=256的STD,NS= 384或512的waterLOGSY。
- 对于 19F 筛选,同时使用 1D 和 T2 实验:1D:F19CPD (pp=zgig) 用于 19 F{1 H} 探头头,F19(pp=zg) 用于 19F/1H 探针头;SCREEN_19F_T2 (pp = cpmgigsp)。
- 使用220 ppm的光谱宽度和-140 ppm的激励频率。实验时间在1到5小时之间(确保生物大分子的长期稳定性),具体取决于硬件和样品浓度。对于 T2,CPMG 时间应在 0 ms 和 200 ms 之间交替。
- 加工
- 将STD,T1ρ 和T2 实验记录为伪2D。为了处理两个单一的一维波谱,IconNMR使用au程序proc_std,无论是否带有松弛选项。第一个选项提供参考一维和两个光谱的差异。第二种选择产生两个独立的光谱,弛豫时间短且长。waterLOGSY是单个1D,应与溶剂信号的负值进行相位。
- 配备HT自动进样器的光谱仪(自动化)
- 用户特定条件
- 使前面提到的任何参数适应用户定义的条件。例如,如果用户提供的蛋白质在一般使用的温度下不稳定,则可以进行不同的温度、浓度、缓冲条件等的优化实验。
4. 数据分析
- 片段库质量控制(d6-DMSO/特异性缓冲液)和定量
- CMC-q
注意:在开始筛选活动之前,片段库的质量控制至关重要。此外,在多次筛选活动中,需要确保片段库的长期稳定性,这就是为什么必须对文库的质量进行定期评估的原因。为此,TopSpin的集成软件CMC-q和CMC-a用于质量和数量评估。CMC-q 和 CMC-a 是 Topspin 中的软件模块,可使用从有机小分子 9 获得的 1H-NMR 波谱进行平滑采集和分析,包括结构验证。- 为了完整性,在d6-DMSO中制备片段浓度为1 mM的评估样品。使用移液机器人自动制备样品,将液体样品收集物填充到3 mm NMR管中。
- 对于溶解度评估,使用由 1 mM 化合物组成的样品在 pH 7.4、150 mM 氯化钠、90% H 2 O/10% D 2 O 和 1 mM 的 3-(三甲基硅基)丙酸-2,2,3,3-d4 酸性钠盐 (TMSP-Na) 下。
- 使用配备三共振 5 mm TCI 低温探头和 HT 自动进样器的 600 MHz NMR 波谱仪收集 298 K 或 293 K 的 NMR 波谱,该探头可同时处理 579 个样品。
- 要设置 CMC-q 软件,请按照用户手册的说明进行操作,该手册实现了 IconNMR 用户的创建、快速通道 NMR 的激活以及更改 HT 自动进样器。
- 校准 90° 脉冲并将其保存在 TopSpin prosol 表中。
- 将 96 样品孔板放置在 HT 自动进样器中的 5 个机架位置之一。
- 要加载SDF文件(结构数据文件),该文件应包含其建议的化学结构,唯一标识符以及批次中每个样品的HT自动进样器中的位置,请转到CMC-q设置窗口中的 浏览 ,然后在选择以.sdf结尾的文件后单击 打开 。
- 在CMC.q批次自动化设置中,设置定义将要测量的实验的验证类型、IconNMR用户并定义溶剂。
- 为 SDF 文件的路径、分子 ID 和样品位置定义 SDF 文件。
- 通过单击开始 开始获取。再次点击 开始获取 。CMC-q 安装程序也可以通过单击 保存来保存。
- 有关 CMC-q 设置步骤的详细说明,请按照布鲁克的用户手册说明进行操作。
- CMC-a
- 对于CMC-a,请使用Topspin中的软件模块,该模块可以使用从有机小分子9获得的1H-NMR波谱进行分析,包括结构验证。
- CMC-q
- 混合料设计
注意:适当的混合物设计对于使用NMR作为平台的筛选起着重要作用。每个混合物的大量片段可以加快筛选速度,但会增加假阳性和假阴性的风险。较低的数字会降低这种风险,但会增加进行筛查所需的时间。通常,在创建混合物时必须避免信号重叠。使用内部文库,对于 1H 筛选可以忽略这一点,因为该文库经过专门设计,具有多样性,在保持高化学多样性的同时几乎没有信号重叠。这反过来意味着无需经过特殊的设计程序即可创建64种混合物。- 由于 19F 筛选依赖于内部文库中含有氟的片段,并且创建文库并不是为了减少这些特定片段的信号重叠,因此请设计适当的混合物。
- 测量含有 19F 的所有片段的单个化合物光谱。
- 注意每个信号的化学位移信息。
- 根据此信息,每种混合物选择20-21个片段。这反过来又给出了5个混合物,每个混合物包含20-21个片段,没有信号重叠,并允许对数据进行半自动分析。
- 在配体观察到的生物大分子-配体相互作用内执行命中鉴定
注意: 在 19F 和 1H 筛选程序之间,对命中有不同的定义。以下命中标识由我们设置并遵循特定规则。命中确定的主题是一种非常主观的方式,可能因用户而异。然而,至关重要的是,一旦商定了命中识别规则,就不会改变,以保持验证和可信度。- 1H 屏幕
- 为了自信地确定命中率,请在存在和不存在靶标的情况下获取 1D 1H 光谱、waterLOGSY 和 T2 弛豫实验,以鉴定粘合剂。所有三个实验都有可能显示结合事件。如果与空白光谱相比,样品光谱中可见大于 6 Hz 的 CSP,则认为这是命中的指示。如果水中可见强烈的正信号以及样品光谱中超过 30% 的 T2 减少,情况也是如此。当将含有光谱的样品与其各自的空白光谱进行比较时,可以在所有三个实验中展示结合事件。然而,在所有三个实验中,结合事件可能不可见。因此,人们一致认为,必须至少发生两个先前描述的事件才能将片段归类为绑定命中。
- 使用 TopSpin 中的 FBS 工具将片段的状态定义为绑定、模糊、未知、聚合和非绑定。
- 完成混音后,在 FBS 工具中批准它。
- 在FBS项目的摘要选项卡中,单击创建 筛选报告。这将打开一个创建.xlsx文件的窗口。然后,用户可以选择在所有配体、仅结合配体、不仅结合配体和要在电子表格中报告的模糊配体之间进行选择。
- 19F 屏幕
- 要区分非结合剂、周活页夹和强结合剂,请将 200 ms 目标测量值和 200 ms 空白测量值之间的积分商除以 0 ms 目标测量值的商,并使用 0 ms 空白测量值:
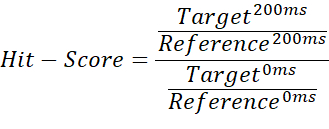
注意:这给出了从 0 到 ~1(命中分数)的值,从而可以为每个绑定状态分配阈值。 - 使用参考 200 毫秒测量值的平均值作为基线阈值,以标记命中分数超过 1 的情况。如果导入的积分包含负值或参考测量值高于目标测量值,则可能会发生这种情况。命中得分≤0.67被认为是弱命中,<0.33被认为是强命中,任何>0.67的命中都是无命中。 示例如图 2 所示。
- 要区分非结合剂、周活页夹和强结合剂,请将 200 ms 目标测量值和 200 ms 空白测量值之间的积分商除以 0 ms 目标测量值的商,并使用 0 ms 空白测量值:
- 1H 屏幕
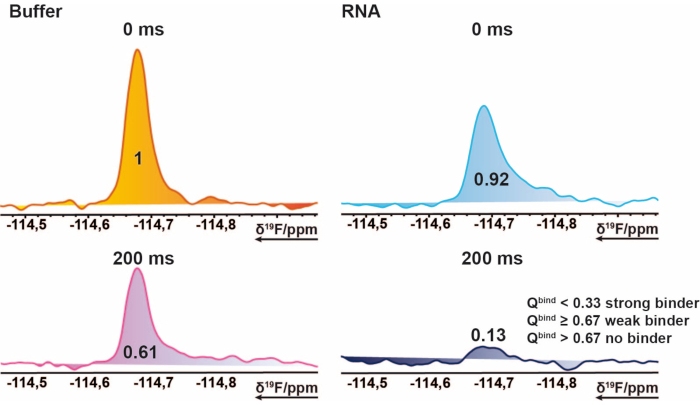
图 2: 19F 筛选的命中识别。 示例性化合物的 19F CPMG NMR波谱部分。此图形表示解释了粘合剂的特性。 19在存在和不存在RNA的情况下从混合物样品中获取的化合物的F-CPMG谱图。这些值表示相应峰值的赋范积分值。 请点击此处查看此图的大图。
- 数据分析
- 准备要分析的数据
注意:重要的是,采集的数据没有明显的缺陷。这意味着不应考虑垫片有问题或阻水不足的数据进行分析。相反,建议再次记录数据,并确保样品(例如,没有气泡)、温度、垫片和水抑制一切正常。在比较DMSO信号时,始终可以评估数据的正确性。 - 1H 筛查
- 要分析 1小时筛选数据,请使用TopSpin 4.0.9中的FBS工具(需要额外的许可证)。
- 按照FBS工具手册中的说明开始数据分析。以下步骤总结了手册中报告的过程。
- 存储来自筛选活动的BMRZ NMR数据,以便每种不同的筛选混合物都有自己的目录,其中子目录包含对样品测量的不同实验。
- 要使用FBS工具,请存储参考光谱,该参考光谱包含从没有生物分子靶标的样品中保存的所有数据,但与混合物以及在不同/nmr目录中测量的单一化合物一起保存。这很重要,因为FBS工具会单独询问每个目录路径。
注意:如果以下数据集存储在存储筛选样品混合物的同一目录中(csv、FragmentScreen XML 文档和 BAK 文件),则 FBS 工具会将目录识别为筛选项目。 - 使用 TopSpin 4.0.9 时,创建包含所获取数据的目录的直接路径,即所谓的 DIR。 选择 /nmr 目录,其中所有混合物都应具有不同的目录。
- 要启动筛选样本的 FBS 工具,请将符号 FBS 项目拖动到 TopSpin 窗口的中间。在所选目录中,如果先前所述的数据集被复制到其中,则应显示FBS项目符号。
- 首次加载新的FBS项目时,窗口" 基于片段的筛选选项 "应自动打开。在此窗口中,选择一个鸡尾酒文件。鸡尾酒文件是一个csv文件,其中包含混合物名称的分配,每个片段的名称以及它们在混合物中的划分。还要定义一个参考配体谱图文件夹,其中包含单个片段的所有测量谱图。最后,定义一个参考空白实验文件夹,该文件夹通常是包含没有所调查目标的混合物数据集的文件夹。
- 基于片段的筛选选项有一个名为 "光谱类型 "的选项卡,可用于定义所研究的光谱以及用于显示光谱的颜色。根据事先处理的数据设置规格类型。在 "显示布局 "选项卡中,定义将根据其规格类型相互比较的光谱。
- 按 "确定" 启动 FBS 项目。
- 在查看数据时,将打开一个单独的窗口,汇总表格中的所有鸡尾酒混合物和每种混合物的所有配体。通过双击单元格,将打开相应的数据集,例如 将 1H 1D 空白光谱与包含目标的数据集进行比较。
- 在分配粘合剂之前,请确保参比峰(所有测量值的DMSO以及单个化合物)相互匹配并具有相同的化学位移。如果观察到差异,请使用 TopSpin 的串行处理选项进行更正。
- 串行处理选项位于"高级"下的"进程"选项卡下。它将更改应用于数据集中所有选定的光谱。这样,可以轻松地将规格类型分配给实验编号,并且可以立即移动所有光谱以与参考对齐。
- 19F 筛选
- 对于 19F 混合物的首次分析,请为每个混合物创建一个积分文件。要定义集成区域,请单击"分析"选项卡中的"集成"功能。确保为混合物中的每个片段定义相应的 19F 单点的清晰积分区域。
- 使用 保存/导出集成区域按钮导出集成 文件以供将来使用。将任何使用的集成文件保存在 C:\Bruker\TopSpin4.0.9\exp\stan\nmr\lists\intrng 或 TopSpin 安装目录的相应路径中。
- 对于 19F 数据,打开包含或不具有调查目标的数据集。
- 要将集成文件加载到当前频谱中,请再次打开"分析"选项卡,转到"集成"并使用"读取/导入集成区域"按钮加载相应的集成文件。这会将该文件的任何已定义区域加载到当前频谱中。
- 保存并返回以在 积分 选项卡中查找所有集成区域的列表。将其复制到电子表格或用于进一步分析数据的任何其他工具中。
- 对每个混合重复此过程,有和没有目标。
- 数据管理
- 为了便于使用和提高工作效率,请设置统一的工作流程,以便进一步分析和存储获取的数据。对于 1H 和 19F 筛查,请为每个筛查使用专门设计的电子表格。
注意:对于 1H 筛选,这纯粹用于数据管理和汇总每个目标,而对于 19F 筛选,它使用第 4.3 章中的解释商在将积分数据复制到其中后自动将每个片段标记为命中/未命中。这降低了分析过程中人为错误的风险,假设文件设置正确,并使信息共享更容易,因为所有重要信息都收集在一个文件中,几乎任何人都可以打开该文件,而无需进一步的程序来初步查看数据。
- 为了便于使用和提高工作效率,请设置统一的工作流程,以便进一步分析和存储获取的数据。对于 1H 和 19F 筛查,请为每个筛查使用专门设计的电子表格。
- 准备要分析的数据
结果
片段库的质量控制
来自内部文库的片段以 50 mM 储备溶液的形式在 90% d6-DMSO 和 10% D 2 O 中交付(10% 的 D2O 可确保由于重复冻融循环而导致的化合物降解最小化14)。单个化合物样品由 1 mM 配体在 50 mM 磷酸盐缓冲液(25 mM KPi pH 6.2 + 50 mM KCl + 5 mM MgCl 2)、pH 6.0 在 90% H 2 O/9% D2O/1% d6-DMSO 中组成。1在500/600 MHz核磁共振波谱仪上测量iNEXT文库中片段的H-NMR实验。该数据进一步用于使用CMC-q软件在1H筛选活动中鉴定单个化合物,该软件允许用户以自动方式完全获取光谱,并评估分析插件CMC-a片段的质量(溶解度和完整性)。CMC-a 的自动分析结果显示为图形输出,类似于图 3 所示。图形输出显示了 96 孔板的表示。红色圆圈表示该片段在结构或浓度上显示不一致。绿色孔表示片段一致。
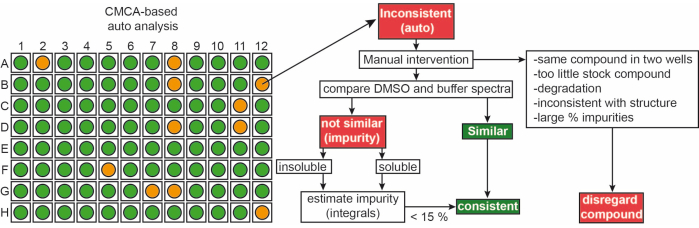
图 3:片段库的质量控制。 基于 CMC-a 的自动输出的示意图。评估碎片特性,如浓度和结构完整性。绿色代表一致,在这种情况下橙色代表不一致。不一致的片段按照所示的工作流程手动修改。 请点击此处查看此图的大图。
在DMSO和缓冲液中,大约65%和35%的片段分别被归类为一致和不一致。此外,30%的不一致分类配体在仔细手动检查光谱9后变得一致。
19F 混合料设计
来自内部库中的103个含有一个或多个氟基团的片段被分成5种混合物(A,B,C,D,E)。每个混合物有 20 到 21 个片段。在这种情况下,必须仔细设计混合物以避免信号重叠。 19测量施加CPMG脉冲序列的每种混合物的F横向弛豫实验。这些实验可以通过改变弛豫延迟来修改。混合物A-E的 19F化学位移如图 4所示。
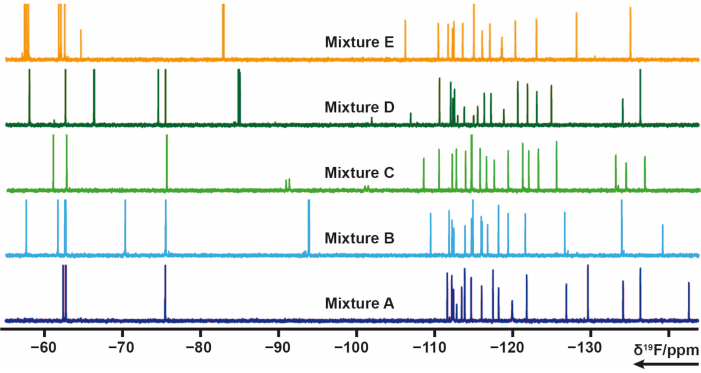
图 4:来自内部库中混合物样品的 19F 1D-NMR 波谱。 请点击此处查看此图的大图。
样品制备
19F筛选程序中的样品制备既可以手动完成,也可以使用移液机器人进行自动移液。每种混合物中的片段在90%d6-DMSO和10%D 2 O中的浓度为2.5mM。筛选样品的最终体积为 170 μL,含 5% D2O 作为锁定剂。将每种混合物移液两次,一次在含有溶液(无靶标)的缓冲液中,一次移入含有靶标的缓冲溶液中。将靶标和片段的比例设置为1:1,最终靶标/配体浓度为50μM。 此外,对照样品是筛选缓冲液中不含混合物的靶标生物分子,以确保靶标完整性,以及仅使用缓冲液和D2O的对照样品,以确保缓冲液质量。
19 架 F-1D和 19架 F-CPMG-T2 的核磁共振筛选数据是第 3.1 节中所述的测量值。例如,在RNA的情况下,为缓冲液中的单个目标样品采集了跳回波序列(pp = zggpjrse,15)。
数据分析
19F筛选程序应用于来自大肠杆菌的TPP核糖开关thiM和来自结核分枝杆菌的蛋白酪氨酸激酶(PtkA)以及其他几个靶点16。19F 筛选文库有 103 个片段,分为 5 个混合物,从混合物 A 到 E 标记,筛选样品的制备可以手动进行,无需使用样品移液机器人。将含有40μM thiM RNA的溶液(缓冲条件)与混合物中的3.2μL混合。制备进一步的对照样品,仅由缓冲液、含有5%DMSO的缓冲液(先前确保生物大分子在所需DMSO浓度存在下的稳定性)和RNA缓冲液组成。制备这13个筛选样品并将其转移到3 mm NMR管中。扫描NMR管的条形码,并根据上述在298 K下进行的19F NMR实验测量存在和不存在RNA的每种混合物以及对照样品。完成测量后,通过比较所有样品额外测量的1H 1D实验中所有DMSO峰的线展宽和强度损失,监测适当的匀场和水抑制。分别使用TopSpin中先前制备的自动化宏对获得的CPMG T219F弛豫谱进行处理。按照协议部分中的说明进行数据分析。通过设置正确的条件和阈值,可以使用预制电子表格或任何类似程序快速轻松地评估从 TopSpin 获得的积分数据(按照协议中的说明)。如前所述,阈值在定义绑定器、弱绑定器或非绑定器时很有用。图5分别显示了ThM RNA和PtkA的CPMG光谱的典型结果。在有些情况下,需要进一步的专家修订。
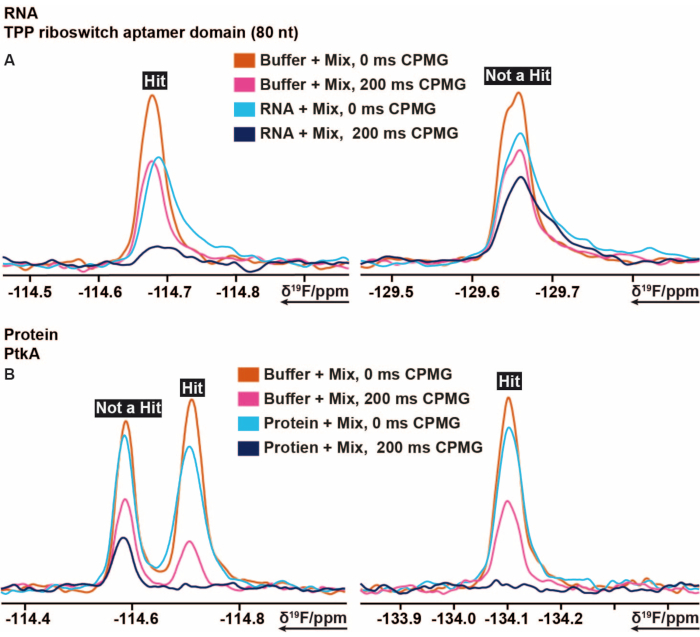
图 5:从 19F CPMG NMR 波谱中切出,显示了基于 CPMG 的实验的不同延迟时间获得的强度变化。 (A)在对来自大肠杆菌的TPP核糖开关thiM RNA进行的基于19F片段的筛选中粘合剂(命中)和非粘合剂的表示。(B)在对结核分枝杆菌的PtkA进行的基于19F片段的筛选中粘合剂和非粘合剂的表示。请点击此处查看此图的大图。
1小时筛选
混合料设计
使用的内部文库非常多样化,以至于在 1H筛选目的中没有进行混合物设计。这意味着通过随机选择12种混合物混合在一个混合物中来制备64种混合物。
样品制备
对于示例性SARS-CoV-2 RNA的 1H筛选,使用移液机器人进行自动移液以制备样品。每种混合物中的片段在90%d6-DMSO和10%D 2 O中的浓度为4.2mM。筛选样品的最终体积为 200 μL,含 5% D2O 作为锁定剂。在pH 6.2下移取64个样品,每个样品在25 mM KPi,50 mM KCl中含有不同的混合物,不含目标RNA。分别用靶RNA移液64个样品,每个样品含有不同的混合物。将RNA:配体比例设置为1:20,导致RNA浓度为10μM,配体浓度为200μM。
数据分析
对于 1H分析,使用了TopSpin中的FBS工具。为了确定片段是否被击中,进行了一维化学位移,waterLOGSY和T2 弛豫实验。对于T2 松弛,强度降低超过30%被视为命中,而对于化学位移,大于6 Hz的偏移是截止值。waterLOGSY必须显示显着的信号变化(在这种情况下从负到正)。如果这三个标准中的任何两个是肯定的,则片段被视为命中。 图 6 中可以看到两个示例。
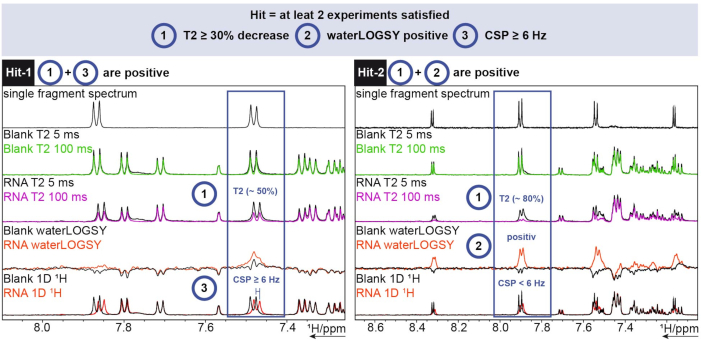
图 6:对显示命中确定标准的示例性 SARS-CoV-2 RNA 进行 1小时筛选。 采集三种不同的实验(1H T2 CPMG (5/100 ms)、waterLOGSY 和 1D 1H)。请点击此处查看此图的大图。
Hit-1显示T2 降低~50%,CSP≥6 Hz。waterLOGSY没有显示出足够显着的信号变化,也不能算作阳性。由于三分之二的实验是阳性的,因此此片段被视为命中。对于Hit-2,T2 显示出~80%的信号强度下降,并且可以看到waterLOGSY的明显信号变化。在这种情况下,CSP 是不够的,但由于前两个标准是肯定的,它仍然被视为命中。
讨论
基于 NMR 的片段/药物筛选的多功能性。BMRZ已成功实施了最先进的自动化核磁共振仪器以及STD-NMR,waterLOGSY和松弛实验,以鉴定药物发现的各种亲和力范围内的片段。安装的硬件包括一个高通量样品制备机器人和与 600 MHz 光谱仪相关的高通量样品存储、更换器和数据采集单元。最近购买的用于 1H、19F、13C 和 15N 的低温探头可确保建议测量所需的灵敏度,并允许在 19F 检测期间进行 1 H (1) 去耦。该探头连接到最新一代的核磁共振控制台,可以使用布鲁克的高级软件工具,包括CMC-q、CMC-assist、CMC-se和FBS(包含在TopSpin中)。基于片段的筛选(FBS)工具包含在最新版本的TopSpin中,有助于分析高通量数据,包括STD,waterLOGSY,T2 / T1r-弛豫实验。液体1D 1H样品收集可以通过使用样品填充机器人以自动方式填充到NMR管中。 通常,在大约两个小时内填充96个管(3毫米)的块。96孔板架直接放置在HT自动进样器中,该自动进样器读取模块的条形码并将NMR管分配给由自动化软件(IconNMR)控制的实验。五个 96 孔板架可以同时在 HT 自动进样器中存储和编程。每个机架的温度可以单独控制和调节。此外,在测量前,可以将每个单独的样品预处理(预热和管干燥以去除冷凝湿度)到所需的温度。
适用于广泛的应用。 这种基于核磁共振的自动化筛选的广泛应用之一是鉴定和开发与生物大分子靶标(DNA/RNA/蛋白质)结合的新型配体。这些配体可以包括通常非共价结合的正位和变构抑制剂。此外,通过核磁共振进行的FBDD通常用作选择有前途的化合物的第一步,要满足的要求是足够数量的生物分子靶标的可用性。这一目标分为两个主要任务。
任务一是开发和表征内部片段库,原因如下:1000多个片段的初始和定期质量控制、表征和定量;测定片段在针对每个靶标优化的缓冲液中的溶解度,特别是针对蛋白质靶标;以及建立几个文库以容纳不同的支架并扩展到其他大分子类别。任务二是通过核磁共振整合基于片段的药物设计(FBDD)的工作流程,使用:自动1D配体观察筛选(观察到1H和 19F);自动替代测定(与(天然)配体竞争实验)以区分正位和变构结合;具有多个片段的自动二次筛选;自动2D蛋白筛选,以及利用EU-OPENSCREEN文库或任何其他文库围绕初始命中对一组衍生物进行二次筛选;以及针对所选靶标对FDA图书馆进行重新剖析筛选。
此外,可以进行各种细胞系(疾病相关)的代谢分型,以揭示连接细胞周期控制和代谢的调节机制。此外,还可以在 体内 和体外对RNA/DNA/蛋白质调控元件进行功能表征,以优化构建 体 /结构域优化(结构研究的稳定性优化(缓冲液、pH、温度和盐筛选),并将基于NMR的片段筛选扩展到膜蛋白和固有无序蛋白,这通常是其他技术无法实现的。
局限性。 使用 19F 和 1H 片段库有其优点和缺点,下文将很少提及。与 1H 相比,19F 测量的最大优势是实际测量时间和后续分析的速度,因为混合物包含的片段数量几乎是其两倍,并且必须进行的实验更少。后续分析对于19F筛选也更容易,因为没有缓冲液的干扰,此外,对于最佳设计的片段混合物,提供了更宽的化学位移范围,几乎没有信号重叠。光谱本身大大简化,通常每个片段只有一个或两个信号,具体取决于氟原子的数量。因此,这些光谱的分析可以自动化,再次减少时间。这是以化学多样性为代价的,至少对于本研究中使用的图书馆而言。由于只有~13%的文库包含19 F,但自然所有这些都可用于1H筛选,因此19F筛选片段的多样性会更低。这可以通过专门设计的19F文库来规避,这些文库具有更多的片段和更大的化学多样性。19F筛选的另一个缺点是每个片段的信号数量少。片段通常由一个以上的氢原子组成。因此,1H观察到的筛选实验可以依靠同一片段的不同信号来检测结合。这在识别1H筛选的命中时提供了更高的置信度,而19F筛选必须依赖于每个片段给出的一个或两个信号。
本文详细介绍了基于核磁共振的现代自动化片段筛选仪器、软件和分析方法及其协议。安装的硬件包括一个高通量样品制备机器人和一个与 600 MHz 光谱仪相关的高通量样品存储、更换器和数据采集单元。最近安装的 1 H、19F、13C 和 15N 低温探头可确保建议测量所需的灵敏度,并允许在 19F 检测期间进行 1H 去耦。此外,最新一代的核磁共振控制台提供了使用高级分析软件辅助采集和动态分析的可能性。上面讨论的技术、工作流程和所描述的协议应该会为追求核磁共振FBS的用户带来显著的成功。
披露声明
没有。
致谢
这项工作得到了iNEXT-Discovery的支持,项目编号为871037,由欧盟委员会的地平线2020计划资助。
材料
| Name | Company | Catalog Number | Comments |
| Bruker Avance III HD | Bruker | 600 MHz NMR Spectrometer | |
| Matrix Clear Polypropylene 2D Barcoded Open-Top Storage Tubes | 3731-11 0.75ML V-BOTTOM TUBE/LATCH RACK | ThermoFisher Scientific | Barcoded Tubes |
| Matrix SepraSeal und DuraSeal& | 4463 Cap Mat, SeptraSeal 10/CS | ThermoFisher Scientific | |
| SampleJet | Bruker | HT Sample Changer | |
| SamplePro Tube | Bruker | Pipetting Robot |
参考文献
- Yanamala, N., et al. NMR-Based Screening of Membrane Protein Ligands. Chemical Biology & Drug Design. 75, 237-256 (2010).
- Souers, A. J., et al. ABT-199, a potent and selective BCL-2 inhibitor, achieves antitumor activity while sparing platelets. Nature Medicine. 19, 202-208 (2013).
- Su, M. C., Te Chang, C., Chu, C. H., Tsai, C. H., Chang, K. Y. An atypical RNA pseudoknot stimulator and an upstream attenuation signal for -1 ribosomal frameshifting of SARS coronavirus. Nucleic Acids Research. 33, 4265-4275 (2005).
- Perera, T. P. S., et al. Discovery & pharmacological characterization of JNJ-42756493 (Erdafitinib), a functionally selective small-molecule FGFR family inhibitor. Molecular Cancer Therapeutics. 16, 1010-1020 (2017).
- Zhang, C., et al. Design and pharmacology of a highly specific dual FMS and KIT kinase inhibitor. Proceedings of the National Academy of Sciences of the United States of America. 110, 5689-5694 (2013).
- Lipinski, C. A., Lombardo, F., Dominy, B. W., Feeney, P. J. Experimental and computational approaches to estimate solubility and permeability in drug discovery and development settings. Advanced Drug Delivery Reviews. 23, 3-25 (1997).
- Congreve, M., Carr, R., Murray, C., Jhoti, H. A 'Rule of Three' for fragment-based lead discovery. Drug Discovery Today. 8, 876-877 (2003).
- Chávez-Hernández, A. L., Sánchez-Cruz, N., Medina-Franco, J. L. A Fragment Library of Natural Products and its Comparative Chemoinformatic Characterization. Molecular Informatics. 39, 2000050 (2020).
- Sreeramulu, S., et al. NMR quality control of fragment libraries for screening. Journal of Biomolecular NMR. , 00327-00329 (2020).
- Gao, J., et al. Automated NMR Fragment Based Screening Identified a Novel Interface Blocker to the LARG/RhoA Complex. PLoS One. 9, 88098 (2014).
- Peng, C., et al. Fast and Efficient Fragment-Based Lead Generation by Fully Automated Processing and Analysis of Ligand-Observed NMR Binding Data. Journal of Medicinal Chemistry. 59, 3303-3310 (2016).
- Cox, O. B., et al. A poised fragment library enables rapid synthetic expansion yielding the first reported inhibitors of PHIP(2), an atypical bromodomain. Chemical Science. 7, 2322-2330 (2016).
- Hwang, T. L., Shaka, A. J. Water Suppression That Works. Excitation Sculpting Using Arbitrary Wave-Forms and Pulsed-Field Gradients. Journal of Magnetic Resonance, Series A. 112, 275-279 (1995).
- Gossert, A. D., Jahnke, W. NMR in drug discovery: A practical guide to identification and validation of ligands interacting with biological macromolecules. Progress in Nuclear Magnetic Resonance Spectroscopy. 97, 82-125 (2016).
- Sklenar, V., Bax, A. A new water suppression technique for generating pure-phase spectra with equal excitation over a wide bandwidth. Journal of Magnetic Resonance. 75, 378-383 (1987).
- Binas, O., et al. 19F NMR-Based Fragment Screening for 14 Different Biologically Active RNAs and 10 DNA and Protein Counter-Screens. ChemBioChem. , (2020).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。