Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Mensch In Vitro Suppression als Screening-Tool für die Anerkennung von Early State of Immune Imbalance
In diesem Artikel
Zusammenfassung
Tregs sind potente Suppressoren des Immunsystems. Es besteht ein Mangel an einzigartigen Oberflächenmarker um sie zu definieren, damit sind die Definitionen der Tregs in erster Linie funktional. Hier beschreiben wir eine optimierte In-vitro- Assay ermöglicht die Identifizierung immune Ungleichgewicht bei den Probanden mit Risiko für die Entwicklung von T1D.
Zusammenfassung
Regulatorische T-Zellen (Tregs) sind kritische Mediatoren der Immuntoleranz gegenüber Selbst-Antigenen. Darüber hinaus sind sie von entscheidender Bedeutung Regulatoren der Immunantwort auf eine Infektion. Trotz der Bemühungen um eine einzigartige Oberfläche Marker auf Tregs zu identifizieren, ist die einzige Besonderheit ihrer Fähigkeit, die Proliferation und Funktion der Effektor-T-Zellen unterdrücken. Es ist zwar klar, dass nur in vitro-Untersuchungen können bei der Beurteilung der menschlichen Treg-Funktion verwendet werden, wird diese Problematik bei der Beurteilung der Ergebnisse von Querschnitts-Studien, in denen gesunder Zellen und Zellen von Patienten mit Autoimmunerkrankungen (wie Typ 1 Diabetes-T1D) müssen isoliert verglichen werden. Es gibt eine große Variabilität zwischen den Labors in der Anzahl und Art der Responder-T-Zellen, Art und Stärke der Stimulation Treg: Responder-Verhältnisse und die Anzahl und Art der Antigen-präsentierenden Zellen (APC) in der menschlichen In-vitro-Suppression-Tests verwendet. Diese Variabilität macht einen Vergleich zwischen Studien zur Messung Treg-Funktion schwierig. Die Treg-Feld muss ein standardisiertes Unterdrückung Assay, die gut funktionieren wird sowohl mit gesunden Probanden und Patienten mit Autoimmunerkrankungen. Wir haben eine in vitro-Assay-Unterdrückung, die sehr wenig Intra-Assay-Variabilität in der Stimulation von T-Zellen von gesunden Freiwilligen im Vergleich zu Patienten mit zugrunde liegenden autoimmune Zerstörung der Bauchspeicheldrüse β-Zellen isoliert zeigt entwickelt. Das Hauptziel dieses Stückes ist es, ein in vitro menschliche Unterdrückung Assay, der Vergleich zwischen den verschiedenen Fächergruppen ermöglicht beschreiben. Darüber hinaus hat dieser Test das Potenzial, einen kleinen Verlust in nTreg Funktion beschreiben und rechnen mit weiteren Verlust in der Zukunft, also die Identifizierung von Personen, die präventive immunmodulatorische Therapie 1 profitieren könnten. Im Folgenden bieten wir ausführliche Beschreibung der Schritte in diesem Verfahren beteiligt. Wir hoffen, dass die Standardisierung der in vitro Suppression Assay verwendet werden, um Treg-Funktion Maßnahme beitragen. Darüber hinaus bieten wir diesen Test als ein Werkzeug zu einem frühen Zustand des Immunsystems Ungleichgewicht und eine mögliche funktionelle Biomarker für T1D zu erkennen.
Protokoll
1. Vor dem Einrichten einer Unterdrückung Assay, überprüfen muss man Mantel tosylactivated Beads mit anti-human CD3 (Klon UCHT1, Endkonzentration 1μg/ml) für Zell-Stimulation und danach, ob die Perlen effizient durch die Einrichtung eines In-vitro-Proliferation-Assay mit menschlichen beschichtet T-Zellen
- Nehmen Sie 1 ml der M-450 tosylactivated Perlen aus der Original-Durchstechflasche, in Magnetfuß und halten, bis alle Perlen auf der Seite des Rohres haften geblieben sind. Entfernen Sie den Puffer, während Röhre befindet sich noch in der magnetischen stehen. Nehmen Sie Schlauch aus magnetischen stehen und 1ml von buffer1 wird das Reagenzglas in magnetischen stehen wieder und entfernen Sie die buffer1 während Röhre ist in der magnetischen stehen; resuspendieren Perlen in 1 ml buffer1 und fügen 40 ul von anti-human CD3, agitieren bei 37 ° C für 15 Minuten, fügen Sie 0,1% w / v BSA und weiter agitieren für die nächsten 16 Stunden.
- Waschen Sie die Kugeln in buffer2 zweimal für 5 Minuten bei 2-8 ° C und einmal in buffer3 für 5 Minuten bei 2-8 ° C unter Verwendung magnetischer stehen, wie oben erläutert, entfernen Sie die Puffer-und resuspendieren die Perlen in 1 ml buffer2; die Perlen 4x10 8 / ml Endkonzentration und einsatzbereit.
- Aliquot 50.000 und 25.000 PBMC / well in dreifacher Ausfertigung in einer 96-Well-Platte und stell 'variable Anzahl von CD3-beschichteten Beads (4x10 8 Perlen / ml, CD3 1μg/ml, z. B. 1, 2, 3, 4, 5 Perlen / Zelle ), um die optimale Anzahl von Kugeln pro Zelle zu bestimmen. Nach 72 Stunden in Kultur, fügen 1μCi [3 H] Thymidin und weiterhin Inkubation bei 37 ° C für die nächsten 16 Stunden. Ernten Sie die Zellen in Multiscreen Ernte Platte (Millipore), fügen Szintillationsflüssigkeit und lesen Sie zählt pro Minute (cpm) / well mit Top Count NXT (Packard, CT). Verwenden Sie die Perlen / Zell-Verhältnis, wenn cpms ab 5000, aber weniger als 15000 zu Überreizung der Tregs, die suppressive Funktion verlieren könnte, vermieden. Normalerweise stimuliert Verhältnis von 3 Perlen / Zelle sowohl Responder und Treg-Zellen in allen Fächergruppen bisher getesteten 1-4.
2. PBMC Isolierung aus Vollblut von gesunden Spendern oder aus menschlichem leukopacks oder Buffy-Coat (BC) in der Regel von gesunden Freiwilligen und kostenlos von örtlichen Blutspendedienst Centers übernommen (Abbildung 1)
- Verdünnen Sie die BC (~ 50ml) 1:6 mit PBS (add 250ml). Jetzt gibt es 300ml Gesamtvolumen. Langsam Schicht 25ml verdünnt BC oben auf 15ml Ficoll-Paque PLUS hinzugefügt 50ml Falcon-Röhrchen, ohne die Schichten. Zentrifuge bei 800xg (1400 in einer Sorvall-Zentrifuge mit Ausschwingrotor SH-3000) für 30 Minuten bei 4 ° C, mit Bremse ausgeschaltet.
- Sorgfältig sammeln PBMC-Schicht (mittlere Phase) und überträgt es auf ein frisches 50ml Falcon-Röhrchen. Wash PBMC, indem die Rohre bis zu 50ml mit DPBS. Sammeln Sie 2-Zell-Pellets in einem Rohr. Zentrifuge bei 400xg für 10 min bei 4 ° C. Waschschritt zweimal wiederholen, jedes Mal, wenn die Kombination von 2-Zell-Pellets in einem einzigen Rohr. Kombinieren Sie alle Zellpellets in einem einzigen 50ml Tube.
- Graf PBMC mit Trypanblau-Test. Machen Sie eine 1:10-Verdünnung in Trypanblau, indem 20 &mgr; l von PBMC zu 180μl der Trypanblau-Färbung. Gut mischen und 20 &mgr; l nehmen, um in Hämazytometer sofort verlassen. Count-Nummern aller ungefärbt und nur blau gefärbten Zellen in zwei quadratische Blöcke mit jeweils 16 kleineren Plätzen. Der Mittelwert der beiden Zahlen und mit 10 multiplizieren. Teilen Sie diese Zahl durch 100, die Zahl der PBMC / ml erhalten. Prozentsatz der lebenden Zellen, wie berechnen [1 - (Anzahl der blauen Zellen / Gesamtzahl der Zellen) x100]. Gehen Sie, wenn die Lebensfähigkeit von ≥ 95%.
3. MACS Vorsortierung der CD4 T-Zellen
- Bevor Sie fortfahren, Transfer 1ml PBMC in ein neues Röhrchen, fügen 4ml von Medien, um Zellen für die Bestrahlung mit 5000rad-diese vorbereiten Antigen-präsentierende Zellen (APC) werden.
- Centrifuge der Rest der Zellen bei 250xg in PBS/2mM EDTA/0.5% BSA-Puffer für 10min bei 4 ° C. Überstand abgießen und die Zellen in 4 ml PBS/2mM EDTA/0.5% BSA-Puffer.
- Add 200 ul von MACS anti-CD4-Microbeads und inkubieren Sie bei 4 ° C für 20 Minuten.
- Wash, indem 40ml PBS/2mM EDTA/0.5% BSA-Puffer und Zentrifuge bei 250xg für 10min bei 4 ° C. Abgießen Überstand und resuspendieren in 8ml entgastem, Raumtemperatur PBS/2mM EDTA/0.5% BSA-Puffer.
- Filter-Trennung der Zellsuspension mit Vorabscheidung Filter vor dem Laden auf einem LS-Spalte.
- Split der Zellsuspension und Schicht 4ml jeweils über kalibriert LS Spalte (mit 3 ml deggassed PBS/2mM EDTA/0.5% BSA-Puffer). LS-Spalte in der MidiMACS Trennzeichen festgelegt. Vor Zellsuspension ausgeht, entweder re-run Durchfluss oder fügen Sie 3ml deggassed Raumtemperatur PBS/2mM EDTA/0.5% BSA-Puffer und lassen Sie den Puffer durchlaufen. Fügen Sie mehr Puffer, bis es klar kommt.
- Pipette 5ml deggassed Puffer auf die LS Spalte entfernen LS Column aus dem MidiMACS Abscheider und in einen neuen sterilen 15ml Sammelröhrchen lassen ~ 1.0ml durchlaufen. Setzen Sie den Kolben in die Spalte und langsam schieben Sie den Rest desVolumen aus.
- Machen Sie dasselbe mit den beiden LS Säulen und verbinden die beiden CD4 +-Fraktionen. Fügen Sie bis zu 50 ml PBS und zählen Zellen. Erwartete Rendite von bis zu 5x10 8 Zellen. Zentrifuge bei 400xg für 10 Minuten und die Zellen auch in 2ml PBS/2mM EDTA/0.5% BSA-Puffer.
4. Fluorescent Activated Cell Sorting (FACS) isoliert (Abbildung 2)
- Machen Sie einen Cocktail an Antikörpern gegen CD-Marker auf die folgenden Zelloberflächenmarker (halten geschützt vor Licht): 20 ul Anti-Human-CD8-FITC (Klon RPA-T8), 20 ul Anti-Human-CD14-FITC (Klon M5E2; LPS-Rezeptor), 20 ul Anti-Human-CD32-FITC (Klon FLI8.26; FcyR-Typ II) und 6 ul Anti-Human-CD116-FITC (Klon M5D12; GM-CSFRα Kette) und alternativ, fügen Sie 40 ul anti -human CD4-APCCy7 (Klon RPA-T4).
- Nehmen Sie 5μl aus der 2ml Zellsuspension und Fleck mit 2μl der Fleck-Cocktail, das ist ein Rohr für die Bestimmung der Schwelle (Fluorochrom Minus One-FMO) 5.
- Add 50 ul Anti-Human-CD25-PE (Klon M-A251, IL-2Rα), um den Fleck Cocktail, und fügen Sie den Cocktail Zellsuspension und inkubieren Sie bei 4 ° C 30 Minuten. Wash-Zellen in PBS-Puffer, Zentrifuge bei 400xg für 10 Minuten und die Zellen auf eine Zellkonzentration von 10 7 / ml.
- Bereiten ungefärbten Zellen und Zellen oder Kügelchen, die mit einzelnen Fluorochrom gefärbt, um als Ausgleich für die Kontrolle Zellsortierung am FACS Aria (BD Biosciences, San Jose, NJ) zu verwenden.
- Erwerben Sie Zellen in der FMO Röhre, die dem Benutzer erlauben, die Schwelle für die Sortierung von CD25 + T-Zellen (Abbildung 2a) gesetzt wird. Setzen Sie einen Schutzzaun um FITC-negative Zellen FITC-positiven Zellen aus Monozyten, Makrophagen und alle anderen CD4 +-non-T-Zellen (Abb. 2b) auszuschließen.
- In einem separaten Grundstück, ziehen Tore für CD25-, CD25low und CD25high T-Zellen-Tregs (Top 1% der Zellen, die die höchste Zahl an CD25) (Abbildung 2c). Zell-Untergruppen zeigen typischerweise hohe Reinheit (Abbildung 2d, 2e und 2f).
- Centrifuge Sammelröhrchen mit Zellen in 400xg für 10 Minuten und halten sie auf Eis, bis Plattierung.
5. Set up Zellkultur in 96-Well-Platte (Schema wie Tabelle 1 im Anhang) in 200μl/well
- Aliquot 50 ul CD3-beschichteten Beads (1 pg / ml) berechnet bis 3 Perlen / Responder-Zelle in einen Brunnen, in komplettem Medium mit 10% gepooltem humanem AB-Serum resuspendiert in U-Boden 96-well Platten werden. (Zum Beispiel, um 2ml Medien mit CD3-beschichteten machen, 7.5μl nehmen ab Lager der CD3-beschichteten Beads-Endkonzentration 4x10 8 / ml und verdünnen in 2ml Medien, jeder 50 ul werden 75.000 beads-3beads/cell enthalten).
- Verdünnen Sie bestrahlten APC auf 5x10 5 / ml Zellkonzentration und fügen 50 ul (wird 2,5 x 10 4 Zellen enthalten) in jedes Well mit zuvor hinzugefügt Stimulation, einschließlich Brunnen als "Tregs nur" bezeichnet, "APC nur" und "Medien nur" in der Tabelle 1.
- Add 2,5 x 10 4 / well CD4CD25-oder CD4CD25low T-Zellen in dreifacher Ausfertigung folgende Design in Tabelle 1.
- Add Tregs zu Co-Kulturen (Reihe B, Tabelle 1) im Verhältnis 1:10 (2.500 Treg-Zellen) und in die Vertiefungen als "Tregs nur" beschriftet und inkubieren Sie die Platte bei 37 ° C in CO 2-Inkubator mit 5% CO 2 , in gesättigten Luftfeuchtigkeit für 72 Stunden.
- Pulse Brunnen mit 1μCi [3 H] Thymidin und weiterhin Inkubation bei 37 ° C für die nächsten 16 Stunden.
6. Ernten und Zählen
- Ernten Sie die Zellen auf Multiscreen Ernte Platte mit Packard Filtermate Mähdrescher oder alternatives System.
- Add Szintillationsflüssigkeit (Microscint 20), decken Ernte Platte mit transparenten Kunststoff-Abdeckung in der Vorbereitung für den letzten Schritt.
- Lesen Sie zählt pro Minute (cpm) / well mit Top Count NXT (Packard, CT) oder alternatives System.
7. Computing Prozentsatz der Unterdrückung
- Wie Zellen in dreifacher Ausführung kultiviert wurden, ist durchschnittlich für jede Bedingung berechnet. Wenn der Variationskoeffizient> 30% ist die Ausreißer eliminiert und nur cpm aus zwei Brunnen gemittelt werden. Prozentsatz der Unterdrückung durch die Berechnung erhalten [(sc) / s] x 100%, wobei s = cpm in einzelnen Kultur und c = cpm in Co-Kultur.
- Wie naiv (CD25-) und in vivo aktiviert (CD25low) Effektor-T-Zellen werden als Responder T-Zellen ausplattiert, ist der Unterschied in der Fähigkeit der Tregs auf jede dieser Teilmengen zu unterdrücken gefangen genommen und als potentielle funktionelle prognostischer Indikator auf der Prämisse, verwendet dass aktivierte Zellen sind schwerer zu unterdrücken.
8. Repräsentative Ergebnisse:
Große Variabilität in der verwendeten Methoden und Ergebnisse aus in vitro menschliche Unterdrückung Assay abgeleitet hat uns veranlasst, eine umfassende Studie über Bedingungen beeinflussen den Test 1 durchzuführen. Wir haben einen Test, der nicht nur Treg Funktionstests, sondern auch ihre Reinheit entwickelt, unter Berücksichtigung der niedrigen Verhältnis zwischen Tregs: Teffs (1:10), die wir bestimmt früher 6. Darüber hinaus Tregs in th unterscheideneir Fähigkeit, erfolgreich zu unterdrücken naiv und in vivo-aktivierten T-Zellen auch bei gesunden Probanden, wie in Abbildung 3 und in unseren früheren Studien 2,4, die mehr hervortritt angezeigt, wenn Immunbalance gefährdet ist, als bei Personen mit Risiko für die Entwicklung von T1D . Der Test funktionierte sehr gut in der Studie, wo wir im Vergleich suppressive Funktion der natürlichen (nTregs), induzierbare (iTregs) und in vitro erweitert nTregs, so dass wir ihre Funktion zwischen gesunden Kontrollgruppe zu vergleichen, kürzlich aufgetretenen (RO) T1D und langjährige (LS ) T1D Themen. Wir schlossen daraus, dass RO T1D Themen besser Kapazitäten zur Erzeugung funktionaler sowohl iTregs und erweitert nTregs im Vergleich zum LS T1D und gesunden Kontrollpersonen 7 hatte. Somit kann dieser Test als besonders geeignetes Mittel in der Anerkennung der sowohl eine frühe und späte Zustand des Immunsystems Ungleichgewicht verwendet werden.
Schema 1: Schematische Darstellung der Schritte in in vitro-Assay Unterdrückung beteiligt

Abbildung 1. Schritte der In-vitro-Assay-Unterdrückung mit Fotos vorgestellt
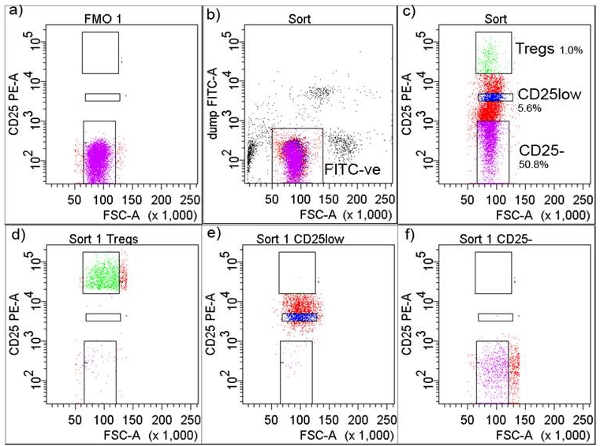
Abbildung 2. Gating-Strategie in FACS Zellisolation. a) CD25 + Schwelle wurde nach Fluorochrom Minus One (FMO), b bereinigt)-Zellen wurden gated als FITC-negative, c) FITC-negative Zellen wurden weiter gated gesammelt und als CD + CD25-, CD + CD25low und CD + CD25high ( Tregs) mit Prozentsätzen, d gezeigt) FACS sortiert Tregs nach dem Sortieren) e FACS sortiert CD + CD25low nach dem Sortieren und f) FACS sortiert CD4 + CD25-T-Zellen nach der Sortierung
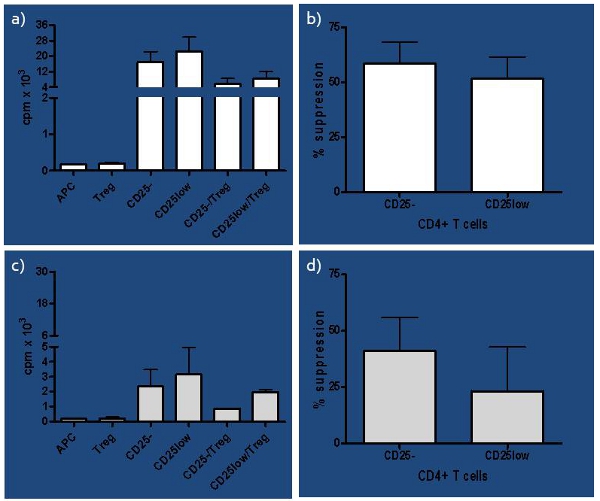
Abbildung 3. Repräsentative Ergebnisse von gesunden Probanden a) Repräsentative Ergebnisse der Zählungen pro Minute (cpm) von gesunden Probanden als Einzel-Kulturen für alle Zell-Untergruppen befassten (naiv-CD25-, in vivo aktiviert-CD25low, Antigen-präsentierende Zellen-APC und regulatorischen T-Zellen-Treg) sowie Co-Kulturen von Responder T-Zellen (CD25-oder CD25low) und Tregs. b) Prozentsatz der Unterdrückung jedes CD25-und CD25low Responder T-Zellen durch autologe Tregs ist für gesunde Kontrollpersonen dargestellt (n = 4). Suppression wurde als [(sc) / s] berechnet x 100%, wobei s = cpm in einzelnen Kultur und c = cpm in Co-Kultur. Obwohl geringe Unterschied in Leistung von Tregs zu Responder T-Zellen unterdrücken bemerkt wurde, war es nicht signifikant (gepaarter t-Test p = 0,08). C) Präsentiert werden cpm gefährdet Themen für jede einzelne Kultur, einschließlich CD25-und CD25low als Responder T-Zellen sowie APC und Tregs und Co-Kulturen, in denen jeweils Responder T-Zell-Untergruppe mit Tregs (CD25-/Tregs und CD25low/Tregs). d) Prozentsatz der Unterdrückung jedes CD25-und CD25low Responder T-Zellen durch autologe ist ausgesät Tregs ist in Gefahr Probanden (n = 4) vorgestellt. Der Unterschied in der Kapazität der Tregs auf CD25-versus CD25low Responder T-Zellen zu unterdrücken war signifikant (gepaarter t-Test p = 0,04).
Tabelle 1. Schematische Aufbau von in vitro-Assay-Unterdrückung
| 1-3 | 4-6 | 7-9 | 10-12 | |
| A | CD4CD25- | CD4CD25low | Medien nur | Medien nur |
| B | CD4CD25-/ Tregs | CD4CD25low / Tregs | Tregs nur | APC nur |
| C | ||||
| D | ||||
| E | ||||
| F | ||||
| G | ||||
| H |
Diskussion
Als einzige Besonderheit an Tregs, sollte suppressive Funktion zuverlässig und gleichmäßig zwischen den Fächern geprüft werden in verschiedenen Phasen der Entwicklung der Krankheit innerhalb der gleichen und zwischen unterschiedlichen Studien. Wir bieten Ihnen Details der Unterdrückung Test in unserem Labor als unseren Beitrag zur Standardisierung von diesem Assay entwickelt. In unserem umfangreichen Studie zur Optimierung, haben wir festgestellt, dass T-Zell-Stimulation mit anti-human CD3-beschichteten Beads (UCH...
Offenlegungen
Danksagungen
Diese Studie wurde vom Max McGee National Research Center for Juvenile Diabetesat Medical College of Wisconsin und Kinder Research Institute of Wisconsin unterstützt. Die Geldgeber hatten keine Rolle in Studiendesign, Datenerhebung und-analyse oder Erstellung des Manuskripts.
Materialien
| Name | Company | Catalog Number | Comments |
| Name des Reagenzes oder Instrument | Firma | Katalog-Nummer | Kommentare (optional) |
|---|---|---|---|
| Ficoll-Paque PLUS | Amersham Pharmacia Biotech | 17-1440-03 | |
| DPBS-1X | Gibco | 14190-144 | |
| Trypanblau | Invitrogen | 15250-061 | |
| Anti-CD4-Microbeads | Miltenyi | 130-045-101 | |
| Pre-Trennfilter | Miltenyi | 130-041-407 | |
| LS Spalte | Miltenyi | 130-042-401 | |
| EDTA | Invitrogen | 15575-020 | |
| BSA | Sigma-Aldrich | B4287 | |
| Anti-human CD4-APCCy7 (Klon RPA-T4) | BD Pharmingen | 557852 | |
| Anti-human CD25-PE (Klon M-A251, IL-2Rα) | BD Pharmingen | 555432 | |
| Anti-human CD8-FITC (Klon RPA-T8) | BD Pharmingen | 555366 | |
| Anti-human CD14-FITC (Klon M5E2; LPS-Rezeptor) | BD Pharmingen | 555397 | |
| Anti-human CD32-FITC (Klon FLI8.26; FcyR-Typ II) | BD Pharmingen | 555448 | |
| Anti-human CD116-FITC (Klon M5D12; GM-CSFRα Kette) | BD Pharmingen | 554532 | |
| Dynalbeads M-450 tosylactivated | Invitrogen | 140-13 | |
| Anti-human CD3 | Ancell | 144-024 | |
| Buffer1 | Homemade | 0,1 M Na 2 B 4 O 7 pH 7,6 | |
| Buffer2 | Homemade | PBS/2mM EDTA / 0,1% BSA pH-Wert 7,4 | |
| Buffer3 | Homemade | 0,2% BSA pH 8,5 Tris/0.1 | |
| Vollständige RPMI Medien | Homemade | RPMI 1640 Medium 2 mM L-Glutamin 5 mM HEPES 100 U / ug / ml peni / Strept 0,5 mM Natriumpyruvat | |
| [3 H] Thymidin | Perkin Elmer | NET027Z005MC | |
| Menschen gebündelt AB-Serum | Atlanta Biologicals | S40110 | |
| Multiscreen Ernte Platte | Millipore | MAHFC1H60 | |
| Microscint 20 | Perkin Elmer | 6013621 |
Referenzen
- Barge, A., Cravotto, G., Gianolio, E., Fedeli, F. How to determine free Gd and free ligand in solution of Gd chelates. A technical note. Contrast Med. Mol. Imaging. 1, 184-188 (2006).
- Nagaraja, T. N., Croxen, R. L., Panda, S., Knight, R. A., Keenan, K. A., Brown, S. L., Fenstermacher, J. D., Ewing, J. R. Application of arsenazo III in the preparation and characterization of an albumin-linked, gadolinium-based macromolecular magnetic resonance contrast agent. J. Neurosci. Methods. 157, 238-245 (2006).
- Supkowski, R. M., Horrocks, W. D. On the determination of the number of water molecules, q, coordinated to europium(III) ions in solution from luminescence decay lifetimes. Inorg. Chim. Acta. 340, 44-48 (2002).
- Menjoge, A. R., Kannan, R. M., Tomalia, D. A. Dendrimer-based drug and imaging conjugates: design considerations for nanomedical applications. Drug Discovery Today. 15, 171-185 (2010).
- Que, E. L., Chang, C. J. Responsive magnetic resonance imaging contrast agents as chemical sensors for metals in biology and medicine. Chem. Soc. Rev. 39, 51-60 (2010).
- Uppal, R., Caravan, P. Targeted probes for cardiovascular MR imaging. Future Med. Chem. 2, 451-470 (2010).
- Major, J. L., Meade, T. J. B. i. o. r. e. s. p. o. n. s. i. v. e. Bioresponsive, cell-penetrating, and multimeric MR contrast agents. Acc. Chem. Res. 42, 893-903 (2009).
- Datta, A., Raymond, K. N. Gd-hydroxypyridinone (HOPO)-based high-relaxivity magnetic resonance imaging (MRI) contrast agents. Acc. Chem. Res. 42, 938-947 (2009).
- Leôn-Rodríguez, L. M. D., Lubag, A. J. M., Malloy, C. R., Martinez, G. V., Gillies, R. J., Sherry, A. D. Responsive MRI agents for sensing metabolism in vivo. Acc. Chem. Res. 42, 948-957 (2009).
- Castelli, D. D., Gianolio, E., Crich, S. G., Terreno, E., Aime, S. Metal containing nanosized systems for MR-molecular imaging applications. Coord. Chem. Rev. 252, 2424-2443 (2008).
- Caravan, P., Ellison, J. J., McMurry, T. J., Lauffer, R. B. Gadolinium(III) chelates as MRI contrast agents: structure, dynamics, and applications. Chem. Rev. 99, 2293-2352 (1999).
- Lauffer, R. B. Paramagnetic metal complexes as water proton relaxation agents for NMR imaging: theory and design. Chem. Rev. 87, 901-927 (1987).
- Yoo, B., Pagel, . An overview of responsive MRI contrast agents for molecular imaging. Front. Biosci. 13, 1733-1752 (2008).
- Pandya, S., Yu, J., Parker, D. Engineering emissive europium and terbium complexes for molecular imaging and sensing. Dalton Trans. 23, 2757-2766 (2006).
- Nwe, K., Xu, H., Regino, C. A. S., Bernardo, M., Ileva, L., Riffle, L., Wong, K. J., Brechbiel, M. W. A new approach in the preparation of dendrimer-based bifunctional diethylenetriaminepentaacetic acid MR contrast agent derivatives. Bioconjugate Chem. 20, 1412-1418 (2009).
- Nwe, K., Bernardo, M., Regino, C. A. S., Williams, M., Brechbiel, M. W. Comparison of MRI properties between derivatized DTPA and DOTA gadolinium-dendrimer conjugates. Bioorg. Med. Chem. 18, 5925-5931 (2010).
- Caravan, P., Das, B., Deng, Q., Dumas, S., Jacques, V., Koerner, S. K., Kolodziej, A., Looby, R. J., Sun, W. -. C., Zhang, Z. A lysine walk to high relaxivity collagen-targeted MRI contrast agents. Chem. Commun. , 430-432 (2009).
- Leôn-Rodríguez, L. M. D., Kovacs, Z. The synthesis and chelation chemistry of DOTA-peptide conjugates. Bioconjugate Chem. 19, 391-402 (2008).
- Boswell, C. A., Eck, P. K., Regino, C. A. S., Bernardo, M., Wong, K. J., Milenic, D. E., Choyke, P. L., Brechbiel, M. W. Synthesis, characterization, and biological evaluation of integrin αVβ3-targeted PAMAM dendrimers. Mol. Pharm. 5, 527-539 (2008).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten