Method Article
Computerbasiertes Multitaper-Spektrogrammprogramm für elektroenzephalographische Daten
In diesem Artikel
Zusammenfassung
Dieses Protokoll stellt ein Open-Source-, kompiliertes MATLAB-Programm bereit, das Multitaper-Spektrogramme für elektroenzephalografische Daten generiert.
Zusammenfassung
Aktuelle Webressourcen bieten begrenzte, benutzerfreundliche Tools zur Berechnung von Spektrogrammen zur Visualisierung und Quantifizierung elektroenzephalografischer (EEG) Daten. In diesem Artikel wird ein Windows-basierter Open-Source-Code zum Erstellen von EEG-Multitaper-Spektrogrammen beschrieben. Das kompilierte Programm ist für Windows-Benutzer ohne Softwarelizenzierung zugänglich. Für Macintosh-Benutzer ist das Programm auf Benutzer mit einer MATLAB-Softwarelizenz beschränkt. Das Programm wird über EEG-Spektrogramme illustriert, die als Funktion von Schlaf- und Wachheitzuständen und Opiat-induzierten Veränderungen in diesen Zuständen variieren. Die EEGs von C57BL/6J-Mäusen wurden nach intraperitonealer Injektion von Saline (Fahrzeugkontrolle) und antinocizeptiven Dosen von Morphin, Buprenorphin und Fentanyl drahtlos für 4 h aufgezeichnet. Spektrogramme zeigten, dass Buprenorphin und Morphin ähnliche Veränderungen der EEG-Leistung bei 1-3 Hz und 8-9 Hz verursachten. Spektrogramme nach Verabreichung von Fentanyl ergaben maximale durchschnittliche Leistungsbänder bei 3 Hz und 7 Hz. Die Spektrogramme entlarvten Differentialopiateffekte auf EEG-Frequenz und -Leistung. Diese computergestützten Methoden sind über Allektikklassen hinweg verallgemeinerbar und können leicht modifiziert werden, um eine breite Palette rhythmischer biologischer Signale zu quantifizieren und anzuzeigen.
Einleitung
EEG-Daten können im Frequenzbereich produktiv analysiert werden, um Verhaltens- und neurophysiologische Erregungsniveaus zu charakterisieren1. Multitaper-Spektrogramme wandeln die EEG-Wellenform in Zeit- und Frequenzbereiche um, was zur Visualisierung der dynamischen Signalleistung bei unterschiedlichen Frequenzen im Zeitbereich führt. Das Multitaper-Spektrogramm verwendet Fourier-Analysen, um Spektraldichteschätzungen zu erstellen. Die Spektraldichteschätzung trennt eine Wellenform in die reinen sinusförmigen Wellen, die das Signal bilden, und ist analog zur Beugung des weißen Lichts durch ein Prisma, um das gesamte Spektrum der Farben2zu sehen. Das Multitaper-Spektrogramm des EEG stellt die kombinierte Aktivität mehrerer Netzwerke von Neuronen mit Entladungsmustern dar, die bei unterschiedlichen Frequenzen oszillieren2. Aufgrund seiner Zeitverschiebungsinvariante gilt die Fourier-Transformation als die beste Transformation zwischen Zeit- und Frequenzdomänen3. Die Fourier-Analyse hat auch eine Reihe von Einschränkungen. EEG-Signale sind nicht stationär. Daher können kleine Änderungen nach Fourier-Methoden nicht wahrgenommen werden, und die Analyse kann sich je nach Größe des Datensatzes ändern. Beim Anwenden einer Fourier-Transformation auf ein nicht stationäres Signal wird jedoch das Fensterverwendet. Dies setzt voraus, dass sich das Spektrum des Signals über kurze Zeiträume nur geringfügig ändert. Eine alternative Methode für die Spektralanalyse ist die Wavelet-Transformation, die für den Nachweis von Hirnerkrankungen besser geeignet sein kann3.
Aus funktioneller Sicht sind die verschiedenen Schwingungen, die ein EEG-Signal umfassen, niedrigere, Merkmalsphänotypen, die für höherstufige, zustandsphänotypen wie Schlaf und Wachheit2oder den Verlust der Wachheit, der durch die Allgemeine Anästhetika verursachtwird, 4,5,6. In Bezug auf Schlaf- und Wachheitszustände zeigt das Spektrogramm deutlich, dass endogen erzeugte Schlafrhythmen kontinuierlich und dynamisch sind7. Quantitative Beschreibungen von Schlaf- und Wachheitszuständen haben traditionell einen Binning-Prozess mit sich gebracht, der jeder speziell definierten Epoche (z. B. 10 s) der EEG-Aufzeichnung eine Schlaf- oder Wachklassifizierung zuweist. Diese Statusabschnitte werden dann als Funktion der Zeit dargestellt. Zeitverlaufsdatendiagramme, oft als Hypnogramme bezeichnet, werden verwendet, um normalen Schlaf von Schlaf zu unterscheiden, der durch Krankheit, Medikamentenverabreichung, Veränderungen in zirkadianen Rhythmen, Schichtarbeit usw. gestört wird. Eine Einschränkung von Hypnogramm-Plots ist, dass sie EEG-Signale falsch darstellen, indem sie Erregungszustände als quadratische Wellenformen ausdrücken. Hypnogramm-Plotten beinhaltet eine Diskretisierung von Erregungszuständen2 und erlaubt keine feinkörnige Darstellung von Zwischen- oder Übergangsstufen. Darüber hinaus erzeugen 10 s Scoring-Epochen eine diskrete Zeit, indem sie eine untere Grenze auf der Zeitskala setzen. Das Ergebnis der Diskretisierung von Zustand und Zeit ist der Verlust neurophysiologischer Informationen über das dynamische Zusammenspiel zwischen Bewusstseinszuständen2 und drogeninduzierter Störung dieser Zustände4. Zum Beispiel wirken verschiedene Anästhesiemittel auf verschiedene molekulare Ziele und neuronale Netzwerke. Pharmakologische Manipulation dieser neuronalen Netzwerke produziert zuverlässig Spektrogramme, die für das Medikament, die Dosis und den Verabreichungsweg einzigartig sind4.
Das vorliegende Protokoll wurde entwickelt, um die Forschung über die Mechanismen zu erleichtern, durch die Opioide den Schlafverändern 8, Atmung9, Nociception10, und Gehirn Neurochemie11. Dieses Protokoll beschreibt die Schritte, die erforderlich sind, um ein multitapered Spektrogramm für EEG-Analysen zu erstellen, das mit proprietärer Software oder einem System ohne MATLAB-Lizenzierung abgeschlossen werden kann. C57BL/6J (B6) Mäuse wurden verwendet, um die Fähigkeit dieser computerbasierten Methode zu validieren, neue EEG-Spektrogramme während normaler, ungestörter Schlaf- und Wachheitzustände und nach systemischer Verabreichung von Opiaten zu erstellen. Die Zuverlässigkeit und Gültigkeit der Analysen wurde durch systematische Vergleiche der Unterschiede zwischen EEG-Spektrogrammen bestätigt, nachdem B6-Mäuse intraperitoneale Injektionen von Kochchen (Fahrzeugkontrolle) und antinocizeptiven Dosen von Morphin, Buprenorphin und Fentanyl erhielten.
Quantitative Studien zur EEG-Dynamik der Neonatalen Maus haben eine translationale Relevanz, indem sie ein Modell für Studien liefern, die auf ein besseres Verständnis des neonatalen menschlichen EEG12abzielen. Die Quantifizierung der EEG-Dynamik ist nicht nur beschreibend und kann zu machine learning-Ansätzen beitragen, die erregungsgemäß zum Teil auf EEG-Daten vorhersagen können13. Ziel des vorliegenden Berichts ist es, die Translationswissenschaft zu fördern, indem ein allgemein zugänglicher, benutzerfreundlicher Code für die Berechnung von Multitaper-Spektrogrammen zur Verfügung gestellt wird, die drogeninduzierte Veränderungen im Maus-EEG charakterisieren.
Protokoll
Alle Verfahren, an denen Mäuse beteiligt waren, wurden dem Guide for the Care and Use of Laboratory Animals(8. Ausgabe, National Academies Press, Washington DC, 2011) nachgehalten und vom Institutional Animal Care and Use Committee der University of Tennessee überprüft und genehmigt.
1. Implantation von Recording Electrodes und Initial Data Collection
- Kaufen Sie Mäuse und halten Sie sie in einem feuchtigkeits- und temperaturgeregelten Raum mit ad libitum Zugang zu Nahrung und Wasser. Erlauben Sie Mäusen, sich eine Woche lang an ihre neue Umgebung anzupassen, bevor sie eine chirurgische Implantation von Aufnahmeelektroden durchgeführt haben. Das Implantationsverfahren wurde ausführlich beschrieben1,14.
- Sterilisieren Sie alle chirurgischen Geräte.
- Anästhesisieren Sie Mäuse mit Isofluran zu 2,5 % bis 3 % in 100 % Sauerstoff.
- Nach dem Verlust des Rechtenreflexes entfernen Sie die Maus aus der Anästhesie-Induktionskammer und übertragen Sie sie in einen stereotaxic-Rahmen.
- Tragen Sie eine ophthalmologische Salbe auf beide Augen auf.
- Reduzieren Sie das Isofluran auf 1,7 %, kontinuierlich über eine Maske geliefert.
- Machen Sie einen Mittellinien-Kopfhautschnitt, um den Schädel freizulegen.
- Bohren Sie zwei Craniotomien über dem linken und rechten Kortex (jeweils an stereotaxic Koordinaten anterior = 1,0 und seitlich = 3,0 relativ zum Bregma15).
- Setzen Sie die EEG-Elektroden in jede Kraniotomie ein und sichern Sie sie mit Zahnacryl.
- Implantieren Sie bipolare Elektroden im dorsalen Trapezmuskel zur Aufnahme des Elektromyogramms (EMG).
HINWEIS: Die vier Elektroden werden zu einem drahtlosen Telemeter geführt, das subkutan über dem unteren rechten Körperquadranten implantiert wird. Diese chirurgischen Techniken können hier (https://www.datasci.com/services/dsi-surgical-services/surgical-videos) eingesehen werden. - Nach der Operation, verabreichen Analgetikakarprofen und legen Sie die Maus in einen warmen Erholungskäfig. Beobachten Sie die Maus, bis sie ambulant ist. Haus implantierte Mäuse einzeln.
- Nach vollständiger Genesung von der Operation täglich mit Mäusen umgehen und die Qualität der EEG- und EMG-Aufnahmen bewerten.
- Konfigurieren Sie das Datenerfassungssystem so, dass alle Signale mit 1.000 mV aufzeichnen.
- Besorgen Sie sich EEG- und EMG-Aufnahmen für die benötigte Dauer.
- Bewerten Sie jeweils 10 s Behälter der digitalen EEG- und EMG-Aufnahmen als Wachheit, schneller Augenbewegungsschlaf (REM) oder Nicht-REM-Schlaf (NREM) mit Schlaf-Scoring-Software.
HINWEIS: Unter den Mausstämmen gibt es genotyp- und staatsspezifische Unterschiede in der EEG-Leistung, ausgedrückt als Prozentsatz der Gesamtleistung16. Bei B6-Mäusen sind Wachzustände durch ein 75-100 mV, gemischtes Frequenz-EEG und durch EMG-Signale gekennzeichnet, die einen prominenten Muskeltonus mit einer starken Amplitude-Erhöhung während der Bewegung aufweisen. Zu den Kriterien für die Bewertung des NREM-Schlafs gehört eine Verringerung der EMG-Amplitude im Verhältnis zur EMG-Amplitude der Wachheit. Das NREM-Schlaf-EEG hat eine langsamere Frequenz und erhöhte Amplitude (100 bis 150 mV) im Vergleich zur Wachheit. REM-Schlaf ist gekennzeichnet durch Muskelatonia und ein EEG-Signal, das dem EEG der Wachheit ähnelt. - Weisen Sie zwei Personen an, unabhängig voneinander den gleichen Datensatz zu erzielen. Mindestens eine Person sollte für den Behandlungszustand geblendet werden. Die Übereinstimmungswerte zwischen den beiden Schlaf-Scorern sollten größer als 90 % sein.
2. Einrichtungen und Ausrüstung
- Verstärken und digitalisieren Sie ungefilterte EEG- und EMG-Signale mit Datenerfassungsinstrumentierung und Software.
HINWEIS: Die im Mitra-Labor am Cold Spring Harbor Laboratory entwickelte Chronux Spectral Analysis Toolbox wird verwendet, um EEG-Signale als Leistung in Bezug auf Zeit- und Frequenzbereiche auszudrücken.
3. Spektrogramm-Berechnung
- Wenn ein Windows-Benutzer, verwenden Sie das kompilierte Programm.
- Wenn ein Macintosh-Benutzer die Unformatdatei ausführt.
- Abrufen von unformatierten, unverarbeiteten EEG-Daten im EDF- oder CSV-Dateiformat und Platzieren Sie sie am gleichen Speicherort wie die kompilierte Programmdatei.
- Benennen Sie die Datendateien mit den folgenden Einschränkungen: Namen dürfen nur aus Buchstaben, Zahlen, Unterstrichen oder Bindestrichen bestehen.
- Benennen Sie die Datendateien mit den folgenden Einschränkungen: Dateinamen dürfen keine Punkte, Kommas, Leerzeichen oder andere Symbole enthalten.
- Laden Sie das kompilierte Multitaper Spectrogram Program (https://drive.google.com/) herunter.
- Starten Sie das Spektrogrammprogramm und folgen Sie den Popup-Eingabeaufforderungen. Wählen Sie Dateityp: *. CSV oder *. Eef.
HINWEIS: Weitere Programminstallationsdetails finden Sie in der Datei readme.txt. - Geben Sie den gesamten EEG-Dateinamen ein (z. B. 419eeg.edf oder 419.eeg.csv).
- Wählen Sie Parameter für die Spektrogrammberechnung aus: Standard oder Neu. Dieser Schritt erfordert die längste Verarbeitungszeit, da das Spektrogramm berechnet wird. Die mathematische Fensterfunktion (Taper) liefert statistisch unabhängige Schätzungen des zugrunde liegenden Spektrums. Je länger die Aufnahmedauer, desto länger dauert dieser Schritt. Auf einer PC-Plattform mit Windows 10 benötigte dies maximal ca. 3 x 4 min für eine 4-Stunden-Aufnahme.
- Verwenden Sie die folgenden Standardspektrogrammparameter:
Abtastfrequenz = 500 Hz. Dies stellt die Anzahl der Stichproben pro Sekunde dar.
fpass = 0,3 Hz und 30 Hz. Fpass definiert die Frequenzen des Eingangs und steuert den Frequenzbereich, der im Ausgang geliefert wird.
Padding = 2. Padding funktioniert, um die Ausgabe fein zu interpolieren, ohne die Ergebnisberechnung in irgendeiner Weise zu beeinflussen. Dies kann bei der Visualisierung und der präzisen Identifizierung von Spektrallinien hilfreich sein. Das Feld ist eine beliebige ganze Zahl von -1 und mehr.
Zeitbandbreitenprodukt (NW) = 15. Das Produkt der Signalzeit und Spektralbreite.
Anzahl der Verjüngungen = 29. Bei der Auswahl der Anzahl der Kegel ist es wichtig, 2NW-1 zu verwenden. Es gibt keine Begrenzung für die Anzahl der verwendeten Verjüngungen. Je mehr Verjüngungen verwendet werden, führt dazu, dass Kegel mit schlechter Konzentration in die angegebene Frequenzbandbreite aufgenommen werden.
Testdurchschnitt = 1. Dieser Parameter bestimmt, ob eine Test- oder Kanalmittelung durchgeführt wird. Wenn dieser Parameter auf 0 gesetzt ist, gibt es keine Kanalmittelung, und die Funktion gibt unabhängige Ergebnisse für jede Testversion oder jeden Kanal aus, die als Eingabedaten übergeben werden. Wenn der Testdurchschnitt jedoch auf 1 festgelegt ist, werden die Ergebnisse, die dem Benutzer ausgegeben werden, über Testversionen oder Kanäle gemittelt.
Zeit zur Berechnung von FFT 30 s. Wird verwendet, um die Entwicklung des Spektrums zu verfolgen, indem das Spektrum über viele kleine Fenster berechnet wird.
Schrittgröße des Fensters für DIE FFT-Berechnung = 5. Der Betrag, den das Gleitzeitfenster nach jeder Spektrumberechnung vorrückt.
HINWEIS: Die in Schritt 3.7.1 angegebenen Standardspektrogrammparameter können bei Bedarf geändert werden.
- Verwenden Sie die folgenden Standardspektrogrammparameter:
- Geben Sie Titel sowohl für das Spektrogramm als auch für eEG ein.
- Speichern Sie das resultierende Spektrogramm und EEG.
- Zahlen speichern, indem Sie auf Datei | Speichern Sie im Abbildungsfenster.
HINWEIS: Die Zahlen werden Programmnutzern Zusammenfassungen liefern, die zu Zahlen in Publikationsqualität entwickelt werden können.
- Zahlen speichern, indem Sie auf Datei | Speichern Sie im Abbildungsfenster.
4. Fehlerbehebung
- Laden Sie die EEG-Daten für den Mausschlaf für die Berechnung des Beispielspektrogramms herunter.
- Führen Sie das Programm mit den Beispieldaten aus, um sicherzustellen, dass der Benutzer das Programm korrekt verwendet. Hier finden Sie die Zahlen für diese Stichprobendaten im Anhang, um sicherzustellen, dass die aus den Stichprobendaten erstellten Zahlen korrekt sind.
HINWEIS: Alle verwendeten Geräte und Materialien sind in der Tabelle der Materialienzur Verfügung gestellt worden.
Ergebnisse
Die folgenden Abbildungen veranschaulichen die Art neuartiger Einblicke in EEG-Indizes der Gehirnerregbarkeit, die von Spektrogrammen bereitgestellt werden.
Abbildung 1A zeigt Ähnlichkeiten und Unterschiede im kortikalen EEG während der Wachheit, des NREM-Schlafs und des REM-Schlafs. Viele Forscher verwenden diese Art von Spuren, zusammen mit EMG-Aufnahmen (nicht gezeigt), um Schlaf und Wachheit zu quantifizieren. Abbildung 1B verwendet ein Hypnogrammdiagramm, um die zeitliche Organisation von Schlaf- und Wachheitszuständen auf der Grundlage von Auswertungen von EEG- und EMG-Aufnahmen zu vermitteln. Staaten wurden in 10 s Epochen bewertet und diese Epochen wurden als Hypnogramm während der 14.400s mit der 4 h Aufnahme geplottet. Hypnogrammdiagramme veranschaulichen nicht die Tatsache, dass Übergänge zwischen Zuständen kontinuierlich und nichtlinear sind. Im Gegensatz zu einem Hypnogramm-Plot veranschaulicht das Spektrogramm (Abbildung 1C) hochdynamische Veränderungen der EEG-Frequenz und -Leistung in Abhängigkeit von der Zeit. Das Spektrogramm hebt auch die Ähnlichkeiten zwischen dem kortikalen EEG-Signal während der Wachheit und während des REM-Schlafes hervor. Die drei Auflagen des Spektrogramms (Abbildung 1C) markieren zudenliegen als Wachheit (WAKE), NREM-Schlaf und REM-Schlaf im Hypnogramm oben (Abbildung 1B) und werden zur Visualisierung der detaillierten Änderungen der EEG-Frequenz und -Leistung bereitgestellt. Das Spektrogramm für die gesamte Aufnahme bietet eine differenzierte Einschätzung des EEG als kontinuierlichen Prozess.
Abbildung 2 enthält vier Multitaper-Spektrogramme, die jeweils 4 h EEG-Aufnahmen nach intraperitonealer Verabreichung von Saline, Morphin, Buprenorphin und Fentanyl zusammenfassen. Alle vier Aufnahmen stammen aus derselben Maus und wurden 2 h nach Lichtbeginn begonnen. Die Opiate, aber nicht saline, hemmten NREM und REM Schlaf, und erhöhte die Menge an Wachheit. Eine Reihe von neuen Merkmalen werden durch die Spektrogramme visualisiert. Der Nachweis neuartiger EEG-Merkmale deutet auf eine mögliche Anwendung zur Opiatdifferenzierung in einer chemischen Bedrohungsumgebung hin. Nach der Saline-Injektion (Abbildung 2A) befand sich die größte Leistung im Bereich von 2 bis 4 Hz, was auf den NREM-Schlaf hindeutet. Beachten Sie, dass die EEG-Spektrogramme durch Opiat-Verabreichung grundlegend verändert wurden und dass jedes Opiat einzigartige spektrale Veränderungen verursachte.
Abbildung 3 zeigt, dass EEG-Änderungen, die durch die Spektrogramme dargestellt werden, quantifiziert und als durchschnittliche dominierende Spektralleistung jeder Halbfrequenz (Abbildung 3A) und als durchschnittliche Spektralleistung innerhalb bestimmter EEG-Frequenzbänder(Abbildung 3B) ausgedrückt werden können. Die größten Unterschiede von Saline wurden durch Buprenorphin verursacht und traten im Delta- und Thetabereich auf.
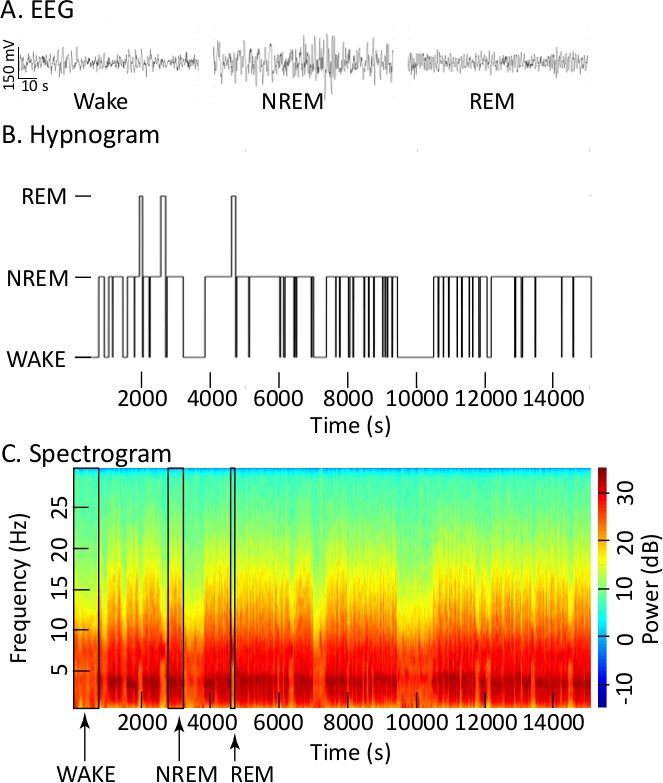
Abbildung 1: Kortikale EEG-Aufnahmen zur Erstellung von Hypnogrammen und Spektrogrammen. (A) EEG-Wellenformen, die während der Wachheit, des NREM-Schlafs und des REM-Schlafs während einer Baseline-Aufnahme (keine Injektion) aufgezeichnet werden. Jede Spur zeigt 90 s Aufnahme. (B) Das Hypnogramm verwendet die Höhe der Balken, um den Bewusstseinszustand (Ordinate) im Vergleich zu 4 h der Aufnahme (Abscissa) zu vermitteln. (C) Verjüngtes Spektrogramm mit einem Farbbalken zur Übertragung von EEG-Leistung in Dezibel (dB, rechte Ordinate) oder Spektralleistungsdichte bei verschiedenen EEG-Frequenzen in Hertz (Hz, linke Ordinate) in Abhängigkeit von 4 h Aufnahmezeit (Abszissa). Dem Spektrogramm wurden schwarze vertikale Linien hinzugefügt, um jeweils eine Episode von Wachheit, NREM-Schlaf und REM-Schlaf abzugrenzen. (Spektrogrammparameter: Abtastfrequenz = 500 Hz, Fpass = 0,3 Hz und 30 Hz, Polsterung = 2, Zeitbandbreite = 15, Anzahl der Kegel 29, Versuchsdurchschnitt = 1, Zeitdauer bis zur Berechnung von 30 s, Schrittgröße des Fensters für FFT-Berechnung = 5). Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
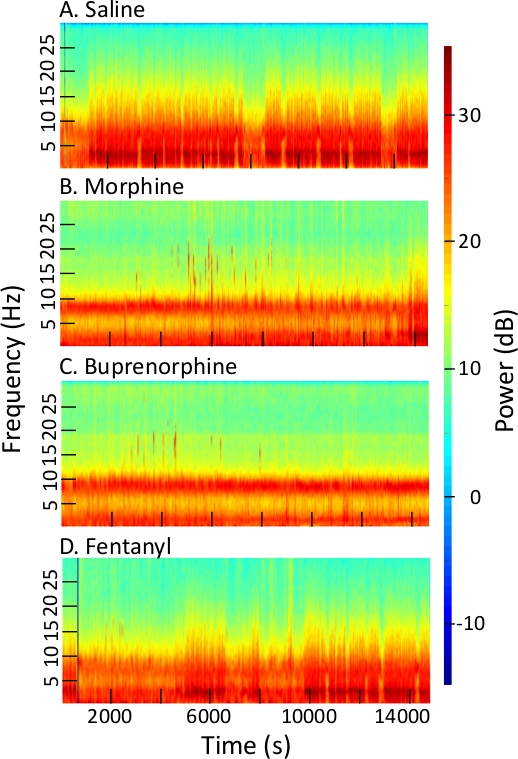
Abbildung 2: Spektrogramme, die Veränderungen der EEG-Leistung und -Frequenz veranschaulichen, die durch opiate Verabreichung verursacht werden. Jedes Spektrogramm zeichnet die EEG-Frequenz in Hertz (Hz, linke Ordinate) und Dezibel (dB) eEG-Leistung mit einem Farbbalken (rechte Ordinate) für 4 h (Abscissa) nach Verabreichung von (A) Kochsaline, (B)Morphin, (C) Buprenorphin und (D) Fentanyl. (Spektrogrammparameter: Abtastfrequenz = 500 Hz, Fpass = 0,3 Hz und 30 Hz, Polsterung = 2, Zeitbandbreite = 15, Anzahl der Kegel 29, Versuchsdurchschnitt = 1, Zeit zur Berechnung von FFT 30 s, Schrittgröße des Fensters für FFT-Berechnung = 5). Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
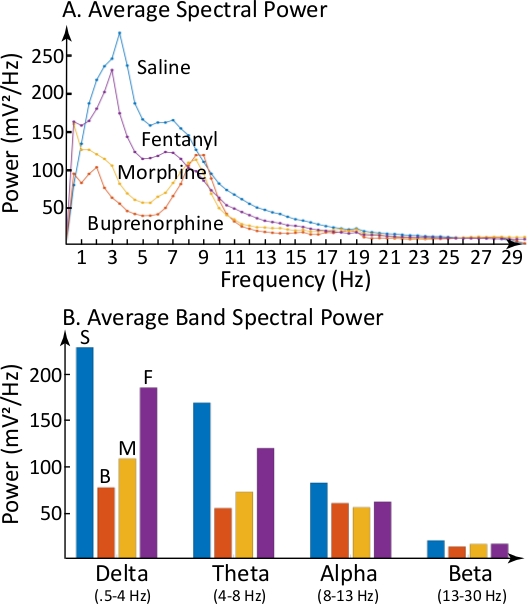
Abbildung 3: Opiate veränderten die durchschnittliche EEG-Leistung innerhalb des Delta- und Theta-EEG-Frequenzbänders differenziell. (A) Fasst die durchschnittliche EEG-Leistung während jeder in Abbildung 2 gezeigten 4-h-Aufnahme zusammen. Ordinate zeichnet die durchschnittliche EEG-Leistung bei jeder Halbfrequenz (Abscissa). Im Verhältnis zur Saline-Steuerung zeigt jede der anderen drei Funktionen opiatspezifische Veränderungen der durchschnittlichen EEG-Leistung. (B) Veranschaulicht die durchschnittliche EEG-Leistung in vier EEG-Frequenzbändern (Delta, Theta, Alpha und Beta) nach Verabreichung von Kochsaline (S), Buprenorphin (B), Morphin (M) und Fentanyl (F). Die Farbcodierung ist für Leistungsfunktionen in A und durchschnittliche Leistungsbänder in Bgleich. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Diskussion
Das hier beschriebene Programm wurde entwickelt, um ein Spektrogramm mit den neun Schritten zu erstellen, die in Protokollabschnitt 3, Spektrogrammberechnung, beschrieben sind. Diese Schritte umfassen das Erfassen des Spektrogrammprogramms, die Sicherstellung des richtigen Dateiformats und das Ändern der Berechnungsparameter für die Generierung einzigartiger Benutzerspektrogramme. Benutzer können Spektrogramme erstellen, die auf eine Reihe von konzeptionellen Fragen und experimentellen Designs zugeschnitten sind. Um die Einfachheit und Effizienz dieses Entwicklungsprozesses zu verbessern, ist es wichtig, die rohen EEG-Daten im richtigen Dateiformat bereitzustellen, das gemäß den oben beschriebenen Einschränkungen benannt wird. Obwohl Beispielsignale für Maus-EEG-Daten bereitgestellt wurden, ist das Spektrogrammprogramm problemlos auf menschliche und nicht-menschliche EEG-Daten anwendbar, die frei von Signalverarbeitungsbeschränkungen sind.
Der empfohlene Ansatz für die Fehlerbehebung und Methodenänderung besteht darin, zunächst einen kleinen Datensatz zu analysieren. Zu den wichtigsten zu berücksichtigenden Programmausgaben gehören Plots des gefilterten EEG sowie des Spektrogramms. Ein ansprechender Aspekt des verjüngten Spektrogramms ist, dass es auf eine Vielzahl von periodischen, biologischen Signalen angewendet werden kann. Die Vielfalt reicht von langanhaltenden zirkadianen (24 h) Rhythmen17 bis hin zu sehr schnellen Rhythmen wie 1.000 Hz Entladungsraten einer Renshaw-Zelle18.
Die Datenformatierung ist eine Einschränkung dieses Spektrogrammprotokolls. Das europäische Datenformat (EF) wird häufig mit EEG-Daten verwendet. Es gibt jedoch viele andere Formatierungsoptionen. Aus diesem Grund wurde die Rohcodedatei (siehe 3.2 oben) für den Fall aufgenommen, dass der Benutzer das Dateiformat ändern möchte. In Bezug auf die Unformat-Programmdatei ist eine weitere Einschränkung die Notwendigkeit der Erfahrung mit der Computer-Programmiersprache, um das Dateiformat zu ändern. Nicht alle Ermittler haben Zugriff auf die proprietäre Software und das gesamte Spektrum an Plug-Ins. Dieses Protokoll wurde entwickelt, um dieses Problem zu umgehen, indem ein kompiliertes Programm zur Verfügung gestellt wird, das auf einem WINDOWS-basierten Gerät ohne Softwarelizenzierung ausgeführt wird. Dies wird durch das RUNTIME-Plugin erreicht, das im kompilierten Programm enthalten ist und keine Software-Registrierung durch den Benutzer erfordert.
Diese EEG-Spektrogrammroutine ist ein neuartiges, Open Source, computerbasiertes Programm, mit dem Benutzer personalisierte Multitaper-Spektrogramme aus einer Vielzahl von Daten erstellen können. Der Benutzer hat die vollständige Kontrolle über alle Rechenaspekte der Spektrogrammerzeugung. Ohne vorherige Stell- und Computerprogrammierung können Spektrogramme schwierig zu generieren sein. Das hier beschriebene Protokoll erleichtert die Spektrogrammerzeugung. Weitere Messwerte für die Signalverarbeitung und die Multitaper-Spektrogrammführung finden Sie im Abschnitt ergänzendes Material.
Ergänzendes Material
http://chronux.org
http://www-users.med.cornell.edu/~jdvicto/pdfs/pubo08.pdf
http://www.fieldtriptoolbox.org/tutorial/timefrequencyanalysis/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4502759/#SD3-data
Offenlegungen
Die Autoren haben keine Interessenkonflikte.
Danksagungen
Diese Arbeit wurde teilweise durch einen NIH-Zuschuss HL-65272 unterstützt. Die Autoren danken Zachary T. Glovak und Clarence E. Locklear für ihre Beiträge zu diesem Projekt.
Materialien
| Name | Company | Catalog Number | Comments |
| Dental acrylic | Lang Dental Manufacturing Co | Jet powder and liquid | |
| EEG/EMG Amplifier | Data Science International | model MX2 | |
| macOS Mojave | Apple | v10.14.4 | |
| MATLAB | Mathworks | v9.4.0.813654 | software for spectrogram comp. |
| Mouse anesthesia mask | David Kopf Instruments | model 907 | |
| Neuroscore | Data Science International | v3.3.9317-1 | software for scoring sleep and wakefulness |
| Ponemah | Data Science International | v5.32 | software for EEG/EMG Data Acquisition |
| Stereotaxic frame | David Kopf Instruments | model 962 | |
| Stereotaxic frame, mouse adapter | David Kopf Instruments | model 921 | |
| Windows 10 | Microsoft | v10.0.17763.503 | |
| Wireless Telemeter | Data Science International | model HD-X02 |
Referenzen
- Wasilczuk, A. Z., Proekt, A., Kelz, M. B., McKinstry-Wu, A. R. High-density electroencephalographic acquisition in a rodent model using low-cost and open source resources. Journal of Visualized Experiments. 117, 10 (2016).
- Prerau, M. J., Brown, R. E., Bianchi, M. T., Ellenbogen, J. M., Purdon, P. L. Sleep neurophysiological dynamics through the lens of multitaper spectral analysis. Physiology. 32, 60-92 (2017).
- Akin, M. Comparison of wavelet transform and FFT methods in the analysis of EEG signals. Journal of Medical Systems. 26 (3), 241-247 (2002).
- Purdon, P. L., Sampson, A., Pavone, A., Brown, E. N. Clinical electroencephalography for anesthesiologists Part 1: Background and basic signatures. Anesthesiology. 123 (4), 937-960 (2015).
- Liu, Q., et al. Frontal EEG temporal and spectral dynamics similarity analysis between propofol and desflurane induced anesthesia using Hilbert-Huang Transform. BioMed Research International. 2018, 4939480 (2018).
- Akeju, O., et al. Spatiotemporal dynamics of dexmedetomidine-induced electroencephalogram oscillations. PLoS One. 11 (10), (2016).
- Ogilvie, R. D. The process of falling asleep. Sleep Medicine Reviews. 5 (3), 247-270 (2001).
- Baghdoyan, H. A., Lydic, R., Brady, S. T., Albers, R. W., Price, D. L., Siegel, G. J. . Basic Neurochemistry. , 982-999 (2012).
- Angel, C., et al. Buprenorphine depresses respiratory variablity in obese mice with altered leptin signaling. Anesthesiology. 128 (5), 984-991 (2018).
- Glovak, Z. T., Mihalko, S., Baghdoyan, H. A., Lydic, R. Leptin status alters buprenorphine-induced antinociception in obese mice with dysfunctional leptin receptors. Neuroscience Letters. 660, 29-33 (2017).
- Zhang, X., et al. Morphine and fentanyl delivered to prefrontal cortex of behaving mice depress breathing and alter neurotransmitter concentrations. Anesthesia & Analgesia. , (2019).
- Cornelissen, L., Kim, S. E., Purdon, P. L., Brown, E. N., Berde, C. B. Age-dependent electroencephalogram (EEG) patterns during sevoflurane general anesthesia in infants. eLIFE. 4, e06513 (2015).
- Chini, M., et al. Neural correlates of anesthesia in newborn mice and humans. Front Neural Circuits. 13 (Article 38), 1-13 (2019).
- Flint, R. R., Chang, T., Lydic, R., Baghdoyan, H. A. GABA-A receptors in the pontine reticular formation of C57BL/6J mouse modulate neurochemical, electrographic, and behavioral phenotypes of wakefulness. Journal of Neuroscience. 30 (37), 12301-12309 (2010).
- Paxinos, G., Franklin, K. B. J. . The Mouse Brain in Stereotaxic Coordinates. , (2018).
- Franken, P., Malafosse, A., Tafti, M. Genetic variation in EEG activity during sleep in inbred mice. American Journal of Physiology. 257 (4), (1998).
- Ko, C. H., et al. Emergence of noise-induced oscillations in the central circadian pacemaker. PLoS Biol. 8 (10), e1000513 (2010).
- Steriade, M., Curró Dossi, R., Conteras, D. Electrophysiological properties of intralaminar thalamocortical cells discharging rhythmic (40 Hz) spike-bursts at 1000 Hz during waking and rapid eye movement sleep. Neuroscience. 56, 1-9 (1993).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten