Method Article
Programme de spectrogrammes multitaper s'informatisé pour les données électroencéphalographiques
Dans cet article
Résumé
Ce protocole fournit un programme MATLAB ouvert et compilé qui génère des spectrogrammes multitapers pour les données électroencéphalographiques.
Résumé
Les ressources Web actuelles fournissent des outils limités et conviviaux pour calculer les spectrogrammes pour visualiser et quantifier les données électroencéphalographiques (EEG). Cet article décrit un code open source basé sur Windows pour la création de spectrogrammes multitapers EEG. Le programme compilé est accessible aux utilisateurs de Windows sans licence logicielle. Pour les utilisateurs de Macintosh, le programme est limité à ceux qui ont une licence logicielle MATLAB. Le programme est illustré par des spectrogrammes EEG qui varient en fonction des états de sommeil et d'éveil, et des altérations induites par les opiacés dans ces états. Les EEGs des souris de C57BL/6J ont été sans fil enregistrés pendant 4 h après injection intrapéritonéale des doses saline (contrôle de véhicule) et antinociceptives de morphine, de buprénorphine, et de fentanyl. Les spectrogrammes ont montré que la buprénorphine et la morphine ont causé des changements similaires dans la puissance de l'EEG à 1-3 Hz et 8-9 Hz. Spectrograms après l'administration de fentanyl a révélé des bandes de puissance moyennes maximales à 3 Hz et 7 Hz. Les spectrogrammes démasqué effets différentiels opiacés sur la fréquence et la puissance eEG. Ces méthodes informatiques sont généralement régétatibles dans toutes les classes de médicaments et peuvent être facilement modifiées pour quantifier et afficher un large éventail de signaux biologiques rythmiques.
Introduction
Les données de l'EEG peuvent être analysées de manière productive dans le domaine de la fréquence pour caractériser les niveaux d'excitation comportementale et neurophysiologique1. Les spectrogrammes multitapers transforment la forme d'onde EEG en domaines du temps et de la fréquence, ce qui entraîne la visualisation de la puissance du signal dynamique à différentes fréquences à travers le temps. Le spectrogramme multitaper utilise l'analyse de Fourier pour produire des estimations de densité spectrale. L'estimation de densité spectrale sépare une forme d'onde dans les ondes sinusoïdales pures composant le signal et est analogue à la diffraction de la lumière blanche à travers un prisme pour voir tout le spectre des couleurs2. Le spectrogramme multitaper de l'EEG représente l'activité combinée de plusieurs réseaux de neurones avec des modèles de décharge qui oscillent à différentes fréquences2. En raison de son décalage horaire invariant, la transformation Fourier est considérée comme la meilleure transformation entre les domaines de temps et de fréquence3. L'analyse de Fourier a également un certain nombre de limitations. Les signaux EEG sont non stationnaires. Par conséquent, de petits changements peuvent ne pas être perçus selon les méthodes Fourier et l'analyse peut changer en fonction de la taille de l'ensemble de données. Cependant, la fenêtre est utilisée lors de l'application d'une transformation Fourier à un signal non stationnaire. Cela suppose que le spectre du signal ne change que marginalement sur de courtes périodes de temps. Une autre méthode pour l'analyse spectrale est la transformation des ondes qui peut être plus appropriée pour détecter les maladies du cerveau3.
D'un point de vue fonctionnel, les différentes oscillations comprenant un signal EEG sont des phénotypes de caractère de niveau inférieur caractéristiques des phénotypes d'état de niveau supérieur tels que le sommeil et l'éveil2, ou la perte d'éveil causée par les anesthésiques généraux4,5,6. En ce qui concerne les états de sommeil et d'éveil, le spectrogramme illustre clairement que les rythmes de sommeil générés endogènement sont continus et dynamiques7. Les descriptions quantitatives des états de sommeil et d'éveil ont traditionnellement impliqué un processus de binning qui attribue une classification du sommeil ou du réveil à chaque époque spécifiquement définie (p. ex., 10 s) de l'enregistrement de l'EEG. Ces bacs d'état sont ensuite tracés en fonction du temps. Les diagrammes de données de cours de temps, souvent appelés hypnogrammes, sont employés pour différencier le sommeil normal du sommeil qui est perturbé par la maladie, l'administration de drogue, les changements dans les rythmes circadiens, le travail de quart, etc. Une limitation des parcelles d'hypnogramme est qu'elles dénaturent les signaux d'EEG en exprimant des états d'excitation comme formes d'ondes carrées. Le tracé d'hypnogramme implique une discrète des états d'excitation2 et ne permet pas un affichage finement granulé des étapes intermédiaires ou de transition. En outre, les époques de notation de 10 s produisent une discrétion du temps en imposant une limite inférieure sur l'échelle de temps. Le résultat de la discrétion de l'état et du temps est la perte de l'information neurophysiologique concernant l'interaction dynamique entre les états de conscience2 et la perturbation drogue-induite de ces états4. Par exemple, différents agents anesthésiques agissent sur différentes cibles moléculaires et réseaux neuronaux. La manipulation pharmacologique de ces réseaux neuronaux produit de façon fiable des spectrogrammes uniques au médicament, à la dose et à l'itinéraire de l'administration4.
Le protocole actuel a été développé pour faciliter la recherche concernant les mécanismes par lesquels les opioids modifient le sommeil8,la respiration9,nociception10,et la neurochimie de cerveau11. Ce protocole décrit les étapes requises pour créer un spectrogramme multitapered pour les analyses EEG qui peuvent être complétés à l'aide d'un logiciel propriétaire ou d'un système qui n'a pas de licence MATLAB. Des souris de C57BL/6J (B6) ont été employées pour valider la capacité de cette méthode informatisée pour créer de nouveaux spectrogrammes d'EEG pendant les états normaux et non perturbés de sommeil et d'éveil et après administration systémique des opiacés. La fiabilité et la validité des analyses ont été confirmées par des comparaisons systématiques des différences entre les spectrogrammes d'EEG après que les souris B6 aient reçu des injections intrapéritones de saline (contrôle de véhicule) et des doses antinociceptives de morphine, de buprénorphine et de fentanyl.
Les études quantitatives de la dynamique néonatale de l'EEG de souris ont une pertinence translationnelle en fournissant un modèle pour les études visant à parvenir à une meilleure compréhension de l'EEG humain néonatal12. Quantifier la dynamique de l'EEG n'est pas seulement descriptif et peut contribuer à des approches d'apprentissage automatique qui peuvent prédire l'excitation basée en partie sur les données de l'EEG13. L'objectif du présent rapport est de promouvoir la science translationnelle en fournissant un code largement accessible et convivial pour l'informatique des spectrogrammes multitapers qui caractérisent les changements induits par la drogue dans l'EEG de souris.
Protocole
Toutes les procédures impliquant des souris ont adhéré au Guide for the Care and Use of Laboratory Animals (8e édition, National Academies Press, Washington DC, 2011) et ont été examinées et approuvées par le Comité institutionnel des soins et de l'utilisation des animaux de l'Université du Tennessee.
1. Implantation d'électrodes d'enregistrement et de collecte de données initiales
- Achetez des souris et conservez-les dans une pièce à température contrôlée avec accès ad libitum à la nourriture et à l'eau. Permettre aux souris de s'adapter à leur nouvel environnement pendant une semaine avant l'implantation chirurgicale d'électrodes d'enregistrement. La procédure d'implantation a été décrite en détail1,14.
- Stérilisez tout l'équipement chirurgical.
- Anesthésiez les souris avec de l'isoflurane à 2,5 % à 3 % livré en oxygène à 100 %.
- Après la perte du réflexe de redressement, retirez la souris de la chambre d'induction d'anesthésie et transférez-la dans un cadre stéréotaxique.
- Appliquer une pommade ophtalmique sur les deux yeux.
- Réduire l'isoflurane à 1,7%, livré en continu via un masque.
- Faire une incision du cuir chevelu midline pour exposer le crâne.
- Percer deux craniotomies au-dessus du cortex gauche et droit (chacun e à des coordonnées stéréotaxiques antérieures de 1,0 et latérales de 3,0 par rapport au bregma15).
- Insérez les électrodes EEG dans chaque craniotomie et fixez-les avec de l'acrylique dentaire.
- Implanter des électrodes bipolaires dans le muscle du trapèze dorsal pour l'enregistrement de l'électromyogramme (EMG).
REMARQUE: Les quatre électrodes sont conduits à un télémètre sans fil implanté sous-cutané au-dessus du quadrant inférieur droit du corps. Ces techniques chirurgicales peuvent être consultées ici (https://www.datasci.com/services/dsi-surgical-services/surgical-videos). - Après la chirurgie, administrer le carprofène analgésique et placer la souris dans une cage de récupération chaude. Observez la souris jusqu'à ce qu'elle soit ambulatoire. Maison des souris implantées individuellement.
- Au rétablissement complet de la chirurgie, manipulez des souris quotidiennement et évaluez la qualité des enregistrements d'EEG et d'EMG.
- Configurer le système d'acquisition de données pour enregistrer tous les signaux de 1 000 mV.
- Obtenir des enregistrements EEG et EMG pour la durée nécessaire.
- Marquez chaque bac de 10 s des enregistrements numériques d'EEG et d'EMG comme éveil, sommeil rapide de mouvement d'oeil (REM), ou sommeil non-REM (NREM) utilisant le logiciel de notation de sommeil.
REMARQUE: Parmi les souches de souris, il existe des différences spécifiques au génotype et à l'État dans la puissance de l'EEG exprimées en pourcentage de la puissance totale16. Chez les souris B6, les états d'éveil sont caractérisés par un EEG à fréquence mixte de 75 à 100 mV et par des signaux EMG montrant une tonus musculaire proéminent avec de fortes augmentations d'amplitude pendant le mouvement. Les critères pour la notation du sommeil NREM comprennent une réduction de l'amplitude EMG par rapport à l'amplitude EMG de l'éveil. L'EEG de sommeil DeREM a une fréquence plus lente et une amplitude accrue (100-150 mV) par rapport à l'éveil. Le sommeil paradoxal est caractérisé par une atonie musculaire et un signal EEG qui est similaire à l'EEG de l'éveil. - Instruire deux personnes à marquer indépendamment le même record. Au moins une personne devrait être aveuglée par la condition de traitement. Les valeurs de concordance entre les deux marqueurs de sommeil devraient être supérieures à 90%.
2. Installations et équipements
- Amplifiez et numérisez les signaux EEG et EMG non filtrés à l'aide d'instruments et de logiciels d'acquisition de données.
REMARQUE: La boîte à outils d'analyse spectrale Chronux développée dans le laboratoire Mitra du Laboratoire de Cold Spring Harbor est utilisée pour exprimer les signaux d'EEG comme puissance par rapport aux domaines du temps et de la fréquence.
3. Calcul spectrogramme
- Si un utilisateur de Windows, utilisez le programme compilé.
- Si un utilisateur Macintosh, exécutez le fichier de code brut.
- Obtenir des données EEG brutes et non traitées en format de fichier EDF ou CSV et les placer au même endroit que le fichier de programme compilé.
- Nommez les fichiers de données en utilisant les contraintes suivantes : les noms doivent se composer uniquement de lettres, de chiffres, de soulignements ou de tirets.
- Nommez les fichiers de données en utilisant les contraintes suivantes : les noms de fichiers ne doivent pas contenir de périodes, de virgules, d'espaces ou d'autres symboles.
- Téléchargez le programme multitaper Spectrogram compilé(https://drive.google.com/).
- Lancez le programme de spectrogrammes et suivez les invites pop-up. Choisissez le type de fichier : CSV ou . Fed.
REMARQUE: D'autres détails d'installation du programme sont situés dans le fichier readme.txt. - Tapez l'intégralité du nom de fichier EEG (p. ex. 419eeg.edf ou 419.eeg.csv).
- Sélectionnez les paramètres pour le calcul du spectrogramme : par défaut ou nouveau. Cette étape nécessite le temps de traitement le plus long car le spectrogramme est en cours de calcul. La fonction de fenlant mathématique (taper) fournit des estimations statistiquement indépendantes du spectre sous-jacent. Plus la durée de l'enregistrement est longue, plus cette étape prendra de temps. Sur une plate-forme PC fonctionnant sous Windows 10, cela nécessitait un maximum d'environ 3 à 4 min pour un enregistrement de 4 h.
- Utilisez les paramètres spectrogrammes par défaut suivants :
Fréquence d'échantillonnage 500 Hz. Cela représente le nombre d'échantillons par seconde.
fpass 0,3 Hz et 30 Hz. Fpass définit les fréquences d'entrée et contrôle la plage de fréquences fournies dans la sortie.
Rembourrage no 2. Padding fonctionne pour interpoler finement la sortie sans affecter le calcul du résultat en aucune façon. Cela peut aider à la visualisation et à l'identification précise des lignes spectrales. Le champ est tout entier de -1 et plus.
Produit de bande passante temporelle (NW) 15. Le produit de la durée temporelle du signal et de la largeur spectrale.
Nombre de cônes 29. Lors du choix du nombre de cônes, il est essentiel d'utiliser 2NW-1. Il n'y a pas de limite au nombre de cônes utilisés. Les cônes plus utilisés se traduira par l'inclusion de cônes avec une faible concentration dans la bande passante de fréquence spécifiée.
Moyenne d'essai 1. Ce paramètre régit l'exécution ou non de la moyenne des essais ou des canaux. Si ce paramètre est réglé à 0, il n'y a pas de moyenne de canal et la fonction produira des résultats indépendants pour chaque essai ou canal passé comme données d'entrée. Toutefois, si la moyenne de l'essai est fixée à 1, les résultats de sortie à l'utilisateur sont en moyenne sur les essais ou les canaux.
Temps de calcul FFT 30 s. Utilisé pour suivre l'évolution du spectre en calculant le spectre sur de nombreuses petites fenêtres.
Taille de la fenêtre pour le calcul FFT 5. Le montant de la fenêtre de temps de glissement avance après chaque calcul de spectre est effectué.
REMARQUE: Les paramètres de spectrogramme par défaut indiqués à l'étape 3.7.1 peuvent être modifiés au besoin.
- Utilisez les paramètres spectrogrammes par défaut suivants :
- Entrez les titres pour le spectrogramme et l'EEG.
- Enregistrer le spectrogramme et l'EEG qui en résultent.
- Enregistrer les chiffres en cliquant sur Fichier Enregistrer dans la fenêtre de la figure.
REMARQUE: Les chiffres fourniront aux utilisateurs du programme des résumés qui peuvent être élaborés en chiffres de qualité de publication.
- Enregistrer les chiffres en cliquant sur Fichier Enregistrer dans la fenêtre de la figure.
4. Dépannage
- Téléchargez l'exemple de souris sommeil EEG données pour l'échantillon de calcul spectrogramme.
- Exécutez le programme avec les données de l'échantillon pour vous assurer que l'utilisateur utilise correctement le programme. Trouvez les chiffres de ces données d'échantillon dans l'annexe pour vous assurer que les chiffres créés à partir des données de l'échantillon sont exacts.
REMARQUE: Tous les équipements et matériaux utilisés ont été fournis dans la Table des Matériaux.
Résultats
Les chiffres suivants illustrent le type d'idées nouvelles sur les indices d'Excitabilité du cerveau qui sont fournis par des spectrogrammes.
La figure 1A illustre les similitudes et les différences dans l'EEG cortical pendant l'éveil, le sommeil NREM, et le sommeil paradoxal. Beaucoup d'investigateurs emploient ce genre de traces, avec des enregistrements d'EMG (non montrés), pour quantifier le sommeil et l'éveil. La figure 1B utilise une parcelle d'hypnogramme pour transmettre l'organisation temporelle des états de sommeil et d'éveil sur la base d'évaluations des enregistrements d'EEG et d'EMG. Les états ont été marqués dans les périodes de 10 s et ces époques ont été tracées comme hypnogramme pendant les 14.400 s comprenant l'enregistrement de 4 h. Les parcelles d'hypnogramme n'illustrent pas le fait que les transitions entre les états sont continues et non linéaires. Contrairement à une intrigue d'hypnogramme, le spectrogramme (Figure 1C) illustre des changements très dynamiques dans la fréquence et la puissance de l'EEG en fonction du temps. Le spectrogramme souligne également les similitudes entre le signal cortical d'EEG pendant l'éveil et pendant le sommeil paradoxal. Les trois boîtes superposées sur le spectrogramme (figure 1C) marquent les états identifiés comme l'éveil (WAKE), le sommeil NREM, et le sommeil paradoxal dans l'hypnogramme ci-dessus (Figure 1B) et sont fournis pour aider à visualiser les changements détaillés dans la fréquence et la puissance de l'EEG. Le spectrogramme pour l'ensemble de l'enregistrement fournit une appréciation nuancée de l'EEG comme un processus continu.
La figure 2 fournit quatre spectrogrammes multitapers, chacun résumant 4 h d'enregistrements d'EEG après administration intrapéritonéale de salin, morphine, buprénorphine, et fentanyl. Les quatre enregistrements proviennent de la même souris et ont été commencés 2 h après le début de la lumière. Les opiacés, mais pas salin, inhibé NREM et REM sommeil, et a augmenté la quantité d'éveil. Un certain nombre de nouvelles caractéristiques sont visualisées par les spectrogrammes. La détection de nouvelles caractéristiques de l'EEG suggère l'application potentielle de la différenciation des opiacés dans un environnement de menace chimique. Après l'injection saline (Figure 2A) la plus grande quantité de puissance résidait dans la gamme de 2 à 4 Hz, ce qui indique le sommeil NREM. Notez que les spectrogrammes d'EEG ont été fondamentalement modifiés par l'administration d'opiacés, et que chaque opiacé a causé des changements spectrals uniques.
La figure 3 démontre que les changements d'EEG illustrés par les spectrogrammes peuvent être quantifiés et exprimés comme puissance spectrale moyenne de domination de chaque demi-fréquence (Figure 3A) et comme puissance spectrale moyenne dans des bandes de fréquences spécifiques de l'EEG (Figure 3B). Les plus grandes différences de saline ont été causées par la buprénorphine et se sont produites dans le delta et les gammes theta.
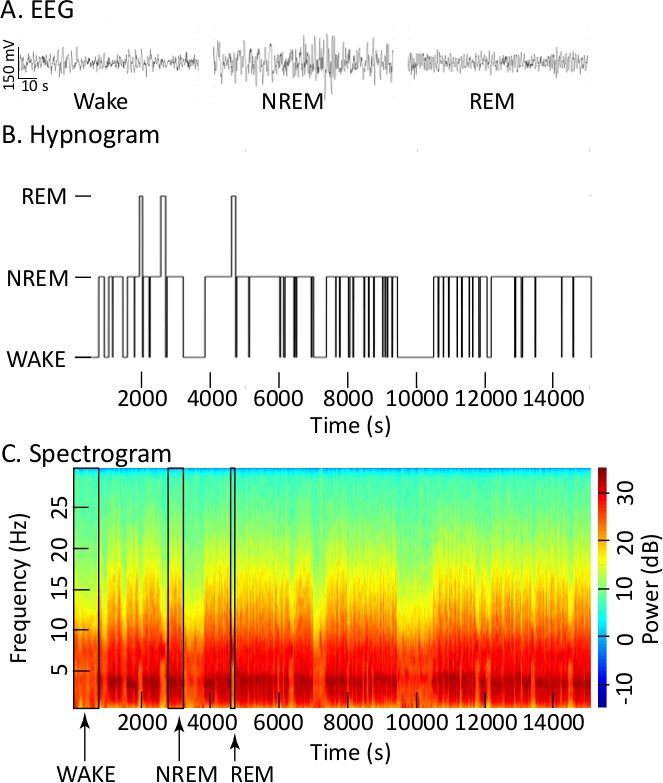
Figure 1 : Enregistrements d'EEG corticales utilisés pour créer des hypnogrammes et des spectrogrammes. (A) formes d'ondes EEG enregistrées pendant l'éveil, le sommeil NREM, et le sommeil paradoxal pendant un enregistrement de ligne de base (pas d'injection). Chaque trace montre 90 s d'enregistrement. (B) L'hypnogramme utilise la hauteur des barres pour transmettre l'état de conscience (ordinate) contre 4 h d'enregistrement (abscissa). (C) Spectrogramme effilé à l'aide d'une barre de couleur pour transmettre la puissance de l'EEG dans les décibels (dB, bonne coordination) ou la densité de puissance spectrale à différentes fréquences EEG dans Hertz (Hz, gauche) en fonction du temps d'enregistrement de 4 h (abscissa). Des lignes verticales noires ont été ajoutées au spectrogramme pour délimiter un épisode chacun de l'éveil, du sommeil NREM, et du sommeil paradoxal. (Paramètres de l'échantillon : fréquence d'échantillonnage de 500 Hz, fpass 0,3 Hz et 30 Hz, rembourrage 2, bande passante temporelle 15, nombre de cônes 29, moyenne d'essai 1, durée de calcul FFT 30 s, taille de la fenêtre pour le calcul FFT 5). Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
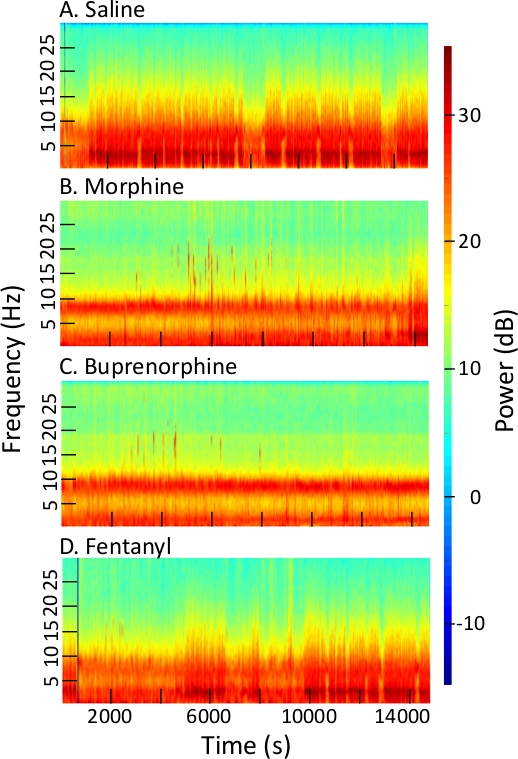
Figure 2 : Spectrogrammes illustrant les changements dans la puissance et la fréquence d'EEG provoqués par l'administration d'opiacés. Chaque spectrogramme trace la fréquence de l'EEG dans Hertz (Hz, gauche) et décibels (dB) de puissance EEG à l'aide d'une barre de couleur (droite) pendant 4 h (abscissa) après administration de (A) saline, (B) morphine, (C) buprénorphine, et (D) fentanyl. (Paramètres de l'échantillon : fréquence d'échantillonnage 500 Hz, fpass 0,3 Hz et 30 Hz, rembourrage 2, bande passante temporelle 15, nombre de cônes 29, moyenne d'essai 1, temps de calcul FFT 30 s, taille de la fenêtre d'étape pour le calcul FFT 5). Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
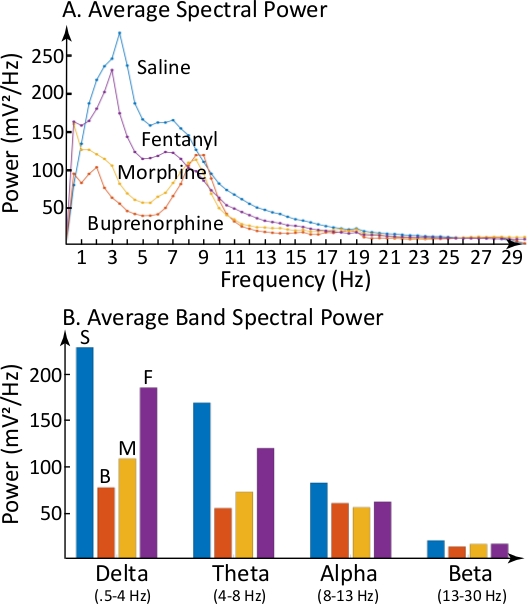
Figure 3 : Les opiacés ont modifié de façon différentielle la puissance moyenne de l'EEG dans les bandes de fréquences du delta et de l'EEG. (A) Résume la puissance moyenne de l'EEG au cours de chaque enregistrement de 4 h présenté à la figure 2. Les parcelles coordonnées ont une puissance moyenne de l'EEG à chaque demi-fréquence (abscissa). Par rapport au contrôle salin, chacune des trois autres fonctions montre des altérations spécifiques aux opiacés dans la puissance moyenne de l'EEG. (B) Illustre la puissance moyenne de l'EEG dans quatre bandes de fréquences EEG (delta, théta, alpha et bêta) après administration de salin (S), de buprénorphine (B), de morphine (M) et de fentanyl (F). Le codage des couleurs est le même pour les fonctions de puissance en A et les bandes de puissance moyennes en B. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
Discussion
Le programme décrit ici a été développé pour créer un spectrogramme en utilisant les neuf étapes décrites dans la section 3 du protocole, Spectrogram Computation. Ces étapes impliquent l'acquisition du programme de spectrogrammes, la garantie du format de fichier correct et la modification des paramètres de calcul pour la génération de spectrogrammes utilisateur uniques. Les utilisateurs peuvent créer des spectrogrammes adaptés à une gamme de questions conceptuelles et de conceptions expérimentales. Afin d'améliorer la facilité et l'efficacité de ce processus de développement, il est essentiel de fournir les données brutes de l'EEG dans le format de fichier correct, nommé en fonction des contraintes décrites ci-dessus. Bien que des signaux d'exemple aient été fournis pour les données de l'EEG de souris, le programme de spectrogrammes s'applique facilement aux données d'EEG humaines et non humaines qui sont exemptes de limitations de traitement du signal.
L'approche recommandée pour le dépannage et la modification des méthodes est de commencer par l'analyse d'un petit ensemble de données. Les principaux résultats du programme à considérer comprennent des parcelles de l'EEG filtré ainsi que le spectrogramme. Un aspect attrayant du spectrogramme effilé est qu'il peut être appliqué à une grande variété de signaux périodiques et biologiques. La variété varie de longues durées circadiennes (24 h) rythmes17 à des rythmes très rapides tels que 1000 Taux de décharge Hz d'une cellule Renshaw18.
Le formatage des données est une contrainte de ce protocole de spectrogramme. Le format européen des données (EDF) est largement utilisé avec les données EEG. Cependant, il existe de nombreuses autres options de mise en forme. Pour cette raison, le fichier de code brut a été inclus (voir 3.2 ci-dessus) au cas où l'utilisateur voudrait modifier le format du fichier. En ce qui concerne le fichier de programme brut, une autre limitation est la nécessité d'une expérience avec le langage de programmation informatique afin de modifier le format du fichier. Tous les enquêteurs n'ont pas accès au logiciel propriétaire et à la gamme complète de plug-ins. Ce protocole a été développé pour contourner ce problème en fournissant un programme compilé qui fonctionne sur un appareil WINDOWS sans licence logicielle. Ceci est réalisé grâce au plugin RUNTIME qui est inclus dans le programme compilé et ne nécessite pas d'enregistrement logiciel par l'utilisateur.
Cette routine de spectrogramme EEG est un nouveau programme informatisé open source qui permet aux utilisateurs de créer des spectrogrammes personnalisés et multitaperà à partir d'un large éventail de données. L'utilisateur a un contrôle complet sur tous les aspects de calcul de la génération de spectrogrammes. Sans connaissance préalable du traitement du signal et de la programmation informatique, les spectrogrammes peuvent être difficiles à générer. Le protocole décrit ici facilitera la génération de spectrogrammes. S'il vous plaît voir la section de matériel supplémentaire pour d'autres lectures de traitement du signal et de guidage spectrogramme multitaper.
Matériel supplémentaire
http://chronux.org
http://www-users.med.cornell.edu/~jdvicto/pdfs/pubo08.pdf
http://www.fieldtriptoolbox.org/tutorial/timefrequencyanalysis/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4502759/#SD3-data
Déclarations de divulgation
Les auteurs n'ont aucun conflit d'intérêts.
Remerciements
Ce travail est soutenu en partie par une subvention des NIH HL-65272. Les auteurs remercient Zachary T. Glovak et Clarence E. Locklear pour leur contribution à ce projet.
matériels
| Name | Company | Catalog Number | Comments |
| Dental acrylic | Lang Dental Manufacturing Co | Jet powder and liquid | |
| EEG/EMG Amplifier | Data Science International | model MX2 | |
| macOS Mojave | Apple | v10.14.4 | |
| MATLAB | Mathworks | v9.4.0.813654 | software for spectrogram comp. |
| Mouse anesthesia mask | David Kopf Instruments | model 907 | |
| Neuroscore | Data Science International | v3.3.9317-1 | software for scoring sleep and wakefulness |
| Ponemah | Data Science International | v5.32 | software for EEG/EMG Data Acquisition |
| Stereotaxic frame | David Kopf Instruments | model 962 | |
| Stereotaxic frame, mouse adapter | David Kopf Instruments | model 921 | |
| Windows 10 | Microsoft | v10.0.17763.503 | |
| Wireless Telemeter | Data Science International | model HD-X02 |
Références
- Wasilczuk, A. Z., Proekt, A., Kelz, M. B., McKinstry-Wu, A. R. High-density electroencephalographic acquisition in a rodent model using low-cost and open source resources. Journal of Visualized Experiments. 117, 10(2016).
- Prerau, M. J., Brown, R. E., Bianchi, M. T., Ellenbogen, J. M., Purdon, P. L. Sleep neurophysiological dynamics through the lens of multitaper spectral analysis. Physiology. 32, 60-92 (2017).
- Akin, M. Comparison of wavelet transform and FFT methods in the analysis of EEG signals. Journal of Medical Systems. 26 (3), 241-247 (2002).
- Purdon, P. L., Sampson, A., Pavone, A., Brown, E. N. Clinical electroencephalography for anesthesiologists Part 1: Background and basic signatures. Anesthesiology. 123 (4), 937-960 (2015).
- Liu, Q., et al. Frontal EEG temporal and spectral dynamics similarity analysis between propofol and desflurane induced anesthesia using Hilbert-Huang Transform. BioMed Research International. 2018, 4939480(2018).
- Akeju, O., et al. Spatiotemporal dynamics of dexmedetomidine-induced electroencephalogram oscillations. PLoS One. 11 (10), (2016).
- Ogilvie, R. D. The process of falling asleep. Sleep Medicine Reviews. 5 (3), 247-270 (2001).
- Baghdoyan, H. A., Lydic, R. Basic Neurochemistry. Brady, S. T., Albers, R. W., Price, D. L., Siegel, G. J. , Elsevier. 982-999 (2012).
- Angel, C., et al. Buprenorphine depresses respiratory variablity in obese mice with altered leptin signaling. Anesthesiology. 128 (5), 984-991 (2018).
- Glovak, Z. T., Mihalko, S., Baghdoyan, H. A., Lydic, R. Leptin status alters buprenorphine-induced antinociception in obese mice with dysfunctional leptin receptors. Neuroscience Letters. 660, 29-33 (2017).
- Zhang, X., et al. Morphine and fentanyl delivered to prefrontal cortex of behaving mice depress breathing and alter neurotransmitter concentrations. Anesthesia & Analgesia. , In Press (2019).
- Cornelissen, L., Kim, S. E., Purdon, P. L., Brown, E. N., Berde, C. B. Age-dependent electroencephalogram (EEG) patterns during sevoflurane general anesthesia in infants. eLIFE. 4, e06513(2015).
- Chini, M., et al. Neural correlates of anesthesia in newborn mice and humans. Front Neural Circuits. 13 (Article 38), 1-13 (2019).
- Flint, R. R., Chang, T., Lydic, R., Baghdoyan, H. A. GABA-A receptors in the pontine reticular formation of C57BL/6J mouse modulate neurochemical, electrographic, and behavioral phenotypes of wakefulness. Journal of Neuroscience. 30 (37), 12301-12309 (2010).
- Paxinos, G., Franklin, K. B. J. The Mouse Brain in Stereotaxic Coordinates. , 4th edn, Academic Press. (2018).
- Franken, P., Malafosse, A., Tafti, M. Genetic variation in EEG activity during sleep in inbred mice. American Journal of Physiology. 257 (4), (1998).
- Ko, C. H., et al. Emergence of noise-induced oscillations in the central circadian pacemaker. PLoS Biol. 8 (10), e1000513(2010).
- Steriade, M., Curró Dossi, R., Conteras, D. Electrophysiological properties of intralaminar thalamocortical cells discharging rhythmic (40 Hz) spike-bursts at 1000 Hz during waking and rapid eye movement sleep. Neuroscience. 56, 1-9 (1993).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon