Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Systemanalyse der neuroinflammatorischen und hämodynamischen Reaktion auf traumatische Hirnverletzungen
* Diese Autoren haben gleichermaßen beigetragen
In diesem Artikel
Zusammenfassung
Dieses Protokoll stellt Methoden vor, um die neuroinflammatorische und hämodynamische Reaktion auf leichte traumatische Hirnverletzungen zu charakterisieren und diese Daten als Teil einer multivariaten Systemanalyse unter Verwendung der partiellen Regression der kleinsten Quadrate zu integrieren.
Zusammenfassung
Leichte traumatische Hirnverletzungen (mTBIs) sind ein erhebliches Problem der öffentlichen Gesundheit. Eine wiederholte Exposition gegenüber mTBI kann zu kumulativen, lang anhaltenden funktionellen Defiziten führen. Zahlreiche Studien unserer Gruppe und anderer haben gezeigt, dass mTBI die Zytokinexpression stimuliert und Mikroglia aktiviert, den zerebralen Blutfluss und Stoffwechsel verringert und die zerebrovaskuläre Reaktivität beeinträchtigt. Darüber hinaus haben mehrere Arbeiten über einen Zusammenhang zwischen Störungen in diesen neuroinflammatorischen und hämodynamischen Markern und kognitiven Beeinträchtigungen berichtet. Hierin beschreiben wir Methoden zur Charakterisierung der neuroinflammatorischen und hämodynamischen Gewebereaktion auf mTBI bei Mäusen. Insbesondere beschreiben wir, wie man ein Gewichtsverlustmodell von mTBI durchführt, wie man den zerebralen Blutfluss mit einer nicht-invasiven optischen Technik namens diffuse Korrelationsspektroskopie longitudinal misst und wie man einen Luminex-Multiplex-Immunoassay an Hirngewebeproben durchführt, um Zytokine und immunmodulatorische Phospho-Proteine (z. B. innerhalb der MAPK- und NFκB-Signalwege) zu quantifizieren, die auf Mikroglia und andere neuronale Immunzellen reagieren und diese regulieren. Schließlich beschreiben wir, wie diese Daten mithilfe eines multivariaten Systemanalyseansatzes integriert werden können, um die Beziehungen zwischen all diesen Variablen zu verstehen. Das Verständnis der Beziehungen zwischen diesen physiologischen und molekularen Variablen wird es uns letztendlich ermöglichen, Mechanismen zu identifizieren, die für mTBI verantwortlich sind.
Einleitung
Überblick
Leichte traumatische Hirnverletzungen (mTBIs) betreffen jährlich ~ 1,6-3,8 Millionen Athleten1. Diese Verletzungen, einschließlich subkonzersiver und erschütternder Verletzungen, können Patienten mit vorübergehenden körperlichen, emotionalen, psychischen und kognitiven Symptomenzurücklassen 2. Darüber hinaus können sich wiederholende mTBI (rmTBI), die innerhalb eines "Fensters der Vulnerabilität" aufrechterhalten werden, zu einer kumulativen Schwere und Dauer kognitiver Konsequenzen führen, die länger anhalten als die Auswirkungen eines einzelnen mTBIallein 3, und letztendlich sogar zu einem dauerhaften Funktionsverlust 4,5,6. Obwohl sich viele Patienten innerhalb eines relativ kurzen Zeitraums (<1 Woche) erholen, leiden 10-40% der Patienten für > 1 Monat unter länger anhaltenden Auswirkungen von mTBI, wobei einige bis zu 1 Jahr 3,7,8,9 dauern. Trotz der hohen Prävalenz und der dauerhaften Folgen dieser Verletzungen sind die Verletzungsmechanismen schlecht verstanden und es gibt keine wirksamen Behandlungsstrategien.
Angesichts der hohen Variabilität der Endpunkte nach mTBI/rmTBI besteht eine Herausforderung bei der Identifizierung molekularer Auslöser im Frühstadium aus Gewebe, das in terminalen mTBI/rmTBI-Studien erhalten wurde, in dem Mangel an Längsschnittdaten, die definitive "akute molekulare Verbindungen" dieser molekularen Auslöser zu längerfristigen Ergebnissen belegen. Um diese Herausforderung zu meistern, hat unsere Gruppe entdeckt, dass akut reduzierter zerebraler Blutfluss, der akut mit einem optischen Werkzeug namens diffuse Korrelationsspektroskopie (DCS) gemessen wurde, stark mit längerfristigen kognitiven Ergebnissen in einem Mausmodell vonrmTBI 10 korreliert. Unter Verwendung dieses hämodynamischen Biomarkers zeigten wir, dass Mäuse mit akut niedrigem zerebralem Blutfluss (und damit einem schlechteren vorhergesagten Langzeitergebnis) einen gleichzeitigen akuten Anstieg der neuronalen Phospho-Signalgebung sowohl innerhalb des MACK- als auch des NFκB-Signalwegs, eine Zunahme der neuronalen Expression von proinflammatorischen Zytokinen und eine Zunahme der Expression des Phagozyten-/Mikrogliamarkers Iba111 aufweisen. . Diese Daten deuten auf eine mögliche Rolle für die neuronale Phospho-Signalgebung, die Zytokinexpression und die Mikrogliaaktivierung sowohl bei der akuten Regulation des zerebralen Blutflusses nach der Verletzung als auch bei der Auslösung einer Signalkaskade hin, die zu neuronaler Dysfunktion und schlechteren kognitiven Ergebnissen führt. Hierin beschreiben wir unseren Ansatz, sowohl die hämodynamische als auch die neuroinflammatorische Umgebung nach rTBI gleichzeitig zu untersuchen und diese komplexen Datensätze zu integrieren. Insbesondere skizzieren wir Verfahren für vier Schlüsselschritte zu diesem umfassenden Ansatz: (1) ein Gewichtsverlustmodell für leichte traumatische Hirnverletzungen, (2) Bewertung des zerebralen Blutflusses mit diffuser Korrelationsspektroskopie, (3) Quantifizierung der neuroinflammatorischen Umgebung und (4) Datenintegration (Abbildung 1). Im Folgenden finden Sie eine kurze Einführung in jeden dieser wichtigen Schritte, um die Leser durch die Gründe für unsere Methoden zu führen. Der Rest des Manuskripts enthält ein detailliertes Protokoll für jeden dieser Schlüsselschritte.
Gewichtsverlustmodell der leichten traumatischen Hirnverletzung
Obwohl viele ausgezeichnete präklinische Modelle für sich wiederholende leichte TBI existieren 12,13,14,15,16,17,18, verwenden wir ein gut etabliertes und klinisch relevantes Gewichtsabfall-geschlossenes Kopfverletzungsmodell. Zu den Hauptmerkmalen dieses Modells gehören (1) stumpfe Auswirkungen des intakten Schädels / der Kopfhaut, gefolgt von einer uneingeschränkten Rotation des Kopfes um den Hals, (2) keine offene strukturelle Hirnverletzung, Ödeme, Blut-Hirn-Schranken-Schäden, akuter Zelltod oder chronischer Hirngewebeverlust und (3) anhaltende (bis zu 1 Jahr) kognitive Defizite, die erst nach mehrerenTreffern auftreten 19 (Abbildung 2).
Beurteilung des zerebralen Blutflusses mit diffuser Korrelationsspektroskopie
Die diffuse Korrelationsspektroskopie (DCS) ist eine nicht-invasive optische Technik, die den Blutfluss 5,20,21 misst. Bei DCS wird eine Nahinfrarot-Lichtquelle auf der Gewebeoberfläche platziert. Ein Detektor wird in einem festen Abstand von der Quelle auf der Gewebeoberfläche platziert, um Licht zu erkennen, das sich durch das Gewebe vermehrt hat (Abbildung 3). Die Streuung von sich bewegenden roten Blutkörperchen führt dazu, dass die erkannte Lichtintensität mit der Zeit schwankt. Ein einfaches analytisches Modell, das als Korrelationsdiffusionstheorie bekannt ist, wird verwendet, um diese Intensitätsschwankungen mit einem Index des Blutflusses in Beziehung zu setzen (CBFi, Abbildung 4). Obwohl die Einheiten von CBF i (cm2 / s) nicht die traditionellen Flusseinheiten (ml / min / 100 g) sind, hat eine frühere Studie an Mäusen gezeigt, dass CBFi stark mit dem zerebralen Blutfluss korreliert, der durch den arteriellen Spin gemessen wird, der mit MRT21 markiert ist.
Als Referenz wurde das hier verwendete DCS-Instrument im eigenen Haus gebaut und besteht aus einem 852 nm langen Kohärenz-Längenlaser, einem Array von 4 Photonenzähl-Lawinen-Photodioden und einer Hardware-Autokorrelatorplatine (einzelne Tau, 8 Kanäle, 100 ns minimale Abtastzeit)21,22. Die Daten werden mit hausgemachter Software erfasst, die in LabView geschrieben ist. Die Tierschnittstelle für das Gerät besteht aus einer 400 μm Multimode-Quellfaser (400-2200 nm Wellenlängenbereich, reiner Kieselsäurekern, TECS Hard Cladding) und einer 780 nm Singlemode-Detektorfaser (780-970 nm Wellenlängenbereich, reiner Kieselsäurekern, TECS Hard Cladding, 730 ± 30 nm Sekundenmodus-Cut-off) im Abstand von 6 mm und eingebettet in einen schwarzen 3D-gedruckten Sensor (4 mm x 8 mm, Abbildung 3).
Quantifizierung des neuroinflammatorischen Umfelds
Obwohl die Neuroinflammation durch verschiedene zelluläre Prozesse reguliert wird, sind zwei wichtige relevante Mechanismen die extrazelluläre Signalübertragung durch Zytokine/Chemokine und die intrazelluläre Signalübertragung durch Phospho-Proteine. Um die neuroinflammatorische Umgebung des Gehirns nach einer Verletzung zu untersuchen, werden Gehirne aus Mäusen extrahiert, mikrodissektiert und Zytokine/Chemokine und Phosphoproteine mit Luminex quantifiziert (Abbildung 5, Abbildung 6, Abbildung 7). Luminex-Multiplex-Immunoassays ermöglichen die gleichzeitige Quantifizierung einer vielfältigen Sammlung dieser Proteine, indem enzymgebundene Immunsorbentien-Assays (ELISAs) an fluoreszierend markierte magnetische Kügelchen gekoppelt werden. Für jedes Protein von Interesse werden unterschiedliche fluoreszierende Tags verwendet, und die Perlen jedes Tags werden mit einem Capture-Antikörper gegen dieses bestimmte Protein funktionalisiert. Hunderte von Perlen zur Erfassung jedes Proteins werden miteinander vermischt, in eine 96-Well-Platte gelegt und mit Proben inkubiert. Nach der Probeninkubation wird ein Magnet verwendet, um die Perlen im Brunnen einzufangen, während die Probe ausgewaschen wird. Als nächstes bindet der biotinylierte Detektionsantikörper an den interessierenden Analyten, um ein Antikörper-Antigen-Sandwich ähnlich einem traditionellen ELISA zu bilden, jedoch mit dem ELISA für jedes Protein, das auf einer anderen fluoreszierend markierten Perle auftritt. Die Zugabe von Phycoerythrin-konjugiertem Streptavidin (SAPE) schließt jede Reaktion ab. Das Luminex-Instrument liest dann die Perlen und trennt das Signal nach jedem fluoreszierenden Tag / Protein.
Datenintegration
Aufgrund der großen Anzahl von Analyten (z. B. Zytokinen), die im Luminex-Assay gemessen wurden, kann die Datenanalyse schwierig zu interpretieren sein, wenn jedes quantifizierte Protein einzeln analysiert wird. Um die Analyse zu vereinfachen und Trends zu erfassen, die bei Analyten beobachtet wurden, verwenden wir eine multivariate Analysemethode, die als partielle Regression der kleinsten Quadrate bezeichnet wird (PLSR, Abbildung 8)23. PLSR funktioniert, indem es eine Achse von Gewichten identifiziert, die jedem gemessenen Protein entsprechen (d. h. Zytokine oder Phosphoproteine, die als "Prädiktorvariablen" bezeichnet werden), die zusammen die Kovarianz der gemessenen Proteine mit einer Antwortvariablen (z. B. zerebraler Blutfluss) optimal erklären. Die Gewichte werden als "Lasten" bezeichnet und zu einem Vektor zusammengefasst, der als latente Variable (LV) bezeichnet wird. Durch die Projektion (als "Scoring" bezeichnet) der gemessenen Proteindaten auf jedes der beiden LVs können die Daten in Bezug auf diese LVs neu dargestellt werden. Nach der Berechnung der PLSR verwenden wir eine Varimax-Rotation, um eine neue LV zu identifizieren, die die Kovarianz zwischen den Stichprobenprojektionen auf den LV und die Prädiktorvariable24 maximiert. Dieser Ansatz ermöglicht es uns, LV1 als die Achse zu definieren, für die die Varianz der Antwortvariablen am besten erklärt wird. LV2 maximiert die Kovarianz zwischen der Antwortvariablen und den LV1-Restdaten, die mit biologischer oder technischer Variabilität zwischen den Proben verbunden sein können. Schließlich führen wir eine Leave One Out Cross Validation (LOOCV) durch, um sicherzustellen, dass das PLSR-Modell nicht stark von einer Stichprobeabhängig ist 23.
In diesem Protokoll beschreiben wir Methoden zur Charakterisierung der neuroinflammatorischen und hämodynamischen Gewebereaktion auf mTBI. Der allgemeine Workflow ist in Abbildung 1 dargestellt. In diesem Protokoll unterliegen Mäuse einem oder mehreren mTBIs unter Verwendung eines Gewichtsverlust-geschlossenen Kopfverletzungsmodells. Der zerebrale Blutfluss wird vor und zu mehreren Zeitpunkten nach der Verletzung in Längsrichtung gemessen. Zum Zeitpunkt des Interesses für die Befragung von neuroinflammatorischen Veränderungen wird das Tier eingeschläfert und das Gehirn wird extrahiert. Hirnregionen von Interesse werden mittels Mikrodissektion isoliert und dann lysiert, um Protein zu extrahieren. Lysate werden dann sowohl für Luminex Multiplex-Immunoassays der Zytokin- und Phosphoproteinexpression als auch für Western Blot verwendet. Schließlich wird dieser ganzheitliche Datensatz mithilfe einer partiellen Regressionsanalyse der kleinsten Quadrate integriert.
Protokoll
Alle Tierverfahren wurden vom Emory University Institutional Animal Care and Use Committee (IACUC) genehmigt und befolgten die NIH-Richtlinien für die Pflege und Verwendung von Labortieren.
1. Gewichtsverlustmodell der leichten traumatischen Hirnverletzung
- Bereiten Sie das Weight-Drop-Setup vor. Montieren Sie einen Schraubstock auf einer ebenen Fläche mit einem 1 m langen Führungsrohr (2,54 cm Innendurchmesser), das vertikal ausgerichtet ist (Überprüfung mit einer Ebene). Verwenden Sie für den Aufprall eine 54 g Schraube (0,95 cm Grundkörperdurchmesser, 2 cm Kopfdurchmesser, 10,2 cm Länge).
- Maus kurz anästhesieren. Induzieren Sie die Maus mit 4,5% Isofluran in 100% Sauerstoff für 45 Sekunden. Bestätigen Sie eine ausreichende Tiefe der Anästhesie durch das Fehlen einer Zehenquetschreaktion.
- Verursachen Sie Verletzungen.
- Entfernen Sie die Maus schnell aus der Anästhesie und legen Sie die Maus auf die Mitte einer dünnen Membran (11,2 cm x 21,3 cm Gewebe).
- Verwenden Sie beide Hände, um das Gewebe straff zu halten, während die Maus in der Mitte liegt. Befestigen Sie den Schwanz der Maus unter einem Daumen. Positionieren Sie den Mauskopf unter dem Führungsrohr (Abbildung 2).
- Lassen Sie die Schraube von der Oberseite des Führungsrohrs auf den dorsalen Aspekt des Mauskopfes fallen und zielen Sie auf einen Aufprall zwischen den Augen und der Vorderseite der Ohren. Beim Aufprall dringt die Maus in das Gewebe ein und ermöglicht eine schnelle Beschleunigung des Kopfes um den Hals (Abbildung 2).
- Genesung
- Nach dem Aufprall die Maus in Rückenlage auf ein 37 °C warmes Pad in Raumluft legen. Überwachen Sie die Genesung für 1 Stunde nach der Verletzung. Innerhalb von 1 Stunde sollten Mäuse in der Lage sein, normal zu gehen, Nahrung und Wasser zu finden und keine grobmotorischen Defizite zu zeigen.
HINWEIS: Analgesie wird nicht nach Genehmigung des Institutional Animal Care and Use Committee angewendet, was aufgrund des verwirrenden Einflusses der Analgesie auf die interessierenden Parameter (dh zerebraler Blutfluss, Entzündungsmarker) gerechtfertigt ist. Bewusstlosigkeit, definiert als die Zeit von der Entfernung aus der Anästhesie bis zur Wiedererlangung des Aufrichtenden Reflexes, wird erwartet und dauert typischerweise von 20 s bis 3 Minuten (Supplemental Table 1). Kurze (<30 s) Episoden von Apnoe und / oder anfallsähnlicher Aktivität können beobachtet werden, insbesondere nach wiederholten Kopfverletzungen, die einmal täglich verteilt sind.
- Nach dem Aufprall die Maus in Rückenlage auf ein 37 °C warmes Pad in Raumluft legen. Überwachen Sie die Genesung für 1 Stunde nach der Verletzung. Innerhalb von 1 Stunde sollten Mäuse in der Lage sein, normal zu gehen, Nahrung und Wasser zu finden und keine grobmotorischen Defizite zu zeigen.
- Wiederholen Sie den Vorgang nach Bedarf. Diese Verletzung kann einmal täglich, wöchentlich oder monatlich wiederholt werden. Die Anzahl und der Abstand der Verletzungen hängen von der gewünschten Verletzungsschwere ab. In der Regel verwenden wir fünf Treffer im Abstand von einmal täglich, um robuste Defizite beim räumlichen Lernen und Gedächtnis zu induzieren.
HINWEIS: Frühere Studien haben gezeigt, dass fünf Treffer im Abstand von einmal täglich ausreichen, um Defizite beim räumlichen Lernen und Gedächtnis zu induzieren, die über 1 Jahr nach der Verletzung ohne Ödeme, Blutungen oder offene strukturelle Verletzungen des Gehirns anhalten19. Mäuse werden täglich gewogen und genau auf Anzeichen von Dehydrierung, motorischen Defiziten und Appetitlosigkeit überwacht. Wenn sie dehydriert sind, erhalten Mäuse feuchtes Chow und eine subkutane Injektion von 1 ml Kochsalzlösung einmal täglich. Um unnötiges Leiden zu verhindern und einen humanen Endpunkt zu gewährleisten, werden Mäuse eingeschläfert, wenn: Dehydration bleibt bestehen oder verschlechtert sich >24 h nach subkutaner Kochsalzbehandlung, das Körpergewicht nimmt gegenüber dem Ausgangswert vor der Verletzung um mehr als 20% ab, motorische Defizite wie Kreisen oder Pfotenziehen auftreten und > 1 h nach der Verletzung bestehen bleiben.
2. Beurteilung des zerebralen Blutflusses mit diffuser Korrelationsspektroskopie
- DCS-Datenerfassung
- Entfernen Sie Haare auf der Kopfhaut. Da DCS am besten in Abwesenheit von Haaren funktioniert, ist es notwendig, Fell auf dem Kopf vor Beginn der Experimente zu entfernen. Typischerweise wird die Haarentfernung 1-3 Tage vor Beginn der Studie durchgeführt.
- Induzieren Sie Mäuse mit 4,5% Isofluran in 100% Sauerstoff für 45 Sekunden und halten Sie mit 1-2% Isofluran in 100% Sauerstoff.
- Rasieren Sie den Kopf zwischen den Augen und den Ohren. Verwenden Sie dann Enthaarungscreme, um Fell auf dem Kopf zu entfernen, wie in Abbildung 3 dargestellt.
- Lassen Sie das Tier sich auf einem Wärmekissen von der Anästhesie erholen und kehren Sie dann in den Käfig zurück.
- Messen Sie den zerebralen Blutfluss mit DCS. Um Bewegungsartefakte während der Messung zu minimieren, untersuchen Sie Mäuse unter kurzer Isofluran-Anästhesie.
HINWEIS: Überwachen Sie die Atem- und Zehenklemmreaktion während der gesamten Messungen visuell und passen Sie die Isoflurankonzentration nach Bedarf an, um eine konsistente Anästhesietiefe zu gewährleisten. Signifikante Variationen in der Tiefe der Anästhesie könnten den Blutfluss angesichts der bekannten vasomodulatorischen Wirkungen von Isofluran25 verändern.- Induzieren Sie mit 4,5% Isofluran in 100% Sauerstoff für 45 Sekunden und halten Sie dann mit 1,0-1,75% Isofluran in 100% Sauerstoff. Bestätigen Sie eine ausreichende Tiefe der Anästhesie durch das Fehlen einer Zehenklemmreaktion und einer normalen Atmung (zwischen ~ 60-80 Atemzügen pro Minute).
- Nach einer 2-minütigen Stabilisierungsphase legen Sie den DCS-Sensor vorsichtig über die rechte Hemisphäre, so dass sich die obere Kante des optischen Sensors mit dem Augenhintergrund ausrichtet und die Seite des Sensors entlang der Mittellinie ausgerichtet ist (Abbildung 3). Bechern Sie eine Hand über den Sensor, um sich vor Raumlicht abzuschirmen. Erfassen Sie 5 Sekunden Daten (1 Hz Erfassung).
- Positionieren Sie den Sensor über der linken Hemisphäre neu und erfassen Sie 5 Sekunden Daten.
- Wiederholen Sie 3 mal / Hemisphäre, um lokale Heterogenitäten unter der Gewebeoberfläche zu berücksichtigen.
- Genesung
- Entfernen Sie die Maus aus der Narkose und legen Sie sie auf ein wärmendes Pad.
- Nachdem die Maus ihren Aufrichtungsreflex wiedererlangt hat, bringt sie sie zurück in den Käfig.
- Entfernen Sie Haare auf der Kopfhaut. Da DCS am besten in Abwesenheit von Haaren funktioniert, ist es notwendig, Fell auf dem Kopf vor Beginn der Experimente zu entfernen. Typischerweise wird die Haarentfernung 1-3 Tage vor Beginn der Studie durchgeführt.
- DCS-Datenanalyse
- Führen Sie eine anfängliche Qualitätskontrolle durch. Jeder Frame von DCS-Daten besteht aus einer gemessenen normalisierten Intensitätsautokorrelationsfunktion
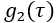 (Abbildung 4A) und einer Photonenzählrate (kHz).
(Abbildung 4A) und einer Photonenzählrate (kHz).- Um Datenrahmen mit signifikantem Bewegungsartefakt zu entfernen, verwerfen Sie Datenrahmen,
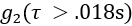 bei denen der Mittelwert des Hecks der
bei denen der Mittelwert des Hecks der 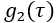 Kurve (d. h. ) > 1,005 beträgt.
Kurve (d. h. ) > 1,005 beträgt. - Um Datenrahmen mit schlechtem Signal-Rausch-Verhältnis zu entfernen, verwerfen Sie Datenrahmen, wenn die erkannte Photonenzählrate < 20 kHz liegt.
- Um Datenrahmen mit signifikantem Bewegungsartefakt zu entfernen, verwerfen Sie Datenrahmen,
- Extrahieren Sie den zerebralen Blutflussindex. Verwenden Sie fminsearch in Matlab, passen Sie jeden iten gemessenen Datenrahmen
 für CBF i(i) an. Beschränken Sie Anpassungen auf
für CBF i(i) an. Beschränken Sie Anpassungen auf 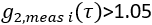 , und suchen Sie den Wert von CBFi , der die folgende Kostenfunktion minimiert:
, und suchen Sie den Wert von CBFi , der die folgende Kostenfunktion minimiert: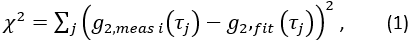
Dabei ist die Summe über alle gemessenen Verzögerungszeiten und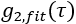 ist die halbunendliche homogene Lösung der Korrelationsdiffusionsgleichung (Abbildung 4B):
ist die halbunendliche homogene Lösung der Korrelationsdiffusionsgleichung (Abbildung 4B):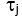
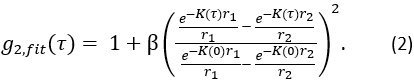
Hier ist β ein Kohärenzfaktor, der durch den Versuchsaufbau bestimmt wird, , , , ,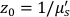
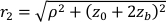 , , Reff = 0,493 für einen angenommenen Gewebebrechungsindex von 1,4, ρ ist 6 mm, und μa und μ sind die Absorption und der reduzierte Streukoeffizient des Gewebes (angenommen auf 0,25 bzw. 9,4/cm bzw. 10,26,27).
, , Reff = 0,493 für einen angenommenen Gewebebrechungsindex von 1,4, ρ ist 6 mm, und μa und μ sind die Absorption und der reduzierte Streukoeffizient des Gewebes (angenommen auf 0,25 bzw. 9,4/cm bzw. 10,26,27). 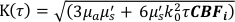
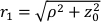
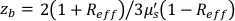
HINWEIS: Da β im Laufe der Zeit um ~ 10% variieren können, passen Sie jeden Datenrahmen für β und CBFi gleichzeitig an. - Führen Sie eine sekundäre Qualitätskontrolle durch. Verwerfen Sie innerhalb jeder Wiederholung (die aus 5 Datenrahmen besteht) Ausreißer. Ausreißer sind definiert als diejenigen CBF i-Werte, die außerhalb von 1,5 Standardabweichungen des mittleren CBFi für diese Wiederholung liegen. Wenn mehr als 1 Datenpunkt als Ausreißer identifiziert wird, verwerfen Sie die gesamte Wiederholung.
- Schätzung des durchschnittlichen zerebralen Blutflussindex: Schätzen Sie einen durchschnittlichen KBFi pro Hemisphäre, indem Sie den Mittelwert über alle Datenrahmen für alle Wiederholungen nehmen (Abbildung 4C). Wenn keine signifikanten hemisphärischen Unterschiede beobachtet werden, führen Sie einen Durchschnitt über die Hemisphären durch, um eine Schätzung des durchschnittlichen globalen CBFi zu erhalten.
- Führen Sie eine anfängliche Qualitätskontrolle durch. Jeder Frame von DCS-Daten besteht aus einer gemessenen normalisierten Intensitätsautokorrelationsfunktion
3. Multiplexe Quantifizierung von Zytokinen und Phospho-Proteinen mittels Luminex-Assays
- Gewebeextraktion
HINWEIS: Die Quantifizierung von Hirnzytokinen und Phospho-Signalproteinen mit Luminex erfordert eine Gewebeextraktion.- Anästhesieren Sie die Maus mit 4,5% Isofluran in 100% Sauerstoff für 1-2 min. Überprüfen Sie auf eine tiefe Anästhesieebene über das Fehlen einer Zehenklemmreaktion. Euthanasie durch Enthauptung.
- Ernten Sie das Gewebe.
- Entfernen Sie das Gehirn. Fixieren Sie typischerweise die linke Hemisphäre für die Histologie und analysieren Sie mehrere Regionen aus der rechten Hemisphäre innerhalb des Kortex und des Hippocampus (Abbildung 5).
- Legen Sie sezierte Proben in Mikrozentrifugenröhrchen, schockgefrieren Sie in flüssigem Stickstoff. Für die Analyse von gefrierempfindlichen Proteinen ist es optimal, Gewebeabschnitte vor dem Einfrieren des Schocks zu unterteilen, um ein späteres Auftauen zu vermeiden.
HINWEIS: Das Protokoll kann pausiert werden, und Gewebeproben können bei -80 ° C gelagert werden, bis die Proben lysiert werden können. Alternativ können Proben lysiert und dann bei -80 °C gelagert werden.
- Lyse-Proben.
- Bereiten Sie den Lysepuffer vor, indem Sie dem Lysepuffer Proteaseinhibitor und 2 mM Phenylmethylsulfonylfluorid hinzufügen.
- Fügen Sie 150 μL des gemischten Lysepuffers pro etwa 3 μg tierisches Gewebe hinzu. Als Referenz sind die visuellen Kortexgewebeproben der Maus ungefähr 3 μg.
- Um das Gewebe zu homogenisieren, tribrieren Sie das Gewebe mechanisch, indem Sie ~ 15-20 Mal mit einer 1000 μL-Pipette nach oben und unten pipettieren. Für eine optimale Probenverreibung kann ein Homogenisatorstößel verwendet werden.
- Legen Sie die Probenröhrchen für 30 min bei 4°C auf einen Rotator.
- Die Proben zentrifugieren Sie bei 4 °C für 10 min bei ca. 15.000 x g und sammeln Sie den Überstand. Die Proben können sofort verarbeitet oder zur weiteren Analyse bei -80 °C gelagert werden.
HINWEIS: Die mit diesem Protokoll hergestellten Probenlysate sind mit Western Blot kompatibel, aus dem der Phagozyten-/Mikrogliamarker Iba1 und/oder der Astrozytenaktivierungsmarker GFAP analysiert werden können, um die Zytokin- und Phosphoproteinanalyse für Neuroinflammationsstudienzu ergänzen 11.
- Multiplex-Immuno-Assay-Protokoll für Zytokine und Phospho-Proteine
HINWEIS: Obwohl insgesamt ähnlich, gibt es einige geringfügige Unterschiede in den Protokollen für Zytokin- und Phospho-Protein-Kits. Unterschiede werden in jedem Schritt notiert. Die Schritte zur Vorbereitung der Proben für den Luminex-Assay werden im Folgenden beschrieben.- Herstellung von Reagenzien (Tag 1, gleiches für Zytokine und Phospho-Proteine)
- Lassen Sie die Reagenzien auf Raumtemperatur (~ 30 min) erwärmen.
- Ultraschall-Multiplex-Magnetperlenflasche für 30 Sekunden, gefolgt von 1 Minute Wirbelung. Stellen Sie sicher, dass die magnetischen Multiplexperlen mit Aluminiumfolie vor Licht geschützt sind, oder verwenden Sie die mitgelieferten Lichtschutzflaschen.
- Bereiten Sie den Waschpuffer vor, indem Sie 0,1% Tween20 in 1xPBS mischen oder alternativ den im Kit enthaltenen Waschpuffer verwenden.
- Präparation von lysierten Gewebeproben (Tag 1, gleiches für Zytokine und Phospho-Proteine)
- Wenn zuvor gefroren, entfernen Sie lysierte Gewebeproben aus dem Gefrierschrank und lassen Sie sie auf Eis auftauen (~ 20 min). Zentrifugenproben für 10 min bei 9.167 x g, um Niederschlag zu entfernen.
- Es werden 25 μL Probe bei der optimalen Proteinkonzentration hergestellt, die durch die lineare Bereichsanalyse bestimmt wird (siehe Abschnitt 3.3). Um das Gesamtvolumen für alle Proben zu normalisieren, verdünnen Sie die Proben im Assay-Puffer, der im Kit enthalten ist.
- Herstellung von 96 Well Plate (Tag 1, gleiches für Zytokine und Phospho-Proteine)
- Verwenden Sie die im Kit enthaltene 96-Well-Platte oder eine mit einem dünnen Boden (z. B. Brand Tech).
- Geben Sie 200 μL Waschpuffer (oder 1x PBS, 0,1% Tween) in jede Vertiefung und mischen Sie auf Plattenschüttler für 10 min bei 750 U / min.
- Dekant Waschpuffer und klopfen Sie die Platte auf ein Papiertuch, um Rückstände zu entfernen.
- Immunoassay-Verfahren für Zytokine (Tag 1)
- Fügen Sie jedem Bohrloch in der richtigen Reihenfolge Folgendes hinzu.
- Fügen Sie allen Vertiefungen 25 μL Assay-Puffer hinzu.
- Fügen Sie 25 μL zusätzlichen Assay-Puffer NUR zu Hintergrundvertiefungen hinzu. Für jeden Versuchslauf haben Sie mindestens zwei Hintergrundbrunnen. Hintergrundvertiefungen haben keine geladene Probe und definieren die Fluoreszenzintensität, die vom Gerät ohne Probe abgelesen wird.
- 25 μL jeder verdünnten Probe zu den entsprechenden Probenvertiefungen hinzufügen.
- Fügen Sie allen Vertiefungen 25 μL 1x magnetische Multiplexperlen hinzu (Abbildung 6). Achten Sie darauf, die Perlen für 1 Minute zu wirbeln, bevor Sie zu den Brunnen hinzufügen.
- Fügen Sie allen Vertiefungen 25 μL Assay-Puffer hinzu.
- Dichtplatte mit Plattenversiegelung abdichten und die Platte mit Aluminiumfolie abdecken. Über Nacht (12-16 h) bei 2-8 °C inkubieren.
- Fügen Sie jedem Bohrloch in der richtigen Reihenfolge Folgendes hinzu.
- Immunoassay-Verfahren für Zytokine (Tag 2)
- Platzieren Sie die 96-Well-Platte auf dem Magnetabscheider und stellen Sie sicher, dass die Wells mit den Magneten ausgerichtet sind. 2 min ruhen lassen. Dekantieren Sie den Brunneninhalt, während die Platte noch am Magnetabscheider befestigt ist.
- Waschen Sie die Platte 2 Mal mit den folgenden Schritten.
- Fügen Sie 200 μL Waschpuffer zu jeder Vertiefung hinzu und legen Sie sie für 2 Minuten bei Raumtemperatur auf den Shaker.
- Legen Sie die Vertiefungsplatte für 2 min bei Raumtemperatur auf den Magnetabscheider.
- Dekantieren Sie den Bohrlochgehalt, während die Wellplatte noch am Magnetabscheider befestigt ist.
- Fügen Sie 25 μL Nachweisantikörper pro Vertiefung hinzu (Abbildung 6). Mit Folie abdecken. 1 Stunde auf einem Plattenschüttler (750 U/min) bei Raumtemperatur inkubieren.
- Lassen Sie den Nachweisantikörper drin und fügen Sie 25 μL Streptavidin-Phycoerythrin (SAPE) in jede Vertiefung (Abbildung 6) hinzu (Abbildung 6). Mit Folie abdecken. Inkubieren Sie für 30 min auf Plattenschüttler (750 U / min) bei Raumtemperatur.
- Die Wellplatte auf einen Magnetabscheider legen und 2 min einwirken lassen. Bohrlochinhalt dekantieren und vom Magnetabscheider lösen.
- Well-Platte zweimal waschen (siehe Schritt 3.2.5.2).
- Fügen Sie 75 μL Luminex Drive Fluid (bei Verwendung eines MAGPIX-Instruments) zu jedem Bohrloch- oder Assay-Puffer hinzu (bei Verwendung von 200- oder FlexMap-3D-Instrumenten). Suspendieren Sie die Perlen auf dem Plattenschüttler für 5 Minuten bei Raumtemperatur erneut.
- Lesen Sie weiter Luminex Instrument (MAGPIX, 200 oder FlexMap 3D) und beziehen Sie sich auf das Benutzerhandbuch für eine ordnungsgemäße Bedienung (Abbildung 6).
- Immunoassay-Verfahren für Phospho-Proteine (Tag 1)
- Fügen Sie jedem Bohrloch in der richtigen Reihenfolge Folgendes hinzu.
- Fügen Sie allen Vertiefungen 25 μL Assay-Puffer hinzu.
- Fügen Sie 25 μL zusätzlichen Assay-Puffer NUR zu Hintergrundvertiefungen hinzu. Für jeden Versuchslauf wird empfohlen, mindestens zwei Hintergrundbohrungen zu haben. Hintergrundvertiefungen haben keine geladene Probe und definieren die Fluoreszenzintensität, die vom Gerät ohne Probe abgelesen wird.
- Fügen Sie 25 μL jeder verdünnten Probe zu jeder Probenvertiefung hinzu.
- Fügen Sie allen Vertiefungen 25 μL 1x magnetische Multiplexperlen hinzu (Abbildung 6).
HINWEIS: Das Luminex-Assay-Kit bietet Multiplex-Magnetperlen in 20-facher Standardlösung. Stellen Sie sicher, dass Sie 20x Stock Multiplex-Magnetperlenlösung für 2 min vortexen und dann im Assay-Puffer auf 1x Lösung verdünnen. Vortex 1x Multiplex-Magnetperlensuspension für 1 Minute, bevor er zu Bohrlöchern hinzugefügt wird.
- Dichtplatte mit Plattenversiegelung abdichten und die Platte mit Aluminiumfolie abdecken. Inkubieren über Nacht (12-16 Stunden) bei 2-8 °C.
- Fügen Sie allen Vertiefungen 25 μL Assay-Puffer hinzu.
- Fügen Sie jedem Bohrloch in der richtigen Reihenfolge Folgendes hinzu.
- Immunoassay-Verfahren für Phospho-Proteine (Tag 2)
- Legen Sie die Bohrlochplatte auf einen Magnetabscheider und stellen Sie sicher, dass die Vertiefungsplatte vollständig mit dem Magnetabscheider ausgerichtet ist. 2 min ruhen lassen. Dekantieren Sie den Bohrlochinhalt, während die Bohrlochplatte noch am Magnetabscheider befestigt ist.
- Waschen Sie die Platte 2 Mal (siehe Schritt b im Immunoassay-Verfahren des Zytokins Tag 2).
- Verdünnen Sie den 20-fachen Stammdetektionsantikörper zu 1x-Lösung im Assay-Puffer. Fügen Sie 25 μL 1x Nachweisantikörper pro Vertiefung hinzu (Abbildung 6). Mit Folie abdecken. 1 h auf Plattenschüttler (750 U/min) bei Raumtemperatur inkubieren.
- Legen Sie die 96-Well-Platte auf den Magnetabscheider und lassen Sie sie 2 min einwirken. Dekanten Sie den Inhalt der Vertiefung, lösen Sie sich vom Magnetabscheider.
- Verdünnen Sie 25x Lager-SAPE im Assay-Puffer auf 1x Puffer. Fügen Sie 25 μL 1x SAPE hinzu (Abbildung 6). Mit Folie abdecken und 15 min auf Plattenschüttler (750 U/min) bei Raumtemperatur inkubieren.
- Lassen Sie die SAPE in den Vertiefungen und fügen Sie 25 μL Verstärkungspuffer zu jeder Vertiefung hinzu. Mit Folie abdecken.
- 15 min auf Plattenschüttler (750 U/min) bei Raumtemperatur inkubieren.
- Legen Sie die Wellplatte für 2 min auf den Magnetabscheider. Bohrlochinhalt dekantieren und vom Magnetabscheider lösen.
- Fügen Sie 75 μL Luminex Drive Fluid (bei Verwendung eines MAGPIX-Instruments) oder Assay-Puffer (bei Verwendung eines 200- oder FlexMap 3D-Instruments) hinzu. Suspendieren Sie die Perlen für 5 Minuten bei Raumtemperatur auf einem Plattenschüttler.
- Lesen Sie mehr über das Luminex-Instrument (MAGPIX, 200 oder FlexMap 3D) und beziehen Sie sich auf das Benutzerhandbuch für eine ordnungsgemäße Bedienung (Abbildung 6).
- Herstellung von Reagenzien (Tag 1, gleiches für Zytokine und Phospho-Proteine)
- Linearität der Probenverdünnungskurve
- Probenvorbereitung: Seriell verdünnte Testproben mit unterschiedlicher Konzentration des Gesamtproteins. Für Bulk-Hirngewebe laden Sie serielle Verdünnungen von 0-25 μg für Zytokine und 0-12 μg für Phospho-Proteine. Die Gesamtproteinkonzentration kann mit dem Bicchininsäure-Assay (BCA) gemessen werden.
- Multiplex-Immunoassay: Führen Sie den Luminex-Assay (siehe Abschnitt 3.2) an ausgewählten Proben durch.
- Datenanalyse
- Zeichnen Sie die Fluoreszenzintensität für jedes Protein im Vergleich zur Menge des geladenen Proteins auf (Abbildung 7).
- Identifizieren Sie für jeden Analyten den Bereich des Gesamtproteins, bei dem die Beziehung zwischen dem Gesamtprotein und der Fluoreszenzintensitätsanzeige linear ist (Abbildung 7).
- Um die Menge des Gesamtproteins zu bestimmen, die für den vollständigen Assay-Lauf geladen werden sollte, identifizieren Sie den linearen Teil der Kurve für jeden Analyten und wählen Sie dann eine Proteinkonzentration aus, die für die Mehrheit der Analyten in den linearen Bereich fällt.
HINWEIS: Obwohl die meisten Proteine einen ähnlichen linearen Bereich teilen, überlappen sich die linearen Bereiche möglicherweise nicht für alle Proteine. Wenn dies der Fall ist, kann es notwendig sein, jede Probe mehrmals mit unterschiedlichen Mengen an Gesamtprotein zu betreiben. Alternativ können nichtlineare Proben aus der Analyse ausgeschlossen werden. Darüber hinaus haben einige Proteine möglicherweise überhaupt keinen linearen Bereich.
4. Partielle Regression der kleinsten Quadrate
HINWEIS: Beispiel-R-Code und eine Beispieldatentabelle werden bereitgestellt, um die partielle Analyse der kleinsten Quadrate durchzuführen.
- Datenaufbereitung: Formatieren Sie die Daten wie in der bereitgestellten Beispieldatentabelle "MyData" gezeigt. Fügen Sie Variablennamen in Zeile 1, Beispielnamen in Spalte A, die Antwortvariable in Spalte B und alle Prädiktorvariablen in Spalte C+ ein. Füllen Sie die letzten beiden Zeilen mit den Hintergrunddaten, und legen Sie beide Beispielnamen auf "Hintergrund" fest.
- Partielle Regression der kleinsten Quadrate in RStudio
- Installieren Sie R von www.r-project.org (kostenlos, Open Source).
- Installieren Sie RStudio Desktop von www.rstudio.com (kostenlose Open-Source-Lizenz).
- Laden Sie den mit dieser Publikation bereitgestellten R-Beispielcode "PLSR_Sample_Code.R" herunter, und speichern Sie ihn in demselben Ordner, der die Datenkalkulationstabelle enthält. Öffnen Sie die Codedatei in RStudio.
- Ändern Sie im Abschnitt Benutzereingabe "dataFileName" in den Namen der Datentabelle.
- Führen Sie die folgenden Schritte aus, indem Sie den auszuführenden Codeabschnitt markieren und in der oberen rechten Ecke des Skripts auf Ausführen klicken.
- Laden Sie notwendige R-Pakete, Funktionen, die Arbeitsverzeichnisadresse und Benutzereingabewerte in RStudio (Unterabschnitt "Preliminaries").
- Laden Sie die Daten in RStudio und bereiten Sie die Rohdaten für die Verarbeitung vor, indem Sie das mittlere Hintergrundsignal von allen Messungen subtrahieren und jeden Analyten z-Scoring durchführen (Unterabschnitt "Daten lesen und Hintergrund subtrahieren")(Abbildung 8A).
- Führen Sie eine partielle Regression der kleinsten Quadrate in RStudio mit dem plsRglm-Paket v1.2.528 durch, das im Comprehensive R Archive Network (CRAN) verfügbar ist. Führen Sie eine Varimax-Rotation (Statistikpaket v3.6.2)23 in der LV1-LV2-Ebene durch, um eine neue horizontale Achse zu identifizieren, die die Stichproben am besten nach der Antwortvariablen trennt (Unterabschnitt "PLS")(Abbildung 8B).
- Führen Sie eine Leave One Out Cross Validation (LOOCV) durch, bei der eine Stichprobe iterativ aus den Daten ausgelassen wird und das PLSR-Modell neu berechnet wird. Berechnen Sie die Standardabweichung für Analytladungen über alle LOOCV-Läufe (Unterabschnitt "LOOCV").
- Repräsentative Plots erstellen: Führen Sie den bereitgestellten Beispielcode wie oben beschrieben aus, um repräsentative Plots zu erstellen, die automatisch als PDF-Dateien in das Arbeitsverzeichnis (den Ordner, der die Daten und Codedateien enthält) exportiert werden.
- Erstellen Sie eine Heatmap der verarbeiteten Daten, wie in Abbildung 8A (Unterabschnitt "PLS") dargestellt. Färben Sie jeden Eintrag entlang eines durch den Z-Score definierten Spektrums. Sortieren Sie Analyten nach der Reihenfolge, die in der latenten Variablen von Interesse berechnet wurde.
- Erstellen Sie ein Punktediagramm mit LV1-Punkten, die entlang der horizontalen Achse und LV2-Punktzahlen entlang der vertikalen Achse dargestellt werden, wie in Abbildung 8B (Unterabschnitt "PLS") dargestellt. Färben Sie jeden Datenpunkt entsprechend seiner Messung der Antwortvariablen, um die Beziehung zwischen jeder latenten Variablen und der Antwortvariablen zu visualisieren.
- Erstellen Sie ein Balkendiagramm mit Ladevorgängen für jede Ihrer Prädiktorvariablen, um zu visualisieren, wie jeder Analyt zu den latenten Variablen beiträgt, wie in Abbildung 8C (Unterabschnitt "LOOCV") dargestellt.
- Erstellen Sie ein Diagramm, das die LV1-Werte gegen Ihre Antwortvariable regressiert, um zu visualisieren, wie gut das PLSR-Modell die Stichproben trennt, wie in Abbildung 8D (Unterabschnitt "PLS") gezeigt.
Ergebnisse
Zuvor gesammelte Daten stammen aus früheren Arbeiten, bei denen eine Gruppe von acht C57BL/6-Mäusen drei Verletzungen mit geschlossenem Kopf (Abbildung 2) im Abstand von einmal täglich11 ausgesetzt war. In dieser Arbeit wurde der zerebrale Blutfluss mit diffuser Korrelationsspektroskopie 4 h nach der letzten Verletzung gemessen (Abbildung 3, Abbildung 4). Nach der CBF-Beurteilung nach der Verletzung wurden...
Diskussion
Hierin beschreiben wir Methoden zur Beurteilung der hämodynamischen und neuroinflammatorischen Reaktion auf wiederholte leichte traumatische Hirnverletzungen. Darüber hinaus haben wir gezeigt, wie diese Daten im Rahmen einer multivariaten Systemanalyse mit partieller Regression der kleinsten Quadrate integriert werden können. Im folgenden Text werden wir einige der wichtigsten Schritte und Einschränkungen im Zusammenhang mit dem Protokoll sowie die Vor- und Nachteile der Methoden gegenüber bestehenden Methoden disku...
Offenlegungen
Nichts.
Danksagungen
Dieses Projekt wurde durch die National Institutes of Health R21 NS104801 (EMB) und R01 NS115994 (LBW/EB) sowie den Children's Healthcare of Atlanta Junior Faculty Focused Award (EMB) unterstützt. Diese Arbeit wurde auch vom US-Verteidigungsministerium durch die Congressionally Directed Medical Research Programs unter der Award-Nr. W81XWH-18-1-0669 (LBW/EMB). Meinungen, Interpretationen, Schlussfolgerungen und Empfehlungen sind die des Autors und werden nicht unbedingt vom Verteidigungsministerium unterstützt. Dieses Material basiert auf Arbeiten, die vom National Science Foundation Graduate Research Fellowship Program unter Grant No. 1937971 unterstützt werden. Alle Meinungen, Ergebnisse und Schlussfolgerungen oder Empfehlungen, die in diesem Material zum Ausdruck gebracht werden, sind die der Autoren und spiegeln nicht unbedingt die Ansichten der National Science Foundation wider.
Materialien
| Name | Company | Catalog Number | Comments |
| Adjustable pipettes | any adjustable pipette | ||
| Aluminum foil | VWR | 89107-726 | |
| Bio-Plex cell lysis kit | C Bio-Rad | 171304012 | |
| BRAND BRANDplates pureGrade Microplates, Nonsterile | BrandTech | 781602 96 | |
| Complete mini protease inhibitor tablet | Sigma-Aldrich | 11836153001 | |
| Depilatory cream | Amazon | Nair | |
| DiH2O | VWR | VWRL0200-1000 | |
| Handheld magnetic separator block for 96 well flat bottom plates | Millipore Sigma Catalogue | 40-285 | |
| Hardware Autocorrelator Board | www.correlator.com | Flex05-8ch | |
| Isoflurane 250 mL | MED-VET INTERNATIONAL | RXISO-250 | |
| Kimwipe (11.2 x 21.3 cm) | VWR | 21905-026 | |
| Laboratory vortex mixer | VWR | 10153-838 | |
| LabView | National Instruments | LabVIEW | |
| Luminex 200, HTS, FLEXMAP 3D, or MAGPIX with xPONENT software | Luminex Corporation | ||
| Luminex Drive Fluid | Luminex | MPXDF-4PK | |
| Luminex sheath fluid | EMD Millipore | SHEATHFLUID | |
| MILLIPLEX MAP Mouse Cytokine/Chemokine Magnetic Bead Panel - Premixed 32 Plex - Immunology Multiplex Assay | Millipore Sigma | MCYTMAG-70K-PX32 | |
| MILLIPLEX MAPK/SAPK Signaling 10-Plex Kit-Cell Signaling Multiplex Assay | Millipore Sigma | 48-660MAG | |
| Mini LabRoller rotator | VWR | 10136-084 | |
| Phenylmethylsulfonyl fluoride | Sigma-Aldrich | P7626-1G | |
| Phosphate-buffered Saline (PBS) | VWR | 97064-158 | |
| Plate Sealer | VWR | 82050-992 | |
| Polypropylene microfuge tubes | VWR | 20901-547 | |
| Mini LabRoller | Millipore Sigma | Z674591 | |
| Reagent Reservoirs | VWR | 89094-668 | |
| R Programming Language | |||
| RStudio | www.rstudio.com | ||
| Sonicator | |||
| Titer plate shaker | VWR | 12620-926 | |
| Tween20 | Sigma-Aldrich | P9416-50ML | |
| 1 m acrylic guide tube | McMaster-Carr | 49035K85 | |
| 4 photon counting avalanche photodiode | Perkin-Elmer | SPCM-AQ4C-IO | |
| 400 um multimode source fiber | Thorlabs Inc. | FT-400-EMT | |
| 54 g bolt | Ace Hardware | 0.95 cm basic body diameter, 2 cm head diameter, 10.2 cm length | |
| 780 nm single mode detector fiber | Thorlabs Inc. | 780HP | |
| 852 nm long-coherence length laser | TOPTICA Photonics | iBeam smart |
Referenzen
- Langlois, J. A., Rutland-Brown, W., Wald, M. M. The epidemiology and impact of traumatic brain injury: a brief overview. Journal of Head Trauma Rehabilitation. 21 (5), 375-378 (2006).
- Iraji, A., et al. Resting State Functional Connectivity in Mild Traumatic Brain Injury at the Acute Stage: Independent Component and Seed-Based Analyses. Journal of Neurotrauma. 32 (14), 1031-1045 (2015).
- Guskiewicz, K. M., et al. Cumulative effects associated with recurrent concussion in collegiate football players: the NCAA Concussion Study. Journal of the American Medical Association. 290 (19), 2549-2555 (2003).
- Longhi, L., et al. Temporal window of vulnerability to repetitive experimental concussive brain injury. Neurosurgery. 56 (2), 364-374 (2005).
- Committee on Sports-Related Concussions in Youth, Board on Children, Youth, and Families, Institute of Medicine, National Research Council. . Sports-Related Concussions in Youth: Improving the Science, Changing the Culture. , (2014).
- Barkhoudarian, G., Hovda, D. A., Giza, C. C. The Molecular Pathophysiology of Concussive Brain Injury - an Update. Physical Medicine and Rehabilitation Clinics of North America. 27 (2), 373-393 (2016).
- McCrory, P., et al. Consensus statement on concussion in sport--the 4th International Conference on Concussion in Sport held in Zurich, November 2012. Clinical Journal of Sport Medicine. 23 (2), 89-117 (2012).
- Belanger, H. G., Vanderploeg, R. D., Curtiss, G., Warden, D. L. Recent neuroimaging techniques in mild traumatic brain injury. Journal of Neuropsychiatry and Clinical Neurosciences. 19 (1), 5-20 (2007).
- Sours, C., Zhuo, J., Roys, S., Shanmuganathan, K., Gullapalli, R. P. Disruptions in Resting State Functional Connectivity and Cerebral Blood Flow in Mild Traumatic Brain Injury Patients. PLoS ONE. 10 (8), 0134019 (2015).
- Buckley, E. M., et al. Decreased Microvascular Cerebral Blood Flow Assessed by Diffuse Correlation Spectroscopy after Repetitive Concussions in Mice. Journal of Cerebral Blood Flow & Metabolism. 35 (12), 1995-2000 (2015).
- Sankar, S. B., et al. Low cerebral blood flow is a non-invasive biomarker of neuroinflammation after repetitive mild traumatic brain injury. Neurobiology of Disease. 124, 544-554 (2019).
- Vagnozzi, R., et al. Temporal window of metabolic brain vulnerability to concussions: mitochondrial-related impairment--part I. Neurosurgery. 61, 379-388 (2007).
- Longhi, L., et al. Temporal window of vulnerability to repetitive experimental concussive brain injury. Neurosurgery. 56, 364-374 (2005).
- Fujita, M., Wei, E. P., Povlishock, J. T. Intensity- and interval-specific repetitive traumatic brain injury can evoke both axonal and microvascular damage. Journal of Neurotrauma. 29, 2172-2180 (2012).
- Angoa-Perez, M., et al. Animal models of sports-related head injury: bridging the gap between preclinical research and clinical reality. Journal of Neurochemistry. 129, 916-931 (2014).
- Prins, M. L., Hales, A., Reger, M., Giza, C. C., Hovda, D. A. Repeat traumatic brain injury in the juvenile rat is associated with increased axonal injury and cognitive impairments. Developmental Neuroscience. 32, 510-518 (2010).
- Viano, D. C., Hamberger, A., Bolouri, H., Saljo, A. Concussion in professional football: animal model of brain injury--part 15. Neurosurgery. 64, 1162-1173 (2009).
- Kane, M. J., et al. A mouse model of human repetitive mild traumatic brain injury. Journal of Neuroscience Methods. 203, 41-49 (2012).
- Meehan, W. P., Zhang, J., Mannix, R., Whalen, M. J. Increasing Recovery Time Between Injuries Improves Cognitive Outcome After Repetitive Mild Concussive Brain Injuries in Mice. Neurosurgery. 71 (4), 885-892 (2012).
- Durduran, T., Yodh, A. G. Diffuse correlation spectroscopy for non-invasive, micro-vascular cerebral blood flow measurement. NeuroImage. 85, 51-63 (2014).
- Sathialingam, E., et al. Small separation diffuse correlation spectroscopy for measurement of cerebral blood flow in rodents. Biomedical Optics Express. 9 (11), 5719 (2018).
- Lee, S. Y., et al. Noninvasive optical assessment of resting-state cerebral blood flow in children with sickle cell disease. Neurophotonics. 6 (03), 1 (2019).
- Wang, H., Liu, Q., Tu, Y. Interpretation of partial least-squares regression models with VARIMAX rotation. Partial Least Squares. 48 (1), 207-219 (2005).
- Eriksson, L., Byrne, T., Johansson, E., Trygg, J., Vikström, C. Multi- and Megavariate Data Analysis Basic Principles and Applications. Umetrics Academy. , (2013).
- Conzen, P. F., et al. Systemic and regional hemodynamics of isoflurane and sevoflurane in rats. Anesthesia and Analgesia. 74 (1), 79-88 (1992).
- Durduran, T., Choe, R., Baker, W. B., Yodh, A. G. Diffuse optics for tissue monitoring and tomography. Reports on Progress in Physics. 73 (7), 076701 (2010).
- Lee, S. Y., et al. Small separation frequency-domain near-infrared spectroscopy for the recovery of tissue optical properties at millimeter depths. Biomedical Optics Express. 10 (10), 5362-5377 (2019).
- . plsRglm: Partial Least Squares Regression for Generalized Linear Models Available from: https://CRAN.R-project.org/package=pplsRglm (2019)
- White, B. R., Bauer, A. Q., Snyder, A. Z., Schlaggar, B. L., Lee, J. M., Culver, J. P. Imaging of functional connectivity in the mouse brain. PLoS One. 6, 16322 (2011).
- Buckley, E. M., Parthasarathy, A. B., Grant, P. E., Yodh, A. G., Franceschini, M. A. Diffuse correlation spectroscopy for measurement of cerebral blood flow: future prospects. Neurophotonics. 1 (1), 011009 (2014).
- Rowan, O., et al. Cerebrovascular reactivity measured in awake mice using diffuse correlation spectroscopy. Neurophotonics. 8 (1), (2021).
- Tate, J., Ward, G. Interferences in immunoassay. The Clinical Biochemist. Reviews. 25 (2), 105-120 (2004).
- Staples, E., Ingram, R. J. M., Atherton, J. C., Robinson, K. Optimising the quantification of cytokines present at low concentrations in small human mucosal tissue samples using Luminex assays. Journal of Immunological Methods. 394 (1-2), 1-9 (2013).
- Gierut, J. J., et al. Network-level effects of kinase inhibitors modulate TNF-α-induced apoptosis in the intestinal epithelium. Science Signaling. 8 (407), 129 (2015).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten