Method Article
Eine Proteinsuspensions-Trapping-Probenvorbereitung für die Tränenproteomik mittels Flüssigkeitschromatographie-Tandem-Massenspektrometrie
* Diese Autoren haben gleichermaßen beigetragen
In diesem Artikel
Zusammenfassung
Dieses Protokoll beschreibt eine Methode zur Entnahme von Tränenproben unter Verwendung von Schirmer-Streifen und einen integrierten quantitativen Workflow zur Entdeckung nicht-invasiver Tränenprotein-Biomarker. Der Arbeitsablauf für die Probenvorbereitung ermöglicht eine schnelle und robuste Vorbereitung von Tränenproben und massenspektrometrische Analysen, was zu einer höheren Ausbeute an Peptidrückgewinnung und Proteinidentifikation führt als bei Standardverfahren in Lösung.
Zusammenfassung
Tränenflüssigkeit gehört zu den leicht zugänglichen Bioflüssigkeiten, die nicht-invasiv gesammelt werden können. Die Tränenproteomik hat das Potenzial, Biomarker für verschiedene Augenerkrankungen und -zustände zu entdecken. Es wurde berichtet, dass die Suspensions-Trapping-Säule ein effizienter und benutzerfreundlicher Arbeitsablauf für die Probenvorbereitung für die breite Anwendung der nachgeschalteten Proteomanalyse ist. Diese Strategie ist jedoch bei der Analyse des menschlichen Tränenproteoms nicht gut untersucht. Das vorliegende Protokoll beschreibt einen integrierten Arbeitsablauf von klinischen menschlichen Tränenproben bis hin zu gereinigten Peptiden für die nicht-invasive Tränenprotein-Biomarker-Forschung mittels Massenspektrometrie, die in Kombination mit bioinformatischer Analyse Einblicke in Krankheitsbiomarker und -überwachung bietet. Eine Proteinsuspensions-Trapping-Probenvorbereitung wurde angewendet und demonstrierte die Entdeckung des Tränenproteoms mit schnellen, reproduzierbaren und benutzerfreundlichen Verfahren als universelle, optimierte Probenvorbereitung für die Analyse menschlicher Tränenflüssigkeit. Insbesondere übertraf das Suspensionsauffangverfahren die Probenvorbereitung in Lösung in Bezug auf die Peptidrückgewinnung, die Proteinidentifikation und die kürzere Probenvorbereitungszeit.
Einleitung
Die Tränenproteomik hat Aufmerksamkeit erhalten, um potenzielle Biomarker für Augenerkrankungen und -zustände 1,2,3,4,5,6 zu erforschen, die Pathogenese der okulären und systemischen Erkrankung zu erforschen und den Vorteil der nicht-invasiven Tränenprobenentnahme mit Schirmer-Streifen zu nutzen. Der technologische Fortschritt der Massenspektrometrie der nächsten Generation hat die Quantifizierung von Proteinen in Tränen im Mikroliterbereich mit einer Genauigkeit und Präzision ermöglicht, die in der Vergangenheit nicht möglich war. Die Methoden der Probenvorbereitung sind noch nicht standardisiert. Ein robuster und standardisierter Workflow für die Probenvorbereitung ist für den Erfolg der klinischen Anwendung in der Tränenprotein-Biomarker-Forschung unerlässlich. Der Workflow für die Probenvorbereitung mit Suspensionsfallen (S-Trap) wurde kürzlich als effektive und empfindliche Probenvorbereitungsmethode für die breit angelegte nachgeschaltete Proteomanalyse beschrieben 7,8. Diese Strategie wurde jedoch bei der Analyse des menschlichen Tränenproteoms nicht gut dokumentiert und übertraf die filtergestützte Probenvorbereitung (FASP) und den Aufschluss in Lösung in Bezug auf die Effizienz des enzymatischen Verschlusses und die größere Anzahl von Proteinidentifikationen durch massenspektrometrische Analysen9. Der S-Trap-basierte Ansatz wurde bei der Herstellung von Netzhautgewebe 10, formalinfixiertem, paraffineingebettetem (FFPE) Gewebe 11, Zellen 12, Mikroorganismen13 und Flüssigbiopsien 14,15 demonstriert.
Dieses Protokoll beschreibt einen integrierten quantitativen Arbeitsablauf von klinischen Proben bis hin zu enzymatisch verdautem Protein für die Entdeckung eines nicht-invasiven Tränenprotein-Biomarker-Panels mit einer schnellen, reproduzierbaren und robusten technischen Strategie. Kurz gesagt, die Tränenflüssigkeit wurde mit einem Standard-Schirmer-Streifen aufgefangen und sofort mit einer ophthalmologischen Rahmenheizung getrocknet, um eine Proteinautolyse bei Raumtemperatur zu verhindern. Die eingebetteten Gesamtproteine wurden gemäß den Empfehlungen des Herstellers mit einem 5%igen Natriumdodecylsulfat (SDS)-Lysepuffer extrahiert, gefolgt von einer Protein-Assay-Messung. Das extrahierte Lysat wurde dann einer Standardreduktion mit Dithiothreitol (DTT) und einer Alkylierung mit Iodacetamid (IAA) unterzogen.
Nach der Ansäuerung mit Phosphorsäure wurde den Aggregatproteinen ein Proteinfällungspuffer mit 90 % Methanol und 100 mM Triethylammoniumbicarbonat (TEAB) zugesetzt. Die Probe wurde dann in eine neue Suspensions-Trapping-Mikrosäule überführt. Enzymatischer Aufschluss mit Trypsin in Sequenzierqualität im Verhältnis 1:25 (w/w, Trypsin: Protein) bei 47 °C für 1 h. Die resultierenden Peptide wurden dann durch Zentrifugation sequentiell mit 50 mM TEAB, 0,2 % wässriger Ameisensäure (FA) und 50 % Acetonitril (ACN) mit 0,2 % FA eluiert. Die eluierten Peptide wurden vakuumgetrocknet und in 0,1 % FA rekonstituiert. Die Peptidkonzentration wurde gemessen und für die massenspektrometrische Analyse auf 0,5 μg/μL eingestellt.
Protokoll
Die Probanden gaben vor der Teilnahme an der Studie eine schriftliche Einverständniserklärung ab. Die Studie wurde von der Humanethikkommission der Hong Kong Polytechnic University genehmigt und entsprach den Grundsätzen der Deklaration von Helsinki.
1. Entnahme der menschlichen Tränenflüssigkeit mit Schirmer-Streifen
- Tragen Sie Handschuhe und desinfizieren Sie, um eine Kontamination der Probe zu vermeiden.
- Vergewissern Sie sich, dass die Innenverpackung intakt, steril und nicht abgelaufen ist.
- Biegen Sie die Oberseite des Schirmer-Streifens bei der 0-mm-Markierung leicht nach innen, wie in der Nähe der halbkreisförmigen Spitze des Streifens angezeigt (Abbildung 1).
- Entfernen Sie den Streifen aus der Innenverpackung, indem Sie das Ende des Streifens festhalten, und vermeiden Sie den direkten Kontakt mit dem Probenentnahmebereich von 0 bis 25 mm.
- Bitten Sie die Person, den Blick von der Position des zu platzierenden Streifens abzuwenden.
- Ziehen Sie das untere Augenlid vorsichtig nach unten und haken Sie das Ende des Streifens im unteren Fornix in der Nähe der lateralen Canthusregion ein (Abbildung 2). Wiederholen Sie den gleichen Vorgang am anderen Auge.
- Bitten Sie die Person, die Augenlider vorsichtig zu schließen, um Reizungen zu minimieren.
- Es wird Tränenflüssigkeit für ca. 5 min oder vorzugsweise 15-20 mm Tränenprobe entnommen.
- Bitten Sie die Versuchsperson, beide Augen zu öffnen, das untere Augenlid sanft nach unten zu ziehen und die Streifen von der Versuchsperson zu entfernen.
- Kontrollieren Sie die hydratisierte Länge auf dem Schirmer-Streifen und notieren Sie die gesammelte Menge in mm.
- Trocknen Sie den Streifen mit einer handelsüblichen, sauberen Rahmenheizung, bis die Flüssigkeit vollständig getrocknet ist.
HINWEIS: Übermäßige Erhitzung, die das Filterpapier möglicherweise verkohlen könnte, sollte vermieden werden. - Legen Sie jeden getrockneten Schirmer-Streifen in ein beschriftetes Kryoröhrchen und lagern Sie ihn bis zur Weiterverarbeitung vorzugsweise an einem kühlen, trockenen Ort im Dunkeln.
2. Herstellung von Chemikalien und Reagenzien
- Lysepuffer (5 % SDS, 50 mM TEAB, pH 7,5), 20 ml
- Pipettieren Sie 1 ml 1 M TEAB und 80 μl 12%ige Phosphorsäure. Vortex und kurz beschallen, um Blasen zu entfernen. Bis zu 20 ml mit deionisiertem Wasser auffüllen.
- 1 g SDS abwiegen und unter Oszillation zur Lösung geben, bis sie sich aufgelöst hat.
- Proteinfällungspuffer (90% Methanol, 100 mM TEAB, pH 7,1), 10 mL
- 893 μl 1 M TEAB und 92 μl deionisiertes Wasser hinzufügen.
- 15 μl 85 Gew.-% Phosphorsäure und 9 mL Methanol in die Lösung geben und kurz vortexen.
- Aufschlusspuffer (50 mM TEAB), 1 ml
- Fügen Sie 50 μl 1 M TEAB hinzu und füllen Sie bis zu 1 ml mit deionisiertem Wasser auf.
- 200 mM Dithiothreitol (DTT)-Lösung, 500 μl
- 15 mg DTT abwiegen und in 500 μl deionisiertem Wasser auflösen; Vortex kurz.
HINWEIS: Vor Gebrauch vorbereiten.
- 15 mg DTT abwiegen und in 500 μl deionisiertem Wasser auflösen; Vortex kurz.
- 400 mM Jodacetamid (IAA)-Lösung, 200 μl
- 15 mg IAA wiegen und in 200 μl deionisiertem Wasser auflösen; Vortex kurz. HINWEIS: Vor Gebrauch vorbereiten und Licht vermeiden.
- 0,2 % Ameisensäure, 50 % Acetonitril, 10 ml
- Bereiten Sie 10 ml 50%iges Acetonitril in deionisiertem Wasser vor.
- 20 μl Ameisensäure zugeben und kurz vortexen.
- 0,2%ige Ameisensäurelösung, 10 ml
- 20 μl Ameisensäure zu 10 mL entionisiertem Wasser geben und kurz vortexen.
- 0,1%ige Ameisensäurelösung, 10 ml
- 10 μl Ameisensäure zu 10 ml deionisiertem Wasser geben; Vortex kurz.
3. Proteinextraktion im Schirmer-Streifen
- Schneiden Sie das vordere Ende über die 0-mm-Markierung des Streifens hinaus ab und entsorgen Sie es, um mögliche Verunreinigungen durch den Kontakt des Bindehautgewebes mit einer sauberen Edelstahlschere zu entfernen.
- Schneiden Sie den Streifen in 1-mm-Schritten in ein 1,5-ml-Mikrozentrifugenröhrchen (Abbildung 3).
- 100 μl Lysepuffer in das Mikrozentrifugenröhrchen geben und bei 1.000 U/min bei Raumtemperatur 1 h in einem Thermomixer vortexen.
- Kurz zentrifugieren und den Überstand in ein neues 1,5 mL Mikrozentrifugenröhrchen überführen.
- Führen Sie die Streifen mit einer sauberen Pinzette in 200-μl-Pipettenspitzen ein. Setzen Sie die Spitzen in dasselbe Röhrchen aus Schritt 3.4 mit Halter und zentrifugieren Sie sie bei Raumtemperatur bei 4.000 × g für 1 Minute weiter, um eine maximale Rückgewinnung der verbleibenden Probe auf dem Streifen zu erzielen.
- Messen Sie die Proteinkonzentration mit Bicinchoninsäure (BCA) oder einem kompatiblen Proteinassay.
4. Vorbereitung der Probenvorbereitung durch Suspensionsabscheidung
- Normalisieren Sie die Proben auf 50 μg Protein basierend auf dem Ergebnis des Proteinassays.
- 200 mM DTT im Verhältnis 1:10 (v/v, DVB-T: Probe) zu einer Endkonzentration von 20 mM DTT zugeben und bei 95 °C für 10 min inkubieren.
- Die Proteinlösung auf Raumtemperatur abkühlen lassen.
- 400 mM IAA im Verhältnis 1:10 (v/v, IAA: Probe) zu einer Endkonzentration von 40 mM IAA zugeben und 10 min im Dunkeln bei Raumtemperatur inkubieren.
- 12%ige wässrige Phosphorsäure im Verhältnis 1:10 (v/v, Säure: Probe) zu einer Endkonzentration von 1,2%iger Phosphorsäure zugeben und kurz vortexen.
- Proteinbindungspuffer im Verhältnis 1:6 zugeben (v/v, Probe: Puffer) und kurz vortexen.
HINWEIS: In diesem Schritt sollte kolloidaler Proteinpartikel gebildet werden, und die Lösung erscheint durchscheinend, wenn die Proteinmenge ausreichend ist. - Öffnen Sie die Kappe der Suspension Trapping Micro Spin Column und montieren Sie die Spin-Säule auf ein 2 mL Mikrozentrifugenröhrchen, um den Durchfluss zu sammeln.
- Geben Sie bis zu 200 μl angesäuertes Proteinlysat-Gemisch in die Säule.
- Zentrifugieren Sie die Säule bei 4.000 × g für 20 s. Proteinpartikel wurden eingefangen; Wiederholen Sie den Vorgang, bis die Proben in die Säule geladen sind.
- Fügen Sie 150 μl Proteinbindungspuffer hinzu und zentrifugieren Sie 20 s lang bei 4.000 × g , um das suspendierte Protein zu waschen. 3x wiederholen.
- Montieren Sie die Suspensions-Trapping-Mikrosäule auf ein neues 1,5-ml-Mikrozentrifugenröhrchen.
- Geben Sie 20 μl 50 mM TEAB-Aufschlusspuffer, der Protease in einem Verhältnis von 1:25 (w/w, Trypsin: Protein) enthält, auf den Filter in der Schleudersäule und vermeiden Sie dabei Blasen und Luftspalte zwischen Filter und Aufschlusslösung.
- Verschließen Sie die Suspension Trapping Micro Spin Column, um Verdunstung zu verhindern. Bei 47 °C für 1 h in einem Thermomischer inkubieren; Während der Verdauung nicht schütteln oder wirbeln.
- Eluieren Sie Peptide mit 40 μl 50 mM TEAB durch Zentrifugalkraft bei 4.000 × g für 20 s.
- 40 μl 0,2 % FA zugeben und bei 4.000 × g 20 s zentrifugieren.
- Fügen Sie 35 μl 0,2 % FA und 50 % Acetonitril hinzu und zentrifugieren Sie 20 s lang bei 4.000 × g .
- Pool drei eluiert und trocknet mit einer Vakuumzentrifuge.
- Bis zur weiteren Analyse bei -80 °C Ultratiefkühlschrank lagern. HINWEIS: Das Protokoll kann hier pausiert werden.
5. Rekonstituieren von Peptiden für die massenspektrometrische Analyse
- Rekonstituieren Sie die Probe mit 12 μl 0,1 % FA, Wirbel und zentrifugieren Sie kurz.
- Messen Sie die Peptidkonzentration mit einem Peptid-Assay-Kit.
- Normalisieren Sie die Peptidkonzentration auf 0,5 μg/μl in 0,1 % FA.
- Füllen Sie die Peptidmischung in ein Autosampler-Fläschchen und bereiten Sie sie auf die massenspektrometrische Analyse vor.
6. Probenaufnahme mittels Flüssigkeitschromatographie-Tandem-Massenspektrometrie
- Laden Sie 3 μg des Peptids mit isokratischem Beladungspuffer (0,1 % FA, 5 % ACN) in eine Fallensäule (C18, 5 μm, 100 μm, 20 mm) mit einer Flussrate von 2 μl/min für 15 min.
- Die Peptide werden mit einer Umkehrphasen-Nanoanalysesäule (C18, 5 μm, 100 μm, 300 mm) bei einer Flussrate von 350 nL/min in einem 155-minütigen Trenngradienten fraktioniert. Verwenden Sie die mobile Phase A, die eine Mischung aus 0,1 % Ameisensäure (v/v), 5 % ACN (v/v) in Wasser enthält, und mobile Phase B mit 0,1 % FA (v/v), 98 % ACN (v/v) in Wasser. Verwenden Sie die folgende Steigung: 0-0,5 min: 5 % B, 0,5-90 min: 10 % B, 90-120 min: 20 % B, 120-130 min: 28 % B, 130-135 min: 45 % B, 135-141 min: 80 % B, 141-155 min: 5 % B.
- Führen Sie eine datenabhängige Erfassung (DDA) mit einem TOF-MS-Scanbereich zwischen 350 und 1800 m/z mit einer Akkumulationszeit von 250 ms und einer dynamischen Zielausschlusszeit von 18 s durch. Führen Sie dann einen MS/MS-Scan bei 100 bis 1.800 m/z im Hochempfindlichkeitsmodus mit einer Akkumulationszeit von 50 ms für die obersten 50 Vorläufer pro Zyklus mit einem Schwellenwert von 125 cps für MS/MS-Signale mit einem Ladezustand von +2 bis +4 durch.
- Analysieren Sie Rohdaten mit der referenzierten Software oder anderen kompatiblen Engines mit einer Referenzdatenbank in FASTA aus der öffentlich zugänglichen UniProt-Datenbank.
Ergebnisse
Dieses Protokoll ermöglicht die Entnahme von Tränenproben mit Schirmer-Streifen, die trocken bei Raumtemperatur gelagert werden, bevor die anschließende Probenvorbereitung für die massenspektrometrische Analyse erfolgt. Der Arbeitsablauf für die filtergestützte Probenvorbereitung (FASP) mit Suspensions-Trapping-Mikrosäule ermöglichte eine schnelle Probenvorbereitung innerhalb von Stunden, verglichen mit den üblicherweise verwendeten In-Solution-Aufschlussverfahren an Tagen, die eine Inkubation über Nacht erfordern. Die Ausbeute an Peptidrückgewinnung war signifikant höher (p < 0,001) als das Standardprotokoll für den Aufschluss in Lösung und mit guter Reproduzierbarkeit bei einem Variationskoeffizienten (%CV) < 7 %. Ein Pool von Tränenproben wurde in sechs technischen Replikaten mit 74,2 ± 5,0 % Peptidrückgewinnung und 52,8 ± 1,6 % Peptidwiederfindung in Proben wiederholt, die mit In-Solution-Verfahren hergestellt wurden. Eine gepoolte Tränenprobe mit einer Proteinmenge von 36,3 μg wurde auf den Schirmer-Streifen gestochen und wie zuvor beschrieben extrahiert, die Extraktionseffizienz des Proteins betrug 81% (29,5 ± 6,8 μg, Mittelwert ± SD).
Beide Workflows luden 3 μg Peptide auf die MS, und die DDA-Suche ergab insgesamt 1.183 ± 118 Proteine (5.757 ± 537 verschiedene Peptide) und 874 ± 70 Proteine (4.400 ± 328 Peptide) bei 1 % FDR in der Suspensions-Trapping-Gruppe bzw. in der In-Solution-Gruppe. Die Analyse der Genontologie (GO) unter Verwendung des PANTHER-Klassifikationssystems ergab sehr ähnliche Proteome für beide Ansätze, wobei Bindung, katalytische Aktivität und molekulare Funktionsregulation ihre wichtigsten molekularen Funktionen sind (Abbildung 4).

Abbildung 1: Biegen Sie die Oberseite des Schirmer-Streifens vor dem Auftragen an der 0-mm-Markierung. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
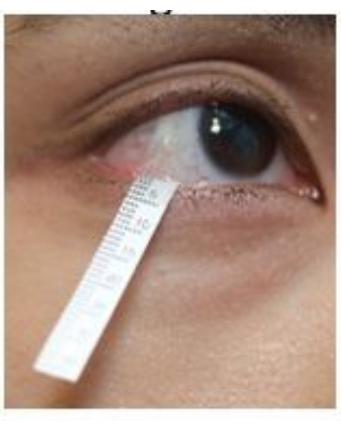
Abbildung 2: Position des Schirmer-Streifens während der Tränenentnahme. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
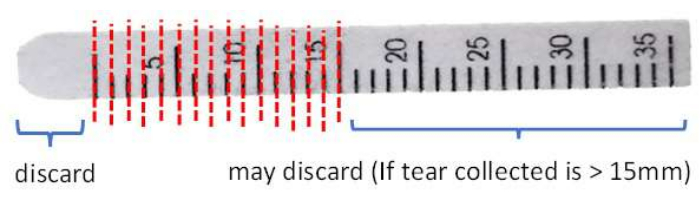
Abbildung 3: Illustration des Schirmer-Streifen-Handlings vor der Proteinextraktion. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
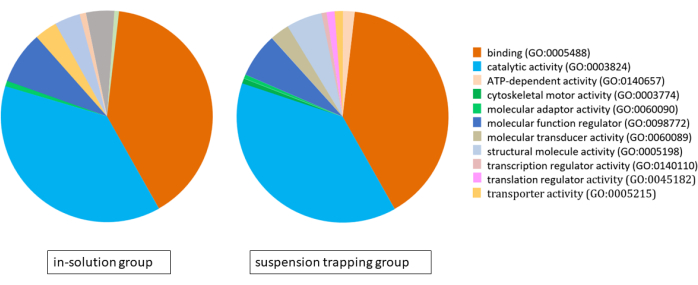
Abbildung 4: Tortendiagramm zur Veranschaulichung der Genontologieanalyse für die Proteome, die mit dem In-Solution-Workflow und dem Suspensionsfallen-Workflow unter Verwendung des PANTHER-Klassifikationssystems identifiziert wurden. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Diskussion
Um mit dieser Methode genaue Ergebnisse zu erzielen, sollten bei allen Verfahren ab der Entnahme von Tränenproben stromlose Einweghandschuhe getragen werden, um eine Kontamination der Proben zu vermeiden. Es ist wichtig, Blasen und Luftspalte zwischen dem Filter und der Probenlösung in jedem Schritt zu vermeiden, indem Mikrospinnsäulen verwendet werden. Wenn das Probenvolumen größer ist als die Kapazität der Säulen, wird empfohlen, den Vorgang zu wiederholen. Dieses Protokoll hat sich in Bezug auf die Vorbereitungszeit, die Proteinrückgewinnung und die Identifizierung des Gesamtproteins als effizienter erwiesen als das herkömmliche In-Solution-Protokoll. Dies liegt vor allem daran, dass die Proben die meisten der erforderlichen Verfahren auf derselben Säule durchlaufen, im Gegensatz zur In-Solution-Methode, die mehrere Übertragungsschritte wie Acetonfällung, Aufschluss und Reinigung (Entsalzung) umfasst, was die Wahrscheinlichkeit von Schwankungen in den resultierenden Daten erhöht.
Zusätzlich zu den Tränenproben, die mit der Mikrokapillarmethode16,17 entnommen werden, bietet dieser FASP-Workflow mit Suspensions-Einfang-Mikrosäule eine alternative Probenvorbereitungsmethode, die eine schnelle und robuste Tränenprobenvorbereitung mit Schirmer-Streifen mit minimaler Materialvorbereitung und benutzerfreundlichen Schritten ermöglicht. Dies ermöglicht eine reproduzierbare Tränenprobenvorbereitung für große Kohortenstudien bei mehreren Augenerkrankungen oder -zuständen mit verbesserter Peptidrückgewinnung und Proteinidentifikation durch MS im Vergleich zu In-Solution-Verfahren. Dieses zuverlässige Verfahren kann regelmäßig bei der Herstellung von Tränen-Biomarker-Proben für die Forschung und andere klinische Zwecke eingesetzt werden. Am wichtigsten ist, dass es nur eine minimale Schulung des Personals für die Entnahme vor Ort erfordert und die Probenlagerung in einem Gefrierschrank überflüssig macht. Die Proben werden vor Ort getrocknet, um die Autolyse und den Abbau von Proteinen zu minimieren. Dies ermöglicht einen bequemen Versand per Post, um die nachgelagerte Analyse zu erleichtern, im Gegensatz zur Verwendung von Mikrokapillarröhrchen.
Offenlegungen
Die Autoren haben keine Interessenkonflikte zu deklarieren.
Danksagungen
Diese Arbeit wurde von der InnoHK-Initiative und der Regierung der Sonderverwaltungsregion Hongkong unterstützt. Forschungszentrum für SHARP Vision; und das Research Centre for Chinese Medicine Innovation (RCMI) an der Hong Kong Polytechnic University.
Materialien
| Name | Company | Catalog Number | Comments |
| 9 mm Plastic Screw Thread Vials | Thermo Scientific | C4000-11 | |
| Acetonitrile, LCMS Grade | Anaqua | AC-1026 | |
| Centrifuge MiniSpin plus | Eppendorf | 5453000097 | |
| DL-dithiothreitol (DTT), BioUltra | Sigma-Aldrich | 43815 | |
| Eppendorf Safe-Lock Tubes, 1.5 mL | Eppendorf | 30120086 | |
| Formic acid, ACS reagent, ≥96% | Sigma-Aldrich | 695076 | |
| Frame Heater OPTIMONSUN Electronic | Breitfeld & Schliekert GmbH | 1203166 | |
| Iodoacetamide (IAA), BioUltra | Sigma-Aldrich | I1149 | |
| Methanol, HPLC Grade | Anaqua | MA-1292 | |
| Nunc Biobanking and Cell Culture Cryogenic Tubes, 2 mL | Thermo Fisher Scientific | 368632 | |
| Phosphoric acid, 85 wt.% in H2O | Sigma-Aldrich | 345245 | |
| Pierce Quantitative Colorimetric Peptide Assay | Thermo Fisher Scientific | 23275 | |
| Pierce Rapid Gold BCA Protein Assay Kit | Thermo Fisher Scientific | A53225 | |
| Quadrupole Time-of-Flight Mass Spectrometry | Sciex | TripleTOF 6600 | |
| Schirmer Ophthalmic Strips | Entod Research Cell UK Ltd | I-DEW Tearstrips | |
| S-Trap Micro Column | Protifi | C02-micro-80 | |
| SureSTART 9 mm Screw Caps | Thermo Scientific | CHSC9-40 | |
| Triethylammonium bicarbonate (TEAB), 1 M | Sigma-Aldrich | 18597 | |
| Ultra-performance Liquid Chromatography | Eksigent | NanoLC 400 | |
| UltraPure Sodium dodecyl sulfate (SDS) | Thermo Fisher Scientific | 15525017 |
Referenzen
- Ma, J. Y. W., Sze, Y. H., Bian, J. F., Lam, T. C. Critical role of mass spectrometry proteomics in tear biomarker discovery for multifactorial ocular diseases (Review). International Journal of Molecular Medicine. 47 (5), 83 (2021).
- Tse, J. S. H., et al. Integrating clinical data and tear proteomics to assess efficacy, ocular surface status, and biomarker response after orthokeratology lens wear. Translational Vision Science & Technology. 10 (11), 18 (2021).
- Cheung, J. K., et al. Human tear proteome dataset in response to daily wear of water gradient contact lens using SWATH-MS approach. Data in Brief. 36, 107120 (2021).
- Tse, J. S., et al. Data on assessment of safety and tear proteome change in response to orthokeratology lens - Insight from integrating clinical data and next generation proteomics. Data in Brief. 29, 105186 (2020).
- Zhan, X., Li, J., Guo, Y., Golubnitschaja, O. Mass spectrometry analysis of human tear fluid biomarkers specific for ocular and systemic diseases in the context of 3P medicine. The EPMA Journal. 12 (4), 449-475 (2021).
- Ponzini, E., et al. Mass spectrometry-based tear proteomics for noninvasive biomarker discovery. Mass Spectrometry Reviews. 41 (5), 842-860 (2022).
- HaileMariam, M., et al. S-Trap, an ultrafast sample-preparation approach for shotgun proteomics. Journal of Proteome Research. 17 (9), 2917-2924 (2018).
- Ding, H., et al. Urine proteomics: evaluation of different sample preparation workflows for quantitative, reproducible, and improved depth of analysis. Journal of Proteome Research. 19 (4), 1857-1862 (2020).
- Ludwig, K. R., Schroll, M. M., Hummon, A. B. Comparison of in-solution, FASP, and S-Trap based digestion methods for bottom-up proteomic studies. Journal of Proteome Research. 17 (7), 2480-2490 (2018).
- Sze, Y. H., et al. High-pH reversed-phase fractionated neural retina proteome of normal growing C57BL/6 mouse. Scientific Data. 8 (1), 27 (2021).
- Marchione, D. M., et al. HYPERsol: High-quality data from archival FFPE tissue for clinical proteomics. Journal of Proteome Research. 19 (2), 973-983 (2020).
- Chhuon, C., et al. A sensitive S-Trap-based approach to the analysis of T cell lipid raft proteome. Journal of Lipid Research. 61 (11), 1512-1523 (2020).
- Hayoun, K., et al. Evaluation of sample preparation methods for fast proteotyping of microorganisms by tandem mass spectrometry. Frontiers in Microbiology. 10, 1985 (2019).
- Templeton, E. M., et al. Comparison of SPEED, S-Trap, and in-solution-based sample preparation methods for mass spectrometry in kidney tissue and plasma. International Journal of Molecular Sciences. 24 (7), 6290 (2023).
- Ding, Z., Wang, N., Ji, N., Chen, Z. S. Proteomics technologies for cancer liquid biopsies. Molecular Cancer. 21 (1), 53 (2022).
- Nättinen, J., Aapola, U., Jylhä, A., Vaajanen, A., Uusitalo, H. Comparison of capillary and Schirmer strip tear fluid sampling methods using SWATH-MS proteomics approach. Translational Vision Science & Technology. 9 (3), 16 (2020).
- Bachhuber, F., Huss, A., Senel, M., Tumani, H. Diagnostic biomarkers in tear fluid: from sampling to preanalytical processing. Scientific Reports. 11 (1), 10064 (2021).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten