Method Article
Aislamiento de células de la glándula salival del ratón madre
En este artículo
Resumen
Un protocolo optimizado para el aislamiento de células madre de la glándula salival del ratón se describe. El método emplea la digestión enzimática y mecánica, y permite el aislamiento de salispheres que contiene células con características de células madre.
Resumen
Madura glándulas salivales tanto de origen humano y el ratón integrado por un mínimo de cinco tipos de células, cada una de las que facilita la producción y excreción de saliva en la cavidad oral. Las células acinares serosas y mucosas son las proteínas y las mucosas de las fábricas que producen las glándulas, respectivamente, y representan el origen de la producción de saliva. Una vez sintetizados, los diversos componentes proteicos enzimáticos y otros de la saliva se secreta a través de una serie de células ductales epiteliales teniendo morfología de tipo, hasta la expulsión definitiva de la saliva a través de un conducto principal en la cavidad de la boca. La composición de la saliva también es modificado por las células ductales durante este proceso.
En la manifestación de enfermedades como el síndrome de Sjögren, y en algunas situaciones clínicas como el tratamiento de radioterapia para el cáncer de cabeza y cuello, la producción de saliva por las glándulas se reduce drásticamente 1,2. La xerostomía como resultado, una sensación subjetiva de boca seca, no sólo afecta a la capacidad del paciente para tragar y hablar, sino que también fomenta el desarrollo de la caries dental y puede ser socialmente debilitante para la víctima.
La restauración de la producción de saliva en las condiciones clínicas antes mencionadas por lo tanto, representa una necesidad clínica no cubierta, y como tal, varios estudios han demostrado la capacidad de regeneración de las glándulas salivales 3-5. En relación con el aislamiento de células madre similares a las células de poblaciones de células de diversos tejidos en el ratón y el cuerpo humano 6.8, hemos demostrado mediante el método descrito que las células madre aisladas de las glándulas salivales del ratón se puede utilizar para rescatar a la producción de saliva en la saliva irradiados glándulas 9,10. Este descubrimiento abre el camino para el desarrollo de células madre basado en terapias para el tratamiento de las condiciones de xerostomía en los seres humanos, y también para la exploración de las glándulas salivales como un microambiente que contiene células pluripotentes, con capacidad de auto-renovación.
Protocolo
1. Regent Preparación
- Buffer: 1% (w / v) de albúmina sérica bovina en solución salina equilibrada de Hank
- Reconstituir las enzimas. Enzima hialuronidasa: 40 mg / ml, se disolvieron en el tampón. Colagenasa II: 23 mg / ml, se disolvieron en el tampón. Utilice soluciones recién preparadas enzima fresca para cada aislamiento. Cuando se disuelve, se almacenan a 4 ° C hasta su uso para la digestión.
- 50 mM de cloruro de calcio en agua destilada. Filtro de esterilización a través de un filtro de 0,2 uM tamaño de los poros.
- Ratón glándulas salivales (MSG) del medio de cultivo: DMEM: F12 con penicilina (100 UI / ml), estreptomicina (100 mg / mL), glutamax (2 mM), factor de crecimiento epidérmico-2 (20 ng / ml), factor de crecimiento de fibroblastos la insulina-2 (20 ng / ml), N2 suplemento (1%), (10 mg / mL) y dexametasona (1 M).
2. Tejidos mecánica y digestión enzimática
- Pesar de las glándulas salivales disecados.
- Picar las glándulas en una pasta homogénea con tijeras de disección estéril curva en una pequeña placa de Petri.
- Recoger tejido picado en 14 ml tubos, con 1 ml de tampón por tejido submandibular 80 mg. Enjuagar los platos petri limpia de tejido utilizando algunos de los buffer.
- Añadir otra 1 mL de tampón por tejido de 80 mg, seguido de 25 solución de la enzima colagenasa l II, 25 l solución de enzima hialuronidasa y 250 l solución de cloruro de calcio por los tejidos de 80 mg. Si se trabaja con grandes cantidades de tejido, los pasos 2,4 a 2,9 se puede realizar en T25 frascos de cultivo de tejidos para mayor comodidad.
- Incubar en un baño de agua agitando a 37 ° C durante 20 minutos. Retire los tubos y triturar con una pipeta de mezcla de enzimas a fondo a través del tejido nuevo.
- Vuelva a colocar en el baño de agua durante 20 minutos.
- Recoge los tejidos por centrifugación a 400 xg, durante 8 minutos. Desechar el sobrenadante.
- Resuspender en tampón de 2 ml por cada 80 mg de tejido, y repetir la enzima y la adición de cloruro de calcio que el anterior. Incubar 20 minutos en baño de agua agitando. Retire los tubos y triturar con una pipeta de mezcla de enzimas a fondo.
- Incubar durante 20 minutos finales en el baño de agua agitando. Recoger las células por centrifugación como anteriormente, desechar el sobrenadante.
3. Pasos para el lavado
- Resuspender cada 80 mg de tejido en el tampón de 2 ml y una pipeta para lavar los tejidos libres de las enzimas.
- Centrifugar como se ha de recoger. Desechar el sobrenadante.
- Repetir el lavado con 1 ml de tampón por mg de tejido 80. Centrífuga para recoger, desechar el sobrenadante.
4. Filtración
- Resuspender solución de tejido en el tampón de 1 ml por mg de tejido 80.
- Añadir la solución a 100 micras de tamaño de poro de filtro colocado más de 50 ml tubo Falcon. No aplicar más de 3 ml de solución de tejido picado por columna, como los filtros pueden obstruirse. Permiten que se filtre a través de. Retire el material de filtrado colgando en la parte inferior del filtro con una pipeta, y añadir a filtrado.
- Use una jeringa con aguja de calibre 26 para tomar filtrado de 50 ml tubos y filtros se aplican a 50 micras de tamaño de poro en tubos de 5 ml. Deje que se filtra a través de, la asistencia al aflojar las tapas, si es necesario.
- Tubos de centrifugación como se ha de recoger. Desechar el sobrenadante.
5. Revestimiento y Mediana Empresa
- Combine todos los pellets en un solo volumen. Contar con contador de células automatizado o hemocitómetro.
- Células de la placa a una densidad de 0,4 x 10 6 células por pocillo de 12 y placa, o 2.67 x 10 6 células por frasco de cultivo de tejidos T25. Añadir un medio de MSG ml a cada pocillo o 6 ml a cada frasco T25.
- Se incuba a 37 ° C. Ámbitos debe ser claramente visible el día 2.
6. Los resultados representativos:
Después de dos o tres días en la cultura, pequeños agregados de células (salispheres) será evidente en los cultivos. Salispheres seguirá creciendo en tamaño durante un período de diez días en la cultura. Representante fase imágenes de microscopía de contraste de salispheres se muestra en la Figura 1. Proliferación de las células que expresan las células madre de proteínas asociadas a marcadores se pueden aislar de estos ámbitos, de manera óptima entre el aislamiento días después del 3-5, y son capaces de diferenciarse en células funcionales, producen la saliva acinar.
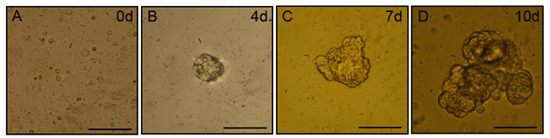
Figura 1. Salisphere formación in vitro. Después de la digestión mecánica y enzimática con el presente Protocolo, las esferas de tamaño cada vez mayor se puede encontrar en las culturas flotante. Los paneles son representativos fase de imágenes de microscopía de contraste de las esferas de los días 0 (A), 4 (B), 7 (C) y 10 (D). Barra de escala = 50 micras.
Discusión
El método de cultivo de tejidos descrito aquí representa un protocolo reproducible para el aislamiento de células madre que contienen salispheres de las glándulas salivales de los ratones. Los estudios que utilizan células aisladas de este modo se ha destacado la capacidad de regeneración de células de la glándula salival madre 9. El trasplante de un centenar de c-Kit + células derivadas de la salispheres inducida recuperación funcional de las glándulas salivales de ratón irradiados. Estos datos son muy interesantes y un punto de partida para la investigación de células madre basado en la terapia para la xerostomía. Muchos caminos quedan por explorar sin embargo, incluyendo el perfil de expresión de los marcadores completa de proteínas de las células madre, la capacidad de las glándulas submandibulares de rescatar la función de las glándulas parótidas irradiados salivales y viceversa, y la caracterización de la supuesta en el nicho de células madre in vivo de las células. En última instancia, la traducción de este protocolo para las muestras de tejido humano y el potencial posterior para el tratamiento de la xerostomía en pacientes humanos con las células aisladas es la aplicación más interesante del método descrito.
Divulgaciones
Materiales
| Name | Company | Catalog Number | Comments |
| Hyaluronidase | Sigma-Aldrich | H3506 | Store at – 20 °C |
| Collagenase II | GIBCO, by Life Technologies | 17101-015 | Store at 4 °C |
| Epidermal Growth Factor-2 | Sigma-Aldrich | E9644 | Make a stock of 10 μg / mL in phosphate buffered saline (PBS). Store at – 20 °C in single use aliquots. |
| Fibroblast Growth Factor-2 | Sigma-Aldrich | F0291 | Make stock of 25 μg / mL in PBS. Store at – 20 °C in single use aliquots. |
| N2 supplement | GIBCO, by Life Technologies | 17502-048 | As manufacturer instructions. |
| Insulin | Sigma-Aldrich | I6634 | Make stock of 2 mg / mL in tap water. Adjust water to pH 2-3 using glacial acetic acid prior to dissolving. |
| Dexamethasone | Sigma-Aldrich | D4902 | |
| 100 μM pore-size sterile cell strainers | BD Biosciences | 352360 | |
| Polystyrene round-bottomed tubes with cell strainer caps (50 μM pore size) | BD Biosciences | 352235 |
Referencias
- Vissink, A. Oral Sequelae of Head and Neck Radiotherapy. Crit Rev Oral Biol Med. 14, 199-212 (2003).
- Napeñ, a. s., J, J., Brennan, M. T., Fox, P. C. Diagnosis and treatment of xerostomia (dry mouth). Odontology. 97, 76-83 (2009).
- Denny, P. C. Parenchymal cell proliferation and mechanisms for maintenance of granular duct and acinar cell populations in adult male mouse submandibular gland. 235, 475-485 (2005).
- Man, Y. G. Persistence of a perinatal cellular phenotype in submandibular glands of adult rat. J. Histochem. Cytochem. 43, 1203-1215 (1995).
- Cotroneo, E., Proctor, G. B., Carpenter, G. H. Regeneration of acinar cells following ligation of rat submandibular gland retraces the embryonic-perinatal pathway of cytodifferentiation. Differentiation. 79, 120-130 (2010).
- Eirew, P. A method for quantifying normal human mammary epithelial stem cells with in vivo regenerative ability. Nat Med. 14, 1384-1389 (2008).
- Gorjup, E. Glandular tissue from human pancreas and salivary gland yields similar stem cell populations. European Journal of Cell Biology. 88, 409-421 (2009).
- Alonso, L., Fuchs, E. Stem cells of the skin epithelium. Proc Natl Acad Sci U S A. 100, 11830-11835 (2003).
- Lombaert, I. M. Rescue of salivary gland function after stem cell transplantation in irradiated glands. Plos One. 3, e2063-e2063 (2008).
- Coppes, R. P., Goot, A. v. a. n. d. e. r., Lombaert, I. M. A. Stem Cell Therapy to Reduce Radiation-Induced Normal Tissue Damage. Seminars in Radiation Oncology. 19, 112-121 (2009).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados