Method Article
Uso del inmunoensayo de electroforesis capilar para buscar biomarcadores potenciales de la esclerosis lateral amiotrófica en plaquetas humanas
En este artículo
Resumen
Los biomarcadores basados en la sangre para enfermedades neurodegenerativas son esenciales para la implementación de estudios clínicos a gran escala. Un análisis de sangre confiable y validado debe requerir un pequeño volumen de muestra, así como ser un método de muestreo menos invasivo, asequible y reproducible. Este artículo demuestra que el inmunoensayo de electroforesis capilar de alto rendimiento satisface los criterios para el desarrollo potencial de biomarcadores.
Resumen
El inmunoensayo de electroforesis capilar (CEI), también conocido como tecnología occidental capilar, se está convirtiendo en un método de elección para la detección de proteínas y fármacos relevantes para la enfermedad en ensayos clínicos. Reproducibilidad, sensibilidad, requisito de volumen de muestra pequeño, anticuerpos de multiplexación para el etiquetado de múltiples proteínas en la misma muestra, capacidad automatizada de alto rendimiento para analizar hasta 24 muestras individuales y requisitos de corto plazo hacen que ceI ventajoso sobre el inmunoensayo clásico de la mancha occidental. Hay algunas limitaciones de este método, como la incapacidad de utilizar un gel degradado (4%–20%) matriz, alto fondo con muestras biológicas sin refinar, y la falta comercial de reactivos individuales. Este documento describe un método eficiente para ejecutar CEI en un entorno de ensayo múltiple, optimizando la concentración de proteínas y la valoración de anticuerpos primarios en una placa de ensayo, y proporcionando plantillas fáciles de usar para la preparación de muestras. También se describen los métodos para medir la sartén TDP-43 y el derivado fosforilado TDP-43 en el litosol de lisato plaquetario como parte de la iniciativa en el desarrollo de biomarcadores a base de sangre para enfermedades neurodegenerativas.
Introducción
El objetivo general de CEI como se describe aquí es proporcionar un protocolo escalonado actualizado para analizar las proteínas diana en las plaquetas humanas. La asignación de una molécula de firma basada en la sangre es una de las tareas más importantes en el campo del desarrollo de biomarcadores en enfermedades neurodegenerativas humanas, como la enfermedad de Alzheimer (AD), la esclerosis lateral amiotrófica (ELA), el lobar frontotemporal degeneración (FTLD), enfermedad de Parkinson (PD), miositis del cuerpo de inclusión (IBM) y otras condiciones patológicas relevantes de la agregación de proteínas. La detección de cantidades diminciales de tales proteínas de firma en grandes volúmenes de sangre con muchos agentes que interfieren es un desafío. Por lo tanto, la especificidad, sensibilidad, capacidad para manejar un gran número de muestras y reproducibilidad del método seleccionado son cruciales.
Las plaquetas humanas pueden servir como un entorno para identificar y asignar proteínas biomarcadoras potenciales para la enfermedad neurodegenerativa. Las plaquetas proporcionan la oportunidad de servir como un modelo de células primarias sustitutas, que reflejan algunas características de las células neuronales1,2,3. Hay ciertas características que hacen de las plaquetas uno de los medios preferidos para analizar las proteínas candidatas a biomarcadores y sus derivados químicos. En primer lugar, las plaquetas se pueden adquirir fácilmente utilizando un enfoque menos invasivo mediante la recolección de sangre de los donantes (es decir, la venopunción) o en grandes volúmenes de los bancos de sangre comunitarios. En segundo lugar, las plaquetas se pueden aislar fácilmente de toda la sangre con un trabajo preparatorio mínimo en laboratorios mínimamente equipados4,5. En tercer lugar, las plaquetas no tienen núcleos; por lo tanto, son una buena célula modelo para estudiar alteraciones en el metabolismo sin regulación transcripcional. En cuarto lugar, se encapsula el contenido de biomoléculas de las plaquetas; por lo tanto, el microambiente plaquetario protege su contenido de sustancias que interfieren en el suero (es decir, proteasas). En quinto lugar, el plasma enriquecido con plaquetas se puede almacenar a temperatura ambiente durante 7-8 días sin perder actividad metabólica. Por lo tanto, las plaquetas proporcionan un modelo de trabajo en el que los factores externos se minimizan y controlan.
Las técnicas tradicionales de inmunoensayo, como la inmunoblotting (por ejemplo, la hincha occidental) y el ensayo inmunoabsorbente ligado a enzimas (ELISA), se utilizan más ampliamente en el análisis específico de proteínas. Sin embargo, estos dos métodos tienen varias desventajas, incluyendo múltiples pasos de ensayo, requisito de productos químicos y reactivos peligrosos, gran tamaño de la muestra, problemas con la reproducibilidad del ensayo y variabilidades de datos entre carreras. Esto motivó el desarrollo de un método que es más simple con menos pasos y alcanzable en un período relativamente corto. Aunque la técnica clásica de la mancha occidental seguirá siendo un método de laboratorio popular, su procedimiento de varios pasos, suministros, residuos tóxicos (es decir, acrilamida, metanol, etc.) y el tiempo de ensayo son cada vez menos deseables al realizar análisis de proteínas.
Un enfoque automatizado de CEI se está convirtiendo gradualmente en un método de elección para los laboratorios que llevan a cabo ensayos de proteínas de alto rendimiento6. CEI elimina la necesidad de geles, aparatos de electroforesis de gel, membranas, electroforesis y dispositivos de electrotransferencia, y más implicaciones de manejo físico. Si se diseña bien, un ensayo CEI debe completarse en un plazo aproximado de 3,5 h, incluido el análisis cuantitativo de datos, el electroferograma de calidad de publicación y gráficos con análisis estadístico. Otra superioridad del sistema CEI es su requisito de 10x-20x menos concentración de proteínas, por lo que es ideal para su uso en muestras humanas utilizadas en ensayos clínicos7,8.
La parte más crítica de CEI es optimizar las condiciones de ensayo para cada anticuerpo comprado a diferentes proveedores, tipo de anticuerpo (monoclonal vs policlonal), concentraciones óptimas de proteínas, preparación de muestras, temperatura de desnaturalización de la muestra y voltaje de electroforesis aplicado en los capilares. Hemos desarrollado un método de optimización de formato de un solo ensayo para el CEI que debe implementarse antes de cualquier nuevo ensayo, lo que ahorrará tiempo y recursos. Este paso de optimización es seguido por una evaluación cuantitativa automatizada de la derivada total y fosforilada de la proteína de unión ADN/ARN de respuesta de transactivación (TARDP). Debido a su tamaño (43 kDa), el acrónimo TDP-43 se utilizará en todo este artículo. Aquí, se evalúa la proteína TDP-43 en el lisato plaquetario humano obtenido de pacientes con ELA para ayudar a desarrollar el valor predictivo de fosforilación (VPP) como un biomarcador de pronóstico potencial.
TDP-43 es un nuevo candidato potencial a biomarcador de enfermedades para la ELA. TDP-43 es una proteína omnipresente en todas las células nucleadas; por lo tanto, las funciones de TDP-43 durante diversos eventos celulares normales y en enfermedades neurodegenerativas se han investigado9,10,11,12,13,14. Aunque el TDP-43 es una proteína nuclear15,tiene la capacidad de entrar y salir entre el núcleo y el citoplasma debido a la presencia de localización nuclear y secuencias de exportación nuclear16,17,18,19. El TDP-43 citoplasma participa en diversos eventos celulares, como la estabilidad y el transporte del ARNm, la respuesta al estrés, la función mitocondrial, autofagosoma20. Sin embargo, no se sabe mucho sobre el papel de los derivados fosforilados de TDP-43 aparte de su participación en la patogénesis de la enfermedad neurodegenerativa21.
Este protocolo ilustra cómo optimizar las condiciones del ensayo para analizar el contenido del TDP-43 y su derivado fosforilado en plaquetas utilizando el enfoque CEI. Dado que el TDP-43 fosforilado no está disponible comercialmente, se propone utilizar un valor de fosforilación predictiva (VPP) para evaluar los perfiles de TDP-43 en pacientes con ELA. Este sistema CEI utiliza un pequeño volumen de mezcla de muestras (2,5–3,0 l por capilar). La configuración total del volumen de ensayo es de 8,0 ml por capilar en función del protocolo del fabricante; por lo tanto, los investigadores pueden utilizar una preparación de mezcla de muestra para dos corridas separadas. El fabricante diseñó el protocolo de ensayo para minimizar los errores de pipeteo, si no eliminarpor por completo. Las 24 mezclas individuales de muestras de lisado plaquetario humano se dividen en medio volumen (es decir, 2,5–3,0 l por muestra) y se analizan consecutivamente por dos anticuerpos diferentes dentro de 7 h. El sistema CEI descrito aquí proporciona una modalidad de ensayo de alto rendimiento deseable. Los usuarios necesitan probar anticuerpos de diferentes proveedores y las modalidades de preparación de muestras para la proteína diana antes de realizar pruebas de detección a gran escala.
Protocolo
Todos los protocolos relativos al procesamiento de plaquetas humanas siguen las directrices de los comités del Centro Médico de la Universidad de Kansas y de la Universidad de Medicina y Biociencias IRB de Kansas City.
1. Preparación de tampones y reactivos
NOTA: Prepare todas las muestras según las directrices del fabricante. Use equipo de protección personal (abrigos de laboratorio, guantes y gafas) durante este procedimiento.
- Preparar tampón de lavado de citrato combinando 0,941 g de sacarosa (concentración final de 11 mM), 6,4 ml de 5 M NaCl (128 mM final), 5,4 ml de 0,2 M NaH2PO4 (4,3 m M final), 9,4 ml de 0,2 M Na2PHO4 (7,5 mM final), 0,352 g de citrato sódico (4,8 mM final) y 0,115 g de ácido cítrico (2,4 mM final). Ajuste el volumen total a 250 ml con ddH2O. Filtrar a través de un disco de filtro de 0,45 m y ajuste el pH a 6,5. Conservar hasta 1 año a 4oC. Lleve la solución a temperatura ambiente (RT) antes de usar22.
- Prepare el tampón de ruptura combinando sacarosa de 250 mM, EDTA de 1 mM y Tris-Cl de 10 mM (pH 7.4) en un volumen final de 100 ml. Conservar hasta 1 año a 4oC. Añadir un cóctel de 2 ml de inhibidores de fosfatasa (1:1000 final) y 1 l de cóctel de inhibidores de la proteasa (1:2000 finales) en 2 ml de tampón de ruptura. Mantener en hielo hasta su uso. Deseche el búfer de ruptura no utilizado.
2. Aislamiento plaquetario
- Recoger 8–10 ml de sangre humana en tubo de recolección de sangre de tapa amarilla que contenga solución de ácido-citrato-dextrosa (ACD) (75 mM de citrato trisódico, 124 mM de dextrosa y 38 mM de ácido cítrico, pH a 7,4; ACD:sangre 1:9). Mezcle suavemente el contenido del tubo 5x–6x invirtiendo a mano.
- Centrifugar los tubos a 200 x g en un rotor de cucharón oscilante durante 20 minutos en RT.
- Recoger plasma rico en plaquetas (PRP) (3-4 ml) en un tubo inferior cónico de 15 ml y dejar aproximadamente 0,5 ml de prP de la capa de color beige (fracción de aspecto brumoso) para evitar la contaminación. Si se produce alguna contaminación de glóbulos rojos, repita este paso.
- Centrifugar las muestras de PRP a 1.200 x g durante 15 min a RT.
- Lavar los pellets plaquetarios (P1) mediante una resuspensión suave en 1 ml de tampón de lavado de citrato y pellet por centrifugación a 1.200 x g durante 15 min a RT.
- Guarde el pellet de plaquetas pura. Descarta el sobrenadante.
- Resuspenda los gránulos plaquetarios en 600 ml del tampón de ruptura que contiene cócteles inhibidores.
- Sonicar la suspensión plaquetaria usando un sonicador. Coloque la muestra en un mini cubo de hielo. Ajuste el sonicador en el ajuste 3 para 20 s en modo continuo.
NOTA: Asegúrese de limpiar la sonda con un 10% de lejía seguida de agua destilada. - Centrifugar las muestras sonicadas a 20.000 x g durante 30 min a 4 oC para eliminar las fracciones membranosas. Sobrenatantes aliquot en 60 l y almacenar a -80 oC. Evite ciclos repetidos de descongelación/congelación para las fracciones citosólicas plaquetarias.
3. Preparación para el CEI
NOTA: Se combinaron 100 ml de lisato de plaquetas en humanos de pacientes con ELA (n x 8–10), y los sujetos sanos (n x 8–10) se agruparon por separado y se utilizaron para la optimización del ensayo.
- Rellene las plantillas generadas internamente para el diseño CEI (Tabla 1) y la preparación de muestras (Tabla 2). La tabla de preparación de la mezcla de muestras es dinámica y calculará automáticamente cuánto volumen debe eliminarse del origen.
NOTA: Cuando el volumen de origen requerido introducido en la Tabla 2 dinámica, el volumen de búfer de muestra 0,1 X se calculará automáticamente. - Pre-etiquetar 25 tubos PCR de 0,2 ml con capilares #1 #25 y colocarlos en un bastidor de PCR. En el hielo.
- Pre-etiquetar tubos de microcentrífuga de 0,6 ml: uno para cada anticuerpo primario y dilución (si es necesario), uno para el tampón de muestra 0,1x, otro para el luminol-S/peróxido y otro para cada muestra que se va a diluir (si es necesario). Colóquelos en hielo en un estante de tubo.
- Saque el tampón de muestra, el tampón de lavado, una placa y un cartucho proporcionados en el módulo de separación del kit maestro CEI de 12–230 kDa.
- A partir de la nevera de 4 oC, saque el tampón de dilución de anticuerpos, los anticuerpos primarios, los anticuerpos secundarios, la luminol, el peróxido de hidrógeno y el envase estándar. Coloque todos los reactivos sobre hielo, excepto el paquete estándar, que permanece en RT.
NOTA: Los reactivos de los envases estándar están liofilizados y sellados con una cubierta de papel de aluminio. Estos deben girarse brevemente usando una mini centrífuga antes de abrirpara reducir la pérdida del producto. Para abrir, los tubos del reactivo pueden ser perforados por una punta de pipeta o tirados hacia atrás de la esquina. - Para preparar la TDT de 400 mM, añadir 40 ml de agua desionizada al tubo transparente que contiene la TDT.
- Para preparar 40 ml de mezcla maestra fluorescente 5x, añada 20 ml del tampón de muestra 10x y 20 ml de la solución de TDT de 400 mM preparada al tubo rosado suministrado en el kit.
- Para preparar la escalera biotinilada, añadir 16 ml de agua desionizada, 2 ml de tampón de muestra de 10x y 2 ml de la solución de TDT de 400 mM preparada al tubo blanco suministrado en el kit. Mezcle suavemente y transfiera en un tubo PCR de 0,2 ml para desnaturalizar.
- Preparar un tampón de muestra de 0,1x añadiendo 1,5 ml de tampón de muestra de 10x y 148,5 l de agua desionizada a un tubo de microcentrífuga de 0,6 ml. Vórtice para mezclar y colocar en hielo.
- Preparar las diluciones de anticuerpos deseadas. Añadir diluyente de anticuerpos en volúmenes designados a cada tubo de microcentrífuga preetiquetado. Si los volúmenes son idénticos, utilice la técnica de pipeteo inverso23; si no es así, enjuague previamente la punta de la pipeta antes de dispensarla.
NOTA: En este ensayo, se utilizaron anticuerpos pan a-TDP-43 y a-p(S409/410-2) TDP-43. El anticuerpo anti-ERK se utilizó para un control interno para asegurarse de que los componentes del ensayo están funcionando. - Realice el pipeteo inverso para la dilución de anticuerpos como se describe a continuación. Alternativamente, se puede encontrar información adicional en la literatura24.
NOTA: Se prefiere la técnica de pipeteo inverso al dispensar pequeños volúmenes secuenciales de soluciones23. Esta técnica ofrece algunas ventajas: (i) proporcionar un volumen preciso, (ii) eliminar la espuma de reactivo en el orificio de la punta, y (iii) ideal para reactivos de pequeño volumen (<5 l), soluciones viscosas, soluciones tensioactivas y soluciones con alta presión de vapor.- Coloque una punta adecuada en una pipeta y presione el émbolo hasta el segundo tope (Paso-2). Sumerja la punta del pipeteo unos milímetros en la solución. Suelte lentamente el émbolo para llenar la punta del pipeteo con la solución mientras la punta todavía está sumergida en la solución. Retire la punta de la solución y toque suavemente contra el borde del depósito del reactivo para que se retire el exceso de líquido que queda en el exterior de la punta.
- Dispensar la solución presionando el émbolo hacia abajo hasta el primer detonado (Paso-1). No dispensar la solución restante en la punta.
- Vacíe la solución restante en la punta del depósito del reactivo presionando el émbolo hasta el segundo tope (Paso-2). Suelte el émbolo a la posición lista para el siguiente paso de pipeteo.
- Añadir el anticuerpo requerido en volúmenes designados a cada tubo de microcentrífuga preetiquetado (Tabla 1) No enjuague previamente la punta del pipeteo: agréguelo directamente al diluyente y enjuague la punta varias veces para eliminar el anticuerpo. Coloque los tubos sobre hielo.
- Para preparar la mezcla de muestras CEI, realice los pasos enumerados a continuación para los tubos PCR etiquetados con tapa 2 a cap-25: Esto está en el mismo orden que aparece en el Cuadro 1.
- Abra todos los tubos, agregue alícuotas de 1,6 l de tampón de muestra fluorescente 5x a cada tubo utilizando una técnica de pipeteo inverso, luego cierre cada tubo de PCR tras la adición del búfer 5x para minimizar la pérdida de muestra.
- Abra todos los tubos, agregue un tampón de muestra de 0,1x en volúmenes designados en la Tabla 2 a cada tubo y, a continuación, cierre inmediatamente después. Si los volúmenes son idénticos, utilice una técnica de pipeteo inverso. Si no es así, enjuague previamente la punta de la pipeta antes de dispensar un tampón de muestra de 0,1x.
- Abra todos los tubos, agregue la muestra de proteína en los volúmenes designados en la Tabla 2 a cada tubo y, a continuación, cierre inmediatamente después. Si los volúmenes son idénticos, utilice la técnica de pipeteo inverso. Si no es así, enjuague previamente la punta de la pipeta antes de dispensar un tampón de muestra de 0,1x.
- Centrifugar brevemente todos los tubos pcR en una centrífuga de sobremesa (13.000 x g para 30 s), tubos de PCR de deslización/vórtice para mezclar y, a continuación, repetir la centrifugación.
- Transfiera todos los tubos PCR a termocicladores con una tapa calentada. Muestras de desnaturalidad a temperatura y duración definidas (es decir, 95 oC durante 5 min; 70 oC durante 10 min).
NOTA: La temperatura y duración de la desnaturalización deben optimizarse para la proteína objetivo. - Repita el paso 3.12.4.
- Vuelva a colocar todos los tubos PCR en el bastidor del tubo y colóquelos en el hielo.
- Durante el paso de desnaturalización, prepare la solución de desarrollo (solución 1:1 luminol-S:peróxido), luego agregue 200 ml de luminol-S y 200 l de peróxido. Colocar en hielo.
- Para cargar una placa precargada CEI con la muestra preparada anteriormente, dispensar reactivos y muestras en la placa de ensayo que se muestra en el diseño del ensayo(Figura 1). Evite introducir burbujas de aire.
NOTA: Si los volúmenes y la solución son idénticos, utilice una técnica de pipeteo inverso. Si no es así, enjuague previamente la punta del pipeteo antes de dispensar y no expulse el resto al pozo de la placa utilizando el segundo tope de tabulación en la pipeta. Un módulo de separación de 12–230 kDa puede contener una guía de carga de placas codificada por colores. Coloque esta guía debajo de la placa mientras agrega reactivos y muestras al pozo, lo que ayuda visualmente a la carga de la muestra. La guía de carga de placas también se puede descargar desde el sitio web de la empresa.- En la fila E, añadir 15 l de mezcla luminol:peróxido a cada pocto.
NOTA: Idealmente, prepare este reactivo justo antes de su uso y agréguelo a cada pozo. Si esto no es conveniente, esta mezcla puede prepararse no más de 30 minutos antes de la carga de la placa. - En la fila D, hasta bien D1, agregue 10 l de estreptavidina-HRP.
- En la fila D, a los pozos D2–D25, agregue 10 éL de anticuerpo secundario designado.
- En la fila B, a cada pocto, añadir 10 éL de diluyente de anticuerpos.
- En la fila C, a bien C1, añadir 10 l de diluyente de anticuerpos.
- En la fila C, a los pozos C2–C25, agregue 10 s de anticuerpo primario designado.
- En la fila A, hasta bien A1, añadir 5 l de escalera biotinilada desde el tubo de PCR #1.
- En la fila A, a los pozos A2–A25, agregue 3 l de la muestra, los tubos de PCR #2 #25 en los pozos correspondientes #2 #25.
- Agregue 500 ml de tampón de lavado a cada pozo de tampón de lavado designado.
- Centrifugar la placa durante 5 min a 1.000 x g en RT.
- En la fila E, añadir 15 l de mezcla luminol:peróxido a cada pocto.
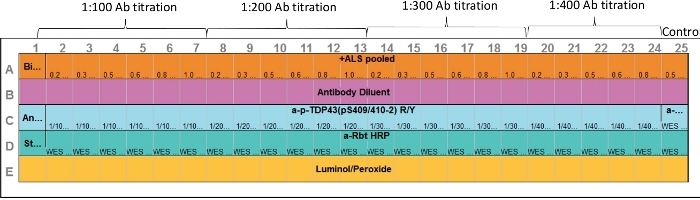
Figura 1: Diseño del ensayo. Tanto la optimización de anticuerpos primarios como la de la muestra de proteína objetivo se pueden realizar en un ensayo. Los capilares 2–7, 8–13, 14–19 y 20–24 representan diversas concentraciones de proteínas y rango de anticuerpos primarios. Capilar 25 representa un control positivo. Se utilizó anticuerpoantir anti-ERK; sin embargo, se puede incluir cualquier control positivo apropiado. Haga clic aquí para ver una versión más grande de esta figura.
4. Realizar el CEI en la placa 1
- En primer lugar, encienda el analizador CEI(Tabla de materiales) y, a continuación, encienda el equipo. Abra el software(Tabla de materiales)
- Conecte el analizador al sistema en línea(Tabla de materiales). Este es un paso necesario para recopilar los datos de ejecución con fines de disparo de problemas y recuperación de datos.
- Haga clic en Instrumento en el menú superior izquierdo y, a continuación, haga clic en Conectar. Seleccione el número de serie del instrumento que aparece como menú emergente. Haga clic en Conectar.
- Seleccione la pestaña"Ensayo"y seleccione Nuevo ensayo o seleccione una plantilla guardada.
- Parámetros de ensayo de entrada (Tabla 1) o modificar plantilla actualmente. Guarde el nombre y la ubicación del archivo.
- Asegúrese de que el indicador de color azul parpadeante en el analizador permanece azul sólido.
- Toque el botón de metal plateado en la parte superior de la puerta naranja para abrir.
- Retire cuidadosamente el cartucho capilar de su embalaje. Inserte el cartucho capilar según lo descrito por el protocolo del fabricante. Si se instala correctamente, la luz interior se convierte en "azul".
- Retire el sello protector de la placa de ensayo. Observe visualmente los pozos precargados para las burbujas de aire. Si se observa, pop ellos con una pequeña punta de pipeta (punta de pipeta P10 de eje largo funciona bien).
- Cargue el soporte de la placa colocando la placa de ensayo y cierre la puerta. En el ordenador, haga clic en el botón Inicio.
- Coloque la bandeja de hielo que contenga reactivos sensibles a la temperatura y muestras en la oscuridad a 4 oC hasta que esté lista para preparar la segunda placa precargada.
- Deje los reactivos/suministros fuera a temperatura ambiente para la segunda placa.
5. Realizar el CEI en la placa 2
NOTA: Esta placa está configurada para analizar los niveles de TDP-43 fosforilados.
- Retirar la bandeja de hielo que se almacena a 4oC y colocarla en el banco, 1 h antes del tiempo de finalización estimado de la primera placa. Recuperar una segunda placa y cartucho.
- Prepare las diluciones de anticuerpos necesarias para la segunda tirada y guárdelas en hielo. Preparar la solución fresca 1:1 luminol-S:peróxido (paso 3.12.8 anterior).
- Remezcle y renticique brevemente la mezcla de muestras y los reactivos necesarios para cargar la placa precargada. Cargue la segunda placa de acuerdo con la Figura 1. Cargue la solución de anticuerpos A-p(S409-410-2) TDP-43 en los pozos de la fila C.
- Una vez completada la primera carrera, deseche la primera placa y el cartucho. Retire el cartucho y colóquelo en el recipiente de un objeto afilado para su eliminación. Mantenga las pegatinas de la placa y el cartucho para fines de referencia.
- Cierre el archivo de software y vuelva a seleccionar la misma plantilla. El software recordará la configuración de la ejecución anterior. Realice los cambios necesarios en la anotación (es decir, cambiando el anticuerpo principal).
- Repita los pasos 4.8–4.10. Guardar todos los reactivos y suministros del módulo de separación del kit maestro de 12–230 kDa
- Deseche la mezcla de muestras CEI, diluciones de anticuerpos, tampón de muestra 0,1x y mezclas luminol-S:peróxido de acuerdo con la normativa universitaria.
6. Análisis de datos
- Una vez completada la ejecución, asegúrese de que se realizan las siguientes comprobaciones de calidad.
- En software, seleccione el icono Mostrar normas y la pestaña Vista de gráfico. Corrija las desalineaciones seleccionando Forzar estándar o haciendo clic con el botón derecho en el pico incorrecto y, a continuación, seleccionando No es un estándar. Realice esta comprobación para cada nuevo capilar.
- Haga clic en Ejemplos y en el icono Vista única. Seleccione #1 capilares (escalera biotinilada) en la pestaña del experimento. Haga clic en el pico en la vista de gráfico y seleccione Eliminar pico,si el software realiza una selección incorrecta del pico.
NOTA: Como ejemplo, la escalera biotinicada de 12–230 KDa mostrará picos de tamaño a 12 kDa, 40 kDa, 66 kDa, 116 kDa, 180 kDa y 230 kDa. El tamaño de los picos de muestra será incorrecto si este paso no se realiza y genera resultados inexactos. - Vea la película electroforética y observe si se produjo alguna migración anormal durante la ejecución.
- Derive los datos (por ejemplo, la tabla de picos, incluido el peso molecular, el área máxima, la altura máxima y la señal a ruido [S/N]) según sea necesario para realizar cálculos adicionales. Hay herramientas de anotación de gráficos ubicadas en la esquina superior derecha de la ventana de Gráfico para proporcionar más información sobre el gráfico.
Resultados
Optimización de la concentración de proteínacitosólica plaquetarias y la valoración de anticuerpos primarios
Es importante establecer un rango dinámico lineal de proteínas citosólicas plaquetarias en el ensayo, ya que los cambios en la señal son directamente proporcionales a los cambios en la proteína en el citosol plaquetario. El uso de mezcla de lisato de plaquetas entera en el ensayo puede reducir la intensidad de la señal de las proteínas diana (TDP-43 y P(S409-412) TDP-43) y contribuir a una señal de fondo alta. Por lo tanto, en este ensayo, se utilizó el sobrenadante transparente (fracción citosólica) después de romper las plaquetas(Figura 2).
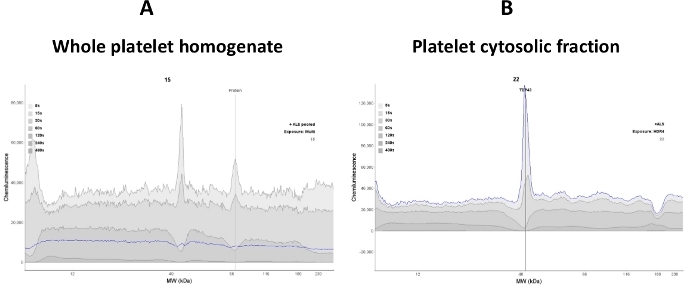
Figura 2: La claridad de la señal depende de la calidad de la muestra. (A) El lisato de plaquetas entera homogeneato interfiere con la unión de anticuerpos anti-TDP-43; por lo tanto, se observó un electroferograma ruidoso. (B) Fracción citosólica plaquetaria se obtuvo de someter el lisato entero a centrifugación (16.000 x g durante 30 min). La mayoría de las proteínas membranosas fueron eliminadas; por lo tanto, se mejoró la unión de anticuerpos anti-TDP-43 a la proteína TDP-43 (traza de línea azul). Haga clic aquí para ver una versión más grande de esta figura.
Se estableció un rango dinámico lineal para la concentración de proteína de citosol plaquetario en 0,2–0,8 mg/ml. Se adoptó una plantilla de ensayo para que tanto la concentración de proteínas como la valoración primaria de anticuerpos se pudieran realizar en un ensayo(Figura 3).
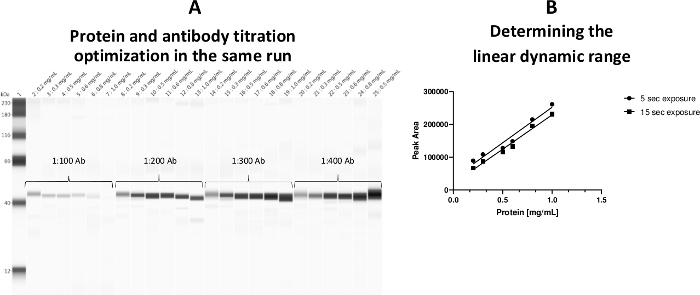
Figura 3: Rango dinámico lineal para la concentración de proteína de citosol plaquetario. (A) Tanto las concentraciones proteicas como las valoraciones de anticuerpos se optimizaron en una placa durante la misma carrera. (B) Se estableció el rango de trabajo lineal (0,2–0,8 mg/ml) para la proteína. Una carga proteica de 0,5 mg/ml fue etiquetada por un anticuerpo a-ERK como el control positivo (capilar 25). Haga clic aquí para ver una versión más grande de esta figura.
Cabe señalar que el contenido de glicerol en el tubo de preparación de la muestra debe ser inferior al 20% (final), de lo contrario la alta concentración de glicerol afectará negativamente a la unión primaria de anticuerpos.
Determinar el tiempo óptimo de exposición
En la versión anterior del software, el tiempo óptimo de exposición tenía que determinarse trazando el área pico contra la concentración de proteínas (mg/ml). La nueva versión proporciona una nueva herramienta denominada perfil de detección de alto rango dinámico (HDR)(Figura 4). El uso del panel de imágenes proporcionó la opción de ver todos los tiempos de exposición (es decir, 5 s, 15 s, 30 s, 60 s, 120 s, 240 s, 480 s) juntos. El software informático analizó todos los tiempos de exposición e identificó automáticamente el mejor tiempo de exposición (HDR). El perfil de detección HDR proporcionó un rango dinámico significativamente más amplio debido a la mayor sensibilidad de CEI, lo que significa una mejor detección y cuantificación en un rango de concentración de muestra sin mayores. Sin embargo, los usuarios todavía tienen la opción de elegir cualquier tiempo de exposición que satisfaga el objetivo experimental. Usando esta característica, se encontró un tiempo óptimo de exposición para la proteína TDP-43. El pico representa el tiempo de exposición óptimo(Figura 4A). Se definió un único tiempo de exposición (4 s) para este anticuerpo después de revisar los nueve tiempos de exposición que oscilan entre 1–512 s(Figura 4B).

Figura 4: Perfil de detección de alto rango dinámico (HDR) para una proteína objetivo. (A) El pico de proteína TDP-43 representa el tiempo de exposición óptimo para la proteína objetivo. la valoración a-TDP-43 Ab fue de 1:300, y la concentración de proteína de citosol plaquetario fue de 0,5 mg/ml. La línea azul definida por software indica el tiempo de exposición óptimo. (B) Esta figura representa un tiempo de exposición único definido por el usuario (4 s) después de revisar los nueve tiempos de exposición que oscilan entre 1–512 s. Haga clic aquí para ver una versión más grande de esta figura.
Niveles de TDP-43 en citosol plaquetario humano de pacientes con ELA
Se realizó un desarrollo de biomarcador de base sanguínea. Utilizando condiciones de ensayo optimizadas, se analizaron fracciones citosólicas de plaquetas obtenidas de pacientes con ELA utilizando dos conjuntos de anticuerpos (es decir, anticuerpos anti-TDP-43 [Pan], un anticuerpo que reconoce los derivados fosforilados de la proteína TDP-43; aquí se utilizó a-P [S409/410-2] TDP-43). En esta demostración, se presentan TDP-43 específicos de la enfermedad y su derivado fosforilado (Figura 5).
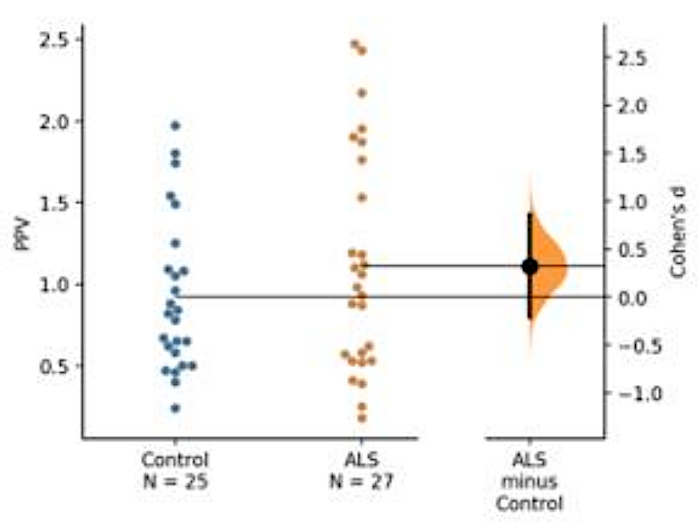
Figura 5: Representación del valor de fosforilación predictiva (VPP) de TDP-43. La cantidad absoluta de TDP-43 fosforilado y TDP-43 sin mostrar mucha diferencia entre la ELA y los grupos de control. Sin embargo, el PpV indicó un ligero aumento en la cohorte de ELA, aunque no hubo diferencia estadística entre los dos grupos debido a un número insuficiente de sujetos (ALS 25, control 27). El valor d de un cohen bajo entre los medios de ELA y el grupo de control mostró un tamaño de efecto bajo entre los dos grupos debido al pequeño tamaño de la muestra (control 25, ALS a 27). Haga clic aquí para ver una versión más grande de esta figura.
El TDP-43 total se cuantificó utilizando la curva de calibración(Figura 6)

Figura 6: Curva de calibración estándar. Las concentraciones de proteínaT-43 recombinantes compradas comercialmente se utilizaron para construir una curva estándar. Cada dato representa el promedio de triplicados. Las intensidades de la banda proteica dependían de la concentración (Inset). Haga clic aquí para ver una versión más grande de esta figura.
La cuantificación de la proteína TDP-43 fosforilada no fue posible debido a la falta de disponibilidad comercial de esta proteína. En su lugar, se estableció un valor de fosforilación pronosticado (VPP) que define el porcentaje de las especies fosforiladas de TDP-43. El VPP se determinó a partir de dos ensayos secuenciales de CEI para la misma muestra utilizando la siguiente ecuación.

La variabilidad del ensayo intra y entre corridas se probó en fracciones citosólicas plaquetarias de ALS humanas agrupadas (Figura 7)
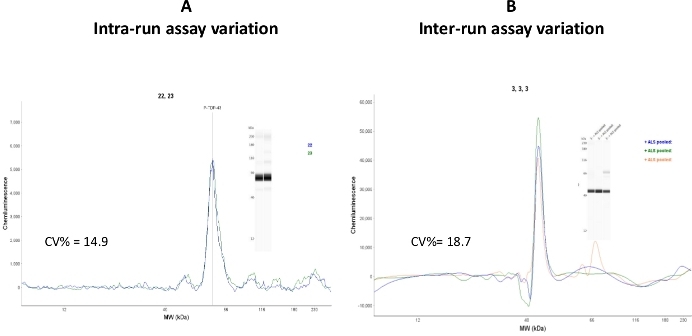
Figura 7: Variaciones del ensayo. (A) Dos capilares cargados con la misma muestra fueron analizados por CEI, y la variación del ensayo intra-corrida se calculó como CV% a 14,9. (B) La misma muestra se analizó en tres días de ensayo diferentes y en tres corridas de ensayo diferentes. La variación del ensayo entre corridas se calculó como CV% a 18,7. Haga clic aquí para ver una versión más grande de esta figura.
Aunque los valores de variación del coeficiente intra-run (variación capilar-capilar) cayeron en el rango aceptable (CV% a 14,9), el valor del ensayo entre corridas fue relativamente alto (CV% a 18,7). Se interpreta que esta variación puede deberse al uso de cartuchos capilares y placas de muestra de diferentes lotes. Se recomienda realizar estudios de reproducibilidad en componentes CEI que tengan el mismo número de lote.
Tabla 1: Plantilla de carga de placas de ensayo CEI. Haga clic aquí para descargar esta tabla.
Tabla 2: Plantilla interactiva de preparación de mezclas de muestras. Después de introducir la concentración de proteína sin valor a partir de muestras desconocidas, las células interactivas calcularán automáticamente cuánto volumen debe utilizarse para preparar la mezcla de muestras. Haga clic aquí para descargar esta tabla.
Discusión
El inmunoensayo capilar basado en electroforéticos es ahora el método de elección para el análisis de muestras de alto rendimiento y las pruebas de detección de fármacos25. Pequeños volúmenes de muestra, componentes de ensayo bien optimizados, plataforma e instrumentación de ensayo fácil de usar, gasto de reactivos y bajo porcentaje de CV son ventajas principales26,27. Aunque existen varios métodos para separar proteínas en diferentes modalidades de ensayo, el CEI basado en anticuerpos descrito aquí puede ser adaptado por pequeños laboratorios que se dedican al desarrollo de biomarcadores a base de sangre. La tecnología de ensayo CEI utilizada aquí proporciona mediciones fiables, reproducibles y sensibles para TDP-4328 y su derivado fosforilado5.
El sistema CEI también proporciona una opción de multiplexación de analizar TDP-43 y sus derivados fosforilados simultáneamente y proporcionar la cuantificación directa de la proteína diana, si hay disponible proteína diana purificada o recombinante. La proteína TDP-43 recombinante de longitud completa está disponible comercialmente; sin embargo, el derivado de TDP-43 fosforilado recombinante no lo es. Dado que el TDP-43 fosforilado no está disponible comercialmente, se implementó un valor de fosforilación predictiva (VPP) para evaluar el perfil de TDP-43 en pacientes con ELA. Pan TDP-43 y cantidades de TDP-43 fosforiladas fueron etiquetados permanentemente con un fluoróforo; por lo tanto, el perfil TDP-43 sigue siendo el mismo con o sin una unidad cuantitativa (es decir, ng/mL, pg/mL, etc.). Aunque determinar la cantidad absoluta de TDP-43 y sus derivados fosforilados (es decir, P [S409-410-12] TDP-43) proporciona una medición más cuantitativa, el cálculo de PPV elimina la necesidad del TDP-43 fosforilado recombinante para la estandarización, ya que no está disponible comercialmente.
CEI proporciona varios puntos de control en la plataforma de ensayo para identificar con precisión el problema en caso de que un ensayo falle. Esto elimina los obstáculos y proporciona un mejor diseño experimental. El procedimiento de ensayo está totalmente automatizado, excepto para llenar la placa de muestra. Esta es una característica significativa en comparación con el análisis de hinchas occidentalestándar. Esta característica proporciona coherencia de ejecución a ejecución. Aunque cada laboratorio tiene procedimientos operativos estándar únicos, es importante adherirse a las prácticas que minimizan los errores humanos. Por ejemplo, es fundamental preparar la mezcla luminol-S/peróxido justo antes de la carga de la placa, ya que la adición de peróxido en luminol inicia la reacción enzimática y consume el sustrato de luminol. La carga de muestras y anticuerpos primarios/secundarios en pozos de placas sin burbujas de aire también son pasos de importancia crítica.
Además, dado que los pozos de placas son pequeños en volumen y no hay espacio entre pozos, los usuarios deben tener cuidado durante el pipeteo, que es el paso más importante ya que todo lo demás está automatizado. El orden de carga de las muestras, anticuerpos y otros reactivos es importante para la coherencia del ensayo(Figura 1). El proceso de preparación de la placa toma alrededor de 40-45 min. Por lo tanto, se recomienda cargar primero la placa con los componentes de ensayo necesarios y preparar la mezcla luminol-S/peróxido justo antes de pipetear. De esta manera, hay una secuencia consistente de adición de reactivos, y se logrará una intensidad de señal de luminiscencia consistente. No se recomienda utilizar un reactivo de luminol-S/peróxido caducado, ya que afecta principalmente a la resistencia del peróxido. Los recientes avances en la introducción del sistema de búfer dividido e incluyendo el rango de compatibilidad con productos químicos y detergentes han mejorado la calidad del ensayo y han producido resultados más reproducibles y predecibles. Ahora, un nuevo analizador combinado del mismo fabricante posee una característica para analizar las muestras etiquetadas con anticuerpos conjugados de quimioluminiscencia y fluorescencia en la misma carrera. Esta nueva característica elimina la necesidad de ejecutar consecutivamente dos placas individuales y elimina la variación de ejecución a ejecución.
Las placas de ensayo deben almacenarse a temperatura ambiente. Si se elige mantener las placas de ensayo en un refrigerador de 4 oC, las placas deben sacarse la noche anterior al ensayo y llevarse a temperatura ambiente. Los pozos de muestra cargados incorrectamente deben lavarse ampliamente (4-5 veces) con el tampón suministrado en el kit antes de agregar la muestra correcta. Cada anticuerpo primario y muestras biológicas son únicas; por lo tanto, la optimización de anticuerpos/proteínas debe realizarse antes de analizar las muestras de proteínas diana en fluidos biológicos.
Aquí, el tiempo de incubación de anticuerpos primarios se estableció para 30 min por defecto. Si la señal es débil, los usuarios deben considerar aumentar el tiempo de incubación de anticuerpos primarios hasta alcanzar la intensidad de señal deseada sin agotamiento de la señal de fluorescencia. En el el lugar de las plaquetas humanas, se prepararon y utilizaron muestras agrupadas de pacientes para un ensayo de optimización. La agrupación de muestras representa mejor la variación entre las biomoléculas objetivo. Se recomienda utilizar sobrenatantes claros en lugar de lisados totales o homogeneizados totales para el CEI.
La alta concentración de proteína en la mezcla entera de lisato plaquetario puede disminuir la relación señal-ruido(Figura 2). Se deben evitar ciclos repetidos de congelación-descongelación de muestras, ya que esto afecta negativamente a la unión de anticuerpos primarios. Los ingredientes del tampón de lysato son importantes, ya que algunos reactivos no son compatibles con CEI29. Se recomienda cotejar la lista de reactivos compatibles que se proporcionan en el sitio web del fabricante antes de la preparación de la muestra. Esta es una limitación del sistema que no tolera condiciones de alta rigelpara para la preparación de muestras. Se recomienda optimizar los parámetros de ejecución del ensayo (es decir, dilución de anticuerpos primarios, concentración de proteínas, tiempo de incubación de anticuerpos primarios, etc.) utilizando muestras agrupadas para analizar posteriormente las muestras individuales.
Divulgaciones
Los autores declaran que no hay interés financiero competidor, excepto proteinSimple, Inc. cubrió el costo de publicación de este manuscrito.
Agradecimientos
Esta investigación fue patrocinada por una subvención intramuros otorgada para A.A. Este trabajo fue apoyado por una subvención CTSA de NCATS otorgada al University of Kansas Medical Center for Frontiers: The Heartland Institute for Clinical and Translational Research (#UL1TR606381). Los contenidos son responsabilidad exclusiva de los autores y no representan necesariamente las opiniones oficiales de los NIH o NCATS. Estamos agradecidos por la clínica DE ELS de la Universidad de Kansas Medical Center por obtener la aprobación de irB para la recolección de muestras de sangre de pacientes voluntarios sanos y de ELA. Los autores agradecen a Emre Agbas por la corrección del manuscrito.
Materiales
| Name | Company | Catalog Number | Comments |
| 12-230 kDa Separation kit | ProteinSimple | SM-W004 | Contains pre-filled assay plate and 25-channel capillary cartridge |
| 3000G Thermocycler | Techne | FTC3G/02 | We used this thermocylcer for heating the sample mix |
| Anti-Mouse detection kit | ProteinSimple | 042-205 | Includes HRP-conjugated secondary antibody, buffer, luminol reagent, molecular weight marker |
| Anti-P(S409-410) TDP-43 antibody | ProteinTech | 22309-1-AP | Primary antibody that recognizes phosphorylated TDP-43 |
| Anti-P(S409-412) TDP-43 antibody | CosmoBio-USA | TIP-PTD-P02 | Primary antibody that recognizes phosphorylated TDP-43 |
| Anti-Rabbit detection kit | ProteinSimple | DM-001 | Includes HRP-conjugated secondary antibody, buffer, luminol reagent, molecular weight marker |
| Anti-TDP-43 (pan) antibody | ProteinTech | 10782-2-AP | Primary antibody that recognizes whole TDP-43 protein |
| Compass for SimpleWestern (SW) | ProteinSimple | Ver.4.0.0. | Compass for SW is the control and data analysis application for SimpleWestern instruments |
| Sonic Dismembrator; Model100 | Fisher Scientific | Sonicator. Used to rupture the cell membrane. This model is discontinued (Model XL2000-350) | |
| Table top centrifuge | Eppendorf | 22625004 | Model# 5810 with swinging plate bucket |
| Wes analyzer | ProteinSimple | 55892-WS-2203 | Performs the capillary gel electrophoresis |
Referencias
- Blair, P., Flaumenhaft, R. Platelet alpha-granules: basic biology and clinical correlates. Blood Reviews. 23 (4), 177-189 (2009).
- Mercado, C. P., Kilic, F. Molecular mechanisms of SERT in platelets: regulation of plasma serotonin levels. Molecular Interventions. 10 (4), 231-241 (2010).
- Goubau, C., et al. Regulated granule trafficking in platelets and neurons: a common molecular machinery. European Journal of Paediatric Neurology. 17 (2), 117-125 (2013).
- Basu, S. S., et al. Human platelets as a platform to monitor metabolic biomarkers using stable isotopes and LC-MS. Bioanalysis. 5 (24), 3009-3021 (2013).
- Wilhite, R., et al. Platelet phosphorylated TDP-43: an exploratory study for a peripheral surrogate biomarker development for Alzheimer's disease. Future Science OA. 3 (4), 238 (2017).
- Worth, A. J., et al. LC-MS Analysis of Human Platelets as a Platform for Studying Mitochondrial Metabolism. Journal of Visualized Experiments. (110), e53941 (2016).
- Statland, J. M., et al. Rasagiline for amyotrophic lateral sclerosis: A randomized, controlled trial. Muscle and Nerve. 59 (2), 201-207 (2019).
- Charytan, D. M., et al. Safety and cardiovascular efficacy of spironolactone in dialysis-dependent ESRD (SPin-D): a randomized, placebo-controlled, multiple dosage trial. Kidney International. 95 (4), 973-982 (2019).
- Ugras, S. E., Shorter, J. RNA-Binding Proteins in Amyotrophic Lateral Sclerosis and Neurodegeneration. Neurology Research International. , 432780 (2012).
- Amador-Ortiz, C., et al. TDP-43 immunoreactivity in hippocampal sclerosis and Alzheimer's disease. Annal of Neurology. 61 (5), 435-445 (2007).
- Baloh, R. H. TDP-43: the relationship between protein aggregation and neurodegeneration in amyotrophic lateral sclerosis and frontotemporal lobar degeneration. FEBS Journal. 278 (19), 3539-3549 (2011).
- Buratti, E., Baralle, F. E. The molecular links between TDP-43 dysfunction and neurodegeneration. Advances in Genetics. 66, 1-34 (2009).
- Guo, W., et al. An ALS-associated mutation affecting TDP-43 enhances protein aggregation, fibril formation and neurotoxicity. Nature Structural Molecular Biology. 18 (7), 822-830 (2011).
- Geser, F., et al. Motor neuron disease clinically limited to the lower motor neuron is a diffuse TDP-43 proteinopathy. Acta Neuropathologica. 121 (4), 509-517 (2011).
- Neumann, M., et al. Ubiquitinated TDP-43 in frontotemporal lobar degeneration and amyotrophic lateral sclerosis. Science. 314 (5796), 130-133 (2006).
- Buratti, E., Baralle, F. E. TDP-43: gumming up neurons through protein-protein and protein-RNA interactions. Trends in Biochemical Sciences. 37 (6), 237-247 (2012).
- Fallini, C., Bassell, G. J., Rossoll, W. The ALS disease protein TDP-43 is actively transported in motor neuron axons and regulates axon outgrowth. Human Molecular Genetics. 21 (16), 3703-3718 (2012).
- Ayala, Y. M., et al. Structural determinants of the cellular localization and shuttling of TDP-43. Journal of Cell Sciences. 121, 3778-3785 (2008).
- Fiesel, F. C., Kahle, P. J. TDP-43 and FUS/TLS: cellular functions and implications for neurodegeneration. FEBS Journal. 278 (19), 3550-3568 (2011).
- Birsa, N., Bentham, M. P., Fratta, P. Cytoplasmic functions of TDP-43 and FUS and their role in ALS. Seminars in Cell and Development Biology. , (2019).
- Liachko, N. F., et al. CDC7 inhibition blocks pathological TDP-43 phosphorylation and neurodegeneration. Annals of Neurology. 74 (1), 39-52 (2013).
- Qureshi, A. H., et al. Proteomic and phospho-proteomic profile of human platelets in basal, resting state: insights into integrin signaling. PLoS One. 4 (10), 7627 (2009).
- Suominen, I., Koivisto, S. Increasing Precision When Pipetting Protein Samples: Assessing Reliability of the Reverse Pipetting Technique. American Laboratory. , (2011).
- . Pipetting tool box for life sciences Available from: https://www.mt.com/us/en/home/library/guides/laboratory-division/life-science/pipetting-toolbox-for-life-sciences.html (2019)
- Hale, L. J., et al. 3D organoid-derived human glomeruli for personalised podocyte disease modelling and drug screening. Nature Communication. 9 (1), 5167 (2018).
- Chen, J. Q., Wakefield, L. M., Goldstein, D. J. Capillary nano-immunoassays: advancing quantitative proteomics analysis, biomarker assessment, and molecular diagnostics. Journal of Translational Medicine. 13, 182 (2015).
- Moser, A. C., Hage, D. S. Capillary electrophoresis-based immunoassays: principles and quantitative applications. Electrophoresis. 29 (16), 3279-3295 (2008).
- Fourier, A., et al. Development of an automated capillary nano-immunoassay-Simple Western assay-to quantify total TDP43 protein in human platelet samples. Analytical and Bioanalytical Chemistry. 411 (1), 267-275 (2019).
- . Compatibility, S.W.S.A.B Available from: https://www.proteinsimple.com/technical_library.html (2017)
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados