Method Article
Analyse directe des cellules isolées par spectrométrie de masse à la pression atmosphérique
Dans cet article
Résumé
Analyse cellulaire unique est effectué par spectrométrie de masse sur les cellules végétales et animales à la pression atmosphérique en utilisant une fibre optique pour l'échantillon aiguisé les cellules pour l'ionisation electrospray ablation laser (LAESI) spectrométrie de masse.
Résumé
Analyse des produits biochimiques dans des cellules individuelles est importante pour comprendre le métabolisme cellulaire, cycle cellulaire, l'adaptation, les états pathologiques, etc Même les types de cellules présentent la même composition biochimique hétérogènes en fonction de leurs conditions physiologiques et les interactions avec l'environnement. Les méthodes classiques de spectrométrie de masse (MS) utilisé pour l'analyse des biomolécules dans des cellules individuelles reposent sur longue préparation des échantillons. Suppression des cellules de leur environnement naturel et de traitement des échantillons approfondie pourrait conduire à des changements dans la composition cellulaire. Méthodes d'ionisation ambiante permettant l'analyse des échantillons dans leur environnement naturel et sans longue préparation des échantillons. 1 Les techniques basées sur l'infrarouge moyen (mi-IR) par ablation laser des matériaux biologiques à 2,94 um de longueur d'onde d'excitation utiliser la soudaine d'eau que les résultats en phase explosion. 2 techniques d'ionisation ambiante basées sur le rayonnement laser IR moyen, comme d'ionisation électrospray ablation laser (LAESI) et la pression atmosphérique infrarouge laser assistée par matrice désorption-ionisation (AP IR-MALDI), ont démontré avec succès la capacité d'analyser directement l'eau tissus riches et les liquides biologiques à la pression atmosphérique. 3-11 En LAESI le panache mi-IR d'ablation laser qui se compose essentiellement de particules neutres de la coalescence des gouttelettes d'échantillon electrospray très chargé pour produire des ions. Récemment, mi-IR ablation des cellules individuelles a été réalisée en fournissant le rayonnement IR moyen par une fibre gravé. Le panache généré par cette ablation était postionized par un electrospray permettant l'analyse des métabolites variés dans des cellules individuelles par LAESI-MS 12. Cet article décrit le protocole détaillé pour l'analyse cellulaire unique en utilisant LAESI-MS. La vidéo présentée montre l'analyse d'une seule cellule épidermique de la peau d'une ampoule de Allium cepa. Le schéma du système est montré dans la figure 1. Un exemple représentatif de l'ablation seule cellule et un spectre de masse LAESI de la cellule sont fournis dans la Figure 2.
Protocole
1. Composants optiques
- L'ablation laser pour l'ionisation electrospray ablation laser (LAESI) spectrométrie de masse (MS) est produite par un laser à impulsion de 5 ns à 2,94 um de longueur d'onde. Un oscillateur paramétrique optique accordable entraîné par un laser Nd: YAG (Opolette 100, Opotek Inc, Carlsbad, CA) est utilisée pour l'ablation de cette étude. Le taux de redoublement est sélectionné entre 5 et 100 Hz. Ceci est un laser de classe IV qui lors de l'exposition directe peut causer de graves dommages permanents à l'œil ou la peau. La réflexion diffuse du faisceau laser peut également être dangereux pour la peau ou les yeux. Porter une lunette laser approprié de protection.
- La fibre optique en verre à base de dioxyde de germanium a été obtenue à partir Fiber Systems Infrarouge, Inc (Silver Spring, MD). S'il ya Hytrel et de polyimide de revêtements sur la fibre suivez les instructions ci-dessous pour les enlever de la fin. Chauffer 1-méthyl-2-one à 130-150 ° C sous une hotte. Tremper les extrémités des fibres que vous voulez bande dans ce liquide pendant environ 1 minute ou jusqu'à ce que le revêtement commence à ramollir et décoller. Tremper le revêtement ramolli dans du méthanol ou l'isopropanol pendant une minute, et essuyer tout revêtement restant avec une serviette non pelucheuse. Après avoir enlevé le revêtement, cliver les deux extrémités de la fibre avec une lame de saphir (KITCO Fibre Optique, Virginia Beach, Virginie) en marquant et en douceur les enfonçant.
- Pour atteindre la netteté voulue, chimiquement etch une extrémité de la pointe de la fibre de 1% (v / v) d'acide nitrique (qualité réactif) solution. Verticalement plonger l'extrémité de la fibre choisie dans la solution acide à une profondeur de 300 à 500 um après le contact initial. Après environ 15 minutes de la gravure, la pointe spontanément détacher de la surface d'acide. Il en résulte une pointe fibre affûtés avec ~ 15 um de rayon de courbure. Rincer à l'eau désionisée pour éliminer tout résidu d'acide.
- Montez la fin gravé de la fibre sur un micromanipulateur (MN-151, Narishige, Tokyo, Japon) et l'apporter à la proximité (~ 20 um) de la surface des cellules pour le dépôt de l'efficacité énergétique.
- Tenir l'extrémité non gravée de la fibre optique par une fibre nue mandrin (BFC300, Siskiyou Corporation, Grants Pass, OR). Pour l'alignement optique, le mandrin de fibre est montée sur un traducteur cinq axes (BFT-5, Siskiyou Corporation, Grants Pass, OR). L'énergie du laser (0,5 à 1 mJ) est couplée dans la fibre par la focalisation du faisceau par un fluorure de calcium plano-convexe ou lentilles ZnSe antireflet (infrarouge, produits optiques, de Farmingdale, New York) sur sa non gravée fin. Miroirs d'or protégées (PF10-03-M01, Thorlabs, Newton, NJ) sont utilisés pour diriger le faisceau laser moyen IR sur la lentille de focalisation.
2. Configuration électronébulisation
- Le système peut être construit par électrospray en utilisant les composants suivants: l'union avec embout métallique conducteur perfluoré, raccords, tubes de manches, l'aiguille du port (par exemple, U-435, M215, F-331Nx, F-242x, 9013, respectivement IDEX Health & Sciences, Oak Harbor, WA), ainsi que des tubes de silice fondue (par exemple, CT360-100-50-5, Nouveau Objectif Inc, Woburn, MA). L'émetteur recommandée est faite d'acier inoxydable et a une pointe effilée avec un ID de 50 microns (par exemple, MT320-50-5-5, Nouveau Objectif Inc, Woburn, MA).
- Préparer une solution de méthanol à 50% avec de l'acide acétique à 0,1% (v / v) pour l'électrospray. La solution est pompée à un débit de 200 à 300 nl / min par une pompe seringue (Harvard Apparatus, Holliston, MA) en utilisant, par exemple, un. 500 seringues ul (81222, Hamilton Company, Reno, NV)
- Appliquer à haute tension entre 2800 et 3000 V pour l'union de métal par une alimentation régulée (PS350, Stanford Research Systems Inc, Sunnyvale, CA) pour générer une électronébulisation stable. Assurez-vous que toutes les connexions électriques sont sécurisés et blindés avec le blindage à la terre. Le contact direct avec la haute tension exposés peut entraîner un choc électrique.
3. Manipulation des échantillons
- Obtenir le tissu vivant ou d'un échantillon de cellules provenant d'une source appropriée et de les garder comme recommandé avant l'analyse. Les ampoules Allium cepa pour cette démonstration ont été achetés dans un magasin local. Couper une ampoule longitudinalement par un scalpel chirurgical. Un segment de quelques centimètres d'une échelle a été sectionnée en une bande. Une monocouche intacte du tissu interne épidermique est décollée.
- La surface humide de l'épiderme est utilisé pour monter le tissu sur une lame de microscope en verre pré-nettoyés. Tenez la lame par un support de plaque d'usage général (FP01, Thorlabs Inc, Newton, NJ), monté sur une platine de translation à trois axes pour le positionnement. Acquérir les spectres de masse immédiatement après le montage de l'échantillon pour éviter la dégradation des cellules.
4. Visualization System
- Deux microscopes à longue distance sont utilisés pour sélectionner les cellules d'analyse et de maintenir la distance entre la pointe de la fibre aiguisé et la surface des cellules. Ce dernier est monté sous l'angle 15 ° -30 ° mesuré à partir de la surface. Ce système se compose d'alMicroscope ong vidéo à distance (7x zoom optique de précision, Edmund Optics, Barrington, NJ), avec une infinité 5x corrigées objectif (Apo M Plan de 5x, Mitutoyo Co., Kanagawa, Japon) équipé d'une caméra CCD (F131 Marlin, Allied Vision Technologies , Stadtroda, Allemagne) pour la surveillance et la capture d'image.
- Le microscope deuxième vidéo est monté à un angle droit de la surface de l'échantillon de visualiser les cellules à partir du haut. Ce système fournit une rétroaction visuelle pour aligner la pointe de la fibre sur la cellule sélectionnée pour l'ablation et l'analyse. Il se compose d'un zoom optique 7x de précision (Edmund Optics, Barrington, NJ), équipé d'un débordement 10x corrigées à long lentille de l'objectif de travail à distance (M Plan d'Apo 10x, Mitutoyo Co., Kanagawa, Japon) et une caméra CCD.
5. Acquisition des spectres de masse
- Allumez le laser, l'électronébulisation et le spectromètre de masse, par exemple, un quadripôle à temps de vol du système (Q-TOF Premier, Waters, Milford, MA). Optimiser la géométrie de la source d'ions LAESI en ajustant la position de la tache de l'ablation et l'émetteur electrospray rapport à l'autre et l'orifice du spectromètre de masse pour atteindre les intensités ioniques maximum.
- Sélectionnez la cellule d'intérêt pour l'analyse en utilisant le système de visualisation haut de vue. Après sélection, déplacez le stade de l'échantillon d'apporter la cellule sélectionnée directement en dessous de la pointe aiguisée de la fibre optique. En utilisant le microscope en vue latérale de réajuster le bout-à-cellule de distance de surface à ~ 20 um.
- Impulsions laser feu à la cellule sélectionnée par la pointe de la fibre gravé. Ce résultat dans la perforation de la paroi cellulaire et l'éjection du cytoplasme sous forme de matières particulaires. Après postionization par l'électronébulisation, les ions produits sont collectées par le spectromètre de masse et les spectres de masse sont enregistrés.
- Après l'acquisition de données, mettre le laser, l'électronébulisation et le spectromètre de masse en mode veille ou éteignez-les. Gardez l'ablation A. échantillon de tissu pour l'observation de la LCPE option par microscopie optique.
6. Les résultats représentatifs
L'ablation réussie d'une seule cellule dans les résultats de l'éclatement de la paroi cellulaire et la collecte d'un spectre de masse LAESI. Une expérience infructueuse résulte habituellement en un rien de l'ablation et / ou pas de spectre de masse. Pour fins de démonstration, nous présentons les résultats de l'analyse LAESI-MS d'une seule cellule épidermique embarqué d'un A. Ampoule de la LCPE. Figure 2a montre une image de microscopie optique représentant après le prélèvement d'une cellule. La paroi cellulaire est perforée et l'étendue de la perforation est limité par les frontières avec les cellules voisines. Les cellules adjacentes semblent être intactes. Figure 2b montre un spectre de masse représentant LAESI produite à partir de la cellule. Une grande variété d'ions sont détectés à partir de la A. cellulaire cepa et basé sur leurs masses exactes, modèles de distribution des isotopes, et, dans certains cas, les spectres de masse en tandem, ils sont provisoirement affectés à des métabolites endogènes. Les ions détectés à partir d'une seule cellule ont été similaires à celles observées dans l'analyse du tissu même par conventionnelles LAESI-MS de plusieurs cellules. 13
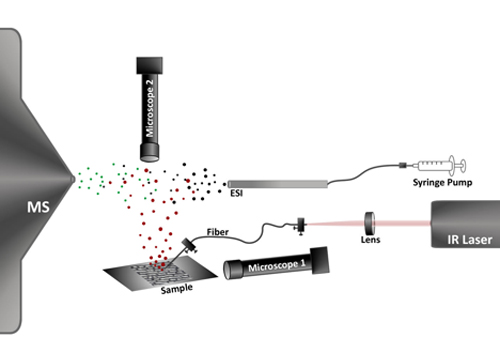
Figure 1. Schéma d'analyse cellulaire unique par LAESI-MS. Une impulsion laser IR mi-est couplée dans une fibre optique et livrés à l'échantillon placé sur lame de verre. La pointe de la fibre aiguisé focalise la lumière dans la cellule cible et l'énergie déposée éclate la cellule. Le panache d'ablation produite (points rouges) est fusionné avec un panache électronébulisation (points noirs) les gouttelettes coalesce (points verts) conduisant à la production d'ions échantillon spécifique. Ces ions sont analysés et détectés par le spectromètre de masse (MS). Deux longs microscopes vidéo à distance, Microscope Microscope 1 et 2, sont utilisés pour contrôler la distance entre la pointe de la fibre et la surface de la cellule et à sélectionner une cellule d'analyse, respectivement.
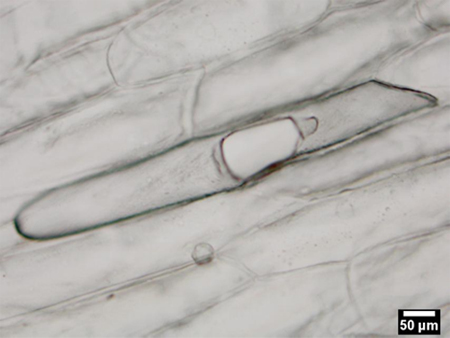
Figure 2a. Ablation marque sur une seule cellule épidermique d'un A. Ampoule de la LCPE. Les cellules adjacentes ne présentent pas de dégâts visibles et par la suite peuvent être analysés séparément.
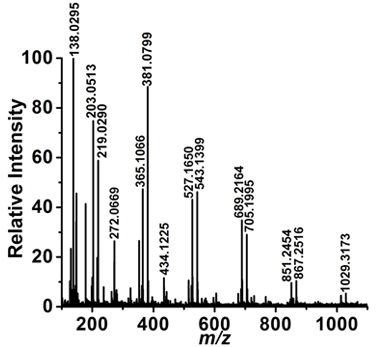
Figure 2b Spectre de masse. Correspondant à l'ablation d'un simple A. cepa épidermique cellulaire montre la présence de métabolites primaires et secondaires.
Discussion
La teneur en eau du cytoplasme des cellules et la résistance à la traction de la paroi cellulaire ou la membrane sont des facteurs critiques qui régissent l'ablation des cellules individuelles pendant LAESI-MS. La fluence laser doit être ajustée pour atteindre les seuils d'ablation des différents types de cellules. La fluence laser livré dépend de l'énergie de l'impulsion laser et de la distance entre la pointe de la fibre et la surface des cellules. Minimiser la perturbation des cellules voisines lors de l'analyse unicellulaire est critique. Garder l'énergie du laser au seuil d'ablation limite l'effet des analyses sur les cellules adjacentes.
Une des applications possibles est d'utiliser des cellules individuelles que les pixels naturelles volumétrique (voxels) pour Imagerie chimique par la SP. Par rapport à la collecte de données sur une grille artificielle souvent rectangulaire, imagerie chimique d'un tissu, une cellule à une époque est plus susceptible de conserver l'organisation spatiale des interactions biochimiques entre les cellules.
Déclarations de divulgation
Remerciements
Les auteurs reconnaissent le soutien financier des institutions suivantes: la National Science Foundation (Grant 0.719.232), le Department of Energy (Grant DEFG02-01ER15129), la WM Keck Foundation (Grant 041 904), et l'Université George Washington Fonds pour l'amélioration de la recherche. Les auteurs sont reconnaissants pour les fibres optiques à base GEO2 généreusement fournis par Fiber Systems Infrarouge (Silver Spring, MD), ainsi que pour la première discussion sur le protocole relatif à la gravure en fibre de Mark E. Reeves et Joan A. Hoffmann de l'université George Washington Université. Les auteurs souhaitent également remercier Jessica A. Stolee pour son aide lors de l'enregistrement vidéo de ce protocole.
matériels
| Name | Company | Catalog Number | Comments |
| Acetic acid | Fluka | 45727 | |
| Methanol | Fluka | 65548 | |
| 1-methyl-2-pyrrolidinon | Sigma-Aldrich | M79603 | |
| Water | Fluka | 39259 |
Références
- Cooks, R. G., Ouyang, Z., Takats, Z., Wiseman, J. M. Ambient Mass Spectrometry. Science. 311, 1566-1570 (2006).
- Chen, Z. Y., Vertes, A. Early plume expansion in atmospheric pressure midinfrared laser ablation of water-rich targets. Physical Review E. E77, 036316-036316 (2008).
- Li, Y., Shrestha, B., Vertes, A. Atmospheric Pressure Molecular Imaging by Infrared MALDI. Mass Spectrometry. Analytical Chemistry. 79, 523-532 (2006).
- Li, Y., Shrestha, B., Vertes, A. Atmospheric Pressure Infrared MALDI Imaging Mass Spectrometry for Plant Metabolomics. Analytical Chemistry. 80, 407-420 (2007).
- Nemes, P., Vertes, A. Laser Ablation Electrospray Ionization for Atmospheric Pressure in Vivo, and Imaging Mass Spectrometry. Analytical Chemistry. 79, 8098-8106 (2007).
- Shrestha, B., Li, Y., Vertes, A. Rapid analysis of pharmaceuticals and excreted xenobiotic and endogenous metabolites with atmospheric pressure infrared MALDI mass spectrometry. Metabolomics. 4, 297-311 (2008).
- Nemes, P., Barton, A. A., Li, Y., Vertes, A. Ambient Molecular Imaging and Depth Profiling of Live Tissue by Infrared Laser Ablation Electrospray Ionization Mass Spectrometry. Analytical Chemistry. 80, 4575-4582 (2008).
- Nemes, P., Barton, A. A., Vertes, A. Three-Dimensional Imaging of Metabolites in Tissues under Ambient Conditions by Laser Ablation Electrospray Ionization Mass Spectrometry. Analytical Chemistry. 81, 6668-6675 (2009).
- Nemes, P., Woods, A. S., Vertes, A. Simultaneous Imaging of Small Metabolites and Lipids in Rat Brain Tissues at Atmospheric Pressure by Laser Ablation Electrospray Ionization Mass Spectrometry. Analytical Chemistry. 82, 982-988 (2010).
- Shrestha, B. Direct analysis of lipids and small metabolites in mouse brain tissue by AP IR-MALDI and reactive LAESI mass spectrometry. Analyst. , Forthcoming (2010).
- Sripadi, P., Nazarian, J., Hathout, Y., Hoffman, E., Vertes, A. In vitro analysis of metabolites from the untreated tissue of Torpedo californica electric organ by mid-infrared laser ablation electrospray ionization mass spectrometry. Metabolomics. 5, 263-276 (2009).
- Shrestha, B., Vertes, A. In Situ Metabolic Profiling of Single Cells by Laser Ablation Electrospray Ionization Mass Spectrometry. Analytical Chemistry. 81, 8265-8271 (2009).
- Shrestha, B., Nemes, P., Vertes, A. Ablation and Analysis of a Single Cell by Consecutive Laser Pulses. Applied Physics A. , (2010).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon