Method Article
HLA-Ig des cellules à base Antigène artificielle Présentation d'Efficient Ex vivo Extension du CTL humaines
Dans cet article
Résumé
Une méthode nouvelle DC indépendante pour l'induction et l'expansion des cellules T spécifiques d'antigènes est décrite. HLA A2-Ig des cellules à base Antigène artificielle Présentation (AAPC) sont chargés avec des peptides HLA-A2 restreint efficacement l'expansion des CTL spécificité antigénique divers. Cette technologie offre un grand potentiel pour CTL à base d'immunothérapie adoptive.
Résumé
CTL avec la fonction d'effecteur optimale jouent un rôle essentiel dans la médiation de la protection contre les différentes infections intracellulaires et le cancer. Toutefois, les particuliers peuvent présenter suppressif microenvironnement immunitaire et, contrairement à l'activation de CTL, leurs cellules autologues présentant l'antigène peuvent avoir tendance à tolerize ou anergize CTL spécifique de l'antigène. En conséquence, bien que toujours en phase expérimentale, basée sur CTL immunothérapie adoptive a évolué pour devenir un traitement prometteur pour diverses maladies comme le cancer et les infections virales. Dans les premières expériences ex vivo élargi CMV (cytomégalovirus) CTL spécifiques ont été utilisés pour le traitement de l'infection à CMV chez les patients immunodéprimés osseuse allogénique greffe de moelle. Alors qu'il est commun d'avoir la vie en danger virémie à CMV chez ces patients, aucun des patients recevant élargi CTL développer des maladies liées au CMV, impliquant l'immunité anti-CMV est établi par le adoptive transférée CTL 1. Des résultats prometteurs ont également été observées pour le mélanome et peut être étendu à d'autres types de cancer 2.
Bien qu'il existe de nombreuses façons d'ex vivo de stimuler et de développer CTL humains, les approches actuelles sont restreintes par les limites de coûts et technique. Par exemple, l'étalon-or actuel est basé sur l'utilisation de DC autologues. Cela nécessite à chaque patient de donner un nombre important de leucocytes et est aussi très coûteuse et laborieuse. Par ailleurs, détaillées dans la caractérisation in vitro de DC élargi CTL a révélé que ceux-ci ont seulement suboptimale fonction effectrice 3.
Nous présentons ici un très efficace système de base pour la VAMP expansion ex vivo de CMV CTL humains spécifiques pour une immunothérapie adoptive (figure 1). L'AAPC ont été faites par le couplage de cellules de taille humaine avec des billes magnétiques HLA-A2-Ig dimère et anti-CD28mAb 4. Une fois VAMP sont présentées, elles peuvent être chargés avec différents peptides d'intérêt, et rester fonctionnel pendant des mois. Dans ce rapport, AAPC ont été chargées avec un peptide dominant de CMV, pp65 (NLVPMVATV). Après culture humaine purifiée CD8 + CTL à partir d'un donneur sain avec de VAMP pour une semaine, le CMV CTL spécifique peut être augmenté de façon spectaculaire dans la spécificité de 98% (figure 2) et amplifiée plus de 10.000 fois. Si plus spécifiques du CMV CTL sont nécessaires, l'expansion peut être facilement atteint par la stimulation répétitive avec VAMP. La caractérisation phénotypique et fonctionnelle montre que ces cellules ont un phénotype élargi mémoire effecteurs et faire des quantités importantes de deux TNFa et l'IFN (figure 3).
Protocole
1. Faire, HLA-A2-Ig base AAPC
- Préparer un tampon de borate stériles
- Dissoudre l'acide borique dans l'eau pour faire 0,1. Ajuster le pH à 7,0.
- Filtrer à travers un filtre 0.22μm stériles et conserver à 4 ° C.
- Préparer le tampon de lavage de billes stériles
- Prenez 956ml PBS w / o de magnésium ou le calcium.
- Ajouter 30 ml de sérum humain AB.
- Ajouter l'EDTA 2 mM de concentration finale.
- Ajouter 0.1gsodium azoture.
- Filtrer à travers un filtre de 0,22 um stériles et conserver à 4 ° C.
- Prenez 1ml de perles Invitrogen époxy M-450 en stock, environ 400 millions de perles (perles peuvent être comptés par hémocytomètre), et mis dans une stérile, flacon en verre à vis.
- Mettez le flacon contre un aimant Dynal MPC-1, tandis que les perles adhèrent à la face du flacon, éliminer le surnageant par aspiration. Laver une fois avec des perles de 1 ml de tampon borate.
- Perles Remettre en suspension dans un mélange de tampon borate de 1 ml et 20 pg de HLA-A2-Ig dimère et 20 ug de CD28 monoclonal anti-humain (clone 9.3).
- Protéines à la conjugaison perle: mettre le flacon en verre sur des rotateurs et tourner à 4 ° C pendant 24 heures.
- Placer le tube dans le MPC-1 aimant et enlever tous tampon borate.
- Laver les billes deux fois avec le tampon de lavage 1ml billes.
- Incuber les perles dans le tampon de lavage 1ml perle, tournez à 4 ° C pendant 24 heures. Parce que le tampon de lavage de billes contient sérum humain AB, il va bloquer tout le site protéine résiduelle contraignant sur les perles.
- Retirer le surnageant de flacon en verre, remplacez-le par 1ml tampon de lavage frais de billes.
2. Le contrôle de qualité des AAPC et le peptide de chargement, le stockage
- Ajouter ~ 5 × 10 5 perles pour FACS 100 ul du tampon de lavage dans des tubes FACS, et tache avec 1 microlitre d'anti-souris IgG1-PE (reconnaître la partie Fc de la molécule HLA-A2-Ig) et 1 microlitre de l'anti-IgG2a de souris-FITC (reconnaître la partie Fc des anticorps monoclonaux anti-CD28). Après coloration pendant 20 minutes dans un tampon de lavage FACS, laver de nouveau et de lire le résultat de la coloration immédiatement par cytométrie en flux (Figure 4).
- De chargement de peptide sur les billes: Laver les billes deux fois en flacon de verre avec 1ml de PBS stérile. Resuspendre avec 1ml de PBS stérile, puis ajouter 10 ul de peptide CMV (1mg/ml)
- Comptez le nombre de billes par hémocytomètre, et l'étiquette du flacon avec la date et la concentration.
- VAMP sont prêtes à l'emploi après au moins 3 jours d'incubation peptide à 4 ° C, pour laisser le temps suffisant de liaison du peptide sur le dimère HLA-A2-Ig. Les billes peuvent être conservés à 4 ° C et rester fonctionnel pendant au moins 6 mois.
3. Homme d'isolement de CTL
- Recueillir ~ 100ml de sang périphérique frais de santé des donneurs HLA-A2 positifs dans 10 tubes BD Vacutainer sodium héparine. Utiliser une aiguille de calibre 21 ou plus pour éviter l'hémolyse.
- Centrifuger à 300xg pendant 10 minutes à température ambiante
- Retirez délicatement la couche de plasma dessus par aspiration. Le plasma peut être utilisé comme supplément pour le milieu de culture.
- Remplacer le plasma recueilli avec du PBS stérile et le transfert du sang dans un flacon stérile T75 culture ou 50ml tubes coniques. Mélanger le sang avec du PBS bien par aspiration et refoulement.
- Une fois que tout le sang est collecté, préparer quatre autres tubes coniques 50 ml et ajouter 15 ml de Ficoll-Paque Plus.
- Lentement superposition 30-35ml de cellules sanguines sur le dessus du Ficoll de chaque tube. Gardez à l'interface distincte entre les Ficoll et les cellules sanguines.
- Centrifuger à 500xg pendant 20 minutes à température ambiante. Tourner le frein "off" et l'accélération aussi bas que possible afin de maintenir une interface claire entre les couches.
- Avec une pipette seriological, aspirer délicatement la couche PBMC et recueillir les PBMC dans un nouveau tube 50ml conique. Lorsque tous les PBMC sont récoltées ajoutez 30ml de PBS et centrifuger à 400xg pendant 10 min. Jeter le surnageant et laver encore une fois avec 30ml de PBS pour enlever tous les résidus de Ficoll.
- Procéder à l'isolement CD8 + des lymphocytes T humains en utilisant Miltenyi CD8 + T kit isolement des cellules selon le protocole du fabricant. Ce kit enrichit fortement pour les cellules CD8 + (généralement> 95%) en appauvrissant CD8 - cellules.
- Compter les cellules T CD8 +. La pureté attendue devrait être supérieure à 95%. Pour confirmer cette utilisation 2x10 5 cellules et effectuer une analyse CD4/3/8 FACS. Le CTL restant peut être soit utilisé immédiatement pour antigène spécifique de stimulation AAPC ou ils peuvent être congelés pour un usage futur.
4. In vitro VAMP système de culture basée
- Préparer un milieu de culture
- Pour TF (facteur de croissance des lymphocytes T, fait dans le laboratoire 4) 2X milieu de culture: milieu RPMI complet ainsi que des bailleurs de fonds de 5% du plasma autologue et 8% facteur de croissance des lymphocytes T. autologue peut être remplacée par inactivés par la chaleur de sérum humain AB.
- Resuspendre 1000000 CTL dans 8ml de milieu de culture TF 2X plus de 8 ml de milieu RPMI complet, ajoutez 1 × 10 6 VAMP, bien mélanger.
- Utiliser une pipette multi-canaux pour les cellules plaque sur 96 puits U plaques de fond de culture de tissu. (160 pi par puits)
- Culture en cellules 37 ° C, 5% de CO 2 incubater pendant 7 jours. Alimenter les cellules le jour 4 avec 80 ul / moyen et TF 2X.
- Les cellules sont prêts à être récoltés le jour 7. Après la récolte, placer les cellules contre l'aimant et enlever la vieille AAPC.
- Spécificité antigénique peut être déterminée par coloration tétramère selon le protocole du fabricant. Phénotype coloration et la coloration des cytokines intracellulaires sont effectués conformément à notre précédente étude 3.
- Cellules récoltées peuvent être réensemencées avec VAMP nouveau dans les mêmes conditions. Le nombre de cellules et de spécificité antigénique devrait augmenter après stimulation répétée.
5. Les résultats représentatifs:
Un exemple de VAMP après conjugaison HLA A2-Ig et anti-CD28 est montré dans la figure 4. Conjugaison réussie protéines est évident par un changement clair de la coloration des anticorps correspondants. Alors que la fréquence de CTL spécifique du CMV dans le sang périphérique est généralement de 0,5 à 1%, après une seule semaine de VAMP médiation de stimulation, la spécificité peut atteindre 55 - 93% (figure 2 et 3). L'expansion de CTL spécifiques de l'antigène peut être très variable entre les différents bailleurs de fonds, mais les résultats sont reproductibles dans le même donneur. Par extrapolation, l'expansion des cellules CMV spécifiques peuvent être des milliers de fois par rapport aux niveaux de précurseur directement ex vivo (données non présentées). Coloration des cytokines intracellulaires (figure 3) montre que ces CTL élargi sont polyfonctionnels, plutôt que épuisée, après culture cellulaire prolongé et la prolifération significative.

Figure 1. Diagramme représentant du VAMP l'expansion ex vivo de CTL humains basée pour l'immunothérapie adoptive dans allogéniques HSCT
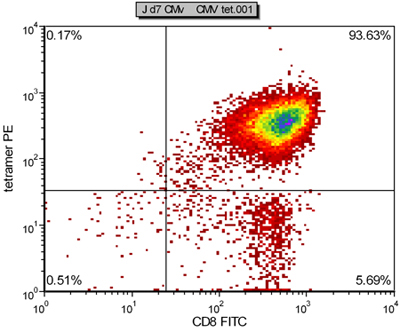
Figure 2. Résultat représentatif coloration tétramère CMV CTL spécifique générée par VAMP après une semaine de la culture
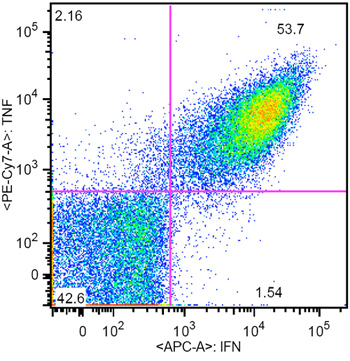
Figure 3. Représentant résultat intracellulaire coloration des cytokines du CMV CTL spécifique générée par VAMP (spécificité du CMV était de 61%)
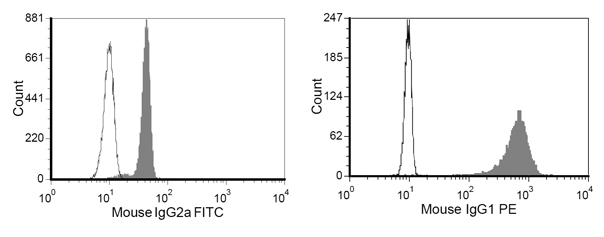
Figure 4. Résultat de la coloration Représentant du M-450 perles époxy après conjugaison des protéines colorées par anti-souris IgG1-PE et anti-souris IgG2-FITC
Discussion
Le système VAMP nous décrivons ici est un système efficace pour l'expansion ex vivo de CTL humain contre une variété d'antigènes. Des précautions particulières doivent être prises en ce qui concerne la qualité de la conjugaison des protéines et la distribution même des AAPC et CTL dans la culture plaque de 96 puits. En utilisant cette approche, nous avons pu élargir CTL pour plus de 8 semaines, durant laquelle nous avons élargi l'antigène CTL spécifique jusqu'à un million de fois 4. Il ya eu différents systèmes APC artificielle en utilisant des lignées cellulaires ou autres plates-formes acellulaire 5; toutefois, selon les données publiées chaque système a son profil unique en ce qui concerne l'expansion et la spécificité en charge des applications différentes. Fait important, car la qualité de CTL est aussi importante que la quantité, la polyfonctionnalité du CTL spécifiques du CMV générée par notre système sont attendus à conférer supérieure d'efficacité anti-virale.
Déclarations de divulgation
Remerciements
Nous tenons à remercier Aaron Selya de discussion utile. Ce travail a été soutenu par NIH AI29575, CA108835, AI077097 à JS, une subvention pilote de la Johns Hopkins Malaria Research Institute et le ministère de la Défense accorde 040 972 PC au MO
matériels
| Name | Company | Catalog Number | Comments |
| Réactifs | Société | Numéro de catalogue | |
|---|---|---|---|
| Vacutainer tube (contient de l'héparine) | Becton Dickinson | 367874 | |
| Human T CD8 + kit d'isolement cellulaire | Miltenyi | 130-094-156 | |
| Dynabeads M-450 Epoxy | Invitrogen | 140,11 | |
| Dynal MPC-1 Aimant | Invitrogen | 120-01D | |
| Ficoll-Paque plus | GE Healthcare | 17-1440-03 | |
| Milieu RPMI 1640 | Gibco | 11875 | |
| HLA-A2-Ig X dimère | Becton Dickinson | 551263 | |
| iTAgMHC tétramère (HLA-A2-CMV)-PE | Beckman Coulter | T20099 | |
| Falcon claires de 96 puits microplaque | Becton Dickinson | 353077 | |
| Rat anti-souris IgG2a-FITC | Becton Dickinson | 553390 | |
| Chèvre anti-souris IgG1-PE | Invitrogen | P21129 | |
| Sérum humain de type AB | Atlanta biologiques | S40110 | |
| Souris anti-humaine-FITC CD8a | Sigma-Aldrich | F0772 | |
| Souris anti-humain CD8a-APC | Becton Dickinson | 340684 | |
| Souris anti-humain IFN-FITC | Becton Dickinson | 340449 | |
| De souris anti-TNFa humain-PE | Becton Dickinson | 340512 |
Références
- Walter, E. A. Reconstitution of cellular immunity against cytomegalovirus in recipients of allogeneic bone marrow by transfer of T-cell clones from the donor. N Engl J Med. 333, 1038-1038 (1995).
- Rosenberg, S. A. Adoptive cell transfer: a clinical path to effective cancer immunotherapy. Nat Rev Cancer. 8, 3669-3669 (2008).
- Oelke, M. Ex vivo induction and expansion of antigen-specific cytotoxic T cells by HLA-Ig-coated artificial antigen-presenting cells. Nat Med. 9, 619-619 (2003).
- Oelke, M. Artificial antigen-presenting cells: artificial solution for real diseases. Trends Mol Med. 11, 412-412 (2005).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon