Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Évaluation des systèmes neuromusculaire Fonction Utilisation percutanée électrique stimulation du nerf
Dans cet article
Résumé
We present a protocol to assess changes in neuromuscular function. Percutaneous electrical nerve stimulation is a non-invasive method that evokes muscular responses. Electrophysiological and mechanical properties of these responses permit the evaluation of neuromuscular function from brain to muscle (supra-spinal, spinal and peripheral levels).
Résumé
Percutaneous electrical nerve stimulation is a non-invasive method commonly used to evaluate neuromuscular function from brain to muscle (supra-spinal, spinal and peripheral levels). The present protocol describes how this method can be used to stimulate the posterior tibial nerve that activates plantar flexor muscles. Percutaneous electrical nerve stimulation consists of inducing an electrical stimulus to a motor nerve to evoke a muscular response. Direct (M-wave) and/or indirect (H-reflex) electrophysiological responses can be recorded at rest using surface electromyography. Mechanical (twitch torque) responses can be quantified with a force/torque ergometer. M-wave and twitch torque reflect neuromuscular transmission and excitation-contraction coupling, whereas H-reflex provides an index of spinal excitability. EMG activity and mechanical (superimposed twitch) responses can also be recorded during maximal voluntary contractions to evaluate voluntary activation level. Percutaneous nerve stimulation provides an assessment of neuromuscular function in humans, and is highly beneficial especially for studies evaluating neuromuscular plasticity following acute (fatigue) or chronic (training/detraining) exercise.
Introduction
Stimulation nerveuse électrique percutanée est largement utilisé pour évaluer la fonction neuromusculaire 1. Le principe de base consiste à induire un stimulus électrique à un nerf moteur périphérique à évoquer une contraction musculaire. Mécanique (mesure de couple) et (activité électromyographique) réponses électrophysiologiques sont enregistrées simultanément. Couple, enregistrée au niveau du joint considéré, est évaluée en utilisant un ergomètre. Le signal électromyographique (EMG) enregistrée à l'aide d'électrodes de surface a été démontrée pour représenter l'activité du muscle 2. Cette méthode non-invasive est pas douloureux et plus facilement mis en œuvre que les enregistrements intramusculaires. Les deux électrodes bipolaires et monopolaires peuvent être utilisés. La configuration d'électrode monopolaire a été montré pour être plus sensible aux variations de l'activité musculaire 3, qui peut être utile pour les petits muscles. Cependant, des électrodes bipolaires se sont avérés être plus efficaces dans l'amélioration de la r signal sur bruitatio 4 et sont le plus couramment utilisé en tant que procédé d'enregistrement et de quantifier l'activité de l'unité de moteur. La méthodologie décrite ci-dessous se concentrera sur les enregistrements bipolaires. L'activité EMG est un indicateur de l'efficacité et l'intégrité du système neuromusculaire. L'utilisation de la stimulation du nerf percutanée offre de nouvelles informations sur la fonction neuromusculaire, à savoir les changements au niveau musculaire, de la moelle, ou supra-spinal (Figure 1).

Figure 1:. Aperçu des mesures neuromusculaires STIM: la stimulation du nerf. EMG: électromyographie. VAL: niveau d'activation volontaire. RMS: Root Mean Square. M max: amplitude maximale de l'onde M.
Au repos, le potentiel d'action musculaire composé, aussi appelé M-ondes, est la réponse à court temps de latence observé après stimulation artefact, et représente excitable masse musculaire par l'activ directe ation des axones moteurs principaux au muscle (figure 2, numéro 3). L'amplitude de l'onde M augmente avec l'intensité jusqu'à atteindre un plateau de sa valeur maximale. Cette réponse, appelé M max, représente la sommation synchrone de toutes les unités de moteur et / ou des fibres de muscle potentiels d'action enregistrées sous les électrodes d'EMG de surface 5. L'évolution de l'amplitude ou la vague aire de pic à pic est utilisé pour identifier les altérations de la transmission neuromusculaire 6. Les changements dans les réponses mécaniques liés à la M-ondes, c.-à-crête contraction couple / force, peuvent être dues à des altérations de l'excitabilité musculaire et / ou dans les fibres musculaires 7. L'association de M max amplitude et contraction couple maximal amplitude (Pt de rapport qualité / M) fournit un indice de l'efficacité électromécanique du muscle 8, à savoir réponse mécanique d'une commande de moteur électrique donné.
52974 / 52974fig2.jpg "/>
Figure 2:. Moteur et les voies réflexives activés par la stimulation du nerf stimulation électrique d'un (moteur / sensoriel) nerf mixte (STIM) induit une dépolarisation de deux axone moteur et Ia afférente tir. Dépolarisation des afférences Ia vers la moelle épinière active un motoneurone alpha, qui à son tour évoque une réponse réflexe H (voie 1 + 2 + 3). Selon l'intensité du stimulus, moteur axone dépolarisation évoque une réponse musculaire directe: M-ondes (voie 3). Au maximale intensité M-ondes, un courant antidromique est également généré (3 ') et entre en collision avec volley réflexe (2). Cette collision annule partiellement ou totalement la réponse réflexe H.
Le réflexe H est une réponse électrophysiologique utilisé pour évaluer les changements dans l'AI-α motoneurone synapse 9. Ce paramètre peut être évaluée au repos ou pendant les contractions volontaires. Réflexe H représente une variante du réflexe d'étirement (Figure 2, numbre 1-3). Le réflexe H active unités motrices monosynaptique recrutés par des voies afférentes Ia 10,11, et peut être soumis à des influences périphériques et centraux 12. La méthode d'évoquer un réflexe H est connu pour avoir une fiabilité intra-sujet élevée pour évaluer l'excitabilité de la moelle au repos et pendant 13,14 contractions isométriques 15.
Lors d'une contraction volontaire, l'ampleur de l'entraînement volontaire de neurones peut être évaluée en utilisant l'amplitude du signal EMG, généralement quantifié en utilisant l'Root Mean Square (RMS). EMG RMS est couramment utilisé un moyen de quantifier le niveau d'excitation du système de moteur pendant la contraction volontaire (figure 1). En raison de la variabilité intra et inter-sujet 16, RMS EMG doit être normalisé en utilisant l'EMG enregistrée lors d'une contraction volontaire maximale spécifique musculaire (RMS EMGmax). En outre, parce que les changements dans le signal EMG peuvent be en raison de modifications au niveau périphérique, la normalisation en utilisant un paramètre périphérique telles que la M-onde est nécessaire pour évaluer seulement l'élément central d'un signal EMG. Cela peut se faire en divisant le EMG RMS par l'amplitude maximale ou la Cmax efficace de la M-onde. Normalisation utilisant RMS Mmax (c.-à-EMG RMS / RMS Cmax) est la méthode privilégiée, car elle prend en considération le changement possible de la durée de l'onde M 17.
Commandes de moteur peut également être évaluées par le calcul du niveau d'activation volontaire (VAL). Cette méthode utilise la technique d'interpolation contraction 18 en superposant une stimulation électrique à M intensité max pendant une contraction volontaire maximale. L'extra-couple induit en stimulant le nerf est comparée à une contraction de commande produit par la stimulation du nerf identiques dans un muscle potentialisée détendue 19. Pour évaluer maximale VAL, la contraction initiale de interpotechnique de règlement décrit par Merton 18 implique un stimulus unique interpolée sur une contraction volontaire. Récemment, l'utilisation de la stimulation double est devenu plus populaire parce que les incréments de couple évoqués sont plus grandes, plus facilement détectée, et moins variable par rapport à la stimulation réponses uniques 20. Le VAL fournit un indice de la capacité du système nerveux central pour activer au maximum les muscles qui travaillent 21. Actuellement, VAL évaluée en utilisant la technique d'interpolation contraction est la méthode la plus utile pour évaluer le niveau d'activation musculaire 22. En outre, le couple de pointe évaluée en utilisant un ergomètre est la force paramètre de test la plus correctement étudié applicable d'utilisation dans la recherche et les paramètres cliniques 23.
Stimulation nerveuse électrique peut être utilisé dans une variété de groupes musculaires (par exemple fléchisseurs du coude, du poignet, fléchisseurs du genou, extenseurs fléchisseurs plantaires). Toutefois, l'accessibilité rend le nerftechnique difficile dans certains groupes de muscles. Les muscles fléchisseurs plantaires, en particulier triceps sural (soléaire et gastrocnemii) des muscles, sont fréquemment étudiés dans la littérature 24. En effet, ces muscles sont impliqués dans la locomotion, justifiant leur intérêt particulier. La distance entre le site de stimulation et les électrodes d'enregistrement permet l'identification des différentes vagues de évoquées les muscles des triceps. La partie superficielle du nerf tibial postérieur dans le creux poplité et le grand nombre de broches rendre plus facile à enregistrer les réponses réflexes rapport à d'autres muscles 24. Pour ces raisons, la méthodologie réflexe actuellement présenté se concentre sur le groupe des muscles triceps (soléaire et gastrocnémien). L'objectif de ce protocole est donc de décrire percutanée technique de stimulation du nerf pour enquêter sur la fonction neuromusculaire dans le triceps sural.
Access restricted. Please log in or start a trial to view this content.
Protocole
Les procédures expérimentales décrites reçu l'approbation éthique institutionnelle et sont conformes à la Déclaration d'Helsinki. Les données ont été recueillies auprès d'un participant représentant qui était au courant des procédures et a donné son consentement éclairé.
1. Instrument Préparation
- Nettoyer la peau à l'emplacement de l'électrode par le rasage, et enlever la saleté avec de l'alcool pour obtenir une faible impédance (<5 kQ).
- Placez deux électrodes de surface AgCl enregistrement (diamètre de 10 mm) à 2/3 de la limite entre les Condylis médial du fémur à la malléole interne du muscle soléaire; sur la bosse la plus importante du muscle pour le jumeau interne; au 1/3 de la distance le long d'une ligne entre la tête du péroné et le talon pour le gastrocnémien latéral; et au 1/3 de la distance le long d'une ligne entre la pointe du péroné et de la pointe de la malléole interne pour le muscle tibial antérieur, avec un interelectrode distance (centre-à-centre) de 2 cm, selon les recommandations de SENIAM 30.
Remarque: Les électrodes du muscle soléaire ont à être placée sous l'insertion distale des muscles gastrocnemii pour assurer qu'ils ne sont pas enregistrer l'activité des chefs des muscles de la gastrocnemii (diaphonie). - Placer une électrode de référence dans une position centrale sur la même branche (entre stimulation et sites d'enregistrement).
- Ajustez la hauteur et la profondeur de la chaise pour obtenir un angle de la cheville de 90 ° (0 ° = full flexion plantaire), de sorte que le soléaire et les muscles gastrocnemii ne sont pas étirés et le réflexe H est pas altérée 11,12.
- Réglez l'angle de genou à 90 ° (0 ° = extension du genou complet) en raison de la nature biarticular des muscles gastrocnemii. Toutefois, l'angle de la cheville optimal pour effectuer un couple maximale volontaire des fléchisseurs plantaires est de 70-80 ° (0 ° = full flexion plantaire) 26. Ainsi, l'angle de la cheville dépendra du paragraphemètre d'intérêt (par rapport enregistrements électrophysiologiques mécaniques).
Remarque: Indépendamment de l'angle initial choisi, il doit rester constante tout au long de l'expérience de standardiser l'excitabilité neuromusculaire 11,12,27,28. - Portez une attention particulière lors de la surveillance de la posture des sujets lors de l'essai de maintenir influences cortico-vestibulaire constants sur l'excitabilité de la piscine de moteur 29.
- Réglez l'angle de genou à 90 ° (0 ° = extension du genou complet) en raison de la nature biarticular des muscles gastrocnemii. Toutefois, l'angle de la cheville optimal pour effectuer un couple maximale volontaire des fléchisseurs plantaires est de 70-80 ° (0 ° = full flexion plantaire) 26. Ainsi, l'angle de la cheville dépendra du paragraphemètre d'intérêt (par rapport enregistrements électrophysiologiques mécaniques).
- Attacher solidement la cheville à un ergomètre, avec l'axe anatomique de l'articulation (malléole externe) alignée avec l'axe de rotation 25 de l'ergomètre.
- Avoir la pression sujet exercer sur un repose-pieds attaché à l'ergomètre pour enregistrer couple fléchisseur plantaire. Gardez le pied immobile pendant toute l'expérience de telle sorte que de petits changements dans le couple peuvent être détectés.
- Remarque: Dans certaines circonstances, le talon peut soulever légèrement la plaque de force si le pied et la cheville ne sont pas garantis, ce qui peut leannonce à une transmission incomplète du couple contre la plaque. La figure 3 présente une description du dispositif expérimental.
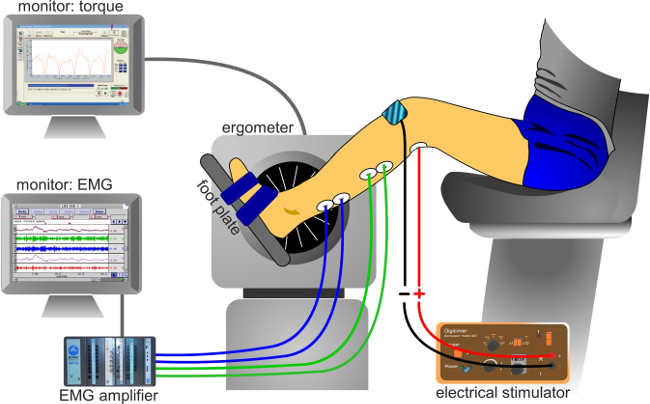
Figure 3:. Dispositif expérimental dispositif expérimental classique pour enregistrer des signaux (EMG) et de couple électromyographique.
- Raccorder les électrodes à l'amplificateur avec des câbles.
- Réglez le taux d'échantillonnage de couple et d'EMG mesures à 2-5 kHz. Enregistrer le signal en utilisant un EMG (AD) système de conversion analogique-numérique. Le signal est affichée sur un moniteur d'un système d'acquisition de données, ce qui donne instantanément valeurs de plusieurs paramètres (par exemple la valeur maximale, l'amplitude crête-à-crête, durée). Le spectre du signal EMG peut être comprise entre 5 Hz et 2 kHz fréquences, mais est principalement comprise entre 10 Hz et 1 kHz 31. Ainsi, la fréquence d'échantillonnage doit être suffisamment élevé pour préserver dur de forme de signaling enregistrement EMG. Amplifier et filtrer les signaux EMG de gain (500 à 100) en utilisant = une fréquence de la bande passante entre 10 Hz et 1 kHz 8,21,32.
- Placez l'anode pour la stimulation électrique sur le tendon rotulien.
- Déterminer le meilleur site de stimulation du nerf tibial postérieur pour obtenir un optimal soléaire réflexe H pour une intensité donnée, en utilisant une électrode cathode ballon tenu à la main dans le creux poplité. Testez plusieurs sites de stimulation à l'électrode de cathode de la balle jusqu'à ce qu'une valeur maximale du réflexe H est atteinte.
- Enregistrez activité EMG jambier antérieur pour assurer que le nerf fibulaire commun est pas activée pour éviter l'influence des afférences Ia antagoniste 12. Régler la largeur d'impulsion de 1 ms à fournir une activation optimale des fibres nerveuses, en particulier des fibres afférentes 10.
- Placez un AgCl cathode auto-adhésif à l'emplacement du site de stimulation pour assurer l'état de relance constante (par exemple la pression, orientation).
Note: Tous ces paramètres (position sujet, l'emplacement de l'électrode et du site de stimulation) ne changent pas pour l'évaluation des différentes mesures électrophysiologiques. Seule l'intensité de la stimulation et de l'état (de repos par rapport à la contraction) varient.
2. Procédures d'essai at Rest
- Demandez au sujet de rester détendu et de garder ses muscles / ses au repos.
- Ajuster l'intensité de stimulation pour obtenir soléaire maximale réflexe H amplitude (H max; gamme habituelle: 20-50 mA). Une onde M du muscle soléaire peut être observée chez H intensité max.
Remarque: Pour des mesures répétées (par exemple, avant et après un protocole fatigante), l'intensité optimale pour obtenir une réponse de max de H peut varier au cours de la session. Comme en gardant une intensité constante peut conduire à une sous-estimation de H max amplitude, il est recommandé que l'expérimentateur réévalue régulièrement H max33 intensité. - Enregistrer un minimum de 3 soléaire réponses réflexe H à cette intensité avec un intervalle minimum de 3 sec pour éviter la dépression post-activation 34.
Remarque: Bien que l'enregistrement de plusieurs réponses est plus approprié en raison de la sensibilité particulière du réflexe H, une stimulation unique peut suffire dans certaines circonstances, par exemple en essayant d'éviter les effets de récupération rapide (par exemple pendant un protocole fatigante). - Augmentez l'intensité de stimulation pour obtenir amplitude maximale soléaire onde M (M max; gamme habituelle: 40-100 mA). Habituellement, réglez l'incrément de l'intensité de la stimulation à 2-4 mA, avec un intervalle de 8-10 sec entre deux stimuli 12,35. L'intensité désirée est atteinte lorsque M max est obtenue, et aucune réponse de réflexe H peut être observée.
- Réglez l'intensité finale de 120 à 150% de l'intensité du stimulus M max de veiller à ce que le M-onde atteint un plateau de sa valeur maximale. Cette intensificationTy est appelée intensité supramaximale dans les instructions ci-dessous.
- Gardez l'intensité de la stimulation constante pour les enregistrements des ondes M soléaire tout au long de la session.
- Fiche 3 soléaire M-ondes et 3 couples de contraction associés à cette intensité.
3. Procédures de test lors de la contraction volontaire
- Comme un warm-up, demandez au sujet d'effectuer 10 brèves et non fatigantes submaximales contractions des muscles fléchisseurs plantaires, avec un repos de quelques secondes entre chacune des contractions. À la fin du warm-up, prendre un minimum 1 min de repos pour éviter les effets fatigantes 11.
- L'activité EMG de d'enregistrer en permanence les triceps. Enregistrement soléaire et les muscles gastrocnemii permet l'analyse du comportement des différentes typologies de muscle pour un seul site de stimulation 24.
- Demandez le sujet pour effectuer une contraction isométrique maximale volontaire (MVC) des fléchisseurs plantaires. Le sujet doit pousser aussi dur que possible contre l'ergomètre en contractant ses muscles fléchisseurs plantaires. Donner de la rétroaction visuelle au sujet pendant l'effort, et l'encouragement verbal standardisé 19. Le MVC est atteint quand on observe un plateau.
- Livrer une stimulation double (100 Hz de fréquence) à une intensité supramaximale durant le plateau de la MVC (du doublet superposé), et un autre stimulation double lorsque le muscle est complètement détendu immédiatement après la contraction (doublet potentialisée) pour évaluer le niveau d'activation volontaire. Livrer cette stimulation jumelé à travers un dispositif spécifique (par exemple Digitimer D185 MultiPulse Stimulator) ou par le biais d'un programme de stimulation associée à un seul stimulateur d'impulsions.
- Demandez le sujet pour effectuer une deuxième MVC du fléchisseur plantaire avec au moins 1 min de repos entre chaque essai 11. Si le couple de pointe du deuxième procès ne sont pas moins de 5% de la première, des essais supplémentaires doivent être effectués 36. Le plus grand couple réalisé parl'objet est considéré comme le couple de MVC.
Analyse des données 4.
- Analyse des données au repos
- Sélectionnez une fenêtre de temps, y compris la réponse EMG associée à la contraction au repos (H-ondes ou M-ondes).
- Mesurer la durée d'amplitude crête-à-crête, de crête à crête et / ou dans la zone des ondes (figure 4A). Si l'amplitude ne soit pas directement assurée par le logiciel, soustraire le minimum pour les valeurs maximales.
- Pour la durée, de mesurer le délai à partir de la pointe maximale et se terminant au sommet minime. Pour la région, calculer l'intégrale d'un signal EMG à partir du début de la vague et se terminant à la fin de la vague.
Remarque: amplitude crête-à-crête peut refléter: 1) la transmission neuromusculaire, 2) l'action de l'unité de moteur potentiel amplitude et / ou 3) dispersion temporelle du moteur l'action de l'unité potentielle 37. La durée de l'onde M reflète neuromusculaire propagation 37.
- Pour la durée, de mesurer le délai à partir de la pointe maximale et se terminant au sommet minime. Pour la région, calculer l'intégrale d'un signal EMG à partir du début de la vague et se terminant à la fin de la vague.
- Pour de multiples essais, calculer la moyenne des vagues. Si la moyenne ne peut être directement fournie par le logiciel, utilisez le logiciel de tableur (par exemple, la fonction de formule dans un tableur) pour calculer cette valeur de plusieurs essais (au moins 3).
- Sélectionnez la contraction de repos.
- Mesurer le couple de crête associé à la contraction de repos (figure 4B).
- Pour de multiples essais, calculer le couple maximal moyen des tics de repos. Si la moyenne ne peut être directement fournie par le logiciel, utilisez le logiciel de tableur (par exemple, la fonction de formule dans un tableur) pour calculer cette valeur à partir des plusieurs essais (au moins 3).
- Répétez ces procédures décrites au point 4.1.2 pour les autres paramètres souhaités (temps de contraction ou de temps de demi-relaxation). L'analyse des paramètres de contraction fournit des indications quant à l'excitation-contraction couplage efficacité 17. En particulier, le contrattemps ion fournit un indice de cinétique de contraction 8, qui peut dépendre le groupe musculaire choisi 38.
- Calculer le rapport entre le couple maximal et la somme de m-ondes à l'aide d'un tableur (Excel), afin de quantifier l'efficacité électromécanique (t P / M). Comme les réponses mécaniques évoqués par stimulation du nerf postérieur tibial correspondent à l'activation du triceps sural dans son ensemble, et des amplitudes de soléaire gastrocnemii M-ondes doivent être additionnées 39.
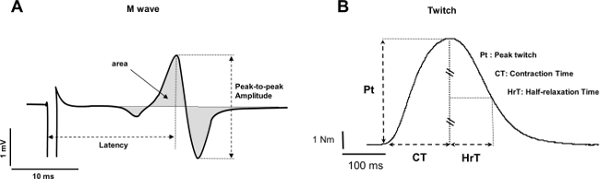
Figure 4: Explication des réponses électrophysiologiques et mécaniques (A) Mesure de amplitude crête-à-crête (mV), la latence (ms) et la région (mV.ms) d'une onde M typique.. (B) Mesure du couple de contraction de pointe (Nm), temps de contraction (ms) et le temps de demi-relaxation (ms) d'une contraction. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
- L'analyse des données dans la contraction
- Sélectionner une fenêtre de temps de 500 ms de l'activité EMG soléaire pendant le plateau de couple MVC y compris le couple maximal à l'exclusion de l'intervalle entre l'artefact de stimulation et la fin de la période de silence de l'EMG. La période de silence correspond à la suppression de l'activité EMG volontaire en cours suite à la stimulation.
- Si la moyenne quadratique (RMS) est pas directement fournies par le logiciel, calculer les RMS pour quantifier l'activité EMG 40 en utilisant la formule suivante: EMG RMS
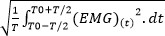
- Mesurer ou calculer les RMS de M max au repos pendant la durée de l'onde.
- Calculer le ratio EMG RMS / RMS Mmax aide d'un tableur.RMS valeur EMG et la valeur RMS Mmax doivent être sélectionnés de la même muscle.
- Mesurer le pic de couple maximal du MVC à partir de la ligne de base du couple au repos à la valeur maximale du couple à l'exclusion du MVC superposé induite par la stimulation de doublet (figure 5).
- Mesurer le couple superposé induite par la stimulation de la doublet pendant MVC, à partir de la valeur de couple volontaire dès le début de la stimulation au pic de la réponse évoquée (Figure 5).
- Sélectionnez le doublet potentialisée.
- Mesurer le couple de pointe associée à la doublet potentialisée.
- Calculer le niveau d'activation volontaire (VAL) en utilisant la formule 40 suivante:

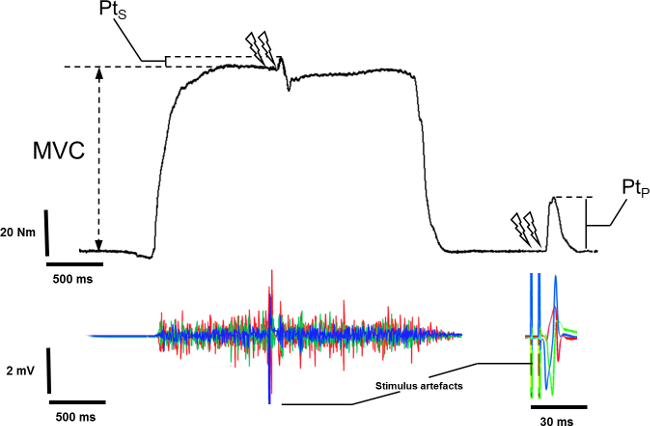
Figure 5: Mesure de superposées etpotentialisée doublet sur signal mécanique. Pour enregistrer le couple de pointe superposée (PTS), la stimulation doublet est évoquée au cours de la plateau de contraction volontaire maximale isométrique (MVC). Pour enregistrer potentialisée couple maximal (Pt P), la stimulation doublet est évoquée au repos après le décalage du MVC.
Access restricted. Please log in or start a trial to view this content.
Résultats
L'augmentation de l'intensité du stimulus conduit à une évolution différente des amplitudes de réponse entre H et M-ondes. Au repos, le réflexe H atteint une valeur maximale avant d'être totalement absent de signaux EMG, tandis que M onde augmente progressivement jusqu'à atteindre un plateau à intensité maximale (voir la figure 4 pour une représentation graphique de l'onde M et la figure 6 pour l'évolution de M-ondes et H-reflex avec ...
Access restricted. Please log in or start a trial to view this content.
Discussion
Stimulation nerveuse percutanée permet la quantification de nombreuses caractéristiques du système neuromusculaire non seulement de comprendre le contrôle fondamental de la fonction neuromotrice chez l'homme sain, mais aussi pour être en mesure d'analyser les adaptations aiguës ou chroniques par la fatigue ou de la formation 17. Ceci est très bénéfique surtout pour les protocoles fatigantes, où des mesures doivent être effectuées dès que possible après l'exercice fin d'éviter le...
Access restricted. Please log in or start a trial to view this content.
Déclarations de divulgation
The authors have nothing to disclose.
Remerciements
The authors have no acknowledgements.
Access restricted. Please log in or start a trial to view this content.
matériels
| Name | Company | Catalog Number | Comments |
| Biodex dynamometer | Biodex Medical System Inc., New York, USA | www.biodex.com | |
| MP150 Data Acquisition System | Biopac Systems Inc., Goleta, USA | ||
| Acknowledge 4.1.0 software | Biopac Systems Inc., Goleta, USA | www.biopac.com | |
| DS7A constant current high voltage stimulator | Digitimer, Hertfordshire, UK | www.digitimer.com | |
| Silver chloride surface electrodes | Control Graphique Medical, Brie-Comte-Robert, France | ||
| Computer | |||
| 1 Cable for connecting the Biodex to the MP150 | |||
| 1 Cable for connecting the Digitimer to the MP150 | |||
| 1 Cable for connecting the MP150 to the computer |
Références
- Desmedt, J. E., Hainaut, K. Kinetics of myofilament activation in potentiated contraction staircase phenomenon in human skeletal muscle. Nature. 217 (5128), 529-532 (1968).
- Bouisset, S., Maton, B. Quantitative relationship between surface EMG and intramuscular electromyographic activity in voluntary movement. American Journal of Physical Medicine. 51 (6), 285-295 (1972).
- Gabriel, D. A. Effects of monopolar and bipolar electrode configurations on surface EMG spike analysis. Medical Engineering and Physics. 33 (9), 1079-1085 (2011).
- Merletti, R., Rainoldi, A., Farina, D. Surface electromyography for noninvasive characterization of muscle. Exercise and Sport Sciences Reviews. 29 (1), 20-25 (2001).
- Lepers, R. Aetiology and time course of neuromuscular fatigue during prolonged cycling exercises. Science, & Motricité. 52, 83-107 (2004).
- Baudry, S., Klass, M., Pasquet, B., Duchateau, J. Age related fatigability of the ankle dorsiflexor muscles during concentric and eccentric contractions. European Journal of Applied Physiology. 100 (5), 515-525 (2007).
- Place, N., Yamada, T., Bruton, J. D., Westerblad, H. Muscle fatigue From observations in humans to underlying mechanisms studied in intact single muscle fibres. European Journal of Applied Physiology. 110 (1), 1-15 (2010).
- Scaglioni, G., Narici, M. V., Maffiuletti, N. A., Pensini, M., Martin, A. Effect of ageing on the electrical and mechanical properties of human soleus motor units activated by the H reflex and M wave. The Journal of Physiology. 548 (Pt. 2), 649-661 (2003).
- Schieppati, M. The Hoffmann reflex a means of assessing spinal reflex excitability and its descending control in man. Progress in Neurobiology. 28 (4), 345-376 (1987).
- Pierrot Deseilligny, E., Burke, D. The circuitry of the human spinal cord: its role in motor control and movement disorders. , Cambridge University Press. (2005).
- Duclay, J., Pasquet, B., Martin, A., Duchateau, J. Specific modulation of corticospinal and spinal excitabilities during maximal voluntary isometric shortening and lengthening contractions in synergist muscles. The Journal of Physiology. 589 (Pt. 11), 2901-2916 (2011).
- Grosprêtre, S., Papaxanthis, C., Martin, A. Modulation of spinal excitability by a sub threshold stimulation of M1 area during muscle lengthening. Neuroscience. 263, 60-71 (2014).
- Mynark, R. G. Reliability of the soleus H reflex from supine to standing in young and elderly. Clinical Neurophysiology. 116 (6), 1400-1404 (2005).
- Palmieri, R. M., Hoffman, M. A., Ingersoll, C. D. Intersession reliability for H reflex measurements arising from the soleus peroneal and tibialis anterior musculature. The International Journal of Neuroscience. 112 (7), 841-850 (2002).
- Chen, Y. S., Zhou, S., Cartwright, C., Crowley, Z., Baglin, R., Wang, F. Test retest reliability of the soleus H reflex is affected by joint positions and muscle force levels. Journal of Electromyography and Kinesiology. 20 (5), 987-987 (2010).
- Lehman, G. J., McGill, S. M. The importance of normalization in the interpretation of surface electromyography A proof of principle. Journal of Manipulative and Physiological Therapeutics. 22 (7), 444-446 (1999).
- Lepers, R. Interest and limits of percutaneous nerve electrical stimulation in the evaluation of muscle fatigue. Science, & Motricité. 70 (70), 31-37 (2010).
- Merton, P. A. Voluntary strength and fatigue. The Journal of Physiology. 123, 553-564 (1954).
- Gandevia, S. C. Spinal and supraspinal factors in human muscle fatigue. Physiological Reviews. 81 (4), 1725-1789 (2001).
- Shield, A., Zhou, S. Assessing voluntary muscle activation with the twitch interpolation technique. Sports Medicine. 34 (4), 253-267 (2004).
- Rozand, V., Pageaux, B., Marcora, S. M., Papaxanthis, C., Lepers, R. Does mental exertion alter maximal muscle activation. Frontiers in Human Neuroscience. 8, 755(2014).
- Place, N., Maffiuletti, N. A., Martin, A., Lepers, R. Assessment of the reliability of central and peripheral fatigue after sustained maximal voluntary contraction of the quadriceps muscle. Muscle and Nerve. 35 (4), 486-495 (2007).
- Kannus, P. Isokinetic evaluation of muscular performance: implications for muscle testing and rehabilitation. International Journal of Sports Medicine. 15, Suppl 1. S11-S18 (1994).
- Tucker, K. J., Tuncer, M., Türker, K. S. A review of the H reflex and M wave in the human triceps surae. Human Movement Science. 24 (5-6), 667-688 (2005).
- Taylor, N. A., Sanders, R. H., Howick, E. I., Stanley, S. N. Static and dynamic assessment of the Biodex dynamometer. European Journal of Applied Physiology and Occupational Physiology. 62 (3), 180-188 (1991).
- Sale, D., Quinlan, J., Marsh, E., McComas, A. J., Belanger, A. Y. Influence of joint position on ankle plantarflexion in humans. Journal of Applied Physiology. 52 (6), 1636-1642 (1982).
- Cattagni, T., Martin, A., Scaglioni, G. Is spinal excitability of the triceps surae mainly affected by muscle activity or body position. Journal of Neurophysiology. 111 (12), 2525-2532 (2014).
- Gerilovsky, L., Tsvetinov, P., Trenkova, G. Peripheral effects on the amplitude of monopolar and bipolar H-reflex potentials from the soleus muscle. Experimental Brain Research. 76 (1), 173-181 (1989).
- Schieppati, M. The Hoffmann reflex a means of assessing spinal reflex excitability and its descending control in man. Progress in Neurobiology. 28 (4), 345-376 (1987).
- Hermens, H. J., Freriks, B., Disselhorst Klug, C., Rau, G. Development of recommendations for SEMG sensors and sensor placement procedures. Journal of Electromyography and Kinesiology. 10 (5), 361-374 (2000).
- Kamen, G., Sison, S. V., Du, C. C., Patten, C. Motor unit discharge behavior in older adults during maximal effort contractions. Journal of Applied Physiology. 79 (6), 1908-1913 (1995).
- Neyroud, D., Rüttimann, J., et al. Comparison of neuromuscular adjustments associated with sustained isometric contractions of four different muscle groups. Journal of Applied Physiology. 114, 1426-1434 (2013).
- Rupp, T., Girard, O., Perrey, S. Redetermination of the optimal stimulation intensity modifies resting H-reflex recovery after a sustained moderate-intensity muscle contraction. Muscle and Nerve. 41 (May), 642-650 (2010).
- Zehr, E. P. Considerations for use of the Hoffmann reflex in exercise studies. European Journal of Applied Physiology. 86 (6), 455-468 (2002).
- Gondin, J., Duclay, J., Martin, A. Soleus and gastrocnemii evoked V wave responses increase after neuromuscular electrical stimulation training. Journal of Neurophysiology. 95 (6), 3328-3335 (2006).
- Rochette, L., Hunter, S. K., Place, N., Lepers, R. Activation varies among the knee extensor muscles during a submaximal fatiguing contraction in the seated and supine postures. Journal of Applied Physiology. 95 (4), 1515-1522 (2003).
- Fuglevand, A. J., Zackowski, K. M., Huey, K. A., Enoka, R. M. Impairment of neuromuscular propagation during human fatiguing contractions at submaximal forces. The Journal of Physiology. 460, 549-572 (1993).
- Vandervoort, A. A., McComas, A. J. Contractile changes in opposing muscles of the human ankle joint with aging. Journal of Applied Physiology. 61 (1), 361-367 (1986).
- Grosprêtre, S., Martin, A. Conditioning effect of transcranial magnetic stimulation evoking motor evoked potential on V wave response. Physiological Reports. 2 (11), e12191(2014).
- Allen, G. M., Gandevia, S. C., McKenzie, D. K. Reliability of measurements of muscle strength and voluntary activation using twitch interpolation. Muscle and Nerve. 18 (6), 593-600 (1995).
- Cooper, M. A., Herda, T. J., Walter Herda, A. A., Costa, P. B., Ryan, E. D., Cramer, J. T. The reliability of the interpolated twitch technique during submaximal and maximal isometric muscle actions. Journal of Strength and Conditioning Research. 27 (10), 2909-2913 (2013).
- Froyd, C., Millet, G. Y., Noakes, T. D. The development of peripheral fatigue and short term recovery during self paced high intensity exercise. The Journal of Physiology. 591 (Pt 5), 1339-1346 (2013).
- Pierrot Deseilligny, E., Morin, C., Bergego, C., Tankov, N. Pattern of group I fibre projections from ankle flexor and extensor muscles in man. Experimental Brain Research. 42 (3-4), 337-350 (1981).
- Brooke, J. D., McIlroy, W. E., et al. Modulation of H reflexes in human tibialis anterior muscle with passive movement. Brain Research. 766 (1-2), 236-239 (1997).
- Hultborn, H., Meunier, S., Morin, C., Pierrot Deseilligny, E. Assessing changes in presynaptic inhibition of I a fibres a study in man and the cat. The Journal of Physiology. 389, 729-756 (1987).
- Meunier, S., Pierrot Deseilligny, E. Cortical control of presynaptic inhibition of Ia afferents in humans. Experimental Brain Research. 119 (4), 415-426 (1998).
- Aymard, C., Baret, M., Katz, R., Lafitte, C., Pénicaud, A., Raoul, S. Modulation of presynaptic inhibition of la afferents during voluntary wrist flexion and extension in man. Experimental Brain Research. 137 (1), 127-131 (2001).
- Abbruzzese, G., Trompetto, C., Schieppati, M. The excitability of the human motor cortex increases during execution and mental imagination of sequential but not repetitive finger movements. Experimental Brain Research. 111 (3), 465-472 (1996).
- Garland, S. J., Klass, M., Duchateau, J. Cortical and spinal modulation of antagonist coactivation during a submaximal fatiguing contraction in humans. Journal of Neurophysiology. 99, 554-563 (2008).
- Rodriguez Falces, J., Place, N. Recruitment order of quadriceps motor units Femoral nerve vs direct quadriceps stimulation. European Journal of Applied Physiology. 113, 3069-3077 (2013).
- Rodriguez Falces, J., Maffiuletti, N. A., Place, N. Spatial distribution of motor units recruited during electrical stimulation of the quadriceps muscle versus the femoral nerve. Muscle and Nerve. 48 (November), 752-761 (2013).
- Bathien, N., Morin, C. Comparing variations of spinal reflexes during intensive and selective attention (author’s transl). Physiology, & Behavior. 9 (4), 533-538 (1972).
- Earles, D. R., Koceja, D. M., Shively, C. W. Environmental changes in soleus H reflex excitability in young and elderly subjects. The International Journal of Neuroscience. 105 (1-4), 1-13 (2000).
- Paquet, N., Hui Chan, C. W. Human soleus H reflex excitability is decreased by dynamic head and body tilts. Journal of Vestibular Research Equilibrium, & Orientation. 9 (5), 379-383 (1999).
- Miyahara, T., Hagiya, N., Ohyama, T., Nakamura, Y. Modulation of human soleus H reflex in association with voluntary clenching of the teeth. Journal of Neurophysiology. 76 (3), 2033-2041 (1996).
- Pinniger, G. J., Nordlund, M. M., Steele, J. R., Cresswell, a GH reflex modulation during passive lengthening and shortening of the human triceps surae. Journal of Physiology. 534 (Pt 3), 913-923 (2001).
- Tallent, J., Goodall, S., Hortobágyi, T., St Clair Gibson, A., French, D. N., Howatson, G. Repeatability of corticospinal and spinal measures during lengthening and shortening contractions in the human tibialis anterior muscle). PLoS ONE. 7 (4), e35930(2012).
- Grospretre, S., Martin, A. H. reflex and spinal excitability methodological considerations. Journal of Neurophysiology. 107 (6), 1649-1654 (2012).
- Hugon, M. Methodology of the Hoffmann reflex in man. New Developments in Electromyography and Chemical Neurophysiology. 3m, 277-293 (1973).
- Bigland Ritchie, B., Zijdewind, I., Thomas, C. K. Muscle fatigue induced by stimulation with and without doublets. Muscle and Nerve. 23 (9), 1348-1355 (2000).
- Kent Braun, J. A., Le Blanc, R. Quantitation of central activation failure during maximal voluntary contractions in humans. Muscle and Nerve. 19 (7), 861-869 (1996).
- Herbert, R. D., Gandevia, S. C. Twitch interpolation in human muscles mechanisms and implications for measurement of voluntary activation. Journal of Neurophysiology. 82, 2271-2283 (1999).
- Miller, M., Downham, D., Lexell, J. Superimposed single impulse and pulse train electrical stimulation A quantitative assessment during submaximal isometric knee extension in young healthy men. Muscle and Nerve. 22 (8), 1038-1046 (1999).
- Button, D. C., Behm, D. G. The effect of stimulus anticipation on the interpolated twitch technique. Journal of Sports Science and Medicine. 7 (4), 520-524 (2008).
- Goss, D. a, Hoffman, R. L., Clark, B. C. Utilizing Transcranial Magnetic Stimulation to Study the Human Neuromuscular System. Journal of Visualized Experiments. (59), e3387(2012).
- Sartori, L., Betti, S., Castiello, U. Corticospinal excitability modulation during action observation. Journal Of Visualized Experiments: Jove. (82), 51001(2013).
- Rozand, V., Lebon, F., Papaxanthis, C., Lepers, R. Does a mental training session induce neuromuscular fatigue. Medicine and Science in Sports and Exercise. 46 (10), 1981-1989 (2014).
- Rozand, V., Cattagni, T., Theurel, J., Martin, A., Lepers, R. Neuromuscular fatigue following isometric contractions with similar torque time integral. International Journal of Sports Medicine. 36, 35-40 (2015).
- Belanger, A. Y., McComas, A. J. Extent of motor unit activation during effort. Journal of Applied Physiology. 51 (5), 1131-1135 (1981).
- Morse, C. I., Thom, J. M., Davis, M. G., Fox, K. R., Birch, K. M., Narici, M. V. Reduced plantarflexor specific torque in the elderly is associated with a lower activation capacity. European Journal of Applied Physiology. 92 (1-2), 219-226 (2004).
- Dalton, B. H., McNeil, C. J., Doherty, T. J., Rice, C. L. Age related reductions in the estimated numbers of motor units are minimal in the human soleus. Muscle and Nerve. 38 (3), 1108-1115 (2008).
- Hunter, S. K., Todd, G., Butler, J. E., Gandevia, S. C., Taylor, J. L. Recovery from supraspinal fatigue is slowed in old adults after fatiguing maximal isometric contractions. Journal of Applied Physiology. 105 (4), 1199-1209 (2008).
- Jakobi, J. M., Rice, C. L. Voluntary muscle activation varies with age and muscle group. Journal of Applied Physiology. 93 (2), 457-462 (2002).
- Lepers, R., Millet, G. Y., Maffiuletti, N. a Effect of cycling cadence on contractile and neural properties of knee extensors. Medicine and Science in Sports and Exercise. 33 (11), 1882-1888 (2001).
- Duchateau, J., Hainaut, K. Isometric or dynamic training differential effects on mechanical properties of a human muscle. Journal of Applied Physiology. 56 (2), 296-301 (1984).
- Millet, G. Y., Martin, V., Martin, A., Vergès, S. Electrical stimulation for testing neuromuscular function From sport to pathology. European Journal of Applied Physiology. 111, 2489-2500 (2011).
- Cattagni, T., Scaglioni, G., Laroche, D., Van Hoecke, J., Gremeaux, V., Martin, A. Ankle muscle strength discriminates fallers from non fallers. Frontiers in Aging Neuroscience. 6, 336(2014).
- Horstman, A. M., Beltman, M. J., et al. Intrinsic muscle strength and voluntary activation of both lower limbs and functional performance after stroke. Clinical Physiology and Functional Imaging. 28 (4), 251-261 (2008).
- Sica, R. E., Herskovits, E., Aguilera, N., Poch, G. An electrophysiological investigation of skeletal muscle in Parkinson’s disease. Journal of the Neurological Sciences. 18 (4), 411-420 (1973).
- Knikou, M., Mummidisetty, C. K. Locomotor Training Improves Premotoneuronal Control after Chronic Spinal Cord Injury. Journal of Neurophysiology. 111 (11), 2264-2275 (2014).
Access restricted. Please log in or start a trial to view this content.
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon