Method Article
Dimensionnement électrochimique précis de particules électro-inactives individuelles
Dans cet article
Résumé
En tant que technique analytique, l’électrochimie à nanoimpact, une approche de plus en plus importante pour compter et caractériser les particules électro-inactives à l’échelle nanométrique, souffre d’une faible précision en raison des distributions de courant hétérogènes qui résultent de son utilisation d’ultramicroélectrodes. Il s’agit ici d’une approche généralisée, appelée « interruption électrocatalytique », qui améliore la précision de ces mesures.
Résumé
L’électrochimie des nanoimpacts permet la caractérisation in situ résolue dans le temps (p. ex., taille, activité catalytique) d’unités de nanomatériaux uniques, fournissant un moyen d’élucider les hétérogénéités qui seraient masquées dans les études d’ensemble. Pour mettre en œuvre cette technique avec des particules inactives redox, une réaction redox en phase solution est utilisée pour produire un courant de fond à l’état stationnaire sur une ultramicroélectrode à disque. Lorsqu’une particule s’adsorbe sur l’électrode, elle produit une réduction progressive de la zone de l’électrode exposée, ce qui produit, à son tour, une diminution progressive du courant proportionnelle à la taille de l’espèce adsorbante. Historiquement, cependant, l’électrochimie à nanoimpact a souffert d'«effets de bord », dans lesquels la couche de diffusion radiale formée à la circonférence des ultramicroélectrodes rend la taille du pas dépendante non seulement de la taille de la particule, mais aussi de l’endroit où elle atterrit sur l’électrode. L’introduction de la génération de courant électrocatalytique atténue toutefois l’hétérogénéité causée par les effets de bord, améliorant ainsi la précision de la mesure. Dans cette approche, appelée « interruption électrocatalytique », un substrat qui régénère la sonde redox au niveau de la couche de diffusion est introduit. Cela déplace l’étape limitant la vitesse de la génération actuelle de la diffusion à la constante de vitesse de réaction homogène, réduisant ainsi l’hétérogénéité du flux et augmentant la précision du dimensionnement des particules d’un ordre de grandeur. Le protocole décrit ici explique la configuration et la collecte de données utilisées dans les expériences de nanoimpact mettant en œuvre cet effet pour améliorer la précision du dimensionnement des matériaux inactifs redox.
Introduction
L’électrochimie à nanoimpact est une technique électrochimique qui permet la détection temporelle de particules individuelles in situ dans un échantillon 1,2,3,4,5,6,7. Les particules individuelles qui peuvent être caractérisées par cette approche couvrent une large gamme de matériaux 6,8,9,10,11,12,13 et englobent des dimensions allant des atomes individuels aux cellules entières 7,8,14,15,16 . Pour permettre la détection et la caractérisation de ces petits matériaux, la technique utilise des ultramicroélectrodes à disque à l’échelle du micron et du submicron. L’impact d’une nanoparticule électroactive sur une telle électrode produit un changement de courant facilement quantifiable lorsque la nanoparticule subit une réaction redox. Pour étendre cela à la détection des matières actives électro-dans, une réaction électrochimique de fond est utilisée pour produire un courant stationnaire qui est réduit par étapes lorsque l’adsorption des nanoparticules modifie la surface de l’électrode17. Dans ce schéma, les ultramicroélectrodes sont utilisées pour augmenter le changement relatif produit par chaque nanoimpact. La couche de diffusion radiale produite par ces microélectrodes réduit cependant la précision de mesure en raison des « effets de bord »18. Ceux-ci se produisent parce que le flux de l’espèce redox vers l’électrode est plus important sur les bords de l’électrode qu’à son centre19. Ainsi, lorsqu’une seule nanoparticule atterrit au bord de la surface de l’électrode, l’événement actuel résultant est plus grand que celui observé pour une particule identique atterrissant au centre de l’électrode19, et cet effet est plus significatif pour les ultramicroélectrodes en raison de leur faible rapport surface/circonférence. Ces effets de bord nuisent considérablement à la précision de l’électrochimie à nanoimpact; En raison de leur présence, les distributions granulométriques estimées produites par le dimensionnement par nanoimpact sont 20 fois plus larges que celles obtenues par des techniques de microscopie « de référence »20. Cette précision réduite nuit à l’utilisation de l’électrochimie à nanoimpact comme technique analytique pour évaluer l’hétérogénéité des matériaux inactifs redox à l’échelle nanométrique 4,17,19,21,22,23,24,25,26.
Nous avons récemment introduit une méthode (Figure 1) qui atténue les effets de bord dans les approches nanoimpact20. Dans cette méthode, l’introduction d’un substrat régénère l’espèce redox près de la surface de l’ultramicroélectrode. Cela déplace l’étape limitant la vitesse dans la génération de courant de la diffusion à la vitesse de la réaction chimique homogène de l’espèce redox dans la solution27,28, réduisant ainsi la mesure dans laquelle le champ de diffusion radiale contribue à des courants hétérogènes. Plus précisément, l’oxydation de la 2,2,6,6-tétraméthylpipéridine 1-oxyl (TEMPO) fournit la réaction redox de fond à l’ultramicroélectrode29. L’ajout de maltose à cela régénère la forme réduite de TEMPO30,31. Cette régénération est rapide32, et elle comprime la couche de diffusion et réduit l’hétérogénéité actuelle associée à l’atterrissage spatial20. En conséquence, l’approche de « l’interruption électrocatalytique » améliore la précision du dimensionnement des particules à nanoimpact d’un ordre de grandeur.
Protocole
1. Mise en place d’un système silencieux
NOTE: Les expériences pertinentes nécessitent un potentiostat capable d’obtenir la mesure hautement résolue dans le temps des faibles courants. Pour ce faire, utilisez un potentiostat commercial de qualité recherche capable d’une résolution temporelle de 1 μs qui peut quantifier les courants au niveau du femtoampère. Pour réduire davantage les interférences électroniques provenant de l’environnement, menez des expériences dans deux cages de Faraday nicheuses. S’assurer que l’installation est capable d’un écart quadratique moyen inférieur à 100 fA pour une expérience de chronoampérométrie échantillonnée à 10 Hz dans du chlorure de potassium 0,1 M.
- Procurez-vous et installez l’équipement, y compris les cages de potentiostat et de Faraday.
REMARQUE : Les cages de Faraday peuvent être obtenues commercialement ou fabriquées sur mesure à l’aide de métaux conducteurs (p. ex. cuivre ou aluminium). Des cages Faraday en aluminium fabriquées sur mesure ont été utilisées pour l’étude décrite ici (voir le tableau des matériaux).
2. Préparation expérimentale
- Utiliser des billes de polystyrène modifiées au carboxylate de 2 μm de diamètre disponibles dans le commerce (voir le tableau des matériaux).
NOTE: Bien que ce système puisse être généralisé à d’autres espèces électro-inactives23,33, il est essentiel de se rappeler que les impacts reposent sur la migration électrophorétique en plus du mouvement brownien. Ainsi, appliquer un potentiel attrayant pour les espèces d’intérêt, et maintenir de faibles concentrations de sel17. - Préparez les solutions suivantes, qui peuvent être conservées à température ambiante pendant au moins 1 mois.
- Préparer une solution carbonatée de 50 mM et titrer à pH 12,0 en utilisant 1 M de NaOH. Surveillez le pH chaque semaine.
- Préparer une solution de perchlorate de sodium 1 M.
- Préparez les solutions suivantes fraîches chaque jour, en les jetant à la fin de la journée.
- Préparer un TEMPO de 10 mM dans une solution carbonatée de 50 mM, pH 12,0.
- Préparer un stock de maltose de 500 mM dans une solution carbonatée de 50 mM, pH 12,0.
- Sélectionnez l’électrode de travail. Pour des résultats cohérents, choisir une ultramicroélectrode (voir le tableau des matériaux) de telle sorte que le rayon de l’espèce à caractériser ne soit pas inférieur à 10% à 15% du rayon de l’électrode 17,21,23,33,34.
REMARQUE : Ce ratio peut être minimisé après avoir déterminé l’ampleur des étapes actuelles associées à l’impact pour la détection optimale d’une espèce d’intérêt particulière. Le matériau de l’électrode choisi doit catalyser la réaction redox de fond. - Préparer deux cellules électrochimiques de 5 mL chacune.
- Préparer une cellule témoin contenant 1 mM de TEMPO et 5 mM de perchlorate de sodium (voir le tableau des matières) dans un tampon carbonaté à pH 12,0.
- Préparer une cellule d’essai contenant une solution de 1 mM de TEMPO, 5 mM de perchlorate de sodium et 120 mM de maltose dans un tampon carbonaté à pH 12,0.
REMARQUE: Le rapport du médiateur redox au substrat (ici, TEMPO au maltose) peut être modifié pour explorer les effets de la vitesse de réaction20. Cette valeur donne un aperçu de la réaction chimique homogène. - Après avoir préparé ces cellules, mettez-les de côté pour des mesures électrochimiques ultérieures.
3. Polissage des électrodes
- Avant chaque cycle expérimental, polir l’électrode séquentiellement pendant 2 minutes chacune avec une suspension d’alumine de 1 μm, 0,3 μm et 0,5 μm (voir le tableau des matériaux) sur des tampons de polissage.
- Déplacez l’électrode selon un motif « figure 8 » pour assurer un polissage uniforme35,36. Rincer généreusement à l’eau désionisée et sécher avec une lingette de laboratoire.
REMARQUE: Ne soniquez pas les ultramicroélectrodes, car cela pourrait les endommager.
4. Mesures électrochimiques
REMARQUE : Voir la figure 2 pour les résultats.
- Utilisez une configuration à trois électrodes pour les mesures électrochimiques. Pour les expériences décrites ici, utilisez une ultramicroélectrode en fibre de carbone de 11 μm, une électrode de compteur de fil de platine et une électrode de référence au calomel saturé (SCE) (voir le tableau des matériaux).
NOTE: Les fenêtres de potentiel électrochimique pour les expériences sont indiquées ci-dessous; à titre de référence, TEMPO a un potentiel formel de 0,49 V par rapport à SCE, et le maltose n’est pas électroactif dans la fenêtre de potentiel utilisée dans ces expériences. Toute fuite de l’électrode de référence peut affecter la concentration totaleen sel 37, réduisant ainsi l’entraînement électrophorétique des particules vers l’ultramicroélectrode et réduisant l’efficacité de comptage17. Si les expériences donnent une faible fréquence d’impact, envisager de passer à une électrode de référence sans fuite38,39. - Placez la cellule de contrôle dans les cages de Faraday et connectez les électrodes aux câbles appropriés. Collectez le premier ensemble de mesures électrochimiques pour chaque cellule. Il s’agira d’une expérience de voltampérométrie cyclique et d’une expérience de chronoampérométrie, comme détaillé ci-dessous.
- Collecter les données de voltampérométrie cyclique à l’aide d’une fenêtre de potentiel de 0,2 V à 0,8 V par rapport à SCE à des vitesses de balayage de 10 mV·s−1, 20 mV·s−1, 30 mV·s−1, 40 mV·s−1 et 50 mV·s−1.
- Recueillir les données de chronoampérométrie en appliquant 0,8 V par rapport à SCE pendant 10 minutes et enregistrer à une fréquence d’échantillonnage de 10 Hz.
REMARQUE : Une période d’échantillonnage de 10 minutes est recommandée pour les expériences de chronoampérométrie afin d’obtenir 10 à 15 impacts individuels aux étapes ultérieures. Aucun impact n’est prévu à ce stade.
- Ensuite, ajouter une solution diluée de billes de polystyrène à une concentration finale de 0,66 pM17 dans chacune des cellules électrochimiques. Après l’ajout des billes de polystyrène, prélever la deuxième série de mesures électrochimiques pour chaque cellule.
NOTE: La fréquence d’impact sera fonction de cette concentration et nécessite une optimisation pour recueillir suffisamment de données pour l’analyse statistique sans saturer le chronoampérogramme avec des impacts qui se chevauchent40,41,42,43.- Recueillir des données de chronoampérométrie en appliquant 0,8 V par rapport à SCE pendant 10 minutes et enregistrer à une fréquence d’échantillonnage de 10 Hz.
- Répéter les mesures chronoampérométriques jusqu’à ce que suffisamment de points de données aient été collectés pour l’analyse statistique. Pour détecter les différences entre les multiples méthodes de dimensionnement avec un niveau de confiance de 95 % et une puissance de 80 %, sélectionnez une taille d’échantillon d’environ 200 événements d’impact individuels.
5. Microscopie électronique à balayage (MEB)
REMARQUE : Utiliser la microscopie électronique à balayage comme technique de référence pour confirmer la taille des nanoparticules et l’hétérogénéité des échantillons19,44.
- Préparation des échantillons
- Pour préparer un échantillon pour l’imagerie, diluer une suspension de billes de latex carboxyle (voir le tableau des matériaux) 1:20 dans de l’eau. Goutte-couler 10 μL sur une lame de verre, sécher sous un flux d’azote et pulvériser l’échantillon avec une couche conductrice d’or-palladium sous argon.
- Imagerie
- En utilisant une tension de faisceau d’accélération de 5 kV et un courant de 0,4 nA, recueillir des images appropriées pour l’analyse statistique. Utilisez ImageJ45,46 ou un logiciel d’analyse d’image équivalent pour déterminer la taille des particules.
6. Analyse des données électrochimiques
- Enregistrer les données électrochimiques à l’aide du logiciel du potentiostat, et analyser ces résultats à l’aide d’un script écrit 20 qui permet d’extraire les magnitudes actuelles des changements détectés dans le courant stationnaire (étapes courantes) résultant d’événements de nanoimpact20.
REMARQUE : Ce texte fait partie des renseignements supplémentaires de notre rapport20 publié précédemment. - Convertissez les amplitudes des pas actuels en rayons de perles à l’aide de l’équation suivante :
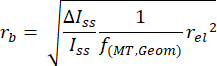
NOTE: Ici, rb est le rayon du cordon, relest le rayon de l’électrode, Δ I ss/ Iss est le rapport entre le changement du courant produit par l’adsorption d’une particule et le courant initial en régime permanent observé avant l’adsorption de cette particule, et f (MT, Geom) = 0,067 est un facteur d’échelle empirique qui dépend à la fois de considérations géométriques et de transport de masse20, 25. - Tracer la fréquence de détection d’un rayon de bille donné par rapport au rayon (Figure 3) pour quantifier les paramètres de distribution.
7. Modélisation
NOTE: Si vous le souhaitez, le mécanisme par lequel fonctionne l’interruption électrocatalytique peut être validé en confirmant le passage de la génération de courant limitée à la diffusion à la génération de courant à vitesse de réaction limitée. Pour décrire et visualiser, utilisez deux programmes de simulation numérique différents : un logiciel d’ajustement de voltammogramme, tel que DigiSim, pour déterminer la constante de vitesse homogène, et une plate-forme de modélisation multiphysique, telle que COMSOL Multiphysics, pour visualiser les changements locaux du profil de diffusion à la surface de l’ultramicroélectrode (voir Tableau des matériaux).
- Raccord Voltammogramme
REMARQUE : Utilisez le logiciel d’ajustement du voltammogramme pour déterminer la constante de vitesse homogène (Figure 4).- Recueillir les voltammogrammes cycliques dans une solution contenant 1 mM TEMPO (seulement) et 1 mM TEMPO plus 120 mM de maltose. Pour chaque condition, collectez des données à différentes vitesses de balayage et utilisez ces données pour les ajustements numériques de ces ensembles de données expérimentales.
- Ajuster les voltammogrammes collectés à partir de l’expérience TEMPO-only en utilisant un mécanisme E, qui décrit un processus de réaction entraîné uniquement par l’électrode47,48. Cela donnera les paramètres de l’électrode.
- À l’aide des paramètres d’électrode obtenus à l’étape 7.1.1.1, ajuster les voltammogrammes obtenus de la solution 1 mM TEMPO plus 120 maltose à un mécanisme EC′47,48, qui décrit un processus d’électrode suivi d’une réaction chimique homogène qui régénère le médiateur redox. Cela donnera la constante de vitesse homogène.
- Recueillir les voltammogrammes cycliques dans une solution contenant 1 mM TEMPO (seulement) et 1 mM TEMPO plus 120 mM de maltose. Pour chaque condition, collectez des données à différentes vitesses de balayage et utilisez ces données pour les ajustements numériques de ces ensembles de données expérimentales.
- Modélisation multiphysique
- Utiliser une plateforme de modélisation multiphysique pour visualiser les changements dans les profils de diffusion à la surface de l’ultramicroélectrode pour les systèmes de contrôle et d’interruption électrocatalytique 20,49,50,51,52 (Figure 5). Utilisez les paramètres de l’électrode et la constante de vitesse homogène obtenue à partir du raccord voltammogramme comme conditions initiales. Un aperçu général du flux de travail, qui peut être adapté à différents logiciels, est fourni ci-dessous.
- Entrez les paramètres globaux. Ceux-ci se composent de valeurs fixes telles que (mais sans s’y limiter) les valeurs de concentration, les coefficients de diffusion, le rayon d’électrode et la température.
- Construisez l’espace de simulation. Il s’agit d’un ensemble de géométries qui incluent l’électrode, la gaine isolante, l’espace de solution environnant représentant la région d’intérêt et un domaine d’éléments infinis représentant l’environnement de masse.
- Introduisez des progiciels de physique pour définir la simulation.
- Associez l’espace électrode à une étude d’électro-analyse. Définissez ici les valeurs initiales et la réaction de l’électrode d’intérêt.
- Associez l’espace de solution environnant à une étude chimique. Définissez ici la réaction chimique homogène qui suit la réaction de l’électrode.
- Introduisez un maillage sur l’ensemble de l’espace de simulation. Cela définit comment la géométrie est divisée pour résoudre le modèle. Pour obtenir des résultats de haute qualité, utilisez un maillage plus fin près de l’électrode.
- Pour observer les changements résultant de la constante de vitesse homogène, faites varier la valeur de ce paramètre à l’aide d’une étude paramétrique pour résoudre le modèle.
- Pour observer les changements en fonction du temps, faites varier la valeur de ce paramètre à l’aide d’une étude dépendante du temps pour résoudre le modèle.
Résultats
L’interruption électrocatalytique atténue les effets de bord en faisant passer le mécanisme de génération de courant primaire de limité par diffusion (c.-à-d. limité par le transport d’une sonde redox vers l’électrode) à limité cinétiquement (c.-à-d. limité par une réaction rapide en phase de solution)20. Cette méthode est modulaire, ce qui signifie qu’elle permet une approche mixte pour choisir le matériau de l’électrode, la sonde redox et le substrat, ce qui rend l’interruption électrocatalytique propice à la détection de nombreux nanomatériauxet biomatériaux 6,7,8,9,10,11,12,13,14,15,22 . La mise en œuvre de cette technique sur une électrode en fibre de carbone d’un rayon de 5,5 μm a permis d’améliorer de 10 fois la précision associée au dimensionnement électrochimique d’un système modèle (billes de polystyrène) dans une solution contenant TEMPO comme sonde redox et du maltose comme substrat.
En suivant ce protocole, les ensembles de données nécessaires pour valider ce mécanisme et sa capacité à restaurer la précision analytique lors du dimensionnement des nanoparticules électro-inactives peuvent être obtenus. Tout d’abord, les données du voltammogramme cyclique recueillies en l’absence de billes de polystyrène ont montré un événement redox réversible dans des expériences de contrôle impliquant TEMPO seul. À partir de là, l’ajout de maltose a entraîné une augmentation du pic oxydatif et une perte simultanée du pic réducteur lorsque le TEMPO oxydé a été régénéré par le maltose. Deuxièmement, les chronoampérogrammes collectés dans ces conditions ont démontré que les courants stationnaires à un potentiel oxydatif étaient plus élevés, ce qui correspond à l’amplification catalytique observée dans les résultats de voltampérométrie cyclique. Cette étape suggère également que la réaction chimique en vrac est maintenue par la réaction de l’électrode; Ainsi, toute amélioration par rapport à la méthode de contrôle durera pendant toute la durée de mesure. Toutefois, cela ne suffit pas à évaluer toute amélioration de la précision de la mesure; Pour ce faire, des données de chronoampérométrie doivent être collectées en présence de billes de polystyrène.
Pour évaluer la précision du dimensionnement, les données du chronoampérogramme ont été recueillies à l’aide de billes de polystyrène carboxylé de 2 μm. Lors de leur addition, des changements progressifs du courant du chronoampérogramme ont été observés lorsque des particules individuelles ont été impactées et absorbées (contrôle de la figure 2A, interruption électrocatalytique de la figure 2B). Chaque changement par étapes de l’amplitude du courant à l’état stationnaire a été converti en rayons de particules, et les données ont été visualisées sous forme d’histogrammes pour comparer la distribution de ces techniques électrochimiques à celle d’une technique de référence, telle que la microscopie électronique à balayage (Figure 3). Cette comparaison a ensuite permis de caractériser les métriques de précision associées à chaque approche de dimensionnement.
La modélisation a été utilisée pour appuyer ces observations expérimentales. Plus précisément, l’ajustement des voltammogrammes cycliques d’avant a donné des paramètres qui caractérisaient à la fois la réaction de l’électrode et la réaction chimique en phase de solution (Figure 4). À partir de la solution témoin, certains paramètres de l’échantillon obtenus étaient Efθ = 0,49 V, k 0 =0,02 cm·s-1 et ν = 10 mV·s-1 à T = 25 °C. À partir de la solution d’essai, les paramètres cinétiques qui limitaient la génération de courant ont pu être obtenus; plus précisément, lorsque Keq approchede l’infini, k obs = 2 200 M-1·s-1. Les simulations numériques pourraient ensuite utiliser ces valeurs comme conditions initiales pour générer un profil de concentration de la sonde redox (Figure 5). En l’absence de maltose, le profil de diffusion résultant était radial, ce qui entraînait un flux de matière hétérogène; Plus précisément, plus de matière diffusée à l’électrode sur les bords. L’introduction du maltose a comprimé le profil de diffusion, produisant à son tour des courants plus homogènes à travers la surface de l’électrode.
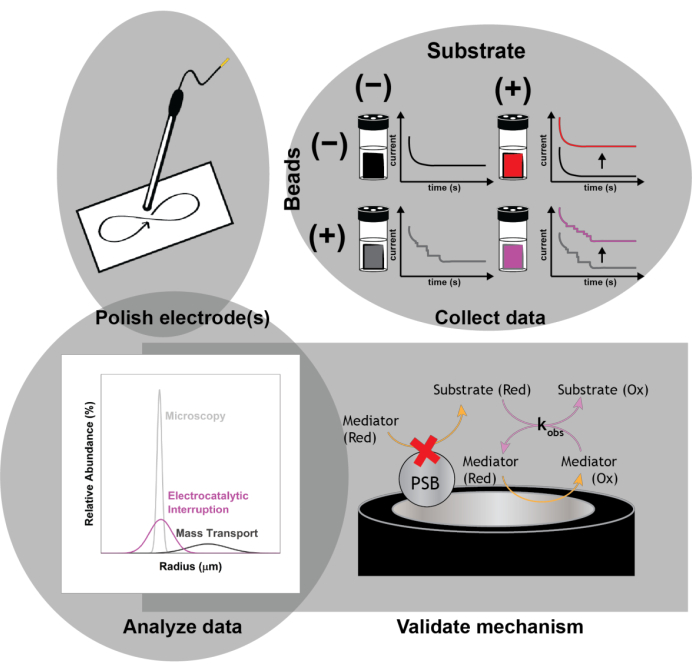
Figure 1 : Schéma du protocole expérimental. Polir les électrodes avant chaque cycle expérimental. Recueillir un ensemble de mesures électrochimiques de base (voltampérométrie cyclique et chronoampérométrie) en l’absence de billes avec et sans interruption électrocatalytique pour observer l’amélioration du courant avec l’ajout du substrat. Piquez les billes et collectez une deuxième série de mesures électrochimiques pour la détermination de la taille des nanoparticules impactantes. Valider le mécanisme d’action à l’aide de simulations numériques. Veuillez cliquer ici pour voir une version agrandie de cette figure.
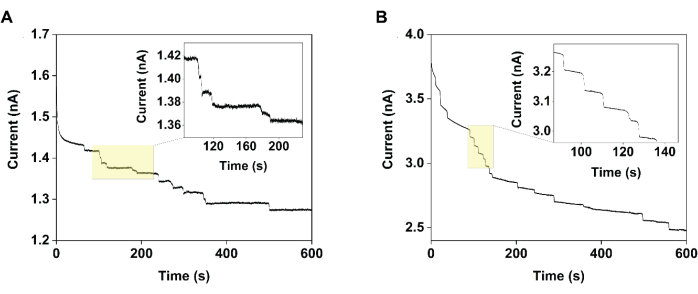
Figure 2 : Chronoampérogrammes collectés à l’aide d’une ultramicroélectrode en fibre de carbone de 11 μm de diamètre démontrant l’amélioration de la précision de mesure obtenue par interruption électrocatalytique. Plus précisément, lors de la mesure du courant en fonction du temps dans une solution de 1 mM TEMPO en absence (A) (témoin) et (B) présence de maltose 120 mM (interruption électrocatalytique), les étapes observées dans ce dernier cas étaient plus homogènes. Reproduit avec la permission de Chung et al.20. Veuillez cliquer ici pour voir une version agrandie de cette figure.
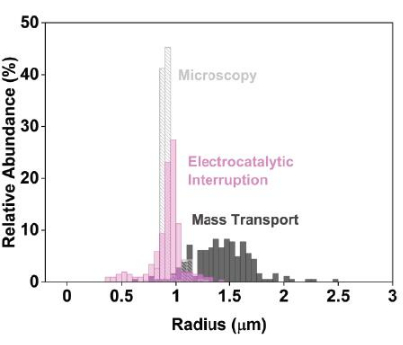
Figure 3 : Données précises de dimensionnement électrochimique lors de l’utilisation de l’interruption électrocatalytique par rapport à l’approche électrochimique conventionnelle à diffusion limitée. Pour représenter ces données, préparez des histogrammes comparant les distributions de taille déterminées par microscopie électronique à balayage (gris clair) et électrochimie (interruption électrocatalytique, rose; témoin, gris foncé). Les études conventionnelles de nanoimpact, dans lesquelles le courant est limité par le transport de masse du médiateur, produisent des distributions de taille estimées artificiellement larges (gris foncé). En revanche, la mise en œuvre d’une interruption électrocatalytique conduit à des estimations de taille plus étroites et plus précises (rose). Reproduit avec la permission de Chung et al.20. Veuillez cliquer ici pour voir une version agrandie de cette figure.
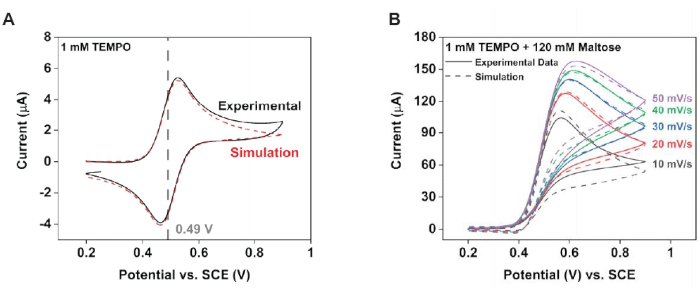
Figure 4 : Modélisation de la cinétique de l’électrode pour caractériser le nouveau schéma de réaction. À l’aide d’un logiciel d’ajustement de voltammogramme cyclique, extraire les paramètres de réaction de l’électrode à partir des données expérimentales. (A) Données avec 1 mM TEMPO. (B) Données avec 1 mM TEMPO plus 120 mM de maltose. Reproduit avec la permission de Chung et al.20. Veuillez cliquer ici pour voir une version agrandie de cette figure.
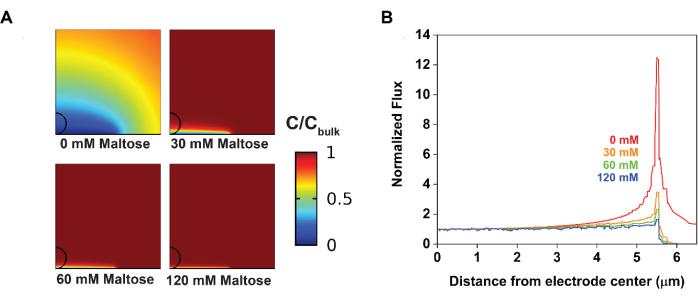
Figure 5 : Changements dans le flux de matière à la surface de l’électrode lors de l’introduction d’une interruption électrocatalytique visualisée par des simulations numériques. (A) L’ajout de maltose comprime la couche de diffusion d’une manière dépendante de la concentration. (B) L’ajout de maltose diminue le flux hétérogène aux bords de l’électrode. Reproduit avec la permission de Chung et al.20. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Discussion
L’interruption électrocatalytique est facile à mettre en œuvre et réduit d’un ordre de grandeur l’imprécision associée à l’électrochimie à nanoimpact. Cette précision accrue permet directement aux chercheurs de distinguer des particules de tailles différentes dans une solution mixte20. Il améliore également la capacité de détecter de manière fiable les particules inactives redox plus petites que la limite historiquement rapportée de 15% à 20% du rayon de l’électrode 17,21,23,34.
Alors que l’interruption électrochimique peut accueillir divers systèmes redox pour la détection de nanoparticules de divers matériaux électro-inactifs, l’identification de tels systèmes redox est restée un défi majeur. Le principal obstacle à la mise en œuvre d’une interruption électrochimique est l’identification d’une réaction chimique suffisamment rapide pour réduire considérablement les contributions confondantes des effets de bord. Plus précisément, alors que certains exemples de réactions EC′, dans lesquelles une réaction d’électrode est suivie d’une réaction chimique qui régénère le réactif de l’électrode, sont bien caractérisés dans la littérature 29,32,53,54,55, peu sont suffisamment rapides pour améliorer la précision de mesure. Dans cette étude, parmi les réactions suffisamment rapides, un système TEMPO-maltose a été choisi, ce qui a donné une constante de vitesse observée de 2 200 M-1·s-1. Ceci, en conjonction avec des simulations multiphysiques qui démontrent que des vitesses de réaction plus rapides conduisent à un flux plus homogène au bord de l’électrode, soutient la conclusion que seules les réactions chimiques rapides produisent des améliorations de courant de plusieurs fois aux ultramicroélectrodes.
L’interruption catalytique ne nécessite pas de manipulation de données ou de modification des ultramicroélectrodes disponibles dans le commerce. Pour expliquer l’hétérogénéité des magnitudes de courant caractéristiques des données de nanoimpact, Bonezzi et Boika ont introduit un modèle théorique qui relie l’amplitude actuelle des pas à la taille des particules25. Cette analyse, cependant, repose fortement sur la moyenne des magnitudes actuelles en fonction de la fréquence de collision. Non seulement cela empêche de mieux comprendre les propriétés des particules individuelles, mais cette technique reste également dépendante du flux du rapporteur redox vers l’électrode et ne supprime pas le problème des effets de bord, ce qui réduit la précision. Deng et al. ont introduit la première approche expérimentale pour traiter les effets de bord, en utilisant une ultramicroélectrode hémisphérique fabriquée à partir de mercure51. Les électrodes de gouttelettes de mercure, cependant, sont toxiques, mécaniquement instables et stables sur une fenêtre potentielle limitée56. De plus, la fabrication (et l’entretien) de microélectrodes parfaitement hémisphériques à l’aide d’autres matériaux reste un défi51,52. Plus récemment, Moazzenzade et al. ont proposé des ultramicroélectrodes en anneau pour la caractérisation des nanoimpacts52. Cette géométrie est prometteuse mais nécessite des capacités de nanofabrication. En revanche, l’interruption catalytique permet des expériences de nanoimpact avec des matériaux universellement trouvés dans un laboratoire d’électrochimie.
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Ce travail a été financé par la subvention des National Institutes of Health (NIH) R35GM142920. La recherche rapportée ici a utilisé les installations partagées de l’UCSB MRSEC (NSF DMR 1720256), membre du Materials Research Facilities Network (www.mrfn.org). Nous remercions Phoebe Hertler d’avoir contribué à l’article original auquel cet ouvrage fait référence. Nous remercions la Dre Claire Chisholm d’avoir contribué à l’acquisition des images de microscopie électronique à balayage.
matériels
| Name | Company | Catalog Number | Comments |
| 0.05 µm microalumina polish | Buehler | 4010075 | |
| 0.3 µm microalumina polish | Buehler | 4010077 | |
| 1 µm microalumina polish | Buehler | 4010079 | |
| 20 mL scintillation vials | Fisher Sci | 03-339-26C | |
| Analytical balance | Ohaus | ||
| Apreo C LoVac FEG SEM | Thermo Fisher | ||
| Carbon fiber microelectrode | ALS | 002007 | Working electrode; purchased from CH Instruments |
| Carboxyl Latex Beads, 4% w/v, 2 µm | ThermoFisher Scientific | C37278 | |
| COMSOL Multiphysics | COMSOL Multiphysics | v6.0 | |
| D-(+)-Maltose monohydrate | Sigma Aldrich | M5885 | |
| DigiSim | Bioanalytical Systems, Inc. | v3.03b | Discontinued; comparable software is available commercially through the same vendor |
| EC-Lab | BioLogic | v11.27 | |
| Faraday cages | Custom; analogous equipment can be commercially purchased or fabriated of conductive sheet metals (e.g., copper or aluminum) | ||
| Hummer Sputter Coater | Anatech USA | ||
| OriginPro | OriginLab | v2022b | |
| P1000 micropipette | Fisher Scientific | ||
| P2 micropipette | Fisher Scientific | ||
| P20 micropipette | Fisher Scientific | ||
| P200 micropipette | Fisher Scientific | ||
| Platinum Wire Electrode | CH Instruments | CHI115 | Counter electrode |
| Potassium chloride | Sigma Aldrich | P3911 | |
| PSA-backed MicroCloth | Buehler | 407218 | |
| Saturated Calomel Electrode | CH Instruments | CHI150 | Reference electrode |
| Sodium carbonate | Fisher Chemical | S263 | |
| Sodium hydroxide | Sigma Aldrich | S8045 | |
| Sodium perchlorate | EM Science | SX0692 | |
| SP-300 | BioLogic | ||
| TEMPO | Oakwood Chemical | 013714 | |
| Ultra Low Current module | BioLogic |
Références
- Heyrovsky, M., Jirkovsky, J. Polarography and voltammetry of ultrasmall colloids: Introduction to a new field. Langmuir. 11 (11), 4288-4292 (1995).
- Kleijn, S. E. F., et al. Landing and catalytic characterization of individual nanoparticles on electrode surfaces. Journal of the American Chemical Society. 134 (45), 18558-18561 (2012).
- Hill, C. M., Clayton, D. A., Pan, S. Combined optical and electrochemical methods for studying electrochemistry at the single molecule and single particle level: Recent progress and perspectives. Physical Chemistry Chemical Physics. 15 (48), 20797-20807 (2013).
- Dick, J. E., Hilterbrand, A. T., Boika, A., Upton, J. W., Bard, A. J. Electrochemical detection of a single cytomegalovirus at an ultramicroelectrode and its antibody anchoring. Proceedings of the National Academy of Sciences of the United States of America. 112 (17), 5303-5308 (2015).
- Mirkin, M. V., Sun, T., Yu, Y., Zhou, M. Electrochemistry at one nanoparticle. Accounts of Chemical Research. 49 (10), 2328-2335 (2016).
- Sokolov, S. V., Eloul, S., Kätelhön, E., Batchelor-McAuley, C., Compton, R. G. Electrode-particle impacts: A users guide. Physical Chemistry Chemical Physics. 19 (1), 28-43 (2017).
- Stevenson, K. J., Tschulik, K. A materials driven approach for understanding single entity nano impact electrochemistry. Current Opinion in Electrochemistry. 6 (1), 38-45 (2017).
- Baker, L. A. Perspective and prospectus on single-entity electrochemistry. Journal of the American Chemical Society. 140 (46), 15549-15559 (2018).
- Cheng, W., Compton, R. G. Electrochemical detection of nanoparticles by 'nano-impact' methods. TrAC Trends in Analytical Chemistry. 58, 79-89 (2014).
- Bard, A. J., Fan, F. -. R. F. Electrochemical detection of single molecules. Accounts of Chemical Research. 29 (12), 572-578 (1996).
- Xiao, X., Bard, A. J. Observing single nanoparticle collisions at an ultramicroelectrode by electrocatalytic amplification. Journal of the American Chemical Society. 129 (31), 9610-9612 (2007).
- Anderson, T. J., Zhang, B. Single-nanoparticle electrochemistry through immobilization and collision. Accounts of Chemical Research. 49 (11), 2625-2631 (2016).
- Goines, S., Dick, J. E. Review-Electrochemistry's potential to reach the ultimate sensitivity in measurement science. Journal of the Electrochemical Society. 167 (3), 037505 (2020).
- Kai, T., Zhou, M., Johnson, S., Ahn, H. S., Bard, A. J. Direct observation of C2O4•- and CO2•- by oxidation of oxalate within nanogap of scanning electrochemical microscope. Journal of the American Chemical Society. 140 (47), 16178-16183 (2018).
- Dick, J. E. Electrochemical detection of single cancer and healthy cell collisions on a microelectrode. Chemical Communications. 52 (72), 10906-10909 (2016).
- Sepunaru, L., Sokolov, S. V., Holter, J., Young, N. P., Compton, R. G. Electrochemical red blood cell counting: One at a time. Angewandte Chemie International Edition. 55 (33), 9768-9771 (2016).
- Quinn, B. M., van't Hof, P. G., Lemay, S. G. Time-resolved electrochemical detection of discrete adsorption events. Journal of the American Chemical Society. 126 (27), 8360-8361 (2004).
- Oldham, K. B. Edge effects in semiinfinite diffusion. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 122, 1-17 (1981).
- Fosdick, S. E., Anderson, M. J., Nettleton, E. G., Crooks, R. M. Correlated electrochemical and optical tracking of discrete collision events. Journal of the American Chemical Society. 135 (16), 5994-5997 (2013).
- Chung, J., Hertler, P., Plaxco, K. W., Sepunaru, L. Catalytic interruption mitigates edge effects in the characterization of heterogeneous, insulating nanoparticles. Journal of the American Chemical Society. 143 (45), 18888-18898 (2021).
- Boika, A., Thorgaard, S. N., Bard, A. J. Monitoring the electrophoretic migration and adsorption of single insulating nanoparticles at ultramicroelectrodes. The Journal of Physical Chemistry B. 117 (16), 4371-4380 (2013).
- Kim, B. -. K., Boika, A., Kim, J., Dick, J. E., Bard, A. J. Characterizing emulsions by observation of single droplet collisions-Attoliter electrochemical reactors. Journal of the American Chemical Society. 136 (13), 4849-4852 (2014).
- Dick, J. E., Renault, C., Bard, A. J. Observation of single-protein and DNA macromolecule collisions on ultramicroelectrodes. Journal of the American Chemical Society. 137 (26), 8376-8379 (2015).
- Lee, J. Y., Kim, B. -. K., Kang, M., Park, J. H. Label-free detection of single living bacteria via electrochemical collision event. Scientific Reports. 6 (1), 30022 (2016).
- Bonezzi, J., Boika, A. Deciphering the magnitude of current steps in electrochemical blocking collision experiments and its implications. Electrochimica Acta. 236, 252-259 (2017).
- Ellison, J., Batchelor-McAuley, C., Tschulik, K., Compton, R. G. The use of cylindrical micro-wire electrodes for nano-impact experiments; Facilitating the sub-picomolar detection of single nanoparticles. Sensors and Actuators B: Chemical. 200, 47-52 (2014).
- Denuault, G., Fleischmann, M., Pletcher, D., Tutty, O. R. Development of the theory for the interpretation of steady state limiting currents at a microelectrode: EC' processes: First and second order reactions. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 280 (2), 243-254 (1990).
- Francke, R., Little, R. D. Redox catalysis in organic electrosynthesis: Basic principles and recent developments. Chemical Society Reviews. 43 (8), 2492-2521 (2014).
- Nutting, J. E., Rafiee, M., Stahl, S. S. Tetramethylpiperidine N-Oxyl (TEMPO), phthalimide N-oxyl (PINO), and related N-Oxyl species: Electrochemical properties and their use in electrocatalytic reactions. Chemical Reviews. 118 (9), 4834 (2018).
- Pierre, G., et al. TEMPO-mediated oxidation of polysaccharides: An ongoing story. Carbohydrate Polymers. 165, 71-85 (2017).
- Liaigre, D., Breton, T., Belgsir, E. M. Kinetic and selectivity control of TEMPO electro-mediated oxidation of alcohols. Electrochemistry Communications. 7 (3), 312-316 (2005).
- Rafiee, M., Karimi, B., Alizadeh, S. Mechanistic study of the electrocatalytic oxidation of alcohols by TEMPO and MHPI. ChemElectroChem. 1 (2), 455-462 (2014).
- Deng, Z., Renault, C. Detection of individual insulating entities by electrochemical blocking. Current Opinion in Electrochemistry. 25, 100619 (2021).
- Laborda, E., Molina, A., Batchelor-McAuley, C., Compton, R. G. Individual detection and characterization of non-electrocatalytic, redox-inactive particles in solution by using electrochemistry. ChemElectroChem. 5 (3), 410-417 (2018).
- Elgrishi, N., et al. A practical beginner's guide to cyclic voltammetry. Journal of Chemical Education. 95 (2), 197-206 (2018).
- Cardwell, T. J., Mocak, J., Santos, J. H., Bond, A. M. Preparation of microelectrodes: comparison of polishing procedures by statistical analysis of voltammetric data. Analyst. 121 (3), 357-362 (1996).
- Lämmel, C., Heubner, C., Liebmann, T., Schneider, M. Critical impact of chloride containing reference electrodes on electrochemical measurements. Electroanalysis. 29 (12), 2752-2756 (2017).
- Walker, N. L., Dick, J. E. Leakless, bipolar reference electrodes: Fabrication, performance, and miniaturization. Analytical Chemistry. 93 (29), 10065-10074 (2021).
- Troudt, B. K., Rousseau, C. R., Dong, X. I. N., Anderson, E. L., Bühlmann, P. Recent progress in the development of improved reference electrodes for electrochemistry. Analytical Sciences. 38 (1), 71-83 (2022).
- Stuart, E. J. E., Zhou, Y. -. G., Rees, N. V., Compton, R. G. Particle-impact nanoelectrochemistry: A Fickian model for nanoparticle transport. RSC Advances. 2 (33), 12702-12705 (2012).
- Boika, A., Bard, A. J. Time of first arrival in electrochemical collision experiments as a measure of ultralow concentrations of analytes in solution. Analytical Chemistry. 87 (8), 4341-4346 (2015).
- Robinson, D. A., et al. Collision dynamics during the electrooxidation of individual silver nanoparticles. Journal of the American Chemical Society. 139 (46), 16923-16931 (2017).
- Lemay, S. G., Moazzenzade, T. Single-entity electrochemistry for digital biosensing at ultralow concentrations. Analytical Chemistry. 93 (26), 9023-9031 (2021).
- Vernon-Parry, K. D. Scanning electron microscopy: An introduction. III-Vs Review. 13 (4), 40-44 (2000).
- Abramoff, M. D., Magalhães, P. J., Ram, S. J. Image processing with ImageJ. Biophotonics International. 11 (7), 36-42 (2004).
- Collins, T. J. ImageJ for microscopy. BioTechniques. 43, S25-S30 (2007).
- Bard, A. J., Faulkner, L. R. . Electrochemical Methods: Fundamentals and Applications. , (2001).
- Compton, R. G., Banks, C. E. . Understanding Voltammetry (Third Edition). , (2018).
- Cutress, I. J., Dickinson, E. J. F., Compton, R. G. Analysis of commercial general engineering finite element software in electrochemical simulations. Journal of Electroanalytical Chemistry. 638 (1), 76-83 (2010).
- Dickinson, E. J. F., Ekström, H., Fontes, E. COMSOL Multiphysics®: Finite element software for electrochemical analysis. A mini-review. Electrochemistry Communications. 40, 71-74 (2014).
- Deng, Z., Elattar, R., Maroun, F., Renault, C. In situ measurement of the size distribution and concentration of insulating particles by electrochemical collision on hemispherical ultramicroelectrodes. Analytical Chemistry. 90 (21), 12923-12929 (2018).
- Moazzenzade, T., Walstra, T., Yang, X., Huskens, J., Lemay, S. G. Ring ultramicroelectrodes for current-blockade particle-impact electrochemistry. Analytical Chemistry. 94 (28), 10168-101747 (2022).
- Nekrassova, O., et al. The oxidation of cysteine by aqueous ferricyanide: A kinetic study using boron doped diamond electrode voltammetry. Electroanalysis. 14 (21), 1464-1469 (2002).
- Kuss, S., Compton, R. G. Electrocatalytic detection of ascorbic acid using N,N,N',N'-tetramethyl-para-phenylene-diamine (TMPD) mediated oxidation at unmodified gold electrodes; Reaction mechanism and analytical application. Electrochimica Acta. 242, 19-24 (2017).
- Shayani-Jam, H., Nematollahi, D. Electrochemically mediated oxidation of glutathione and N-acetylcysteine with 4,4′-biphenol. Electrochimica Acta. 56 (25), 9311-9316 (2011).
- Vyskočil, V., Barek, J. Mercury electrodes-Possibilities and limitations in environmental electroanalysis. Critical Reviews in Analytical Chemistry. 39 (3), 173-188 (2009).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon