Method Article
Dimensionamento elettrochimico preciso di singole particelle elettro-inattive
In questo articolo
Riepilogo
Come tecnica analitica, l'elettrochimica a nanoimpatto, un approccio sempre più importante per contare e caratterizzare particelle elettro-inattive su scala nanometrica, soffre di scarsa precisione a causa delle distribuzioni di corrente eterogenee che derivano dal suo uso di ultramicroelettrodi. Qui è delineato un approccio generalizzato, definito "interruzione elettrocatalitica", che migliora la precisione in tali misurazioni.
Abstract
L'elettrochimica a nanoimpatto consente la caratterizzazione in situ risolta nel tempo (ad esempio, dimensioni, attività catalitica) di singole unità di nanomateriali, fornendo un mezzo per chiarire le eterogeneità che sarebbero mascherate negli studi di ensemble. Per implementare questa tecnica con particelle redox inattive, viene utilizzata una reazione redox in fase di soluzione per produrre una corrente di fondo stazionaria su un ultramicroelettrodo a disco. Quando una particella assorbe sull'elettrodo, produce una riduzione graduale dell'area dell'elettrodo esposta, che produce, a sua volta, una diminuzione graduale della corrente commisurata alle dimensioni della specie adsorbente. Storicamente, tuttavia, l'elettrochimica a nanoimpatto ha sofferto di "effetti bordo", in cui lo strato di diffusione radiale formato alla circonferenza degli ultramicroelettrodi rende la dimensione del passo dipendente non solo dalla dimensione della particella ma anche da dove atterra sull'elettrodo. L'introduzione della generazione di corrente elettrocatalitica, tuttavia, mitiga l'eterogeneità causata dagli effetti dei bordi, migliorando così la precisione di misura. In questo approccio, definito "interruzione elettrocatalitica", viene introdotto un substrato che rigenera la sonda redox nello strato di diffusione. Ciò sposta la fase limitante della generazione corrente dalla diffusione alla costante di velocità di reazione omogenea, riducendo così l'eterogeneità del flusso e aumentando la precisione del dimensionamento delle particelle di un ordine di grandezza. Il protocollo qui descritto spiega il set-up e la raccolta dei dati impiegati negli esperimenti di nanoimpatto che implementano questo effetto per una maggiore precisione nel dimensionamento di materiali redox inattivi.
Introduzione
L'elettrochimica a nanoimpatto è una tecnica elettrochimica che consente la rilevazione risolta nel tempo di singole particelle in situ in un campione 1,2,3,4,5,6,7. Le singole particelle che possono essere caratterizzate da questo approccio coprono una vasta gamma di materiali 6,8,9,10,11,12,13 e comprendono dimensioni da singoli atomi a cellule intere 7,8,14,15,16 . Per consentire il rilevamento e la caratterizzazione di materiali così piccoli, la tecnica utilizza ultramicroelettrodi a disco su scala micron e submicron. L'impatto di una nanoparticella elettroattiva su tale elettrodo produce un cambiamento di corrente facilmente quantificabile quando la nanoparticella subisce una reazione redox. Per espandere questo alla rilevazione di materiali attivi elettro-in, viene utilizzata una reazione elettrochimica di fondo per produrre una corrente stazionaria che viene ridotta inmodo graduale poiché l'adsorbimento delle nanoparticelle cambia l'area superficiale dell'elettrodo17. In questo schema, gli ultramicroelettrodi sono impiegati per aumentare il cambiamento relativo prodotto da ciascun nanoimpatto. Lo strato di diffusione radiale prodotto da tali microelettrodi, tuttavia, riduce la precisione di misura a causa di "effetti bordo"18. Questi si verificano perché il flusso delle specie redox all'elettrodo è maggiore ai bordi dell'elettrodo che al suo centro19. Pertanto, quando una singola nanoparticella atterra sul bordo della superficie dell'elettrodo, l'evento di corrente risultante è maggiore di quello visto per una particella identica che atterra al centro dell'elettrodo19, e questo effetto è più significativo per gli ultramicroelettrodi a causa del loro piccolo rapporto area-circonferenza. Questi effetti di bordo sminuiscono significativamente la precisione dell'elettrochimica a nanoimpatto; A causa della loro presenza, le distribuzioni granulometriche stimate prodotte dal dimensionamento a nanoimpatto sono 20 volte più ampie di quelle ottenute utilizzando tecniche di microscopia "gold standard"20. Questa precisione ridotta toglie l'uso dell'elettrochimica a nanoimpatto come tecnica analitica per valutare l'eterogeneità dei materiali redox inattivi su scala nanometrica 4,17,19,21,22,23,24,25,26.
Abbiamo recentemente introdotto un metodo (Figura 1) che mitiga gli effetti limite negli approcci di nanoimpatto20. In questo metodo, l'introduzione di un substrato rigenera le specie redox vicino alla superficie dell'ultramicroelettrodo. Ciò sposta la fase limitante della velocità nella generazione di corrente dalla diffusione alla velocità della reazione chimica omogenea delle specie redox nella soluzione27,28, riducendo così la misura in cui il campo di diffusione radiale contribuisce a correnti eterogenee. In particolare, l'ossidazione del 2,2,6,6-tetrametilpiperidina 1-ossile (TEMPO) fornisce la reazione redox di fondo all'ultramicroelettrodo29. L'aggiunta di maltosio a questo rigenera la forma ridotta di TEMPO30,31. Questa rigenerazione è rapida32, e comprime lo strato di diffusione e riduce l'attuale eterogeneità associata all'atterraggio spaziale20. Di conseguenza, l'approccio di "interruzione elettrocatalitica" migliora la precisione del dimensionamento delle particelle nanoimpact di un ordine di grandezza.
Protocollo
1. Stabilire un sistema a bassa rumorosità
NOTA: Gli esperimenti rilevanti richiedono un potenziostato in grado di ottenere la misura altamente risolta nel tempo di basse correnti. Per raggiungere questo obiettivo, utilizzare un potenziostato commerciale di livello di ricerca in grado di una risoluzione temporale di 1 μs in grado di quantificare le correnti a livello di femtoampere. Per ridurre ulteriormente le interferenze elettroniche dall'ambiente, condurre esperimenti all'interno di due gabbie di Faraday nidificanti. Assicurarsi che la configurazione sia in grado di eseguire una deviazione quadratica media della radice inferiore a 100 fA per un esperimento di cronoamperometria campionato a 10 Hz in cloruro di potassio 0,1 M.
- Ottenere e configurare l'attrezzatura, comprese le gabbie potenziostato e di Faraday.
NOTA: Le gabbie di Faraday possono essere ottenute commercialmente o fabbricate su misura utilizzando metalli conduttivi (ad esempio, rame o alluminio). Per lo studio qui descritto sono state utilizzate gabbie di Faraday in alluminio fabbricate su misura (vedi Tabella dei materiali).
2. Preparazione sperimentale
- Utilizzare perle di polistirene modificato con carbossilato di diametro 2 μm disponibili in commercio (vedi Tabella dei materiali).
NOTA: Mentre questo sistema può essere generalizzato ad altre specie elettro-inattive23,33, è fondamentale ricordare che gli impatti si basano sulla migrazione elettroforetica oltre al moto browniano. Pertanto, applicare un potenziale attraente per le specie di interesse e mantenere basse concentrazioni di sale17. - Preparare le seguenti soluzioni, che possono essere conservate a temperatura ambiente per almeno 1 mese.
- Preparare una soluzione di carbonato da 50 mM e titolare a pH 12,0 utilizzando NaOH 1 M. Monitorare il pH settimanalmente.
- Preparare una soluzione di perclorato di sodio 1 M.
- Preparare le seguenti soluzioni fresche ogni giorno, scartandole alla fine della giornata.
- Preparare un TEMPO da 10 mM in una soluzione di carbonato da 50 mM, pH 12,0.
- Preparare un brodo di maltosio da 500 mM in una soluzione di carbonato da 50 mM, pH 12,0.
- Selezionare l'elettrodo di lavoro. Per risultati coerenti, selezionare un ultramicroelettrodo (vedi Tabella dei materiali) in modo tale che il raggio della specie da caratterizzare non sia inferiore al 10%-15% del raggio dell'elettrodo 17,21,23,33,34.
NOTA: Questo rapporto può essere ridotto al minimo dopo aver determinato l'entità dei passi correnti associati all'impatto per il rilevamento ottimale di una particolare specie di interesse. Il materiale dell'elettrodo selezionato deve catalizzare la reazione redox di fondo. - Preparare due celle elettrochimiche da 5 ml ciascuna.
- Preparare una cella di controllo contenente 1 mM di TEMPO e 5 mM di perclorato di sodio (vedere tabella dei materiali) in tampone carbonatico a pH 12,0.
- Preparare una cella di prova contenente una soluzione di 1 mM TEMPO, 5 mM di perclorato di sodio e 120 mM di maltosio in tampone carbonatico a pH 12,0.
NOTA: Il rapporto tra il mediatore redox e il substrato (qui, TEMPO al maltosio) può essere variato per esplorare gli effetti della velocità di reazione20. Questo valore fornisce informazioni sulla reazione chimica omogenea. - Dopo aver preparato queste cellule, metterle da parte per le successive misurazioni elettrochimiche.
3. Lucidatura dell'elettrodo
- Prima di ogni esecuzione sperimentale, lucidare l'elettrodo in sequenza per 2 minuti ciascuno con un impasto di allumina da 1 μm, 0,3 μm e 0,5 μm (vedi Tabella dei materiali) su tamponi di lucidatura.
- Spostare l'elettrodo in uno schema "figura 8" per garantire una lucidatura uniforme35,36. Risciacquare liberamente con acqua deionizzata e asciugare con una salvietta da laboratorio.
NOTA: non sonicare gli ultramicroelettrodi, poiché ciò potrebbe danneggiarli.
4. Misure elettrochimiche
NOTA: vedere la Figura 2 per i risultati.
- Utilizzare una configurazione a tre elettrodi per le misurazioni elettrochimiche. Per gli esperimenti qui descritti, utilizzare un ultramicroelettrodo in fibra di carbonio da 11 μm, un elettrodo contatore a filo di platino e un elettrodo di riferimento per calomelano saturo (SCE) (vedi Tabella dei materiali).
NOTA: Le finestre di potenziale elettrochimico per gli esperimenti sono indicate di seguito; per riferimento, TEMPO ha un potenziale formale di 0,49 V rispetto a SCE e il maltosio non è elettroattivo nella finestra di potenziale utilizzata in questi esperimenti. Qualsiasi perdita dall'elettrodo di riferimento può influire sulla concentrazione totale di sale37, riducendo così il pilotaggio elettroforetico delle particelle verso l'ultramicroelettrodo e riducendo l'efficienza di conteggio17. Se gli esperimenti producono una bassa frequenza di impatto, prendere in considerazione il passaggio a un elettrodo di riferimento senza perdite38,39. - Impostare la cella di controllo nelle gabbie di Faraday e collegare gli elettrodi ai cavi appropriati. Raccogli la prima serie di misurazioni elettrochimiche per ogni cella. Questo consisterà in un esperimento di voltammetria ciclica e un esperimento di cronoamperometria, come dettagliato di seguito.
- Raccogliere i dati di voltammetria ciclica utilizzando una finestra potenziale da 0,2 V a 0,8 V rispetto a SCE a velocità di scansione di 10 mV·s−1, 20 mV·s−1, 30 mV·s−1, 40 mV·s−1 e 50 mV·s−1.
- Raccogli i dati di cronoamperometria applicando 0,8 V rispetto a SCE per 10 minuti e registra a una frequenza di campionamento di 10 Hz.
NOTA: Un periodo di campionamento di 10 minuti è raccomandato per gli esperimenti di cronoamperometria per ottenere 10-15 impatti individuali nelle fasi successive. Non sono previsti impatti in questo frangente.
- Quindi, aggiungere una soluzione diluita di perle di polistirene ad una concentrazione finale di 0,66 pM17 in ciascuna delle celle elettrochimiche. Dopo l'aggiunta delle perle di polistirolo, raccogliere la seconda serie di misurazioni elettrochimiche per ciascuna cella.
NOTA: La frequenza di impatto sarà una funzione di questa concentrazione e richiede un'ottimizzazione per raccogliere dati sufficienti per l'analisi statistica senza saturare il cronoamperogramma con impatti sovrapposti40,41,42,43.- Raccogli i dati di cronoamperometria applicando 0,8 V rispetto a SCE per 10 minuti e registra a una frequenza di campionamento di 10 Hz.
- Ripetere le misurazioni cronoamperometriche fino a quando non sono stati raccolti punti dati sufficienti per l'analisi statistica. Per rilevare le differenze tra i metodi di dimensionamento multiplo con un livello di confidenza del 95% e una potenza dell'80%, selezionare una dimensione del campione di circa 200 singoli eventi di impatto.
5. Microscopia elettronica a scansione (SEM)
NOTA: Utilizzare la microscopia elettronica a scansione come tecnica "gold standard" per confermare le dimensioni delle nanoparticelle e l'eterogeneità del campione 19,44.
- Preparazione del campione
- Per preparare un campione per l'imaging, diluire una sospensione di perline di lattice carbossilico (vedi Tabella dei materiali) 1:20 in acqua. Colare 10 μL su un vetrino, asciugare sotto un flusso di azoto e rivestire il campione con uno strato conduttivo di oro-palladio sotto argon.
- Imaging
- Utilizzando una tensione del fascio accelerante di 5 kV e una corrente di 0,4 nA, raccogliere le immagini appropriate per l'analisi statistica. Utilizzare ImageJ45,46 o un software di analisi delle immagini equivalente per determinare le dimensioni delle particelle.
6. Analisi dei dati elettrochimici
- Registrare i dati elettrochimici utilizzando il software del potenziostato e analizzare questi risultati utilizzando uno script scritto 20 in grado di estrarre le grandezze correnti dai cambiamenti rilevati nella corrente stazionaria (passi correnti) derivanti da eventi di nanoimpatto20.
NOTA: questo script è incluso come parte delle informazioni supplementari nel nostro rapporto20 pubblicato in precedenza. - Convertite le ampiezze dei passi correnti in raggi di tallone utilizzando la seguente equazione:
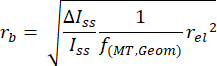
NOTA: Qui, rb è il raggio del tallone, relè il raggio dell'elettrodo, Δ I ss/Iss è il rapporto tra la variazione della corrente prodotta dall'adsorbimento di una particella e la corrente iniziale di stato stazionario osservata prima dell'adsorbimento di quella particella, e f(MT,Geom) = 0,067 è un fattore di scala empirico che dipende da considerazioni sia geometriche che di trasporto di massa20, 25. - Tracciare la frequenza di rilevamento di un determinato raggio del tallone rispetto al raggio (Figura 3) per quantificare le metriche di distribuzione.
7. Modellazione
NOTA: Se lo si desidera, il meccanismo con cui funziona l'interruzione elettrocatalitica può essere convalidato confermando il passaggio dalla generazione di corrente limitata dalla diffusione alla generazione di corrente limitata dalla velocità di reazione. Per descrivere e visualizzare, utilizzare due diversi programmi di simulazione numerica: un software di adattamento voltammografico, come DigiSim, per determinare la costante di velocità omogenea, e una piattaforma di modellazione multifisica, come COMSOL Multiphysics, per visualizzare le modifiche locali al profilo di diffusione sulla superficie dell'ultramicroelettrodo (vedi Tabella dei materiali).
- Raccordo voltammogramma
NOTA: Utilizzare il software di adattamento voltammografico per determinare la costante di velocità omogenea (Figura 4).- Raccogliere voltammogrammi ciclici in una soluzione contenente 1 mM TEMPO (solo) e 1 mM TEMPO più 120 mM di maltosio. Per ogni condizione, raccogliere dati a varie velocità di scansione e utilizzare questi dati per gli adattamenti numerici di questi set di dati sperimentali.
- Montare i voltammogrammi raccolti dall'esperimento TEMPO-only usando un meccanismo E, che descrive un processo di reazione guidato esclusivamente dall'elettrodo47,48. Questo produrrà i parametri dell'elettrodo.
- Utilizzando i parametri dell'elettrodo ottenuti al punto 7.1.1.1, adattare le voltammografie risultanti dalla soluzione di maltosio 1 mM TEMPO più 120 ad un meccanismo EC47,48, che descrive un processo elettrodico seguito da una reazione chimica omogenea che rigenera il mediatore redox. Questo produrrà la costante di velocità omogenea.
- Raccogliere voltammogrammi ciclici in una soluzione contenente 1 mM TEMPO (solo) e 1 mM TEMPO più 120 mM di maltosio. Per ogni condizione, raccogliere dati a varie velocità di scansione e utilizzare questi dati per gli adattamenti numerici di questi set di dati sperimentali.
- Modellazione multifisica
- Utilizzare una piattaforma di modellazione multifisica per visualizzare i cambiamenti nei profili di diffusione sulla superficie dell'ultramicroelettrodo sia per i sistemi di controllo che per quelli di interruzione elettrocatalitica 20,49,50,51,52 (Figura 5). Utilizzare i parametri dell'elettrodo e la costante di velocità omogenea ottenuti dal raccordo voltammografico come condizioni iniziali. Di seguito viene fornita un'ampia panoramica del flusso di lavoro, che può essere adattato a diversi software.
- Immettere i parametri globali. Questi sono costituiti da valori fissi come (ma non limitati a) i valori di concentrazione, i coefficienti di diffusione, il raggio dell'elettrodo e la temperatura.
- Costruisci lo spazio di simulazione. Questo è un insieme di geometrie che includono l'elettrodo, la guaina isolante, lo spazio della soluzione circostante che rappresenta la regione di interesse e un dominio di elementi infiniti che rappresenta l'ambiente di massa.
- Introdurre pacchetti di fisica per definire la simulazione.
- Associare lo spazio dell'elettrodo a uno studio di elettroanalisi. Definisci qui i valori iniziali e la reazione dell'elettrodo di interesse.
- Associare lo spazio della soluzione circostante a uno studio di chimica. Definisci qui la reazione chimica omogenea che segue la reazione dell'elettrodo.
- Introdurre una mesh sull'intero spazio di simulazione. Questo definisce il modo in cui la geometria viene divisa per risolvere il modello. Per ottenere risultati di alta qualità, utilizzare una maglia più fine vicino all'elettrodo.
- Per osservare i cambiamenti come risultato della costante di velocità omogenea, variare il valore di questo parametro utilizzando uno studio parametrico per risolvere il modello.
- Per osservare i cambiamenti in funzione del tempo, variare il valore di questo parametro utilizzando uno studio dipendente dal tempo per risolvere il modello.
Risultati
L'interruzione elettrocatalitica mitiga gli effetti limite spostando il meccanismo di generazione della corrente primaria da limitata alla diffusione (cioè limitata dal trasporto di una sonda redox all'elettrodo) a cineticamente limitata (cioè limitata da una reazione rapida in fase di soluzione)20. Questo metodo è modulare, il che significa che consente un approccio mix-and-match alla scelta del materiale dell'elettrodo, della sonda redox e del substrato, e questo rende l'interruzione elettrocatalitica suscettibile di rilevamento di molti nano e bio-materiali 6,7,8,9,10,11,12,13,14,15,22 . L'implementazione di questa tecnica su un elettrodo in fibra di carbonio con raggio di 5,5 μm ha prodotto un miglioramento di 10 volte nella precisione associata al dimensionamento elettrochimico di un sistema modello (perle di polistirolo) in una soluzione contenente TEMPO come sonda redox e maltosio come substrato.
Seguendo questo protocollo, è possibile ottenere i set di dati necessari per convalidare questo meccanismo e la sua capacità di ripristinare la precisione analitica durante il dimensionamento di nanoparticelle elettro-inattive. In primo luogo, i dati ciclici del voltammogramma raccolti in assenza di perle di polistirene hanno mostrato un evento redox reversibile in esperimenti di controllo che coinvolgono solo TEMPO. Da qui, l'aggiunta di maltosio ha comportato un aumento del picco ossidativo e una concomitante perdita del picco riduttivo poiché il TEMPO ossidato è stato rigenerato dal maltosio. In secondo luogo, i cronoamperogrammi raccolti in queste condizioni hanno dimostrato che le correnti stazionarie a un potenziale ossidativo erano più elevate, coerenti con l'amplificazione catalitica osservata nei risultati della voltammetria ciclica. Questo passaggio suggerisce anche che la reazione chimica di massa è mantenuta dalla reazione dell'elettrodo; Pertanto, eventuali miglioramenti rispetto al metodo di controllo dureranno per tutta la durata della misurazione. Tuttavia, questo da solo non è sufficiente per valutare eventuali miglioramenti della precisione di misurazione; Per fare ciò, i dati di cronoamperometria devono essere raccolti in presenza di perle di polistirolo.
Per valutare la precisione delle dimensioni, sono stati raccolti i dati del cronoamperogramma utilizzando perle di polistirene carbossilato da 2 μm. Dopo la loro aggiunta, sono stati osservati cambiamenti graduali nella corrente del cronoamperogramma quando le singole particelle hanno impattato e assorbito (controllo Figura 2A, Figura 2B interruzione elettrocatalitica). Ogni cambiamento graduale nella magnitudine della corrente stazionaria è stato convertito in raggi di particelle e i dati sono stati visualizzati come istogrammi per confrontare la distribuzione da queste tecniche elettrochimiche a quella di una tecnica gold standard, come la microscopia elettronica a scansione (Figura 3). Questo confronto ha poi permesso la caratterizzazione delle metriche di precisione associate a ciascun approccio di dimensionamento.
La modellazione è stata utilizzata per supportare queste osservazioni sperimentali. In particolare, il montaggio delle voltammografie cicliche di prima ha prodotto parametri che hanno caratterizzato sia la reazione dell'elettrodo che la reazione chimica in fase di soluzione (Figura 4). Dalla soluzione di controllo, alcuni parametri del campione ottenuti sono stati Efθ = 0,49 V, k 0 =0,02 cm·s-1 e ν = 10 mV·s-1 a T = 25° C. Dalla soluzione di prova, è stato possibile ottenere i parametri cinetici che hanno limitato la generazione di corrente; in particolare, quando Keq si avvicina all'infinito, kobs = 2.200 M-1·s-1. Le simulazioni numeriche potrebbero quindi utilizzare questi valori come condizioni iniziali per generare un profilo di concentrazione della sonda redox (Figura 5). In assenza di maltosio, il profilo di diffusione risultante era radiale, portando a flussi di materiale eterogenei; in particolare, più materiale diffuso all'elettrodo ai bordi. L'introduzione del maltosio ha compresso il profilo di diffusione, producendo, a sua volta, correnti più omogenee attraverso la superficie dell'elettrodo.
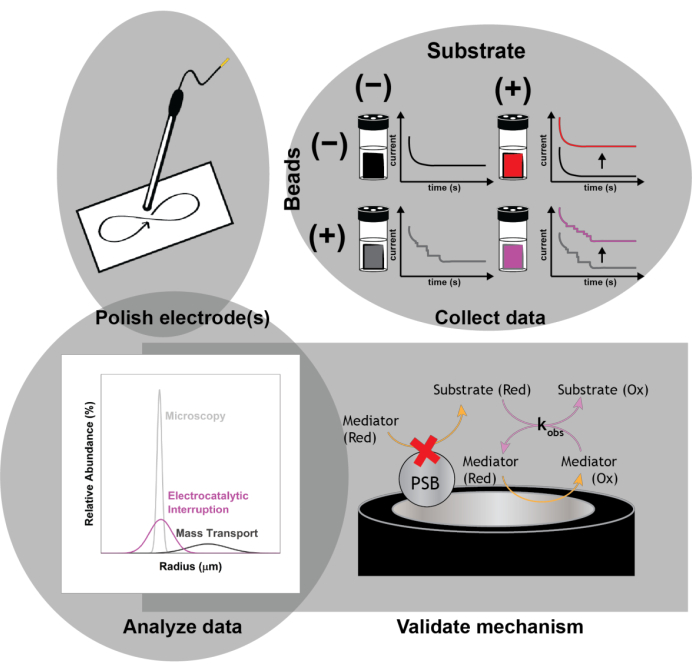
Figura 1: Schema del protocollo sperimentale. Lucidare gli elettrodi prima di ogni corsa sperimentale. Raccogliere un set di base di misure elettrochimiche (voltammetria ciclica e cronoamperometria) in assenza di perline con e senza interruzione elettrocatalitica per osservare l'aumento di corrente con l'aggiunta del substrato. Spike nelle perle e raccogliere una seconda serie di misurazioni elettrochimiche per la determinazione delle dimensioni delle nanoparticelle impattanti. Convalidare il meccanismo d'azione utilizzando simulazioni numeriche. Fare clic qui per visualizzare una versione ingrandita di questa figura.
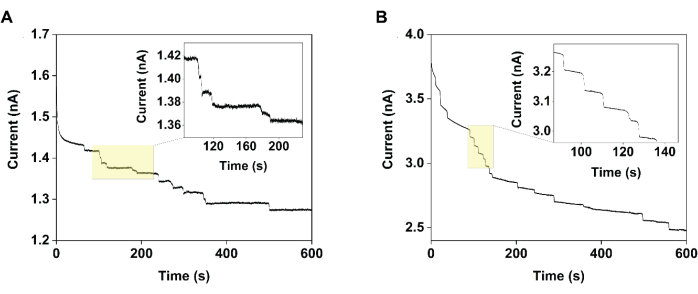
Figura 2: Cronoamperogrammi raccolti utilizzando un ultramicroelettrodo in fibra di carbonio da 11 μm di diametro che dimostrano il miglioramento della precisione di misura ottenuto utilizzando l'interruzione elettrocatalitica. In particolare, quando si misura la corrente rispetto al tempo in una soluzione di 1 mM TEMPO in (A) assenza (controllo) e (B) presenza di 120 mM di maltosio (interruzione elettrocatalitica), gli step osservati in quest'ultimo caso erano più omogenei. Ristampato con il permesso di Chung et al.20. Fare clic qui per visualizzare una versione ingrandita di questa figura.
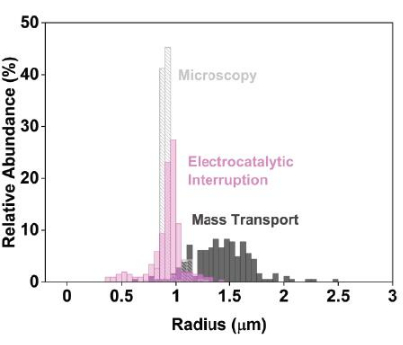
Figura 3: Dati precisi sul dimensionamento elettrochimico quando si utilizza l'interruzione elettrocatalitica rispetto all'approccio elettrochimico convenzionale a diffusione limitata. Per rappresentare questi dati, preparare istogrammi confrontando le distribuzioni dimensionali determinate utilizzando la microscopia elettronica a scansione (grigio chiaro) e l'elettrochimica (interruzione elettrocatalitica, rosa; controllo, grigio scuro). Gli studi convenzionali di nanoimpatto, in cui la corrente è limitata dal trasporto di massa del mediatore, producono distribuzioni dimensionali stimate artificialmente ampie (grigio scuro). Al contrario, l'implementazione dell'interruzione elettrocatalitica porta a stime dimensionali più strette e precise (rosa). Ristampato con il permesso di Chung et al.20. Fare clic qui per visualizzare una versione ingrandita di questa figura.
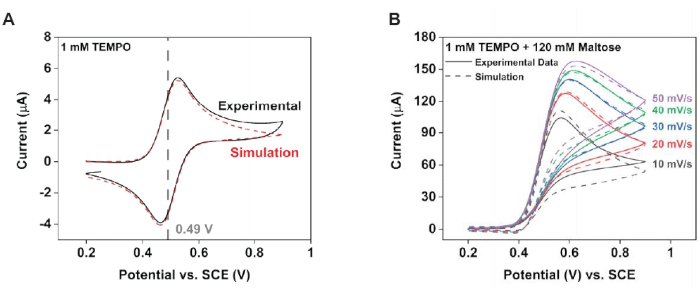
Figura 4: Modellazione della cinetica dell'elettrodo per caratterizzare il nuovo schema di reazione. Utilizzando il software di adattamento della voltammografia ciclica, estrarre i parametri di reazione dell'elettrodo dai dati sperimentali. (A) Dati con 1 mM TEMPO. (B) Dati con 1 mM TEMPO più 120 mM di maltosio. Ristampato con il permesso di Chung et al.20. Fare clic qui per visualizzare una versione ingrandita di questa figura.
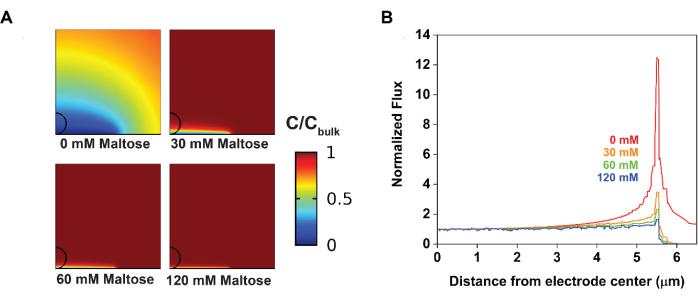
Figura 5: Variazioni del flusso di materiale sulla superficie dell'elettrodo dopo l'introduzione dell'interruzione elettrocatalitica visualizzate mediante simulazioni numeriche . (A) L'aggiunta di maltosio comprime lo strato di diffusione in modo dipendente dalla concentrazione. (B) L'aggiunta di maltosio deprime il flusso eterogeneo ai bordi degli elettrodi. Ristampato con il permesso di Chung et al.20. Fare clic qui per visualizzare una versione ingrandita di questa figura.
Discussione
L'interruzione elettrocatalitica è facile da implementare e riduce l'imprecisione associata all'elettrochimica a nanoimpatto di un ordine di grandezza. Questa maggiore precisione consente direttamente ai ricercatori di discriminare tra particelle di dimensioni diverse in una soluzione mista20. Migliora anche la capacità di rilevare in modo affidabile particelle redox-inattive più piccole del limite storicamente riportato del 15% -20% del raggio dell'elettrodo 17,21,23,34.
Mentre l'interruzione elettrochimica può ospitare vari sistemi redox per il rilevamento di nanoparticelle di vari materiali elettro-inattivi, l'identificazione di tali sistemi redox è rimasta una grande sfida. Il principale ostacolo all'implementazione dell'interruzione elettrochimica è l'identificazione di una reazione chimica abbastanza rapida da ridurre significativamente i contributi confondenti degli effetti di bordo. In particolare, mentre alcuni esempi di reazioni EC′, in cui una reazione dell'elettrodo è seguita da una reazione chimica che rigenera il reagente dell'elettrodo, sono ben caratterizzati in letteratura 29,32,53,54,55, pochi sono sufficientemente veloci per migliorare la precisione di misura. In questo studio, tra quelle reazioni che sono sufficientemente veloci, è stato scelto un sistema TEMPO-maltosio, e questo ha prodotto una costante di velocità osservata di 2.200 M-1·s-1. Questo, in combinazione con simulazioni multifisiche che dimostrano che velocità di reazione più elevate portano a un flusso più omogeneo sul bordo dell'elettrodo, supporta la conclusione che solo le reazioni chimiche veloci producono miglioramenti di corrente di diverse volte agli ultramicroelettrodi.
L'interruzione catalitica non richiede la manipolazione dei dati o modifiche agli ultramicroelettrodi disponibili in commercio. Per spiegare le magnitudini correnti eterogenee caratteristiche dei dati di nanoimpatto, Bonezzi e Boika hanno introdotto un modello teorico che mette in relazione la magnitudine del passo corrente con la dimensione delle particelle25. Questa analisi, tuttavia, si basa fortemente sulla media delle magnitudini attuali in funzione della frequenza di collisione. Non solo questo preclude la comprensione delle proprietà delle singole particelle, ma questa tecnica rimane anche dipendente dal flusso del reporter redox all'elettrodo e non rimuove il problema degli effetti di bordo, con conseguente riduzione della precisione. Deng et al. hanno introdotto il primo approccio sperimentale per affrontare gli effetti dei bordi, utilizzando un ultramicroelettrodo emisferico fabbricato dal mercurio51. Gli elettrodi a goccia di mercurio, tuttavia, sono tossici, meccanicamente instabili e stabili solo su una finestra potenziale limitata56. Inoltre, fabbricare (e mantenere) microelettrodi perfettamente emisferici utilizzando altri materiali rimane impegnativo51,52. Più recentemente, Moazzenzade et al. hanno proposto ultramicroelettrodi ad anello per la caratterizzazione del nanoimpatto52. Questa geometria è promettente ma richiede capacità di nanofabbricazione. Al contrario, l'interruzione catalitica consente esperimenti di nanoimpatto con materiali universalmente presenti in un laboratorio di elettrochimica.
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Questo lavoro è stato finanziato dal National Institutes of Health (NIH) grant R35GM142920. La ricerca qui riportata ha fatto uso di strutture condivise dell'UCSB MRSEC (NSF DMR 1720256), membro del Materials Research Facilities Network (www.mrfn.org). Ringraziamo Phoebe Hertler per aver contribuito all'articolo originale a cui questo lavoro fa riferimento. Ringraziamo la dottoressa Claire Chisholm per l'assistenza nell'acquisizione delle immagini al microscopio elettronico a scansione.
Materiali
| Name | Company | Catalog Number | Comments |
| 0.05 µm microalumina polish | Buehler | 4010075 | |
| 0.3 µm microalumina polish | Buehler | 4010077 | |
| 1 µm microalumina polish | Buehler | 4010079 | |
| 20 mL scintillation vials | Fisher Sci | 03-339-26C | |
| Analytical balance | Ohaus | ||
| Apreo C LoVac FEG SEM | Thermo Fisher | ||
| Carbon fiber microelectrode | ALS | 002007 | Working electrode; purchased from CH Instruments |
| Carboxyl Latex Beads, 4% w/v, 2 µm | ThermoFisher Scientific | C37278 | |
| COMSOL Multiphysics | COMSOL Multiphysics | v6.0 | |
| D-(+)-Maltose monohydrate | Sigma Aldrich | M5885 | |
| DigiSim | Bioanalytical Systems, Inc. | v3.03b | Discontinued; comparable software is available commercially through the same vendor |
| EC-Lab | BioLogic | v11.27 | |
| Faraday cages | Custom; analogous equipment can be commercially purchased or fabriated of conductive sheet metals (e.g., copper or aluminum) | ||
| Hummer Sputter Coater | Anatech USA | ||
| OriginPro | OriginLab | v2022b | |
| P1000 micropipette | Fisher Scientific | ||
| P2 micropipette | Fisher Scientific | ||
| P20 micropipette | Fisher Scientific | ||
| P200 micropipette | Fisher Scientific | ||
| Platinum Wire Electrode | CH Instruments | CHI115 | Counter electrode |
| Potassium chloride | Sigma Aldrich | P3911 | |
| PSA-backed MicroCloth | Buehler | 407218 | |
| Saturated Calomel Electrode | CH Instruments | CHI150 | Reference electrode |
| Sodium carbonate | Fisher Chemical | S263 | |
| Sodium hydroxide | Sigma Aldrich | S8045 | |
| Sodium perchlorate | EM Science | SX0692 | |
| SP-300 | BioLogic | ||
| TEMPO | Oakwood Chemical | 013714 | |
| Ultra Low Current module | BioLogic |
Riferimenti
- Heyrovsky, M., Jirkovsky, J. Polarography and voltammetry of ultrasmall colloids: Introduction to a new field. Langmuir. 11 (11), 4288-4292 (1995).
- Kleijn, S. E. F., et al. Landing and catalytic characterization of individual nanoparticles on electrode surfaces. Journal of the American Chemical Society. 134 (45), 18558-18561 (2012).
- Hill, C. M., Clayton, D. A., Pan, S. Combined optical and electrochemical methods for studying electrochemistry at the single molecule and single particle level: Recent progress and perspectives. Physical Chemistry Chemical Physics. 15 (48), 20797-20807 (2013).
- Dick, J. E., Hilterbrand, A. T., Boika, A., Upton, J. W., Bard, A. J. Electrochemical detection of a single cytomegalovirus at an ultramicroelectrode and its antibody anchoring. Proceedings of the National Academy of Sciences of the United States of America. 112 (17), 5303-5308 (2015).
- Mirkin, M. V., Sun, T., Yu, Y., Zhou, M. Electrochemistry at one nanoparticle. Accounts of Chemical Research. 49 (10), 2328-2335 (2016).
- Sokolov, S. V., Eloul, S., Kätelhön, E., Batchelor-McAuley, C., Compton, R. G. Electrode-particle impacts: A users guide. Physical Chemistry Chemical Physics. 19 (1), 28-43 (2017).
- Stevenson, K. J., Tschulik, K. A materials driven approach for understanding single entity nano impact electrochemistry. Current Opinion in Electrochemistry. 6 (1), 38-45 (2017).
- Baker, L. A. Perspective and prospectus on single-entity electrochemistry. Journal of the American Chemical Society. 140 (46), 15549-15559 (2018).
- Cheng, W., Compton, R. G. Electrochemical detection of nanoparticles by 'nano-impact' methods. TrAC Trends in Analytical Chemistry. 58, 79-89 (2014).
- Bard, A. J., Fan, F. -. R. F. Electrochemical detection of single molecules. Accounts of Chemical Research. 29 (12), 572-578 (1996).
- Xiao, X., Bard, A. J. Observing single nanoparticle collisions at an ultramicroelectrode by electrocatalytic amplification. Journal of the American Chemical Society. 129 (31), 9610-9612 (2007).
- Anderson, T. J., Zhang, B. Single-nanoparticle electrochemistry through immobilization and collision. Accounts of Chemical Research. 49 (11), 2625-2631 (2016).
- Goines, S., Dick, J. E. Review-Electrochemistry's potential to reach the ultimate sensitivity in measurement science. Journal of the Electrochemical Society. 167 (3), 037505 (2020).
- Kai, T., Zhou, M., Johnson, S., Ahn, H. S., Bard, A. J. Direct observation of C2O4•- and CO2•- by oxidation of oxalate within nanogap of scanning electrochemical microscope. Journal of the American Chemical Society. 140 (47), 16178-16183 (2018).
- Dick, J. E. Electrochemical detection of single cancer and healthy cell collisions on a microelectrode. Chemical Communications. 52 (72), 10906-10909 (2016).
- Sepunaru, L., Sokolov, S. V., Holter, J., Young, N. P., Compton, R. G. Electrochemical red blood cell counting: One at a time. Angewandte Chemie International Edition. 55 (33), 9768-9771 (2016).
- Quinn, B. M., van't Hof, P. G., Lemay, S. G. Time-resolved electrochemical detection of discrete adsorption events. Journal of the American Chemical Society. 126 (27), 8360-8361 (2004).
- Oldham, K. B. Edge effects in semiinfinite diffusion. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 122, 1-17 (1981).
- Fosdick, S. E., Anderson, M. J., Nettleton, E. G., Crooks, R. M. Correlated electrochemical and optical tracking of discrete collision events. Journal of the American Chemical Society. 135 (16), 5994-5997 (2013).
- Chung, J., Hertler, P., Plaxco, K. W., Sepunaru, L. Catalytic interruption mitigates edge effects in the characterization of heterogeneous, insulating nanoparticles. Journal of the American Chemical Society. 143 (45), 18888-18898 (2021).
- Boika, A., Thorgaard, S. N., Bard, A. J. Monitoring the electrophoretic migration and adsorption of single insulating nanoparticles at ultramicroelectrodes. The Journal of Physical Chemistry B. 117 (16), 4371-4380 (2013).
- Kim, B. -. K., Boika, A., Kim, J., Dick, J. E., Bard, A. J. Characterizing emulsions by observation of single droplet collisions-Attoliter electrochemical reactors. Journal of the American Chemical Society. 136 (13), 4849-4852 (2014).
- Dick, J. E., Renault, C., Bard, A. J. Observation of single-protein and DNA macromolecule collisions on ultramicroelectrodes. Journal of the American Chemical Society. 137 (26), 8376-8379 (2015).
- Lee, J. Y., Kim, B. -. K., Kang, M., Park, J. H. Label-free detection of single living bacteria via electrochemical collision event. Scientific Reports. 6 (1), 30022 (2016).
- Bonezzi, J., Boika, A. Deciphering the magnitude of current steps in electrochemical blocking collision experiments and its implications. Electrochimica Acta. 236, 252-259 (2017).
- Ellison, J., Batchelor-McAuley, C., Tschulik, K., Compton, R. G. The use of cylindrical micro-wire electrodes for nano-impact experiments; Facilitating the sub-picomolar detection of single nanoparticles. Sensors and Actuators B: Chemical. 200, 47-52 (2014).
- Denuault, G., Fleischmann, M., Pletcher, D., Tutty, O. R. Development of the theory for the interpretation of steady state limiting currents at a microelectrode: EC' processes: First and second order reactions. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 280 (2), 243-254 (1990).
- Francke, R., Little, R. D. Redox catalysis in organic electrosynthesis: Basic principles and recent developments. Chemical Society Reviews. 43 (8), 2492-2521 (2014).
- Nutting, J. E., Rafiee, M., Stahl, S. S. Tetramethylpiperidine N-Oxyl (TEMPO), phthalimide N-oxyl (PINO), and related N-Oxyl species: Electrochemical properties and their use in electrocatalytic reactions. Chemical Reviews. 118 (9), 4834 (2018).
- Pierre, G., et al. TEMPO-mediated oxidation of polysaccharides: An ongoing story. Carbohydrate Polymers. 165, 71-85 (2017).
- Liaigre, D., Breton, T., Belgsir, E. M. Kinetic and selectivity control of TEMPO electro-mediated oxidation of alcohols. Electrochemistry Communications. 7 (3), 312-316 (2005).
- Rafiee, M., Karimi, B., Alizadeh, S. Mechanistic study of the electrocatalytic oxidation of alcohols by TEMPO and MHPI. ChemElectroChem. 1 (2), 455-462 (2014).
- Deng, Z., Renault, C. Detection of individual insulating entities by electrochemical blocking. Current Opinion in Electrochemistry. 25, 100619 (2021).
- Laborda, E., Molina, A., Batchelor-McAuley, C., Compton, R. G. Individual detection and characterization of non-electrocatalytic, redox-inactive particles in solution by using electrochemistry. ChemElectroChem. 5 (3), 410-417 (2018).
- Elgrishi, N., et al. A practical beginner's guide to cyclic voltammetry. Journal of Chemical Education. 95 (2), 197-206 (2018).
- Cardwell, T. J., Mocak, J., Santos, J. H., Bond, A. M. Preparation of microelectrodes: comparison of polishing procedures by statistical analysis of voltammetric data. Analyst. 121 (3), 357-362 (1996).
- Lämmel, C., Heubner, C., Liebmann, T., Schneider, M. Critical impact of chloride containing reference electrodes on electrochemical measurements. Electroanalysis. 29 (12), 2752-2756 (2017).
- Walker, N. L., Dick, J. E. Leakless, bipolar reference electrodes: Fabrication, performance, and miniaturization. Analytical Chemistry. 93 (29), 10065-10074 (2021).
- Troudt, B. K., Rousseau, C. R., Dong, X. I. N., Anderson, E. L., Bühlmann, P. Recent progress in the development of improved reference electrodes for electrochemistry. Analytical Sciences. 38 (1), 71-83 (2022).
- Stuart, E. J. E., Zhou, Y. -. G., Rees, N. V., Compton, R. G. Particle-impact nanoelectrochemistry: A Fickian model for nanoparticle transport. RSC Advances. 2 (33), 12702-12705 (2012).
- Boika, A., Bard, A. J. Time of first arrival in electrochemical collision experiments as a measure of ultralow concentrations of analytes in solution. Analytical Chemistry. 87 (8), 4341-4346 (2015).
- Robinson, D. A., et al. Collision dynamics during the electrooxidation of individual silver nanoparticles. Journal of the American Chemical Society. 139 (46), 16923-16931 (2017).
- Lemay, S. G., Moazzenzade, T. Single-entity electrochemistry for digital biosensing at ultralow concentrations. Analytical Chemistry. 93 (26), 9023-9031 (2021).
- Vernon-Parry, K. D. Scanning electron microscopy: An introduction. III-Vs Review. 13 (4), 40-44 (2000).
- Abramoff, M. D., Magalhães, P. J., Ram, S. J. Image processing with ImageJ. Biophotonics International. 11 (7), 36-42 (2004).
- Collins, T. J. ImageJ for microscopy. BioTechniques. 43, S25-S30 (2007).
- Bard, A. J., Faulkner, L. R. . Electrochemical Methods: Fundamentals and Applications. , (2001).
- Compton, R. G., Banks, C. E. . Understanding Voltammetry (Third Edition). , (2018).
- Cutress, I. J., Dickinson, E. J. F., Compton, R. G. Analysis of commercial general engineering finite element software in electrochemical simulations. Journal of Electroanalytical Chemistry. 638 (1), 76-83 (2010).
- Dickinson, E. J. F., Ekström, H., Fontes, E. COMSOL Multiphysics®: Finite element software for electrochemical analysis. A mini-review. Electrochemistry Communications. 40, 71-74 (2014).
- Deng, Z., Elattar, R., Maroun, F., Renault, C. In situ measurement of the size distribution and concentration of insulating particles by electrochemical collision on hemispherical ultramicroelectrodes. Analytical Chemistry. 90 (21), 12923-12929 (2018).
- Moazzenzade, T., Walstra, T., Yang, X., Huskens, J., Lemay, S. G. Ring ultramicroelectrodes for current-blockade particle-impact electrochemistry. Analytical Chemistry. 94 (28), 10168-101747 (2022).
- Nekrassova, O., et al. The oxidation of cysteine by aqueous ferricyanide: A kinetic study using boron doped diamond electrode voltammetry. Electroanalysis. 14 (21), 1464-1469 (2002).
- Kuss, S., Compton, R. G. Electrocatalytic detection of ascorbic acid using N,N,N',N'-tetramethyl-para-phenylene-diamine (TMPD) mediated oxidation at unmodified gold electrodes; Reaction mechanism and analytical application. Electrochimica Acta. 242, 19-24 (2017).
- Shayani-Jam, H., Nematollahi, D. Electrochemically mediated oxidation of glutathione and N-acetylcysteine with 4,4′-biphenol. Electrochimica Acta. 56 (25), 9311-9316 (2011).
- Vyskočil, V., Barek, J. Mercury electrodes-Possibilities and limitations in environmental electroanalysis. Critical Reviews in Analytical Chemistry. 39 (3), 173-188 (2009).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon