Method Article
Dimensionamento eletroquímico preciso de partículas eletro-inativas individuais
Neste Artigo
Resumo
Como técnica analítica, a eletroquímica de nanoimpacto, uma abordagem cada vez mais importante para a contagem e caracterização de partículas eletro-inativas em escala nanométrica, sofre de baixa precisão devido às distribuições de corrente heterogêneas que surgem do uso de ultramicroeletrodos. Delinea-se aqui uma abordagem generalizada, denominada "interrupção eletrocatalítica", que aumenta a precisão em tais medições.
Resumo
A eletroquímica de nanoimpacto permite a caracterização in situ resolvida no tempo (por exemplo, tamanho, atividade catalítica) de unidades de nanomateriais individuais, fornecendo um meio de elucidar heterogeneidades que seriam mascaradas em estudos de conjunto. Para implementar esta técnica com partículas inativas redox, uma reação redox em fase de solução é usada para produzir uma corrente de fundo de estado estacionário em um ultramicroeletrodo de disco. Quando uma partícula adsorve no eletrodo, ela produz uma redução gradual na área exposta do eletrodo, o que produz, por sua vez, uma diminuição gradual na corrente proporcional ao tamanho da espécie adsorvente. Historicamente, no entanto, a eletroquímica de nanoimpacto tem sofrido "efeitos de borda", em que a camada de difusão radial formada na circunferência dos ultramicroeletrodos torna o tamanho do passo dependente não apenas do tamanho da partícula, mas também de onde ela pousa no eletrodo. A introdução da geração de corrente eletrocatalítica, no entanto, atenua a heterogeneidade causada pelos efeitos de borda, melhorando a precisão da medição. Nessa abordagem, denominada "interrupção eletrocatalítica", é introduzido um substrato que regenera a sonda redox na camada de difusão. Isso desloca a etapa limitante da velocidade da geração atual da difusão para a constante de taxa de reação homogênea, reduzindo assim a heterogeneidade do fluxo e aumentando a precisão do dimensionamento de partículas em uma ordem de magnitude. O protocolo aqui descrito explica a configuração e coleta de dados empregada em experimentos de nanoimpacto implementando este efeito para melhorar a precisão no dimensionamento de materiais inativos redox.
Introdução
A eletroquímica de nanoimpacto é uma técnica eletroquímica que permite a detecção de partículas individuais in situ resolvidas no tempo em uma amostra 1,2,3,4,5,6,7. As partículas individuais que podem ser caracterizadas por esta abordagem abrangem uma ampla gama de materiais 6,8,9,10,11,12,13 e abrangem dimensões desde átomos individuais até células inteiras 7,8,14,15,16 . Para acomodar a detecção e caracterização de materiais tão pequenos, a técnica utiliza ultramicroeletrodos de disco em escala de mícron e submícron. O impacto de uma nanopartícula eletroativa em tal eletrodo produz uma mudança de corrente facilmente quantificável à medida que a nanopartícula sofre uma reação redox. Para expandir isso para a detecção de materiais ativos eletro-inativos, uma reação eletroquímica de fundo é usada para produzir uma corrente de estado estacionário que é reduzida de forma gradual à medida que a adsorção das nanopartículas altera a área de superfície do eletrodo17. Neste esquema, ultramicroeletrodos são empregados para aumentar a mudança relativa produzida por cada nanoimpacto. A camada de difusão radial que esses microeletrodos produzem, no entanto, reduz a precisão da medida devido aos "efeitos de borda"18. Isso ocorre porque o fluxo da espécie redox para o eletrodo é maior nas bordas do eletrodo do que em seu centro19. Assim, quando uma única nanopartícula pousa na borda da superfície do eletrodo, o evento de corrente resultante é maior do que o observado para uma partícula idêntica pousando no centro do eletrodo19, e esse efeito é mais significativo para ultramicroeletrodos devido à sua pequena relação área-circunferência. Esses efeitos de borda prejudicam significativamente a precisão da eletroquímica de nanoimpactos; Devido à sua presença, as distribuições estimadas de tamanho de partículas produzidas pelo dimensionamento de nanoimpacto são 20 vezes maiores do que aquelas obtidas usando técnicas de microscopia "padrão ouro"20. Essa precisão reduzida prejudica o uso da eletroquímica de nanoimpacto como técnica analítica para avaliar a heterogeneidade de materiais inativos redox na escala nanométrica4,17,19,21,22,23,24,25,26.
Recentemente introduzimos um método (Figura 1) que mitiga os efeitos de borda em abordagens de nanoimpacto20. Neste método, a introdução de um substrato regenera as espécies redox próximas à superfície do ultramicroeletrodo. Isso desloca o passo limitante na geração de corrente da difusão para a taxa de reação química homogênea das espécies redox em solução27,28, reduzindo assim o grau em que o campo de difusão radial contribui para correntes heterogêneas. Especificamente, a oxidação da 2,2,6,6-tetrametilpiperidina 1-oxil (TEMPO) fornece a reação redox de fundo no ultramicroeletrodo29. A adição de maltose a esta regenera a forma reduzida do TEMPO30,31. Essa regeneração é rápida32, comprime a camada de difusão e reduz a heterogeneidade atual associada à aterrissagem espacial20. Como resultado, a abordagem de "interrupção eletrocatalítica" melhora a precisão do dimensionamento de partículas de nanoimpacto em uma ordem de magnitude.
Protocolo
1. Estabelecimento de um sistema de baixo ruído
NOTA: Os experimentos relevantes requerem um potenciostato capaz de alcançar a medição altamente resolvida no tempo de baixas correntes. Para conseguir isso, empregar um potenciostato comercial de grau de pesquisa capaz de uma resolução temporal de 1 μs que pode quantificar correntes no nível femtoampere. Para reduzir ainda mais a interferência eletrônica do ambiente, realize experimentos dentro de duas gaiolas de Faraday de nidificação. Certifique-se de que a configuração é capaz de um desvio quadrático da média da raiz inferior a 100 fA para um experimento de cronoamperometria amostrado a 10 Hz em cloreto de potássio 0,1 M.
- Obter e montar o equipamento, incluindo o potenciostato e as gaiolas de Faraday.
NOTA: As gaiolas de Faraday podem ser obtidas comercialmente ou fabricadas sob medida usando metais condutores (por exemplo, cobre ou alumínio). Gaiolas de Faraday de alumínio fabricadas sob medida foram usadas para o estudo descrito aqui (ver Tabela de Materiais).
2. Preparação experimental
- Use esferas de poliestireno modificadas com carboxilato de 2 μm de diâmetro disponíveis comercialmente (consulte a Tabela de Materiais).
NOTA: Embora esse sistema possa ser generalizado para outras espécies eletro-inativas23,33, é fundamental lembrar que os impactos dependem da migração eletroforética, além do movimento browniano. Assim, aplicar um potencial atrativo para as espécies de interesse, e manter baixas concentrações de sais17. - Prepare as seguintes soluções, que podem ser armazenadas à temperatura ambiente por pelo menos 1 mês.
- Preparar uma solução de carbonato de 50 mM e titular até pH 12,0 usando NaOH 1 M. Monitore o pH semanalmente.
- Preparar uma solução de perclorato de sódio 1 M.
- Prepare as seguintes soluções frescas todos os dias, descartando-as no final do dia.
- Preparar um TEMPO de 10 mM em solução de carbonato de 50 mM, pH 12,0.
- Preparar um estoque de maltose de 500 mM em solução de carbonato de 50 mM, pH 12,0.
- Selecione o eletrodo de trabalho. Para resultados consistentes, selecionar um ultramicroeletrodo (ver Tabela de Materiais) de tal forma que o raio da espécie a ser caracterizada não seja inferior a 10%-15% do raio do eletrodo17,21,23,33,34.
NOTA: Esta razão pode ser minimizada depois de determinar a magnitude das etapas atuais associadas ao impacto para a detecção ideal de uma determinada espécie de interesse. O material do eletrodo selecionado deve catalisar a reação redox de fundo. - Preparar duas células eletroquímicas de 5 mL cada.
- Preparar uma célula de controlo contendo 1 mM de TEMPO e 5 mM de perclorato de sódio (ver Tabela de Materiais) em tampão carbonato a pH 12,0.
- Preparar uma célula de ensaio contendo uma solução de 1 mM TEMPO, 5 mM de perclorato de sódio e 120 mM de maltose em tampão carbonato a pH 12,0.
NOTA: A razão entre o mediador redox e o substrato (aqui, TEMPO para maltose) pode ser variada para explorar os efeitos da taxa de reação20. Este valor fornece informações sobre a reação química homogênea. - Depois de preparar essas células, reserve-as para medições eletroquímicas posteriores.
3. Polimento do eletrodo
- Antes de cada corrida experimental, polir o eletrodo sequencialmente por 2 min cada com uma lama de alumina de 1 μm, 0,3 μm e 0,5 μm (ver Tabela de Materiais) em almofadas de polimento.
- Mova o eletrodo em um padrão "figura 8" para garantir um polimento uniforme35,36. Enxágue com água deionizada e seque com um lenço umedecido de laboratório.
NOTA: Não sonicar os ultramicroeletrodos, pois isso pode danificá-los.
4. Medições eletroquímicas
NOTA: Consulte a Figura 2 para obter os resultados.
- Utilize uma configuração de três eletrodos para as medições eletroquímicas. Para os experimentos aqui descritos, empregar um ultramicroeletrodo de fibra de carbono de 11 μm, um contraeletrodo de fio de platina e um eletrodo de referência de calomelano saturado (SCE) (ver Tabela de Materiais).
NOTA: As janelas de potencial eletroquímico para os experimentos são observadas abaixo; para referência, o TEMPO tem um potencial formal de 0,49 V versus ECS, e a maltose não é eletroativa na janela de potencial usada nesses experimentos. Qualquer vazamento do eletrodo de referência pode afetar a concentração total de sal37, reduzindo o direcionamento eletroforético das partículas para o ultramicroeletrodo e reduzindo a eficiência de contagem17. Se os experimentos produzirem uma frequência de impacto baixa, considere mudar para um eletrodo de referência sem vazamento38,39. - Coloque a célula de controle nas gaiolas de Faraday e conecte os eletrodos aos cabos apropriados. Coletar o primeiro conjunto de medidas eletroquímicas para cada célula. Este consistirá em um experimento de voltametria cíclica e um experimento de cronoamperometria, conforme detalhado abaixo.
- Colete os dados de voltametria cíclica usando uma janela potencial de 0,2 V a 0,8 V versus SCE a taxas de varredura de 10 mV·s−1, 20 mV·s−1, 30 mV·s−1, 40 mV·s−1 e 50 mV·s−1.
- Coletar os dados da cronoamperometria aplicando 0,8 V versus ECS por 10 minutos e registrar a uma taxa de amostragem de 10 Hz.
NOTA: Um período de amostragem de 10 minutos é recomendado para experimentos de cronoamperometria para obter 10-15 impactos individuais em etapas posteriores. Não são esperados impactos nesta conjuntura.
- Em seguida, coloque uma solução diluída de esferas de poliestireno até uma concentração final de 0,66 pM17 em cada uma das células eletroquímicas. Após a adição das esferas de poliestireno, coletar o segundo conjunto de medidas eletroquímicas para cada célula.
OBS: A frequência de impacto será função desta concentração e requer otimização para coletar dados suficientes para análise estatística sem saturar o cronoamperograma com sobreposição de impactos40,41,42,43.- Coletar dados de cronoamperometria aplicando 0,8 V versus SCE por 10 min e registrar a uma taxa de amostragem de 10 Hz.
- Repita as medidas cronoamperométricas até que tenham sido coletados pontos de dados suficientes para análise estatística. Para detectar diferenças entre os métodos de dimensionamento múltiplo com nível de confiança de 95% e poder de 80%, selecione um tamanho de amostra de aproximadamente 200 eventos de impacto individuais.
5. Microscopia eletrônica de varredura (MEV)
OBS: Utilizar a microscopia eletrônica de varredura como técnica "padrão ouro" para confirmar o tamanho das nanopartículas e a heterogeneidade das amostras19,44.
- Preparo da amostra
- Para preparar uma amostra para aquisição de imagens, diluir uma suspensão de esferas de látex carboxila (ver Tabela de Materiais) 1:20 em água. Lançar 10 μL em uma lâmina de vidro, secar sob uma corrente de nitrogênio e revestir a amostra com uma camada condutora de ouro-paládio sob argônio.
- Imagiologia
- Usando uma tensão de feixe acelerador de 5 kV e uma corrente de 0,4 nA, colete imagens conforme apropriado para análise estatística. Use o ImageJ45,46 ou um software de análise de imagem equivalente para determinar os tamanhos das partículas.
6. Análise de dados eletroquímicos
- Registrar os dados eletroquímicos usando o software do potenciostato, e analisar esses resultados usando um script escrito 20 que pode extrair as magnitudes de corrente das mudanças detectadas na corrente de estado estacionário (passos atuais) resultantes de eventos de nanoimpacto20.
NOTA: Este script é incluído como parte das informações suplementares em nosso relatório publicado anteriormente20. - Converta as amplitudes das etapas atuais em raios de contas usando a seguinte equação:
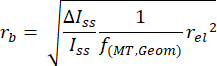
NOTA: Aqui, rb é o raio do talão, relé o raio do eletrodo, Δ Iss/Iss é a razão entre a mudança na corrente produzida pela adsorção de uma partícula e a corrente inicial de estado estacionário observada antes da adsorção dessa partícula, e f(MT,Geom) = 0,067 é um fator de escala empírico que depende de considerações geométricas e de transporte de massa20, 25º. - Plote a frequência de detecção de um determinado raio do cordão versus o raio (Figura 3) para quantificar as métricas de distribuição.
7. Modelagem
NOTA: Se desejado, o mecanismo pelo qual a interrupção eletrocatalítica funciona pode ser validado confirmando a mudança da geração de corrente limitada por difusão para a geração de corrente limitada por taxa de reação. Para descrever e visualizar, use dois programas de simulação numérica diferentes: um software de ajuste de voltamograma, como o DigiSim, para determinar a constante de taxa homogênea, e uma plataforma de modelagem multifísica, como o COMSOL Multiphysics, para visualizar as mudanças locais no perfil de difusão na superfície do ultramicroeletrodo (ver Tabela de Materiais).
- Encaixe de voltammograma
NOTA: Use o software de encaixe de voltamografia para determinar a constante de taxa homogênea (Figura 4).- Recolher voltamogramas cíclicos numa solução contendo 1 mM TEMPO (apenas) e 1 mM TEMPO mais 120 mM de maltose. Para cada condição, colete dados em várias taxas de varredura e use esses dados para ajustes numéricos desses conjuntos de dados experimentais.
- Ajustar os voltamogramas coletados do experimento somente TEMPO usando um mecanismo E, que descreve um processo de reação conduzido unicamente pelo eletrodo47,48. Isso produzirá os parâmetros do eletrodo.
- Usando os parâmetros do eletrodo obtidos da etapa 7.1.1.1, ajustar os voltamogramas resultantes da solução de 1 mM TEMPO mais 120 maltose a um mecanismo EC′47,48, que descreve um processo de eletrodo que é seguido por uma reação química homogênea que regenera o mediador redox. Isso produzirá a constante de taxa homogênea.
- Recolher voltamogramas cíclicos numa solução contendo 1 mM TEMPO (apenas) e 1 mM TEMPO mais 120 mM de maltose. Para cada condição, colete dados em várias taxas de varredura e use esses dados para ajustes numéricos desses conjuntos de dados experimentais.
- Modelagem multifísica
- Utilizar uma plataforma de modelagem multifísica para visualizar as mudanças nos perfis de difusão na superfície do ultramicroeletrodo tanto para os sistemas de controle quanto para os sistemas de interrupção eletrocatalítica 20,49,50,51,52 (Figura 5). Utilizar os parâmetros do eletrodo e a constante de velocidade homogênea obtida a partir do encaixe do voltamograma como condições iniciais. Uma ampla visão geral do fluxo de trabalho, que pode ser adaptado a diferentes softwares, é fornecida abaixo.
- Insira os parâmetros globais. Estes consistem em valores fixos, tais como (mas não limitado a) os valores de concentração, coeficientes de difusão, raio do eletrodo e temperatura.
- Construa o espaço de simulação. Este é um conjunto de geometrias que incluem o eletrodo, a bainha isolante, o espaço de solução circundante representando a região de interesse, e um domínio de elemento infinito representando o entorno do volume.
- Introduza pacotes de física para definir a simulação.
- Associar o espaço do eletrodo a um estudo de eletroanálise. Defina os valores iniciais e a reação do eletrodo de interesse aqui.
- Associe o espaço de solução circundante a um estudo de química. Defina aqui a reação química homogênea que segue a reação do eletrodo.
- Introduza uma malha sobre todo o espaço de simulação. Isso define como a geometria é dividida para resolver o modelo. Para obter resultados de alta qualidade, use uma malha mais fina perto do eletrodo.
- Para observar mudanças como resultado da constante de taxa homogênea, varie o valor desse parâmetro usando um estudo paramétrico para resolver o modelo.
- Para observar as mudanças em função do tempo, varie o valor desse parâmetro usando um estudo dependente do tempo para resolver o modelo.
Resultados
A interrupção eletrocatalítica atenua os efeitos de borda deslocando o mecanismo primário de geração de corrente de limitado por difusão (isto é, limitado pelo transporte de uma sonda redox para o eletrodo) para limitado cineticamente (ou seja, limitado por uma reação rápida em fase de solução)20. Este método é modular, ou seja, permite uma abordagem de mistura e combinação na escolha do material do eletrodo, da sonda redox e do substrato, o que torna a interrupção eletrocatalítica passível de detecção de muitos nano e biomateriais 6,7,8,9,10,11,12,13,14,15,22 . A implementação desta técnica em um eletrodo de fibra de carbono de 5,5 μm de raio produziu uma melhoria de 10 vezes na precisão associada ao dimensionamento eletroquímico de um sistema modelo (esferas de poliestireno) em uma solução contendo TEMPO como sonda redox e maltose como substrato.
Seguindo este protocolo, os conjuntos de dados necessários para validar este mecanismo e sua capacidade de restaurar a precisão analítica ao dimensionar nanopartículas eletro-inativas podem ser obtidos. Primeiro, os dados de voltamograma cíclico coletados na ausência de esferas de poliestireno mostraram um evento redox reversível em experimentos de controle envolvendo apenas TEMPO. A partir daí, a adição de maltose resultou em aumento do pico oxidativo e perda concomitante do pico redutivo à medida que o TEMPO oxidado foi regenerado pela maltose. Em segundo lugar, os cronoamperogramas coletados nessas condições demonstraram que as correntes de estado estacionário em potencial oxidativo eram maiores, consistentes com a amplificação catalítica observada nos resultados de voltametria cíclica. Esta etapa também sugere que a reação química de volume é mantida pela reação do eletrodo; Assim, quaisquer melhorias sobre o método de controle durarão ao longo da duração da medição. No entanto, isso por si só é insuficiente para avaliar quaisquer melhorias na precisão da medição; Para isso, os dados de cronoamperometria devem ser coletados na presença de esferas de poliestireno.
Para avaliar a precisão do dimensionamento, os dados do cronoamperograma foram coletados usando esferas de poliestireno carboxilado de 2 μm. Após sua adição, mudanças graduais na corrente do cronoamperograma foram observadas à medida que partículas individuais impactadas e absorvidas (Figura 2A controle, Figura 2B interrupção eletrocatalítica). Cada mudança gradual na magnitude da corrente de estado estacionário foi convertida em raios de partículas, e os dados foram visualizados como histogramas para comparar a distribuição dessas técnicas eletroquímicas com a de uma técnica padrão-ouro, como a microscopia eletrônica de varredura (Figura 3). Essa comparação permitiu, então, a caracterização das métricas de precisão associadas a cada abordagem de dimensionamento.
A modelagem foi utilizada para apoiar essas observações experimentais. Especificamente, o ajuste dos voltamogramas cíclicos de antes produziu parâmetros que caracterizaram tanto a reação do eletrodo quanto a reação química em fase solução (Figura 4). A partir da solução controle, alguns parâmetros amostrais obtidos foram Efθ = 0,49 V, k 0 =0,02 cm·s-1 e ν = 10 mV·s-1 a T = 25°C. A partir da solução de ensaio, foi possível obter os parâmetros cinéticos que limitavam a geração de corrente; especificamente, à medidaque K eq se aproxima do infinito, kobs = 2.200 M-1·s-1. As simulações numéricas poderiam então utilizar esses valores como condições iniciais para gerar um perfil de concentração da sonda redox (Figura 5). Na ausência de maltose, o perfil de difusão resultante foi radial, levando a fluxo heterogêneo de material; especificamente, mais material difundido para o eletrodo nas bordas. A introdução da maltose comprimiu o perfil de difusão, produzindo, por sua vez, correntes mais homogêneas através da superfície do eletrodo.
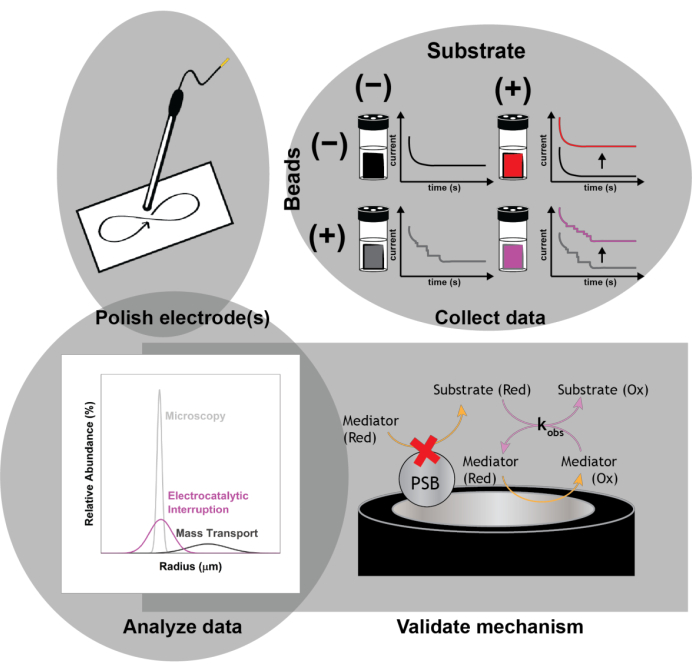
Figura 1: Esquema do protocolo experimental. Polir os eletrodos antes de cada corrida experimental. Coletar um conjunto basal de medidas eletroquímicas (voltametria cíclica e cronoamperometria) na ausência de esferas com e sem implementação de interrupção eletrocatalítica para observar o aumento da corrente com a adição do substrato. Spike nas esferas e coletar um segundo conjunto de medidas eletroquímicas para a determinação do tamanho das nanopartículas impactantes. Validar o mecanismo de ação usando simulações numéricas. Clique aqui para ver uma versão maior desta figura.
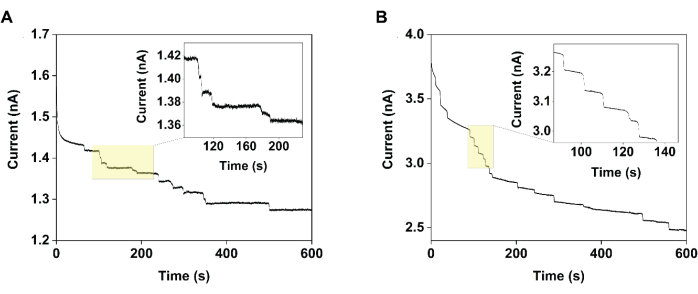
Figura 2: Cronoamperogramas coletados usando um ultramicroeletrodo de fibra de carbono de 11 μm de diâmetro demonstrando a melhoria na precisão de medição obtida com a interrupção eletrocatalítica. Especificamente, ao medir a corrente versus tempo em uma solução de 1 mM TEMPO na (A) ausência (controle) e (B) presença de 120 mM de maltose (interrupção eletrocatalítica), os passos observados neste último caso foram mais homogêneos. Reproduzido com permissão de Chung et al.20. Clique aqui para ver uma versão maior desta figura.
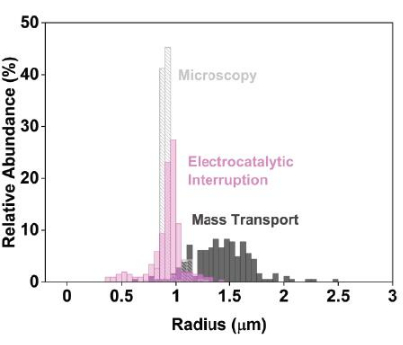
Figura 3: Dados precisos de dimensionamento eletroquímico ao usar interrupção eletrocatalítica em comparação com a abordagem eletroquímica convencional limitada por difusão. Para representar esses dados, preparar histogramas comparando as distribuições de tamanho determinadas por microscopia eletrônica de varredura (cinza claro) e eletroquímica (interrupção eletrocatalítica, rosa; controle, cinza escuro). Estudos convencionais de nanoimpacto, nos quais a corrente é limitada pelo transporte de massa do mediador, produzem distribuições de tamanho estimadas artificialmente amplas (cinza escuro). Em contraste, a implementação da interrupção eletrocatalítica leva a estimativas de tamanho mais estreitas e precisas (rosa). Reproduzido com permissão de Chung et al.20. Clique aqui para ver uma versão maior desta figura.
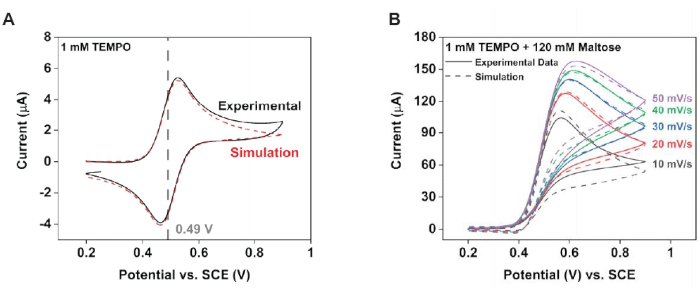
Figura 4: Modelagem da cinética dos eletrodos para caracterização do novo esquema de reação. Usando software de ajuste de voltamograma cíclico, extraia os parâmetros de reação do eletrodo dos dados experimentais. (A) Dados com 1 mM TEMPO. (B) Dados com 1 mM TEMPO mais 120 mM maltose. Reproduzido com permissão de Chung et al.20. Clique aqui para ver uma versão maior desta figura.
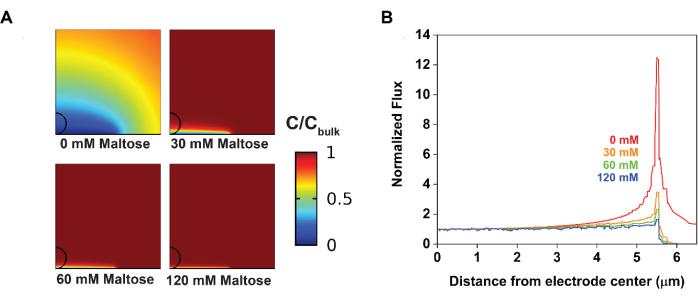
Figura 5: Mudanças no fluxo de material na superfície do eletrodo ao introduzir interrupção eletrocatalítica visualizadas por simulações numéricas . (A) A adição de maltose comprime a camada de difusão de forma dependente da concentração. (B) A adição de maltose deprime o fluxo heterogêneo nas bordas dos eletrodos. Reproduzido com permissão de Chung et al.20. Clique aqui para ver uma versão maior desta figura.
Discussão
A interrupção eletrocatalítica é fácil de implementar e reduz a imprecisão associada à eletroquímica de nanoimpacto em uma ordem de magnitude. Essa precisão aprimorada permite diretamente aos pesquisadores discriminar entre partículas de tamanhos diferentes em uma solução mista20. Também aumenta a capacidade de detectar de forma confiável partículas redox-inativas menores do que o limite historicamente relatado de 15%-20% do raio do eletrodo 17,21,23,34.
Embora a interrupção eletroquímica possa acomodar vários sistemas redox para a detecção de nanopartículas de vários materiais eletro-inativos, a identificação de tais sistemas redox tem permanecido um grande desafio. A principal barreira para a implementação da interrupção eletroquímica é a identificação de uma reação química que seja rápida o suficiente para reduzir significativamente as contribuições de confusão dos efeitos de borda. Especificamente, enquanto alguns exemplos de reações EC′, em que uma reação de eletrodo é seguida por uma reação química que regenera o reagente do eletrodo, são bem caracterizados na literatura 29,32,53,54,55, poucos são suficientemente rápidos para melhorar a precisão da medição. Neste estudo, a partir daquelas reações suficientemente rápidas, optou-se por um sistema TEMPO-maltose, o que obteve, uma constante de velocidade observada de 2.200 M-1·s-1. Isso, em conjunto com simulações multifísicas que demonstram que taxas de reação mais rápidas levam a um fluxo mais homogêneo na borda do eletrodo, suporta a conclusão de que apenas reações químicas rápidas produzem aumentos de corrente de várias vezes em ultramicroeletrodos.
A interrupção catalítica não requer manipulação de dados ou modificações em ultramicroeletrodos disponíveis comercialmente. Para explicar as magnitudes de corrente heterogêneas características dos dados de nanoimpacto, Bonezzi e Boika introduziram um modelo teórico que relaciona a magnitude do passo atual com o tamanho da partícula25. Essa análise, no entanto, depende fortemente da média das magnitudes atuais em função da frequência colisional. Isso não apenas impede a compreensão das propriedades de partículas individuais, mas essa técnica também permanece dependente do fluxo do repórter redox para o eletrodo e não remove o problema dos efeitos de borda, resultando em precisão reduzida. introduziram a primeira abordagem experimental para abordar os efeitos de borda, utilizando um ultramicroeletrodo hemisférico fabricado a partir de mercúrio51. Os eletrodos de gotículas de mercúrio, no entanto, são tóxicos, mecanicamente instáveis e estáveis em apenas uma janela de potencial limitada56. Além disso, fabricar (e manter) microeletrodos perfeitamente hemisféricos usando outros materiais permanece um desafio51,52. Mais recentemente, Moazzenzade e colaboradores propuseram ultramicroeletrodos em anel para caracterização denanoimpactos52. Esta geometria é promissora, mas requer capacidades de nanofabricação. Em contraste, a interrupção catalítica permite experimentos de nanoimpacto com materiais universalmente encontrados em um laboratório de eletroquímica.
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
Este trabalho foi financiado pelo National Institutes of Health (NIH) grant R35GM142920. A pesquisa aqui relatada fez uso de instalações compartilhadas da UCSB MRSEC (NSF DMR 1720256), membro da Materials Research Facilities Network (www.mrfn.org). Agradecemos a Phoebe Hertler por contribuir com o artigo original que este trabalho referencia. Agradecemos à Dra. Claire Chisholm pelo auxílio na aquisição das imagens de microscopia eletrônica de varredura.
Materiais
| Name | Company | Catalog Number | Comments |
| 0.05 µm microalumina polish | Buehler | 4010075 | |
| 0.3 µm microalumina polish | Buehler | 4010077 | |
| 1 µm microalumina polish | Buehler | 4010079 | |
| 20 mL scintillation vials | Fisher Sci | 03-339-26C | |
| Analytical balance | Ohaus | ||
| Apreo C LoVac FEG SEM | Thermo Fisher | ||
| Carbon fiber microelectrode | ALS | 002007 | Working electrode; purchased from CH Instruments |
| Carboxyl Latex Beads, 4% w/v, 2 µm | ThermoFisher Scientific | C37278 | |
| COMSOL Multiphysics | COMSOL Multiphysics | v6.0 | |
| D-(+)-Maltose monohydrate | Sigma Aldrich | M5885 | |
| DigiSim | Bioanalytical Systems, Inc. | v3.03b | Discontinued; comparable software is available commercially through the same vendor |
| EC-Lab | BioLogic | v11.27 | |
| Faraday cages | Custom; analogous equipment can be commercially purchased or fabriated of conductive sheet metals (e.g., copper or aluminum) | ||
| Hummer Sputter Coater | Anatech USA | ||
| OriginPro | OriginLab | v2022b | |
| P1000 micropipette | Fisher Scientific | ||
| P2 micropipette | Fisher Scientific | ||
| P20 micropipette | Fisher Scientific | ||
| P200 micropipette | Fisher Scientific | ||
| Platinum Wire Electrode | CH Instruments | CHI115 | Counter electrode |
| Potassium chloride | Sigma Aldrich | P3911 | |
| PSA-backed MicroCloth | Buehler | 407218 | |
| Saturated Calomel Electrode | CH Instruments | CHI150 | Reference electrode |
| Sodium carbonate | Fisher Chemical | S263 | |
| Sodium hydroxide | Sigma Aldrich | S8045 | |
| Sodium perchlorate | EM Science | SX0692 | |
| SP-300 | BioLogic | ||
| TEMPO | Oakwood Chemical | 013714 | |
| Ultra Low Current module | BioLogic |
Referências
- Heyrovsky, M., Jirkovsky, J. Polarography and voltammetry of ultrasmall colloids: Introduction to a new field. Langmuir. 11 (11), 4288-4292 (1995).
- Kleijn, S. E. F., et al. Landing and catalytic characterization of individual nanoparticles on electrode surfaces. Journal of the American Chemical Society. 134 (45), 18558-18561 (2012).
- Hill, C. M., Clayton, D. A., Pan, S. Combined optical and electrochemical methods for studying electrochemistry at the single molecule and single particle level: Recent progress and perspectives. Physical Chemistry Chemical Physics. 15 (48), 20797-20807 (2013).
- Dick, J. E., Hilterbrand, A. T., Boika, A., Upton, J. W., Bard, A. J. Electrochemical detection of a single cytomegalovirus at an ultramicroelectrode and its antibody anchoring. Proceedings of the National Academy of Sciences of the United States of America. 112 (17), 5303-5308 (2015).
- Mirkin, M. V., Sun, T., Yu, Y., Zhou, M. Electrochemistry at one nanoparticle. Accounts of Chemical Research. 49 (10), 2328-2335 (2016).
- Sokolov, S. V., Eloul, S., Kätelhön, E., Batchelor-McAuley, C., Compton, R. G. Electrode-particle impacts: A users guide. Physical Chemistry Chemical Physics. 19 (1), 28-43 (2017).
- Stevenson, K. J., Tschulik, K. A materials driven approach for understanding single entity nano impact electrochemistry. Current Opinion in Electrochemistry. 6 (1), 38-45 (2017).
- Baker, L. A. Perspective and prospectus on single-entity electrochemistry. Journal of the American Chemical Society. 140 (46), 15549-15559 (2018).
- Cheng, W., Compton, R. G. Electrochemical detection of nanoparticles by 'nano-impact' methods. TrAC Trends in Analytical Chemistry. 58, 79-89 (2014).
- Bard, A. J., Fan, F. -. R. F. Electrochemical detection of single molecules. Accounts of Chemical Research. 29 (12), 572-578 (1996).
- Xiao, X., Bard, A. J. Observing single nanoparticle collisions at an ultramicroelectrode by electrocatalytic amplification. Journal of the American Chemical Society. 129 (31), 9610-9612 (2007).
- Anderson, T. J., Zhang, B. Single-nanoparticle electrochemistry through immobilization and collision. Accounts of Chemical Research. 49 (11), 2625-2631 (2016).
- Goines, S., Dick, J. E. Review-Electrochemistry's potential to reach the ultimate sensitivity in measurement science. Journal of the Electrochemical Society. 167 (3), 037505 (2020).
- Kai, T., Zhou, M., Johnson, S., Ahn, H. S., Bard, A. J. Direct observation of C2O4•- and CO2•- by oxidation of oxalate within nanogap of scanning electrochemical microscope. Journal of the American Chemical Society. 140 (47), 16178-16183 (2018).
- Dick, J. E. Electrochemical detection of single cancer and healthy cell collisions on a microelectrode. Chemical Communications. 52 (72), 10906-10909 (2016).
- Sepunaru, L., Sokolov, S. V., Holter, J., Young, N. P., Compton, R. G. Electrochemical red blood cell counting: One at a time. Angewandte Chemie International Edition. 55 (33), 9768-9771 (2016).
- Quinn, B. M., van't Hof, P. G., Lemay, S. G. Time-resolved electrochemical detection of discrete adsorption events. Journal of the American Chemical Society. 126 (27), 8360-8361 (2004).
- Oldham, K. B. Edge effects in semiinfinite diffusion. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 122, 1-17 (1981).
- Fosdick, S. E., Anderson, M. J., Nettleton, E. G., Crooks, R. M. Correlated electrochemical and optical tracking of discrete collision events. Journal of the American Chemical Society. 135 (16), 5994-5997 (2013).
- Chung, J., Hertler, P., Plaxco, K. W., Sepunaru, L. Catalytic interruption mitigates edge effects in the characterization of heterogeneous, insulating nanoparticles. Journal of the American Chemical Society. 143 (45), 18888-18898 (2021).
- Boika, A., Thorgaard, S. N., Bard, A. J. Monitoring the electrophoretic migration and adsorption of single insulating nanoparticles at ultramicroelectrodes. The Journal of Physical Chemistry B. 117 (16), 4371-4380 (2013).
- Kim, B. -. K., Boika, A., Kim, J., Dick, J. E., Bard, A. J. Characterizing emulsions by observation of single droplet collisions-Attoliter electrochemical reactors. Journal of the American Chemical Society. 136 (13), 4849-4852 (2014).
- Dick, J. E., Renault, C., Bard, A. J. Observation of single-protein and DNA macromolecule collisions on ultramicroelectrodes. Journal of the American Chemical Society. 137 (26), 8376-8379 (2015).
- Lee, J. Y., Kim, B. -. K., Kang, M., Park, J. H. Label-free detection of single living bacteria via electrochemical collision event. Scientific Reports. 6 (1), 30022 (2016).
- Bonezzi, J., Boika, A. Deciphering the magnitude of current steps in electrochemical blocking collision experiments and its implications. Electrochimica Acta. 236, 252-259 (2017).
- Ellison, J., Batchelor-McAuley, C., Tschulik, K., Compton, R. G. The use of cylindrical micro-wire electrodes for nano-impact experiments; Facilitating the sub-picomolar detection of single nanoparticles. Sensors and Actuators B: Chemical. 200, 47-52 (2014).
- Denuault, G., Fleischmann, M., Pletcher, D., Tutty, O. R. Development of the theory for the interpretation of steady state limiting currents at a microelectrode: EC' processes: First and second order reactions. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 280 (2), 243-254 (1990).
- Francke, R., Little, R. D. Redox catalysis in organic electrosynthesis: Basic principles and recent developments. Chemical Society Reviews. 43 (8), 2492-2521 (2014).
- Nutting, J. E., Rafiee, M., Stahl, S. S. Tetramethylpiperidine N-Oxyl (TEMPO), phthalimide N-oxyl (PINO), and related N-Oxyl species: Electrochemical properties and their use in electrocatalytic reactions. Chemical Reviews. 118 (9), 4834 (2018).
- Pierre, G., et al. TEMPO-mediated oxidation of polysaccharides: An ongoing story. Carbohydrate Polymers. 165, 71-85 (2017).
- Liaigre, D., Breton, T., Belgsir, E. M. Kinetic and selectivity control of TEMPO electro-mediated oxidation of alcohols. Electrochemistry Communications. 7 (3), 312-316 (2005).
- Rafiee, M., Karimi, B., Alizadeh, S. Mechanistic study of the electrocatalytic oxidation of alcohols by TEMPO and MHPI. ChemElectroChem. 1 (2), 455-462 (2014).
- Deng, Z., Renault, C. Detection of individual insulating entities by electrochemical blocking. Current Opinion in Electrochemistry. 25, 100619 (2021).
- Laborda, E., Molina, A., Batchelor-McAuley, C., Compton, R. G. Individual detection and characterization of non-electrocatalytic, redox-inactive particles in solution by using electrochemistry. ChemElectroChem. 5 (3), 410-417 (2018).
- Elgrishi, N., et al. A practical beginner's guide to cyclic voltammetry. Journal of Chemical Education. 95 (2), 197-206 (2018).
- Cardwell, T. J., Mocak, J., Santos, J. H., Bond, A. M. Preparation of microelectrodes: comparison of polishing procedures by statistical analysis of voltammetric data. Analyst. 121 (3), 357-362 (1996).
- Lämmel, C., Heubner, C., Liebmann, T., Schneider, M. Critical impact of chloride containing reference electrodes on electrochemical measurements. Electroanalysis. 29 (12), 2752-2756 (2017).
- Walker, N. L., Dick, J. E. Leakless, bipolar reference electrodes: Fabrication, performance, and miniaturization. Analytical Chemistry. 93 (29), 10065-10074 (2021).
- Troudt, B. K., Rousseau, C. R., Dong, X. I. N., Anderson, E. L., Bühlmann, P. Recent progress in the development of improved reference electrodes for electrochemistry. Analytical Sciences. 38 (1), 71-83 (2022).
- Stuart, E. J. E., Zhou, Y. -. G., Rees, N. V., Compton, R. G. Particle-impact nanoelectrochemistry: A Fickian model for nanoparticle transport. RSC Advances. 2 (33), 12702-12705 (2012).
- Boika, A., Bard, A. J. Time of first arrival in electrochemical collision experiments as a measure of ultralow concentrations of analytes in solution. Analytical Chemistry. 87 (8), 4341-4346 (2015).
- Robinson, D. A., et al. Collision dynamics during the electrooxidation of individual silver nanoparticles. Journal of the American Chemical Society. 139 (46), 16923-16931 (2017).
- Lemay, S. G., Moazzenzade, T. Single-entity electrochemistry for digital biosensing at ultralow concentrations. Analytical Chemistry. 93 (26), 9023-9031 (2021).
- Vernon-Parry, K. D. Scanning electron microscopy: An introduction. III-Vs Review. 13 (4), 40-44 (2000).
- Abramoff, M. D., Magalhães, P. J., Ram, S. J. Image processing with ImageJ. Biophotonics International. 11 (7), 36-42 (2004).
- Collins, T. J. ImageJ for microscopy. BioTechniques. 43, S25-S30 (2007).
- Bard, A. J., Faulkner, L. R. . Electrochemical Methods: Fundamentals and Applications. , (2001).
- Compton, R. G., Banks, C. E. . Understanding Voltammetry (Third Edition). , (2018).
- Cutress, I. J., Dickinson, E. J. F., Compton, R. G. Analysis of commercial general engineering finite element software in electrochemical simulations. Journal of Electroanalytical Chemistry. 638 (1), 76-83 (2010).
- Dickinson, E. J. F., Ekström, H., Fontes, E. COMSOL Multiphysics®: Finite element software for electrochemical analysis. A mini-review. Electrochemistry Communications. 40, 71-74 (2014).
- Deng, Z., Elattar, R., Maroun, F., Renault, C. In situ measurement of the size distribution and concentration of insulating particles by electrochemical collision on hemispherical ultramicroelectrodes. Analytical Chemistry. 90 (21), 12923-12929 (2018).
- Moazzenzade, T., Walstra, T., Yang, X., Huskens, J., Lemay, S. G. Ring ultramicroelectrodes for current-blockade particle-impact electrochemistry. Analytical Chemistry. 94 (28), 10168-101747 (2022).
- Nekrassova, O., et al. The oxidation of cysteine by aqueous ferricyanide: A kinetic study using boron doped diamond electrode voltammetry. Electroanalysis. 14 (21), 1464-1469 (2002).
- Kuss, S., Compton, R. G. Electrocatalytic detection of ascorbic acid using N,N,N',N'-tetramethyl-para-phenylene-diamine (TMPD) mediated oxidation at unmodified gold electrodes; Reaction mechanism and analytical application. Electrochimica Acta. 242, 19-24 (2017).
- Shayani-Jam, H., Nematollahi, D. Electrochemically mediated oxidation of glutathione and N-acetylcysteine with 4,4′-biphenol. Electrochimica Acta. 56 (25), 9311-9316 (2011).
- Vyskočil, V., Barek, J. Mercury electrodes-Possibilities and limitations in environmental electroanalysis. Critical Reviews in Analytical Chemistry. 39 (3), 173-188 (2009).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados