A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
מידול ממברנות מציאותי באמצעות תערובות שומנים מורכבות במחקרי סימולציה
In This Article
Summary
גיוון השומנים בממברנה במבנה ובהרכב הוא תורם חשוב לתהליכים תאיים ויכול להיות סמן למחלות. סימולציות של דינמיקה מולקולרית מאפשרות לנו לחקור ממברנות ואת יחסי הגומלין שלהן עם ביומולקולות ברזולוציה אטומית. כאן, אנו מספקים פרוטוקול לבנייה, הפעלה וניתוח של מערכות ממברנות מורכבות.
Abstract
שומנים הם אבני בניין מבניות של קרום התא; מיני שומנים משתנים בין אברוני תאים ובין אורגניזמים. מגוון זה גורם לתכונות מכניות ומבניות שונות בממברנה המשפיעות ישירות על המולקולות והתהליכים המתרחשים בממשק זה. הרכב השומנים הוא דינמי ויכול לשמש לווסת תהליכי איתות תאי. גישות חישוביות משמשות יותר ויותר לחיזוי אינטראקציות בין ביומולקולות ומספקות תובנות מולקולריות לתצפיות ניסיוניות. דינמיקה מולקולרית (MD) היא טכניקה המבוססת על מכניקה סטטיסטית המנבאת את תנועת האטומים בהתבסס על הכוחות הפועלים עליהם. ניתן להשתמש בסימולציות MD כדי לאפיין את האינטראקציה של ביומולקולות. כאן, נציג בקצרה את הטכניקה, נתאר צעדים מעשיים למתחילים המעוניינים לדמות דו-שכבות ליפידים, נדגים את הפרוטוקול עם תוכנה ידידותית למתחילים, ונדון באלטרנטיבות, אתגרים ושיקולים חשובים של התהליך. במיוחד, אנו מדגישים את הרלוונטיות של שימוש בתערובות שומנים מורכבות כדי למדל קרום תא מעניין כדי ללכוד את הסביבות ההידרופוביות והמכניות המתאימות בסימולציה. אנו דנים גם בכמה דוגמאות שבהן הרכב הממברנה ותכונותיה מווסתים את האינטראקציות של דו-שכבות עם ביומולקולות אחרות.
Introduction
ליפידים הם המרכיבים העיקריים של הממברנות, המספקים גבולות לתאים ומאפשרים מידור תוך-תאי 1,2,3. ליפידים הם אמפיפיליים, עם קבוצת ראש קוטבית ושני זנבות חומצות שומן הידרופוביות; אלה מתאספים בעצמם לשכבה דו-שכבתית כדי למזער את המגע של השרשראות ההידרופוביות עם מים 3,4. שילובים שונים של קבוצות ראש הידרופיליות וזנבות הידרופוביים יוצרים סוגים שונים של ליפידים בקרומים ביולוגיים, כגון גליצרופוספוליפידים, ספינגוליפידים וסטרולים (איור 1)1,5,6. גליצרופוספוליפידים הם אבני הבניין העיקריות של קרומי תאים אאוקריוטים המורכבים מגליצרופוספט, חומצות שומן ארוכות שרשרת וקבוצות ראש בעלות משקל מולקולרי נמוך7. המינוח הליפידי מבוסס על הבדלים בקבוצות ראש; דוגמאות כוללות פוספטידיל-כולין (PC), פוספטידיל-אתנולמין (PE), פוספטידיל-סרין (PS), פוספטידיל-גליצרול (PG), פוספטידיל-אינוסיטול (PI), או חומצה פוספטידית לא מעובדת (PA)5,6. באשר לזנבות הידרופוביים, אורך ומידת הרוויה משתנים, יחד עם מבנה עמוד השדרה. הצירופים האפשריים רבים, והתוצאה היא אלפי מיני שומנים בתאי יונקים6. שינויים בהרכב השומנים בממברנה מובילים לתכונות מכניות ומבניות שונות של הממברנה המשפיעות על פעילותם של חלבוני ממברנה אינטגרליים וחלבונים היקפיים 2,6.
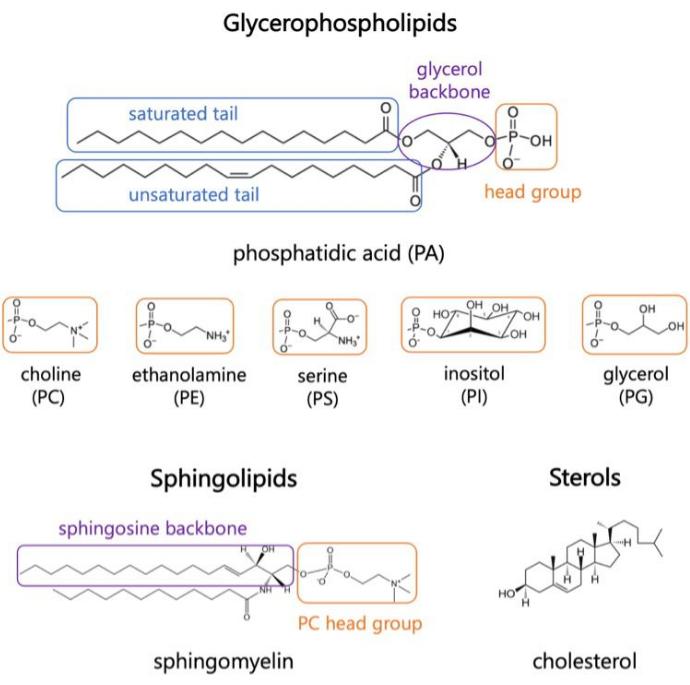
איור 1. מבני שומנים מייצגים. זנבות חומצות שומן מוצגים בקופסאות כחולות, קבוצות ראש שומנים נפוצות בכתום, ודגימות עמוד שדרה בסגול. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
שומנים הם שחקנים פעילים בתהליכים תאיים, הפעלת חלבונים במפל איתות, והומאוסטזיס תאים בריא 8,9. דינמיקה שומנים שהשתנו הם תוצאה של זיהום או יכולים להיות סמנים של פתוגנזה של מחלה 10,11,12,13,14,15. כמחסומים עבור התא, המחקר של שומנים בממברנה ותפקידם בחלחול של מולקולות קטנות רלוונטי עבור מערכות העברת תרופות ומנגנוני שיבוש הממברנה16,17. מגוון כימי ויחסים שונים של מיני שומנים בין אברונים, רקמות ואורגניזמים יוצרים דינמיקה מורכבת של ממברנות2. לכן חשוב לשמור על מאפיינים אלה במחקרי מידול של דו-שכבות שומנים, במיוחד כאשר מטרת המחקר היא לבחון אינטראקציות של ביומולקולות אחרות עם הממברנה. מיני השומנים שיש לקחת בחשבון במודל תלויים באורגניזם ובתא התא המעניין. לדוגמה, שומני PG חשובים להעברת אלקטרונים בבאטריה18 פוטוסינתטית, בעוד שליפידים אינוזיטול זרחניים (PIPs) הם שחקנים מרכזיים בדינמיקה של קרום פלזמה (PM) ומפל איתות בתאי יונקים19,20. בתוך התא, PM, הרשתית האנדופלסמית (ER), Golgi, ואת הממברנות המיטוכונדריאליות מכילים שפע שומנים ייחודי המשפיע על תפקודם. לדוגמה, חדר המיון הוא המרכז לביוגנזה של שומנים ומעביר כולסטרול החוצה אל PM ו Golgi; הוא מכיל מגוון שומנים גבוה עם שפע של PC ו- PE, אך תוכן סטרול נמוך, אשר מקדם נזילות הממברנה21,22,23,24. לעומת זאת, PM משלב מאות ואף אלפי מיני שומנים בהתאם לאורגניזם25, הוא מכיל רמות גבוהות של ספינגולפידים וכולסטרול המקנים לו קשיחות אופיינית בהשוואה לקרומים אחרים בתא24. יש לשקול אסימטריה בעלון עבור ממברנות כמו PM, שיש לו עלון חיצוני עשיר בספינגומיילין, PC וכולסטרול, ועלון פנימי עשיר ב-PE, PI ו-PS החשובים לאיתות מפלים24. לבסוף, גיוון השומנים גם גורם להיווצרותם של מיקרו-דומיינים הנבדלים זה מזה באריזה ובסדר הפנימי, המכונים רפסודות שומנים24,26; אלה מפגינים אסימטריה רוחבית, משערים שהם ממלאים תפקידים חשובים באיתות תאי26, וקשה לחקור אותם בשל אופיים הארעי.
טכניקות ניסיוניות כגון פלואורוסקופיה, ספקטרוסקופיה ומערכות ממברנות מודל כמו שלפוחיות חד-לאומיות ענקיות (GUVs) שימשו לחקר אינטראקציות של ביומולקולות עם ממברנות. עם זאת, קשה לתפוס את האופי המורכב והדינמי של המרכיבים המעורבים בשיטות ניסיוניות בלבד. לדוגמה, קיימות מגבלות על הדמיה של תחומים טרנסממברניים של חלבונים, על מורכבות הממברנות המשמשות במחקרים כאלה, ועל זיהוי מצבי ביניים או ארעיים במהלך תהליך העניין27,28,29. מאז הופעת הסימולציה המולקולרית של חד-שכבות שומנים ודו-שכבות בשנות ה-80 שלהמאה ה-29, ניתן כיום לכמת מערכות ליפידים-חלבונים ואת יחסי הגומלין ביניהן ברמה המולקולרית. סימולציית דינמיקה מולקולרית (MD) היא טכניקה חישובית נפוצה המנבאת את תנועת החלקיקים בהתבסס על הכוחות הבין-מולקולריים שלהם. פוטנציאל אינטראקציה תוספתי מתאר את יחסי הגומלין הקשורים והלא קשורים בין חלקיקים של המערכת30. קבוצת הפרמטרים המשמשת למידול אינטראקציות אלה נקראת שדה כוח סימולציה (FF). פרמטרים אלה מתקבלים מחישובי ab initio, חישובים אמפיריים למחצה ומכניקת הקוונטים, ומותאמים לנתונים משוכפלים מניסויי עקיפה של קרני רנטגן ואלקטרונים, NMR, אינפרא אדום, ראמאן וספקטרוסקופיית נויטרונים, בין שיטות אחרות31.
סימולציות MD יכולות לשמש לחקר מערכות ברמות שונות של רזולוציה32,33,34. מערכות שמטרתן לאפיין אינטראקציות ביומולקולריות ספציפיות, קשרי מימן ופרטים אחרים ברזולוציה גבוהה נחקרות באמצעות סימולציות של אטום (AA). לעומת זאת, סימולציות של גרגירים גסים (CG) מקבצות אטומים לקבוצות פונקציונליות גדולות יותר כדי להפחית את עלות החישוב ולבחון דינמיקה בקנה מידה גדול יותר33. בין שני אלה ממוקמות סימולציות של אטומים מאוחדים (UA), שבהן אטומי מימן משולבים עם האטומים הכבדים שלהם בהתאמה כדי להאיץ את החישוב33,35. סימולציות MD הן כלי רב עוצמה לחקר הדינמיקה של קרומי שומנים והאינטראקציות שלהם עם מולקולות אחרות ויכולות לשמש לספק מנגנונים ברמה המולקולרית לתהליכים בעלי עניין בממשק הממברנה. בנוסף, סימולציות MD יכולות לשמש לצמצום מטרות ניסוי ולחזות תכונות מקרומולקולריות של מערכת נתונה בהתבסס על אינטראקציות מיקרוסקופיות.
בקצרה, בהינתן קבוצה של קואורדינטות התחלתיות, מהירויות ומערכת של תנאים כמו טמפרטורה ולחץ קבועים, המיקומים והמהירויות של כל חלקיק מחושבים באמצעות אינטגרציה מספרית של פוטנציאל האינטראקציה וחוק התנועה של ניוטון. זה חוזר על עצמו באופן איטרטיבי, ובכך יוצר מסלול סימולציה30. חישובים אלה מבוצעים עם מנוע MD; בין מספר חבילות קוד פתוח, GROMACS36 הוא אחד המנועים הנפוצים ביותר וזה שאנו מתארים כאן. הוא כולל גם כלים לניתוח ובניית קואורדינטות ראשוניות של מערכות לסימולציה37. מנועי MD אחרים כוללים NAMD38; CHARMM39, ו- AMBER40, שהמשתמש יכול לבחור לפי שיקול דעתו בהתבסס על ביצועים חישוביים של מערכת נתונה. זה קריטי לדמיין את המסלולים במהלך הסימולציה, כמו גם לניתוח ופרשנות של התוצאות. מגוון כלים זמינים; כאן נדון בדינמיקה מולקולרית חזותית (VMD) המציעה מגוון רחב של תכונות, כולל הדמיה תלת-ממדית (תלת-ממדית) עם שיטות ציור וצביעה נרחבות, הדמיית נתונים נפחית, בנייה, הכנה וניתוח מסלולים של מערכות סימולציה MD, ויצירת סרטי מסלול ללא מגבלות על גודל המערכת, אם הזיכרון זמין41,42,43.
דיוק הדינמיקה החזויה בין רכיבי המערכת מושפע ישירות מה-FF שנבחר להתפשטות המסלול. מאמצי פרמטריזציה אמפיריים של FF ננקטים על ידי קבוצות מחקר מעטות. ה- FF המבוסס והנפוץ ביותר עבור MD כולל CHARMM39, AMBER 40, Martini44, OPLS 45 ו- SIRAH 46. שדה הכוח47 (C36) של CHARMM36 תוסף האטום כולו (C36) נמצא בשימוש נרחב עבור AA MD של מערכות ממברנות מכיוון שהוא משחזר במדויק נתונים מבניים ניסיוניים. הוא פותח במקור על ידי קהילת CHARMM, והוא תואם למספר מנועי MD כמו GROMACS ו- NAMD. למרות שיפורים על פני FFs נפוצים, יש מאמץ מתמשך לשפר את קבוצות הפרמטרים כדי לאפשר תחזיות המשחזרות באופן הדוק תצפיות ניסיוניות, מונע על ידי אינטרסים במערכות מסוימות של מחקר48,49.
אתגר בעת הדמיית קרומי שומנים הוא קביעת אורך מסלול הסימולציה. זה תלוי במידה רבה במדדים שיש לנתח ובתהליך ששואפים לאפיין. בדרך כלל, תערובות שומנים מורכבות דורשות זמן רב יותר כדי להגיע לשיווי משקל, מכיוון שליותר מינים חייב להיות מספיק זמן כדי להתפזר במישור הממברנה ולהגיע לארגון רוחבי יציב. סימולציה אמורה להיות בשיווי משקל כאשר הנכס של הריבית הגיע לרמה ומשתנה סביב ערך קבוע. מקובל להשיג לפחות 100-200 ns של מסלול מאוזן כדי לבצע ניתוח סטטיסטי מתאים על המאפיינים והאינטראקציות של עניין. מקובל להריץ סימולציות של קרום בלבד בין 200-500 ns, בהתאם למורכבות תערובת השומנים ושאלת המחקר. אינטראקציות חלבון-שומנים דורשות בדרך כלל זמני סימולציה ארוכים יותר, בין 500-2000 ns. כמה גישות להאצת הדגימה והדינמיקה הנצפית עם מערכות ממברנות הן: (i) מודל מימטי ממברנה נייד מאוד (HMMM), המחליף פחמני קצה של שומנים בממברנה בממס אורגני כדי להאיץ דגימה50; ו-(ii) חלוקה מחדש של מסת מימן (HMR), המשלבת חלק קטן מהמסות של אטומים כבדים במערכת עם אלה של אטומי מימן כדי לאפשר שימוש בסימולציה גדולה יותר51.
הפרוטוקול הבא דן בגישה ידידותית למתחילים לבנייה, הפעלה וניתוח של מודלים מציאותיים של ממברנות באמצעות AA MD. בהתחשב באופי של סימולציות MD, יש להריץ מסלולים מרובים כדי לקחת בחשבון את יכולת השחזור ואת הניתוח הסטטיסטי הנכון של התוצאות. זה נוהג כיום להריץ לפחות שלושה עותקים משוכפלים לכל מערכת של עניין. לאחר שמיני השומנים נבחרו עבור האורגניזם ותהליך העניין, צעדים בסיסיים לבנייה, הפעלה וניתוח של מסלול סימולציה של מערכת הממברנה בלבד מתוארים ומסוכמים באיור 2.
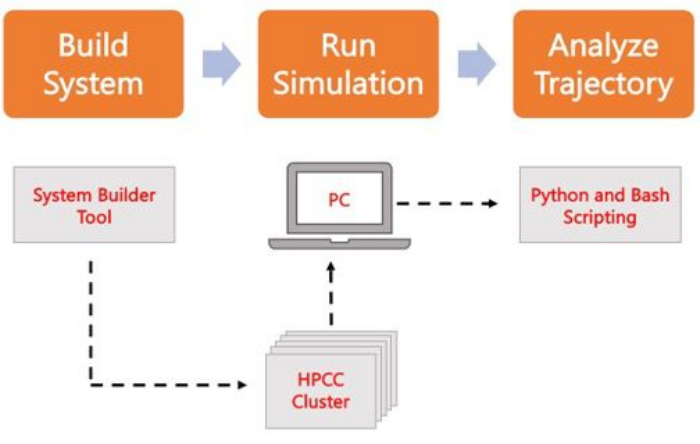
איור 2. סכמטי להפעלת סימולציות MD. קופסאות כתומות תואמות את שלושת השלבים העיקריים המתוארים בפרוטוקול. מתחתיו נמצא תהליך העבודה של תהליך הסימולציה. במהלך הגדרת המערכת, המערכת המכילה את הקואורדינטות הראשוניות של מערכת ממברנות מומסות נבנית עם מחולל קלט מערכת כמו CHARMM-GUI Membrane Builder. לאחר העברת קבצי הקלט לאשכול מחשוב בעל ביצועים גבוהים, מסלול הסימולציה מופץ באמצעות מנוע MD, כגון GROMACS. ניתוח מסלול יכול להיעשות על אשכול המחשב או תחנת עבודה מקומית יחד עם ויזואליזציה. לאחר מכן מתבצע ניתוח, באמצעות חבילות עם קוד ניתוח מובנה כגון GROMACS ו- VMD, או באמצעות סקריפטים של Bash או ספריות Python שונות. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
Access restricted. Please log in or start a trial to view this content.
Protocol
1. בניית קואורדינטות המערכת
- נווט אל CHARMM-GUI.org (C-GUI) באמצעות דפדפן אינטרנט. בתפריט העליון, נווט אל מחולל הקלט ולאחר מכן בחר בונה ממברנות מהאפשרויות האנכיות בצד שמאל של המסך.
- לבניית שכבה דו-שכבתית, בחרו ' בונה דו-שכבתי'.
הערה: משתמשים בפעם הראשונה חייבים להפעיל את החשבון החינמי שלהם לפני בניית קבוצת הקואורדינטות הראשונה שלהם. - בחר מערכת ממברנה בלבד. שמור את מזהה העבודה שנוצר כדי לאחזר את המערכת והמשך מהמקום שבו הפסקת במהלך התהליך במידת הצורך.
- הצג את המערכות באופן חזותי במהלך כל שלב בתהליך הבנייה על ידי לחיצה על הצג מבנה בתיבה הממוקמת בראש הדף, או על ידי הורדת קובץ PDB שנוצר. שימו לב לרכיבים חסרים, טעויות במיני השומנים שנבחרו או בגודל התיקון.
- בחר את רכיבי המערכת.
- בחרו באפשרות ' שומנים הטרוגניים' , גם אם אתם בונים שכבה דו-שכבתית חד-רכיבית; ולאחר מכן בחר/י סוג תיבה מלבנית .
- בחר 45 מולקולות מים לכל שומנים עבור אפשרות הידרציה; זה מספיק כדי להבטיח bilayer hydrated מלא.
- הגדר את אורך XY כך שיתבסס על מספר רכיבי השומנים. לאחר מכן, בחר את מספר הליפידים שייכללו עבור כל מין שומנים שנקבע לפני הדגם. עבור מקרה המבחן שנדון בסעיף הבא, נבנה מודל ממברנה עם 600 שומנים המופצים באופן סימטרי בשני עלונים. כדי למדל את ER של תאים אאוקריוטים תערובת של 336 DOPC, 132 DPPE, 60 CHOL, 72 שומנים POPI שימש עבור מודל PI; ו-330 DOPC, 126 DPPE, 54 CHOL, 66 POPI ו-24 DOPS ליפידים עבור דגם PI-PS.
הערה: C-GUI מספק ספרייה של מבני שומנים לבחירה; לחץ על התמונות לצד שם המין עבור המבנה הכימי שלו. - הקלד את מספר המולקולות הרצוי בעלון העליון והתחתון בשתי התיבות שליד שם השומנים. עבור מקרה הבוחן, הרכב קרום סימטרי רצוי - ודא שאין שגיאות על מספר ללא תחרות של שומנים בעלון העליון ואת העלון התחתון. אם רוצים אסימטריה, יש לוודא שהמספר הכולל של השומנים בכל עלון נכון. לפרטים על בניית דו-שכבות אסימטריות, עיין בעבודה של Park et al.52,53.
- עבור לראש רשימת מיני השומנים ולחץ על הצג את הלחצן נתוני מערכת. להרכיב רכיבים ולהשלים את המערכת.
- בחר באפשרות לכלול יונים מנטרלים באמצעות אלגוריתם מבוסס מרחק להתכנסות מהירהיותר 54.
- השאר את ריכוז ברירת המחדל של KCl על 0.15 mM. זהו ריכוז מלח טיפוסי כדי להפוך את קופסת הסימולציה לנייטרלית עבור דו-שכבות ממברנה.
הערה: אם ברצונך להשתמש בריכוז אחר, הקפד ללחוץ על הלחצן חשב הרכב ממס לאחר עריכתו.
- בחר את תנאי הסימולציה ואת הגדרותיה.
- בחר CHARMM36m כאפשרות FF; הוא משמש בדרך כלל להדמיות שומנים וחלבונים, אך המשתמש יכול לבחור אפשרויות אחרות שנדונו במבוא.
- בחר GROMACS כמנוע MD כדי להשיג קבצי קלט לדוגמה בתבנית המתאימה.
הערה: GROMACS מומלץ למשתמשים חדשים מכיוון שיש לו משאבים מקוונים מרובים, ערכות לימוד ופורומים לתמיכה. המשתמש יכול לבחור מתוך מספר מנועי MD כדי לחקור אפשרויות במונחים של ביצועי סימולציה ותחביר קוד. - בחר את אנסמבל Constant Particle-Pressure-Temperature (NPT), ללא ספק ההרכב הדינמי הנפוץ ביותר בסימולציה של דו-שכבות ליפידים.
- הגדר את הטמפרטורה והלחץ בקלווין ובברים כ- 303 K ו- 1 בר, בהתאמה. זה אופייני להגדיר את הטמפרטורה בין 298 K ו 310 K לחקר תהליכים ביולוגיים כדי להבטיח דו שכבה במצב הפרעה נוזלית.
הערה: הטמפרטורה תלויה בתנאי התהליך שיש לדמות וניתן לשנותה לפי הצורך. בהתאם למיני השומנים במודל, הגדר את הטמפרטורה להיות מעל טמפרטורת המעבר של רכיבי שומנים טהורים לפני הפעלת הסימולציה.
- הורד את הקבצים המתקבלים והעבר לאשכול המחשבים.
- דמיינו את המערכת הסופית בתוכנה לבחירתכם, כגון VMD או PyMol, ובדקו אם יש התקנה נכונה.
הערה: טוב לבדוק, למשל, שיש מספיק מים סביב הממברנה כך ששומנים אינם מתקשרים עם אטומי תמונה במהלך הסימולציה, והתקנה נכונה של עלון (דו-שכבתי ללא רווח או מים ביניהם).
- דמיינו את המערכת הסופית בתוכנה לבחירתכם, כגון VMD או PyMol, ובדקו אם יש התקנה נכונה.
2. הרצת סימולציות MD
- העלה ובטל את דחיסת הקבצים מ- C-GUI באשכול המחשוב שלך. נווט אל ספריית Gromacs . צור סקריפט לשליחת הרפיה.
- פעל בהתאם להנחיות של האשכול עבור התבנית של קובץ Script לשליחה.
- העתק את הפקודות המפורטות עד מעל להערת # Production בקובץ README לסקריפט המסירה.
הערה: ברירת מחדל זו מ- C-GUI היא לולאה המפעילה הרפיה בת 6 שלבים של המערכת. אם רוצים פרוטוקול שונה ומבוסס היטב, ערוך אותו כדי לקרוא את הקואורדינטות שזה עתה נבנו והורדו מ- C-GUI.
- העתק את הפקודות המפורטות עד מעל להערת # Production בקובץ README לסקריפט המסירה.
- הגש את סקריפט ההרפיה ואשר שכל קבצי הפלט הורדו עבור כל השלבים לפני המעבר להפעלת הייצור. בסיום, בדוק את קבצי הפלט הבאים מ- GROMACS, שנוצרו במהלך ריצת 6 השלבים: *.log, *.tpr, *.gro, *.edr, *.trr / *.xtc
- צור קובץ Script להפעלת ייצור.
- השתמש באחת מהפקודות gmx grompp ו- gmx mdrun מכל אחד משלבי ההרפיה כתבנית.
- לפני השימוש בסקריפט, הקפד ליצור קובץ *.mdp הכולל אפשרויות הדמיה דומות לקובץ step7_production.mdp שסופק.
הערה: אפשרויות ברירת המחדל שסופקו הן סטנדרטיות להדמיות ממברנה; ditances מפורטים בננומטר והזמן ניתן ב- picoseconds או במספר צעדים (picoseconds / integration time step). עדכן את nsteps כדי לרוץ עד אורך הסימולציה הרצוי (זה שווה dt * nsteps) ו- nst[x,v,f]out כדי לעדכן את תדירות החיסכון בנתונים במספר שלבי האינטגרציה. עבור ניתוח מקרה, הגדר את nsteps ל- 250,000,000 עבור אורך סימולציה של 500ns (זמן סימולציה / שלב אינטגרציה = 500,000 ps / 0.002ps), ו- nst[x,v,f] החוצה ל- 50,000 כדי לשמור נתונים כל 100 ps
- לפני הפעלת הסימולציה בפועל, הפעל מחקרי ביצועים כדי לקבוע את השימוש הטוב ביותר במשאבים.
- הפעל את המערכת עבור 1-2 ns באמצעות מספר שונה של צמתי מחשוב.
הערה: מקרה המבחן של ER הוגש באשכול55 של מרכז UB למחקר חישובי חישובי (CCR) עבור 2 ns, שם הביצועים נבדקו עבור 1-10 צמתים. - השווה את הביצועים ב- ns/day עבור כל הגדרה כדי לקבוע את המשאבים האופטימליים עבור הריצה. מקובל לבחור את מספר הצמתים שמביאים לביצועים מרביים של 75%-80%.
- הפעל את המערכת עבור 1-2 ns באמצעות מספר שונה של צמתי מחשוב.
- הפעל את ריצת הייצור.
- הפעל כל מערכת בטריפליקטים כדי להבטיח יכולת שחזור ולבצע ניתוח סטטיסטי על הנתונים.
- הרחב את המסלול בהתבסס על אמות המידה אם זמן התור המותר להגשה באשכול המחשוב אוזל. השתמש בפקודות gmx convert-tpr ולאחר מכן gmx mdrun כדי להמשיך באיסוף מסלולים.
הערה: האפשרויות מתוארות בתיעוד המקוון של GROMACS (https://manual.gromacs.org/). - עבור מערכת הממברנה בלבד, יש לבחון אם המערכת הגיעה לשיווי משקל על ידי חישוב השטח לליפיד לאורך זמן. אם לא, האריכו את מסלול הסימולציה.
3. ניתוח המסלול
- דמיינו את המערכת לפני ביצוע ניתוח כדי לקבוע מולקולות מעניינות וחלק מהמסלול המיועד לאפיון.
- דחיסת קובצי מסלול גולמיים ( *.trr) על-ידי שינוי תבנית הקובץ ל- *.xtc ו/או דילוג על מסגרות כדי להקטין את גודל הקובץ ולהקל על העברה יעילה יותר לתחנה המקומית לצורך תצוגה חזותית וניתוח.
הערה: עבור מערכות ממברנות גדולות, ניתן לבחור להסיר מים מהמסלול כדי להקטין עוד יותר את גודל הקובץ. ניתן לעשות זאת עם קבצי אינדקס ב- GROMACS, סקריפטים של TCL ב- VMD, או ספריות Python כגון MDAnalysis ו- MDTraj. - בצע ניתוחים נבחרים במהלך החלק השווה של המסלול, כפי שנקבע מסדרת הזמן של השטח לשומנים.
הערה: עיין בדיון לקבלת פרטים נוספים על ניתוחי ממברנות טיפוסיים וכיצד להפעיל אותם.
Access restricted. Please log in or start a trial to view this content.
תוצאות
כדי להמחיש את השימוש בפרוטוקול ואת התוצאות שניתן להשיג, נדון מחקר השוואה עבור מודלים ממברניים עבור הרשתית האנדופלסמית (ER). שני המודלים במחקר זה היו (i) מודל PI, המכיל את ארבעת מיני השומנים המובילים שנמצאו בחדר המיון, ו-(ii) מודל PI-PS, שהוסיף את מיני השומנים האניונים פוספטידיל-סרין (PS). מודלים אלה ש...
Access restricted. Please log in or start a trial to view this content.
Discussion
טכניקות ניסיוניות יכולות לדמיין ביומולקולות ברזולוציה גבוהה באמצעות מיקרוסקופ קריו-אלקטרונים (cryo-EM)58, טכניקות פלואורסצנטיות ומיקרוסקופ כוח אטומי (AFM)59. עם זאת, מאתגר ללכוד את יחסי הגומלין והדינמיקה של אינטראקציות מולקולריות העומדות בבסיס מסלולים ביולוגיים, פתו?...
Access restricted. Please log in or start a trial to view this content.
Disclosures
למחברים אין אינטרסים מתחרים לחשוף.
Acknowledgements
המחברים מודים לג'ינהוי לי ולריקרדו רמירז על מסלולי הסימולציה והדיונים שלהם במהלך כתיבת כתב היד הזה. O.C. נתמך על ידי האוניברסיטה במלגת באפלו הנשיאותית והיוזמה של המכון הלאומי לבריאות למקסום מענק הכשרה לפיתוח סטודנטים 1T32GM144920-01 הוענק למרגריטה ל. דובוקוביץ '(PI).
Access restricted. Please log in or start a trial to view this content.
Materials
| Name | Company | Catalog Number | Comments |
| Anaconda3 | Anaconda Inc (Python & related libraries) | N/A | |
| CHARMM-GUI.org | Im lab, Lehigh University | N/A | |
| GROMACS | GROMACS development team | N/A | |
| Linux HPC Cluster | UB CCR | N/A | |
| MATLAB | MathWorks | N/A | |
| VMD | Theoretical and Computational Biophysics Group | N/A |
References
- Vanni, S., Riccardi, L., Palermo, G., De Vivo, M. Structure and Dynamics of the Acyl Chains in the Membrane Trafficking and Enzymatic Processing of Lipids. Accounts of Chemical Research. 52 (11), 3087-3096 (2019).
- Harayama, T., Riezman, H. Understanding the diversity of membrane lipid composition. Nature Reviews Molecular Cell Biology. 19 (5), 281-296 (2018).
- Tanaka, M. Comprehensive Biophysics. Edward, H. . E. gelman , Elsevier. 261-272 (2012).
- Bruce Alberts, A. J., Julian Lewis,, Martin Raff,, Keith Roberts,, Peter Walter, Molecular Biology of the Cell. , Garland Science. (2002).
- Watson, H. Biological membranes. Essays in Biochemistry. 59, 43-69 (2015).
- Coskun, Ü, Simons, K. Cell Membranes: The Lipid Perspective. Structure. 19 (11), 1543-1548 (2011).
- Biobased Surfactants (Second Edition) eds. Douglas G, H. ayes, Daniel, K. Y., Solaiman,, Richard, D. , AOCS Press. 515-529 (2019).
- González-Rubio, P., Gautier, R., Etchebest, C., Fuchs, P. F. J. Amphipathic-Lipid-Packing-Sensor interactions with lipids assessed by atomistic molecular dynamics. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1808, 2119-2127 (2011).
- Halbleib, K., et al. Activation of the Unfolded Protein Response by Lipid Bilayer Stress. Molecular Cell. 67, 673-684 (2017).
- Andreasen, M., Lorenzen, N., Otzen, D. Interactions between misfolded protein oligomers and membranes: A central topic in neurodegenerative diseases. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1848 (9), 1897-1907 (2015).
- Calianese, D. C., Birge, R. B. Biology of phosphatidylserine (PS): basic physiology and implications in immunology, infectious disease, and cancer. Cell Commununication and Signaling. 18 (1), 41(2020).
- Nieto-Garai, J. A., Contreras, F. X., Arboleya, A., Lorizate, M. Role of Protein-Lipid Interactions in Viral Entry. Advanced Biology. 6, 2101264(2022).
- Mazzon, M., Mercer, J. Lipid interactions during virus entry and infection. Cell Microbiology. 16, 1493-1502 (2014).
- Colombelli, C., Aoun, M., Tiranti, V. Defective lipid metabolism in neurodegeneration with brain iron accumulation (NBIA) syndromes: not only a matter of iron. Journal of Inherited Metabolic Disease. 38 (1), 123-136 (2015).
- Saini-Chohan, H. K., Mitchell, R. W., Vaz, F. M., Zelinski, T., Hatch, G. M. Delineating the role of alterations in lipid metabolism to the pathogenesis of inherited skeletal and cardiac muscle disorders: Thematic Review Series: Genetics of Human Lipid Diseases. Journal of Lipid Research. 53 (1), 4-27 (2012).
- Martinotti, C., Ruiz-Perez, L., Deplazes, E., Mancera, R. L. Molecular Dynamics Simulation of Small Molecules Interacting with Biological Membranes. ChemPhysChem. 21 (14), 1486-1514 (2020).
- Li, J., Kalyanram, P., Rozati, S., Monje-Galvan, V., Gupta, A. Interaction of Cyanine-D112 with Binary Lipid Mixtures: Molecular Dynamics Simulation and Differential Scanning Calorimetry Study. ACS Omega. 7 (11), 9765-9774 (2022).
- Nagy, L., et al. Protein/Lipid Interaction in the Bacterial Photosynthetic Reaction Center: Phosphatidylcholine and Phosphatidylglycerol Modify the Free Energy Levels of the Quinones. Biochemistry. 43 (40), 12913-12923 (2004).
- Ramirez, R. X., Campbell, O., Pradhan, A. J., Atilla-Gokcumen, G. E., Monje-Galvan, V. Modeling the molecular fingerprint of protein-lipid interactions of MLKL on complex bilayers. Frontiers in Chemistry. 10, (2023).
- Dondelinger, Y., et al. MLKL Compromises Plasma Membrane Integrity by Binding to Phosphatidylinositol Phosphates. Cell Reports. 7 (4), 971-981 (2014).
- van Meer, G., Voelker, D. R., Feigenson, G. W. Membrane lipids: where they are and how they behave. Nature Reviews Molecular Cell Biology. 9 (2), 112-124 (2008).
- van Meer, G., de Kroon, A. I. P. M. Lipid map of the mammalian cell. Journal of Cell Science. 124 (1), 5(2011).
- Lee, H. R., Lee, G. Y., You, D. G., Kim, H. K., Young, D. Y. Hepatitis C virus p7 induces membrane permeabilization by interacting with phosphatidylserine. International Journal of Molecular Sciences. 21 (3), 897(2020).
- Casares, D., Escribá, P. V., Rosselló, C. A. Membrane Lipid Composition: Effect on Membrane and Organelle Structure, Function and Compartmentalization and Therapeutic Avenues. International Journal of Molecular Sciences. 20 (9), 2167(2019).
- Marrink, S. J., et al. Computational Modeling of Realistic Cell Membranes. Chemical Reviews. 119 (9), 6184-6226 (2019).
- Janmey, P. A., Kinnunen, P. K. J. Biophysical properties of lipids and dynamic membranes. Trends in Cell Biology. 16 (10), 538-546 (2006).
- Brémaud, E., Favard, C., Muriaux, D. Deciphering the Assembly of Enveloped Viruses Using Model Lipid Membranes. Membranes. 12, 441(2022).
- Campbell, O., Monje-Galvan, V. Protein-driven membrane remodeling: Molecular perspectives from Flaviviridae infections. Biophysical Journal. 122 (11), 1890-1899 (2022).
- Loschwitz, J., Olubiyi, O. O., Hub, J. S., Strodel, B., Poojari, C. S. Computer simulations of protein-membrane systems. Progress in molecular biology and translational science. 170, 273-403 (2020).
- Shell, M. S. Thermodynamics and Statistical Mechanics: An Integrated ApproachCambridge Series in Chemical Engineering. Scott Shell, M. , Cambridge University Press. 21-49 (2015).
- Yang, J., et al. Molecular Dynamic Simulation of Ni-Al Alloy-H2O Reactions Using the ReaxFF Reactive Force Field. ACS Omega. 8 (11), 9807-9814 (2023).
- Ingólfsson, H. I., Arnarez, C., Periole, X., Marrink, S. J. Computational 'microscopy' of cellular membranes. Journal of Cell Science. 129 (2), 257-268 (2016).
- Klauda, J. B. Perspective: Computational modeling of accurate cellular membranes with molecular resolution. The Journal of Chemical Physics. 149 (22), 220901(2018).
- Chavent, M., Duncan, A. L., Sansom, M. S. P. Molecular dynamics simulations of membrane proteins and their interactions: from nanoscale to mesoscale. Current Opinion in Structural Biology. 40, 8-16 (2016).
- Khakbaz, P., Monje-Galvan, V., Zhuang, X., Klauda, J. B. Biogenesis of Fatty Acids, Lipids and Membranes. Otto Geiger, , Springer International Publishing. 1-19 (2017).
- Abraham, M. J., et al. GROMACS: High performance molecular simulations through multi-level parallelism from laptops to supercomputers. SoftwareX. 1, 19-25 (2015).
- Lemkul, J. A. From Proteins to Perturbed Hamiltonians: A Suite of Tutorials for the GROMACS-2018 Molecular Simulation Package. Living Journal of Computational Molecular Science. 1 (1), 5068(2018).
- Phillips, J. C., et al. Scalable molecular dynamics on CPU and GPU architectures with NAMD. The Journal of Chemical Physics. 153 (4), 044130(2020).
- Klauda, J. B., et al. Update of the CHARMM All-Atom Additive Force Field for Lipids: Validation on Six Lipid Types. The Journal of Physical Chemistry B. 114 (23), 7830-7843 (2010).
- Wang, J., Wolf, R. M., Caldwell, J. W., Kollman, P. A., Case, D. A. Development and testing of a general amber force field. Journal of Computational Chemistry. 25 (9), 1157-1174 (2004).
- John Stone, A. A., et al. Using VMD. , http://csbmb.beckman.illinois.edu/BIOP586C/vmd-tutorial-2011.pdf (2011).
- Humphrey, W., Dalke, A., Schulten, K. VMD: Visual molecular dynamics. Journal of Molecular Graphics. 14 (1), 33-38 (1996).
- Hsin, J., Arkhipov, A., Yin, Y., Stone, J. E., Schulten, K. Using VMD: An Introductory Tutorial. Current Protocols in Bioinformatics. 24 (1), 5.7.1-5.7.48 (2008).
- Souza, P. C. T., et al. Martini 3: a general purpose force field for coarse-grained molecular dynamics. Nature Methods. 18 (4), 382-388 (2021).
- Jorgensen, W. L., Maxwell, D. S., Tirado-Rives, J. Development and Testing of the OPLS All-Atom Force Field on Conformational Energetics and Properties of Organic Liquids. Journal of the American Chemical Society. 118 (45), 11225-11236 (1996).
- Machado, M. R., et al. The SIRAH 2.0 Force Field: Altius, Fortius, Citius. Journal of Chemical Theory and Computation. 15 (4), 2719-2733 (2019).
- Huang, J., et al. CHARMM36m: an improved force field for folded and intrinsically disordered proteins. Nature Methods. 14 (1), 71-73 (2017).
- Mu, J., Liu, H., Zhang, J., Luo, R., Chen, H. F. Recent Force Field Strategies for Intrinsically Disordered Proteins. Journal of Chemical Information and Modeling. 61 (3), 1037-1047 (2021).
- Inakollu, V. S. S., Geerke, D. P., Rowley, C. N., Yu, H. Polarisable force fields: what do they add in biomolecular simulations. Current Opinion in Structural Biology. 61, 182-190 (2020).
- Ohkubo, Y. Z., et al. Accelerating Membrane Insertion of Peripheral Proteins with a Novel Membrane Mimetic Model. Biophysical Journal. 102 (9), 2130-2139 (2012).
- Hopkins, C. W., Le Grand, S., Walker, R. C., Roitberg, A. E. Long-Time-Step Molecular Dynamics through Hydrogen Mass Repartitioning. Journal of Chemical Theory and Computation. 11 (4), 1864-1874 (2015).
- Park, S., Beaven, A. H., Klauda, J. B., Im, W. How Tolerant are Membrane Simulations with Mismatch in Area per Lipid between Leaflets. Journal of Chemical Theory and Computation. 11 (7), 3466-3477 (2015).
- Park, S., Im, W., Pastor, R. W. Developing initial conditions for simulations of asymmetric membranes: a practical recommendation. Biophysical Journal. 120 (22), 5041-5059 (2021).
- Wu, E. L., et al. CHARMM-GUI Membrane Builder toward realistic biological membrane simulations. Journal of Computational Chemistry. 35 (27), 1997-2004 (2014).
- Center for Computational Research, U.a.B.. CCR Facility Description. , https://ubir.buffalo.edu/xmlui/handle/10477/79221 (2019).
- Piggot, T. J., Allison, J. R., Sessions, R. B., Essex, J. W. On the Calculation of Acyl Chain Order Parameters from Lipid Simulations. Journal of Chemical Theory and Computation. 13 (11), 5683-5696 (2017).
- Li, J., Monje-Galvan, V. Effect of Glycone Diversity on the Interaction of Triterpenoid Saponins and Lipid Bilayers. ACS Applied Bio Materials. , (2023).
- Renaud, J. P., et al. Cryo-EM in drug discovery: achievements, limitations and prospects. Nature Reviews Drug Discovery. 17 (7), 471-492 (2018).
- Ando, T., Uchihashi, T., Kodera, N. High-Speed AFM and Applications to Biomolecular Systems. Annual Review of Biophysics. 42 (1), 393-414 (2013).
- Martínez, L., Andrade, R., Birgin, E. G., Martínez, J. M. PACKMOL: A package for building initial configurations for molecular dynamics simulations. Journal of Computational Chemistry. 30 (13), 2157-2164 (2009).
- Jewett, A. I., et al. Moltemplate: A Tool for Coarse-Grained Modeling of Complex Biological Matter and Soft Condensed Matter Physics. Journal of Molecular Biology. 433 (11), 166841(2021).
- Jo, S., Kim, T., Iyer, V. G., Im, W. CHARMM-GUI: A web-based graphical user interface for CHARMM. Journal of Computational Chemistry. 29 (11), 1859-1865 (2008).
- Polêto, M. D., Lemkul, J. A. Integration of experimental data and use of automated fitting methods in developing protein force fields. Communications Chemistry. 5 (1), 38(2022).
- Hynninen, A. P., Crowley, M. F. New faster CHARMM molecular dynamics engine. Journal of Computational Chemistry. 35 (5), 406-413 (2014).
- Kim, S. Issues on the Choice of a Proper Time Step in Molecular Dynamics. Physics Procedia. 53, 60-62 (2014).
- Grubmüller, H., Heller, H., Windemuth, A., Schulten, K. Generalized Verlet Algorithm for Efficient Molecular Dynamics Simulations with Long-range Interactions. Molecular Simulation. 6 (1-3), 121-142 (1991).
- Darden, T., York, D., Pedersen, L. Particle mesh Ewald: An N·log(N) method for Ewald sums in large systems. Journal of Chemical Physics. 98 (12), 10089-10092 (1993).
- Hepatitis C. , https://www.who.int/news-room/fact-sheets/detail/hepatitis-c (2021).
- Braun, E., et al. Best Practices for Foundations in Molecular Simulations [Article v1.0]. Living Journal of Computational Molecular Science. 1 (1), 5957(2018).
- Moradi, S., Nowroozi, A., Shahlaei, M. Shedding light on the structural properties of lipid bilayers using molecular dynamics simulation: a review study. RSC Advances. 9 (8), 4644-4658 (2019).
- Monje-Galvan, V., Klauda, J. B. Modeling Yeast Organelle Membranes and How Lipid Diversity Influences Bilayer Properties. Biochemistry. 54 (45), 6852-6861 (2015).
- Michaud-Agrawal, N., Denning, E. J., Woolf, T. B., Beckstein, O. MDAnalysis: A toolkit for the analysis of molecular dynamics simulations. Journal of Computational Chemistry. 32 (10), 2319-2327 (2011).
- Gowers, R., et al. MDAnalysis: A Python Package for the Rapid Analysis of Molecular Dynamics Simulations. SciPy. , (2016).
- McGibbon, R. obert T., et al. MDTraj: A Modern Open Library for the Analysis of Molecular Dynamics Trajectories. Biophysical Journal. 109 (8), 1528-1532 (2015).
- Fortunato, M. E., Colina, C. M. pysimm: A python package for simulation of molecular systems. SoftwareX. 6, 7-12 (2017).
- Scherer, M. K., et al. PyEMMA 2: A Software Package for Estimation, Validation, and Analysis of Markov Models. Journal of Chemical Theory and Computation. 11 (11), 5525-5542 (2015).
- Song, W., et al. PyLipID: A Python Package for Analysis of Protein-Lipid Interactions from Molecular Dynamics Simulations. Journal of Chemical Theory and Computation. 18 (2), 1188-1201 (2022).
- Monje-Galvan, V., Klauda, J. B. Peripheral membrane proteins: Tying the knot between experiment and computation. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1858 (7, Part B), 1584-1593 (2016).
- Monje-Galvan, V., Voth, G. A. Binding mechanism of the matrix domain of HIV-1 gag on lipid membranes. eLife. 9, e58621(2020).
- Wang, B., Guo, C. Concentration-Dependent Effects of Cholesterol on the Dimerization of Amyloid-β Peptides in Lipid Bilayers. ACS Chemical Neuroscience. 13 (18), 2709-2718 (2022).
Access restricted. Please log in or start a trial to view this content.
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved