Method Article
Tomografia Computerizzata guidata nel dominio del tempo Tomography Diffuse fluorescenza in animali di piccola taglia per la localizzazione dei biomarcatori tumorali
In questo articolo
Riepilogo
Diffuse la tomografia di fluorescenza offre un approccio relativamente a basso costo e potenzialmente ad alta dappertutto per preclinica In vivo Immagine del tumore. La metodologia di raccolta dei dati ottici, la calibratura e la ricostruzione delle immagini è presentato per una tomografia computerizzata guidata senza contatto nel dominio del tempo di sistema utilizzando il targeting fluorescente del tumore recettore fattore di crescita epidermico biomarker in un modello di glioma mouse.
Abstract
Piccoli animali di imaging di fluorescenza molecolare (FMI) può essere un potente strumento per la scoperta della droga preclinica e studi di sviluppo 1. Tuttavia, l'assorbimento della luce da cromofori dei tessuti (ad esempio, l'emoglobina, acqua, lipidi, la melanina) che stabilisce limiti propagazione ottica segnale attraverso spessori superiori a pochi millimetri 2. Rispetto ad altre lunghezze d'onda visibili, l'assorbimento del tessuto per il rosso e nel vicino infrarosso (near-IR) assorbimento della luce si riduce e non elastico di scattering della luce diventa il dominante del tessuto meccanismo di interazione. Lo sviluppo relativamente recente di agenti fluorescenti che assorbono ed emettono luce nel vicino-IR gamma (600-1000 nm), ha guidato lo sviluppo di sistemi di imaging e modelli di propagazione della luce che possono raggiungere tutto il corpo tridimensionale imaging in piccoli animali 3.
Nonostante i grandi passi avanti in questo settore, la natura mal posto della tomografia di fluorescenza diffusa resta un importanteproblema per la stabilità, il recupero contrasto e la risoluzione spaziale delle tecniche di ricostruzione di immagine e l'approccio ottimale per FMI nei piccoli animali deve essere ancora concordato. La maggior parte dei gruppi di ricerca hanno investito in charge-coupled device (CCD) basati su sistemi che forniscono abbondante la sensibilità dei tessuti di campionamento, ma non ottimale 4-9, mentre il nostro gruppo e pochi altri 10-13 hanno perseguito sistemi basati su rivelatori di sensibilità molto elevate , che in questo momento consentire campionamento tessuto denso essere raggiunta solo a costo di immagini a bassa velocità. Qui mostriamo la metodologia per l'applicazione di singoli fotoni tecnologia di rilevamento in un sistema di tomografia di fluorescenza di localizzare una lesione cancerosa del cervello in un modello murino.
La fluorescenza tomografia (FT) sistema impiegato fotone singolo conteggio utilizzando tubi fotomoltiplicatori (PMT) e ricco di informazioni nel dominio del tempo di rilevamento di luce in un non-contatto conformazione 11. Questo fornisce una simultanea colcolta di eccitazione e di emissione di luce trasmessa, e comprende il controllo dell'esposizione automatica a fluorescenza di eccitazione 14, riferimenti laser, e co-registrazione con un piccolo animale tomografia computerizzata (microCT) del sistema 15. Un modello di topo nudo è stata utilizzata per l'imaging. L'animale è stato inoculato ortotopicamente con una linea cellulare umana glioma (U251), l'emisfero cerebrale sinistro e ripreso 2 settimane dopo. Il tumore è stato fatto per fluorescenza mediante iniezione di un tracciante fluorescente, IRDye 800CW-EGF (LI-COR Biosciences, Lincoln, NE) mirato al recettore del fattore di crescita epidermico, una proteina di membrana cellulare note per essere sovra-espresso nella linea U251 tumore e molti altri tumori 18. Un secondo, non mirati tracciante fluorescente, Alexa Fluor 647 (Life Technologies, Grand Island, NY) è stato anche iniettato per tenere conto di non-effetti mediati dal recettore per l'adozione dei traccianti mirati a fornire un mezzo per quantificare vincolante tracciante e la disponibilità del recettore / densità 27. A CT-guidata, time-dominio algoritmo è stato utilizzato per ricostruire la posizione di entrambi traccianti fluorescenti (cioè, la posizione del tumore) nel cervello di topo e la loro capacità di localizzare il tumore è stato verificato mediante contrasto risonanza magnetica.
Sebbene dimostrata per imaging di fluorescenza in un modello murino glioma, il metodo presentato in questo video può essere esteso a diversi modelli tumorali in vari modelli animali di piccole potenzialmente fino alle dimensioni di un topo 17.
Protocollo
1. Preparazione degli animali
- Anestetizzare topo nudo (Charles River, Wilmington, MA) con intra-peritoneale iniezione di ketamina xilazina (100 mg / kg: 10 mg / kg ip).
- Luogo del mouse nel frame stereotassico, fare un'incisione nel cuoio capelluto sul lato sinistro del cranio e, utilizzando un ago calibro 18, creare un 1 mm di diametro foro nel cranio, 2 mm dalla linea centrale e 2 mm dietro il bregma.
- Iniettare 5 × 10 5 U251 cellule umane di glioblastoma neuronali (gentilmente fornito dal Dr. Mark Israele a Dartmouth College, Hanover, NH) in 5 ml di soluzione tampone fosfato nell'emisfero cerebrale sinistro ad una profondità di circa 2 mm sotto la superficie del cervello. Utilizzare un micro-siringa Hamilton 18 ed un smussato fine 27-gauge per l'impianto delle cellule ed inserire la punta dell'ago 3 millimetri dalla superficie esterna del cranio e poi ritirarsi 1 mm a creare una tasca per le cellule.
- Suture sito di incisione e consentire recupero da un intervento chirurgico.
- Attendere ~ 14 giorni per permettere al tumore di crescere prima di imaging.
2. Fluorescenza Tomografia sistema di calibrazione
- Il giorno di imaging mouse, avviare il sistema e consentire laser e sensori di luce per riscaldare per circa 20 minuti per evitare derive della sensibilità del sistema.
- Mettere a 100 °-by-4 ° di ingegneria linea diffusore (Thorlabs, Newton, NJ), al centro diretta del portale imaging, normale al laser di eccitazione: un picosecondo-pulsato 80-MHz multimodale 635 nm diodo laser (PicoQuant Photonics Nord America Inc., Westfield, MA). Regolare l'angolo del diffusore per massimizzare la quantità di segnale rilevata da tutti i canali di raccolta luce cinque. Una descrizione completa della geometria di imaging viene fornito altrove 11,14,15.
- Posizionare OD 2 filtri a densità neutra (Thorlabs, Newton, NJ) davanti a tutti i tubi fotomoltiplicatori fluorescenza di rilevamento (PMT) e OD 1 filtri a densità neutra (Thorlabs, Newton, NJ) di fronte a PMT rilevamento tutti trasmittanza. Raccogliere 100 profili temporali diffusione impulsi (TPSF) del laser, ciascuno con una 1-s tempo di integrazione.
- Normalizzare ogni TPSF dal riferimento laser, corretto per la deriva temporale di riferimento laser, e la media di tutte le iterazioni per ogni rivelatore. Questi sono i medi TPSFs rilevatore specifiche funzioni di risposta dello strumento (IRF) utilizzati nella ricostruzione dell'immagine ottica.
3. Imaging Protocol
- Anestetizzare la topo con 2% di isoflurano ossigeno (1 L / min).
- Iniettare 1 nanomole di IRDye 800CW-EGF e 1 nanomole di Alexa Fluor 647 in 100 ml di soluzione tampone fosfato, per via intraperitoneale, 12 ore prima di imaging per indirizzare la crescita epidermico fattore di sovraespressione del recettore nel tumore.
- Posizionare il mouse sulle vetroresina supporta del letto imaging, disponendo il mouse in modo che il suo naso rimane in un cono di fornire l'anestesia isoflurano.
- EnAssicurarsi che il mouse viene posizionato opportunamente sul letto: cioè, che quando il letto è fissato nel sistema tomografia fluorescenza il mouse è al centro approssimativo del cavalletto di imaging. Tale posizionamento può essere guidata ruotando il laser di eccitazione 180 ° sul mouse, assicurando che il punto focale del laser illumina un punto approssimativamente al centro del mouse dal punto di vista del laser a tutti gli angoli.
- Una volta posizionato, trasferire accuratamente il letto di imaging e il mouse per il microCT (eXplore Locus, GE Healthcare, London, ON) scanner e raccogliere informazioni anatomiche con una risoluzione di 93 micron isotropo per la testa tutto il mouse.
- Visualizzare la serie di immagini CT e scegliere la fetta (s) di essere ripreso con il sistema di tomografia fluorescenza.
- Trasferire accuratamente il letto di imaging e il mouse al sistema tomografia di fluorescenza. Scegli il numero di posizioni di origine per raccogliere i dati relativi il mouse per ogni SLIC di imaginge (32), il tempo di integrazione per ogni misurazione TPSF (1 s), il numero di iterazioni per ogni posizione della sorgente (10), e la posizione e il numero di fette di imaging desiderati dalla serie di immagini CT dal punto 3,6. I numeri tra parentesi sono valori tipici per ciascun parametro di imaging cedere ~ 5 minuti di acquisizione dati per fetta imaging.
- Mettere filtri notch triple (Chroma Technology Corp., Bellows Falls, VT) di fronte ai PMT rivelazione a fluorescenza, a limitare ogni luce laser di raggiungere i rivelatori di fluorescenza, e OD 2 filtri a densità neutra di fronte PMT di rilevazione della trasmittanza per evitare la saturazione di tali rivelatori.
- Eseguire il software di acquisizione dati, raccogliendo fluorescenza e TPSFs trasmittanza in ciascuna posizione determinata sorgente rivelatore e per ogni lunghezza d'onda di eccitazione (635 nm e 755 nm per eccitare il Alexa 647 e IRDye 800CW-EGF traccianti, rispettivamente). Per ogni serie di TPSFs collezionati, monitorare e registrare l'intensità del lasercon un canale di riferimento PMT.
4. Ricostruzione di immagini
- Determinare la superficie esterna del mouse e la posizione delle aste di supporto di imaging letto dalle immagini CT e creare maschere che copre i confini del mouse e le aste di imaging separatamente.
- Utilizzare la maschera mouse per produrre un mesh ad elementi finiti dell'animale utilizzando il software NIRFAST 19.
- Localizzare le posizioni della sorgente e del rivelatore dal sistema tomografia fluorescenza sulla superficie della rete basata su fluorescenza e microCT registrazione coordinate spaziali 20.
- Rimuovere ottici punti di dati associati con posizioni di origine o rivelatore che interagiscono con la posizione delle aste di imaging letto di supporto.
- Normalizzare i dati raccolti in ciascuna posizione del rivelatore di origine dal riferimento laser, corrette per la deriva temporale di riferimento laser, e corretto per sensibilità del filtro, che sono stati determinati per via sperimentale al momento dell'acquisto 15.
- Prendere il Rapporto Nato dei dati (fluorescenza diviso trasmittanza) per ciascuna sorgente-rivelatore di posizione e si moltiplicano con un modello di simulazione in avanti di trasmittanza in base alla mesh ad elementi finiti animale uniformi proprietà ottiche. Questo viene fatto per ridurre gli errori associati alla accoppiamento sorgente o rilevatore-tessuto 21, per calibrare i dati al modello 22, e per regolare i dati per altri aspetti del modello-dati corrispondenza 23,24.
- Costruire un vettore di dati composto della differenza scala dei dati raccolti rapporto nati ad entrambe le lunghezze d'onda. Il fattore di scala è stato scelto per ottimizzare il contrasto vincolante EGFR. Eseguire dominio del tempo ricostruzione delle immagini con i dati di differenza calibrato utilizzando il TPSF per ciascun canale di rilevamento come input, e creare mappe fluorescenza del mdc mirata tracciante 15.
5. Risultati rappresentativi
"> Un esempio di una ricostruzione fluorescenza con sovrapposto un co-registrato immagine anatomica CT dalla testa di un topo con un tumore U251 glioma ortotopica è presentato in figura 1b. Il centro di massa del glioma determinata dalla ricostruzione fluorescente (figura 1b ) era entro 1 mm dal centro tumore di massa determinata dal contrasto migliorare la risonanza magnetica (Figura 1a). Le immagini CT e MRI sono stati co-registrazione basato su un reciproco-informazioni di trasformazione.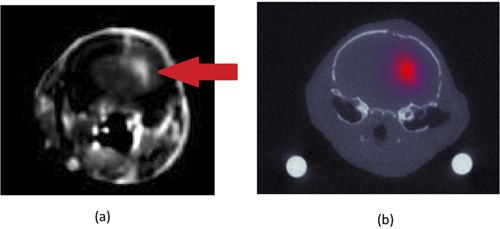
Figura 1. Con mdc (gadolinio) immagine di risonanza magnetica della testa mouse (a). Il mouse è stato inoculato ortotopicamente con una linea cellulare umana glioma U251. La posizione del tumore, che assorbe l'agente di contrasto più del cervello normale, può essere visto nel cerebrale sinistro (a destra in immagine) e indicato dalla freccia bianca. Il corresponding immagine tomografia computerizzata (dalla stessa posizione sulla testa mouse) è rappresentato in (b) con il fattore di crescita epidermico mirata fluorescenza meno il sovrapposta mirati ricostruzione fluorescenza. Le unità di fluorescenza sono in mm inverso e si riferiscono al coefficiente di assorbimento di fluorescenza associato mirata moltiplicato per la sua efficienza quantica e dalla sua concentrazione.
Discussione
Fluorescenza tomografia (FT) è un sensibile, modalità di radiazioni ionizzanti senza l'imaging molecolare basata su visibile e vicino infrarosso trasporto leggero attraverso il tessuto biologico. La maggior parte l'interesse per FT si è concentrata sulla sua capacità di accelerare la scoperta di farmaci e lo sviluppo di piccoli animali in modelli sperimentali 1 e un settore chiave della ricerca è stato lo studio di espressione biomarker del cancro e la risposta alle terapie molecolari 26. Attualmente, ci sono due approcci concorrenti al sistema di progettazione FT. Il disegno più comune si basa su raffreddati charge-coupled device (CCD) per il rilevamento della fluorescenza 4-9. Questo design garantisce una elevata densità di misurazioni, massimizzando campionamento tessutale poiché ciascun pixel nella fotocamera CCD in grado di rilevare la luce che ha viaggiato un unico percorso attraverso il tessuto. Tuttavia, le telecamere CCD hanno una limitata gamma dinamica e rumore di lettura limita la loro sensibilità finale. Il secondo disegno evita la possibilità limitazioni zioni di rilevamento della fotocamera CCD impiegando altamente sensibile a singolo fotone conteggio tecnologia basata sull'uso di rivelatori come tubi fotomoltiplicatori o fotodiodi a valanga 10-13. Lo svantaggio di questi metodi di individuazione più sensibili è che ogni rivelatore può raccogliere la luce in un singolo punto, quindi, per ottenere campionamento denso tessuto, sia rivelatori molti devono essere utilizzati (che è molto costoso), oppure molte sporgenze devono essere esposte con lo stesso rivelatore (che può richiedere molto tempo). Mentre il livello ottimale di campionamento tessuto per FT piccolo animale non è stato concordato, e può variare caso per caso, si conviene che il singolo fotone strumentazione conteggio è più adatto per esplorare i limiti di sensibilità in termini di FT della sua capacità di rilevare basse concentrazioni di marcatori molecolari. In questo studio, forniamo una metodologia per la realizzazione FT utilizzando singoli fotoni strumentazione di rilevamento conteggio di localizzare i tumori nei topi.
ENT "> Ci sono quattro passaggi critici coinvolti per la produzione di serie di dati robusti con il tempo-correlata single-photon FT conteggio. La prima è l'applicazione di una procedura di calibrazione adatto e semplice. Nella metodologia presentata, le rispettive sensibilità di ciascun canale di rilevazione sono contabilizzate per la raccolta da una misura di base di luce di eccitazione trasmessa attraverso una linea-diffusore progettato per dirigere frazioni uguali di luce per ogni rivelatore 15. Inoltre, la luce rilevata durante un esperimento è continuamente tarato al laser di riferimento, sia in termini di intensità e significano . tempo, che può variare nel tempo, per il funzionamento di un canale di riferimento laser 11,15 La seconda fase critica è la raccolta accurata e co-registrazione di imaging anatomico per guidate ricostruzioni fluorescenza I dati FT offre non solo informazioni anatomiche.; Pertanto, al fine di creare un modello di trasporto luce che può essere utilizzato per ricostruire la lozione di sorgenti fluorescenti all'interno di un campione dalla fluorescenza rilevata sulla superficie del campione, l'anatomia del campione in relazione al sistema FT deve essere accuratamente conosciuto. Nel nostro sistema, le informazioni anatomico viene acquisita da un micro-tomografia computerizzata sistema di coordinate spaziali che sono stati registrati spazialmente con quelli del sistema FT 15,20. La terza fase critica significa anche garantire che una esposizione ottimale (cioè, il tempo totale di rilevamento di fotoni per ogni proiezione laser) è alle dipendenze di ogni fonte-rivelatore di posizione. Questo è importante per due ragioni: primo, per garantire che vi sia sufficiente di segnale-rumore in ciascuna posizione di rilevazione e secondo per evitare la saturazione rivelatore, che potrebbe danneggiare le unità di rilevamento. Al fine di ottenere l'esposizione ottimale in ogni posizione rivelatore, un controllo automatico dell'esposizione viene impiegato, che triangola essenzialmente ottimizzare l'esposizione da due, bassa segnale esposizioni 14. La quarta criticapassaggio della metodologia fa riferimento ai dati raccolti fluorescenza alla quantità di luce trasmessa eccitazione. Questo riferimento viene spesso chiamato il rapporto Nato, e offre molti vantaggi per FT, con il principale dei quali una mitigazione del modello-dati gli errori di configurazione 23,24. Il sistema presentato è stato progettato per rilevare la luce di eccitazione sia fluorescenza e trasmette contemporaneamente incanalando la luce di ogni canale di rilevamento in 2 tubi fotomoltiplicatori separati. In questo modo, si evita qualsiasi effetto di movimento sulla precisione del rapporto Born.Con un robusto set di dati che a mano, la ricostruzione immagine del tempo nel dominio dei dati implica la soluzione del problema inverso della mesh ad elementi finiti con l'espressione:
d = Jx
dove d è un vettore con n x m elementi per n source-rivelatore proiezioni e m TPSF tempo cancelli; J è un n x m-by-l sensibilità matrice (o Jacobiana), per i nodi l nel mesh, ed x è il vettore di fluorescenza proprietà ottiche in ciascun nodo, con l dimensione d è i dati calibrati raccolti durante l'esperimento e J è simulato usando la soluzione di elemento finito. al ravvicinamento diffusione nel dominio del tempo di trasporto fluorescenza 25. La dimensione temporale di J è anche convoluta con le funzioni specifiche del rivelatore strumento di reazione. X è una rappresentazione della mappa fluorescenza di interesse ed è risolto per utilizzare un Levenberg Marqardt-non-negative almeno approccio quadrati con Tikhonov regolarizzazione 15.
La metodologia qui presentata, che descrive un procedimento in grado di localizzare tumori fluorescente in topi usando altamente sensibili Photon Counting rivelazione di fluorescenza, ha il potenziale per spingere i limiti di FT. In uno studio precedente, il potenziale di impiegare questoapproccio larger-than-topi modelli animali, come i ratti, così come la sensibilità migliorata rispetto alla progettazione di sistemi esistenti in topo di dimensioni esemplari, è stata dimostrata 17. L'applicazione immediata di questo approccio sarebbe per il monitoraggio di espressione biomarker in vivo in modelli animali di tumore di piccole dimensioni per valutare l'efficacia dei farmaci in un high-throughput mezzi. La capacità del sistema per eccitare e rilevare fluorescenza a lunghezze d'onda multiple permette la rilevazione simultanea di più marcatori fluorescenti. Altri marcatori fluorescenti fornire un mezzo di interrogare molteplici aspetti di una patologia, simultaneamente, o potrebbero essere utilizzati, come in questo studio, di impiegare metodi di imaging più quantitativi come dual-reporter metodi di misurazione in vivo potenziale di legame, un marker di densità recettore 26,27.
Divulgazioni
Non ci sono conflitti di interesse dichiarati.
Riconoscimenti
Questo lavoro è stato finanziato da borse di studio del National Cancer Institute di R01 CA120368, le R01 CA109558 (KMT, RWH, FEG, BWP), RO1 CA132750 (MJ, BWP) e K25 CA138578 (FL), e la Canadian Institutes of Research Award borsa Salute post-dottorato (KMT ). Lo sviluppo del sistema di tomografia di fluorescenza è stato parzialmente finanziato da Advanced Research Technologies (Montreal, QC).
Materiali
| Name | Company | Catalog Number | Comments |
| Nome del reattivo | Azienda | Numero di catalogo | Commenti (opzionale) |
| IRDye 800CW-EGF | LI-COR Biosciences | 926-08446 | |
| Alexa Fluor 647, succinimidil estere | Life Technologies | A20106 | Reagito con acqua per ridurre il legame non specifico |
Riferimenti
- Rudin, M., Weissleder, R. Molecular imaging in drug discovery and development. Nat. Rev. Drug Discov. 2, 123-131 (2003).
- Arridge, S. Optical tomography in medical imaging. Inverse Problems. 15, R41-R93 (1999).
- Leblond, F., Davis, S. C., Valdes, P. A., Pogue, B. W. Pre-clinical whole-body fluorescence imaging: Review of instruments, methods and applications. J. Photochem. Photobiol. B. 98, 77-94 (2010).
- Cao, J., Moosman, A., Johnson, V. E. A Bayesian chi-squared goodness-of-fit test for censored data models. Biometrics. 66, 426-434 (2010).
- Da Silva, A. Optical calibration protocol for an x-ray and optical multimodality tomography system dedicated to small-animal examination. Appl. Optics. 48, 151-162 (2009).
- Deliolanis, N. Free-space fluorescence molecular tomography utilizing 360 degrees geometry projections. Opt. Lett. 32, 382-384 (2007).
- Guo, X. A combined fluorescence and microcomputed tomography system for small animal imaging. IEEE Trans. Biomed. Eng. 57, 2876-2883 (2010).
- Lin, Y. Quantitative fluorescence tomography using a combined tri-modality FT/DOT/XCT system. Opt. Express. 18, 7835-7850 (2010).
- Zhang, X. High-resolution reconstruction of fluorescent inclusion in mouse thorax using anatomically guided sampling and parallel Monte Carlo computing. Biomedical Optics Express. 2, 2449-2460 (2011).
- Dominguez, J. B., Berube-Lauziere, Y. Diffuse light propagation in biological media by a time-domain parabolic simplified spherical harmonics approximation with ray-divergence effects. Appl. Optics. 49, 1414-1429 (2010).
- Kepshire, D. A microcomputed tomography guided fluorescence tomography system for small animal molecular imaging. Rev. Sci. Instrum. 80, 043701 (2009).
- Lin, Y. A photo-multiplier tube-based hybrid MRI and frequency domain fluorescence tomography system for small animal imaging. Phys. Med. Biol. 56, 4731-4747 (2011).
- Niedre, M. J. Early photon tomography allows fluorescence detection of lung carcinomas and disease progression in mice in vivo. Proc. Natl. Acad. Sci. U.S.A. 105, 19126-19131 (2008).
- Kepshire, D. L., Dehghani, H., Leblond, F., Pogue, B. W. Automatic exposure control and estimation of effective system noise in diffuse fluorescence tomography. Opt. Express. 17, 23272-23283 (2009).
- Tichauer, K. M. Imaging workflow and calibration for CT-guided time-domain fluorescence tomography. Biomedical Optics Express. 2, 3021-3036 (2011).
- Kennedy, J. C., Pottier, R. H. Endogenous protoporphyrin IX, a clinically useful photosensitizer for photodynamic therapy. Journal of photochemistry and photobiology. 14, 275-292 (1992).
- Leblond, F., Tichauer, K. M., Holt, R., El-Ghussein, F., Pogue, B. W. Towards whole-body optical imaging of rats using single-photon counting fluorescence tomography. Opt. Lett. 36, 3723-3725 (2011).
- Gibbs-Strauss, S. L. . Noninvasive fluorescence monitoring for functional assessment of murine glioma treatment [dissertation]. , (2008).
- Dehghani, H. Near infrared optical tomography using NIRFAST: Algorithm for numerical model and image reconstruction. Commun. Numer. Meth. En. 25, 711-732 (2009).
- Holt, R., El-Ghussein, F., Tichauer, K. M., Leblond, F., Pogue, B. W. . Proceedings of SPIE. , 789213 (2011).
- Ntziachristos, V., Weissleder, R. Experimental three-dimensional fluorescence reconstruction of diffuse media by use of a normalized Born approximation. Opt. Lett. 26, 893-895 (2001).
- Davis, S. C. Magnetic resonance-coupled fluorescence tomography scanner for molecular imaging of tissue. The Review of scientific instruments. 79, 064302 (2008).
- Leblond, F., Tichauer, K. M., Pogue, B. W. Singular value decomposition metrics show limitations of detector design in diffuse fluorescence tomography. Biomedical Optics Express. 1, 1514-1531 (2010).
- Soubret, A., Ripoll, J., Ntziachristos, V. Accuracy of fluorescent tomography in the presence of heterogeneities: Study of the normalized born ratio. Ieee T. Med. Imaging. 24, 1377-1386 (2005).
- Zhu, Q. A three-dimensional finite element model and image reconstruction algorithm for time-domain fluorescence imaging in highly scattering media. Phys. Med. Biol. 56, 7419-7434 (2011).
- Weissleder, R., Pittet, M. J. Imaging in the era of molecular oncology. Nature. 452, 580-589 (2008).
- Tichauer, K. M. In vivo quantification of tumor receptor binding potential with dual-reporter molecular imaging. Mol. Imag. Biol. , (2011).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon