Method Article
Flusso di lavoro senza macchie V3 per un controllo pratico, conveniente e affidabile del carico totale delle proteine nell'blotting occidentale
In questo articolo
Riepilogo
Il flusso di lavoro V3 è una procedura western blot che utilizza gel senza macchie. La tecnologia senza macchie consente ai ricercatori di visualizzare la qualità della separazione proteica, di verificare l'efficienza di trasferimento e, soprattutto, di convalidare il cambiamento nella proteina di interesse utilizzando la quantificazione totale delle proteine come controllo di carico affidabile.
Abstract
La macchia occidentale è una tecnica di laboratorio molto utile e ampiamente adottata, ma la sua esecuzione è impegnativa. Il flusso di lavoro è spesso caratterizzato come una "scatola nera" perché uno sperimentalista non sa se è stato eseguito correttamente fino all'ultimo di diversi passaggi. Inoltre, la qualità dei dati western blot è talvolta messa in discussione a causa della mancanza di efficaci strumenti di controllo della qualità in atto durante tutto il processo di soffiatura occidentale. Qui descriviamo il flusso di lavoro occidentale V3, che applica la tecnologia senza macchie per affrontare le principali preoccupazioni associate al tradizionale protocollo western blot. Questo flusso di lavoro consente ai ricercatori: 1) di eseguire un gel in circa 20-30 minuti; 2) visualizzare la qualità della separazione del campione entro 5 minuti dalla corsa del gel; 3) trasferire proteine in 3-10 min; 4) verificare quantitativamente l'efficienza dei trasferimenti; e, soprattutto, 5) per convalidare i cambiamenti nel livello della proteina di interesse utilizzando il controllo totale del carico proteico. Questo nuovo approccio elimina la necessità di spogliare e riprobing la macchia per le proteine delle pulizie come β-actina, β-tubulina, GAPDH, ecc. Il flusso di lavoro senza macchie V3 rende il processo western blot più veloce, trasparente, più quantitativo e affidabile.
Introduzione
Western blot è una tecnica molto utile9, tuttavia, ci sono due sfide principali con l'gonfiore occidentale: processo lungo e laborioso e qualità dei dati. Un protocollo tradizionale richiede circa 2 giorni. Coinvolge molti passaggi tra cui la preparazione del campione, la fusione del gel, l'elettroforesi e il trasferimento delle proteine, il blocco della membrana seguito dall'incubazione degli anticorpi, l'imaging e molto spesso lo stripping, il riprobing e infine l'analisi dei dati. Durante questo processo, non ci sono strumenti affidabili e flessibili per il controllo dei processi. Pertanto, gli errori possono essere introdotti in ogni fase e questi errori hanno il potenziale per generare artefatti di dati; pertanto, i controlli di caricamento sono essenziali nell'blotting occidentale per identificare e correggere gli errori. Il controllo del carico viene solitamente effettuato controllando il livello proteico di una proteina di riferimento in ogni campione per vedere se è ugualmente presentato. Le persone usano spesso proteine delle pulizie, come β-actina, β-tubulina, GAPDH, come controllo del carico.
La qualità dei dati western blot dipende da un controllo affidabile del carico. Ma ci sono due preoccupazioni legittime quando si utilizzano proteine di pulizia per i controlli di carico: 1) l'immunodetezione a base di anticorpi delle bande proteiche delle pulizie è spesso satura e quindi non si possono distinguere le differenze di carico tra icampioni 30; 2) il livello di espressione delle proteine di pulizia può variare nei campioni in determinate condizioni sperimentali, ad esempio il trattamento con siRNA, la morte cellulare, la differenziazione cellulare, ecc.11,28,3,6,10,21. A causa di queste preoccupazioni, le riviste scientifiche richiedono ora che "per confronti quantitativi, dovrebbero essere utilizzati reagenti appropriati, controlli e metodi di imaging con intervalli di segnale lineari" (linee guida sulla natura). Allo stesso modo, gli editori del Journal of Clinical Investigation chiedono controlli di carico più affidabili24. Per questi motivi, una proteina delle pulizie deve essere convalidata per essere utilizzata come controllo del carico. In primo luogo, bisogna assicurarsi che sia misurato nell'intervallo dinamico lineare del metodo di immunodetezione14,29. In secondo luogo, bisogna assicurarsi che sia espresso in modo coerente in tutti icampioni 26,31,25,19,20.
Una soluzione alternativa a un controllo di carico affidabile è utilizzare la misurazione totale delle proteine dalla macchia. Alcuni ricercatori hanno macchiato le macchie proteiche totali, come Coomassie, Flamingo Pink, Sypro Ruby, Amido Black, Ponceau S e tecnologia senza macchie, per misurare il segnale proteico totale in ogni corsia come controllo del carico16,20,13,27,1,4,12. Il controllo totale del carico proteico evita le insidie associate alle proteine delle pulizie. In primo luogo, è un vero riflesso della quantità di proteine caricate per ogni campione. In secondo luogo, la macchia proteica totale presenta un'eccellente gamma dinamica lineare nell'intervallo di carico comune per l'analisi western blot (proteina 10-50 μg di un lisato cellulare complesso) e differenzia accuratamente la differenza di carico tra i campioni12.
La tecnologia senza macchie è un nuovo metodo di colorazione proteica totale in cui un composto unico viene mescolato in soluzione di gel di acrilammide e distribuito uniformemente nel gel fusa. Una volta completata l'elettroforesi, il gel viene esposto alla luce UV per un minimo di 1 minuto in modo che il composto di macchia reagisca con i residui di triptofano nella proteina. Le proteine diventano eccitabili sotto la luce UV per dare un forte segnale fluorescente che può essere visualizzato e quantificato in un imager abilitato senza macchie come il sistema ChemiDoc MP. Il composto stesso privo di macchie, tuttavia, non assorbe la luce UV, con conseguente basso sfondo dell'immagine in gel. La modifica dei residui di triptofano è irreversibile e le proteine possono essere visualizzate non solo nel gel ma anche sulla macchia in qualsiasi momento dopo il trasferimento di proteine.
La tecnologia senza macchie viene applicata nel flusso di lavoro occidentale V3 (Figura 1) per affrontare i principali reclami relativi al flusso di lavoro tradizionale, in particolare i problemi relativi all'utilizzo delle proteine delle pulizie come controlli di caricamento. Utilizzando questo flusso di lavoro, si potrebbe: 1) eseguire un gel in circa 20-30 minuti, 2) controllare l'integrità del campione e la qualità della separazione proteica in 5 minuti dopo l'esecuzione del gel; 3) trasferire proteine in 3-10 min; 4) controllare quantitativamente l'efficienza del trasferimento; e 5) soprattutto, convalidare i cambiamenti nel livello della proteina di interesse utilizzando il controllo totale del carico proteico.
Protocollo
1. Preparazione del campione proteico
(Viene descritta una procedura tipica per estrarre proteine dalla coltura cellulare)
- Mettere il piatto di coltura cellulare HeLa nel ghiaccio e lavare le cellule con saline tris-buffered ghiacciate (TBS; 20 mM Tris-HCl, pH 7.5, 150 mM NaCl).
- Aspirare il TBS, quindi aggiungere 1 ml per tampone RIPA ghiacciato piatto da 100 mm (50 mM Tris-HCl pH 8.0, 150 mM NaCl, 1% NP-40, 0,5% di deossicholato di sodio, 0,1% SDS) integrato con inibitori della fosfatasi e della proteasi.
- Raschiare le cellule aderenti dal piatto usando un raschietto a celle di plastica fredda; trasferire delicatamente la sospensione cellulare in un tubo di microcentrifugo preraffreddato.
- Mantenere l'agitazione costante per 30 min a 4 °C su un rotatore.
- Girare a 16.000 x g per 20 min in una centrifuga preraffreddata a 4 °C.
- Rimuovere delicatamente il tubo dalla centrifuga e posizionare sul ghiaccio. Trasferire il supernatante in un tubo fresco tenuto sul ghiaccio e scartare il pellet.
- Rimuovere un piccolo volume (10-20 μl) di lysate per eseguire un test proteico. Determinare la concentrazione proteica per ciascun campione utilizzando il kit di saggi RC DC.
- Se necessario, aliquotere i campioni proteici per la conservazione a lungo termine a -20 °C. I cicli di congelamento e disgelo ripetuti causano la degradazione delle proteine e devono essere evitati.
- Prendere circa 20 μg di ogni campione, aggiungere un volume uguale di 2x Laemmli Sample Buffer (4% SDS, 10% 2-mercaptoetanolo, 20% glicerolo, 0,004% blu bromofenolo, 125 mM Tris-HCl, pH 6,8).
- Riscaldare ogni cella lysate in tampone campione a 95 °C per 5 min.
- Centrifuga a 16.000 x g in un microcentrifugo per 1 min.
2. Elettroforesi gel con gel senza macchie (~ 30 min)
- Prendi un criterio TGX Qualsiasi gel prefabbricato privo di macchie KD (un gel in formato midi), rimuovi il pettine e il nastro dal fondo della cassetta.
- Posizionare la cassetta nella cella Criterion e riempire la camera tampone superiore integrata con tampone di corsa da 60 ml (25 mM Tris, 190 mM di glicina, 0,1% SDS, pH 8,3). Risciacquare i pozzi con tampone in esecuzione.
- Riempire ogni metà del serbatoio tampone inferiore con un buffer di corsa di 400 ml alla linea di riempimento contrassegnata.
- Caricare i campioni proteici e i marcatori proteici appropriati.
- Posizionare il coperchio sul serbatoio, allineando i tappi di banana codificati a colori con i corrispondenti martinetti sul coperchio.
- Eseguire il gel per ~ 30 min a 200 V o 20 min a 300 V.
3. Imaging gel senza macchie utilizzando il sistema CHEMIDOC MP per controllare la qualità della separazione delle proteine (~ 5 min)
- Rimuovere la cassetta di gel dalla cella. Utilizzare lo strumento di apertura della cassetta in gel nel coperchio Criterion Cell per aprire la cassetta e rilasciare il gel.
- Applicare un paio di millilitri di acqua al centro del vassoio campione UV dell'imager ChemiDoc MP. Sollevare con cura il gel dalla cassetta e posizionarlo sul vassoio.
- Avviare il software Image Lab e acquisire l'immagine gel senza macchie (Figura 1A) con le impostazioni seguenti:
Applicazione: gel senza macchie
Tempo di attivazione del gel: 1 min
Area di imaging: gel criterio
Tempo di esposizione dell'immagine: ottimizzato automaticamente per le bande più intense - Rimuovere il gel dal vassoio del campione e procedere immediatamente alla fase di trasferimento.
4. Trasferimento proteico con il sistema Trans-Blot Turbo (~ 10 min)
- Aprire un pacchetto di trasferimento PVDF Trans-Blot Turbo Midi; posizionare la pila inferiore (che include la membrana) sulla base della cassetta di trasferimento.
- Posizionare il gel sopra la membrana, posizionare la pila superiore sul gel e stendere le bolle.
- Posizionare il coperchio sulla base della cassetta e ruotare il quadrante per bloccarlo.
- Inserire la cassetta nell'alloggiamento del blotter.
- Avviare il trasferimento selezionando un programma Turbo preimpostato e scegliendo la dimensione del gel Criterion (midi), quindi premere RUN. Una corsa tipica richiede solo 7 minuti.
- Al fine del trasferimento, smontare il sandwich gonfio e posizionare sia la macchia che il gel in un contenitore con acqua deionizzata.
5. Gel privo di macchie e imaging Blot utilizzando il sistema CHEMIDOC MP per controllare l'efficienza e la qualità del trasferimento proteico (~ 5 min)
- Posizionare il gel post-trasferimento sul vassoio campione dell'imager ChemiDoc MP.
- Avviare il software Image Lab e acquisire l'immagine senza macchie del gel post-trasferimento (Figura 1B) con le seguenti impostazioni:
Applicazione: gel senza macchie
Tempo di attivazione del gel: nessuno
Area di imaging: gel criterio
Tempo di esposizione dell'immagine: uguale al tempo di esposizione per l'immagine del gel pretrasferente - Rimuovere il gel dal vassoio del campione, quindi immaginere la macchia (Figura 1C) con le seguenti impostazioni. Mantenere la macchia bagnata con alcune gocce d'acqua o TBST durante l'imaging.
Applicazione: macchia senza macchie
Area di imaging: gel criterio
Tempo di esposizione dell'immagine: ottimizzato automaticamente per le bande più intense - Rimuovere la membrana assorbimento dal vassoio del campione e posizionarla in un contenitore con TBST (0,1% Tween 20 in TBS).
6. Incubazione anticorpale
- Bloccare posizionando la macchia in una soluzione di albumina siere bovina al 3% (BSA) in TBST a temperatura ambiente per 1 ora.
- Incubare la macchia durante la notte a 4 °C nella soluzione contenente anticorpi primari del topo sollevati contro la prima proteina bersaglio e l'anticorpo primario del coniglio sollevato contro la seconda proteina bersaglio.
- Versare la soluzione contenente l'anticorpo primario. Quindi, lavare la macchia agitando in 20 ml di TBST per 5 minuti. Ripetere 4 volte per un totale di 5 lavaggi.
- Incubare per 1 ora a temperatura ambiente nella soluzione anticorpale secondaria contenente un anticorpo goat-anti-mouse coniugato Dylight 650 e un anticorpo Goat-anti-rabbit coniugato Dylight 549.
- Versare la soluzione contenente l'anticorpo primario. Quindi, lavare la macchia agitando in 20 ml di TBST per 5 minuti. Ripetere 4 volte per un totale di 5 lavaggi.
7. Imaging e analisi dei dati da parte del software Image Lab - Normalizzazione totale delle proteine (~ 5 min)
- Acquisire un'immagine fluorescente multiplexing della macchia (Figura 1E) aprendo un nuovo protocollo multicanale, configurare tre canali fluorescenti ed eseguire il protocollo.
Canale 1:
Applicazione: blot Dylight 650
Area di imaging: gel criterio
Tempo di esposizione dell'immagine: ottimizzato automaticamente per le bande più intense
Canale 2:
Applicazione: blot Dylight 549
Area di imaging: gel criterio
Tempo di esposizione dell'immagine: ottimizzato automaticamente per le bande più intense
Canale 3:
Applicazione: macchia senza macchie
Area di imaging: criterio gel Tempo di esposizione dell'immagine: ottimizzato automaticamente per le bande più intense - Fate clic sull'icona Normalizzazione (Normalization) nella casella Strumenti analisi (Analysis Tool Box) e fate clic su Sì (Yes) per rilevare corsie e bande.
- Selezionare e utilizzare "Strumenti corsie e bande" per apportare modifiche alle corsie e alle bande, se necessario.
- Selezionare l'immagine senza macchie come canale di normalizzazione.
- Selezionate MW Analysis Tools e assegnate le corsie standard MW selezionando le caselle sottostanti.
- Per visualizzare i volumi normalizzati, fare clic sulla tabella analisi sulla barra degli strumenti. Tutti i calcoli verranno eseguiti automaticamente dal software, inclusi il fattore di normalizzazione e i volumi normalizzati. I valori di intensità della banda proteica target sono ora regolati per la variazione del carico proteico. Ciò consentirà confronti accurati delle proteine bersaglio tra i campioni.
Risultati
1. Valutazione dell'integrità del campione, della qualità della separazione proteica e dell'efficienza di trasferimento con immagini in gel senza macchie.
L'estratto proteico dalle cellule HeLa è stato separato a 300 V per 20 minuti su un gel privo di macchie Criterion AnyKD TGX da 18 pozzetti. I campioni proteici sono stati caricati 3 volte a quattro quantità diverse (Corsie 1-3, 40 μg; Corsie 4-6, 30 μg; Corsie 7-9, 20 μg; Corsie 10-12, 10 μg). Il gel è stato attivato sotto la luce UV per 1 min. Figura 2A mostra l'immagine del gel acquisita subito dopo la separazione proteica. L'integrità del campioneproteico (ad esempio la degradazione) e la qualità della separazione (ad esempio precipitazioneproteica) possono essere valutate visivamente con questa immagine gel. Le proteine sono state poi trasferite per 7 minuti in una membrana di nitrocellulosa utilizzando Trans-Blot Turbo. La figura 2B mostra l'immagine priva di macchie del gel post-trasferimento. Entrambe le immagini sono state acquisite con lo stesso tempo di esposizione (6,8 sec). La corsia 3 e la 12 sono state selezionate per misurare l'efficienza del trasferimento. Utilizzando lo strumento volume nel software Image Lab, è stata disetrar da una scatola rettangolare (blu) per coprire la corsia 3 e 12 su entrambe le immagini in gel. Il calcolo basato sui valori di volume di queste scatole indicava che l'efficienza di trasferimento di entrambe le corsie era dell'80% (Figura 2C). In questo esperimento, il gel TGX AnyKD è stato selezionato per studiare proteine bersaglio di piccole e medie dimensioni e non è stato ottimizzato per il trasferimento di grandi proteine. L'ottimizzazione dell'efficienza di trasferimento richiederebbe l'uso di gel percentualeinferiore (ad esempio 4-20%) e/o una regolazione del tempo di trasferimento per facilitare il trasferimento di grandi proteine. 2. Il controllo totale del carico proteico senza macchie è un'alternativa affidabile al controllo del carico delle pulizie nell'assorbimento occidentale per quantificare un piccolo cambiamento nel livello di proteine di interesse.
MCM-7 è un fattore di replicazione con licenza di DNA il cui livello diminuisce del 20-50% nelle linee cellulari linfoblastoidi (LCL) dopo il trattamento di irradiazione. In questo esperimento, i lisati (30 μg ciascuno) di quattro colture di linea cellulare linfoblastoide (LCL) trattate con irradiazione sono state separate su un gel privo di macchie Di 12 po' di criterio AnyKD TGX. Il gel è stato attivato per 1 minuto sotto la luce UV e trasferito da Trans-Blot Turbo su una membrana PVDF per l'immunoblotting. La proteina delle pulizie GAPDH (verde) è stata sondata con un anticorpo di coniglio (Cell Signaling Technology, USA, 1:2,500) e un anticorpo Dylight 549 coniugato Capra-anti-coniglio (Rockland, USA, 1:20,000). La proteina di interesse MCM-7 (rosso) è stata sondata usando un anticorpo del topo (Abcam, USA, 1:1,000) e un anticorpo di capra-anti-topo coniugato Dylight 649 (Rockland, 1:10,000).
La figura 3A mostra un'immagine fluorescente multiplex delle proteine totali (blu), MCM-7 (rosso) e GAPDH (verde) rilevate in quattro campioni LCL trattati con controllo e irradiazione. La figura 3B è un'immagine priva di macchie della stessa macchia che mostra i modelli proteici totali in ogni campione (30 μg). Il software di laboratorio di immagini ha selezionato le corsie campione (scatole blu) per misurare MCM-7, GAPDH e il volume totale di proteine in ogni corsia. I livelli di MCM-7 sono stati normalizzati sia rispetto alla misurazione totale delle proteine senza macchie che contro GAPDH. I livelli di proteine MCM-7 normalizzati sono stati analizzati statisticamente e il volume medio della banda proteica MCM-7 e la deviazione standard (n=4) sono presentati nel grafico(Figura 3C). Entrambi i metodi di normalizzazione hanno rivelato una piccola diminuzione (circa il 25%) nei livelli proteici MCM-7 dopo il trattamento di irradiazione. I dati con la normalizzazione totale delle proteine presentavano una deviazione standard inferiore a quella con GAPDH come controllo del carico.
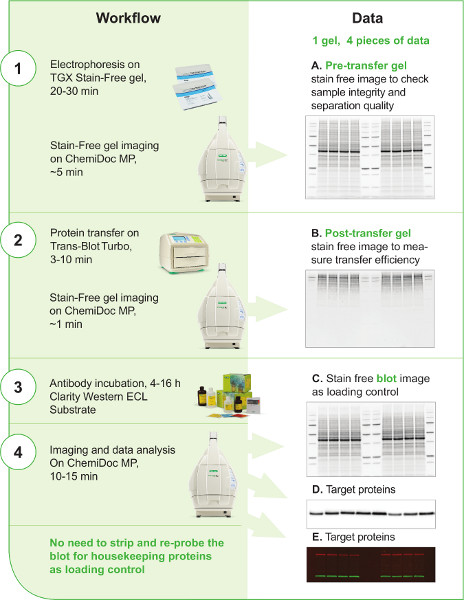
Figura 1. Flusso di lavoro occidentale V3. Il flusso di lavoro V3 è rappresentato nella colonna sinistra in 4 passaggi. I principali strumenti e reagenti utilizzati nel flusso di lavoro sono mostrati in ogni fase. È incluso anche il tempo stimato per ogni passaggio. La colonna destra mostra che è possibile generare almeno 4 immagini nel flusso di lavoro V3. Viene descritto l'uso di ogni dato. Le immagini senza macchie del gel pretrasfero, del gel post-trasferimento e della macchia(A, B, C) non possono essere generate facilmente con le tradizionali tecniche di soffiatura occidentale; Queste immagini e dati forniscono informazioni importanti e checkpoint lungo la procedura per migliorare il controllo e la riproducibilità dello scienziato del flusso di lavoro western blot. I segnali proteici bersaglio possono essere catturati su un'immagine macchia chemiluminescente(D) se è stato applicato un anticorpo secondario coniugato con HRP nel rilevamento o su un'immagine macchiafluorescente( E ) se è stato eseguito il multiplexing fluorescente western blotting per rilevare più di una proteina bersaglio contemporaneamente sulla stessa macchia.
Clicca qui per visualizzare l'immagine più grande.

Figura 2. Immagini senza macchie di gel pretrasferibili e post-trasferimento nel flusso di lavoro occidentale V3 per valutare l'integrità del campione, la qualità della separazione e l'efficienza del trasferimento. (A) Immagine senza macchie di gel pretrasfero. (B) Immagine senza macchie di gel post-trasferimento. ( C )Misurazionedell'efficienza del trasferimento proteico.
Clicca qui per visualizzare l'immagine più grande.
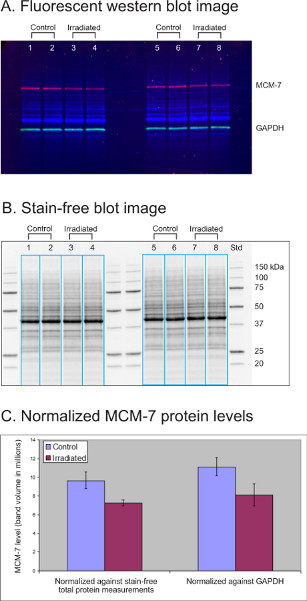
Figura 3. Confronto tra la misurazione totale delle proteine senza macchie e l'immunodetezione GAPDH come controlli di carico per normalizzare il livello di proteine di interesse. (A) Immagine western fluorescente macchia. (B) Immagine macchiata senza macchie. (C) Livelli di proteine MCM-7 normalizzati.
Clicca qui per visualizzare l'immagine più grande.
Discussione
Il protocollo privo di macchie V3 descritto sopra è per multiplexing fluorescente western blotting. Può anche essere applicato nell'blotting occidentale utilizzando il rilevamento chemiluminescente. Nel protocollo multiplex fluorescente western blot, le immagini macchiate senza macchie vengono acquisite in due punti di tempo: 1) subito dopo il trasferimento di proteine; 2) alla fase di imaging fluorescente multiplex dopo l'incubazione degli anticorpi. La prima immagine senza macchie viene utilizzata per calcolare l'efficienza di trasferimento e la seconda immagine senza macchie viene utilizzata come controllo di caricamento. Quando viene applicato il metodo chemiluminescente, non è possibile scattare un'immagine multiplex per i segnali proteici senza macchie e bersaglio, perché il segnale chemiluminescente verrà mostrato anche nel canale privo di macchie. In questo caso, si consiglia di utilizzare l'immagine senza macchie scattata subito dopo la fase di trasferimento delle proteine per il controllo del carico e l'analisi di normalizzazione.
Il flusso di lavoro occidentale V3 offre i seguenti vantaggi unici rispetto al tradizionale flusso di lavoro western blot che utilizza le proteine delle pulizie come controlli di caricamento:
Innanzitutto, il flusso di lavoro V3 fornisce un controllo del carico pratico, conveniente e più affidabile per convalidare i cambiamenti nel livello della proteina di interesse. Il protocollo V3 utilizza un controllo totale del carico proteico per normalizzare il livello della proteina di interesse misurata in ciascun campione. Evita due insidie nell'uso delle proteine delle pulizie come controlli di carico: immunodetezione satura e livelli di espressione delle proteine delle pulizie incoerenti tra i campioni in determinate condizioni sperimentali. Non sono più necessari passaggi di stripping e riprobing con anticorpi diretti contro le pulizie. Utilizzando la tecnologia senza macchie, non è necessario macchiare e de-macchiare una macchia con macchie come Coomassie o Sypro Ruby per la misurazione totale delle proteine. Bastano pochi secondi per acquisire un'immagine macchiata e circa 5 minuti per eseguire la normalizzazione totale delle proteine utilizzando il software Image Lab.
In secondo luogo, il flusso di lavoro V3 consente agli scienziati di assumere un migliore controllo della procedura occidentale perché rende la procedura più trasparente e introduce diversi checkpoint per il controllo di qualità. Con l'aiuto di una tecnologia senza macchie, i ricercatori possono visualizzare i loro campioni proteici sia sul gel che sulla macchia. Gli scienziati possono valutare l'integrità del campione proteico (degradato o meno), la qualità della separazione (precipitata o meno), l'efficienza di trasferimento e la qualità del trasferimento (anche il trasferimento o meno). Questi checkpoint aiutano le ricerche a terminare l'esperimento quando vedono grandi difetti nel processo ed evitano di perdere tempo su campioni e macchie scadenti. Questa tecnologia aiuta anche gli scienziati a valutare se c'è una quantità significativa di perdita proteica dopo lo stripping della membrana e se la macchia è adatta per riprobing di un obiettivo diverso 4.
Ecco alcuni suggerimenti per garantire una buona esperienza e dati di qualità utilizzando il flusso di lavoro occidentale V3.
- Immagine del gel immediatamente dopo l'esecuzione del gel. Non immergere il gel in alcun tampone prima della prima immagine nella procedura in quanto può lavare via il composto di macchie.
- Utilizzare la stessa area di imaging per acquisire tutte le immagini nel protocollo. Ciò consentirà al software di sovrapporre le immagini per l'analisi dei dati come la normalizzazione totale delle proteine.
- Mantenere costante il tempo di esposizione durante l'imaging dei gel di pretrasfero e post-trasferimento. Ciò consentirà al software di misurare quantitativamente l'efficienza del trasferimento.
- Mantenere la membrana bagnata con alcune gocce d'acqua o TBST quando si acquisisce l'immagine della macchia. Ciò eviterà possibili problemi di fondo sporchi per il rilevamento delle proteine bersaglio.
- Utilizzare la membrana PVDF a bassa fluorescente per multiplexare l'blotting occidentale fluorescente.
È importante notare che la molecola priva di macchie dopo l'attivazione UV è irreversibilmente legata ai residui di triptofano. Questa modifica irreversibile può potenzialmente influenzare il riconoscimento dell'antigene quando si utilizzano anticorpi monoclonali se l'epitopo contiene triptofano. È improbabile che gli anticorpi policlonali siano colpiti perché riconoscono più epitopi sull'antigene. Le molecole non legate senza macchie sono facilmente lavate via dal gel e dalla membrana e quindi non interferiranno con le interazioni anticorpo-antigene.
In conclusione, il flusso di lavoro occidentale V3 rende il processo western blot più veloce, trasparente, quantitativo e più affidabile. I ricercatori ora possono facilmente applicare il controllo totale del carico proteico in un esperimento western blot per rendere i loro dati più affidabili. Il flusso di lavoro privo di macchie V3 è stato adottato da un certo numero di laboratori e le loro pubblicazioni hanno dimostrato che le riviste accettano dati senza macchie come controllo del carico nella macchia occidentale22,17,7,8,5,23,18,15.
Divulgazioni
Gli autori, Anton Posch, Jonathan Kohn, Kenneth Oh, Matt Hammond e Ning Liu sono dipendenti di Bio-Rad Laboratories, Inc.
Riconoscimenti
Gli autori ringraziano il Dr. Wolf-Dieter Stalz, il Dr. Arnaud Remy, il Dr. Anton Posch, la Dott.ssa Patricia Piatti, Tom Davies, Kris Simonyi e Jeff Durban per la loro recensione critica e la modifica di questo manoscritto. Gli autori ringraziano anche Allison Schwartz per il supporto tecnico.
Materiali
| Name | Company | Catalog Number | Comments |
| REAGENTS | |||
| 4-20% Criterion TGX Stain-Free Precast Gel | Bio-Rad | 567-8093 | Choose a gel size and percentage that meet the specific need in a experiment |
| Trans-Blot Turbo Midi PVDF Transfer Packs | Bio-Rad | 170-4157 | Choose either PVDF or nitrocellulose and match the membrane size to the gel size |
| Clarity Western ECL Substrate, 500 ml | Bio-Rad | 170-5061 | |
| EQUIPMENT | |||
| Criterion Cell | Bio-Rad | 165-6100 | |
| Trans-Blot Turbo Transfer Starter System | Bio-Rad | 170-4155 | |
| ChemiDoc MP System | Bio-Rad | 170-8280 | |
Riferimenti
- Aldridge, G. M., Podrebarac, D. M., Greenough, W. T., Weiler, I. J. The use of total protein stains as loading controls: an alternative to high-abundance single-protein controls in semi-quantitative immunoblotting. J. Neurosci. Methods. 172 (2), 250-254 (2008).
- Bauer, D. E., Haroutunian, V., McCullumsmith, R. E., Meador-Woodruff, J. H. Expression of four housekeeping proteins in elderly patients with schizophrenia. J. Neural. Transm. 116 (4), 487-491 (2009).
- Castaño, Z., Kypta, R. M. Housekeeping Proteins: Limitations as References During Neuronal Differentiation. Open Neurosci. J. 2, 36-40 (2008).
- Colella, A. D., Chegenii, N., Tea, M. N., Gibbins, I. L., Williams, K. A., Chataway, T. K. Comparison of Stain-Free gels with traditional immunoblot loading control methodology. Anal. Biochem. 430 (2), 108-110 (2012).
- Cully, T. R., Edwards, J. N., Friedrich, O., Stephenson, D. G., Murphy, R. M., Launikonis, B. S. Changes in plasma membrane Ca-ATPase and stromal interacting molecule 1 expression levels for Ca2+ signaling in dystrophic mdx mouse muscle. Am. J. Physiol. Cell Physiol. 303 (5), (2012).
- Dittmer, A., Dittmer, J. Beta-actin is not a reliable loading control in Western blot analysis. Electrophoresis. 27 (14), 2844-2845 (2006).
- Dutka, T. L., Lamboley, C. R., McKenna, M. J., Murphy, R. M., Lamb, G. D. Effects of carnosine on contractile apparatus Ca2+ sensitivity and sarcoplasmic reticulum Ca2+ release in human skeletal muscle fibers. J. Appl. Physiol. 112 (5), 728-736 (2012).
- Elliott, S., Busse, L., Swift, S., McCaffery, I., Rossi, J., Kassner, P., Begley, C. G. Lack of expression and function of erythropoietin receptors in the kidney. Nephrol. Dial. Transplant. 27 (7), 2733-2745 (2012).
- Eslami, A., Lujan, J., Western, Blotting: Sample Preparation to Detection. J. Vis. Exp. (44), (2010).
- Ferguson, R. E., Carroll, H. P., Harris, A., Maher, E. R., Selby, P. J., Banks, R. E. Housekeeping proteins: a preliminary study illustrating some limitations as useful references in protein expression studies. Proteomics. 5 (2), 566-571 (2005).
- Greer, S., Honeywell, R., Geletu, M., Arulanandam, R., Raptis, L. Housekeeping genes; expression levels may change with density of cultured cells. J. Immunol. Methods. 355 (1-2), 76-79 (2010).
- Gürtler, A., Kunz, A., Gomolka, M., Hornhardt, S., Friedl, A. A., McDonald, K., Kohn, J. E., Posch, A. Stain-Free Technology as Normalization Tool in Western Blot Analysis. Anal. Biochem. 433 (2), 105-111 (2013).
- Hagiwara, M., Kobayashi, K., Tadokoro, T., Yamamoto, Y. Application of SYPRO Ruby- and Flamingo-stained polyacrylamide gels to Western blot analysis. Anal. Biochem. 397 (2), 262-264 (2010).
- Heidebrecht, F., Heidebrecht, A., Schulz, I., Behrens, S. E., Bader, A. Improved semiquantitative Western blot technique with increased quantification range. J. Immunol. Methods. 345 (1-2), 40-48 (2009).
- Jensen, R. B., Ozes, A., Kim, T., Estep, A. Kowalczykowski SC BRCA2 is epistatic to the RAD51 paralogs in response to DNA damage. DNA Repair. , (2013).
- Lanoix, D., St-Pierre, J., Lacasse, A. A., Viau, M., Lafond, J., Vaillancourt, C. Stability of reference proteins in human placenta: general protein stains are the benchmark. Placenta. 33 (3), 151-156 (2012).
- Larkins, N. T., Murphy, R. M., Lamb, G. D. Influences of temperature, oxidative stress, and phosphorylation on binding of heat shock proteins in skeletal muscle fibers. Am. J. Physiol. Cell Physiol. 3 (6), (2012).
- Laurie, K. J., Dave, A., Straga, T., Souzeau, E., Chataway, T., Sykes, M. J., Casey, T., Teo, T., Pater, J., Craig, J. E., Sharma, S., Burdon, K. P. Identification of a Novel Oligomerization Disrupting Mutation in CRYΑA Associated with Congenital Cataract in a South Australian. , (2012).
- Li, X., Bai, H., Wang, X., Li, L., Cao, Y., Wei, J., Liu, Y., Liu, L., Gong, X., Wu, L., Liu, S., Liu, G. Identification and validation of rice reference proteins for western blotting. J. Exp. Bot. 62 (14), 4763-4772 (2011).
- Liu, N. K., Xu, X. M. Beta-tubulin is a more suitable internal control than beta-actin in western blot analysis of spinal cord tissues after traumatic injury. J. Neurotrauma. 23 (12), 1794-1801 (2006).
- Lowe, D. A., Degens, H., Chen, K. D., Alway, S. E. Glyceraldehyde-3-phosphate dehydrogenase varies with age in glycolytic muscles of rats. J. Gerontol. A Biol. Sci. Med. Sci. 55 (3), 160-164 (2000).
- Mollica, J. P., Dutka, T. L., Merry, T. L., Lamboley, C. R., McConell, G. K., McKenna, M. J., Murphy, R. M., Lamb, G. D. S-glutathionylation of troponin I (fast) increases contractile apparatus Ca2+ sensitivity in fast-twitch muscle fibres of rats and humans. J. Physiol. 590, 1443-1463 (2012).
- Murphy, R. M., Dutka, T. L., Horvath, D., Bell, J. R., Delbridge, L. M., Lamb, G. D. Ca2+-dependent Proteolysis of Junctophilin 1 and Junctophilin 2 in Skeletal and Cardiac. 591, 719-729 (2012).
- Neill, U. S. All Data are not created Equal. J. Clin. Invest. 119, 224 (2009).
- Pérez-Pérez, R., López, J. A., García-Santos, E., Camafeita, E., Gómez-Serrano, M., Ortega-Delgado, F. J., Ricart, W., Fernández-Real, J. M., Peral, B. Uncovering suitable reference proteins for expression studies in human adipose tissue with relevance to obesity. PLoS One. 7 (1), (2012).
- Rocha-Martins, M., Njaine, B., Silveira, M. S. Avoiding Pitfalls of Internal Controls: Validation of Reference Genes for Analysis by qRT-PCR and Western Blot throughout Rat Retinal Development. PLoS One. 7 (8), (2012).
- Romero-Calvo, I., Ocón, B., Martínez-Moya, P., Suárez, M. D., Zarzuelo, A., Martínez-Augustin, O., de Medina, F. S. Reversible Ponceau staining as a loading control alternative to actin in Western blots. Anal. Biochem. 401 (2), 318-320 (2010).
- Said, H. M., Polat, B., Hagemann, C., Anacker, J., Flentje, M., Vordermark, D. Absence of GAPDH regulation in tumor-cells of different origin under hypoxic conditions in-vitro. BMC Res. Notes. 13 (2), 8 (2009).
- Suzuki, O., Koura, M., Noguchi, Y., Uchio-Yamada, K., Matsuda, J. Use of sample mixtures for standard curve creation in quantitative western blots. Exp. Anim. 60 (2), 193-196 (2011).
- Welinder, C., Ekblad, L. Coomassie staining as loading control in Western blot analysis. J. Proteome Res. 10 (3), 1416-1419 (2011).
- You, J., Hodge, C., Wen, L., McAvoy, J. W., Madigan, M. C., Sutton, G. Using soybean trypsin inhibitor as an external loading control for Western blot analysis of tear proteins: application to corneal disease. Exp. Eye Res. 99, 55-62 (2012).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon