Method Article
Riconfigurabile microfluidici canale con Pin-discretizzati fianchi
In questo articolo
Riepilogo
Un canale di microfluidica con fianchi deformabili offre controllo di flusso, la gestione delle particelle, canale dimensione personalizzazione e altre riconfigurazioni mentre è in uso. Descriviamo un metodo per la realizzazione di un canale di microfluidica con fianchi costituiti da una matrice di pin che permette la loro forma da modificare.
Abstract
Componenti microfluidici necessario disporre di varie forme per realizzare microfluidici chiave diverse funzioni come la miscelazione, separazione, intrappolamento delle particelle o reazioni. Un canale di microfluidica che deforma anche dopo fabbricazione pur mantenendo la forma del canale consente elevata riconfigurabilità spatiotemporal. La riconfigurabilità è necessaria in tali funzioni chiave microfluidici che sono difficili da raggiungere in sistemi microfluidici "riconfigurabili" o "integrata". Descriviamo un metodo per la realizzazione di un canale di microfluidica con una parete deformabile, costituito da una matrice allineata lateralmente delle estremità dei perni rettangolari. I perni nelle direzioni longitudinale di azionamento cambia le posizioni finali dei perni e così, la forma delle pareti laterali del canale discretizzato. Pin lacune possono causare perdite indesiderate o adesione ai pin adiacente causato dalle forze di menisco. Per colmare le lacune di pin, abbiamo introdotto degli idrocarburi-fluoropolymer basati su sospensione gap filler: accompagnati da una barriera elastomerica. Questo dispositivo microfluidico riconfigurabile può generare flusso forte temporale nel canale cilindrata, oppure può fermare il flusso in qualsiasi regione del canale. Questa caratteristica faciliterà, su richiesta, la manipolazione di cellule, liquidi viscosi, bolle di gas e non-fluidi, anche se la loro esistenza o comportamento è sconosciuto al momento della fabbricazione.
Introduzione
Dispositivi microfluidici - dispositivi micro-imprese che controllano le piccole quantità di liquido e flussi - offrono miniaturizzazione delle procedure biomediche in un formato di "chip" con maggiore portabilità e, spesso, convenienza. Come descritto in una recente recensione1, vari componenti microfluidici composto da spazi e caratteristiche positive sono stati sviluppati per realizzare funzioni fluidiche base e chiave quali la miscelazione, separazione, intrappolamento delle particelle o reazioni.
Mentre il comportamento di molti dispositivi microfluidici è determinato in fase di progettazione, alcuni tipi di dispositivi microfluidici consentono modifiche post-fabbricazione della loro struttura o il comportamento. Qui ci riferiamo a questa funzione come "riconfigurabilità". La riconfigurabilità dei sistemi microfluidici generalmente riduce i tempi e i costi necessari per la progettazione di un dispositivo, e/o consente la personalizzazione del layout di microfluidica o funzioni nel corso del tempo.
Precedentemente descritto riconfigurabile microfluidic dispositivi rientrano in tre categorie. Nel primo, deformazione dei canali elastomeriche permette le portate e le indicazioni per essere cambiato durante l'uso. Per ottenere la riconfigurabilità, elastomerici canali vengono deformati da varie forze esterne e controllabile come fonti di pressione pneumatica2, Braille attuatori3o compressione tenuta4. Nel secondo, riconfigurabile dispositivi si basano su disegni modulari, come il multistrato circuiti fluidici, modulari canali con magnetico interconnessioni e basati su tubazione microfluidica5. Nel terzo, il dispositivo stesso non è riconfigurabile, ma microdroplet trasporto su elettrodo matrici (spesso denominate digital microfluidica)6,7 e sospensione goccia-based microfluidic dispositivi8 attivare su richiesta commutazione del flusso o il percorso del fluido.
Tuttavia, molti di questi riconfigurazioni sono limitati a livello macroscopico e topologico. Ad esempio, molti dispositivi microfluidici integrato interrompono flusso o cambiare la direzione del flusso comprimendo microcanali in regioni predefinite. Tuttavia, la posizione e il numero delle regioni vengono compressi non sono riconfigurabili. Sebbene la microfluidica digitale ha una varietà di capacità di gestione dei fluidi, possibili flussi dovrebbero essere limitati in gran parte dal volume di ogni goccia. Inoltre, quando le cellule sono coltivate in tali goccioline di terreni di coltura cellulare, sforzo supplementare è necessaria per evitare evaporazione e dispersione di gas dalle goccioline e osmolalità shock e cambiamento di pH improvvisa.
Per realizzare la riconfigurabilità del livello di funzionalità di canale, abbiamo proposto un dispositivo microfluidico con pareti mobili che consisteva di matrici di elementi di macchine per la riconfigurazione dinamica li quando in uso9. Per formare una parete deformabile, piccoli perni rettangolari erano allineati affinché ciascuna estremità dei perni definito un segmento del fianco. I perni di scorrimento, ha permesso la deformazione del fianco che ha permesso di trasporto o campitura delle cellule, bolle e particelle all'interno del canale. Per ridurre al minimo il volume morto e massimizzare la riconfigurabilità, la distanza tra i perni adiacente doveva essere ridotto al minimo. Tuttavia, forte azione capillare agendo sulla piccola lacune tra i pin di collegamento all'interno e all'esterno il microchannel provoca perdite di liquidi entrando il divario di pin, causando evaporazione media, contaminazione batterica o citotossica e alla fine delle cellule morte. Pertanto, abbiamo sviluppato canali di reconfigurable microfluidici senza perdite discretizzato sidewall-tipo che resistere alle azioni cicliche pin e a lungo termine delle cellule cultura10.
In questo articolo, forniamo un protocollo per costruire microfluidici cella cultura dispositivo con una parete discretizzata che possa essere riconfigurata seguendo l'aumento graduale nella zona della coltura delle cellule. Ermeticità dei fianchi canale discreto è testato usando la formazione immagine di fluorescenza. La compatibilità di coltura cellulare e la capacità di patterning di cella vengono valutati mediante coltura cellulare su chip.
Questo sistema di microfluidica è adatto ogni volta che il canale appropriato design non può essere predeterminato e deve essere modificato su richiesta. Ad esempio, questo sistema potrebbe essere utilizzato per regolare la velocità di flusso e larghezza di canale basata sulla crescita delle cellule o migrazione, nematodi attivi flusso o trappola o altri piccoli oggetti che si comportano in modo imprevisto nel canale, o ad accettare vari campioni di raw o bioproducts che non sono stati ancora concepiti al momento della progettazione.
Protocollo
1. incisione di pin (Figura 2A)
- Sgrassare perni rettangolari tramite immersione in acetone.
- Passivare i perni immergendo in 4 mL di acido nitrico 10%, quindi riscaldare la soluzione a 65 ° C per 30 min in un forno.
- Sonicare i perni in acqua deionizzata per 5 min rimuovere l'acido residuo e asciugare con un tovagliolo di carta. Immergere i perni in 0,5 mL di agente di distacco della muffa per 2 h.Sonicate i perni in acqua deionizzata per 5 min.
- Fabbricare un piatto acquaforte (Figura 2C).
- Disegnare o iscrivere due linee parallele con un gap di 4 mm su un vetrino utilizzando un righello.
- Applicare un adesivo resistente alle sostanze chimiche e bassa viscosità per una superficie di due rettangolare tagliata vetrini.
- Legare i due vetrini tagliati su lastra di vetro a un gap di 4 mm. Utilizzare la linea parallela come guida.
- Erogare due linee di adesivo siliconico sul piatto acquaforte (vedere Figura 2C per la posizione e le dimensioni del contorno).
Nota: Un modello 3D-stampato (un file di modello STL è incluso come un materiale supplementare) vi aiuterà a disegnare linee con facilità e precisione. - Mettere i perni sul piatto incisione in modo che le punte lunghe mm 2 sulla loro estremità diritte sono immersi nel modello linea collante. Erogare il collante nuovamente per assicurarsi che i perni siano completamente coperti e disegnare un contorno. Trasferire il piatto incisione per un fermentatore umidificato, riscaldato a 38 ° C. Aspettare una notte per curare l'adesivo.
- Aggiungere 0,2 mL di acido nitrico M 0,5 0,2 mL di acido cloridrico 5,0 M lentamente in un flaconcino di vetro.
Attenzione: La miscela, noto anche come acqua regia, è molto corrosivo e potenzialmente esplosiva. Indossare guanti di gomma resistente agli acidi e occhiali di sicurezza e prestare la massima attenzione quando si maneggia acidi. Non conservare mai la soluzione. Ridurre l'acido nitrico come possibile per diminuire la sua aggressività. - Mettere il piatto di acquaforte su una piastra riscaldata a 65 ° C. Versare 0,4 mL della miscela acida sopra la regione scoperta dei perni. Aspettare 10 min e trasferire l'acido in un becher.
- Neutralizzare tutto l'acido restante compreso la regione acidata dei perni con 5 mL di soluzione di bicarbonato di sodio 0,8 M in acqua deionizzata.
- Rimuovere i perni dal piatto di acquaforte tirando longitudinalmente i perni con le pinzette. Sonicare i perni in acqua deionizzata per 5 min seguita da sonicazione in acetone per 5 min.
- Passivare acidata regione dei perni come descritto al punto 1.2.
- Verificare la larghezza dei perni acidati con un microscopio di negozio con un reticolo. Regolare il tempo di incisione descritto in 1.7 in modo che la larghezza della regione acidata è 0,2 ± 0,02 mm.
- Trasferire i perni in un flaconcino di vetro contenente 5 ml di etanolo al 70%. Portare il flaconcino per una cappa laminare. Pick up i pin dal flaconcino e lasciarli asciugare.
2. fabbricazione di lastra in Silicone con serbatoi e uno spazio per i perni.
- Realizzare uno stampo per uno spazio per perni e una parete fissa dai tipici processi litografici.
- Cappotto un vetrino sgrassati con 1 mL di photoresist negativo epossidica utilizzando una macchina a rotazione a 1.000 giri/min. Asciugare il photoresist su una piastra calda 95 ° C per 15 min. Ripetere questo passaggio una volta.
- Girare il cappotto il terzo strato di photoresist stesso a 2.000 giri/min su vetrino con photoresist rivestito. Asciugare il photoresist su una piastra di 95 ° C per 30 min.
- Esporre lo strato di photoresist a 450 mJ/cm2 di luce ultravioletta 365 nm da una sorgente di luce UV spot attraverso un film di photoplotted. Cuocere il photoresist esposto su una piastra di 95 ° C per 15 min. sviluppare il photoresist spruzzando un solvente (acetato di 2-metossi-1-metiletil) usando uno spruzzatore a mano e piega con gas azoto.
- Posto sul vetrino con fantasia photoresist nella parte inferiore di un piatto di plastica.
- Versare prepolimero di polidimetilsilossano (PDMS) sulla muffa ad uno spessore di 3 mm. Togliere l'aria dal prepolimero PDMS in un essiccatore sotto vuoto a-800 kPa per 10 min.
- Curare il prepolimero PDMS in un forno a 65 ° C per 1 h. Demold lastra PDMS parzialmente curata usando un bisturi. Completamente curare il PDMS in forno a 120° C per 1 h.
- Lungo il modello di orientamento, tagliare bordi irregolari lontani dalla lastra PDMS con il bisturi stesso. Rendere più precisa e un taglio pulito come possibile, in particolare alla superficie che definisce la fessura di inserimento (Vedi Figura 1A) per i perni.
- Perforare 2 fori mm di diametro per l'ingresso/uscita nelle estremità del canale principale della lastra PDMS con punzoni di biopsia. Allo stesso modo, perforare 1 fori mm-dimeter alle estremità del canale di sfiato aria. Vedere Figura 1A per il layout di canale e la posizione di questi fori.
3. montaggio del dispositivo di montaggio sul posto dei Gap Filler e barriera.
- Fabbricare un assembly microchannel.
- Immergere un 10 × 20 mm n ° 4 coprioggetto in una soluzione di pulizia riscaldata a 60 ° C per 10 min.
- Sciacquare due volte i vetrini con acqua deionizzata e asciugare a 120 ° C per 10 min.
- Plasma-bond il PDMS lastra da un coprioggetto:
- Posizionare la lastra PDMS (lato in funzione canale alto) e il pulito 10 × 20 mm n ° 4 coprioggetto nella camera a vuoto di un velo di polverizzazione.
- Iniziare a pompare giù la camera a 60 PA. generare aria vuoto del plasma (20 mA) per 30 s.
- Immediatamente sfogare la camera. Bond lato canale caratteristica del PDMS lastra dal coprioggetto con i loro bordi allineati.
- Posizionare gli strati incollati in un forno a 65 ° C per 10 min.
- Portare gli strati incollati a una cappa laminare usando un contenitore sterile. Sterilizzarli con luce UV per 30 min.
- Nella cappa laminare, inserire i perni nello slot in modo che loro estremità formano altri fianco del microchannel. Pins adiacenti dovrebbero essere differenti in lunghezza per evitare il contatto di entrambe le estremità verticale (vedere Figura 1B). Grande distanza tra le estremità verticale è preferibile. Uno spazio di (N-1) × (larghezza perno) è possibile quando vengono preparati N tipi di perni con lunghezze differenti pin (L in Figura 2A).
- Fabbricare una base ( Figura 2B).
- Fare o leggere un file di parte della base e fare due file di controllo numerico (NC) (contenente percorsi utensile; incluso come materiale supplementare) utilizzando software CAD/CAM. Il primo file NC supplementare utilizza un 4 mm-diametro fine mulino e la seconda un 1 mm di diametro fine mulino.
- Fissare un bordo di 3 mm di spessore chiaro polimetilmetacrilato (PMMA) su una fresa CNC.
- Aprire il primo file NC sul controller di un mulino di NC (CNC) del computer. Installare una fresa a 4 mm per il laminatoio CNC e individuare zero pezzo toccando la fresa alla scheda di PMMA. Eseguire il codice NC per tagliare il bordo.
Nota: Soffiare occasionalmente la punta di mulino di fine con aria compressa per la rimozione di raffreddamento e chip. - Ripetere 3.2.3 utilizzando il secondo file NC e un laminatoio di estremità di 1 mm.
- Sgrassare i pezzi lavorati con detergente e asciugare con un tovagliolo di carta. Spruzzare le parti con etanolo al 70% e portarli a una cappa laminare.
- Fabbricare una barriera elastomerica e riempitivo di pin:
Nota: La procedura 3.3.1 - 3.3.7 dovrebbe essere eseguita in modo asettico in una cappa laminare.- Preparare del gap filler con petrolato bianco e polvere di politetrafluoroetilene con un rapporto 2:1 in peso. Omogeneizzare la miscela utilizzando un omogeneizzatore ad ultrasuoni.
- Versare del gap filler in una siringa dispenser. Inserire un pistone e spingerlo a riempire la punta della siringa. Inserire un ago e spingere lo stantuffo nuovamente fino a quando la punta dell'ago è pieno. Allo stesso modo, preparare una siringa dosatore con un pistone e un ago e riempire con adesivo siliconico.
- Collegare ogni siringa a un distributore pneumatico utilizzando un adattatore tubo. Regolare le pressioni di erogazione per adesivo siliconico e filler a 250 kPa e 280 kPa.
- Dosare la colla del silicone sul bordo di una tasca della base. Collocare un 10 × 20 mm n ° 4 coprioggetto sulla tasca e premere fermamente per legare.
- Dosare la colla del silicone ad una profondità di circa 1 mm per disegnare due segmenti lungo due slot esterno della base. Il dosaggio del gap filler ad una profondità di circa 1 mm, per disegnare segmenti lungo l'altro slot.
- Dosare la colla del silicone sul bordo di un'altra tasca. Inserire un assembly microchannel (3.1) sulla tasca e premerlo con forza di legame.
- Ripetere 3.3.5 per garantire che sia del gap filler e adesivo siliconico completamente incorporare i perni e che non c'è nessuna apertura alle slot machine.
- Mettere il dispositivo in un contenitore sterile come una scatola di acciaio inox con coperchio. Trasferire il contenitore di un fermentatore umidificato, riscaldato a 38 ° C. Nella cappa laminare, curare la barriera elastomerica per un giorno.
- Spostare ogni pin fino a 1 mm lungo pins adiacenti per liberare i perni dalla barriera elastomerica polimerizzato.
- Sterilizzare il dispositivo con luce UV per 30 min.
4. valutazione del dispositivo microfluidico
- Ricerca delle perdite mediante fluorescenza
- Aprire il microchannel utilizzando un utensile o un robot desktop. Rendere la larghezza del canale come coerente in tutto il canale come possibile.
- Diluire un colorante fluorescente verde con acqua deionizzata a 10 µM per rendere la soluzione di fluorescenza.
- Aggiungere soluzione di fluorescenza a una delle porte fine di microchannel con una micropipetta. Questo passaggio verrà riempito il canale con la soluzione.
- Mettere il dispositivo microfluidico e due pezzi di carta assorbente bagnata con acqua deionizzata in un grande piatto di plastica. Incubare la piastra a 37 ° C e 5% di CO2 per almeno 24 h.
- Registrare immagini di fluorescenza verde di microchannel con un microscopio invertito a fluorescenza con una fotocamera di microscopio.
- Aprire le immagini fluorescenti con un software di analisi di immagine appropriata e confermare che non c'è nessuna perdita (fluorescenza verde) all'interfaccia del gap filler e le spine.
- Cellule di seme per il microchannel.
- Preparare un recipiente della cultura cella contenente cellule confluenti di 70-80% (a seconda di tipi cellulari). Staccare e sospendere le cellule in coltura.
- Centrifugare le cellule (la velocità e l'ora dipendono dai tipi di cella) e aspirare il mezzo.
- Risospendere le cellule con una piccola quantità di mezzo. Contare le celle con un contatore di cellule e regolare la densità delle cellule da 1,5 × 106 a 1,5 × 107 cellule/mL.
- Aprire il microchannel utilizzando un utensile o un robot desktop (Figura 1B) per rendere un canale largo dritto 400 µm. Regolare le posizioni di pin per rendere la parete laterale come piatto in tutto il canale come possibile. Aggiungere la sospensione cellulare ad uno del porto fine del microchannel e riempire il canale.
- Individuare uno dei perni che definisce la parete laterale della regione per avviare la cultura. Sotto un microscopio invertito, chiudere i due perni adiacenti per racchiudere le celle tra la regione della coltura delle cellule.
- Chiudere tutti i pin nell'ordine dall'interno all'esterno per espellere tutte le cellule dal canale. Delicatamente aspirare sospensione i porti di fine e aggiungere il terreno a loro.
- Incubare il dispositivo come descritto in 4.1.4. Quando le cellule sono circa 70-80% confluenti, aprire lentamente un pin per ampliare la zona di coltura.
Risultati
Nella Figura 1viene illustrata la costruzione del microchannel riconfigurabile. Perni rettangolari multipli sono stati disposti su un substrato di vetro ed erano allineati in modo che il lato lungo i piedini era in contatto. Un foglio PDMS con perforato fori e un incavo della profondità stessa come l'altezza del perno coperto le estremità dei perni per formare i serbatoi di entrata/uscita canale, canale soffitto e parete laterale un altro fronte alla parete di canale che ha consistito dei perni. La regione circondata da pins, un muro (uno dei volti del foglio PDMS) e il substrato di vetro formano un canale microfluidico.
Come descritto in precedenza, la riconfigurabilità del sistema proposto microfluidica è raggiunto da molti piccoli perni posizionati in parallelo con le lacune molto piccole ma diverso da zero. Il problema nei rapporti precedenti era il forte flusso generato attraverso le lacune dall'effetto capillare. Per ovviare a questo problema, le lacune in primo luogo sono state riempite con un riempitivo. In questo protocollo, una miscela di dispersi di idrocarburi viscoso e polvere di fluoropolimero fu usata come un riempitivo. Tuttavia, il gap filler stesso è inoltre conforme all'effetto capillare. Di conseguenza, come mostrato nella Figura 1, il microchannel riconfigurabile risultante ha idrocarburi/fluoropolymer gap filler: sia una barriera elastomerica costituita intorno al perimetro esterno del gap filler. Diradamento la metà dei pin è necessario per ospitare una quantità sufficiente di riempitivo per assicurare lo spessore e la forza della barriera elastomerica tra due perni.
Figura 2 A Mostra un disegno di un perno che forma un segmento di muro laterale. Grado dell'acciaio inossidabile 316L è stato selezionato come il materiale grazie alla sua resistente alla corrosione e bassa lisciviazione proprietà. Tuttavia, un processo di passivazione supplementare è stato richiesto di rendere compatibile la coltura cellulare perni. Un perno deve avere una punta precisamente rettangolare senza bave per formare con successo un segmento di muro laterale. Inoltre, un perno deve avere una "maniglia" affinché il pin può essere spostato facilmente spingendo la maniglia. Perché ogni pin ha una sezione centrale stretto, lo spessore di elastomero tra i pin era abbastanza per resistere a taglio causato dal movimento del perno. A differenza di altre parti del dispositivo, la realizzazione di perni, ad eccezione di diradamento centrale, deve essere effettuata tramite una società specializzata in elettroerosione (EDM) perché è uno dei metodi più precisi e più redditizio di lavorazione piccola parti in metalli duri. Esecuzione di diradamento centrale da acquaforte te stesso riduce il costo di lavorazione e il rischio di piegamento o rottura durante la lavorazione.
Per confermare che il gap filler, la barriera elastomerica e alla fine la tenuta del microchannel riconfigurabile funzionare correttamente, la rilevazione di perdita di fluorescenza è stata utilizzata. La figura 3 Mostra un'immagine di fluorescenza della zona vicino al bordo della barriera elastomerica 3 giorni dopo il microchannel è stato riempito con acqua contenente colorante tracciante fluorescente. L'immagine di fluorescenza dimostra che il liquido di riempimento del canale ha raggiunto una profondità di circa 200 µm dal bordo visibile della barriera elastomerica. Tuttavia, il liquido non ha raggiunto il gap filler. Inoltre, è stata osservata nessuna perdita di gap filler: attraverso la barriera elastomerica. Questa osservazione indica che il molto stretto tra la stretta metà dei perni e barriera elastomerica ha impedito la migrazione di liquido attraverso le lacune.
Infine, abbiamo effettuato la coltura cellulare a lungo termine con la zona di coltura adattata espandendo gradualmente la parete laterale del dispositivo microfluidico riconfigurabile come mostrato in Figura 4A. A d 0, un piccolo numero di cellule sono stato confinato all'interno di uno spazio pari a una pin-larghezza e altre cellule sono state aspirate. A 2 d, le cellule sono state fissate alla superficie inferiore e iniziato a proliferare. Due perni sono stati ritratti in modo che tutte le cellule erano chiaramente visibili, anche se il confluency era ancora bassa. Alla 5D, le cellule hanno continuato a proliferare e la confluenza è aumentato. Alle 6 e 9 d, altri due perni sono stati ritratti per mantenere il underconfluent di cellule. L'effetto di graduale espansione della zona della coltura è illustrato nella Figura 4B. Ci erano cambiamenti improvvisi nella densità delle cellule il giorno che i piedini sono stati ritratti. Tuttavia, il tasso di crescita del conteggio delle cellule è stato mantenuto costante, mentre quello visto nella coltura cellulare tipico è esponenziale.
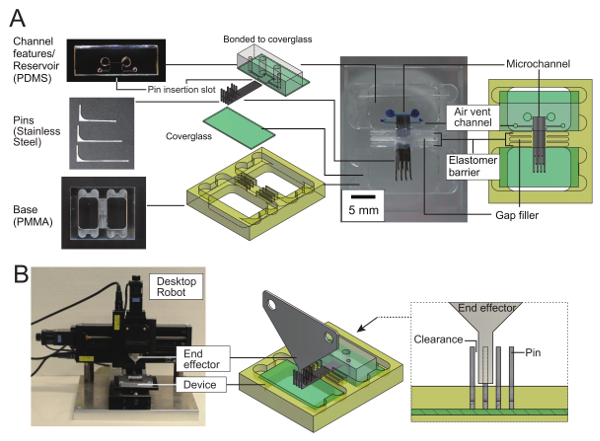
Figura 1 : Dispositivo microfluidico riconfigurabile con un perno-discretizzati sidewall. (A) parti e la costruzione di un dispositivo microfluidico riconfigurabile. Il dispositivo ha un canale rettilineo con una parete laterale formata dalle estremità dei 10 perni in acciaio inox inseriti PDMS/vetro microchannel caratteristiche. Gap filler: e una barriera elastomerica evita liquido fuoriuscita attraverso le lacune di pin. Vetrini, riempitivo e la barriera di elastomero sono fissati un polimetilmetacrilato (PMMA) base. (B) automatizzato pin manipolatore. Un effettore finale composta da un foglio di metallo è fissato un desktop robot a 3 assi. Per spostare un pin, l'effettore finale spinge la sua fine verticale. Perni con diverse lunghezze sono collocati a intervalli di tre volte la larghezza del perno. L'intervallo che assicura il fine dell'effettore compagni un pin in una sola volta con spazio sufficiente. Clicca qui per visualizzare una versione più grande di questa figura.
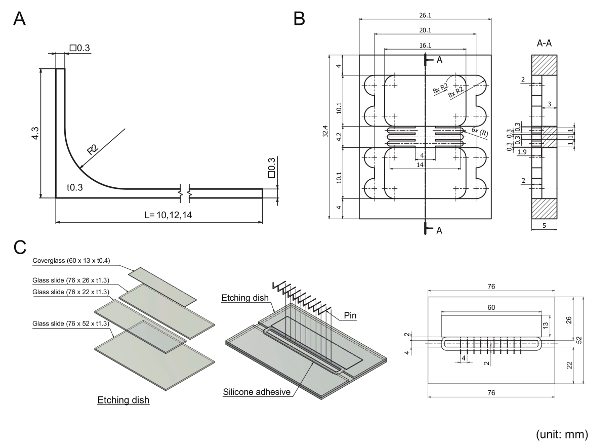
Figura 2 : Disegno meccanico dei pezzi lavorati utilizzati nel protocollo. Unità sono espresse in millimetri; R indica una quota di raggio; il simbolo quadrato (□) indica caratteristiche quadrati; t indica lo spessore. (A) un perno in acciaio inox 316 L come una parte del fianco. Pin può essere ordinato e lavorati come descritto. Assottigliamento del mezzo perno per fare cane osso-come forme non viene riflessa in questo disegno perché questo non è stato ordinato come parte della lavorazione, ma è stato effettuato come parte del protocollo. (B) una base di polimetilmetacrilato (PMMA) che trattiene i vetrini, riempitivo e barriera elastomerica in posizione contro il movimento di perno. (C) un piatto di incisione che è usato per incidere la metà dei perni. Per costruire un piatto di acquaforte, quattro pezzi di vetro sono incollati con adesivo siliconico. Uno schema di distribuzione di adesivo siliconico viene disegnato sul piatto seguito dalla disposizione dei pin sul piatto come mostrato nel disegno. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 3 : Rilevazione della fluorescenza di perdita da un microchannel riconfigurabile attraverso le lacune pin. Immagine di fluorescenza del colorante fluorescente verde il microchannel riconfigurabile di riempimento è sovrapposta su un'immagine di contrasto di fase della struttura sigillo, che è costituito da un riempitivo (opaco) e barriera elastomerica (traslucida). Un bordo della barriera elastomero è visibile come menisco-come le caratteristiche ed è indicato con una linea tratteggiata superiore; l'interfaccia tra elastomero barriera e gap filler è indicato come menisco-come le caratteristiche che a contatto con l'area nera ed è indicato dalla linea tratteggiata inferiore. Clicca qui per visualizzare una versione più grande di questa figura.
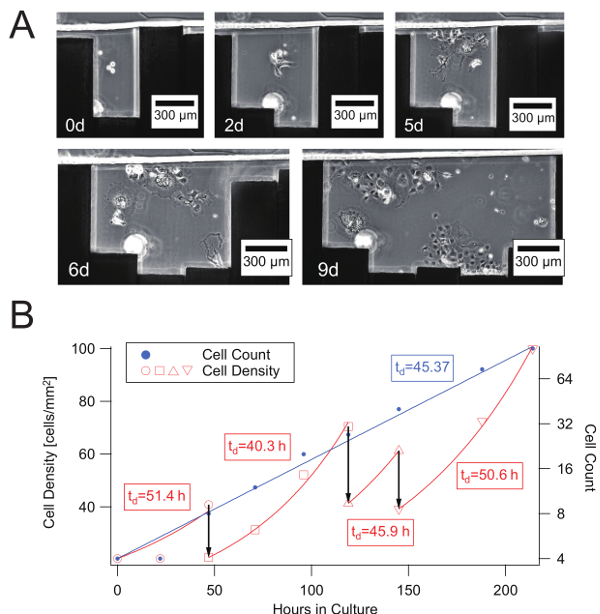
Figura 4 : Crescita progressiva e continua delle cellule con zona di coltura di cella variabile in un microchannel riconfigurabile. (A) crescita delle cellule COS-7 in una zona di coltura cellulare confinata muovendo i fianchi. (B) crescita curva e tempo evoluzione della densità di cellule COS-7 confinate in zone della coltura di dimensioni variabili nel microchannel riconfigurabile mostrato nella A). Tre frecce verticali indicano espansione della zona della coltura delle cellule a 2, 5 e 6 d, rispettivamente. Oltre al conteggio delle cellule, densità delle cellule sono indicati per le stesse zone di coltura, montati singolarmente a ogni curva di crescita esponenziale e utilizzato per stimare il tempo di raddoppiamento locale (td [h]) mostrato nei frame. Clicca qui per visualizzare una versione più grande di questa figura.
Discussione
Il pin-discretizzati microchannel è un canale di microfluidica full-optional, e crediamo che ha ovviamente elevata riconfigurabilità nella forma del canale rispetto a qualsiasi esistenti canali microfluidici. Il protocollo che abbiamo fornito qui consentirà dispositivi microfluidici capaci di coltura cellulare con gradualmente ampliando cella cultura superficie per mantenere le culture sotto confluency per una lunga durata. Il dispositivo fornirà anche nel canale campitura delle cellule senza patterning proteine substrato in anticipo o qualsiasi altra considerazione al momento della progettazione o di fabbricazione. Inoltre, questo dispositivo microfluidico riconfigurabile genera facilmente forte nel canale spostamento flusso, che contribuirebbe a implementare la gestione di tali materiali di difficile--flow che pochissimi microfluidici esistenti dispositivi in grado di gestire. Ciò significa che l'interazione tra le cellule e altri microrganismi, gas e altri fluidi-non può essere valutato utilizzando questo dispositivo senza grandi modifiche nella progettazione del dispositivo.
Abbiamo considerato l'applicazione di pressione di Laplace o pressione idrostatica a un ingresso del canale come metodi di controllo di flusso esterno. Non è consigliabile che spinge il liquido in un vicolo cieco perché genererà flusso verso il canale di sfiato di aria attraverso le lacune tra i pin e il pavimento/soffitto del canale. Molte operazioni di fluido non richiedono operazioni pin. Ad esempio, di miscelazione è possibile schiacciare il liquido da un pin (cioè, un solo pin in movimento avanti e indietro diverse volte).
Le parti più critiche del dispositivo sono i perni. Precisione di lunghezza, parallelismo, perpendicolarità e qualità di superficie sono necessari per le spine, come essi devono formare un microchannel, deve muoversi agevolmente e deve guidare il movimento di pins adiacenti. Pertanto, si consiglia che i perni devono essere effettuati tramite una società specializzata in lavorazioni meccaniche di precisione inviando un disegno simile alla Figura 2A. Ci possono essere le aziende che richiedono ulteriori dimensionamento geometrico e indicazioni esplicite rugosità superficiale. Tuttavia, i perni sono riutilizzabili se sono maneggiati con cura e occasionalmente passivati con acido nitrico.
La barriera elastomerica è un'altra caratteristica fondamentale, e la sua formazione è il punto più critico nei processi di fabbricazione del dispositivo. Una base con precisione lavorata sarà necessari per ottenere risultati affidabili e ripetibili. Appoggiando i dentini sulla barriera non polimerizzata è anche un passo fondamentale. I perni devono essere tenuti ben allineati e incorporato nel gap filler e la barriera senza bolle d'aria. Questi passaggi evitare perdite attraverso i perni, che è un problema comune con questo dispositivo microfluidico.
Altri problemi comuni nell'utilizzo di questo dispositivo sono perni) con accoppiamento per attrito sobri e morte delle cellule b) e tasso di crescita bassa. Possibili cause per questi in un) includono irregolare acquaforte (conico o ondulati) del perno centrale, qualità scadente del disadattato acidato superficie e dimensionale tra l'altezza della punta di perno e l'altezza dello strato di photoresist su uno stampo per lastre in silicone. Regolazione della formulazione di mordenzante, temperatura e l'agitazione può contribuire a migliorare il movimento del perno. Inoltre, prova di montaggio senza l'utilizzo di cera o adesivo fornirà suggerimenti per risolvere il problema. Possibili fattori in b) sono insufficienti passivazione dei perni, errori nella selezione degli adesivi per barriere elastomeriche e polimerizzazione incompleta degli adesivi. Alcune cellule possono richiedere il rivestimento interno del microchannel con fibronectina o altre proteine o polimeri che promuovono l'adesione delle cellule. Inoltre, ottimizzazione nella pratica di coltura delle cellule come trypsinization e centrifugazione diminuirà le cellule morte nel microchannel.
Una delle limitazioni del protocollo presentato fabbricazione è che solo una delle pareti laterali viene discretizzata. La riconfigurabilità del canale migliorerà ulteriormente se entrambi i fianchi sono costruiti da matrici di pin. Anche se richiede il doppio dei perni e passi di lavorazione più lunghi, si tratta di una soluzione tecnicamente praticabile.
Divulgazioni
Gli autori dichiarano di non avere nessun concorrenti interessi finanziari.
Riconoscimenti
Questa ricerca è stata sostenuta da KAKENHI (20800048, 23700543).
Materiali
| Name | Company | Catalog Number | Comments |
| Oven | Yonezawa | MI-100 | |
| 10% Nitric Acid | Wako Chemicals | 149-06845 | |
| Stainless steel pins | Micro Giken | N/A | 0.3 mm crosssection, Grade 316L stainless steel, wire-cut EDM |
| Mold release agent | Fluoro Technology | FG-5093SH | |
| Polydimethylsiloxane (PDMS) | Shin-Etsu Chemicals | KE-106 | |
| Negative epoxy photoresist | Nippon Kayaku | SU-8 3050 | |
| Coverglasses (Rectangular) | Matsunami Glass | 26 x 60mm No.4 | |
| Acetone | Kanto Chemicals | 01060-79 | |
| Glass slides (Large) | Matsunami Glass | 76 x 52mm No.1 | |
| Silicone adhesive | Shin-Etsu Chemicals | KE-41 | |
| White petrolatum | Nikko Rica | Sun White P-1 | |
| Polytetrafluoroethylene (PTFE) powder | Power House Accele | Microfluon II | |
| Clear acrylic plate (3 mm-thick) | Various | N/A | |
| Pneumatic dispenser | Musashi Engineering | ML-5000XII | |
| Hydrochloric acid | Kanto Chemicals | 180768-00 | |
| Computer numerical control (CNC) mill | Pro Spec Tools | PSF240-CNC | |
| End mill (4 mm diameter) | Mitsubishi Materials | MS2MSD0400 | |
| End mill (1 mm diameter) | Mitsubishi Materials | MS2MSD0100 | |
| Adhesive (chemical-resistant and low viscosity ) | Cotronics | Duralco 4460 | |
| Borisilicate glass vials | Various | To prepare HNO3+HCl solution (Aqua regia). Always select borosilicate glass. | |
| Sodium bicarbonate | Kanto Chemicals | 37116-00 | |
| Ultrasonic cleaner | AS ONE | AS12GTU | |
| Ultrasonic drill | Shinoda Tools | SOM-121 | Used as a ultrasonic homogenizer. |
| Spin coater | Active | ACT-220DII | |
| Hotplate | AS ONE | ND-1 | |
| Photoplotted film (12,700 dpi) | Unno Giken | N/A | Negative image of the recess at the bottom of a PDMS slab are plotted. |
| 2-methoxy-1-methylethyl acetate | Wako Chemicals | 130-10505 | |
| UV spot light source | Hamamatsu | L8327 | Ultraviolet source |
| Nitrogen | Various | N/A | |
| Vacuum desiccator and pump | AS ONE | MVD-100, GM-20S | |
| Scalpels | Various | No.11 | |
| Biopsy punches (1.0mm and 2.0mm) | Kai Medical | BP-10F(1.0m), BP-20F(2.0mm) | |
| Glass engraving pen | Various | N/A | |
| Cleaning solution | Tama Chemicals | TMSC | Dilute 1:100 with deionized water |
| Sputter coater | San-yu Electron | SC-708 | For plasma bonding. |
| Dispenser syringe (5 ml) | Musashi Engineering | PSY-5E | |
| Plunger | Musashi Engineering | FLP-5E | |
| Blunt needle (21G) | Musashi Engineering | PN-21G-B | |
| Adapter tube | Musashi Engineering | AT-5E | |
| Fermenter | Japan Kneader | PF100 | |
| Green fluorescent dye (Alexa Fluor 488 carboxylic acid) | Thermo Fisher | A33077 | |
| Large plastic dish | Greiner bio-one | 688161 | |
| Absorbent paper | Asahi Kasei | BEMCOT M-1 | |
| Inverted microscope | Leica | DMi8 | |
| Microscope camera | Qimaging | Retiga 2000R | |
| Dulbecco modified Eagle medium (DMEM) | GE Health Care | SH30021.01 | |
| Antibiotic-antimycotic solution | Thermo Fisher | 15240-062 | |
| Trypsin/EDTA solution | Thermo Fisher | 25200-056 | |
| Phosphate buffered saline (PBS) | GE Health Care | SH30256.01 | |
| Fetal bovine serum (FBS) | Biowest | S1820 | |
| Cell counter | FPI | OC-C-S02 | |
| Cell culture vessel | VIOLAMO | VTC-D100 | |
| 15 ml conical tube | Corning | 352095 | |
| Shop microscope | PEAK | 2034-20 | |
| Hand sprayer | FURUPLA | No.3530 | |
| Coverglasses (Rectangular) | Matsunami Glass | 10 x 20mm No.4 | |
| CAD/CAM software | Autodesk | Inventor HSM | |
| Nitrogen gas pressure regulator | AS ONE | GF1-2506-RN-V | Set to 0.1 MPa |
Riferimenti
- Nge, P. N., Rogers, C. I., Woolley, A. T. Advances in microfluidic materials, functions, integration, and applications. Chem Rev. 113 (4), 2550-2583 (2013).
- Araci, I. E., Brisk, P. Recent developments in microfluidic large scale integration. Curr Opin Biotechnol. 25, 60-68 (2014).
- Gu, W., Chen, H., Tung, Y. -. C., Meiners, J. -. C., Takayama, S. Multiplexed hydraulic valve actuation using ionic liquid filled soft channels and Braille displays. Appl Phys Lett. 90 (3), 033505 (2007).
- Konda, A., Taylor, J. M., Stoller, M. A., Morin, S. A. Reconfigurable microfluidic systems with reversible seals compatible with 2D and 3D surfaces of arbitrary chemical composition. Lab Chip. 15 (9), 2009-2017 (2015).
- Hahn, Y., Hong, D., Kang, J., Choi, S. A Reconfigurable microfluidics platform for microparticle separation and fluid mixing. Micromachines. 7 (8), 139 (2016).
- Kintses, B., van Vliet, L. D., Devenish, S. R. A., Hollfelder, F. Microfluidic droplets: new integrated workflows for biological experiments. Curr Opin Chem Biol. 14 (5), 548-555 (2010).
- Jebrail, M. J., Bartsch, M. S., Patel, K. D. Digital microfluidics: a versatile tool for applications in chemistry, biology and medicine. Lab Chip. 12 (14), 2452-2463 (2012).
- Frey, O., Misun, P. M., Fluri, D. A., Hengstler, J. G., Hierlemann, A. Reconfigurable microfluidic hanging drop network for multi-tissue interaction and analysis. Nat Commun. 5, 4250 (2014).
- Futai, N. Reconfigurable microchannels with discretized moving sidewalls. Chem Micro-Nano Syst. 10 (1), 24-25 (2011).
- Oono, M., et al. Reconfigurable microfluidic device with discretized sidewall. Biomicrofluidics. 11 (3), 034103 (2017).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon