È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
L'analisi genetica di ereditario Transthyretin Ala97Ser relative amiloidosi
In questo articolo
Riepilogo
Qui, presentiamo un protocollo per confermare la presenza di mutazione di punto per la diagnosi di amiloidosi ereditaria da transtiretina, utilizzando Ala97Ser, la mutazione più comune endemica in Taiwan, come esempio.
Abstract
Test genetici è la prova più affidabile per transthyretin ereditario legate amiloidosi e deve essere eseguita nella maggior parte dei casi di amiloidosi da transtiretina (ATTR). ATTR è una malattia rara ma fatale con fenotipi eterogenei; di conseguenza, la diagnosi a volte è in ritardo. Con l'aumento dell'attenzione e riconoscimento più ampio su manifestazioni iniziali di ATTR, nonché trattamenti emergenti, studi diagnostici appropriati, tra cui la transtiretina (TTR) genetica test, per confermare i tipi e varianti di ATTR sono pertanto fondamentale per migliorare la prognosi. Analisi genetiche con metodi di reazione a catena (PCR) polimerasi confermano la presenza di mutazioni puntiformi TTR molto più rapidamente e più sicuro rispetto ai metodi tradizionali come la macchia del sud. Qui, dimostriamo la conferma genetica della mutazione ATTR Ala97Ser, la mutazione più comune endemica in Taiwan. Il protocollo comprende quattro fasi principali: raccolta dei campioni di sangue intero, estrazione del DNA, l'analisi genetica di tutti e quattro gli essoni TTR con PCR e sequenziamento del DNA.
Introduzione
Amiloidosi da transtiretina (TTR) (ATTR) sono la forma più comune di amiloidosi sistemica1e possono essere causato da una mutazione dominante ereditata autosomal in gene transtiretina (TTR)2. Mutazioni di TTR destabilizzano la struttura della proteina tetramerica e portano alla sua dissociazione nei monomeri che ricompone in fibrille amiloidi2. Più di 100 mutazioni di TTR amiloidogeniche sono stati segnalati in tutto il mondo1. Analisi genetiche con metodi di reazione a catena (PCR) polimerasi confermano la presenza di mutazione di punto TTR e presentano vantaggi tra cui evitare la manipolazione della sonda marcata radioattivamente a rispetto del sud della macchia3. PCR è una tecnica veloce, facile, economico e affidabile che è stata applicata in numerosi campi in scienze moderne4.
La diagnosi precoce di questa malattia progressiva e fatale è impegnativa, data la sua eterogeneità fenotipica. Con l'aumento dell'attenzione e riconoscimento più ampio su manifestazioni iniziali di ATTR, nonché i trattamenti emergenti5, studi diagnostici adatti tra cui test genetico TTR sono quindi criticamente fondamentali per migliorare la prognosi. Inoltre, mutazioni differenti sono associate con diversa penetranza del tratto, l'età di esordio, i modelli di progressione, sopravvivenza mediana, la gravità della malattia e l'efficacia di trapianto del fegato, o TTR stabilizzatori2,6, e gradi variabili di coinvolgimento neurologico e cardiologico, che hanno grandi implicazioni per la consulenza genetica7,8,9. Inoltre, un accurato test genetico è l'unico strumento che differenzia i due tipi distinti di ATTR: ereditaria (mutante) e wild type (forma non mutante, amiloidosi sistemica senile, SSA)7. È indispensabile per confermare i tipi di ATTR, perché le terapie variano ampiamente2. Di conseguenza, c'è una crescente necessità di descrivere il protocollo graduale del test genetico TTR.
L'approccio molecolare per rilevare la mutazione sarà illustrato utilizzando Ala97Ser, la mutazione più comune endemica in Taiwan, come esempio. Modifiche in fase di estrazione di DNA ridurre la quantità delle tre soluzioni utilizzate e produce una quantità sufficiente di DNA. In questo protocollo, tutti e quattro gli essoni TTR sono stati analizzati, mentre le regioni tra cui 5' a Monte, 3' a valle, promotori, introni, e regioni non tradotte (UTR) non sono state sequenziate.
Protocollo
I test eseguiti in laboratorio è stato effettuato in conformità con i requisiti della clinica laboratorio miglioramento emendamenti (CLIA) del 1988, il regolamento, approvato dal Consiglio di revisione istituzionale di Chang Gung Memorial Hospital e Università (licenza n. 100 - 4470A3 e 104-2462A3). Consenso informato è stato ottenuto da tutti i pazienti.
1. raccolta di campioni di sangue
- Prelevare il sangue intero in provette EDTA-trattati commercialmente disponibili. Mescolare delicatamente e conservare il campione di sangue a 4 ° C fino al trattamento.
2. DNA estrazione da sangue periferico
Utilizzare un Kit di estrazione del DNA per l'estrazione del DNA genomico (Vedi Tabella materiali).
- Aggiungere 10 mL di soluzione 1 per il campione di sangue di 4,0 mL. Incubare il campione in ghiaccio per 10 min.
- Centrifugare il campione a 2.000 x g per 5 min a 4 ° C. Rimuovere e gettare il surnatante con attenzione. Risospendere il pellet in 3 mL di soluzione 1.
- Centrifugare il campione a 2.000 x g per 5 min a 4 ° C nuovo ed eliminare il surnatante. Risospendere il pellet in 3 mL di soluzione 2.
- Aggiungere 10 µ l di soluzione madre pronase (225 mg/mL) per ottenere una concentrazione finale di 100 µ g/mL e mescolare bene. Incubare a 37 ° C durante la notte.
- Raffreddare il tubo sul ghiaccio per 10 min Aggiungi 0,8 mL di soluzione 3 al campione e capovolgere 3 - 5 volte. Collocare il campione in ghiaccio per 5 min.
- Centrifugare il campione a 3.000 x g per 15 min a 4 ° C. Trasferire con cautela il surnatante in una provetta sterile conica per centrifuga 15 mL.
- 6 µ l di soluzione madre di RNAsi (10 mg/mL) per ottenere una concentrazione finale di 20 µ g/mL. Incubare a 37 ° C per 15 min.
- Aggiungere 2,5 mL di alcool isopropilico e mescolare accuratamente capovolgendo più volte per precipitare il DNA (fili di materiale bianco e fioccoso formerà). Utilizzando una pipetta di grosso calibro, trasferire il precipitante di DNA in una nuova provetta da centrifuga da 1,5 mL.
- Centrifugare a 12.000 x g per 3 min a 4 ° C. Gettare il surnatante con attenzione. Pellet di DNA lavare aggiungendo 500 µ l di etanolo al 70%.
- Centrifugare a 12.000 x g per 1 min ed eliminare il surnatante. Asciugare all'aria a pellet di DNA a temperatura ambiente. Aggiungere 100 µ l di ddH2O e incubare a 65 ° C per 15 min risospendere il DNA.
3. quantificazione del DNA genomica
Utilizzare uno spettrofotometro (Vedi Tabella materiali) per rilevare la quantità e la qualità del DNA genomic.
- Accedere al computer collegato alla macchina spettrofotometro. Aprire il software.
- Inizializzare la macchina spettrofotometro:
- Fare clic su "Acido nucleico" sul software spettrofotometro.
- Pulire il piedistallo con una salvietta USA e getta carta e acqua purificata.
- Lo spettrofotometro in bianco:
- Caricare 2 µ l di acqua purificata sul piedistallo.
- Abbassare il braccio superiore dello spettrofotometro e fare clic su "Vuoto" per calibrarlo.
- Quando è fatto, sollevare il braccio superiore e asciugare il piedistallo con un panno.
- Misura il campione:
- Fare clic su tipo di campione "DNA-50".
- Caricare 2 µ l di campione di DNA sul piedistallo.
- Abbassare il braccio superiore e fare clic su "Misura" per misurare il rapporto A260/A280 e la concentrazione del campione.
- Pulire il piedistallo tra ogni esecuzione con un panno e acqua purificata.
- Fare clic su "Print Screen" per raccogliere i dati.
4. genetiche analisi delle mutazioni
Amplificare il DNA dell'obiettivo con la PCR4. Eseguire PCR in una reazione a 25 µ l miscela utilizzando una DNA polimerasi kit (Vedi Tabella materiali). La tabella 1 Mostra il gene TTR intronic primer.
| gene | Sequenza più superelegante |
| Exon1 | F: 5'-TCAGATTGGCAGGGATAAGC-3' R: 5'-GCAAAGCTGGAAGGAGTCAC-3' |
| Exon2 | F: 5'-TCTTGTTTCGCTCCAGATTTC-3' R: 5'-TCTACCAAGTGAGGGGCAAA-3' |
| Exon3 | F: 5'-GTGTTAGTTGGTGGGGGTGT-3' R: 5'-TGAGTAAAACTGTGCATTTCCTG-3' |
| Exon4 | F: 5'-GACTTCCGGTGGTCAGTCAT-3' R: 5'-GCGTTCTGCCCAGATACTTT-3' |
Tabella 1. Gli iniettori introniche del gene TTR. (Sequenza di Riferimento NCBI: NC_000018.10)
- Aggiungere i reagenti nella tabella 2 in una provetta PCR 0,2 mL.
| Componenti | Volume (µ l) | Concentrazione finale |
| 10 x Buffer | 2.5 | 1 x |
| MgCl2 (25 mM) | 1.5 | 1,5 mM |
| 360 GC Enhancer | 1 | - |
| Polimerasi del DNA 360 | 0.2 | 2 U/reazione |
| dNTP Mix (25 mM) | 2 | 2 mM ogni |
| Primer F (10 µM) | 1 | 0,4 ΜM |
| Primer R (10 µM) | 1 | 0,4 ΜM |
| DNA (100 ng) | 2 | |
| Acqua di PCR-grado | 13,8 | - |
| Volume totale | 25 | - |
Tabella 2. Condizioni di reazione di PCR.
- Mescolare delicatamente e centrifugare brevemente su una centrifuga da banco per raccogliere tutti i componenti alla parte inferiore del tubo. Posizionare il tubo in un termociclatore.
- Eseguire PCR per 30 cicli. Ogni ciclo è costituito da una fase di denaturazione per 30 s a 94 ° C, primer di ricottura per 30 s a 58 ° C e l'estensione della polimerasi per 45 s a 72 ° C (Vedi tabella 3).
| Passo | Temperatura (° C) | Tempo | ciclo |
| Denaturazione iniziale | 95 | 5 min | 1 |
| Denaturazione del DNA | 94 | 30 s | 30 cicli |
| Punto di ricottura di primer | 58 | 30 s | 30 cicli |
| Passaggio di estensione della polimerasi | 72 | 45 s | 30 cicli |
| Passo di allungamento post | 72 | 10 min | 1 |
| Fine della PCR in bicicletta | 4 | Tempo indeterminato |
Tabella 3. Ciclismo condizioni per amplificare i prodotti di PCR.
- Convalidare il prodotto PCR visualizzando con elettroforesi su gel:
- Preparare un gel di agarosio all'1.2%:
- Mescolare 1,2 g di agarosio in polvere con 100 mL di 0.5 x TBE in un fiasco di microwavable. Forno a microonde per 2 minuti fino a quando l'agarosio è completamente sciolto. Raffreddare la miscela di agarosio a 55 ° C.
- Aggiungere 2 µ l di una soluzione di bromuro di etidio (10 mg/mL) alla miscela di agarosio e mescolare delicatamente. Versare il composto di agarosio in un cassetto del gel per circa 5-7 mm, quindi aggiungere il comb(s) luogo. Lasciare solidificare (almeno 30 min) e rimuovere con attenzione comb(s).
- Campioni di caricare ed eseguire un gel dell'agarosi:
- Inserire la cella di elettroforesi su gel e vassoio. Riempire la cella di elettroforesi con 0,5 x TBE fino a quando il gel è coperto.
- Accuratamente caricare 2 µ l di una 100 bp DNA ladder (Vedi Tabella materiali) in una corsia del gel come marcatore molecolare. Miscela di tintura/campione di carico (5 µ l di miscela del prodotto di PCR con 1 µ l 6 x caricamento tintura) nelle corsie aggiuntive.
- Accendere l'alimentazione. Esegua il gel per 25 min a 100 V.
- Rimuovere il gel dalla cella elettroforesi. Visualizzare i frammenti di DNA sotto UV luce in un sistema di imaging.
- Preparare un gel di agarosio all'1.2%:
5. sequenziamento
- Purificare i prodotti di PCR utilizzando un kit commerciale e commercialmente o con un sequenziatore automatico di sequenza (Vedi Tabella materiali).
- Inviare sequenze nucleotidiche al server NCBI BLAST per confrontare la query del nucleotide al nucleotide database10. Dopo i risultati vengono visualizzati, eseguire allineamenti di sequenza e identificare la mutazione prevista.
Risultati
Elettroforesi del gel dell'agarosi di due pazienti e un sano singole bande ha rivelato delle dimensioni previste, tra cui un prodotto PCR di bp 454 per esone 4 del gene TTR (Figura 1).
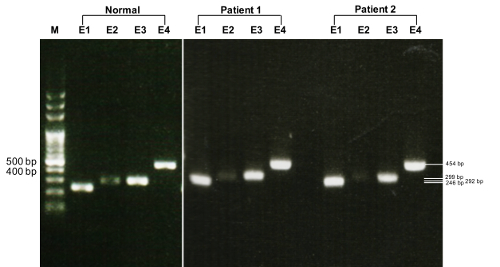
Figura 1 . Elettroforesi del gel raffigurante PCR amplificato gene TTR. Normale: un in...
Discussione
Ci sono due passaggi critici all'interno del protocollo. In primo luogo, al fine di avere un numero sufficiente di cellule bianche del sangue, un esemplare di hemodiluted dovrebbe essere evitato11. In secondo luogo, l'uso appropriati degli iniettori di PCR è fondamentale per ottenere risultati affidabili12. Abbiamo utilizzato lo strumento web di Primer-BLAST per progettare il primer4,13; un minimo di 40 paia di bas...
Divulgazioni
Gli autori non hanno nulla a rivelare.
Riconoscimenti
Desideriamo ringraziare Miss Shin-Fun Wu per il suo aiuto negli esperimenti. Questo studio è stato sostenuto da una sovvenzione dal programma di ricerca medica di Chang Gung (CMRPG3C0371, CMRPG3C0372, CMRPG3C0373) e IRB 100-4470A3, 104-2462A3, Taiwan.
Materiali
| Name | Company | Catalog Number | Comments |
| EDTA-treated tubes | BD | ||
| DNA Extraction Kit | Stratagen | 200600 | |
| NanoDrop ND2000 spectrophotometer | Thermo Fisher Scientific | NanoDrop 2000 | |
| Delicate Task Wipers | Kimberly-Clark | Kimtech Science Kimwipes | |
| AmpliTaq Gold 360 DNA Polymerase kit | Applied Biosystems | 4398823 | |
| TTR gene intronic primers | Exon1 | F: 5’-TCAGATTGGCAGGGATAAGC-3’ | |
| Exon1 | R: 5’-GCAAAGCTGGAAGGAGTCAC-3’ | ||
| Exon2 | F: 5’-TCTTGTTTCGCTCCAGATTTC-3’ | ||
| Exon2 | R: 5’-TCTACCAAGTGAGGGGCAAA-3’ | ||
| Exon3 | F: 5’-GTGTTAGTTGGTGGGGGTGT-3’ | ||
| Exon3 | R: 5’-TGAGTAAAACTGTGCATTTCCTG-3’ | ||
| Exon4 | F: 5’-GACTTCCGGTGGTCAGTCAT-3’ | ||
| Exon4 | R: 5’-GCGTTCTGCCCAGATACTTT-3’ | ||
| thermocycler | Applied Biosystems | GeneAmp PCR System 9700 | |
| electrophoresis cell | ADVANCE | Mupid-2plus | |
| DNA ladder | Protech | PT-M1-100 | |
| dye | BioLabs | B7021 | |
| AlphaImager EC | Alpha Innotech | AlphaImager EC | |
| automatic sequencer | Applied Biosystems | 3730xl DNA Analyzer |
Riferimenti
- Planté-Bordeneuve, V., Said, G. Familial amyloid polyneuropathy. The Lancet Neurology. 10 (12), 1086-1097 (2011).
- Planté-Bordeneuve, V., et al. Long-term treatment of transthyretin familial amyloid polyneuropathy with tafamidis: a clinical and neurophysiological study. Journal of Neurology. 264 (2), 268-276 (2017).
- Nichols, W. C., Benson, M. D. Hereditary amyloidosis: detection of variant prealbumin genes by restriction enzyme analysis of amplified genomic DNA sequences. Clinical Genetics. 37 (1), 44-53 (1990).
- Lorenz, T. C. Polymerase Chain Reaction: Basic Protocol Plus Troubleshooting and Optimization Strategies. Journal of Visualized Experiments. (63), e3998 (2012).
- Hsu, H. C., et al. Phenotypic expressions of hereditary Transthyretin Ala97Ser related Amyloidosis (ATTR) in Taiwanese. BMC Neurology. 17 (1), 178 (2017).
- Barroso, F. A., et al. Long-term safety and efficacy of tafamidis for the treatment of hereditary transthyretin amyloid polyneuropathy: results up to 6 years. Amyloid. 24 (3), 194-204 (2017).
- Rapezzi, C., et al. Disease profile and differential diagnosis of hereditary transthyretin-related amyloidosis with exclusively cardiac phenotype: an Italian perspective. European Heart Journal. 34 (7), 520-528 (2013).
- Mariani, L. L., et al. Genotype-phenotype correlation and course of transthyretin familial amyloid polyneuropathies in France. Annals of Neurology. 78 (6), 901-916 (2015).
- Hammarström, P., Jiang, X., Hurshman, A. R., Powers, E. T., Kelly, J. W. Sequence-dependent denaturation energetics: A major determinant in amyloid disease diversity. Proceedings of the National Academy of Sciences of the United States of America. 99, 16427-16432 (2002).
- Johnson, M., Zaretskaya, I., Raytselis, Y., Merezhuk, Y., McGinnis, S., Madden, T. L. NCBI BLAST: a better web interface. Nucleic Acids Research. 36, 5-9 (2008).
- Fox, A. J., et al. Next generation sequencing for the detection of actionable mutations in solid and liquid tumors. Journal of Visualized Experiments. (115), (2016).
- Date, Y., Nakazato, M., Kangawa, K., Shirieda, K., Fujimoto, T., Matsukura, S. Detection of three transthyretin gene mutations in familial amyloidotic polyneuropathy by analysis of DNA extracted from formalin-fixed and paraffin-embedded tissues. Journal of the Neurological Sciences. 150 (2), 143-148 (1997).
- Ye, J., Coulouris, G., Zaretskaya, I., Cutcutache, I., Rozen, S., Madden, T. L. Primer-BLAST: a tool to design target-specific primers for polymerase chain reaction. BMC Bioinformatics. 13, 134 (2012).
- Green, M. R., Sambrook, J. . Molecular cloning: A laboratory manual. , (2012).
- Buckingham, L., Flaws, M. L. . Molecular diagnostics: Fundamentals, methods, and clinical applications. , (2012).
- Tan, S. C., Yiap, B. C. DNA, RNA, and Protein Extraction: The Past and The Present. Journal of Biomedicine and Biotechnology. 2009, (2009).
- Rapezzi, C., et al. Systemic cardiac amyloidoses: disease profiles and clinical courses of the 3 main types. Circulation. 120 (13), 1203-1212 (2009).
- Gertz, M. A., Dispenzieri, A., Sher, T. Pathophysiology and treatment of cardiac amyloidosis. Nature Reviews Cardiology. 12 (2), 91-102 (2015).
- Vrana, J. A., et al. Clinical diagnosis and typing of systemic amyloidosis in subcutaneous fat aspirates by mass spectrometry-based proteomics. Haematologica. 99 (7), 1239-1247 (2014).
- Nakamura, M., et al. Identification of a new transthyretin variant (Ile49) in familial amyloidotic polyneuropathy using electrospray ionization mass spectrometry and nonisotopic RNase cleavage assay. Human Heredity. 49 (4), 186-189 (1999).
- Ueda, M., Ando, Y. Recent advances in transthyretin amyloidosis therapy. Translational Neurodegeneration. 3, 19 (2014).
- Brown, E. E., et al. Genetic testing improves identification of transthyretin amyloid (ATTR) subtype in cardiac amyloidosis. Amyloid. 24 (2), 92-95 (2017).
- Tasaki, M., et al. Rapid detection of wild-type and mutated transthyretins. Annals of Clinical Biochemistry. 53 (4), 508-510 (2015).
- Plante-Bordeneuve, V., et al. Diagnostic pitfalls in sporadic transthyretin familial amyloid polyneuropathy (TTR-FAP). Neurology. 69 (7), 693-698 (2007).
- Hsu, J. L., et al. A prospective, observational study of patients with uncommon distal symmetric painful small-fiber neuropathy. PLoS ONE. 12 (9), 0183948 (2017).
- Salvi, F., Pastorelli, F., Plasmati, R., Bartolomei, I., Dall'Osso, D., Rapezzi, C. Genotypic and phenotypic correlation in an Italian population of hereditary amyloidosis TTR-related (HA-TTR): Clinical and neurophysiological aids to diagnosis and some reflections on misdiagnosis. Amyloid. 19, 58-60 (2012).
- Suhr, O. B., Lundgren, E., Westermark, P. One mutation, two distinct disease variants: Unravelling the impact of transthyretin amyloid fibril composition. Journal of Internal Medicine. 281 (4), 337-347 (2017).
- Vilà-Rico, M., et al. Quantitative analysis of post-translational modifications in human serum transthyretin associated with familial amyloidotic polyneuropathy by targeted LC-MS and intact protein MS. Journal of Proteomics. 127, 234-246 (2015).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon