È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Stimolazione combinata dei nervi periferici e dei parametri di impulso controllabili Stimolazione magnetica transcranica per sondare il controllo e l'apprendimento sensomotorio
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
L'inibizione afferente a breve latenza (SAI) è un protocollo di stimolazione magnetica transcranica per sondare l'integrazione sensomotoria. Questo articolo descrive come SAI può essere utilizzato per studiare i circuiti sensomotori convergenti nella corteccia motoria durante il comportamento sensomotorio.
Abstract
L'abilità motoria qualificata dipende dall'integrazione efficiente dell'afferenza sensoriale nei comandi motori appropriati. L'inibizione afferente fornisce un valido strumento per sondare l'influenza procedurale e dichiarativa sull'integrazione sensomotoria durante azioni motorie qualificate. Questo manoscritto descrive la metodologia e i contributi dell'inibizione afferente a breve latenza (SAI) per comprendere l'integrazione sensomotoria. SAI quantifica l'effetto di una raffica afferente convergente sulla gittata motoria corticospinale evocata dalla stimolazione magnetica transcranica (TMS). La raffica afferente è innescata dalla stimolazione elettrica di un nervo periferico. Lo stimolo TMS viene consegnato a una posizione sopra la corteccia motoria primaria che suscita una risposta motoria affidabile in un muscolo servito da quel nervo afferente. L'entità dell'inibizione nella risposta motoria evocata riflette l'entità della raffica afferente convergente sulla corteccia motoria e coinvolge i contributi GABAergici e colinergici centrali. Il coinvolgimento colinergico nella SAI rende la SAI un possibile marker delle interazioni dichiarativo-procedurali nelle prestazioni sensomotorie e nell'apprendimento. Più recentemente, gli studi hanno iniziato a manipolare la direzione della corrente TMS in SAI per distinguere il significato funzionale di distinti circuiti sensomotori nella corteccia motoria primaria per azioni motorie qualificate. La capacità di controllare parametri di impulso aggiuntivi (ad esempio, la larghezza dell'impulso) con TMS (cTMS) con parametri di impulso controllabili all'avanguardia (cTMS) ha migliorato la selettività dei circuiti sensomotori sondati dallo stimolo TMS e ha fornito l'opportunità di creare modelli più raffinati di controllo e apprendimento sensomotorio. Pertanto, l'attuale manoscritto si concentra sulla valutazione SAI utilizzando cTMS. Tuttavia, i principi qui delineati si applicano anche alle SAI valutate utilizzando stimolatori TMS convenzionali a larghezza di impulso fissa e altre forme di inibizione afferente, come l'inibizione afferente a lunga latenza (LAI).
Introduzione
Più circuiti sensomotori convergono nella corteccia motoria per modellare le proiezioni del tratto piramidale ai motoneuroni e agli interneuroni spinali1. Tuttavia, come questi loop sensomotori interagiscono per modellare le proiezioni corticospinali e il comportamento motorio rimane una questione aperta. L'inibizione afferente a breve latenza (SAI) fornisce uno strumento per sondare le proprietà funzionali dei circuiti sensorimotori convergenti nell'output della corteccia motoria. SAI combina la stimolazione magnetica transcranica corticale motoria (TMS) con la stimolazione elettrica del corrispondente nervo afferente periferico.
La TMS è un metodo non invasivo per stimolare in modo sicuro i motoneuroni piramidali trans-sinapticamente nel cervello umano 2,3. TMS comporta il passaggio di una grande corrente elettrica transitoria attraverso un filo arrotolato posto sul cuoio capelluto. La natura transitoria della corrente elettrica crea un campo magnetico in rapida evoluzione che induce una corrente elettrica nel cervello4. Nel caso di un singolo stimolo TMS, la corrente indotta attiva una serie di input eccitatori ai motoneuroni piramidali 5-7. Se la forza degli input eccitatori generati è sufficiente, l'attività discendente suscita una risposta muscolare controlaterale nota come potenziale evocato dal motore (MEP). La latenza del MEP riflette il tempo di conduzione corticomotoria8. L'ampiezza del MEP indicizza l'eccitabilità dei neuroni corticospinali9. Il singolo stimolo TMS che suscita il MEP può anche essere preceduto da uno stimolo condizionante10,11,12. Questi paradigmi a impulsi accoppiati possono essere utilizzati per indicizzare gli effetti di vari pool di interneuroni sulla gittata corticospinale. Nel caso di SAI, lo stimolo di condizionamento elettrico periferico viene utilizzato per sondare l'impatto della raffica afferente sull'eccitabilità corticale motoria11,13,14,15. La tempistica relativa dello stimolo TMS e della stimolazione elettrica periferica allinea l'azione dello stimolo TMS sulla corteccia motoria con l'arrivo delle proiezioni afferenti alla corteccia motoria. Per SAI nei muscoli distali degli arti superiori, lo stimolo nervoso mediano precede tipicamente lo stimolo TMS di 18-24 ms11,13,15,16. Allo stesso tempo, la SAI aumenta all'aumentare della forza della raffica afferente indotta dallo stimolo periferico 13,17,18.
Nonostante la sua forte associazione con le proprietà estrinseche della proiezione afferente alla corteccia motoria, SAI è un fenomeno malleabile implicato in molti processi di controllo motorio. Ad esempio, la SAI è ridotta nei muscoli rilevanti per il compito prima di un movimento imminente 19,20,21 ma viene mantenuta nelle rappresentazioni motorie adiacenti irrilevanti del compito19,20,22. Si ipotizza che la sensibilità alla pertinenza del compito rifletta un meccanismo di inibizione surround23 che mira a ridurre il reclutamento di effettori indesiderati. Più recentemente, è stato proposto che la riduzione della SAI nell'effettore rilevante per il compito possa riflettere un fenomeno di gating correlato al movimento progettato per sopprimere l'afferenza sensoriale attesa21 e facilitare le correzioni durante la pianificazione e l'esecuzione sensomotoria24. Indipendentemente dal ruolo funzionale specifico, la SAI è correlata alla riduzione della destrezza manuale e dell'efficienza di elaborazione25. La SAI alterata è anche associata ad un aumentato rischio di caduta negli anziani 26 e alla compromissione della funzione sensomotoria nella malattia di Parkinson 26,27,28 e negli individui con distonia focale della mano 29.
Evidenze cliniche e farmacologiche indicano che le vie inibitorie che mediano la SAI sono sensibili alla modulazione colinergica centrale30. Ad esempio, la somministrazione dell'antagonista del recettore muscarinico dell'acetilcolina scopolamina riduce SAI31. Al contrario, aumentando l'emivita dell'acetilcolina tramite inibitori dell'acetilcolinesterasi aumenta SAI32,33. Coerentemente con l'evidenza farmacologica, SAI è sensibile a diversi processi cognitivi con coinvolgimento colinergico centrale, tra cui l'eccitazione 34, la ricompensa35, l'allocazione dell'attenzione 21,36,37 e la memoria38,39,40. La SAI è anche alterata nelle popolazioni cliniche con deficit cognitivi associati alla perdita di neuroni colinergici, come il morbo di Alzheimer 41,42,43,44,45,46,47, il morbo di Parkinson (con decadimento cognitivo lieve)48,49,50 e il decadimento cognitivo lieve 47,51,52. La modulazione differenziale di SAI da parte di varie benzodiazepine con affinità differenziali per vari tipi di subunità del recettore dell'acido γ-aminobutirrico di tipo A (GABAA) suggerisce che le vie inibitorie SAI sono distinte dalle vie che mediano altre forme di inibizione dell'impulso accoppiato30. Ad esempio, il lorazepam diminuisce la SAI ma migliora l'inibizione corticale a breve intervallo (SICI)53. Zolpidem riduce la SAI ma ha scarso effetto su SICI53. Il diazepam aumenta la SICI ma ha un impatto minimo su SAI53. La riduzione della SAI da parte di questi modulatori allosterici positivi della funzione del recettore GABAA, unita all'osservazione che il GABA controlla il rilascio di acetilcolina nel tronco cerebrale e nella corteccia54, ha portato all'ipotesi che il GABA modula la via colinergica che proietta alla corteccia sensomotoria per influenzare SAI55.
Recentemente, SAI è stato utilizzato per studiare le interazioni tra i cicli sensomotori che impostano i processi di controllo motorio procedurale e quelli che allineano i processi procedurali agli obiettivi espliciti dall'alto verso il basso e ai processi di controllo cognitivo 21,36,37,38. Il coinvolgimento colinergico centrale nella SAI31 suggerisce che la SAI può indicizzare un'influenza esecutiva sul controllo sensomotorio procedurale e sull'apprendimento. È importante sottolineare che questi studi hanno iniziato a identificare gli effetti unici della cognizione su specifici circuiti sensomotori valutando SAI utilizzando diverse direzioni di corrente TMS. Gli studi SAI impiegano tipicamente corrente indotta posteriore-anteriore (PA), mentre solo una manciata di studi SAI ha impiegato corrente indotta antero-posteriore (AP)55. Tuttavia, l'uso di TMS per indurre AP rispetto alla corrente PA durante la valutazione SAI recluta circuiti sensomotori distinti16,56. Ad esempio, i circuiti sensomotori AP-sensibile, ma non PA-sensibile, sono alterati dalla modulazione cerebellare37,56. Inoltre, i circuiti sensomotori AP-sensibile, ma non PA-sensibile, sono modulati dal carico di attenzione36. Infine, l'attenzione e le influenze cerebellari possono convergere sugli stessi circuiti sensomotori AP-sensibili, portando ad alterazioni disadattive in questi circuiti37.
I progressi nella tecnologia TMS offrono ulteriore flessibilità per manipolare la configurazione dello stimolo TMS impiegato durante applicazioni a impulso singolo, a impulsi accoppiati e ripetitive57,58. Gli stimolatori TMS a parametri di impulso controllabili (cTMS) sono ora disponibili in commercio per uso di ricerca in tutto il mondo e forniscono un controllo flessibile sulla larghezza e sulla forma dell'impulso57. La maggiore flessibilità deriva dal controllo della durata di scarica di due condensatori indipendenti, ciascuno responsabile di una fase separata dello stimolo TMS. La natura bifasica o monofasica dello stimolo è governata dall'ampiezza di scarica relativa da ciascun condensatore, un parametro chiamato rapporto M. Gli studi cTMS hanno combinato la manipolazione della larghezza dell'impulso con diverse direzioni di corrente per dimostrare che le larghezze di impulso fisse utilizzate dagli stimolatori TMS convenzionali (70-82 μs)59,60 probabilmente reclutano un mix di circuiti sensorimotori funzionalmente distinti durante SAI 56. Pertanto, la cTMS è uno strumento interessante per districare ulteriormente il significato funzionale di vari cicli sensomotori convergenti nelle prestazioni sensomotorie e nell'apprendimento.
Questo manoscritto descrive un approccio SAI unico allo studio dell'integrazione sensomotoria che integra la stimolazione elettrica periferica con la cTMS durante i comportamenti sensomotori. Questo approccio migliora il tipico approccio SAI valutando l'effetto delle proiezioni afferenti su popolazioni di interneuroni selezionati nella corteccia motoria che governano la produzione corticospinale durante il comportamento sensomotorio in corso. Sebbene relativamente nuova, la cTMS offre un netto vantaggio nello studio dell'integrazione sensomotoria in popolazioni tipiche e cliniche. Inoltre, l'approccio attuale può essere facilmente adattato per l'uso con stimolatori TMS convenzionali e per quantificare altre forme di inibizione e facilitazione afferente, come l'inibizione afferente a lunga latenza (LAI)13 o la facilitazione afferente a breve latenza (SAF)15.
Protocollo
Il seguente protocollo può essere applicato a vari esperimenti. Le informazioni fornite descrivono un esperimento in cui SAI viene utilizzato per quantificare l'integrazione sensomotoria durante una risposta del dito a una sonda validamente o non validamente segnalata. In questo protocollo, la SAI viene valutata senza un compito, quindi contemporaneamente durante il compito sensomotorio e poi di nuovo senza un compito. Lo stimolatore cTMS può essere sostituito da qualsiasi stimolatore TMS convenzionale disponibile in commercio. Tuttavia, la larghezza dell'impulso dello stimolatore TMS convenzionale sarebbe fissata tra 70-82 μs a seconda dell'hardware specifico59,60. Questo studio è stato approvato dall'Office of Research Ethics dell'Università di Waterloo. Tutti i partecipanti hanno fornito il consenso informato scritto.
1. Requisiti hardware/software
NOTA: La Figura 1 mostra uno schema dei requisiti hardware per integrare gli stimolatori elettrici e TMS periferici con un compito sensomotorio controllato dal computer. La Figura 2A illustra la configurazione per SAI per la corrente indotta da PA e AP. La figura 2B illustra la sequenza di eventi per il compito sensomotorio e la tempistica relativa della valutazione SAI. Un sistema di guida stereotassica per tracciare l'orientamento della bobina TMS rispetto al partecipante è fortemente raccomandato per ridurre la variabilità prova per prova nella risposta fisiologica associata alla variazione della posizione della bobina e della traiettoria61.
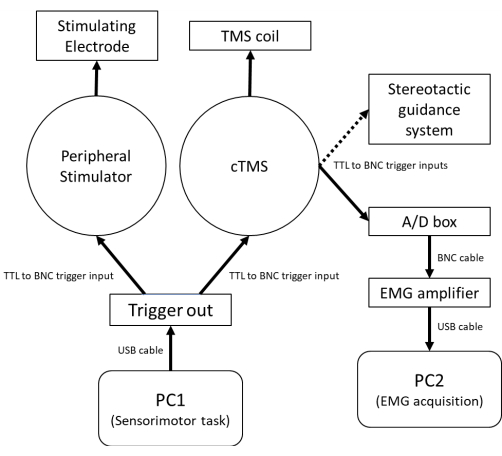
Figura 1: Uno schema dell'hardware utilizzato per valutare SAI a riposo e durante il comportamento sensomotorio concorrente. PC1, che viene utilizzato per controllare il compito sensomotorio e la temporizzazione dello stimolo cTMS / stimolazione elettrica periferica, è collegato a un convertitore digitale-analogico in grado di generare un trigger di uscita TTL da 5 V tramite un cavo USB. Per le prove incondizionate, il trigger dal canale digitale input-output 1 viene inviato allo stimolatore cTMS tramite un cavo BNC. Per le prove condizionate, il trigger dal canale digitale input-output 1, che viene inviato allo stimolatore cTMS, è preceduto da un trigger dal canale digitale input-output 2 allo stimolatore elettrico periferico. Un cavo BNC dal canale di uscita trigger sull'unità cTMS viene inviato alla scheda analogico-digitale del sistema EMG per attivare la registrazione dell'amplificatore EMG e la visualizzazione/salvataggio dei dati da parte del software di acquisizione EMG su PC2. Un cavo BNC opzionale dal trigger out cTMS viene inoltre inviato al sistema di guida stereotassica per registrare la posizione e la traiettoria della bobina al momento dello stimolo cTMS. Abbreviazioni: PC = personal computer; USB = bus seriale universale; TTL = cavo di trigger logico transistor-transistor; BNC = connettore Neill-Concelman a baionetta; cTMS = stimolatore magnetico transcranico controllabile con parametro di impulso; TMS = stimolazione magnetica transcranica; A/D = analogico-digitale; EMG = elettromiografia. Fare clic qui per visualizzare una versione ingrandita di questa figura.
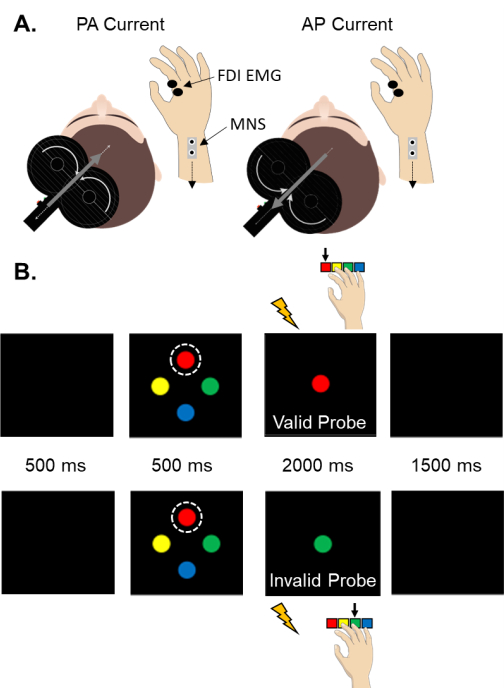
Figura 2: Configurazione della SAI e compito sensomotorio. (A) Uno schema della configurazione per la valutazione della SAI nel muscolo IDE. Da notare, la corrente indotta nel cervello è opposta alla direzione della corrente nella bobina TMS. (B) Una rappresentazione di una prova valida di stecca del dito indice (in alto) e di una prova di stecca del dito indice non valida (in basso). Il segnale è sempre rappresentato come lo stimolo superiore (evidenziato dal cerchio tratteggiato). Il colore del segnale corrisponde a una risposta specifica del dito. I partecipanti sono stati istruiti a rispondere al colore della sonda nel modo più veloce e preciso possibile. I segnali e le sonde potrebbero essere di qualsiasi colore. La probabilità di un segnale valido era del 70%. Segnali non validi si sono verificati nel 30% degli studi. Abbreviazioni: SAI = inibizione afferente a breve latenza; PA = posteriore-anteriore; AP = antero-posteriore; FDI = prima dorsale interossea; EMG = elettromiografia; MNS = stimolo nervoso mediano. Fare clic qui per visualizzare una versione ingrandita di questa figura.
- Dotare un personal computer (PC1) di un software per controllare il compito sensomotorio tramite una scheda digitale-analogica USB (o porta seriale) con due canali di uscita digitali.
- Impostare una routine software senza attività per controllare l'ordine degli stimoli cTMS incondizionati e degli stimoli cTMS che saranno condizionati dalla stimolazione elettrica periferica con un intervallo di interstimolo (ISI) di 21 ms. Randomizzare l'intervallo tra due stimoli qualsiasi (ad esempio, condizionati o incondizionati) utilizzando una distribuzione rettangolare con una durata compresa tra 5-8 s.
- Assicurarsi che la routine invii un trigger di uscita digitale al trigger nella porta dell'unità cTMS per gli stimoli incondizionati. Assicurarsi che la routine invii uscite digitali separate all'unità cTMS e allo stimolatore elettrico periferico per gli stimoli condizionati.
- Assicurarsi che il trigger dello stimolatore periferico precede il trigger cTMS di 21 ms. Assicurarsi che il numero di stimoli incondizionati e condizionati sia compreso tra 8 e 24. Idealmente, l'ordine degli studi incondizionati e condizionati dovrebbe essere randomizzato.
- Impostare una routine software per controllare il compito sensomotorio. Assicurati che questo software blocchi anche i trigger di uscita digitale inviati al cTMS e agli stimolatori elettrici periferici in uno o più punti specifici durante il comportamento.
NOTA: L'esperimento delineato ha utilizzato un compito sensomotorio (Figura 2B). I trigger dello stimolatore periferico e dello stimolatore cTMS sono stati programmati per verificarsi 225-275 ms dopo l'inizio del segnale di risposta utilizzando una distribuzione rettangolare. Lo scopo di questa tempistica era valutare i cambiamenti nell'integrazione sensomotoria in base alla validità tra il segnale di risposta e il segnale di preparazione precedente, che era valido nel 70% di tutti gli studi. - Equipaggiare un secondo personal computer (PC2) con un amplificatore elettromiografico (EMG) a due canali collegato a un convertitore analogico-digitale. Assicurarsi che il convertitore digitale-analogico disponga di un canale di ingresso digitale per bloccare l'EMG allo stimolo TMS. Assicurarsi che PC2 sia dotato di software di acquisizione dati EMG per registrare le risposte muscolari evocate dalla TMS.
NOTA: PC1 può essere utilizzato per controllare il compito sensomotorio e registrare l'EMG. Tuttavia, i ricercatori dovrebbero verificare in modo indipendente la tempistica dei trigger dello stimolatore TMS, dello stimolatore periferico e del sistema EMG. Più dispositivi collegati a un singolo PC aumentano il rischio di conflitti tra processori centrali, con conseguente instabilità nella temporizzazione relativa dei marcatori di evento. - Impostare il software di acquisizione dati EMG con le seguenti impostazioni: tre canali di registrazione, 2 EMG, un trigger di ingresso, registrazioni attivate con un'epoca compresa tra -0,3 s e 0,5 s attorno al trigger TTL, un fattore di amplificazione EMG di 1.000x, una frequenza di campionamento di 4.000 Hz, un filtro passa banda da 3 Hz a 1 kHz e un filtro di rete (opzionale).
NOTA: il protocollo corrente utilizza un metodo di registrazione epocale. Il software di acquisizione EMG monitora continuamente il segnale EMG. Tuttavia, vengono visualizzati e registrati solo i dati epocali bloccati nel tempo allo stimolo TMS. - Collegare un canale di uscita digitale da PC1 all'ingresso trigger sullo stimolatore cTMS. Collegare il secondo canale di uscita digitale da PC1 all'ingresso trigger sullo stimolatore elettrico periferico. Quando si utilizza il sistema operativo del PC, confermare in modo indipendente la tempistica relativa delle due uscite digitali da PC1.
- Collegare l'uscita del trigger all'ingresso digitale del sistema EMG. Se si utilizza un sistema di guida stereotassico, potrebbe essere possibile suddividere l'uscita del trigger al sistema di guida per registrare la prova per posizione di prova della bobina cTMS al momento dello stimolo cTMS.
2. Screening dei partecipanti e consenso informato
- Controllare il partecipante per controindicazioni a TMS 9,62,63,64,65.
- Informare il partecipante sugli obiettivi e le procedure dello studio. Esaminare i rischi delineati nel documento di consenso approvato dal comitato di revisione etica dell'istituzione. Rispondi a qualsiasi domanda sui potenziali rischi. Ottenere il consenso informato scritto prima di iniziare qualsiasi procedura di studio.
3. Posizionamento dell'elettrodolo elettromiografico (EMG)
- Istruire il partecipante a sedersi sulla sedia sperimentale con i gomiti appoggiati sulle braccia della sedia e piegati per consentire al polso / mano di appoggiarsi comodamente sullo spazio di lavoro della scrivania. Regolare l'altezza dell'area di lavoro della sedia e della scrivania in base alle esigenze.
- Pulire la pelle sopra il primo interosseo dorsale (FDI), abductor pollicis brevis (APB) e il processo stiloideo ulnare utilizzando una crema leggermente abrasiva posta su un batuffolo di cotone rotondo. Rimuovere i residui utilizzando un tampone per la preparazione dell'alcool.
- Per ogni muscolo, posizionare un elettrodo adesivo monouso Ag-AgCl sulla pancia muscolare. Posizionare un secondo elettrodo su un punto di riferimento osseo nelle vicinanze. Infine, posizionare un elettrodo adesivo Ag-AgCl aggiuntivo sul processo stiloide ulnare per fungere da terra.
NOTA: Un sito di riferimento comune per gli IDE è la prominenza ossea alla base della seconda falange prossimale sul lato radiale della mano. Un sito di riferimento APB comune è la prominenza ossea della falange prossimale sul lato radiale del pollice. - Collegare ogni coppia di elettrodi e la massa all'amplificatore EMG e al sistema di acquisizione dati. Utilizzare il canale 1 per gli IDE e il canale 2 per l'APB.
4. Posizionamento dell'elettrodo dello stimolatore elettrico periferico
- Collegare il trigger di uscita digitale dello stimolatore periferico al canale di ingresso del trigger sul sistema EMG per attivare la registrazione EMG quando viene erogato lo stimolo periferico.
- Utilizzare una crema leggermente abrasiva per pulire la pelle all'interno dell'avambraccio. Inizia dalla piega di flessione del polso ed estendi fino a ~ 6 cm prossimale. Estendere la pulizia alla zona a partire dalla linea mediana del polso fino al lato radiale dell'avambraccio. Rimuovere eventuali residui utilizzando un tampone per la preparazione dell'alcool.
- Applicare il gel conduttore su un elettrodo a barra stimolante riutilizzabile. Utilizzare quanto basta gel per coprire i dischi metallici dei punti di contatto anodico e catodico. Posizionare l'elettrodo stimolante sulla pelle sul lato palmare del polso con il catodo prossimale all'anodo. Posizionare il catodo leggermente mediale e prossimale al processo stiloideo radiale.
- Non usare gel eccessivo. Se il gel crea un ponte tra i terminali dell'anodo e del catodo, pulire l'elettrodo per rimuovere tutto il gel e riapplicarlo. Un ponte in gel tra l'anodo e il catodo devierà correnti sostanziali lungo la pelle, rendendo difficile stimolare il nervo mediano.
- Sullo stimolatore periferico, impostare il selettore del tipo di stimolo su monofasico, impostare la durata dello stimolo su 200 μs e selezionare una tensione e un amperaggio appropriati, ricontrollando eventuali fattori di moltiplicazione. La tensione (Vmax) è stata impostata a 200 V per l'hardware utilizzato qui, con un amperaggio iniziale di 0,05 x 10 mA.
- Mentre si tiene l'elettrodo stimolante, fornire un singolo stimolo elettrico premendo l'interruttore di attivazione sullo stimolatore a corrente costante. Quindi, ispezionare visivamente il muscolo APB e il display EMG (canale 2) per la prova di una contrazione muscolare. La contrazione muscolare, nota come onda M, è provocata dall'attivazione diretta dell'assone motorio da parte dello stimolo elettrico e dovrebbe verificarsi tra 6-9 ms dopo l'artefatto dello stimolo elettrico periferico.
- Se non ci sono prove di una contrazione muscolare, chiedi al partecipante se ha sentito una sensazione di formicolio irradiarsi verso le dita o immediatamente sotto l'elettrodo. La posizione ottimale sarà la posizione dell'elettrodo che provoca la contrazione muscolare APB più significativa all'intensità dello stimolo corrente.
- Se non viene segnalata alcuna sensazione o la sensazione è limitata alla pelle immediatamente sotto l'elettrodo, aumentare l'amperaggio con incrementi di 0,05 (moltiplicato per un fattore 10) fino a quando il partecipante riferisce una sensazione di formicolio che si irradia fino alle dita / pollice. Se viene riportata una sensazione radiante in una cifra diversa dal pollice, riposizionare l'elettrodo spostando l'elettrodo radialmente fino a quando la sensazione si irradia al pollice.
- Una volta determinata la posizione ottimale dell'elettrodo stimolante, fissare l'elettrodo al polso con tre pezzi di nastro adesivo. Posizionare il primo pezzo sopra il centro dell'elettrodo, quindi utilizzare il secondo e il terzo pezzo per fissare la parte superiore e inferiore dell'elettrodo.
NOTA: In base all'esperienza, si consiglia di fissare prima la banda di nastro sul retro dell'elettrodo e quindi far scorrere il nastro lungo il lato dell'elettrodo fino alla pelle. Questo approccio sembra proteggere l'elettrodo e minimizzare il potenziale di movimento laterale durante l'esperimento. - Dopo aver fissato l'elettrodo, chiedere al partecipante di assumere l'orientamento desiderato degli arti da utilizzare durante la stimolazione TMS. Controlla che sia ancora presente una contrazione del pollice.
5. Determinazione dell'intensità dello stimolo nervoso mediano
- Determinare la soglia dello stimolo periferico regolando l'amperaggio dell'intensità dello stimolo periferico fino a suscitare un'onda M di 0,2 mV37,56. Se l'onda M supera l'ampiezza target desiderata di 0,2 mV su tre stimoli successivi, diminuire l'amperaggio. Se l'onda M è inferiore all'ampiezza target desiderata di 0,2 mV su tre stimoli successivi, aumentare l'amperaggio. La soglia è il primo valore di amperaggio in cui l'onda M supera 0,2 mV.
NOTA: Un'alternativa comune è impostare l'intensità a 3x la soglia sensoriale percettiva o 1x la soglia motoria 11,16,17,66,67,68. La soglia sensoriale è l'intensità dello stimolo alla quale i partecipanti riportano correttamente una sensazione su 5 su 10 stimoli elettrici. La soglia motoria è l'intensità dello stimolo alla quale viene suscitata una contrazione visibile su 5 stimoli su 10.
6. Determinazione della traiettoria ottimale della bobina per la stimolazione magnetica transcranica
- Utilizzare un file di immagine di risonanza magnetica (MRI) modello per creare un nuovo file di progetto del sistema di guida stereotassica per monitorare la posizione del partecipante e l'orientamento della bobina. Quindi, collegare il trigger di uscita digitale dallo stimolatore TMS al canale di ingresso del trigger sul sistema EMG per attivare la registrazione EMG quando viene erogato lo stimolo TMS.
NOTA: Quando disponibile, può essere utilizzata una risonanza magnetica specifica per soggetto. Tuttavia, il MEP è sufficiente per determinare la posizione ottimale della bobina per gli studi di stimolazione della corteccia motoria. - Applicare lo strumento di tracciamento della bobina del sistema di guida alla bobina TMS PA. Utilizzare lo strumento di calibrazione della bobina per calibrare l'orientamento dello strumento di tracciamento della bobina rispetto al punto medio della bobina TMS. Ripetere questo passaggio utilizzando un secondo strumento di tracciamento della bobina per una bobina AP con geometria identica alla bobina PA.
- Applicare lo strumento di tracciamento del soggetto del sistema di guida sulla fronte del partecipante utilizzando due elettrodi EMG. Utilizzare un pennarello a secco a punta fine o un applicatore eye-liner per posizionare i segni al centro della punta del naso, della nasion e delle fosse preauricolari sinistra e destra. Utilizza lo strumento di calibrazione del soggetto del sistema di guida per toccare e registrare la posizione di ciascun marcatore.
- Impostare una posizione iniziale della bobina posizionando la bobina sulla testa del partecipante e registrando la traiettoria della bobina. Assicurarsi che la superficie centrale della bobina sia tangenziale al cuoio capelluto. Allineare la linea mediana della bobina a 45° rispetto al piano medio sagittale della testa del partecipante.
- Per ottenere un'approssimazione iniziale dell'hotspot della corteccia motoria, immagina una linea tangenziale che collega un punto 5 cm anteriore al vertice e 5 cm laterale al vertice e posiziona una bobina di 70 mm a circa 2 cm dal punto anteriore lungo la linea tangenziale.
NOTA: Un approccio alternativo per approssimare l'hotspot motorio corticale per i muscoli distali della mano controlaterale è che lo sperimentatore posizioni il dito indice sinistro (se stimola la corteccia motoria sinistra del partecipante) sul vertice della testa e il pollice della mano sinistra sul punto preauricolare dell'orecchio sinistro. La posizione dell'articolazione metacarpo-falangea del dito indice può essere utilizzata per visualizzare una posizione approssimativa in cui posizionare il centro della bobina.
- Per ottenere un'approssimazione iniziale dell'hotspot della corteccia motoria, immagina una linea tangenziale che collega un punto 5 cm anteriore al vertice e 5 cm laterale al vertice e posiziona una bobina di 70 mm a circa 2 cm dal punto anteriore lungo la linea tangenziale.
- Sullo stimolatore cTMS, impostare il selettore del tipo di impulso su Monofasico-positivo per indurre una corrente PA nel tessuto neurale sottostante. Quindi, impostare il rapporto M su 0,2 e l'intensità dello stimolo (nota anche come potenza) al 30% dell'uscita massima dello stimolatore. Infine, impostare la larghezza dell'impulso (nota anche come durata della fase positiva) su 120 μs (la larghezza di impulso più lunga utilizzata nello studio).
NOTA: La posizione della bobina e la traiettoria determinate utilizzando la corrente indotta da PA saranno impiegate per la corrente indotta da AP 16,36,37,38,56,69. - Fornire da tre a cinque stimoli TMS mentre il partecipante mantiene una leggera contrazione del muscolo FDI (~5%-10% della massima contrazione volontaria). Se non viene suscitato alcun potenziale evocato dal motore (MEP), aumentare l'intensità dello stimolatore del 10% e fornire da tre a cinque stimoli TMS aggiuntivi.
- Ripetere il passaggio precedente fino a quando un MEP di almeno 0,2 mV è costantemente suscitato ad ogni stimolo, o fino a quando l'intensità dello stimolatore raggiunge il 60% -70% della massima uscita dello stimolatore. Se non viene suscitato alcun MEP affidabile, mantenere costanti i parametri di stimolazione e spostare lo stimolatore TMS in un cerchio con ~ 2 cm di diametro attorno al sito di stimolazione originale. Aumentare il diametro del cerchio di 1 cm se un MEP affidabile non è ancora stato suscitato in nessun punto del cerchio originale.
- Una volta ottenuto un MEP affidabile, confermare l'hotspot del motore FDI mantenendo costanti i parametri di stimolazione e spostando lo stimolatore TMS di 2 cm a nord, est, sud e ovest della posizione corrente della bobina. Fornire da tre a cinque stimoli TMS in ogni posizione70. Registrare la posizione e la traiettoria della nuova bobina se viene suscitato un MEP costantemente più grande in uno dei quattro quadranti. Utilizzare la nuova posizione e traiettoria della bobina come hotspot del motore corticale.
7. Determinazione dell'intensità dello stimolo per la stimolazione magnetica transcranica
- Avviare lo strumento di valutazione della soglia del motore TMS disponibile gratuitamente (MTAT 2.1)71,72,73 per determinare l'intensità dello stimolo necessaria per ottenere un MEP di 1 mV (soglia 1 mV)16,67,74. Impostare il metodo di stima su Senza informazioni a priori e fare clic su Start.
NOTA: il protocollo corrente utilizza un'intensità TMS di 1 mV16. Tuttavia, alcuni studi preferiscono impostare l'intensità come 120% della soglia motoria a riposo dell'individuo. Per la corrente AP, un MEP da 1 mV potrebbe non essere ottenibile. In tali casi, determinare l'uscita dello stimolatore che suscita il MEP massimo suscitato dalla configurazione dello stimolo AP, a condizione che il MEP massimo sia di almeno 0,5 mV. - Determinare l'uscita massima dello stimolatore disponibile per la larghezza dell'impulso di 120 μs. Quindi, utilizzare un grafico di conversione per ridimensionare l'intervallo di uscita dello stimolatore da 0 a 100 in modo che l'uscita dello stimolatore corrisponda alla scala del software MTAT 2.1.
NOTA: Per il modello utilizzato nello studio attuale, l'uscita massima dello stimolatore per una larghezza di impulso di 120 μs è del 50%. Pertanto, i valori forniti dal software MTAT 2.1 sono divisi per 2 per determinare il valore impostato sullo stimolatore. Per una larghezza di impulso di 70 μs, l'uscita massima dello stimolatore è del 66%, quindi tutti i valori forniti dal software MTAT 2.1 vengono moltiplicati per 0,66 (e arrotondati allo 0,5% più vicino). Per una larghezza di impulso di 30 μs, l'uscita massima dello stimolatore è del 100%. Pertanto, non è necessaria alcuna regolazione del ridimensionamento. - Impostare l'intensità dello stimolatore TMS sulla percentuale iniziale di uscita massima dello stimolatore indicata dal software MTAT 2.1 e fornire un singolo stimolo TMS. Se il MEP registrato nell'intervallo di tempo 20-50 ms dopo lo stimolo TMS supera 1 mV, indicare "sì" premendo il tasto Y . Se il MEP registrato è inferiore a 1 mV, indicare "no" premendo il tasto N . Ripetere questo passaggio fino a quando l'intensità dello stimolo visualizzata dal software MTAT cambia da nero a verde.
NOTA: Il valore iniziale indicato dal software MTAT 2.1 è sempre 37%. Per una larghezza di impulso di 120 μs, il valore effettivo dello stimolatore è del 18,5%. Per una larghezza di impulso di 70 μs, il valore effettivo dello stimolatore è del 24%. Per una larghezza di impulso di 30 μs, il valore dello stimolatore è del 37%. - Ripetere l'operazione per ogni combinazione di direzione corrente e durata dello stimolo. Per la corrente AP, ruotare la direzione corrente a 180 ° ruotando fisicamente la bobina per indurre la corrente PA di 180 ° o utilizzare una bobina personalizzata prodotta per indurre la corrente AP.
NOTA: quando si utilizzano più direzioni di corrente TMS e larghezze di impulso, tutte le soglie possono essere determinate prima della raccolta dei dati o appena prima di utilizzare quella specifica combinazione di direzione corrente e larghezza di impulso nel protocollo.
8. Inibizione afferente a breve latenza (nessuna linea di base dell'attività)
- Collegare la bobina che indurrà la corrente PA nel cervello allo stimolatore cTMS. Impostare il tipo di impulso su Monofasico-Positivo e il rapporto M su 0,2. Impostare la larghezza dell'impulso su 120 μs. Infine, impostare l'intensità dello stimolo sulla soglia di 1 mV determinata nel passaggio 7.
NOTA: se si utilizzano entrambe le direzioni correnti PA e AP, l'ordine in cui viene condotta la fase 8 deve essere randomizzato tra i partecipanti. Se si utilizzano più larghezze di impulso, l'ordine in cui viene eseguita la fase 8 deve essere controbilanciato tra i partecipanti. PA120 e AP30 erano le uniche configurazioni attuali impiegate nell'esperimento descritto. - Impostare l'intensità dello stimolo elettrico periferico sull'intensità determinata nel passaggio 5. Quindi, avvia la routine software senza attività su PC1. Quindi, impostare l'intervallo di interstimolo tra gli stimoli elettrici periferici e TMS su 21 ms.
- Posizionare la bobina TMS sull'hotspot del motore FDI determinato al punto 6. Chiedere al partecipante di mantenere una leggera contrazione del muscolo FDI (~5%-10% della contrazione volontaria massima). Quindi, eseguire il software no-task su PC1 per attivare sia gli stimolatori periferici che quelli cTMS.
- Ripetere i passaggi per la configurazione della corrente AP30 usando la bobina che induce la corrente AP nel cervello.
NOTA: si consiglia di ripetere la linea di base senza attività alla fine dell'esperimento, tempo permettendo. Le valutazioni ISC pre- e post-attività sono fortemente consigliate al fine di fornire una base di riferimento per le ISC e stabilire eventuali differenze preesistenti tra i gruppi (se del caso).
9. Inibizione afferente a breve latenza (compito sensomotorio)
- Collegare la bobina PA allo stimolatore cTMS. Impostare il tipo di impulso su Monofasico-Positivo e il rapporto M su 0,2. Impostare la larghezza dell'impulso su 120 μs. Infine, impostare l'intensità dello stimolo sulla soglia di 1 mV determinata nel passaggio 7.
NOTA: Quando si utilizzano più configurazioni di corrente TMS (ad esempio, PA120, AP30), la configurazione corrente utilizzata durante il compito sensomotorio deve essere controbilanciata tra i partecipanti. Si consiglia di utilizzare lo stesso controbilanciamento utilizzato per determinare l'ordine per la valutazione di base senza attività. - Impostare l'intensità dello stimolo elettrico periferico sull'intensità determinata nel passaggio 5. Quindi, avviare la routine del software di attività sensomotorie su PC1. Impostare l'intervallo di interstimolo tra gli stimoli elettrici periferici e TMS su 21 ms.
- Posizionare la bobina TMS sull'hotspot del motore FDI determinato al punto 6. Chiedere al partecipante di mantenere una leggera contrazione del muscolo FDI (~5%-10% della contrazione volontaria massima).
- Eseguire la routine del software del compito sensomotorio per controllare l'attività sensomotoria e inviare i trigger digitali bloccati dal comportamento agli stimolatori periferici e cTMS. Mantenere il numero desiderato di prove incondizionate e condizionate tra 8 e 24 stimoli per condizione.
- Ripetere i passaggi per la configurazione della corrente AP30 usando la bobina per indurre la corrente AP nel cervello.
10. Trattamento e analisi dei dati
- Ispezionare visivamente i dati EMG offline e scartare eventuali tracce in cui il quadrato medio radice dell'EMG prestimolo (-50 all'inizio dello stimolo) supera un'ampiezza del criterio. Calcola l'errore quadratico medio principale per ogni prova come segue:
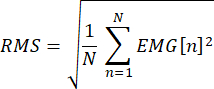
dove N è il numero di punti dati compreso tra -50 e l'inizio dello stimolo, e l'EMG è la tensione nel punto n. Per SAI condotto con il muscolo a riposo, utilizzare un criterio di ampiezza di 10-15 μV. Per la SAI valutata con una leggera contrazione tonica, utilizzare un criterio di ampiezza che è l'RMSE medio in tutti gli studi più due deviazioni standard, supponendo che i livelli di contrazione siano stati monitorati durante lo studio. - Per ogni prova, calcolare l'ampiezza MEP picco-picco per l'FDI come differenza tra i valori minimi e massimi nella finestra temporale tra 20 ms e 50 ms dopo l'artefatto di stimolo TMS nel canale 170.
- Per le prove condizionate, calcolare l'ampiezza dell'onda M picco-picco per l'APB come artefatto di stimolo post-periferico da picco a picco da 5 ms a 15 ms nel canale 2.
NOTA: Il calcolo dell'ampiezza dell'onda M da picco a picco è un metodo per confermare che l'intensità dello stimolo non è variata tra le condizioni durante l'esperimento. - Calcolare l'ampiezza media MEP per gli studi incondizionati e condizionati e l'onda M media per gli studi condizionati per ogni combinazione di direzione corrente TMS, larghezza dell'impulso e condizione comportamentale.
- Esprimere l'ampiezza MEP condizionata come rapporto dell'ampiezza MEP incondizionata per ciascun partecipante utilizzando l'equazione inferiore a11:
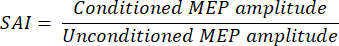
NOTA: rapporti più bassi riflettono un'inibizione più potente. Moltiplicando il rapporto per il 100% è comune esprimere l'ampiezza MEP condizionata come percentuale dell'ampiezza MEP incondizionata. - Calcola la media tra tutti i partecipanti per ogni direzione corrente TMS, larghezza dell'impulso e combinazione di condizioni comportamentali. Segnala questi valori. Sebbene i valori medi siano generalmente riportati, se possibile, dimostrare i singoli dati in cifre.
Risultati
La figura 3 illustra esempi di MEP incondizionati e condizionati da un singolo partecipante suscitato nel muscolo FDI durante il compito sensomotorio utilizzando la corrente indotta PA120- e AP30- (il pedice indica la larghezza dell'impulso). I grafici a barre nella colonna centrale illustrano le ampiezze MEP medie grezze picco-picco per le prove incondizionate e condizionate. I grafici a barre a destra mostrano le latenze di insorgenza SAI e MEP per la corrente indotta...
Discussione
Il metodo SAI qui descritto sonda un sottoinsieme di percorsi neurali che svolgono un ruolo nelle prestazioni sensomotorie e nell'apprendimento. Valutare la SAI mentre i partecipanti svolgono compiti sensomotori controllati è fondamentale per districare i complessi contributi dei numerosi circuiti sensomotori che convergono sui neuroni corticospinali motori per modellare la produzione motoria in popolazioni sane e cliniche. Ad esempio, una metodologia simile è stata utilizzata per identificare l'influenza cerebellare s...
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Gli autori riconoscono i finanziamenti del Natural Sciences and Engineering Research Council (NSERC), della Canada Foundation for Innovation (CFI) e dell'Ontario Research Fund (ORF) assegnati a S.K.M.
Materiali
| Name | Company | Catalog Number | Comments |
| Acquisition software (for EMG) | AD Instruments, Colorado Springs, CO, USA | PL3504/P | LabChart Pro version 8 |
| Alcohol prep pads | Medline Canada Corporation, Mississauga, ON, Canada | 211-MM-05507 | Alliance Sterile Medium, Antiseptic Isopropyl Alcohol Pad (200 per box) |
| Amplifier (for EMG) | AD Instruments, Colorado Springs, CO, USA | FE234 | Quad Bio Amp |
| Cotton round | Cliganic, San Francisco, CA, USA | CL-BE-019-6PK | Premium Cotton Rounds (6-pack, 90 per package) |
| cTMS coils | Rogue Research, Montréal, QC, Canada | COIL70F80301 | 70 mm Medium Inductance Figure-8 coil |
| cTMS coils | Rogue Research, Montréal, QC, Canada | COIL70F80301-IC | 70 mm Medium Inductance Figure-8 coil (Inverted Current) |
| cTMS stimulator | Rogue Research, Montréal, QC, Canada | CTMSMU0101 | Elevate cTMS stimulator |
| Data acquisition board (for EMG) | AD Instruments, Colorado Springs, CO, USA | PL3504 | PowerLab 4/35 |
| Digital to analog board | National Instruments, Austin, TX, USA | 782251-01 | NI USB-6341, X Series DAQ Device with BNC Termination |
| Dispoable adhesive electrodes (for EMG) | Covidien, Dublin, Ireland | 31112496 | Kendal 130 Foam Electrodes |
| Electrogel | Electrodestore.com | E9 | Electro-Gel for Electro-Cap (16 oz jar) |
| Nuprep | Weaver and Company, Aurora, CO, USA | 10-30 | Nuprep skin prep gel (3-pack of 4 oz tubes) |
| Peripheral electrical stimulator | Digitimer, Hertfordshire, UK | DS7R | DS7R High Voltage Constant Current Stimulator |
| Reusable bar electrode | Electrodestore.com | DDA-30 | Black Bar Electrode, Flat, Cathode Distal |
| Software (for behaviour and stimulator triggering) | National Instruments, Austin, TX, USA | 784503-35 | Labview 2020 |
| TMS stereotactic coil guidance system | Rogue Research, Montréal, QC, Canada | KITBSF0404 | BrainSight Neuronavigation System |
| Transpore tape | 3M, Saint Paul, MN, USA | 50707387794571 | Transpore Medical Tape (1 in x 10 yds) |
Riferimenti
- Bizzi, E., Ajemian, R. From motor planning to execution: a sensorimotor loop perspective. Journal of Neurophysiology. 124 (6), 1815-1823 (2020).
- Chen, R. Studies of human motor physiology with transcranial magnetic stimulation. Muscle & Nerve Supplement. 9, S26-S32 (2000).
- Hallett, M. Transcranial magnetic stimulation: A primer. Neuron. 55 (2), 187-199 (2007).
- Hallett, M. Transcranial magnetic stimulation and the human brain. Nature. 406 (6792), 147-150 (2000).
- Day, B. L., et al. Electric and magnetic stimulation of human motor cortex - Surface EMG and single motor unit responses. Journal of Physiology. 412, 449-473 (1989).
- Di Lazzaro, V., et al. Comparison of descending volleys evoked by transcranial magnetic and electric stimulation in conscious humans. Electroencephalography and Clinical Neurophysiology/Electromyography and Motor Control. 109 (5), 397-401 (1998).
- Di Lazzaro, V., Rothwell, J. C. Corticospinal activity evoked and modulated by non-invasive stimulation of the intact human motor cortex. Journal of Physiology. 592 (19), 4115-4128 (2014).
- Chen, R., et al. The clinical diagnostic utility of transcranial magnetic stimulation: Report of an IFCN committee. Clinical Neurophysiology. 119 (3), 504-532 (2008).
- Rossini, P. M. Non-invasive electrical and magnetic stimulation of the brain, spinal cord, roots and peripheral nerves: Basic principles and procedures for routine clinical and research application. An updated report from an I.F.C.N. Committee. Clinical Neurophysiology. 126 (6), 1071-1107 (2015).
- Kujirai, T., et al. Corticocortical inhibition in human motor cortex. The Journal of Physiology. 471, 501-519 (1993).
- Tokimura, H., et al. Short latency inhibition of human hand motor cortex by somatosensory input from the hand. The Journal of Physiology. 523, 503-513 (2000).
- Nakamura, H., Kitagawa, H., Kawaguchi, Y., Tsuji, H. Intracortical facilitation and inhibition after transcranial magnetic stimulation in conscious humans. The Journal of Physiology. 498, 817-823 (1997).
- Chen, R., Corwell, B., Hallett, M. Modulation of motor cortex excitability by median nerve and digit stimulation. Experimental Brain Research. 129 (1), 77-86 (1999).
- Asmussen, M. J., Jacobs, M. F., Lee, K. G., Zapallow, C. M., Nelson, A. J. Short-latency afferent inhibition modulation during finger movement. PLoS One. 8 (4), e60496 (2013).
- Devanne, H. Afferent-induced facilitation of primary motor cortex excitability in the region controlling hand muscles in humans. European Journal of Neuroscience. 30 (3), 439-448 (2009).
- Ni, Z., et al. Transcranial magnetic stimulation in different current directions activates separate cortical circuits. Journal of Neurophysiology. 105 (2), 749-756 (2011).
- Bailey, A. Z., Asmussen, M. J., Nelson, A. J. Short-latency afferent inhibition determined by the sensory afferent volley. Journal of Neurophysiology. 116 (2), 637-644 (2016).
- Fischer, M., Orth, M. Short-latency sensory afferent inhibition: conditioning stimulus intensity, recording site, and effects of 1 Hz repetitive TMS. Brain Stimulation. 4 (4), 202-209 (2011).
- Voller, B., et al. Short-latency afferent inhibition during selective finger movement. Experimental Brain Research. 169 (2), 226-231 (2006).
- Asmussen, M. J., et al. Modulation of short-latency afferent inhibition depends on digit and task-relevance. PLoS One. 9 (8), e104807 (2014).
- Suzuki, L. Y., Meehan, S. K. Attention focus modulates afferent input to motor cortex during skilled action. Human Movement Science. 74, 102716 (2020).
- Bonassi, G., et al. Selective sensorimotor modulation operates during cognitive representation of movement. Neuroscience. 409, 16-25 (2019).
- Beck, S., Hallett, M. Surround inhibition in the motor system. Experimental Brain Research. 210 (2), 165-172 (2011).
- Seki, K., Fetz, E. E. Gating of sensory input at spinal and cortical levels during preparation and execution of voluntary movement. Journal of Neuroscience. 32 (3), 890-902 (2012).
- Young-Bernier, M., Davidson, P. S., Tremblay, F. Paired-pulse afferent modulation of TMS responses reveals a selective decrease in short latency afferent inhibition with age. Neurobiology of Aging. 33 (4), 1-11 (2012).
- Pelosin, E., et al. Attentional control of gait and falls: Is cholinergic dysfunction a common substrate in the elderly and Parkinson's disease. Frontiers in Aging Neuroscience. 8, 104 (2016).
- Dubbioso, R., Manganelli, F., Siebner, H. R., Di Lazzaro, V. Fast intracortical sensory-motor integration: A window into the pathophysiology of Parkinson's disease. Frontiers in Human Neuroscience. 13, 111 (2019).
- Oh, E., et al. Olfactory dysfunction in early Parkinson's disease is associated with short latency afferent inhibition reflecting central cholinergic dysfunction. Clinical Neurophysiology. 128 (6), 1061-1068 (2017).
- Richardson, S. P., et al. Changes in short afferent inhibition during phasic movement in focal dystonia. Muscle & Nerve. 37 (3), 358-363 (2008).
- Ziemann, U., et al. TMS and drugs revisited 2014. Clinical Neurophysiology. 126 (10), 1847-1868 (2015).
- Di Lazzaro, V. Muscarinic receptor blockade has differential effects on the excitability of intracortical circuits in the human motor cortex. Experimental Brain Research. 135 (4), 455-461 (2000).
- Di Lazzaro, V., et al. Neurophysiological predictors of long term response to AChE inhibitors in AD patients. Journal of Neurology, Neurosurgery and Psychiatry. 76 (8), 1064-1069 (2005).
- Fujiki, M., Hikawa, T., Abe, T., Ishii, K., Kobayashi, H. Reduced short latency afferent inhibition in diffuse axonal injury patients with memory impairment. Neuroscience Letters. 405 (3), 226-230 (2006).
- Koizume, Y., Hirano, M., Kubota, S., Tanaka, S., Funase, K. Relationship between the changes in M1 excitability after motor learning and arousal state as assessed by short-latency afferent inhibition. Behavioral Brain Research. 330, 56-62 (2017).
- Thabit, M. N., et al. Momentary reward induce changes in excitability of primary motor cortex. Clinical Neurophysiology. 122 (9), 1764-1770 (2011).
- Mirdamadi, J. L., Suzuki, L. Y., Meehan, S. K. Attention modulates specific motor cortical circuits recruited by transcranial magnetic stimulation. Neuroscience. 359, 151-158 (2017).
- Mirdamadi, J. L., Meehan, S. K. Specific sensorimotor interneuron circuits are sensitive to cerebellar-attention interactions. Frontiers in Human Neuroscience. 16, 920526 (2022).
- Suzuki, L. Y., Meehan, S. K. Verbal working memory modulates afferent circuits in motor cortex. European Journal of Neuroscience. 48 (10), 3117-3125 (2018).
- Mineo, L., et al. Modulation of sensorimotor circuits during retrieval of negative autobiographical memories: Exploring the impact of personality dimensions. Neuropsychologia. 110, 190-196 (2018).
- Bonnì, S., Ponzo, V., Di Lorenzo, F., Caltagirone, C., Koch, G. Real-time activation of central cholinergic circuits during recognition memory. European Journal of Neuroscience. 45 (11), 1485-1489 (2017).
- Nardone, R., et al. Abnormal short latency afferent inhibition in early Alzheimer's disease: A transcranial magnetic demonstration. Journal of Neural Transmission. 115 (11), 1557-1562 (2008).
- Nardone, R., Bratti, A., Tezzon, F. Motor cortex inhibitory circuits in dementia with Lewy bodies and in Alzheimer's disease. Journal of Neural Transmission. 113 (11), 1679-1684 (2006).
- Di Lazzaro, V., et al. In vivo cholinergic circuit evaluation in frontotemporal and Alzheimer dementias. Neurology. 66 (7), 1111-1113 (2006).
- Di Lazzaro, V., et al. Functional evaluation of cerebral cortex in dementia with Lewy bodies. NeuroImage. 37 (2), 422-429 (2007).
- Di Lazzaro, V., et al. In vivo functional evaluation of central cholinergic circuits in vascular dementia. Clinical Neurophysiology. 119 (11), 2494-2500 (2008).
- Marra, C., et al. Central cholinergic dysfunction measured "in vivo" correlates with different behavioral disorders in Alzheimer's disease and dementia with Lewy body. Brain Stimulation. 5 (4), 533-538 (2012).
- Mimura, Y., et al. Neurophysiological biomarkers using transcranial magnetic stimulation in Alzheimer's disease and mild cognitive impairment: A systematic review and meta-analysis. Neuroscience & Biobehavioral Reviews. 121, 47-59 (2021).
- Yarnall, A. J., et al. Short latency afferent inhibition: a biomarker for mild cognitive impairment in Parkinson's disease. Movement Disorders. 28 (9), 1285-1288 (2013).
- Celebi, O., Temuçin, C. M., Elibol, B., Saka, E. Short latency afferent inhibition in Parkinson's disease patients with dementia. Movement Disorders. 27 (8), 1052-1055 (2012).
- Martin-Rodriguez, J. F., Mir, P. Short-afferent inhibition and cognitive impairment in Parkinson's disease: A quantitative review and challenges. Neuroscience Letters. 719, 133679 (2020).
- Nardone, R., et al. Short latency afferent inhibition differs among the subtypes of mild cognitive impairment. Journal of Neural Transmission. 119 (4), 463-471 (2012).
- Tsutsumi, R., et al. Reduced interhemispheric inhibition in mild cognitive impairment. Experimental Brain Research. 218 (1), 21-26 (2012).
- Di Lazzaro, V., et al. Segregating two inhibitory circuits in human motor cortex at the level of GABAA receptor subtypes: A TMS study. Clinical Neurophysiology. 118 (10), 2207-2214 (2007).
- Giorgetti, M., et al. Local GABAergic modulation of acetylcholine release from the cortex of freely moving rats. European Journal of Neuroscience. 12 (6), 1941-1948 (2000).
- Turco, C. V., Toepp, S. L., Foglia, S. D., Dans, P. W., Nelson, A. J. Association of short- and long-latency afferent inhibition with human behavior. Clinical Neurophysiology. 132 (7), 1462-1480 (2021).
- Hannah, R., Rothwell, J. C. Pulse duration as well as current direction determines the specificity of transcranial magnetic stimulation of motor cortex during contraction. Brain Stimulation. 10 (1), 106-115 (2017).
- Peterchev, A. V., D'Ostilio, K., Rothwell, J. C., Murphy, D. L. Controllable pulse parameter transcranial magnetic stimulator with enhanced circuit topology and pulse shaping. Journal of Neural Engineering. 11 (5), 056023 (2014).
- Peterchev, A. V., Murphy, D. L., Lisanby, S. H. Repetitive transcranial magnetic stimulator with controllable pulse parameters (cTMS). Annual International Conference of the IEEE Engineering in Medicine and Biology Society. 2010, 2922-2926 (2010).
- Rothkegel, H., Sommer, M., Paulus, W., Lang, N. Impact of pulse duration in single pulse TMS. Clinical Neurophysiology. 121 (11), 1915-1921 (2010).
- MagPro Family User Guide. MagVenture A/S Available from: https://tsgdoc.socsci.ru.nl/images/a/ac/Magpro_family.pdf (2022)
- Bashir, S., Edwards, D., Pascual-Leone, A. Neuronavigation increases the physiologic and behavioral effects of low-frequency rTMS of primary motor cortex in healthy subjects. Brain Topography. 24 (1), 54-64 (2011).
- Rossi, S., Hallett, M., Rossini, P. M., Pascual-Leone, A. Screening questionnaire before TMS: An update. Clinical Neurophysiology. 122 (8), 1686 (2011).
- Keel, J. C., Smith, M. J., Wassermann, E. M. A safety screening questionnaire for transcranial magnetic stimulation. Clinical Neurophysiology. 112 (4), 720 (2001).
- Wassermann, E. M. Risk and safety of repetitive transcranial magnetic stimulation: report and suggested guidelines from the International Workshop on the Safety of Repetitive Transcranial Magnetic Stimulation, June 5-7, 1996. Electroencephalography and Clinical Neurophysiology. 108 (1), 1-16 (1998).
- Rossi, S., et al. Safety and recommendations for TMS use in healthy subjects and patient populations, with updates on training, ethical and regulatory issues: Expert guidelines. Clinical Neurophysiology. 132 (1), 269-306 (2021).
- Udupa, K., Ni, Z., Gunraj, C., Chen, R. Effects of short latency afferent inhibition on short interval intracortical inhibition. Journal of Neurophysiology. 111 (6), 1350-1361 (2013).
- Udupa, K., Ni, Z., Gunraj, C., Chen, R. Interactions between short latency afferent inhibition and long interval intracortical inhibition. Experimental Brain Research. 199 (2), 177-183 (2009).
- Turco, C. V., El-Sayes, J., Fassett, H. J., Chen, R., Nelson, A. J. Modulation of long-latency afferent inhibition by the amplitude of sensory afferent volley. Journal of Neurophysiology. 118 (1), 610-618 (2017).
- Sakai, K., et al. Preferential activation of different I waves by transcranial magnetic stimulation with a figure-of-eight-shaped coil. Experimental Brain Research. 113 (1), 24-32 (1997).
- Groppa, S., et al. A practical guide to diagnostic transcranial magnetic stimulation: Report of an IFCN committee. Clinical Neurophysiology. 123 (5), 858-882 (2012).
- . ClinicalResearcher.org Available from: https://www.clinicalresearcher.org/software.htm (2022)
- Awiszus, F. TMS and threshold hunting. Supplements to Clinical Neurophysiology. 56, 13-23 (2003).
- Silbert, B. I., Patterson, H. I., Pevcic, D. D., Windnagel, K. A., Thickbroom, G. W. A comparison of relative-frequency and threshold-hunting methods to determine stimulus intensity in transcranial magnetic stimulation. Clinical Neurophysiology. 124 (4), 708-712 (2013).
- Cash, R. F., Isayama, R., Gunraj, C. A., Ni, Z., Chen, R. The influence of sensory afferent input on local motor cortical excitatory circuitry in humans. Journal of Physiology. 593 (7), 1667-1684 (2015).
- Hayes, K. D., Khan, M. E. R., Barclay, N. E., Meehan, S. K. The persistent effects of sports-related concussion during adolescence on sensorimotor integration. Canadian Association for Neuroscience Meeting. , (2022).
- Turco, C. V., et al. Short- and long-latency afferent inhibition; Uses, mechanisms and influencing factors. Brain Stimulation. 11 (1), 59-74 (2018).
- Casula, E. P., Rocchi, L., Hannah, R., Rothwell, J. C. Effects of pulse width, waveform and current direction in the cortex: A combined cTMS-EEG study. Brain Stimulation. 11 (5), 1063-1070 (2018).
- D'Ostilio, K., et al. Effect of coil orientation on strength-duration time constant and I-wave activation with controllable pulse parameter transcranial magnetic stimulation. Clinical Neurophysiology. 127 (1), 675-683 (2016).
- Barclay, N. E., Graham, K. R., Hayes, K. D., Meehan, S. K. Program No. 474.08.The contribution of oscillatory activity to the modulation of different sensorimotor circuits under varying working memory load. Society for Neuroscience Annual Meeting. , (2022).
- Dubbioso, R., Raffin, E., Karabanov, A., Thielscher, A., Siebner, H. R. Centre-surround organization of fast sensorimotor integration in human motor hand area. NeuroImage. 158, 37-47 (2017).
- Adams, F. C., et al. Tactile sensorimotor training does not alter short- and long-latency afferent inhibition. Neuroreport. 34 (3), 123-127 (2023).
- Paparella, G., Rocchi, L., Bologna, M., Berardelli, A., Rothwell, J. Differential effects of motor skill acquisition on the primary motor and sensory cortices in healthy humans. Journal of Physiology. 598 (18), 4031-4045 (2020).
- Deveci, S., et al. Effect of the brain-derived neurotrophic factor gene Val66Met polymorphism on sensory-motor integration during a complex motor learning exercise. Brain Research. 1732, 146652 (2020).
- Turco, C. V., Locke, M. B., El-Sayes, J., Tommerdahl, M., Nelson, A. J. Exploring behavioral correlates of afferent inhibition. Brain Sciences. 8 (4), 64 (2018).
- Mang, C. S., Bergquist, A. J., Roshko, S. M., Collins, D. F. Loss of short-latency afferent inhibition and emergence of afferent facilitation following neuromuscular electrical stimulation. Neuroscience Letters. 529 (1), 80-85 (2012).
- Mirdamadi, J. L., Block, H. J. Somatosensory changes associated with motor skill learning. Journal of Neurophysiology. 123 (3), 1052-1062 (2020).
- Bologna, M., et al. Bradykinesia in Alzheimer's disease and its neurophysiological substrates. Clinical Neurophysiology. 131 (4), 850-858 (2020).
- Schirinzi, T. Amyloid-mediated cholinergic dysfunction in motor impairment related to Alzheimer's disease. Journal of Alzheimer's Disease. 64 (2), 525-532 (2018).
- Cohen, L. G., Starr, A. Localization, timing and specificity of gating of somatosensory evoked potentials during active movement in man. Brain. 110 (2), 451-467 (1987).
- Brown, K. E., et al. The reliability of commonly used electrophysiology measures Active and resting motor threshold are efficiently obtained with adaptive threshold hunting. Brain Stimulation. 10 (6), 1102-1111 (2017).
- Turco, C. V., Pesevski, A., McNicholas, P. D., Beaulieu, L. D., Nelson, A. J. Reliability of transcranial magnetic stimulation measures of afferent inhibition. Brain Research. 1723, 146394 (2019).
- Rehsi, R. S., et al. Investigating the intra-session reliability of short and long latency afferent inhibition. Clinical Neurophysiology Practice. 8, 16-23 (2023).
- Toepp, S. L., Turco, C. V., Rehsi, R. S., Nelson, A. J. The distribution and reliability of TMS-evoked short- and long-latency afferent interactions. PLoS One. 16 (12), e0260663 (2021).
- Alle, H., Heidegger, T., Krivanekova, L., Ziemann, U. Interactions between short-interval intracortical inhibition and short-latency afferent inhibition in human motor cortex. Journal of Physiology-London. 587 (21), 5163-5176 (2009).
- Noda, Y., et al. A combined TMS-EEG study of short-latency afferent inhibition in the motor and dorsolateral prefrontal cortex. Journal of Neurophysiology. 116 (3), 938-948 (2016).
- Noda, Y. Reduced prefrontal short-latency afferent inhibition in older adults and its relation to executive function: A TMS-EEG study. Frontiers in Aging Neuroscience. 9, 119 (2017).
- Noda, Y., et al. Reduced short-latency afferent inhibition in prefrontal but not motor cortex and its association with executive function in schizophrenia: A combined TMS-EEG study. Schizophrenia Bulletin. 44 (1), 193-202 (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon