Method Article
ラベルフリーバイオセンサー技術を活用乳癌におけるヒト白血球抗原バイオマーカーの検出
要約
無傷のクラスI HLA /ペプチド複合体は、潜在的な関連癌バイオマーカーを表す、癌細胞により流されている。ラベルフリー検出技術を利用し、T細胞受容体はモノクローナル抗体を模倣し、小屋MIF / HLA-A * 02の検出:MDA-MB-231細胞の上清中の01複合体、ヒト血清にスパイクし、そして患者の血漿をの開発を可能にする、実証されている小説癌診断プラットフォーム。
要約
米国癌協会によると、20万人以上の女性が毎年浸潤性乳癌と診断され、約4万は病気で死亡する。ヒト白血球抗原(HLA)クラスIサンプル細胞タンパク質のプロテアソーム分解に由来するペプチドを、循環細胞傷害性Tリンパ球(CTL)の問い合わせのための細胞表面上のこれらのフラグメントを提示する。 * 02乳癌特異的ペプチド/ HLA-Aを認識するT細胞受容体模倣体の発生(TCRM)モノクローナル抗体(mAb):01は、マクロファージ遊走阻止因子に由来するものなどの複合体(MIF 19-27)およびNY-ESO- 1 157-165は、有効な抗腫瘍CTL応答の非存在下で検出および乳癌細胞の破壊を可能にする。無傷のクラスI HLA /ペプチド複合体は、乳癌細胞により流され、潜在的に関連する癌バイオマーカーを表す。この作品、癌診断のための画期的なバイオマーカーのスクリーニングシステムではT細胞受容体の導波モード共鳴(GMR)センサ技術を用いた新規な、ラベルフリーバイオセンサーと組み合わせ模倣するモノクローナル抗体を組み込んだ。■が提示される。小屋MIF / HLA-A * 02の検出:MDA-MB-231細胞上清中の01複合体は、ヒト血清をスパイクし、そして患者の血漿を示されている。この作品の影響は、ターゲットと免疫療法のためのコンパニオン疾患の診断の開発を通じてオーダーメイド医療に革命をもたらす可能性があります。
概要
長さが8〜11個のアミノ酸のクラスIヒト白血球抗原(HLA)のサンプルのペプチドは、細胞内タンパク質のレパートリーのプロテアソーム分解に由来し、あらゆる有核細胞1,2の表面にこれらのペプチドを提示する。 HLA複合体は、循環細胞傷害性Tリンパ球(CTL)へ( 図1)は、各セルの状態を示す「自然のバイオマーカー」である。 CTLによる問題の細胞の排除における疾患関連ペプチド結果の認識。したがって、適応免疫応答は、ウイルス感染および腫瘍を排除するのに非常に効果的である。しかしながら、免疫系はしばしば効果的なCTL応答を回避することができるウイルスまたは腫瘍の選択を促進する圧力を加える。乳癌関連タンパク質、マクロファージ遊走阻止因子に由来するもののような01の錯体(MIF:特定のペプチド/ HLA-A * 02を認識するT細胞受容体模倣(TCRM)モノクローナル抗体(mAb)19-27)3およびNY-ESO-1 157-165、有効な抗腫瘍CTL応答4,5の非存在下での乳癌細胞の検出および破壊を可能にする。この代表的な作業は、人口の30%までで表現されるHLA-A * 0201分子に焦点を当てている。しかし、TCRMの生産が続く他の関連するHLA /ペプチド複合体の同定は、はるかに広い人口にこの作品の有用性を拡大し、目標と免疫療法とコンパニオン疾患の診断の開発を可能にします。
細胞表面にバインドされたペプチド/ HLA複合体の一部がプラズマ中に放出される。によりペプチド/ HLAプールの非常に複雑な性質のため、HLA関連するバイオマーカーのためのimmunopeptidomeをマイニングのための現在の方法は時間がかかる。このプロセスは、血漿からの可溶性HLAのアフィニティー精製を必要とし、逆相高圧液体クロマトグラフィーによってHLA関連ペプチドの分離タンデム質量分析(MS / MS)6,7によって(RP-HPLC)、およびペプチド配列決定。このプロセスは、新たな治療標的の発見のために実行可能な選択肢ではあるが、それはすでに治療ワクチンやバイオ医薬品パイプライン8-10におけるHLA関連標的のためのコンパニオン診断ツールとして面倒なプロセスである。これらの目標に向けられたTCRMは、関連する臨床試験に患者を層別化を目的とした急速なコンパニオン診断開発のためのツールを提供し、より多くの情報に基づいた治療選択肢を提供する。
この作品では、癌の診断のための画期的なバイオマーカーのスクリーニングシステムは、TCRMと最小限の処理ステップとの生物学的相互作用を監視し、ラベルフリーバイオアッセイ系を利用した提示されている。無標識バイオアッセイ系は、誘電体導波路格子11-14に生じる導波モード共鳴(GMR)効果を利用した方法に基づいている。ときに広帯域光の連絡回折このシステムに必要なプレートで格子、2特定の波長が反映されます。固定された受容体とそのリガンドの間の結合相互作用は、スペクトラムアナライザ12の共振波長シフトを追跡することによって、リアルタイムでモニターされる。別個の共振ピークは、入射TE(入射面に垂直な電気ベクトル)およびTM(入射面に垂直な磁気ベクトル)潜在的に検出精度11,14を増加させることができる複数のデータポイントを提供する偏光状態のために起こる。このラベルフリーアッセイ系で抗体予め感作されたプレートを用いて、データ分析を用いたアッセイの実行時間は約45分である。さらに、複数の患者試料を、HPLC-MS / MSベースのフォーマット上で、96または384ウェルフォーマットで明らかな利点を調べることができる。
プロトコル
倫理声明:デ·同定されたヒト組織および血漿サンプルは治験審査委員会の下にヘンドリック医療センターから入手した、プロトコルを承認した。
ビオチン化抗体の1追加
注:このステップの監視はオプションです。監視していない場合は、代替プロトコルを参照してください。
- 市販のアビジン派生物でコーティングしたプレートを( 材料および装置表を参照)を取得します。
- ウェルに50μlのリン酸緩衝生理食塩水(PBS)pH7.2での追加。
注:28℃でプレインキュベートPBSは、温度関連の共鳴シフトを最小化する。 - オープンバイオアッセイスキャナソフトウェアブランク、標準規格の選択とサンプルプレートレイアウトで、温度設定(28℃)、毎分スキャンの数を含んで実験手順を定義するためのセットアップウィザードに従ってください(1)、および実験の長さ( 150分取工程のために対応するため)。
- ラベルフリーのバイオアッセイのスキャナに準備されたアッセイプレートを挿入し、最初のスキャンを開始します。最初のスキャンが完了すると、「起動に自己参照」を選択します。ベースラインは、実験の開始時に収集されたスキャンの初期設定である。これはこの特定のプレート上で行わ最初の読み取りの場合は、温度を平衡化し、ベースラインのドリフトを排除するために、スキャナが実行できるようにする。サンプルを添加したベースラインのスクリーンショットについては、図2を参照してください。
- ベースラインが安定化し、または少なくとも5スキャンした後、読み取りを一時停止し、プレートを取り出す。
- シンクにダンプすることで、PBSを除去し、プレート上のコントロールウェルが、すべてに[PBSのpHは7.2で10μg/ mlの]で50μlのRL21Aビオチン化抗体を追加します。対照ウェルに50μlのPBSを追加します。
- バックバイオアッセイスキャナーにプレートを挿入し、飽和状態に達するまで、読み出しを再開、約1.5時間。
- 読み込みを一時停止し、プレートを取り出す。
- 洗うプレートを200μlを200μl/ウェルのPBS pH7.2で3回すすいだ続い/ウェルのリン酸緩衝生理食塩水+ 0.05%ツイーン20(PBST)で3回洗浄する。 PBSで繰り返します。次のステップに移動する前にペーパータオル上でプレートから過剰のPBSをタップします。
注:このステップは自動プレート洗浄機で実行またはシンクに液体を投棄し、ピペットでPBSTを交換してプレートを200μlのPBSTで3回洗浄することができます。 - すべてのアクティブなウェルに50μlのPBS pHが7.2を追加します。
- バックバイオアッセイスキャナーにプレートを挿入し、洗浄後の共鳴を監視するために読んで再開する。
- 読み取りを停止し、プレートを取り出す。
ステップ1のための代替プロトコル:
- すべてのウェルに[10μg/ mlのPBS]で50μlのRL21Aビオチン化抗体を追加します。
- 1.5時間室温でインキュベートまたは4℃で一晩。
- 200μlのプレートを3回洗浄/ウェルのPBSTステップ1.9のように、200μl/ウェルのPBSで3回リンスが続く。
- PBSを除去し、適切なアッセイ緩衝液のウェルあたり50μlを添加する。このアッセイのために、市販の正常ヒト血清をPBSで希釈した1:20を用いた。
- オープンバイオアッセイスキャナソフトウェアおよび実験手順を定義するために、セットアップウィザードに従ってください。
- バイオアッセイスキャナにプレートを挿入し、ベースラインを読み始める。これはこの特定のプレート上で行わ最初の読み取りの場合は、温度を平衡化し、ベースラインのドリフトを除去するためにスキャナの実行をしてみましょう。
- ベースラインが安定化し、または少なくとも5スキャンした後、読み取りを一時停止し、プレートを取り出す。
- 井戸からアッセイ緩衝液を除去します。
- アッセイ緩衝液中に[0.625から10 / mlの]の範囲の濃度で、関連する(FLSL)または無関係(SLLV、YLEV、またはKVL)ペプチドベアリング01モノマー:スパイクは、HLA A * 02で制御します。プレートの対照ウェルに標準を50μl加え
- サンプルにアッセイ緩衝液中の分析物の50μlのを追加プレートのウェル。このアッセイのために、市販のヒト血清を使用したスパイク。
- バックバイオアッセイスキャナーにプレートを挿入し、飽和状態に達するまで、読み出しを再開、約30〜60分。
- 読み込みを一時停止し、プレートを取り出す。
- 200μlのプレートを3回洗浄/ウェルのPBSTステップ1.9のように、200μl/ウェルのPBSで3回リンスが続く。
- すべてのアクティブなウェルに50μlのアッセイ緩衝液を追加します。
- バックバイオアッセイスキャナーにプレートを挿入し、洗浄後の共鳴を監視するために読んで再開する。
- 読み取りを停止し、プレートを取り出す。
注:アッセイ緩衝液は、PBS、組織培養培地、またはヒト血清は、アッセイの目的に依存し、PBS中で1:20に希釈することができる。
3.データ分析
- バイオアッセイスキャナソフトウェアまたはエクスポート望ましい統計分析ソフトウェアに生データファイルを用いて分析する。バイオアッセイスキャナソフトウェアは自動的に基づいて結合曲線を生成し、実験のセットアップ中に設けられた板のレイアウト。
注:分析のためのバイオアッセイスキャナソフトウェアを使用していない場合は、手順3.2から3.4に従ってください。 - 後続の各データ点からベースラインとネガティブコントロールを減算します。
- 各時点での複製ウェルの平均値と標準偏差を計算する。
- バーグラフの結合曲線または選択エンドポイントデータのグラフを生成する。
結果
01分子3:実験の代表的なセットは、HLA-A * 02のコンテキスト内で十分に特徴付けTCRM、RL21A、特にペプチドを認識するマウスIgG2aモノクローナル抗体(MIF 19-27またはFLSL)を用いて行った。同族ペプチド/ HLAモノマー、ならびに無関係のHLAモノマー15は 、記載された手順を示すために使用された。 図3は、アッセイフォーマットを示す。
RL21Aは、他のペプチド/ HLAが3複合体と少ない交差反応性を持つFLSL / HLAモノマーに特異的である。この特異性は、ラベルフリーバイオアッセイ系( 図4)を使用して要約されている。固定化FLSL / HLAモノマー( 図5)上のRL21A抗 体の滴定により決定されるように、この実験のための標識フリーバイオアッセイ系の感度は低ナノモル範囲である。バックグラウンド信号が著しく血清サンプルにおいて増加したが、よスパイクされたヒト血清中FLSL / HLAモノマーの重特異検出は、 図6に達成され、濃度勾配は、これらのサンプルで容易に識別可能である。最後に、MDA-MB-231細胞株からの上清を、以前にFLSL / HLA-A * 02に提示することが示さ:01分子を、このラベルフリーアッセイプラットフォーム( 図7)を使用して、可溶性FLSLモノマーを含むことが示されている。 FLSL / HLAモノマーのその後の添加はRL21A上の信号( 図7)を増加させる。システムの感度に、よく負の共鳴シフトを含む周知変動による図4および図5における標準偏差の関数として見られるように、温度の変動の結果として起こり得る。これらの変化は、全てのサンプルのプレインキュベーションおよび室温( すなわち、28℃)のわずかに過剰の温度でバイオアッセイプレートリーダーによって劇的に低減することができる。
図8において、簡潔に、96型ウェルポリスチレンプレートをPBSTで洗浄し、0.5%低脂肪乳でブロックし、PBSTで洗浄し、室温で2時間、のためRL21Aの[10μg/ mlの]を塗布し、段階希釈して、室温で2時間インキュベートした。正常ヒト血清におけるFLSL HLAモノマーは、標準曲線を生成するために、PBSで1:10に希釈するか、または患者の血漿をPBSで1:10に希釈した。無傷のHLAを検出し、PBSTで洗浄した。プレートをPBSTで洗浄し、ウサギ抗 - ヒトβ2ミクログロブリン[5000 1]を用いて室温で1時間インキュベートした。次いで、プレートを、ヤギ抗ウサギIgGを[1:10,000]で30分間インキュベートし、PBSTで洗浄した。比色検出は、基板は、15分間のインキュベーション時間でABTS(2,2'-アジノビス[3-ゾリン-6-スルホン酸] -diammonium塩)を用いて実施し、マイクロプレートリーダーで405nmで観察された。 FLSL / HLAは、3つの患者サンプル中で検出された。
図8Bにおいては、患者の血漿RL.064をPBSで1:20に希釈した後、追加したプレートへのEDと60分間ラベルフリー検出器で監視。患者の血清中のFLSL / HLA複合体の特異的検出を達成した。スチューデントt検定をグラフ化および統計ソフトウェア(p <0.05)を用いて行った。
図8Cに、組織切片をマウス陽性対照としての抗HLA-A2(BB7.2)、RL21A、IgG2bおよびIgG2aをそれぞれ、陰性対照とを1μg/ mlで染色した。染色は、製造業者の指示通りに核染色用の抗マウス検出キット、DAB(ジアミノベンザジン)、およびヘマトキシリンQSを用いて検出した。 RL21Aによる腫瘍組織の染色はFLSL / HLA複合体の提示を確認する。
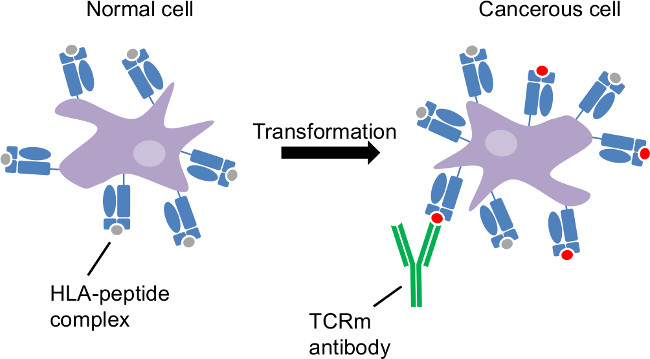
図1:クラスIヒト白血球抗原による腫瘍抗原提示癌性形質転換は、細胞内の障害である。 HLAサンプルintracellulアルタンパク質および細胞表面における癌関連の変化を明らかにする。 CTLとTCRMは、これらの細胞への異なるHLAペプチド複合体を介して癌細胞を認識することができる。

図2:初期ベースラインを示すデータ収集のバイオアッセイスキャナソフトウェアでデータ取得を行うときのスクリーンショットの例はFLSL / HLA複合体の10μg/ mlのでコーティングされたプレートにRL21A抗 体を添加したスキャンします。抗体の濃度は、指示されている。各行はよく時間をかけて監視される個々を表します。

図3:アッセイ形式のrelを取り込むアッセイプレートの回折格子表面に固定化された抗体のイラストレーション。溶液中のevantペプチド/ HLA複合体。

図4:FLSL / HLA複合体のためのRL21Aの特異無関係のHLAモノマー(YLEV、SLLV、およびKVL)に比べその関連(FLSL)のHLAモノマーのためのビオチン化RL21A TCRMの特異性の実証。。ビオチン化RL21A TCRM [10μg/ mlの]アビジンコーティングしたアッセイプレートの表面上に固定化され、検出は、PBS中で非標識の関連または無関係のHLAモノマー[10μg/ mlの]を用いて行った。 RL21AはFLSL / HLA複合体に特異的であった。二元配置ANOVAは、グラフおよび統計ソフトウェアた(p <0.001)を用いて行った。

図5:その同族ペプチド/ HLA複合体へのRL21Aの結合感度 detectiのイラスト。制限とFLSL / HLA複合体にRL21Aの感度を結合に。ビオチン化HLAモノマーFLSL [10μg/ mlの]はアッセイプレートの表面上に固定され、示されているように、非標識RL21AはPBSで連続希釈でプレートに添加した。このシステムの検出は、低ナノモル範囲であった。
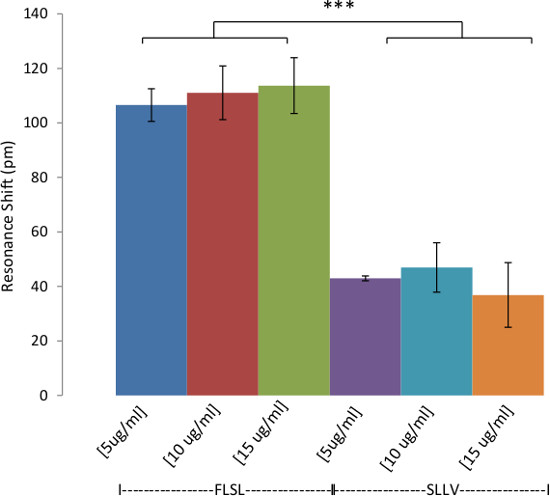
図6:スパイクヒト血清中のHLA複合体の検出ヒト血清中のHLAの検出の実証。。ビオチン化RL21A TCRM [10μg/ mlの]はアビジンコーティングしたアッセイプレートの表面上に固定化した。関連(FLSL)または無関係(SLLV)HLAモノマーでスパイクプールした正常ヒト血清をPBSで1:20に希釈し、プレートに添加し、60分間、無標識検出器でモニターした。ヒト血清中のFLSL / HLA複合体の特異的検出を達成した。一般的には、バックグラウンドシグナル(無関係SLLVモノマー)が高い小胞体希釈した血清試料をPBS中の精製された分析物( 図4参照)と比較した。 ANOVAは、グラフおよび統計ソフトウェアた(p <0.0001)を用いて行った双方向。
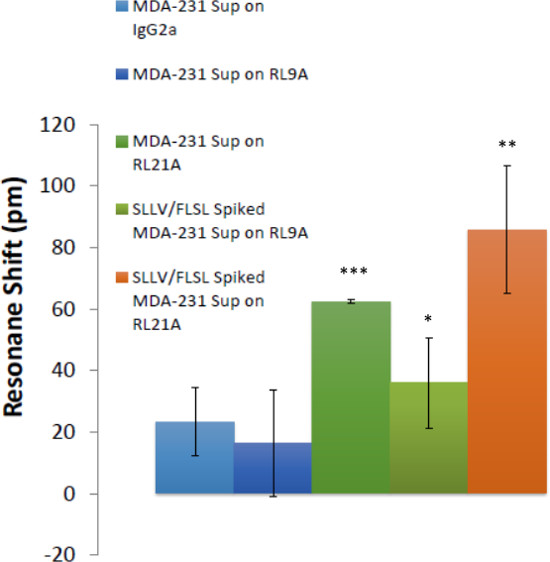
図7:可溶性HLA複合体は、乳癌細胞培養上清中に検出された乳癌細胞上清中のHLAを検出する能力が実証される。ビオチン化RL21A TCRM、RL9A TCRM(陰性対照)、およびアイソタイプ対照をアッセイプレート表面上に固定化した。スパイク[5μg/ mlの]と非埋め込みMDA-231細胞培養上清を添加し、結合はラベルフリー検出器に60分間モニターした。 FLSLとSLLV HLAモノマーは、サンプルがRL9AとRL21A結合のためのポジティブコントロールを表すスパイク。 ANOVAは、グラフおよび統計ソフトウェアた(p <0.0001)を用いて行った一方向。
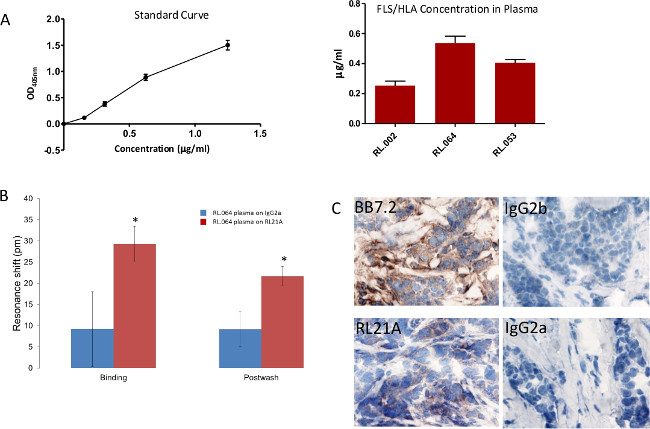
図8:患者サンプル中FLSL / HLA複合体の特異的検出(A)免疫吸着アッセイ(ELISA)リンクされた伝統的な酵素は、患者の血漿中のFLSL / HLA特異的複合体を検出するために利用した。 (B)ビオチン化RL21A TCRMまたはIgG2aの【を10μg/ mlの]アビジンアッセイプレート上に固定化した。患者RL.064から(C)乳房腫瘍組織が 以前FLSL / HLA複合体の腫瘍プレゼンテーションを確認するために3を説明したように染色した。 この図の拡大版をご覧になるにはこちらをクリックしてください。
ディスカッション
本明細書に記載の方法は、高スループットの96または384ウェルフォーマットで患者の血清、血漿、尿または唾液サンプル中の可溶性ペプチド/ HLA複合体の迅速な検出を可能にする癌診断用のバイオマーカーのスクリーニングシステムを導入する。モノクローナル抗体を模倣するT細胞受容体と標識不使用検出システムを利用し、このアッセイ系は、従来のELISAによって3.5時間と比較して、1時間未満に分析時間を切断する。このハイスループットアプローチは、治療用癌ワクチンやバイオ医薬品のための臨床試験への患者の迅速な層別化を可能にします。これらの疾患標的の検出のための現在の方法は、個々の患者の試料のアフィニティー精製およびHPLC-MS / MS、面倒で時間のかかるプロセスを必要とする。この方法は、従来のELISA技術に適しているが、このような抗β2ミクログロブリン抗体などの二次検出試薬は、発生期のHLの構造を変化させる可能性が懸念されている分子とTCRM制限検出への結合を阻害する。ラベルフリー検出は、これらの懸念を緩和する。この手順は、表面プラズモン共鳴システムなどの他の無標識システムでの使用のために改変することができる。しかし、これは非常に本研究で用いたバイオアッセイ系と比較して、より高いスループット能力を減少させるであろう。
このプロトコルは、事実上、いくつかの重要なステップの遵守と患者血清と血漿中の非HLAバイオマーカーの検出のために修飾することができる。 <200 PMシフトはおそらくその後の検出工程のために低信号になりますように最初の抗体コーティングプロセスのモニタリングは、表面の最適化のために推奨されます。血清タンパク質の存在量が低濃度の分析物の結合をマスクすることができるように、ベースラインと洗浄後の読み取りエンドポイント解析のために有用である。最後に、試料の温度変化は、ウェル変動で生じ得る。これは、すべてのサンプルがプレインキュベートすることをお勧めしますdはラベルフリーbiosassay部温度コントローラは、室温以上、2-3℃に設定すること。冷蔵試料は、動作温度に到達するのに十分な時間を許容されるべきである。
このプロトコルの将来の変更は、プレート表面上のTCRMの多重化を含む。バイオアッセイシステムは、少なくとも8プレックスの密度で、ウェルのスポッティングに現在適している。各ウェルに4-8 TCRMを導入することにより、試験試料体積当たり低減し、患者ごとにますます複雑なデータの収集を可能にしている。この機能は、さらなる治療選択肢に関して患者に知らせることができます。
開示事項
著者、デブラWawro Weidanzとロバート·マグナソンは、それぞれこの記事で使用バイオアッセイプレートリーダーおよびアッセイプレートを生産レゾナントセンサ社、で最高経営責任者兼最高技術責任者である。
謝辞
These studies were supported in part by the Development Corporation of Abilene which provides laboratory space and salary support for Experimmune, a Center for Immunotherapeutic Development at Texas Tech University Health Sciences Center and Resonant Sensors Incorporated.
資料
| Name | Company | Catalog Number | Comments |
| Name of the Material/Equipment | Company | Catalog Number | Comments/Description (optional) |
| ResoSens Label-free Bioassay Detection System | Resonant Sensors Incorporated | ||
| Avidin Sensitized Bionetic 96-well Plates | Resonant Sensors Incorporated | ||
| ResoVu software | Resonant Sensors Incorporated | ||
| RL21A Biotinylated TCRm mAb | PureMHC, LLC | ||
| RL9A Biotinylated TCRm mAb | PureMHC, LLC | ||
| FLSL HLA-A*02:01 Monomer | Experimmune | full peptide sequence: FLSELTQQL | |
| SLLV HLA-A*02:01 Monomer | Experimmune | full peptide sequence: SLLMWITQV | |
| YLEV HLA-A*02:01 Monomer | Experimmune | full peptide sequence: YLEPGPVTV | |
| KVL HLA-A*02:01 Monomer | Experimmune | full peptide sequence: KVLEYVIKV | |
| Pooled Normal Human Serum | ThermoFisher | BP2657100 | |
| MDA-MB-231 Cell Supernatant | ATCC | HTB-26 | Cells grown in IMDM , 10% FBS and 1% penn/strep. Supernatants harvested from 3 day confluent cultures. |
| Iscove's Modification of Dulbecco's Medium (IMDM) | Life Technologies | 12440-053 | |
| Fetal Bovine Serum (FBS) | Life Technologies | 10082-147 | |
| Penicillin/Streptomycin | Life Technologies | 15070-63 | |
| Sodium Hydroxide | ThermoFisher | 5318-1 | |
| Phosphate Buffered Saline (PBS) | ThermoFisher | BP665-1 | |
| Phosphate Buffered Saline + 0.05% Tween 20 (PBST) | ThermoFisher | BP337-500 | |
| 2,2’-Azinobis [3-ethylbenzothiazoline-6-sulfonic acid]-diammonium salt (ABTS) | ThermoFisher | 37615 | |
| rabbit anti-human β2 microglobulin | Dako | A0072 | |
| Peroxidase conjugated goat anti-rabbit IgG | Jackson Immunoresearch | 111-035-144 | |
| Nunc microplates | ThermoFisher | 439454 | |
| Synergy 2 microplate reader | Biotek | ||
| Immpress Reagent Kit | Vector | MP-7402 | |
| Immpact DAB | Vector | SK-4105 | |
| Hematoxylin QS | Vector | H3403 | |
| IgG2a | MP BioMedicals | 50328 | |
| IgG2b | MP BioMedicals | 50330 | |
| anti-HLA-A2 (BB7.2) | Experimmune | ||
| Prism 5 | Graphpad |
参考文献
- Shastri, N., Schwab, S., Serwold, T. Producing nature's gene-chips: the generation of peptides for display by MHC class I molecules. Annu Rev Immunol. 20, 463-493 (2002).
- Peaper, D. R., Cresswell, P. Regulation of MHC class I assembly and peptide binding. Annu Rev Cell Dev Biol. 24, 343-368 (2008).
- Hawkins, O., et al. An HLA-presented fragment of macrophage migration inhibitory factor is a therapeutic target for invasive breast cancer. J Immunol. 186 (11), 6607-6616 (2011).
- Verma, B., et al. TCR mimic monoclonal antibody targets a specific peptide/HLA class I complex and significantly impedes tumor growth in vivo using breast cancer models. J Immunol. 184 (4), 2156-2165 (2010).
- Verma, B., et al. TCR mimic monoclonal antibodies induce apoptosis of tumor cells via immune effector-independent mechanisms. J Immunol. 186 (5), 3265-3276 (2011).
- Bassani-Sternberg, M., et al. Soluble plasma HLA peptidome as a potential source for cancer biomarkers. Proc Natl Acad Sci U S A. 107 (44), 18769-18776 (2010).
- Hickman, H. D., Yewdell, J. W. Mining the plasma immunopeptidome for cancer peptides as biomarkers and beyond. Proc Natl Acad Sci U S A. 107 (44), 18747-18748 (2010).
- Neethling, F. A., et al. Assessing vaccine potency using TCRmimic antibodies. Vaccine. 26 (25), 3092-3102 (2008).
- Mittendorf, E. A., et al. Clinical trial results of the HER-2/neu (E75) vaccine to prevent breast cancer recurrence in high-risk patients: from. US Military Cancer Institute Clinical Trials Group Study I-01 and I-02. Cancer. 118 (10), 2594-2602 (2012).
- Winter, H., Fox, B. A., Ruttinger, D. Future of cancer vaccines. Methods Mol Biol. 1139, 555-564 (2014).
- Magnusson, R., Wawro, D., Zimmerman, S., Ding, Y. Resonant photonic biosensors with polarization-based multiparametric discrimination in each channel. Sensors. 11 (2), 1476-1488 (2011).
- Kaja, S., et al. Detection of novel biomarkers for ovarian cancer with an optical nanotechnology detection system enabling label-free diagnostics. J Biomed Opt. 17 (8), 081412-081411 (2012).
- Magnusson, R., Wang, S. S. New principle for optical filters. Appl. Phys. Lett. 61, 1022-1024 (1992).
- Wawro, D., Tibuleac, S., Magnusson, R., Liu, H. Optical fiber endface biosensor based on resonances in dielectric waveguide gratings. Proc. SPIE. 3911, 86-94 (2000).
- Altman, J. D., et al. Phenotypic analysis of antigen-specific T lymphocytes. Science. 274 (5284), 94-96 (1996).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved