Method Article
Rilevamento dei leucociti umani Antigen Biomarkers in Breast Cancer Utilizzando libero-Label Biosensor Tecnologia
In questo articolo
Riepilogo
Intatte classe I complessi HLA / peptide sono capannone dalle cellule tumorali, che rappresenta un potenziale biomarcatore cancro rilevante. Utilizzando la tecnologia dei sensori senza etichetta e il recettore delle cellule T mimando anticorpi monoclonali, rilevamento di capannone MIF / HLA-A * 02: 01 complessi in sovranatanti cellulari MDA-MB-231, spillo siero umano, e plasma del paziente è dimostrata, consentendo lo sviluppo di un romanzo cancro piattaforma diagnostica.
Abstract
Secondo l'American Cancer Society, più di 200.000 donne saranno con diagnosi di cancro al seno invasivo ogni anno e circa 40.000 moriranno dalla malattia. Campioni La classe antigene leucocitario umano (HLA) I peptidi derivati dal proteasoma degradazione delle proteine cellulari e presenta questi frammenti sulla superficie cellulare per essere interrogati dai linfociti circolanti T citotossici (CTL). Generazione di mimica recettore delle cellule T (TCRM) anticorpi monoclonali (MAK, MAB), che riconoscono il cancro al seno specifico peptide / HLA-A * 02: 01 complessi, come quelli derivati dalla migrazione dei macrofagi fattore inibitorio (MIF 19-27) e NY-ESO- 1 157-165 consentire l'individuazione e la distruzione delle cellule del cancro al seno, in assenza di una efficace risposta CTL anti-tumorale. Intatte classe I complessi HLA / peptide sono capannone dalle cellule di cancro al seno e rappresentano potenzialmente rilevanti biomarcatori tumorali. In questo lavoro, un sistema di screening per il cancro svolta biomarcatore diagnosticos incorporando recettore delle cellule T anticorpi monoclonali mimici combinati con un romanzo, biosensore senza etichetta che utilizza in modalità guidata di risonanza (GMR) tecnologia dei sensori è presentato. Rilevamento di capannone MIF / HLA-A * 02: 01 complessi in sovranatanti cellulari MDA-MB-231, a spillo siero umano e plasma del paziente è dimostrata. L'impatto di questo lavoro potrebbe rivoluzionare la medicina personalizzata attraverso lo sviluppo della diagnostica delle malattie compagno per immunoterapie mirate.
Introduzione
Gli antigeni di classe I (HLA) campioni peptidi di 8-11 aminoacidi di lunghezza derivanti dalla degradazione proteasoma della proteina intracellulare repertorio e presenta questi peptidi sulla superficie di ogni cellula nucleata 1,2. Il complesso HLA è "biomarker della natura", indicante la salute di ogni cella (Figura 1) per circolanti linfociti T citotossici (CTL). Il riconoscimento di malattia associata peptidi provoca l'eliminazione della cellula incriminata dal CTL. Pertanto, la risposta immunitaria adattativa è altamente efficace per eliminare l'infezione virale e tumore. Tuttavia, il sistema immunitario esercita una pressione che spesso promuove selezione di virus o tumore grado di eludere una risposta efficace CTL. Recettore delle cellule T (mimando TCRM) anticorpi monoclonali (MAK, MAB), che riconoscono specifici peptide / HLA-A * 02: 01 complessi, come quelli derivati da proteine associate al cancro al seno, fattore inibitorio migrazione di macrofagi (MIF19-27) 3 e NY-ESO-1 157-165, consentire l'individuazione e la distruzione delle cellule del cancro al seno, in assenza di un anti-tumorale efficace CTL risposta 4,5. Questo lavoro rappresentativo è focalizzata sulla HLA-A * 0201 molecola, che si esprime fino al 30% della popolazione. Tuttavia, l'identificazione delle altre pertinenti complessi HLA / peptide, seguita dalla produzione di TCRM consente lo sviluppo di immunoterapie mirate e diagnostica delle malattie guidata, espandendo l'utilità di questo lavoro ad una popolazione molto più ampio.
Una parte dei complessi peptide / HLA dirette superficie cellulare viene rilasciata nel plasma. A causa della elevata complessità del peptide / piscine HLA, gli attuali metodi per l'estrazione del immunopeptidome per biomarcatori HLA associati sono tempo. Questo processo richiede la purificazione per affinità di HLA solubili dal plasma, separazione dei peptidi HLA associati da fase inversa cromatografia liquida ad alta pressione(RP-HPLC) e peptide sequenziamento mediante spettrometria di massa tandem (MS / MS) 6,7. Anche se questo processo è una valida opzione per la scoperta di nuovi bersagli terapeutici, è un processo complicato come strumento diagnostico compagno per obiettivi connessi HLA già nel vaccino terapeutico o di una condotta biofarmaceutica 8-10. TCRM diretto contro questi obiettivi forniscono gli strumenti per un rapido sviluppo compagno diagnostica volte a stratificazione dei pazienti in studi clinici rilevanti e fornire opzioni terapeutiche più informate.
In questo lavoro, un sistema di screening svolta biomarker per la diagnosi del cancro è presentato che utilizza TCRM e un sistema di test biologico privo di etichetta che controlla le interazioni biologiche con minime fasi di lavorazione. Il sistema di saggio biologico senza etichetta si basa su un metodo, che utilizza l'effetto di risonanza modo guidato (GMR) che si verifica in reticoli guida dielettrica 11-14. Quando la luce a banda larga di diffrazionegrattugiatura nelle piastre necessari per questo sistema, due specifiche lunghezze d'onda vengono riflesse. L'interazione di legame tra un recettore immobilizzato e il suo ligando è monitorata in tempo reale tracciando spostamento della lunghezza d'onda di risonanza con un analizzatore di spettro 12. Picchi di risonanza separati verificano per incidente TE (vettore elettrico normale al piano di incidenza) e TM (magnetica vettore normale al piano di incidenza) stati di polarizzazione forniscono più punti di dati che possono potenzialmente aumentare la precisione di rilevamento 11,14. Utilizzando anticorpi lastre pre-sensibilizzate in questo sistema di analisi privo di etichetta, il tempo di esecuzione del test con l'analisi dei dati è di circa 45 min. Inoltre, più campioni del paziente possono essere interrogati in un formato da 96 o 384 pozzetti, un chiaro vantaggio rispetto un formato basato HPLC-MS / MS.
Protocollo
Etica dichiarazione: campioni De-identificati tessuti e plasma umano sono stati ottenuti da Hendrick Medical Center in un Institutional Review Board ha approvato il protocollo.
1. Aggiunta di anticorpo biotilinato
NOTA: Il monitoraggio di questo passaggio è facoltativo. Vedere protocollo alternativo, se non di monitoraggio.
- Ottenere piastre in commercio derivati rivestito avidina (vedi Materiali e attrezzature Table).
- Aggiungere 50 ml di fosfato salina tamponata (PBS) pH 7,2 per pozzi.
NOTA: Preincubare PBS a 28 ° C per minimizzare relativi alla temperatura risonanza turni. - Aprire software dello scanner bioassay e seguire l'installazione guidata per definire la procedura sperimentale che prevede la selezione di bianchi, standardi e campioni nel layout di piastra, regolazione della temperatura (28 ° C), il numero di scansioni al minuto (1), e la durata della sperimentazione ( 150 min per ospitare per fasi preparative).
- Inserire la piastra di test predisposto nello scanner bioassay libera etichetta e avviare la prima scansione. Quando la prima scansione, selezionare "auto di riferimento per iniziare". La linea di base è l'insieme iniziale di scansioni raccolti all'inizio dell'esperimento. Se questa è la prima lettura effettuata su questa piastra specifica, consentire allo scanner di funzionare per equilibrare la temperatura ed eliminare la deriva della linea di base. Vedere la Figura 2 per uno screenshot di una linea di base seguito da aggiunta del campione.
- Dopo la linea di base è stabilizzato, o almeno 5 scansioni, mettere in pausa la lettura ed espellere la piastra.
- Rimuovere PBS dal dumping nel lavandino e aggiungere 50 microlitri RL21A anticorpo biotinilato a [10 mg / ml in PBS pH 7,2] a tutti, ma pozzetti di controllo sulla piastra. Aggiungere 50 microlitri PBS ai pozzetti di controllo.
- Inserire la piastra posteriore nello scanner bioassay e riprendere la lettura fino a saturazione, di circa 1,5 ore.
- Pausa di lettura ed espellere la piastra.
- Lavare il piastra 3 volte con 200 microlitri / pozzetto tampone fosfato + 0,05% Tween 20 (PBST) seguito da 3 lavaggi con 200 microlitri / pozzetto di PBS pH 7,2. Ripetere con PBS. Toccare eccesso PBS dalla piastra su carta assorbente prima di passare alla fase successiva.
NOTA: Questa fase può essere eseguita su un lavatore automatico delle lastre o lavare la piastra 3 volte con 200 microlitri PBST scaricando liquido in un lavandino e sostituendo PBST con una pipetta. - Aggiungere 50 ml di PBS pH 7,2 per tutti i pozzi attivi.
- Inserire la piastra posteriore nello scanner bioassay e riprendere la lettura per il monitoraggio post-wash risonanza.
- Fermare la lettura ed espellere la piastra.
Protocollo alternativo per Step 1:
- Aggiungere 50 ml RL21A anticorpo biotinilato a [10 mg / ml di PBS] a tutti i pozzetti.
- Incubare a temperatura ambiente per 1,5 ore o per una notte a 4 ° C.
- Lavare la piastra 3 volte con 200 microlitri / bene PBST seguito da 3 risciacqui con 200 microlitri / pozzetto PBS come al punto 1.9.
- Rimuovere la PBS e aggiungere 50 ml per pozzetto di un adeguato tampone. Per questo test, disponibile in commercio siero umano normale è stato utilizzato diluito 1:20 in PBS.
- Aprire software dello scanner bioassay e seguire l'installazione guidata per definire procedura sperimentale.
- Inserire la piastra nello scanner bioassay e iniziare una linea di base leggere. Se questa è la prima lettura effettuata su questa piastra specifica, far funzionare scanner per equilibrare la temperatura ed eliminare la deriva della linea di base.
- Dopo la linea di base è stabilizzato, o almeno 5 scansioni, mettere in pausa la lettura ed espellere la piastra.
- Rimuovere il tampone dai pozzetti.
- Controlli Spike con HLA A * 02: 01 monomero cuscinetto rilevante (FLSL) o irrilevanti (SLLV, YLEV, o KVL) peptidi a concentrazioni che vanno da [,625-10 mg / ml] in tampone. Aggiungere 50 ml di standard ai pozzetti di controllo della piastra
- Aggiungere 50 ml di analita in tampone al campionepozzetti della piastra. Per questo test, a spillo siero umano disponibile in commercio è stata utilizzata.
- Inserire la piastra posteriore nello scanner bioassay e riprendere la lettura fino a saturazione, di circa 30-60 min.
- Pausa di lettura ed espellere la piastra.
- Lavare la piastra 3 volte con 200 microlitri / bene PBST seguito da 3 risciacqui con 200 microlitri / pozzetto PBS come al punto 1.9.
- Aggiungere 50 microlitri tampone a tutti i pozzetti attivi.
- Inserire la piastra posteriore nello scanner bioassay e riprendere la lettura per il monitoraggio post-wash risonanza.
- Fermare la lettura ed espellere la piastra.
NOTA: Il tampone potrebbe essere PBS, tessuto di coltura, o di siero umano diluito 1:20 in PBS a seconda l'obiettivo del test.
Analisi 3. Dati
- Analizzare con il software dello scanner saggio biologico o esportare file di dati grezzi a preferito software di analisi statistica. Il software dello scanner saggio biologico genera automaticamente la curva vincolante basata sullalayout della piastra fornita durante l'installazione sperimentale.
NOTA: Se non si utilizza il software dello scanner saggio biologico per l'analisi, seguire i passaggi 3,2-3,4. - Sottrarre la linea di base e il controllo negativo per ogni successivo punto dati.
- Calcolare la media e la deviazione standard per i pozzi di replica per ogni punto temporale.
- Genera un grafico della curva di legame o selezionare Dati finali per grafici a barre.
Risultati
Un insieme rappresentativo di esperimenti è stata effettuata utilizzando la ben caratterizzato TCRM, RL21A, un anticorpo murino IgG2a monoclonale che riconosce specificamente un peptide (MIF 19-27 o FLSL) nell'ambito del HLA-A * 02: 01 molecola 3. L'affine monomero peptide / HLA, nonché irrilevante HLA monomero 15, è stato utilizzato per dimostrare la procedura descritta. Figura 3 illustra il formato del dosaggio.
RL21A è specifico per il monomero FLSL / HLA con crocetta reattività con altri peptide / HLA complessi 3. Questa specificità è ricapitolato usando il sistema di saggio biologico senza etichetta (Figura 4). La sensibilità del sistema di saggio biologico libera etichetta per questo esperimento è nel range nanomolare basso come determinato mediante titolazione dell'anticorpo RL21A sulla FLSL immobilizzato / HLA monomero (Figura 5). Anche se il segnale di fondo è significativamente aumentata in campioni di siero, srilevamento pecific di FLSL / HLA monomero nel siero umano spillo è raggiunto in figura 6 ed un gradiente di concentrazione è facilmente distinguibile in questi campioni. Infine, supernatanti dalla linea di cellule MDA-MB-231, mostrato in precedenza per presentare la FLSL / HLA-A * 02: 01 molecola, sono indicati per contenere solubile FLSL monomero utilizzando questa piattaforma test gratuito etichetta (Figura 7). La successiva aggiunta di FLSL / HLA monomero aumenta il segnale RL21A (Figura 7). A causa della sensibilità del sistema, oltre alla variazione ben compreso possono verificarsi come risultato di variazioni di temperatura come visto in funzione delle deviazioni standard in figure 4 e 5 turni risonanza negativi. Queste variazioni possono essere ridotti drasticamente pre-incubazione di tutti i campioni e il lettore di piastre saggio biologico ad una temperatura in leggero eccesso di temperatura ambiente (cioè, 28 ° C).
In Figura 8, brevemente, 96-well lastre di polistirene sono stati rivestiti con [10 ug / ml] di RL21A per 2 ore a temperatura ambiente, lavata con PBST, bloccato con 0,5% latte magro, lavato con PBST, e incubate per 2 ore a temperatura ambiente con diluizioni seriali di FLSL HLA monomero nel siero umano normale diluito 1:10 in PBS per generare una curva standard o plasma del paziente diluito 1:10 in PBS. La piastra è stata lavata con PBST, incubate 1 ora a temperatura ambiente con coniglio β2 microglobulina anti-umano [1: 5,000] per rilevare HLA intatto, e lavato in PBST. Le piastre sono state poi incubate per 30 min con capra anti-IgG di coniglio [1: 10.000] e lavati con PBST. Rilevamento colorimetrico stata eseguita usando ABTS (2,2'-Azinobis [acido 3-ethylbenzothiazoline-6-solfonico] sale -diammonium) substrato con un tempo di incubazione 15 min e osservato a 405 nm su un lettore di micropiastre. FLSL / HLA è stata rilevata in tre campioni di pazienti.
Nella Figura 8B, RL.064 plasma del paziente è stato diluito 1:20 in PBS e quindi aggiungereed alla piastra e monitorato sul rivelatore senza etichetta per 60 min. Individuazione specifica del complesso FLSL / HLA nel siero del paziente è stata compiuta. Test t di Student è stato eseguito utilizzando grafici e statistiche software (p <0.05).
In Figura 8C, sezioni di tessuto sono state colorate a 1 mg / ml con topo anti-HLA-A2 (BB7.2) come controllo positivo, RL21A, IgG2b e IgG2a rispettivamente come controlli negativi. La colorazione è stato rilevato utilizzando un kit anti-topo rilevamento, DAB (diaminobenzadine), e QS ematossilina per la colorazione nucleare come indicato dal produttore. La colorazione del tessuto tumorale da RL21A conferma la presentazione di complessi FLSL / HLA.
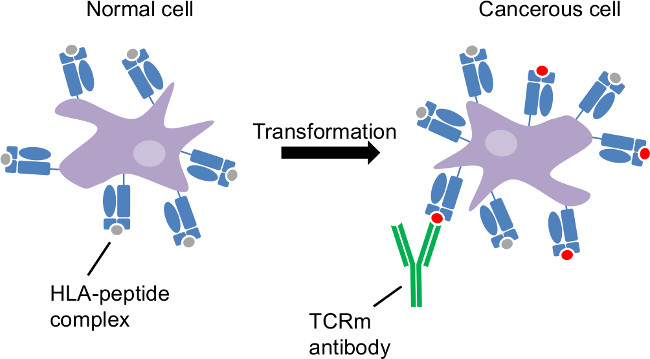
Figura 1:. Tumore presentazione dell'antigene da parte dell'antigene umano leucociti classe I trasformazione cancerosa è un disordine intracellulare. Campione intracellul HLAproteine AR e rivelare i cambiamenti legati al cancro alla superficie cellulare. CTL e TCRM sono in grado di riconoscere le cellule cancerose mediante complessi HLA-peptide distinte a tali cellule.

Figura 2:. Schermata di acquisizione dei dati nel software dello scanner bioassay Esempio di acquisizione dati che mostra la linea di base iniziale scan seguito RL21A anticorpi Oltre a una piastra ricoperta con 10 ug / ml di complesso FLSL / HLA. Le concentrazioni di anticorpi sono come indicato. Ogni linea rappresenta un individuo ben monitorato nel tempo.

Figura 3:. Formato Assay Illustrazione di anticorpi immobilizzato sulla superficie del reticolo di diffrazione della rel piastra test catturaEvant peptide / complessi HLA in soluzione.

Figura 4: Specificità RL21A per FLSL / HLA complesso dimostrazione della specificità del biotinilato RL21A TCRM per la sua rilevante (FLSL) HLA monomero rispetto irrilevante monomero HLA (YLEV, SLLV, e KVL).. Biotinilato RL21A TCRM [10 ug / ml] è stato immobilizzato sulla superficie della piastra rivestita dosaggio avidina e la rilevazione è stata eseguita utilizzando non marcato monomero HLA rilevante o irrilevante [10 ug / ml] in PBS. RL21A era specifico per FLSL / HLA Complex. ANOVA a due vie è stata effettuata utilizzando grafici e statistiche software (p <0.001).

Figura 5:. Binding sensibilità del RL21A al suo peptide complesso affine / HLA Illustrazione del detectiil limite di sensibilità e RL21A legame al complesso FLSL / HLA. Biotinilato HLA Monomero FLSL [10 ug / ml] è stato immobilizzato sulla superficie della piastra del test e RL21A non marcato è stato aggiunto alla piastra in diluizioni seriali in PBS come indicato. Rilevamento di questo sistema era nell'intervallo nanomolare bassa.
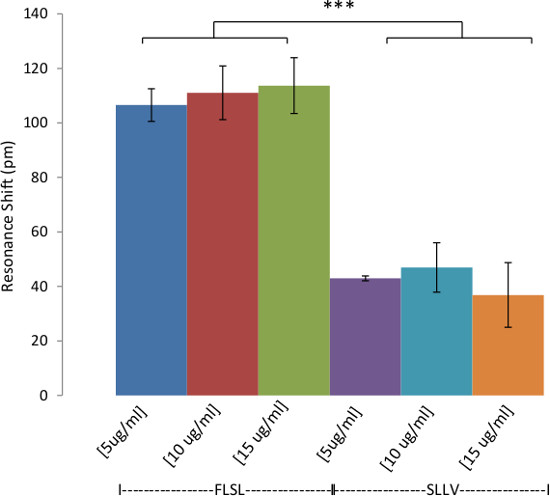
Figura 6: Rilevamento di HLA Complessi in Spiked Human Serum Dimostrazione della rilevazione di HLA nel siero umano.. Biotinilato RL21A TCRM [10 mg / ml] è stato immobilizzato sulla superficie della piastra test avidina rivestita. Siero umano normale pool di spillo con relativa (FLSL) o irrilevanti (SLLV) HLA monomero è stato diluito 1:20 in PBS e poi aggiunto alla piastra e monitorato sul rivelatore senza etichetta per 60 min. Individuazione specifica del complesso FLSL / HLA nel siero umano è stato compiuto. In generale, segnale di fondo (irrilevante SLLV monomero) è altoer per i campioni di siero diluiti rispetto al analiti purificate in PBS (vedi Figura 4). Due vie ANOVA è stata effettuata utilizzando grafici e statistiche software (p <0,0001).
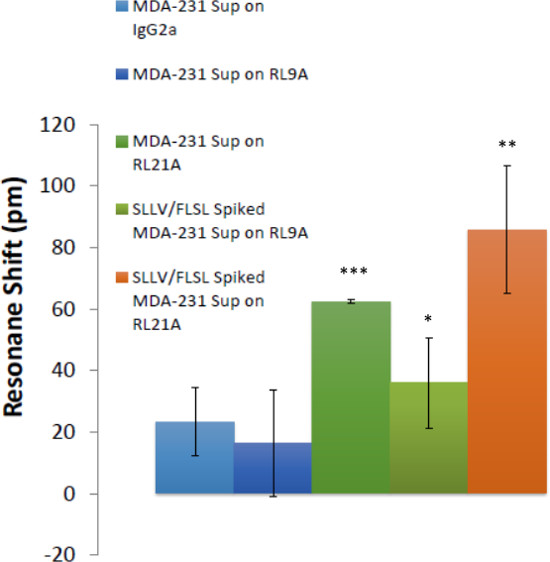
Figura 7:. Complessi HLA sono stati rilevati nel cancro al seno supernatanti di colture cellulari La capacità di rilevare HLA in seno surnatanti di cellule di cancro è dimostrata. Biotinilato RL21A TCRM, RL9A TCRM (controllo negativo), e un controllo isotipico state immobilizzate sulla superficie della piastra test. Spiked [5 mg / ml] e non addizionati supernatanti di colture cellulari MDA-231 sono stati aggiunti e vincolante è stata monitorata per 60 minuti sul rivelatore senza etichetta. FLSL e SLLV HLA monomero spillo campioni rappresentano controlli positivi per RL9A e RL21A vincolanti. One-way ANOVA è stata effettuata utilizzando grafici e statistiche software (p <0,0001).
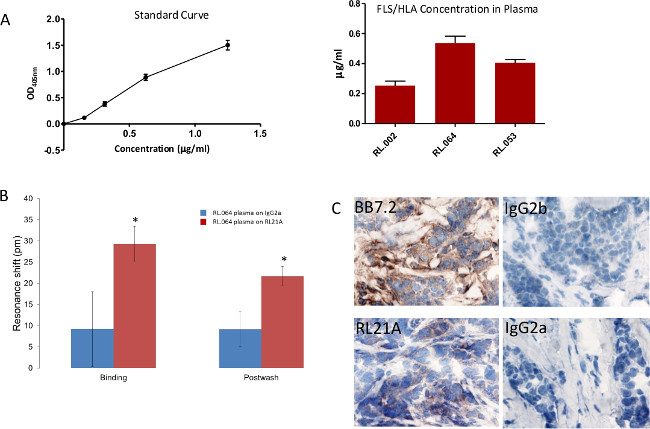
Figura 8:. Rilevamento specifico di complessi FLSL / HLA in campioni dei pazienti (A) Un enzima tradizionale Immunoenzimatico Assay (ELISA) è stata utilizzata per rilevare FLSL / HLA complessi specifici nel plasma dei pazienti. (B) biotilinato RL21A TCRM o IgG2a [10 mg / ml] è stato immobilizzato sul piatto test avidina. (C) tessuto tumorale del seno da RL.064 paziente era macchiato come descritto in precedenza 3 per verificare presentazione tumore dei complessi FLSL / HLA. Clicca qui per vedere una versione più grande di questa figura.
Discussione
Il metodo descritto introduce un sistema di screening per la diagnosi del cancro biomarker che permettano la rapida individuazione di solubili complessi peptide / HLA in campioni di siero, plasma, urina o saliva di pazienti in un volume alto 96- o 384 pozzetti. Questo sistema di dosaggio utilizzando recettore delle cellule T imitando anticorpi monoclonali e un sistema di rilevamento senza etichetta taglia il tempo di analisi per meno di 1 ora rispetto a 3,5 hr mediante ELISA convenzionale. Questo approccio high-throughput consente una rapida stratificazione dei pazienti per gli studi clinici per i vaccini terapeutici del cancro o farmaci biologici. Gli attuali metodi per l'individuazione di questi obiettivi di malattia richiedono purificazione per affinità e HPLC-MS / MS dei campioni individuali, un processo che richiede tempo e ingombrante. Anche se questo metodo è suscettibile di tecniche convenzionali ELISA, vi è la preoccupazione che i reagenti di rivelazione secondari come l'anticorpo anti-microglobulina β2 potrebbero alterare la struttura del nascente HLUna molecola ed inibire il legame al rilevamento limitazione TCRM. Free Detection-Label allevia queste preoccupazioni. Questa procedura può essere modificata per l'uso su altri sistemi senza etichetta come un sistema di risonanza plasmonica di superficie. Tuttavia, ciò ridurrebbe notevolmente le capacità di throughput superiori rispetto al sistema di saggio biologico utilizzato in questo studio.
Questo protocollo può essere efficacemente modificato per l'individuazione di biomarker non-HLA nel siero del paziente e plasma con aderenza ad alcuni punti critici. Il monitoraggio del processo di rivestimento anticorpo iniziale è raccomandato per l'ottimizzazione della superficie, come <200 pm spostamento probabilmente porterà a segnale basso per la fase successiva rilevazione. La linea di base e post-wash legge sono utili per l'analisi finale, come l'abbondanza di proteine del siero può mascherare vincolante di bassa concentrazione dell'analita. Infine, variazione di temperatura dei campioni può provocare a variazioni ben bene. Si raccomanda che tutti i campioni siano pre-incubate und il biosassay libera termoregolatore unità etichetta fissato a 2-3 ° C sopra la temperatura ambiente. Campioni refrigerati dovrebbe essere consentito un tempo sufficiente per raggiungere la temperatura di esercizio.
Modifiche future di questo protocollo comprenderanno multiplexing del TCRM sulla superficie della piastra. Il sistema biologico è attualmente suscettibili di macchia di pozzetti ad una densità di almeno 8-plex. Con l'introduzione di 4-8 TCRM a ciascun pozzetto, per volumi di campione di prova sono ridotti e consentire la raccolta di dati sempre più complesse per paziente. Questa capacità potrebbe informare ulteriormente i pazienti per quanto riguarda le opzioni terapeutiche.
Divulgazioni
Gli autori, Debra Wawro Weidanz e Robert Magnusson, rispettivamente Amministratore Delegato e Chief Technology Officer di Resonant Sensori Incorporated, che produce il lettore e test piastra piastre bioassay utilizzati in questo articolo.
Riconoscimenti
These studies were supported in part by the Development Corporation of Abilene which provides laboratory space and salary support for Experimmune, a Center for Immunotherapeutic Development at Texas Tech University Health Sciences Center and Resonant Sensors Incorporated.
Materiali
| Name | Company | Catalog Number | Comments |
| Name of the Material/Equipment | Company | Catalog Number | Comments/Description (optional) |
| ResoSens Label-free Bioassay Detection System | Resonant Sensors Incorporated | ||
| Avidin Sensitized Bionetic 96-well Plates | Resonant Sensors Incorporated | ||
| ResoVu software | Resonant Sensors Incorporated | ||
| RL21A Biotinylated TCRm mAb | PureMHC, LLC | ||
| RL9A Biotinylated TCRm mAb | PureMHC, LLC | ||
| FLSL HLA-A*02:01 Monomer | Experimmune | full peptide sequence: FLSELTQQL | |
| SLLV HLA-A*02:01 Monomer | Experimmune | full peptide sequence: SLLMWITQV | |
| YLEV HLA-A*02:01 Monomer | Experimmune | full peptide sequence: YLEPGPVTV | |
| KVL HLA-A*02:01 Monomer | Experimmune | full peptide sequence: KVLEYVIKV | |
| Pooled Normal Human Serum | ThermoFisher | BP2657100 | |
| MDA-MB-231 Cell Supernatant | ATCC | HTB-26 | Cells grown in IMDM , 10% FBS and 1% penn/strep. Supernatants harvested from 3 day confluent cultures. |
| Iscove's Modification of Dulbecco's Medium (IMDM) | Life Technologies | 12440-053 | |
| Fetal Bovine Serum (FBS) | Life Technologies | 10082-147 | |
| Penicillin/Streptomycin | Life Technologies | 15070-63 | |
| Sodium Hydroxide | ThermoFisher | 5318-1 | |
| Phosphate Buffered Saline (PBS) | ThermoFisher | BP665-1 | |
| Phosphate Buffered Saline + 0.05% Tween 20 (PBST) | ThermoFisher | BP337-500 | |
| 2,2’-Azinobis [3-ethylbenzothiazoline-6-sulfonic acid]-diammonium salt (ABTS) | ThermoFisher | 37615 | |
| rabbit anti-human β2 microglobulin | Dako | A0072 | |
| Peroxidase conjugated goat anti-rabbit IgG | Jackson Immunoresearch | 111-035-144 | |
| Nunc microplates | ThermoFisher | 439454 | |
| Synergy 2 microplate reader | Biotek | ||
| Immpress Reagent Kit | Vector | MP-7402 | |
| Immpact DAB | Vector | SK-4105 | |
| Hematoxylin QS | Vector | H3403 | |
| IgG2a | MP BioMedicals | 50328 | |
| IgG2b | MP BioMedicals | 50330 | |
| anti-HLA-A2 (BB7.2) | Experimmune | ||
| Prism 5 | Graphpad |
Riferimenti
- Shastri, N., Schwab, S., Serwold, T. Producing nature's gene-chips: the generation of peptides for display by MHC class I molecules. Annu Rev Immunol. 20, 463-493 (2002).
- Peaper, D. R., Cresswell, P. Regulation of MHC class I assembly and peptide binding. Annu Rev Cell Dev Biol. 24, 343-368 (2008).
- Hawkins, O., et al. An HLA-presented fragment of macrophage migration inhibitory factor is a therapeutic target for invasive breast cancer. J Immunol. 186 (11), 6607-6616 (2011).
- Verma, B., et al. TCR mimic monoclonal antibody targets a specific peptide/HLA class I complex and significantly impedes tumor growth in vivo using breast cancer models. J Immunol. 184 (4), 2156-2165 (2010).
- Verma, B., et al. TCR mimic monoclonal antibodies induce apoptosis of tumor cells via immune effector-independent mechanisms. J Immunol. 186 (5), 3265-3276 (2011).
- Bassani-Sternberg, M., et al. Soluble plasma HLA peptidome as a potential source for cancer biomarkers. Proc Natl Acad Sci U S A. 107 (44), 18769-18776 (2010).
- Hickman, H. D., Yewdell, J. W. Mining the plasma immunopeptidome for cancer peptides as biomarkers and beyond. Proc Natl Acad Sci U S A. 107 (44), 18747-18748 (2010).
- Neethling, F. A., et al. Assessing vaccine potency using TCRmimic antibodies. Vaccine. 26 (25), 3092-3102 (2008).
- Mittendorf, E. A., et al. Clinical trial results of the HER-2/neu (E75) vaccine to prevent breast cancer recurrence in high-risk patients: from. US Military Cancer Institute Clinical Trials Group Study I-01 and I-02. Cancer. 118 (10), 2594-2602 (2012).
- Winter, H., Fox, B. A., Ruttinger, D. Future of cancer vaccines. Methods Mol Biol. 1139, 555-564 (2014).
- Magnusson, R., Wawro, D., Zimmerman, S., Ding, Y. Resonant photonic biosensors with polarization-based multiparametric discrimination in each channel. Sensors. 11 (2), 1476-1488 (2011).
- Kaja, S., et al. Detection of novel biomarkers for ovarian cancer with an optical nanotechnology detection system enabling label-free diagnostics. J Biomed Opt. 17 (8), 081412-081411 (2012).
- Magnusson, R., Wang, S. S. New principle for optical filters. Appl. Phys. Lett. 61, 1022-1024 (1992).
- Wawro, D., Tibuleac, S., Magnusson, R., Liu, H. Optical fiber endface biosensor based on resonances in dielectric waveguide gratings. Proc. SPIE. 3911, 86-94 (2000).
- Altman, J. D., et al. Phenotypic analysis of antigen-specific T lymphocytes. Science. 274 (5284), 94-96 (1996).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon