このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
酸化還元活性金属-有機骨格の固体電気化学における中間体の磁気特性評価
要約
Ex situ 磁気探査は、磁気電極に関するバルクおよび局所情報を直接提供して、その電荷蓄積メカニズムを段階的に明らかにすることができます。ここでは、電子スピン共鳴(ESR)と磁化率が、酸化還元活性金属有機骨格(MOF)中の常磁性種とその濃度の評価を監視するために実証されています。
要約
電気化学的エネルギー貯蔵は、過去5年間に酸化還元活性金属有機構造体(MOF)の応用として広く議論されてきました。MOFは、重量または面容量とサイクル安定性の点で優れた性能を示しますが、残念ながら、その電気化学的メカニズムはほとんどの場合よく理解されていません。X線光電子分光法(XPS)やX線吸収微細構造(XAFS)などの従来の分光技術は、特定の元素の価数変化に関する曖昧で定性的な情報しか提供しておらず、そのような情報に基づいて提案されたメカニズムはしばしば非常に議論の余地があります。本稿では、固体電気化学セルの作製、電気化学測定、セルの分解、MOF電気化学中間体の回収、不活性ガス保護下での中間体の物理測定など、一連の標準化された方法を報告します。これらの手法を用いて、酸化還元活性MOFの単一の電気化学的ステップにおける電子およびスピン状態進化を定量的に明らかにすることにより、MOFだけでなく、強く相関する電子構造を持つ他のすべての材料の電気化学的エネルギー蓄積メカニズムの性質を明確に理解することができます。
概要
1990年代後半、特に2010年代に金属有機フレームワーク(MOF)という用語が導入されて以来、MOFに関する最も代表的な科学的概念は、ゲストカプセル化、分離、触媒特性、分子センシングなどの構造的多孔性から生じてきました1,2,3,4 .一方、科学者たちは、MOFを最新のスマートデバイスに統合するには、刺激応答性電子特性を持つことが不可欠であることをすぐに認識しました。このアイデアは、過去10年間で導電性2次元(2D)MOFファミリーの誕生と繁栄を引き起こし、それによってMOFがエレクトロニクス5、そしてより魅力的な電気化学エネルギー貯蔵デバイス6で重要な役割を果たすための門を開きました。これらの2次元MOFは、アルカリ金属電池、水系電池、擬似キャパシタ、スーパーキャパシタ7,8,9の活物質として組み込まれており、優れた安定性とともに驚異的な容量を示しています。ただし、より高性能な2D MOFを設計するには、電荷蓄積メカニズムを詳細に理解することが重要です。したがって、この記事は、エネルギー貯蔵アプリケーション向けのより高性能なMOFの合理的な設計に役立つMOFの電気化学的メカニズムの包括的な理解を提供することを目的としています。
2014年には、金属カチオンと配位子の両方に酸化還元活性点を持つMOFの固体電気化学的メカニズムを初めて報告しました10,11。これらのメカニズムは、X線光電子分光法(XPS)、X線吸収微細構造(XAFS)、X線回折(XRD)、固体核磁気共鳴(NMR)など、さまざまなin situおよびexsitu分光技術の助けを借りて解釈されました。それ以来、この研究パラダイムは、分子ベースの材料の固体電気化学の研究における傾向となっています12。これらの方法は、金属クラスタービルディングブロックと有機配位子の分子軌道とエネルギー準位がそのようなMOFで互いにほぼ独立しているため、カルボン酸架橋配位子を持つ従来のMOFの酸化還元イベントを特定するのに適しています12,13。
しかし、有意なπ-d共役を伴う強相関2D MOFに遭遇すると、これらの分光法の限界が露呈した。これらの制限の1つは、前述のほとんどの2D MOFのバンドレベルは、金属クラスターと配位子の単純な組み合わせと見なすことはできず、むしろそれらのハイブリッド化であるのに対し、ほとんどの分光法は酸化状態に関する平均化された定性的情報しか提供しないことです14。他の制限は、これらのデータの解釈が常に局在原子軌道の仮定に基づいていることです。したがって、金属-配位子ハイブリダイゼーションおよび非局在化電子状態との中間状態は、通常、これらの分光法のみでは見落とされ、誤って記述される15。これらの電気化学中間体の電子状態を解明するプローブは、2次元MOFだけでなく、共有結合有機骨格16、分子伝導体、共役高分子17など、共役系または強相関電子構造が類似する他の材料についても、新しいプローブを開発する必要があります。
材料の電子構造を評価するための最も一般的で強力なツールは、電子スピン共鳴(ESR)および超伝導量子干渉デバイス(SQUID)の磁化率測定です18,19。どちらも系内の不対電子に依存しているため、これらのツールは、スピン密度、スピン分布、およびスピン-スピン相互作用に関する暫定的な情報を提供できます。ESRは不対電子の高感度検出を提供し、磁化率測定は上位特性20に対してより定量的な信号を提供します。残念ながら、どちらの手法も電気化学中間体の分析に使用すると、必然的に大きな課題に直面します。これは、ターゲット試料が純粋ではなく、ターゲット材料、導電助剤、結着剤、電解液からの副生成物の混合物であるため、得られたデータ21、22は、材料と不純物の両方からの寄与の合計であるためである。一方、ほとんどの中間体は、空気、水、特定の電解質、またはその他の予測不可能な摂動を含む環境に敏感です。中間体の取り扱いと測定には特別な注意が必要です。通常、電極材料と電解質の新しい組み合わせを扱う際には、試行錯誤が必要です。
ここでは、電気化学と温度可変のex situESR分光法、およびex situ磁化率測定を利用して、一連の手法を使用して2D MOFおよび同様の材料の電子状態またはスピン状態を分析するための電気化学磁気測定と呼ばれる新しいパラダイムを提示します20。このアプローチの有効性を実証するために、代表的な2D MOFであるCu3THQ2(THQ=1,2,4,5-テトラヒドロキシベンゾキノン;Cu-THQと呼ぶ)を例として使用します。導電助剤や電解質の選定、電極や電気化学セルの作製、測定時の問題点など、サンプルの取り扱いや測定の詳細についてご説明します。電気化学磁気測定は、XRDやXAFSなどの従来の特性評価と比較することにより、ほとんどのMOFの電気化学的メカニズムを包括的に理解できます。このアプローチは、固有の中間状態をキャプチャし、酸化還元イベントの誤った割り当てを回避することができます。電気化学磁気測定を用いたエネルギー貯蔵機構の解明は、MOFの構造と機能の関係の理解にも貢献し、MOFやその他の共役材料のよりインテリジェントな合成戦略につながります。
Access restricted. Please log in or start a trial to view this content.
プロトコル
1. 電極作製
- Cu-THQ MOF の合成
注:Cu−THQ MOF多結晶粉末は、以前に公開された手順14、20、23に従って水熱法を介して合成された。- 60 mgのテトラヒドロキシキノンを20 mLのアンプルに入れ、次に10 mLの脱気水を加えます。別のガラスバイアルに、110 mgの硝酸銅(II)三水和物を別の10 mLの脱気水に溶解します。ピペットを使用して46 μLの競合配位子エチレンジアミンを加えます。
注意: 脱イオン水を脱気するには、使用前に窒素ガスを30分間流してください。反応混合物の加熱時間が長すぎると、43°付近に回折ピーク(Cu Kα)が現れたCu不純物が形成されることがあります。 - テトラヒドロキシキノンを含むアンプルに銅溶液を導入する。溶液の色はすぐに赤から紺に変わります。得られた溶液を凍結、ポンプ、および解凍24を3回して、溶存酸素をさらに除去する。
- 真空下でトーチを使用してアンプルをフレームシールします。溶液を60°Cに4時間加熱します。
- 反応後、アンプルを慎重に開き、上清を取り除きます。沈殿物を室温脱イオン水3x30 mLおよび熱脱イオン水30 mL(80°C)で3x遠心分離し、10,000 rpmで5分間洗浄します。
- 振とうして沈殿物をアセトンに分散させ、次いで濾過し、アセトンで洗浄する。製品を真空下で353 Kで一晩加熱し、Cu-THQ MOF中の残留溶媒を除去します。
- 60 mgのテトラヒドロキシキノンを20 mLのアンプルに入れ、次に10 mLの脱気水を加えます。別のガラスバイアルに、110 mgの硝酸銅(II)三水和物を別の10 mLの脱気水に溶解します。ピペットを使用して46 μLの競合配位子エチレンジアミンを加えます。
- CuTHQ 電極の準備
注:Cu-THQ MOFと電極を区別するために、前者はCu-THQと呼ばれ、Cu-THQ、カーボン、およびバインダーの混合物は単にCuTHQと呼ばれます。- Cu-THQ/CB/PVDF電極を作製するには、10 mgのポリフッ化ビニリデン(PVDF)を1.4 mLのN-メチル-2-ピロリドン(NMP)に溶解します。50 mgのCu-THQ MOFと40 mgのカーボンブラック(CB)を一晩激しく攪拌して溶液に分散させます。均質なスラリーを直径15 mm、質量~9.7 mgのAlディスクにコーティングします。
- Cu-THQ/Gr/SP/SA電極を作製するには、Cu-THQ/CB/PVDF電極と同じ手順で、スラリー組成が異なります:Cu-THQ MOF(80 mg)、アルギン酸ナトリウム(SA、2 mg)、およびグラフェン/スーパーP(Gr/SP、重量比1:1.8希釈、合計18 mg)水/イソプロパノール(体積比1:1希釈、合計1.2 mL)。
- 電極を真空下で353 Kで12時間乾燥させます。乾燥後の窒素ガスを抜き、質量負荷を測定します。
2.バッテリーの組み立てと後処理
注意: 電気化学中間体の空気に敏感な性質のため、バッテリーの組み立てと後処理は、厳格な空気のない方法でアルゴングローブボックスで実行する必要があります。
- Li/CuTHQコイン電池の組み立て
- バッテリーを組み立てる前に、直径15.5 mmのリチウムディスクと直径17 mmのCelgardセパレーターをいくつか切断します。
- Li/CuTHQコイン電池(CR2032)を下から上に、マイナスシェル、スペーサー(高さ= 0.5 mm)、リチウム、セパレーター、CuTHQ電極(手順1.2.1または1.2.2で準備)、スペーサー、スプリング、プラスシェルの順に組み立てます(図1A)。
- セパレーターを追加する前後に、合計0.04 mLの電解質(エチレンカーボネート(EC)/ジエチルカーボネート(DEC)中の1.0 M LiBF4 を1:1 wt%で滴下します。組み立てた後、コイン電池を保持するために金属製のピンセットを使用しないでください。
- 電気化学中間体の調製
- 自家製のデバイス(図1B)で締め付けネジ(密閉されていない)を使用してコイン電池を圧縮し、デバイスをグローブボックス内の測定ケーブルに接続します。機器(グローブボックスの外側)をコイン電池に対応するポートに接続します。サイクリックボルタンメトリーおよびガルバノスタティック充放電測定20 を実行して、異なる電位で中間体を達成します(図2)。
- 電気化学的サイクルの後、短絡を避けるためにコイン電池を慎重に分解してください。
- サイクルしたCuTHQ電極を5mLのバッテリーグレードの炭酸ジメチル(DMC)ですすぎます。電極を30分間自然乾燥させます。きれいなヘラを使用して、AlディスクからAlホイルにサンプルを収集します。
- サンプル粉末を自家製のガラス漏斗を通してESRチューブまたはSQUIDチューブに移します(図1C)。サンプルチューブをキャップと透明フィルムでしっかりと密封します。あるいは、サンプルチューブをゴムチューブに接続してバルブでシールし、続いて真空下でサンプルチューブのヘッドをフレームシールします。
- 磁気測定20の後、サンプルチューブを開き、サンプルをAl箔上にダンプします。空気中で0.01 mgの分解能を持つ分析天びんを使用してサンプルの質量を測定します。試料の総質量からCu-THQの質量を推定します。
注:サイクルされたCu-THQ MOFの質量は、使用する電極のタイプに応じて、総質量の50%または80%と推定されます。この推定値は、挿入されたLiイオンと残留電解質を考慮していません。
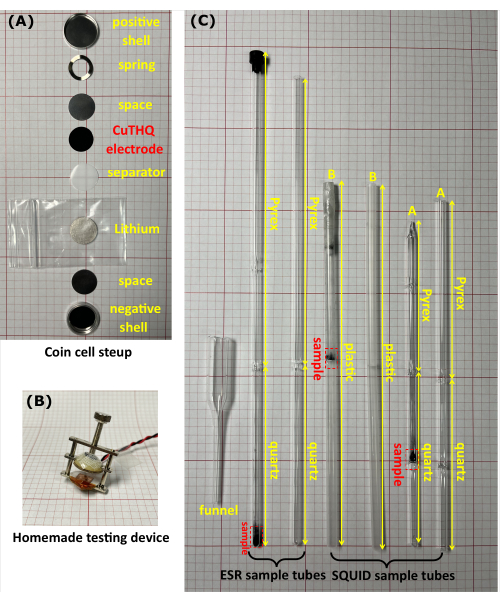
図1: その場 磁気測定実験に使用した装置 。 (A)CR2032コイン電池の写真。(B)自家製の装置を使用して、グローブボックス内の密封されていないコインセルを評価しました。(C)ESRおよびSQUIDサンプルチューブの写真(サンプルが入った場合とない場合)。ESRチューブは、10cmの高純度石英チップ(測定部)と17cmのホウケイ酸ガラスヘッドで構成されています。SQUIDチューブには2種類あります。チューブAは、中点に石英振動板を備えた2 cm x 5 cmの石英チップと10 cmのホウケイ酸ガラスヘッドで構成され、チューブBは、中点にプラスチックダイアフラムを備えたプラスチックチューブ(長さ20 cm)です。すべてのサンプルチューブの外径は5mmです。 この図の拡大版を表示するには、ここをクリックしてください。
3. 可変温度でのESRスペクトルの登録
- 室温でのESRスペクトルの記録
- ESR分光計の準備ができたら、準備したサンプルチューブをマイクロ波キャビティに挿入し、サンプルを中央に配置します。マイクロ波の位相、結合、周波数を自動調整して、キャビティの共振状態に到達します。画面中央のQディップで、対称的な形状と最大奥行きを確認します。
注意: サンプルにカーボンブラックなどの導電性カーボンが多すぎると、オートチューンプロセスが失敗したり、キャビティの品質係数(Q値)が小さくなったりする可能性があります。サンプルの典型的な質量は3 mgです。 - 次のような最適なパラメータを選択します:マイクロ波:電力;磁場:掃引時間;センターフィールド:スイープ幅;変調:周波数、幅;チャンネル:振幅、時定数。次に、磁場を掃引し、ESRスペクトルを記録します。測定パラメータの代表的な値を図 3 と 図4に示します。
- Mnマーカーの挿入量を800に調整します。手順3.1.1と3.1.2を繰り返して、MnマーカーでESRスペクトルを記録します。Mn(II)イオンに6本の超微細線を使用して磁場を校正します。
- ESR分光計の準備ができたら、準備したサンプルチューブをマイクロ波キャビティに挿入し、サンプルを中央に配置します。マイクロ波の位相、結合、周波数を自動調整して、キャビティの共振状態に到達します。画面中央のQディップで、対称的な形状と最大奥行きを確認します。
- Cu-THQのライン形状解析
- ESR データセットを Python (バージョン 3.9.7) にインポートします。強度をサンプル質量、マイクロ波電力の平方根、変調幅、および振幅で割って、ESRスペクトルを正規化します。
- 準備された状態でのCu-THQ MOFのキャリブレーションおよび正規化されたESRスペクトルを軸対称ローレンツ関数25に適合させます。
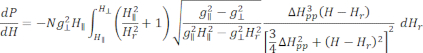
ここで、Nは計器パラメータgrlとHII定数を含むスケール係数、(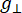 および
および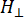 )はランダーg係数と対応する共鳴磁場の平行(垂直)成分、ΔHppはピークtoピーク線幅、Hrは整数変数です。
)はランダーg係数と対応する共鳴磁場の平行(垂直)成分、ΔHppはピークtoピーク線幅、Hrは整数変数です。
注: ローレンツ関数の Python コードは、補足コーディング ファイル 1 (AxialLorentz という名前) にあります。 - 軸対称Cu(II)イオンの異方性g値とピークtoピーク線幅を取得します。
- キャリブレーションおよび正規化されたESRスペクトルを、ラジカルサンプルのローレンツ関数に適合させます。ラジカルの等方性g値とピークtoピーク線幅を取得します。
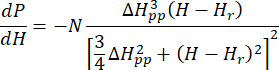
これは、補足コーディングファイル1ではSymLorentzと名付けられています。
- ラジカル濃度の定量
- 3.45 mgの4-ヒドロキシ-2,2,6,6-テトラメチルピペリジン-1-オキシル(TEMPOL)と96.55 mgのKBrをメノウ乳鉢で一緒に粉砕し、均一な混合物が得られます。1 mg(0.2 μmol)、2 mg(0.4 μmol)、および4 mg(0.8 μmol)のTEMPOL/KBr混合物をそれぞれ3つのESRサンプルチューブに入れます。
- 手順3.1.1および3.1.2に従って、TEMPOL/KBr標準のESRスペクトルを記録します。
- ESRスペクトルの二重積分とTEMPOL/KBr標準におけるスピン数との間の線形ベースラインフィッティングを行います。TEMPOL/KBr標準26の線形ベースラインを使用して、サイクルされたCu-THQのスピン数を決定します。
- 低温でのESRスペクトルの記録
注意: 極低温を達成するには、液体ヘリウムを使用してください。液体ヘリウムを扱うときは極低温手袋を着用する必要があります。- まず、ステップ3.1に従って、室温でのESRスペクトルを確認します。
- サーマルシールドを高真空レベルまで排気します。結露を避けるために、窒素ガスを使用してマイクロ波キャビティをパージします。
- 容器からクライオスタットに液体ヘリウムを導入します。サンプルを徐々に最低温度(約10 K)まで冷却します。熱平衡に達するまで30分待ちます。
- 加温中の温度依存ESRスペクトルを記録します。ESRスペクトルが低温での電力飽和の影響を受けず、電力飽和がない場合でも信号強度(ピークtoピーク高さ)とマイクロ波電力の平方根の比率が一定であることを確認してください。
注意: 電力が飽和すると、信号強度はマイクロ波電力の平方根よりもゆっくりと増加します。サンプリング密度は、温度が上昇するにつれて徐々に低下する可能性があります。
4. 磁化率測定
- サンプルチューブをサンプルロッドの底に取り付けます。サンプルチューブの表面がきれいであることを確認してください。
- サンプルチャンバーをパージし、サンプルチューブをSQUIDに挿入します。磁場を印加し、サンプルを検出コイル内の中央に配置します。センタリング後に外部磁場を除去します。
注:スピン濃度が低すぎて検出できない場合は、磁場を増やすか、冷却後にセンタリングを2 Kにすることを検討してください。SQUID測定の典型的なサンプル質量は約6mgです。 - システムを 10 K/分の速度で 20 K まで冷却します。冷却を30分間一時停止してから、さらに2 Kまで1時間冷却します。
- 300 Kに加温しながら、1,000 Oeの磁場下でサイクルしたCuTHQ電極の磁化率を測定します。これは、ゼロフィールド冷却(ZFC)プロセスと呼ばれます。次に、再び2 Kまで冷却し、界磁冷却(FC)プロセスにおける磁化率を記録します。
- CuTHQ電極を異なる還元度で循環させて、手順4.1〜4.4を繰り返します。
- 同じ条件で炭素材料の磁化率(Gr/SP)を測定します。この結果を使用して、CuTHQ電極の磁化率を補償します。
- 磁化率の温度依存性を修正したキュリーワイスの法則に適合させます。
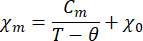
ここで、χ m はモル磁化率、Cmはモルキュリー定数、θ はワイス温度、χ0は温度に依存しない項です。
Access restricted. Please log in or start a trial to view this content.
結果
以前の研究では、電気化学的にサイクルされたCuTHQ20のex situESR分光法とex situ磁化率測定の詳細な議論が含まれていました。ここでは、この論文で説明されているプロトコルに従って得られる最も代表的で詳細な結果を示します。
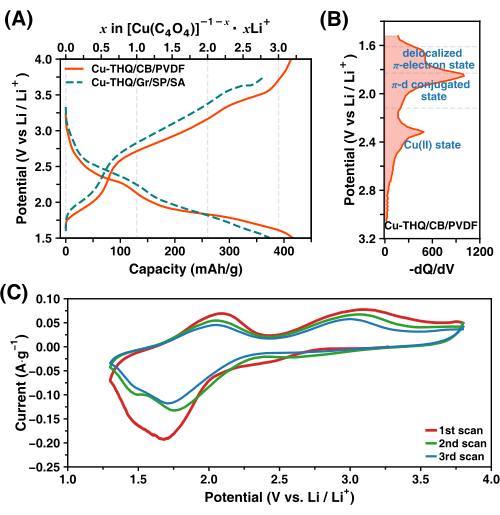
...
Access restricted. Please log in or start a trial to view this content.
ディスカッション
カソードを製造するには、電気化学的プロセス中に低分極を達成するために、活物質を導電性炭素と混合する必要があります。炭素添加剤は、 その場 磁気測定の最初の臨界点です。炭素にラジカル欠陥がある場合、電気化学的に誘導された有機ラジカルの出現はESRスペクトルで観察できません。これは、これら2種類のラジカルが類似したg値を有し、それらのESR線が重なる可能性があ...
Access restricted. Please log in or start a trial to view this content.
開示事項
著者には、宣言する利益相反はありません。
謝辞
本研究は、日本学術振興会(JSPS)科研費(JP20H05621)の助成を受けて行われました。Z. Zhangはまた、立松財団と豊田理研奨学金の財政的支援に感謝しています。
Access restricted. Please log in or start a trial to view this content.
資料
| Name | Company | Catalog Number | Comments |
| 1-Methyl-2-pyrrolidone | FUJIFILM Wako Chemicals | 139-17611 | Super Dehydrated |
| 1mol/L LiBF4 EC:DEC (1:1 v/v%) | Kishida | LBG-96533 | electrolyte |
| 4-Hydroxy-2,2,6,6-tetramethylpiperidine-1-oxyl | FUJIFILM Wako Chemicals | 089-04191 | TEMPOL, for Spin Labeling |
| Ampule tube | Maruemu Corporation | 5-124-05 | 20mL |
| Carbon black, Super P Conductive | Alfa Aesar | H30253 | |
| Conductive Carbon Black | Mitsubishi Chemical | ||
| Copper (II) Nitrate Trihydrate | FUJIFILM Wako Chemicals | 033-12502 | deleterious substances |
| Dimethyl Carbonate | FUJIFILM Wako Chemicals | 046-31935 | battery grade |
| Ethylenediamine | FUJIFILM Wako Chemicals | 053-00936 | deleterious substances |
| Graphene Nanoplatelets | Tokyo Chemical Industry | G0442 | 6-8nm(thick), 15µm(wide) |
| Poly(vinylidene fluoride) | Sigma Aldrich | 182702 | |
| Potassium Bromide | FUJIFILM Wako Chemicals | 165-17111 | for Infrared Spectrophotometry |
| Sodium Alginate | FUJIFILM Wako Chemicals | 199-09961 | 500-600 cP |
| SQUID Magnetometer | Quantum Design | MPMS-XL 5 | |
| Tetrahydroxy-1,4-benzoquinone Hydrate | Tokyo Chemical Industry | T1090 | |
| X-Band ESR | JEOL | JES-F A200 |
参考文献
- Lee, J., et al. Metal-organic framework materials as catalysts. Chemical Society Reviews. 38 (5), 1450-1459 (2009).
- Dolgopolova, E. A., Rice, A. M., Martin, C. R., Shustova, N. B. Photochemistry and photophysics of MOFs: steps towards MOF-based sensing enhancements. Chemical Society Reviews. 47 (13), 4710-4728 (2018).
- Qian, Q., et al. MOF-based membranes for gas separations. Chemical Reviews. 120 (16), 8161-8266 (2020).
- Wang, Q., Astruc, D. State of the art and prospects in metal-organic framework (MOF)-based and MOF-derived nanocatalysis. Chemical Reviews. 120 (2), 1438-1511 (2020).
- Wang, M., Dong, R., Feng, X. Two-dimensional conjugated metal-organic frameworks (2D c-MOFs): chemistry and function for MOFtronics. Chemical Society Reviews. 50 (4), 2764-2793 (2021).
- Baumann, A. E., Burns, D. A., Liu, B., Thoi, V. S. Metal-organic framework functionalization and design strategies for advanced electrochemical energy storage devices. Communications Chemistry. 2 (1), 86(2019).
- Nam, K. W., et al. Conductive 2D metal-organic framework for high-performance cathodes in aqueous rechargeable zinc batteries. Nature Communications. 10 (1), 4948(2019).
- Sheberla, D., et al. Conductive MOF electrodes for stable supercapacitors with high areal capacitance. Nature Materials. 16 (2), 220-224 (2017).
- Wang, Z., et al. Ultrathin two-dimensional conjugated metal-organic framework single-crystalline nanosheets enabled by surfactant-assisted synthesis. Chemical Science. 11 (29), 7665-7671 (2020).
- Zhang, Z., Yoshikawa, H., Awaga, K. Monitoring the solid-state electrochemistry of Cu(2,7-AQDC) (AQDC = anthraquinone dicarboxylate) in a lithium battery: Coexistence of metal and ligand redox activities in a metal-organic framework. Journal of the American Chemical Society. 136 (46), 16112-16115 (2014).
- Zhang, Z., Yoshikawa, H., Awaga, K. Discovery of a "bipolar charging" mechanism in the solid-state electrochemical process of a flexible metal-organic framework. Chemistry of Materials. 28 (5), 1298-1303 (2016).
- Li, C., Hu, X., Hu, B. Cobalt(II) dicarboxylate-based metal-organic framework for long-cycling and high-rate potassium-ion battery anode. Electrochimica Acta. 253, 439-444 (2017).
- Liu, J., et al. Reversible formation of coordination bonds in Sn-based metal-organic frameworks for high-performance lithium storage. Nature Communications. 12 (1), 3131(2021).
- Jiang, Q., et al. A redox-active 2D metal-organic framework for efficient lithium storage with extraordinary high capacity. Angewandte Chemie. 59 (13), 5273-5277 (2020).
- Sakaushi, K., Nishihara, H. Two-dimensional π-conjugated frameworks as a model system to unveil a multielectron-transfer-based energy storage mechanism. Accounts of Chemical Research. 54 (15), 3003-3015 (2021).
- Li, H., et al. 2D organic radical conjugated skeletons with paramagnetic behaviors. Advanced Materials Interfaces. 8 (18), 2100943(2021).
- Peeks, M. D., et al. Electronic delocalization in the radical cations of porphyrin oligomer molecular wires. Journal of the American Chemical Society. 139 (30), 10461-10471 (2017).
- Krug von Nidda, H. A., et al. Anisotropic exchange in LiCuVO4 probed by ESR. Physical Review B. 65 (13), 134445(2002).
- Zeng, Z., et al. Pro-aromatic and anti-aromatic π-conjugated molecules: An irresistible wish to be diradicals. Chemical Society Reviews. 44 (18), 6578-6596 (2015).
- Chen, Q., Adeniran, O., Liu, Z. F., Zhang, Z., Awaga, K. Graphite-like charge storage mechanism in a 2D π-d conjugated metal-organic framework revealed by stepwise magnetic monitoring. Journal of the American Chemical Society. 145 (2), 1062-1071 (2023).
- Julien, C. M., Mauger, A., Groult, H., Zhang, X., Gendron, F. LiCo1-yByO2 as cathode materials for rechargeable lithium batteries. Chemistry of Materials. 23 (2), 208-218 (2011).
- Niemöller, A., Jakes, P., Eichel, R. A., Granwehr, J. In operando EPR investigation of redox mechanisms in LiCoO2. Chemical Physics Letters. 716, 231-236 (2019).
- Park, J., et al. Synthetic routes for a 2D semiconductive copper hexahydroxybenzene metal-organic framework. Journal of the American Chemical Society. 140 (44), 14533-14537 (2018).
- Rondeau, R. E. A technique for degassing liquid samples. Journal of Chemical Education. 44 (9), 530(1967).
- Flores-Llamas, H. Inhomogeneously broadened EPR lineshape of axial powder. Applied Magnetic Resonance. 9 (2), 289-298 (1995).
- Sun, L., et al. Room-temperature quantitative quantum sensing of lithium ions with a radical-embedded metal-organic framework. Journal of the American Chemical Society. 144 (41), 19008-19016 (2022).
- Chen, Y., et al. Successive storage of cations and anions by ligands of π-d-conjugated coordination polymers enabling robust sodium-ion batteries. Angewandte Chemie. 60 (34), 18769-18776 (2021).
- Roessler, M. M., Salvadori, E. Principles and applications of EPR spectroscopy in the chemical sciences. Chemical Society Reviews. 47 (8), 2534-2553 (2018).
- Ji, X., et al. Pauli paramagnetism of stable analogues of pernigraniline salt featuring ladder-type constitution. Journal of the American Chemical Society. 142 (1), 641-648 (2020).
- Noel, M., Santhanam, R. Electrochemistry of graphite intercalation compounds. Journal of Power Sources. 72 (1), 53-65 (1998).
- Wu, K. H., Ting, T. H., Wang, G. P., Ho, W. D., Shih, C. C. Effect of carbon black content on electrical and microwave absorbing properties of polyaniline/carbon black nanocomposites. Polymer Degradation and Stability. 93 (2), 483-488 (2008).
- Yao, M., Taguchi, N., Ando, H., Takeichi, N., Kiyobayashi, T. Improved gravimetric energy density and cycle life in organic lithium-ion batteries with naphthazarin-based electrode materials. Communications Materials. 1 (1), 70(2020).
- Krzystek, J., et al. EPR spectra from "EPR-silent" species: High-frequency and high-field EPR spectroscopy of pseudotetrahedral complexes of nickel(II). Inorganic Chemistry. 41 (17), 4478-4487 (2002).
Access restricted. Please log in or start a trial to view this content.
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved