Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Магнитометрическая характеристика промежуточных продуктов в твердотельной электрохимии окислительно-восстановительных металлоорганических каркасов
В этой статье
Резюме
Магнитная съемка ex situ может напрямую предоставлять объемную и локальную информацию о магнитном электроде, чтобы шаг за шагом выявить его механизм накопления заряда. Показано, что электронный спиновый резонанс (ЭПР) и магнитная восприимчивость позволяют контролировать оценку парамагнитных частиц и их концентрацию в окислительно-восстановительном металлоорганическом каркасе (МОФ).
Аннотация
Электрохимическое хранение энергии было широко обсуждаемым применением окислительно-восстановительных металлоорганических каркасов (MOF) в последние 5 лет. Хотя MOF демонстрируют выдающиеся характеристики с точки зрения гравиметрической или площадной емкости и циклической стабильности, к сожалению, их электрохимические механизмы в большинстве случаев недостаточно изучены. Традиционные спектроскопические методы, такие как рентгеновская фотоэлектронная спектроскопия (XPS) и тонкая структура рентгеновского поглощения (XAFS), предоставили лишь расплывчатую и качественную информацию об изменениях валентности определенных элементов, и механизмы, предложенные на основе такой информации, часто весьма спорны. В этой статье мы сообщаем о ряде стандартизированных методов, включая изготовление твердотельных электрохимических ячеек, электрохимические измерения, разборку ячеек, сбор электрохимических промежуточных продуктов MOF и физические измерения промежуточных продуктов под защитой инертных газов. Используя эти методы для количественного выяснения эволюции электронного и спинового состояний на одной электрохимической стадии окислительно-восстановительных MOF, можно дать четкое представление о природе электрохимических механизмов накопления энергии не только для MOF, но и для всех других материалов с сильно коррелированными электронными структурами.
Введение
С тех пор, как в конце 1990-х годов был введен термин «металлоорганический каркас» (MOF), и особенно в 2010-х годах, наиболее репрезентативные научные концепции, касающиеся MOF, возникли из-за их структурной пористости, включая гостевую инкапсуляцию, разделение, каталитические свойства и молекулярное зондирование 1,2,3,4 . Между тем, ученые быстро поняли, что для MOF важно обладать электронными свойствами, реагирующими на стимулы, чтобы интегрировать их в современные интеллектуальные устройства. Эта идея вызвала появление и процветание проводящего двумерного (2D) семейства MOF за последние 10 лет, тем самым открыв ворота для MOF, чтобы играть ключевые роли в электронике5 и, что более привлекательно, в электрохимических устройстваххранения энергии 6. Эти 2D MOF были включены в качестве активных материалов в батареи щелочных металлов, водные батареи, псевдоконденсаторы и суперконденсаторы 7,8,9 и продемонстрировали огромную емкость, а также отличную стабильность. Однако для разработки более эффективных 2D-MOF крайне важно детально понять их механизмы хранения заряда. Таким образом, эта статья направлена на всестороннее понимание электрохимических механизмов MOF, которые могут помочь в рациональном проектировании более эффективных MOF для приложений хранения энергии.
В 2014 году мы впервые сообщили о твердотельных электрохимических механизмах MOF с окислительно-восстановительными активными центрами как на катионах металлов, так и на лигандах10,11. Эти механизмы были интерпретированы с помощью различных спектроскопических методов in situ и ex situ, таких как рентгеновская фотоэлектронная спектроскопия (XPS), тонкая структура рентгеновского поглощения (XAFS), рентгеновская дифракция (XRD) и твердотельный ядерный магнитный резонанс (ЯМР). С тех пор эта исследовательская парадигма стала тенденцией в исследованиях твердотельной электрохимии материалов на молекулярной основе12. Эти методы отлично подходят для идентификации окислительно-восстановительных событий обычных MOF с карбоксилатными мостиковыми лигандами, поскольку молекулярные орбитали и энергетические уровни строительных блоков металлических кластеров и органических лигандов почти независимы друг от друга в таких MOF12,13.
Однако при столкновении с сильно коррелированными 2D-MOF со значительным π-d сопряжением были выявлены ограничения этих спектроскопических методов. Одним из этих ограничений является то, что зонные уровни большинства вышеупомянутых 2D MOF нельзя рассматривать как простую комбинацию металлических кластеров и лигандов, а скорее представляют собой их гибридизацию, в то время как большинство спектроскопических методов предоставляют только усредненную качественную информацию о степенях окисления14. Другое ограничение заключается в том, что интерпретация этих данных всегда основана на предположении о локализованных атомных орбиталях. Поэтому промежуточные состояния с металл-лигандной гибридизацией и делокализованные электронные состояния обычно упускаются из виду и описываются некорректно только этими спектроскопическими методами15. Необходимо разработать новые зонды для электронных состояний этих электрохимических промежуточных продуктов не только 2D MOF, но и других материалов с аналогичными сопряженными или сильно коррелированными электронными структурами, таких как ковалентные органические каркасы16, молекулярные проводники и сопряженные полимеры17.
Наиболее распространенными и мощными инструментами для оценки электронных структур материалов являются измерения магнитной восприимчивости электронного спинового резонанса (ESR) и сверхпроводящего квантового интерференционного устройства (SQUID)18,19. Поскольку оба полагаются на неспаренные электроны в системе, эти инструменты могут предоставить предварительную информацию о плотностях спина, распределении спинов и спин-спиновых взаимодействиях. ESR обеспечивает чувствительное обнаружение неспаренных электронов, в то время как измерение магнитной восприимчивости дает больше количественных сигналов для верхних свойств20. К сожалению, оба метода неизбежно сталкиваются с большими проблемами при использовании для анализа электрохимических промежуточных продуктов. Это связано с тем, что целевые образцы не являются чистыми, а представляют собой смесь целевого материала, проводящей добавки, связующего и побочного продукта электролита, поэтому полученные данные21,22 представляют собой сумму вкладов как материала, так и примесей. Между тем, большинство промежуточных продуктов чувствительны к окружающей среде, включая воздух, воду, определенные электролиты или любые другие непредсказуемые возмущения; При обращении с промежуточными продуктами и их измерении необходима особая осторожность. Метод проб и ошибок обычно необходим при работе с новой комбинацией материала электрода и электролита.
Здесь мы представляем новую парадигму, называемую электрохимической магнитометрией, для анализа электронных состояний или спиновых состояний 2D MOF и аналогичных материалов с использованием ряда методов, используя электрохимию и спектроскопию ЭПР ex situ с переменной температурой, а также измерения магнитной восприимчивости ex situ 20. Чтобы продемонстрировать эффективность этого подхода, мы используем в качестве примера Cu3THQ 2 (THQ = 1,2,4,5-тетрагидроксибензохинон; обозначается как Cu-THQ), репрезентативный2D MOF. Мы расскажем о выборе проводящих добавок и электролитов, изготовлении электродов и электрохимических элементов, а также о деталях обработки и измерения образцов, включая возможные проблемы во время измерения. Сравнивая с классическими характеристиками, такими как XRD и XAFS, электрохимическая магнитометрия может обеспечить всестороннее понимание электрохимического механизма большинства MOF. Этот подход способен фиксировать уникальные промежуточные состояния и избегать неправильного назначения окислительно-восстановительных событий. Выяснение механизмов накопления энергии с помощью электрохимической магнитометрии также может способствовать лучшему пониманию структурно-функциональных взаимосвязей в MOF, что приводит к более интеллектуальным синтетическим стратегиям для MOF и других сопряженных материалов.
Access restricted. Please log in or start a trial to view this content.
протокол
1. Изготовление электродов
- Синтез Cu-THQ MOF
ПРИМЕЧАНИЕ: Поликристаллический порошок Cu-THQ MOF был синтезирован гидротермальным методом в соответствии с ранее опубликованными процедурами 14,20,23.- Поместите 60 мг тетрагидроксихинона в ампулу объемом 20 мл, затем добавьте 10 мл дегазированной воды. В отдельном стеклянном флаконе растворите 110 мг тригидрата нитрата меди (II) еще в 10 мл дегазированной воды. Добавьте 46 мкл конкурирующего лиганда этилендиамина с помощью пипетки.
ПРИМЕЧАНИЕ: Чтобы дегазировать деионизированную воду, перед использованием пропустите газообразный азот в течение 30 минут. Если реакционная смесь нагревается слишком долго, может образоваться примесь Cu с дифракционным пиком, появляющимся около 43° (Cu Kα). - Вводят раствор меди в ампулу, содержащую тетрагидроксихинон. Цвет раствора сразу меняется с красного на темно-синий. Заморозьте, перекачайте и разморозьте24 полученный раствор три раза для дальнейшего удаления растворенного кислорода.
- Пламенем запечатайте ампулу с помощью горелки под вакуумом. Нагревайте раствор до 60 °C в течение 4 ч.
- После реакции осторожно вскройте ампулу и извлеките надосадочную жидкость. Вымойте осадок 30 мл деионизированной воды комнатной температуры 3x и 30 мл горячей деионизированной воды (80 °C) центрифугированием 3x при 10 000 об/мин в течение 5 мин.
- Диспергируйте осадок в ацетон путем встряхивания, затем процеживают и промывают ацетоном. Нагрейте продукт под вакуумом до 353 К в течение ночи, чтобы удалить остатки растворителя в Cu-THQ MOF.
- Поместите 60 мг тетрагидроксихинона в ампулу объемом 20 мл, затем добавьте 10 мл дегазированной воды. В отдельном стеклянном флаконе растворите 110 мг тригидрата нитрата меди (II) еще в 10 мл дегазированной воды. Добавьте 46 мкл конкурирующего лиганда этилендиамина с помощью пипетки.
- Подготовка электродов CuTHQ
ПРИМЕЧАНИЕ: Чтобы различать MOF Cu-THQ и электрод, первый называется Cu-THQ, а смесь Cu-THQ, углерода и связующего называется просто CuTHQ.- Чтобы приготовить электрод Cu-THQ / CB / PVDF, растворите 10 мг поливинилиденфторида (PVDF) в 1,4 мл N-метил-2-пирролидона (NMP). Диспергируйте 50 мг Cu-THQ MOF и 40 мг технического углерода (CB) в растворе, энергично помешивая в течение ночи. Нанесите однородную суспензию на алюминиевый диск диаметром 15 мм и массой ~9,7 мг.
- Чтобы приготовить электрод Cu-THQ/Gr/SP/SA, следуйте той же процедуре, что и электроду Cu-THQ/CB/PVDF, но с другим составом суспензии: Cu-THQ MOF (80 мг), альгинат натрия (SA, 2 мг) и графен/Super P (разбавление Gr/SP 1:1,8 по массе, всего 18 мг) в воде/изопропаноле (разведение 1:1 по объему, всего 1,2 мл).
- Сушат электроды под вакуумом при 353 К в течение 12 ч. Выпустите газообразный азот после сушки и измерьте массовую нагрузку.
2. Сборка батареи и последующая обработка
ПРИМЕЧАНИЕ: Из-за чувствительной к воздуху природы электрохимических промежуточных продуктов сборка и последующая обработка батареи должны выполняться в аргоновом перчаточном ящике со строгим безвоздушным способом.
- Сборка монетных ячеек Li/CuTHQ
- Перед сборкой аккумулятора отрежьте несколько кусков литиевых дисков диаметром 15,5 мм и сепараторов Celgard диаметром 17 мм.
- Соберите монетные ячейки Li/CuTHQ (CR2032) снизу вверх в следующем порядке: отрицательная оболочка, прокладка (высота = 0.5 мм), литий, сепаратор, электрод CuTHQ (подготовленный на шаге 1.2.1 или 1.2.2), прокладка, пружина и положительная оболочка (рис. 1A).
- До и после добавления сепаратора капните в общей сложности 0,04 мл электролита (1,0 М LiBF4 в этиленкарбонате (EC)/диэтилкарбонате (DEC) при массе 1:1%). Не используйте металлический пинцет для удержания монетной ячейки после ее сборки.
- Получение электрохимических промежуточных продуктов
- Сожмите монетную ячейку с помощью стяжного винта (не герметичного) самодельным устройством (рисунок 1Б) и подсоедините прибор к измерительным кабелям в бардачке. Подключите прибор (снаружи перчаточного ящика) к портам, соответствующим монетной ячейке. Выполните циклическую вольтамперометрию и гальваностатические измерения заряда/разряда20 для получения промежуточных продуктов при различных потенциалах (рис. 2).
- После электрохимического циклирования осторожно разберите монетную ячейку, чтобы избежать короткого замыкания.
- Промойте циклический электрод CuTHQ 5 мл диметилкарбоната аккумуляторного качества (DMC). Высушите электрод естественным путем в течение 30 минут. Соберите образец с диска Al на фольгу Al с помощью чистого шпателя.
- Перенесите порошок образца в пробирку ESR или пробирку SQUID через самодельную стеклянную воронку (рис. 1C). Плотно закройте пробирку с образцом крышкой и прозрачной пленкой. В качестве альтернативы подсоедините пробирку для образца к резиновой пробирке и герметизируйте ее клапаном, после чего пламенем герметизируют головку пробирки для образца под вакуумом.
- После магнитных измерений20 откройте пробирку для образца и выгрузите образец на алюминиевую фольгу. Измерьте массу образца с помощью аналитических весов с разрешением 0,01 мг на воздухе. Оцените массу Cu-THQ по общей массе образца.
ПРИМЕЧАНИЕ: Масса циклированного Cu-THQ MOF оценивается в 50% или 80% от общей массы, в зависимости от типа используемых электродов; эта оценка не учитывает вставленные ионы лития и остаточный электролит.
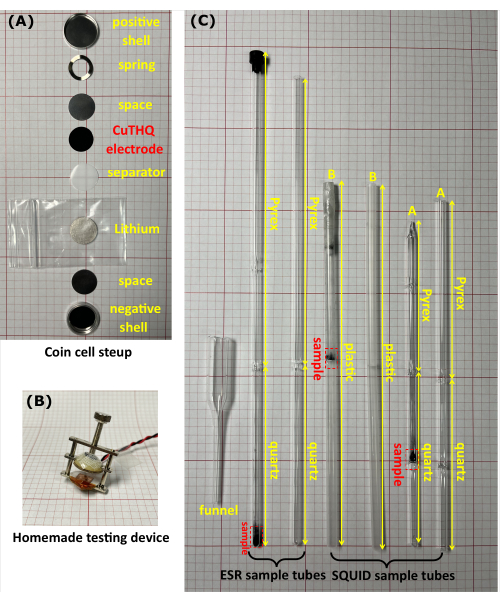
Рисунок 1: Оборудование, используемое для экспериментов по магнитометрии ex situ. (A) Фотография монетной ячейки CR2032. (B) Самодельное устройство использовалось для оценки незапечатанной ячейки для монет в перчаточном ящике. (C) Фотографии пробирок с образцами СОЭ и СКВИД с образцами внутри и без них. Трубка ESR состоит из кварцевого наконечника высокой чистоты толщиной 10 см (измерительная секция) и головки из боросиликатного стекла диаметром 17 см. Существует два вида трубок SQUID. Трубка A состоит из кварцевого наконечника размером 2 см x 5 см с кварцевой диафрагмой в средней точке и головкой из боросиликатного стекла диаметром 10 см, а трубка B представляет собой пластиковую трубку (длиной 20 см) с пластиковой диафрагмой в средней точке. Все пробирки для образцов имеют наружный диаметр 5 мм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
3. Регистрация спектров ЭПР при переменных температурах
- Регистрация спектров ЭПР при комнатной температуре
- Как только спектрометр ESR будет готов, вставьте подготовленную пробирку для образца в микроволновую полость и центрируйте образец. Автонастройка микроволновой фазы, связи и частоты для достижения состояния резонанса резонатора. Проверьте Q-dip в центре экрана на предмет симметричной формы и максимальной глубины.
ПРИМЕЧАНИЕ: Если образец содержит слишком много проводящего углерода, такого как технический углерод, процесс автонастройки может завершиться сбоем или привести к малому коэффициенту качества (Q-значению) полости. Типичная масса образца составляет 3 мг. - Выбирайте оптимальные параметры, такие как: микроволновая печь: мощность; магнитное поле: время развертки; центральное поле: ширина развертки; модуляция: частотная, ширинная; Канал: амплитуда, постоянная времени. Затем проведите развертку магнитного поля и запишите спектр ЭПР. Типичные значения параметров измерений приведены на рисунках 3 и 4.
- Отрегулируйте количество вставки маркера Mn до 800. Повторите шаги 3.1.1 и 3.1.2 для записи спектра СОЭ с маркером Mn. Откалибруйте магнитное поле, используя шесть сверхтонких линий для ионов Mn (II).
- Как только спектрометр ESR будет готов, вставьте подготовленную пробирку для образца в микроволновую полость и центрируйте образец. Автонастройка микроволновой фазы, связи и частоты для достижения состояния резонанса резонатора. Проверьте Q-dip в центре экрана на предмет симметричной формы и максимальной глубины.
- Анализ формы линии Cu-THQ
- Импортируйте набор данных ESR в Python (версия 3.9.7). Нормализуйте спектр ESR, разделив интенсивность на массу образца, квадратный корень из микроволновой мощности, ширину модуляции и амплитуду.
- Подгонка калиброванного и нормализованного спектра ЭПР подготовленного Cu-THQ MOF к осесимметричной функцииЛоренца 25:
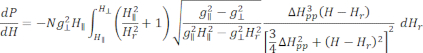
Где N — масштабный коэффициент, включающий параметры прибора g llи константы HII, ( и ) — параллельная (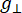 перпендикулярная) составляющая g-фактора посадочного модуля и
перпендикулярная) составляющая g-фактора посадочного модуля и 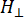 соответствующее резонансное магнитное поле, Δ Hpp — ширина линии от пика до пика, а Hr— интегральная переменная.
соответствующее резонансное магнитное поле, Δ Hpp — ширина линии от пика до пика, а Hr— интегральная переменная.
ПРИМЕЧАНИЕ: Коды Python для функции Лоренца доступны в дополнительном файле кодирования 1 (который называется AxialLorentz). - Получите анизотропное значение g и ширину линии от пика до пика для осесимметричных ионов Cu(II).
- Подгонка калиброванного и нормализованного спектра СОЭ с функцией Лоренца для радикальных выборок. Получите изотропное значение g и ширину линии от пика до пика для радикалов.
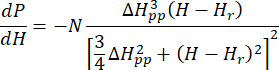
Он назван SymLorentz в файле дополнительного кодирования 1.
- Количественная оценка концентрации радикалов
- Измельчите 3,45 мг 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксила (TEMPOL) и 96,55 мг KBr вместе в агатовой ступке до получения однородной смеси. Поместите 1 мг (0,2 мкмоль), 2 мг (0,4 мкмоль) и 4 мг (0,8 мкмоль) смесей TEMPOL/KBr в три пробирки для образцов СОЭ соответственно.
- Выполните шаги 3.1.1 и 3.1.2, чтобы записать спектры ЭПР для стандартов TEMPOL/KBr.
- Проведите линейную подгонку базовой линии между двойным интегрированием спектров ЭПР и числом спинов в стандартах TEMPOL/KBr. Определите количество вращений в циклическом Cu-THQ, используя линейную базовую линию стандартов TEMPOL/KBr26.
- Регистрация спектров ЭПР при низких температурах
ПРИМЕЧАНИЕ: Используйте жидкий гелий для достижения криогенной температуры. Необходимо надевать криогенные перчатки при работе с жидким гелием.- Сначала проверьте спектр СОЭ при комнатной температуре, выполнив шаг 3.1.
- Опорожните теплозащитный экран до высокого уровня вакуума. Продуйте микроволновую полость газообразным азотом, чтобы избежать конденсации.
- Ввести жидкий гелий из сосуда в криостат. Постепенно охладите образец до самой низкой температуры (около 10 К). Подождите 30 минут, чтобы достичь теплового равновесия.
- Запишите спектры ЭПР, зависящие от температуры, во время потепления. Подтвердите, что спектр ESR не страдает от эффекта насыщения мощности при низкой температуре, а отношение между интенсивностью сигнала (высотой пика к пику) и квадратным корнем из мощности СВЧ остается постоянным при отсутствии насыщения мощности.
ПРИМЕЧАНИЕ: Когда мощность насыщена, интенсивность сигнала увеличивается медленнее, чем квадратный корень из микроволновой мощности. Плотность выборки может постепенно уменьшаться по мере повышения температуры.
4. Измерения магнитной восприимчивости
- Прикрепите пробирку для образца к нижней части стержня для образца. Убедитесь, что поверхность пробирки для образца чистая.
- Продуйте камеру для образцов и вставьте пробирку для образца в SQUID. Приложите магнитное поле и центрируйте образец в катушке обнаружения. Удалите внешнее магнитное поле после центрирования.
ПРИМЕЧАНИЕ: Если концентрация спина слишком мала для обнаружения, рассмотрите возможность увеличения магнитного поля или центрирования после охлаждения до 2 К. Типичная масса образца для измерений SQUID составляет приблизительно 6 мг. - Охладите систему до 20 К со скоростью 10 К/мин. Сделайте паузу в охлаждении на 30 мин, затем дополнительно охладите до 2 К в течение 1 ч.
- Измерьте магнитную восприимчивость циклического электрода CuTHQ под магнитным полем 1,000 Э при нагревании до 300 К; это называется процессом с нулевым полем охлаждения (ZFC). Затем снова охладите до 2 К и запишите магнитную восприимчивость в процессе с полевым охлаждением (FC).
- Повторите шаги с 4.1 по 4.4 с электродами CuTHQ, циклически обработанными с разной степенью восстановления.
- Измерьте магнитную восприимчивость углеродных материалов (Gr/SP) в тех же условиях. Используйте этот результат для компенсации магнитной восприимчивости электродов CuTHQ.
- Подгонка температурной зависимости магнитной восприимчивости к модифицированному закону Кюри-Вейса:
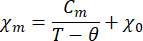
Где χ m — молярная магнитная восприимчивость, Cm— молярная постоянная Кюри, θ — температура Вейса, χ0— температурно-независимый член.
Access restricted. Please log in or start a trial to view this content.
Результаты
Наша предыдущая работа включала подробное обсуждение спектроскопии ЭПР ex situ и измерений магнитной восприимчивости ex situ для электрохимически циклированного CuTHQ20. Здесь мы представляем наиболее репрезентативные и подробные результаты, которые могут быть получе?...
Access restricted. Please log in or start a trial to view this content.
Обсуждение
Для получения катодов необходимо смешать активный материал с проводящим углеродом, чтобы добиться низкой поляризации во время электрохимического процесса. Углеродная добавка является первой критической точкой для магнитометрии ex situ ; если углерод имеет радикальные дефекты, то п...
Access restricted. Please log in or start a trial to view this content.
Раскрытие информации
У авторов нет конфликтов интересов, о которых можно было бы заявить.
Благодарности
Это исследование было поддержано грантом KAKENHI (JP20H05621) Японского общества содействия развитию науки (JSPS). З. Чжан также благодарит Фонд Татемацу и стипендию Toyota Riken за финансовую поддержку.
Access restricted. Please log in or start a trial to view this content.
Материалы
| Name | Company | Catalog Number | Comments |
| 1-Methyl-2-pyrrolidone | FUJIFILM Wako Chemicals | 139-17611 | Super Dehydrated |
| 1mol/L LiBF4 EC:DEC (1:1 v/v%) | Kishida | LBG-96533 | electrolyte |
| 4-Hydroxy-2,2,6,6-tetramethylpiperidine-1-oxyl | FUJIFILM Wako Chemicals | 089-04191 | TEMPOL, for Spin Labeling |
| Ampule tube | Maruemu Corporation | 5-124-05 | 20mL |
| Carbon black, Super P Conductive | Alfa Aesar | H30253 | |
| Conductive Carbon Black | Mitsubishi Chemical | ||
| Copper (II) Nitrate Trihydrate | FUJIFILM Wako Chemicals | 033-12502 | deleterious substances |
| Dimethyl Carbonate | FUJIFILM Wako Chemicals | 046-31935 | battery grade |
| Ethylenediamine | FUJIFILM Wako Chemicals | 053-00936 | deleterious substances |
| Graphene Nanoplatelets | Tokyo Chemical Industry | G0442 | 6-8nm(thick), 15µm(wide) |
| Poly(vinylidene fluoride) | Sigma Aldrich | 182702 | |
| Potassium Bromide | FUJIFILM Wako Chemicals | 165-17111 | for Infrared Spectrophotometry |
| Sodium Alginate | FUJIFILM Wako Chemicals | 199-09961 | 500-600 cP |
| SQUID Magnetometer | Quantum Design | MPMS-XL 5 | |
| Tetrahydroxy-1,4-benzoquinone Hydrate | Tokyo Chemical Industry | T1090 | |
| X-Band ESR | JEOL | JES-F A200 |
Ссылки
- Lee, J., et al. Metal-organic framework materials as catalysts. Chemical Society Reviews. 38 (5), 1450-1459 (2009).
- Dolgopolova, E. A., Rice, A. M., Martin, C. R., Shustova, N. B. Photochemistry and photophysics of MOFs: steps towards MOF-based sensing enhancements. Chemical Society Reviews. 47 (13), 4710-4728 (2018).
- Qian, Q., et al. MOF-based membranes for gas separations. Chemical Reviews. 120 (16), 8161-8266 (2020).
- Wang, Q., Astruc, D. State of the art and prospects in metal-organic framework (MOF)-based and MOF-derived nanocatalysis. Chemical Reviews. 120 (2), 1438-1511 (2020).
- Wang, M., Dong, R., Feng, X. Two-dimensional conjugated metal-organic frameworks (2D c-MOFs): chemistry and function for MOFtronics. Chemical Society Reviews. 50 (4), 2764-2793 (2021).
- Baumann, A. E., Burns, D. A., Liu, B., Thoi, V. S. Metal-organic framework functionalization and design strategies for advanced electrochemical energy storage devices. Communications Chemistry. 2 (1), 86(2019).
- Nam, K. W., et al. Conductive 2D metal-organic framework for high-performance cathodes in aqueous rechargeable zinc batteries. Nature Communications. 10 (1), 4948(2019).
- Sheberla, D., et al. Conductive MOF electrodes for stable supercapacitors with high areal capacitance. Nature Materials. 16 (2), 220-224 (2017).
- Wang, Z., et al. Ultrathin two-dimensional conjugated metal-organic framework single-crystalline nanosheets enabled by surfactant-assisted synthesis. Chemical Science. 11 (29), 7665-7671 (2020).
- Zhang, Z., Yoshikawa, H., Awaga, K. Monitoring the solid-state electrochemistry of Cu(2,7-AQDC) (AQDC = anthraquinone dicarboxylate) in a lithium battery: Coexistence of metal and ligand redox activities in a metal-organic framework. Journal of the American Chemical Society. 136 (46), 16112-16115 (2014).
- Zhang, Z., Yoshikawa, H., Awaga, K. Discovery of a "bipolar charging" mechanism in the solid-state electrochemical process of a flexible metal-organic framework. Chemistry of Materials. 28 (5), 1298-1303 (2016).
- Li, C., Hu, X., Hu, B. Cobalt(II) dicarboxylate-based metal-organic framework for long-cycling and high-rate potassium-ion battery anode. Electrochimica Acta. 253, 439-444 (2017).
- Liu, J., et al. Reversible formation of coordination bonds in Sn-based metal-organic frameworks for high-performance lithium storage. Nature Communications. 12 (1), 3131(2021).
- Jiang, Q., et al. A redox-active 2D metal-organic framework for efficient lithium storage with extraordinary high capacity. Angewandte Chemie. 59 (13), 5273-5277 (2020).
- Sakaushi, K., Nishihara, H. Two-dimensional π-conjugated frameworks as a model system to unveil a multielectron-transfer-based energy storage mechanism. Accounts of Chemical Research. 54 (15), 3003-3015 (2021).
- Li, H., et al. 2D organic radical conjugated skeletons with paramagnetic behaviors. Advanced Materials Interfaces. 8 (18), 2100943(2021).
- Peeks, M. D., et al. Electronic delocalization in the radical cations of porphyrin oligomer molecular wires. Journal of the American Chemical Society. 139 (30), 10461-10471 (2017).
- Krug von Nidda, H. A., et al. Anisotropic exchange in LiCuVO4 probed by ESR. Physical Review B. 65 (13), 134445(2002).
- Zeng, Z., et al. Pro-aromatic and anti-aromatic π-conjugated molecules: An irresistible wish to be diradicals. Chemical Society Reviews. 44 (18), 6578-6596 (2015).
- Chen, Q., Adeniran, O., Liu, Z. F., Zhang, Z., Awaga, K. Graphite-like charge storage mechanism in a 2D π-d conjugated metal-organic framework revealed by stepwise magnetic monitoring. Journal of the American Chemical Society. 145 (2), 1062-1071 (2023).
- Julien, C. M., Mauger, A., Groult, H., Zhang, X., Gendron, F. LiCo1-yByO2 as cathode materials for rechargeable lithium batteries. Chemistry of Materials. 23 (2), 208-218 (2011).
- Niemöller, A., Jakes, P., Eichel, R. A., Granwehr, J. In operando EPR investigation of redox mechanisms in LiCoO2. Chemical Physics Letters. 716, 231-236 (2019).
- Park, J., et al. Synthetic routes for a 2D semiconductive copper hexahydroxybenzene metal-organic framework. Journal of the American Chemical Society. 140 (44), 14533-14537 (2018).
- Rondeau, R. E. A technique for degassing liquid samples. Journal of Chemical Education. 44 (9), 530(1967).
- Flores-Llamas, H. Inhomogeneously broadened EPR lineshape of axial powder. Applied Magnetic Resonance. 9 (2), 289-298 (1995).
- Sun, L., et al. Room-temperature quantitative quantum sensing of lithium ions with a radical-embedded metal-organic framework. Journal of the American Chemical Society. 144 (41), 19008-19016 (2022).
- Chen, Y., et al. Successive storage of cations and anions by ligands of π-d-conjugated coordination polymers enabling robust sodium-ion batteries. Angewandte Chemie. 60 (34), 18769-18776 (2021).
- Roessler, M. M., Salvadori, E. Principles and applications of EPR spectroscopy in the chemical sciences. Chemical Society Reviews. 47 (8), 2534-2553 (2018).
- Ji, X., et al. Pauli paramagnetism of stable analogues of pernigraniline salt featuring ladder-type constitution. Journal of the American Chemical Society. 142 (1), 641-648 (2020).
- Noel, M., Santhanam, R. Electrochemistry of graphite intercalation compounds. Journal of Power Sources. 72 (1), 53-65 (1998).
- Wu, K. H., Ting, T. H., Wang, G. P., Ho, W. D., Shih, C. C. Effect of carbon black content on electrical and microwave absorbing properties of polyaniline/carbon black nanocomposites. Polymer Degradation and Stability. 93 (2), 483-488 (2008).
- Yao, M., Taguchi, N., Ando, H., Takeichi, N., Kiyobayashi, T. Improved gravimetric energy density and cycle life in organic lithium-ion batteries with naphthazarin-based electrode materials. Communications Materials. 1 (1), 70(2020).
- Krzystek, J., et al. EPR spectra from "EPR-silent" species: High-frequency and high-field EPR spectroscopy of pseudotetrahedral complexes of nickel(II). Inorganic Chemistry. 41 (17), 4478-4487 (2002).
Access restricted. Please log in or start a trial to view this content.
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены