このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
Caenorhabditisのelegansの研究のための細菌を新陳代謝的に不活性化する方法論
要約
実験室での 線虫Caenorhabditis elegans の餌源は、生きた 大腸菌です。細菌は代謝的に活性であるため、 線虫 の代謝および薬物研究において交絡変数を示します。パラホルムアルデヒドを使用して細菌を代謝的に不活性化する詳細なプロトコルは、ここに記載されています。
要約
線虫Caenorhabditis elegansは、遺伝学、発生、老化、代謝、および行動の研究のための一般的なモデル生物です。線虫は生きたバクテリアの餌を摂取するため、その食物源の代謝活性は、線虫に対するさまざまな介入の直接的な影響を探す実験を混乱させる可能性があります。細菌代謝の交絡作用を避けるために、C.エレガンスの研究者は、紫外線(UV)照射、熱殺傷、抗生物質など、細菌を代謝的に不活性化する複数の方法を使用してきました。UV処理は比較的低スループットであり、細菌の死滅を成功させるために各プレートを検査する必要があるため、液体培養では使用できません。第2の治療法である熱殺傷は、細菌の食感と栄養価に悪影響を及ぼし、線虫の発生停止につながります。最後に、抗生物質治療は、細菌の増殖を防ぐだけでなく、線虫の生理機能を直接変化させる可能性があります。この原稿では、パラホルムアルデヒド(PFA)を使用して細菌を代謝的に不活性化する代替方法について説明します。PFA処理は、細菌細胞内のタンパク質を架橋し、細胞構造と栄養成分を維持しながら代謝活性を防ぎます。この方法はハイスループットであり、PFA処理したバクテリアの1つのプレートの増殖をテストすることでバッチ全体が検証されるため、液体培養または固体プレートで使用できます。PFA処理による代謝不活性化は、C.エレガンスにおける薬物または代謝物の補給、ストレス耐性、メタボロミクス、および行動の研究における細菌代謝の交絡効果を排除するために使用できます。
概要
線虫は、1965年にモデル生物として提唱され1、それ以来、遺伝学、発生、行動、老化、代謝の研究に広く採用されてきました2。C.エレガンスは、その大きなひなサイズと透明なクチクラにより、蛍光レポーターによるハイスループットスクリーニングに特に適しています3。また、C.エレガンスは、その短いライフサイクル、雌雄同体生殖、ヒトとの遺伝的相同性などから、発生4や老化生物学5の研究において貴重なモデル体系となっています。さらに、C.エレガンスは比較的維持が容易です。線虫は、液体培養または固体寒天プレートで増殖し、生きた大腸菌OP50細菌の餌を消費することができます4。
しかし、線虫の生きた食物源は、代謝、薬物補給、および行動の研究を混乱させる可能性があります。生きたバクテリアは独自の代謝を持っているため、バクテリアに影響を与える実験条件は、ワームが利用できる栄養素と代謝物も変化させます。例えば、細菌の鉄、アミノ酸、葉酸の濃度の違いは、線虫の発生、生理機能、寿命に多様な影響を及ぼします6。多くの一般的なラボの慣行は、OP50によって生成される栄養素組成と代謝物にそのような変化を引き起こす可能性があります。具体的には、線虫の繁殖を防ぐために一般的に使用される化合物である5-フルオロ-2'-デオキシウリジン(FUdR)への曝露は、アミノ酸生合成経路を含むOP50遺伝子発現の広範な変化を誘発する7。また、生きたバクテリアは、活性化合物を部分的または完全に代謝できるため、C.エレガンスに低分子を添加する研究を混乱させる可能性があります。さらに、これらの低分子が細菌に及ぼす影響は、寿命を延ばす薬メトホルミン8で報告されているように、線虫の生理機能を変化させる可能性があります。最後に、生きたバクテリアは、魅力的な匂い物質を分泌する9、外因性の神経調節物質10を産生する、密集したバクテリアの芝生に酸素勾配を作り出す11など、行動を変化させる方法で線虫の環境を変化させることができる。
C.エレガンス研究に対する細菌代謝の交絡効果を軽減するために、細菌を殺すための複数の方法が開発されています(表1)。OP50を殺すための3つの一般的な戦略は、UV照射、熱殺傷、および抗生物質治療です。これらの方法はどれも簡単で比較的低コストですが、細菌と線虫の両方に望ましくない影響を与える可能性があります。UV架橋剤12を介したUV殺滅は、低スループットであり、その速度は、UV架橋剤に収まることができるプレートの数によって制限される。さらに、UV殺傷の有効性はバッチ内のプレートごとに異なる可能性があり、大規模な実験ではすべてのプレートでの成長試験が困難になる可能性があります。培養液を>60°Cの温度にさらしてOP50を熱殺傷するには、別の課題があります。高熱は、線虫に不可欠な栄養素を損傷し、細菌の細胞構造を破壊し、線虫が食物に費やす時間を減らす、より柔らかい食感を作り出します13。また、熱死細菌を与えられた線虫は発生初期に停止する可能性があるため、この方法はC.エレガンスのライフサイクル全体を通じて使用することはできません13。抗生物質治療は、細菌の代謝を抑制するための第3の一般的な方法である14が、抗生物質は線虫の成長と代謝を変化させることもできる15。
バクテリアの構造と必須栄養素を維持しながら、生きたバクテリアの代謝効果を排除する1つの解決策は、パラホルムアルデヒド(PFA)16でOP50を殺すことです。PFAはホルムアルデヒドのポリマーであり、細胞内のタンパク質を架橋して17、内側の原形質膜18のような内部細胞構造を破壊することなく細菌の複製を防ぐことができる。このように細胞内部構造が保たれているため、PFA処理された細菌は増殖や代謝活性を示さないが、C.エレガンスにとって食用で栄養豊富な食物源であり続ける16。 ここでは、パラホルムアルデヒドを使用して細菌を代謝的に不活性化する方法を示す詳細なプロトコルが提供されています。
| 方式 | 必要な材料 | スケーラブル。 | 栄養。 | ワームへの影響は? | ||||
| UV/紫外線 | UV架橋剤 | 制限対象: | はい | NGM12、23、24の寿命に対するさまざまな影響 | ||||
| UV架橋剤に収まる段数 | FUdR24、26、27の寿命に対するさまざまな影響 | |||||||
| プレートあたりの照射時間 | 食の嗜好性の低下16 | |||||||
| すべてのプレートの成長をチェックする機能8 | ||||||||
| 熱 | >60°Cインキュベーター | はい | いいえ:細胞壁を破壊し、栄養価を低下させます | 発達停止 13 | ||||
| 食の嗜好の低下13 | ||||||||
| NGM31の寿命を延ばす | ||||||||
| 抗生物質 | 抗生物質(カナマイシン、カルベニシリンなど) | はい | はい | 成長と発展を遅らせる15 | ||||
| 液体媒体の寿命を延ばす19 | ||||||||
| NGM15の寿命を延ばす | ||||||||
| PFAの | 0.5%パラホルムアルデヒド | はい | はい | 小さなひなのサイズの減少16 | ||||
| 開発時間の小幅な増加16 | ||||||||
| 食の嗜好性の低下16 | ||||||||
表 1.OP50を殺す方法の比較。 紫外線殺傷、熱殺傷、抗生物質処理、PFA処理は、細菌の栄養状態と、処理された細菌を与えられた線虫の健康にさまざまな影響を及ぼします。 大腸菌 を複製的に不活性化するこれらの方法は、必要な材料とスケーラビリティも異なります。
プロトコル
1.細菌接種
- 10 gのトリプトン、5 gの酵母抽出物、および10 gの塩化ナトリウム(NaCl)を950 mLの蒸留水に溶解して、ルリアブロス(LB)を調製します。
- 5Mの水酸化ナトリウム(NaOH)を添加して、LBのpHを7.0に調整します。これには、約0.2mLのNaOHしか必要ありません。
- pH 調整した LB 培地を液体サイクルで 15 psi で 45 分間オートクレーブします。溶液を冷まし、室温で保存します。
- 500 mL三角フラスコ内のLB100 mLに細菌の単一コロニーを接種します。バクテリアを37°Cのシェーカーインキュベーターで一晩培養します。
- バクテリアコロニーの健康状態、フラスコのサイズ、シェーカーの設定速度に応じて、バクテリアが増殖するのにかかる時間は異なる場合があります。~14時間後、600 nm(OD600)での細菌の光学濃度(OD)を確認します。
- OD600 が 3.0 (1 x 109 コロニー形成単位 (CFU)/mL) のときに、シェーカーからバクテリアを除去します。OD600 が 3.0 未満の場合は、目的の OD に達するまでフラスコをシェーカー インキュベーターに戻します。
- バクテリアを50 mLのコニカルチューブに分注し、4°Cで保存するか、次のステップに進みます。
2. パラホルムアルデヒドの取り扱い
注:使用されるパラホルムアルデヒド(PFA)の濃度、および曝露期間は、気候、場所、および処理する細菌の種類によって多少異なる場合があります。OP50 の適切な出発点は、0.5% PFA に 1 時間曝露することですが、HT115 では 0.25% PFA に 1 時間曝露するだけで十分です。
- 32%PFAストックを調製するか、市販の32%PFA溶液を使用します。PFAを扱うときは、適切な個人用保護具(PPE)を使用してください。手袋と目の保護具を着用してください。
- 適切な換気で化学ヒュームフード内にPFAを追加します。PFAを含む洗浄剤とチップは、ドラフト内の適切な化学的危険容器に廃棄してください。
3.パラホルムアルデヒドによる細菌治療
- バクテリアがOD600 から 3.0 に達したら、血清ピペットを使用して、50 mL を新しい 250 mL 三角フラスコに移します。残りは、ライブコントロール、モック処理コントロール (ステップ 4 を参照)、または必要に応じて PFA で処理するために保存します。
- あるフラスコから別のフラスコに注ぐことは避け、新しいフラスコの側面にバクテリアが飛び散らないように注意してください。フラスコの側面にあるコロニーは、より低用量のPFAを投与される場合があります。
- ケミカルフードで、781 μL の 32% PFA を 50 mL のバクテリアに添加し、最終濃度を 0.5% にします。使用したチップは、固形廃棄物の化学物質危険容器に廃棄してください。
- フラスコをホイルで覆い、37°Cのシェーカーインキュベーターに1時間戻します。1時間後、フラスコをインキュベーターから取り出し、手順5に進みます。
4. 模擬処理コントロール
- バクテリアがOD600 3.0に達したら、血清ピペットを使用して、50 mLのバクテリアを50 mLのコニカルチューブに移します。
- ステップ 5.3 に進み、PFA 処理グループと同様の洗浄ステップを完了します。
5.バクテリアを洗浄して残留PFAを除去する
- ケミカルフード内で、血清ピペットを使用して、処理した細菌を三角フラスコから50 mLのコニカルチューブに移します。バクテリアを注ぐ代わりに血清ピペットを使用すると、PFAによる直接処理を避けた可能性のあるフラスコの縁にあるバクテリアコロニーからの汚染を防ぐことができます。
- 処理したバクテリアを約3000 x g で20分間遠心分離します。上澄み液は、薬品フード内の廃薬品危険容器に廃棄して除去します。
- 25 mLのLBとボルテックスを加えて、細菌ペレットを再懸濁します(チューブを完全に充填すると、ペレットの再懸濁が難しくなります)。遠心分離とペレット再懸濁を4回繰り返します。
- さまざまなアッセイに最適な量でペレットを再懸濁します。ライフスパンアッセイでは、200 μL の細菌を 10 mL の LB に再懸濁した 60 mm プレートに播種し、10 mL の LB に細菌を再懸濁すると、元の 50 mL の培養物から 5 倍の濃度が得られます。
- バクテリアを4°Cで保存します。
6. 細菌増殖の品質チェック
- 最終洗浄と再懸濁の後、準備したバクテリアでLBプレートを(滅菌ピペットチップを使用して)ストリークします。洗浄と再懸濁に使用したLBを別のプレートにストリークして、使用したLBが汚染されていないことを確認することをお勧めします。
- プレートを37°Cのインキュベーターに一晩置きます。成長がないか確認します。バクテリアは、LBプレート上でコロニーが成長しないと、複製死したと見なされます。
7. 呼吸計による細菌代謝の品質チェック
- ステップ5.4からの最終洗浄と再懸濁の後、呼吸計19,20などの利用可能なツールを使用して、細菌が代謝的に死んでいることを確認し、基礎酸素消費率(OCR)を測定します。
- M9溶液を調製する:3gのリン酸カリウム一塩基性(KH 2PO 4)、6gのリン酸二塩基性ナトリウム(Na2HPO4)、および5gの塩化ナトリウム(NaCl)を950mLの蒸留水に溶解する。15psiで45分間液体サイクルでオートクレーブし、溶液を室温まで冷却します。1 mL の 1 M 硫酸マグネシウム (MgSO4) を加え、室温で保存します。
- 呼吸計カートリッジの水和:96ウェルプレートのすべてのウェルに200 μLのキャリブラントを添加します。カートリッジを96ウェルプレートに入れ、37°Cのインキュベーターで一晩インキュベートします。
- アッセイのキャリブレーション:翌日、水和カートリッジを機械に入れ、キャリブレーションを開始します。
- アッセイテストプレートのセットアップ:新しい96ウェルプレートを使用して、160 μLのM9と40 μLの調製した細菌(1 x 109 CFU/mL)をウェルに添加します。200 μL の M9 を 4 コーナーウェルに添加し、ブランクウェルとして使用します。160 μL の M9 と 40 μL の LB を洗浄および再懸濁に用いて、ネガティブコントロールとして使用します。200 μL の M9 を、使用しない残りのウェルに加えます。
- アッセイの実行:カートリッジのキャリブレーションが完了したら、ステップ7.5のアッセイプレートを分析用のマシンに挿入します。設定には、ミキシング、待機、測定、ループのステップが含まれます。結果は酸素消費率(OCR)として表示されます。バクテリアは代謝的に死んでおり、OCRがゼロになるとすぐに使用できます。
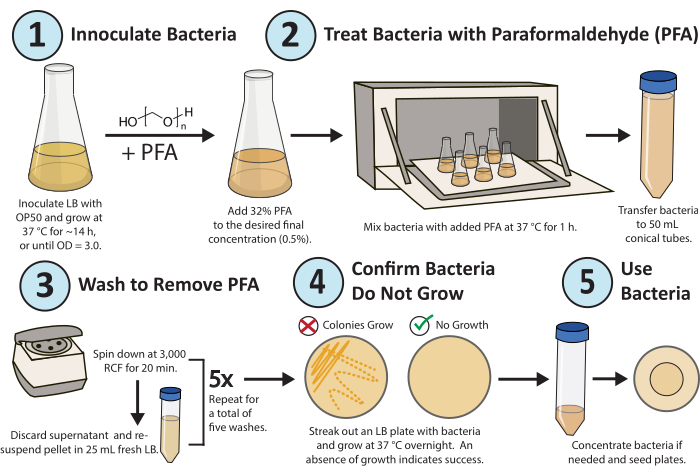
図 1.パラホルムアルデヒド処理のワークフロー。大腸菌OP50バクテリアの単一コロニーを一晩で増殖させます。PFAを最終濃度0.5%になるように添加し、PFA処理した培養液を37°Cで1時間振とうします。 最後に、培養液を新鮮なLB 5xで洗浄してPFAを除去します。処理した細菌が複製的に不活性であることを確認するには、処理した細菌のLBプレートをストリークし、一晩増殖させます。この図の拡大版をご覧になるには、ここをクリックしてください。
結果
プロトコルの詳細なワークフローを図1に示します。パラホルムアルデヒドを用いた線虫群の代謝および薬物研究において、細菌の複製(図2A)および代謝(図2B)を一貫して不活性化するハイスループットメソッドが開発され、最適化されました16。目標は、線虫のさまざまな健康状態に影響を与えること?...
ディスカッション
他の細菌殺傷法と比較したPFA殺菌の利点
PFA処理は、線虫の栄養価の高い食物源を維持しながら、細菌の代謝を防ぐためのハイスループットな方法です。PFA処理によるバクテリアの死滅には、他の方法に比べて複数の利点があります。UV処理では、すべてのプレートを正常に殺傷するためにテストする必要がありますが、PFA処理されたバクテリアのバッチからの単一のプ?...
開示事項
著者は何も開示していません。
謝辞
この研究は、NIH R21AG059117とミシガン大学のPaul F. Glenn Laboratories for Biology of Aging Researchから資金提供を受けました。SBはT32AG000114から資金提供を受けました。ESKはNSF DGE 1841052から資金提供を受けました。
資料
| Name | Company | Catalog Number | Comments |
| Aluminum Foil | Staples | 2549291 | |
| Bunsen burner | VWR | 470121-700 | |
| Cell Density Meter | Denville | 80-3000-45 | |
| Centrifuge | Eppendorg | 5430 | |
| Chemical fume hood | Labcono | 975050411384RG | |
| Conincal tubes (50 mL) | Fisher | 339652 | |
| Cuvettes | Fisher | 14-955-127 | |
| E. coli OP50 | CGC | OP50 | |
| Erlenmyer flasks | Fisher | 250 mL: FB501250 500 mL: FB501500 1000 mL: FB5011000 | |
| Inoculation loop | Fisher | 22-363-605 | |
| LB Agar | Fisher | BP1425500 | |
| Liquid waste collection bottle | Thomas Scientific | 1230G50 | |
| Magnesium Sulfate (MgSO4) | Sigma | M7506 | |
| Paraformaldehyde (32%) | Electron Microscopy Sciences | 15714-S | Paraformaldehyde – methanol free solution |
| Pipettor | Eppendorf | Eppendorf Easypet 3 | |
| Plastic dishes (100 mm) | Fisher | FB0875712 | |
| Potassium Phosphate Monobasic (KH2PO4) | Fisher | P2853 | |
| Seahorse XF Calibrant | Agilent | 100840-000 | |
| Seahorse XFe96 Extracellular Flux Assay Kit and Cell Culture Microplate | Agilent | 101085-004 | |
| Serological pipettes (50 mL) | Genesee Scientific | 12-107 | |
| Shaker incubator | Thermo | 11 676 083 | |
| Sodium Chloride (NaCl) | Fisher | S640-3 | |
| Sodium Hydroxide (NaOH) | Fisher | S318500 | |
| Sodium Phosphate Dibasic Anhydrous (Na2HPO4) | Sigma | S374-500 | |
| Solid waste collection bucket | M&M Industries | 5.0 Gallon M1 Traditional Pail | |
| Tryptone | Genesee Scientific | 20-251 | |
| Vortex | Thermo | 11676331 | |
| Weighing balance | C Goldenwall | HZ10K6B | |
| Yeast Extract | Genesee Scientific | 20-255 |
参考文献
- Riddle, D. L., Blumenthal, T., Meyer, B. J., Priess, J. R. C. . Elegans II. 33, (1997).
- Corsi, A. K., Wightman, B., Chalfie, M. A transparent window into biology: A primer on caenorhabditis elegans. WormBook. , 1-31 (2015).
- Kaletta, T., Hengartner, M. O. Finding function in novel targets: C. elegans as a model organism. Nature reviews. Drug discovery. 5 (5), 387-398 (2006).
- Meneely, P. M., Dahlberg, C. L., Rose, J. K. Working with worms: Caenorhabditis elegans as a model organism. Current Protocols Essential Laboratory Techniques. 19 (1), (2019).
- Zhang, S., Li, F., Zhou, T., Wang, G., Li, Z. Caenorhabditis elegans as a useful model for studying aging mutations. Frontiers in Endocrinology. 11, 554994 (2020).
- Feng, M., Gao, B., Garcia, L. R., Sun, Q. Microbiota-derived metabolites in regulating the development and physiology of Caenorhabditis elegans. Frontiers in Microbiology. 14, 1035582 (2023).
- McIntyre, G., Wright, J., Wong, H. T., Lamendella, R., Chan, J. Effects of FUdR on gene expression in the C. elegans bacterial diet OP50. BMC Research Notes. 14 (1), 207 (2021).
- Cabreiro, F., et al. Metformin retards aging in c. Elegans by altering microbial folate and methionine metabolism. Cell. 153 (1), 228-239 (2013).
- Worthy, S. E., et al. Identification of attractive odorants released by preferred bacterial food found in the natural habitats of c. Elegans. PLoS One. 13 (7), e0201158 (2018).
- Chen, Y. C., Seyedsayamdost, M. R., Ringstad, N. A microbial metabolite synergizes with endogenous serotonin to trigger C. elegans reproductive behavior. Proceedings of the National Academy of Sciences of the United States of America. 117 (48), 30589-30598 (2020).
- Kim, D. H., Flavell, S. W. Host-microbe interactions and the behavior of Caenorhabditis elegans. Journal of Neurogenetics. 34 (3-4), 500-509 (2020).
- Gems, D., Riddle, D. L. Genetic, behavioral, and environmental determinants of male longevity in Caenorhabditis elegans. Genetics. 154 (4), 1597-1610 (2000).
- Qi, B., Kniazeva, M., Han, M. A vitamin-b2-sensing mechanism that regulates gut protease activity to impact animal's food behavior and growth. eLife. 6, e26243 (2017).
- Garigan, D., et al. Genetic analysis of tissue aging in caenorhabditis elegans: A role for heat-shock factor and bacterial proliferation. Genetics. 161 (3), 1101-1112 (2002).
- Virk, B., et al. Folate acts in E. coli to accelerate C. elegans aging independently of bacterial biosynthesis. Cell Reports. 14 (7), 1611-1620 (2016).
- Beydoun, S., et al. An alternative food source for metabolism and longevity studies in Caenorhabditis elegans. Communications Biology. 4 (1), 258 (2021).
- Thavarajah, R., Mudimbaimannar, V. K., Elizabeth, J., Rao, U. K., Ranganathan, K. Chemical and physical basics of routine formaldehyde fixation. Journal of Oral and Maxillofacial Pathology. 16 (3), 400-405 (2012).
- Felix, H. Permeabilized and immobilized cells. Methods in Enzymology. 137, 637-641 (1988).
- Lobritz, M. A., et al. Antibiotic efficacy is linked to bacterial cellular respiration. Proceedings of the National Academy of Sciences of the United States of America. 112 (27), 8173-8180 (2015).
- Nadanaciva, S., et al. Assessment of drug-induced mitochondrial dysfunction via altered cellular respiration and acidification measured in a 96-well platform. Journal of Bioenergetics and Biomembranes. 44 (4), 421-437 (2012).
- Shtonda, B. B., Avery, L. Dietary choice behavior in Caenorhabditis elegans. The Journal of Experimental biology. 209 (Pt 1), 89-102 (2006).
- MacNeil, L. T., Watson, E., Arda, H. E., Zhu, L. J., Walhout, A. J. Diet-induced developmental acceleration independent of tor and insulin in C. elegans. Cell. 153 (1), 240-252 (2013).
- Kumar, S., et al. Lifespan extension in C. elegans caused by bacterial colonization of the intestine and subsequent activation of an innate immune response. Developmental Cell. 49 (1), 100-117 (2019).
- Nakagawa, H., et al. Effects and mechanisms of prolongevity induced by Lactobacillus gasseri sbt2055 in Caenorhabditis elegans. Aging Cell. 15 (2), 227-236 (2016).
- Kaeberlein, T. L., et al. Lifespan extension in Caenorhabditis elegans by complete removal of food. Aging Cell. 5 (6), 487-494 (2006).
- Beaudoin-Chabot, C., et al. The unfolded protein response reverses the effects of glucose on lifespan in chemically-sterilized C. elegans. Nature Communication. 13 (1), 5889 (2022).
- Komura, T., Takemoto, A., Kosaka, H., Suzuki, T., Nishikawa, Y. Prolonged lifespan, improved perception, and enhanced host defense of Caenorhabditis elegans by Lactococcus cremoris subsp. cremoris.Microbiology Spectrum. 10 (3), e0045421 (2022).
- Ye, X., Linton, J. M., Schork, N. J., Buck, L. B., Petrascheck, M. A pharmacological network for lifespan extension in Caenorhabditis elegans. Aging Cell. 13 (2), 206-215 (2014).
- Hastings, J., et al. Wormjam: A consensus C. elegans metabolic reconstruction and metabolomics community and workshop series. Worm. 6 (2), e1373939 (2017).
- O'Donnell, M. P., Fox, B. W., Chao, P. H., Schroeder, F. C., Sengupta, P. A neurotransmitter produced by gut bacteria modulates host sensory behaviour. Nature. 583 (7816), 415-420 (2020).
- Stuhr, N. L., Curran, S. P. Bacterial diets differentially alter lifespan and healthspan trajectories in C. elegans. Communications Biology. 3 (1), 653 (2020).
- Dirksen, P., et al. Cembio - the Caenorhabditis elegans microbiome resource. G3 (Bethesda). 10 (9), 3025-3039 (2020).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved