このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
単呼吸法を用いたヒトの運動中の二重試験ガス肺拡散容量測定
要約
このプロトコルは、運動中の一酸化炭素(DL、CO)および一酸化窒素(DL、NO)への拡散能力の複合単呼吸測定によって測定される肺胞毛細管予備能を評価する方法を提示します。エクササイズ中にこのテクニックを使用するための仮定と推奨事項が、この記事の基礎を形成します。
要約
一酸化炭素(DL、CO)と一酸化窒素(DL、NO)の拡散能力の複合単回呼吸測定は、健康な集団と患者集団の両方で肺胞毛細血管予備能を測定するための有用な手法です。測定値は、肺毛細血管を動員して拡張する参加者の能力の推定値を提供します。この方法は最近、軽度から中程度の強度の運動中に健康なボランティアで高いテスト再テストの信頼性を示すことが報告されています。注目すべきは、このテクニックでは最大12回の繰り返し操作が可能で、1回の呼吸で5秒という比較的短い息止め時間で済むことです。代表的なデータは、最大作業負荷の最大60%の強度の増加で、安静から運動へのDL、NO およびDL、CO の段階的な変化を示しています。拡散能力の測定と肺胞毛細血管予備能の評価は、健康な集団と慢性肺疾患などの患者集団の両方で運動に反応する肺の能力を評価するための有用なツールです。
概要
運動は、安静状態と比較してエネルギー需要の大幅な増加につながります。心臓と肺は、心拍出量と換気の増加によって応答し、肺胞毛細血管床の拡張、主に肺毛細血管の動員と膨張を引き起こします1。これにより、肺拡散容量(DL)の増加によって測定できる十分な肺ガス交換が保証されます2,3,4。運動中にDLを測定する最初の試みは、100年以上前にさかのぼります5,6,7。安静状態からDLを増加させる能力は、しばしば肺胞毛細血管予備能と呼ばれる8,9。
実験的には、肺胞毛細血管膜拡散能(DM)および肺毛細血管血液量(VC)の肺胞毛細血管予備能に対する相対的な寄与は、吸気酸素の古典的な多重画分()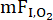 法10を含むさまざまな方法によって評価することができる。この文脈で有用であり得る代替技術は、DLから一酸化炭素(CO)および一酸化窒素(NO)(DL、CO / NO)が同時に測定されるデュアルテストガス法である11。この技術は1980年代に開発され、NOとヘモグロビン(Hb)の反応速度がCOよりも大幅に高いという事実を利用して、COの肺拡散はNOよりもVCに大きく依存します。 したがって、CO拡散に対する耐性(~75%)の主な部位は赤血球内にあります。 一方、NO拡散に対する主な抵抗(~60%)は、肺胞毛細血管膜と肺血漿12にあります。したがって、DL,COおよびDL,NOの同時測定により、D L12に対するDMおよびVCの相対的な寄与の評価が可能になり、運動中に観察されるDL,NOの変化は、肺胞毛細血管膜の拡張を大きく反映する。運動中に測定値を取得する場合のこの方法のさらなる利点は、標準化された10秒の息止めで複数の繰り返し操作が異なる酸素レベルで実行される従来の
法10を含むさまざまな方法によって評価することができる。この文脈で有用であり得る代替技術は、DLから一酸化炭素(CO)および一酸化窒素(NO)(DL、CO / NO)が同時に測定されるデュアルテストガス法である11。この技術は1980年代に開発され、NOとヘモグロビン(Hb)の反応速度がCOよりも大幅に高いという事実を利用して、COの肺拡散はNOよりもVCに大きく依存します。 したがって、CO拡散に対する耐性(~75%)の主な部位は赤血球内にあります。 一方、NO拡散に対する主な抵抗(~60%)は、肺胞毛細血管膜と肺血漿12にあります。したがって、DL,COおよびDL,NOの同時測定により、D L12に対するDMおよびVCの相対的な寄与の評価が可能になり、運動中に観察されるDL,NOの変化は、肺胞毛細血管膜の拡張を大きく反映する。運動中に測定値を取得する場合のこの方法のさらなる利点は、標準化された10秒の息止めで複数の繰り返し操作が異なる酸素レベルで実行される従来の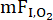 技術と比較して、比較的短い息止め時間(~5秒)と少ない操作を伴うことです。最近では
技術と比較して、比較的短い息止め時間(~5秒)と少ない操作を伴うことです。最近では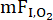 、息止め時間が短く、各強度13での操作が少なくなっていますが。それにもかかわらず、
、息止め時間が短く、各強度13での操作が少なくなっていますが。それにもかかわらず、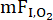 セッションごとに合計6回のDL、CO操作しか許可されませんが、最大12回のDL、CO / NO操作を繰り返しても、結果の推定値に測定可能な影響はありません14。長時間の息止めと複数回の操作の両方は、非常に高い強度または呼吸困難を経験する患者集団で実行するのが難しい場合があるため、これらは運動中に測定値を取得する際の重要な考慮事項です。
セッションごとに合計6回のDL、CO操作しか許可されませんが、最大12回のDL、CO / NO操作を繰り返しても、結果の推定値に測定可能な影響はありません14。長時間の息止めと複数回の操作の両方は、非常に高い強度または呼吸困難を経験する患者集団で実行するのが難しい場合があるため、これらは運動中に測定値を取得する際の重要な考慮事項です。
本論文は、運動中のDL、CO / NO の測定と肺胞毛細血管予備能の指標としての使用に関する理論的考察と実践的な推奨事項を含む詳細なプロトコルを提供します。この方法は、実験設定に容易に適用でき、肺での拡散制限がさまざまな集団の酸素摂取にどのように影響するかを評価できます。
理論と測定原理
DL,CO/NO 法では、吸入後にガスが換気された肺胞腔に均等に分布すると仮定して、混合ガスを 1 回吸入します。混合ガスは、不活性トレーサーガスを含むいくつかのガスからなる。呼気終末空気中のその画分に基づいて、換気された肺胞腔内のトレーサーガスの希釈を使用して、肺胞容積(VA)を計算できます15。混合ガスには試験ガスCOとNOも含まれており、どちらも換気された肺胞空間で希釈され、肺胞毛細血管膜を横切って拡散します。肺胞分画に基づいて、胞巣腔からの拡散定数とも呼ばれる個々の消失率(k)を計算できます。慣例により、単呼吸操作中に測定される試験ガスのDL は、以下の式16によって導かれる。
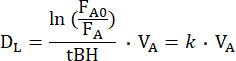
ここで、FA0は、個々のDL操作の息止め開始時の試験ガスの肺胞分率(COまたはNO)であり、FAは、息止め終了時の試験ガスの肺胞分率であり、tBHは、息止め時間である。DLは、血漿と赤血球内部を通って肺胞毛細血管膜を横切ってヘモグロビンに至る試験ガスのコンダクタンスと機械的に等価です。したがって、それはDMのコンダクタンスと肺毛細血管血のいわゆる比コンダクタンス(θ)の両方に依存し、後者は血液中の試験ガスのコンダクタンスとヘモグロビンとの反応速度の両方に依存する10。コンダクタンスの逆数が抵抗であることを考えると、テストガスの移動に対する総抵抗は、直列10の次の抵抗に依存します。
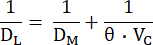
これらの成分は、異なるθ値を有し、したがって、それぞれのDL値がVCに異なるように依存するため、DLをCOおよびNOに同時に測定することによって区別することができる。COの肺拡散はNOよりもVCに大きく依存しており、CO拡散に対する耐性の主な部位(~75%)は赤血球内に位置している12。対照的に、NO拡散に対する主な抵抗(~60%)は、NOとヘモグロビンの反応速度がCOの反応速度よりも大幅に大きいため、肺胞毛細血管膜と肺血漿にあります。 したがって、DL,COとDL,NOを同時に測定することにより、DMとVCの両方の変化が前者に著しく影響します。 一方、後者はVCへの依存度がはるかに低いため、DLを決定する要因の統合評価が可能になります。
DL,CO/NO メトリックのレポートは、異なる単位を使用して行うことができます。したがって、欧州呼吸器学会 (ERS) は mmol/min/kPa を使用しますが、米国胸部学会 (ATS) は mL/min/mmHg を使用します。単位間の変換係数は2.987 mmol / min / kPa = mL / min / mmHgです。
プロトコル
デンマーク首都圏の科学倫理委員会は、以前に、健康なボランティアと慢性閉塞性肺疾患(COPD)患者の両方で、安静時、運動中、および仰臥位でのDL、CO / NO の測定を承認しました 私たちの施設での(プロトコルH-20052659、H-21021723、およびH-21060230)。
注意: 運動中にDL、CO / NOを測定する前に、動的肺活量測定と心肺運動テスト(CPET)を実行する必要があります。動的スパイロメトリーは、個々のDL、CO/NO操作の品質管理に使用され、CPETは、運動中にDL、CO/NOを測定する作業負荷を決定するために使用されます。特に閉塞性肺疾患による気流制限のある患者では、動的肺活量測定を全身プレチスモグラフィーで補完して、肺活量の有効な測定値を得ることが有利な場合があります。.CPETを開始する前に、既知の禁忌を除外するための医学的健康診断が推奨されます17。重要なことに、CPETは、以前の激しい運動が少なくとも最大24時間XLに影響を与える可能性があるため、運動中に得られたDL、CO / NO測定の少なくとも48時間前に実行する必要があります18,19。
1. 動的肺活量測定
注:動的スパイロメトリーは、ERSおよびATS20の現在の臨床ガイドラインに従って実行する必要があります。
- 体重(100g単位)と身長(1mm単位)を測定します。
- 参加者に直立した椅子に座ってもらいます。
- 他の場所で説明されているように、強制期限切れ操作中に動的スパイロメトリーを実行して、1秒(FEV1)および参加者の強制呼気量(FVC)の強制呼気量(FVC)を特定します。
2.心肺運動テスト(CPET)
注:CPETは、現在の臨床的推奨事項21に沿って実行する必要があります。
- 参加者の身長に応じてサイクルエルゴメーターを調整し、心拍数(HR)モニターを胸部に置きます。
- 参加者をサイクルエルゴメーターに置きます。参加者に代謝測定システムに接続されたマスクを装備して、テスト中の換気と肺ガス交換を測定します。
- 参加者に、自己選択したペース≥毎分60ラウンド(RPM)でサイクリングを開始し、自己申告の活動レベル、毎日のフィットネス、および疾患状態に基づいて、最大下ワークロードで5分間のウォームアップ期間を実行するように指示します(例:15〜150 W)。
- 参加者が自発的な枯渇に達するまで、毎分5〜20Wのワークロードを増やします。増分は、参加者の現在のフィットネスレベルに基づいている必要があるため、テストは段階フェーズの開始から8〜12分後に終了すると予想されます。
- 次の48時間は他の激しい運動を避けるように参加者に指示します。
3.単呼吸拡散容量装置の校正
注意: 流量センサーとガス分析計を校正して、測定値が有効で信頼できることを確認する必要があります。正確な手順は、メーカーとデバイスによって異なります。生物学的防除を含む校正手順は、各研究日に完了する必要があり、週に実行される研究日が 1 日未満の場合は、追加の毎週の校正を実行する必要があります。実験装置を 図1に示します。
- コンピュータでソフトウェアプログラムを開くと、じん肺の十分な温度を確保するために50分の自動ウォームアップ期間が開始されます。
- テストガスの入った容器が開いていることを確認してください( 図1Dを参照)。
- まず、ニューモタックからのサンプリングラインをCALと呼ばれるMS-PFT分析ユニットプラグインに接続して、ガス校正を実行します( 図1Bを参照)。
- ホームページで [Calibration ](校正)を選択し( 図2Aを参照)、[ Gas calibration](ガス校正)を選択して、ガス校正を開始します。Start(スタート) またはF1(F1 )を押してキャリブレーションを開始します( 図2Bを参照)。
- サンプリングラインをニューモタックに取り付けて、ガス校正が完了し、受け入れられたら。
- 有効な 3 L シリンジを使用して容量校正を行います。ホームページで [Calibration](キャリブレーション )を選択し( 図2Aを参照)、[Volume calibration]( ボリュームキャリブレーション)を選択して、ボリュームキャリブレーションを開始します。 F1を押してキャリブレーションを開始し、ソフトウェアの指示に従います( 図2Cを参照)。
- 吸気バッグがMS-PFT分析ユニットに接続されていることを確認してください( 図1Cを参照)。
- 座位で安静時に生物学的防除測定を行うことにより、校正手順を完了します。これは、方法の信頼性を確保するために、健康な非喫煙者が行う必要があります。特定の被験者の DL、CO または DL、NO の週ごとの変動がそれぞれ 1.6 および 6.5 mmol/min / kPa (5 および 20 mL/min / mmHg) を超える場合、変動は機械エラーが原因である可能性があり、さらに調査する必要があります12, 22。
4. 参加者の準備
- DL、CO/NO が測定される選択した強度 (最大ワークロードの % (Wmax)) について、以前の CPET 結果から目的のワークロードを計算します。
- 参加者がCPETを実行してから少なくとも48時間後に、参加者に実験室に戻って、運動中にDL、CO / NO 測定を取得するように依頼します。
- 患者の毛細血管血から身長(cmからmm単位)、体重(kg単位から100 g単位)、およびHb(mmol / Lから0.1 mmol / L単位)を測定します。
- プログラムのホームページで、 患者>新しい患者 ( 図2Aを参照)を選択し、必要なデータ(参加者のID、姓、名、生年月日、性別、身長、体重)を入力します。 OK または F1 を選択して続行します( 図2Dを参照)。
5. 直立した休息の間のDL、CO/NO の測定
注:DL、CO / NO 測定は、ERSタスクフォース12からの現在の臨床推奨事項に従って実行されます。
- ホームページで、 測定>膜拡散なし を選択します( 図2Eを参照)。
- ソフトウェアの自動リセットを開始し、すべてのテストガスのガス分析計をゼロにし、接続された吸気バッグ内のテストガスの混合を開始します。 F1 を押して自動リセットを開始します( 図2Fを参照)。
- 自動リセットには140〜210秒かかります。ソフトウェアの指示に従って、測定を開始するタイミングを認識します。ソフトウェアが 患者を接続するように指示したら、すぐに測定を開始することが重要です。
- ノーズクリップ付きの直立椅子に参加者を置きます。以下に説明するように、操作の実行方法を参加者に指示します。
- 参加者にノーズクリップを使用し、気泡に接続されたマウスピースから通常の潮汐呼吸を開始するように依頼します。測定のためのクローズドシステムを確保するために、参加者の唇がマウスピースの周りで閉じていることを確認してください。
- 3回の正常な呼吸の後、残存容積(RV)に達するために急速な最大呼気を実行するように参加者に指示します。
- RV に達したら、すぐに参加者に、< 4 秒の吸気時間を目標に、総肺活量 (TLC) に対して迅速な最大吸気を実行するように指示します。最大吸気中、バルブが開き、参加者は吸入直前に吸気バッグ内の既知の濃度のNO(800 ppm NO / N2)と混合されたガス混合物を吸入できます。
- 参加者にTLCで5(4-8)秒の息止めを行うように依頼します。吸気中、吸気量(VI)≥FVC(またはプレチスモグラフィーベースの肺活量の90%)、4〜8秒の息止め時間が目標とされています23(表1)。
- 息を止めた後、参加者に、中断することなく強く安定した最大呼気を実行するように指示します。
- 最大有効期限が切れたら、参加者にマウスピースとノーズクリップを手放すように依頼します。その後、ソフトウェアはコマンドなしでD L,NO と DL,CO を計算します。
- 操作全体を通して口頭での励ましを使用して、参加者がRVとTLCに到達するようにします。 表1に従って操作の受容性を評価します。
- 少なくとも4分間のウォッシュアウト期間の後、2つの操作が許容基準(表1)を満たすまで、または同じセッションで合計12の操作(以下を参照)が実行されるまで、操作を再度実行します。
- DL、NO およびDL、CO は、 表2に概説されている基準に従って報告されます。また、報告されているように、息止め時間、吸気量、および肺胞容積を推奨します。さらに、許容可能で再現可能な操作の数を報告する必要があり、許容性または再現性の基準を満たさない操作に基づく調査結果は慎重に解釈する必要があります。
6. 運動中のDL、CO/NO 測定
注:エクササイズ中のDL、CO/NO 測定のタイムラインを 図3に示します。
- サイクルエルゴメーターは、参加者がサイクリング位置を変えずにマウスピースで呼吸できる距離に置きます。自転車の正しい作業位置で測定を実行できるように、機器の高さを上げます( 図2を参照)。
- 参加者をサイクルエルゴメーターに置き、心拍モニターを胸に置きます。ステップ5.3で概説されているように、各操作を実行するように参加者に指示します。
- 測定前のウォームアップとして、最大下負荷で5分間のサイクリングを開始するように参加者に指示します。
- F1を押してデバイスの自動リセットを開始すると同時に、ワークロードを目標強度まで増やします(手順5.2を参照)。自動リセットには140〜210秒かかりますが、これは参加者が定常状態に達したことを確認するのに十分です。
- 自動リセットが終了したら、マウスピースを参加者に向け、参加者が目標強度でサイクリングを続けている間、以下に説明する操作を実行します。
- 手順 5.4 から 5.5 の手順に従います。各ワークロードで受容性と再現性の基準(表1)を評価し、休息中の測定値について報告します(ステップ5.6および 表2を参照)。
- 操作が完了したら、マウスピースを取り外し、作業負荷を15〜40Wに減らします。 アクティブリカバリフェーズを2分間実行した後、手順6.4と6.5を繰り返します。2分間のアクティブリカバリと自動リセット中の140〜210秒は、4〜5分の十分なウォッシュアウト期間を提供します。
結果
このプロトコルは 2021 年に実施され、執筆時点では、運動中に合計 124 回の測定が行われました (つまり、健康なボランティアで 51 回、さまざまな重症度の COPD 患者で 73 回) が実施されました。操作、達成された合格性と再現性の基準に関するデータ、および失敗率はすべて 表 3 に示されています。
計算
例として、以下に説明す?...
ディスカッション
このプロトコルは、デュアルテストガスシングルブレス技術を使用して、運動中のDL、CO / NO の測定に標準化されたアプローチを提供します。得られたDL、CO / NOメトリックは肺毛細血管の動員と膨張により増加するため、この方法は肺胞毛細血管予備能の生理学的に意味のある尺度を提供します。
プロトコルの重要なステップ
この方法では...
開示事項
この記事で紹介されている機器とソフトウェアは無料ではありません。作成者は、ソフトウェアのライセンスを提供する会社とは関係ありません。すべての著者は、競合する金銭的利益がないことを宣言します。
謝辞
この研究は、スヴェンド・アンダーセン財団から資金援助を受けました。身体活動研究センターは、TrygFonden Grants ID 101390、ID 20045、およびID 125132によってサポートされています。JPHはヘルシーフォンデンとコペンハーゲン大学病院、リグスホスピタレットから資金提供を受けており、HLHはベケット財団から資金提供を受けています。
資料
| Name | Company | Catalog Number | Comments |
| HemoCue Hb 201+ | HemoCue, Brønshøj, Denmark | Unkown | For measurements of hemoglobin |
| Jaeger MasterScreen PFT pro (Lung Function Equipment) | CareFusion, Höchberg, Germany | Unkown | For measurements of DLCO/NO |
| Mouthpiece | SpiroBac, Henrotech, Aartselaar, Belgium | Unkown | Used together with the Lung Fuction Equipment. (dead space 56 ml, resistance to flow at 12 L s−1 0.9 cmH2O) |
| Nose-clip | IntraMedic, Gentofte, Denmark | JAE-892895 | |
| Phenumotach | IntraMedic, Gentofte, Denmark | JAE-705048 | Used together with the Lung Fuction Equipment |
| SentrySuite Software Solution | Vyaire's Medical GmbH, Leibnizstr. 7, D-97204 Hoechberg Germany | Unkown | |
| Test gasses | IntraMedic, Gentofte, Denmark | Unkown | Concentrations: 0.28% CO, 20.9% O2, 69.52% N2 and 9.3% He |
参考文献
- Johnson Jr, R. L., Heigenhauser, G. J. F., Hsia, C. C., Jones, N. L., Wagner, P. D. Determinants of gas exchange and acid-base balance during exercise. Compr Physiol. , 515-584 (2011).
- Rampulla, C., Marconi, C., Beulcke, G., Amaducci, S. Correlations between lung-transfer factor, ventilation, and cardiac output during exercise. Respiration. 33 (6), 405-415 (1976).
- Tedjasaputra, V., Bouwsema, M. M., Stickland, M. K. Effect of aerobic fitness on capillary blood volume and diffusing membrane capacity responses to exercise. J Physiol. 594 (15), 4359-4370 (2016).
- Tamhane, R. M., Johnson, R. L., Hsia, C. C. W. Pulmonary membrane diffusing capacity and capillary blood volume measured during exercise from nitric oxide uptake. Chest. 120 (6), 1850-1856 (2001).
- Bohr, C. On the determination of gas diffusion through the lungs and its size during rest and work. Zentralblatt für Physiologie. 23 (12), 374-379 (1909).
- Krogh, A., Krogh, M. On the rate of diffusion of carbonic oxide into the lungs of man. Skandinavisches Archiv Für Physiologie. 23 (1), 236-247 (1910).
- Krogh, M. The diffusion of gases through the lungs of man. J Physiol. 49 (4), 271-300 (1915).
- Hsia, C. C., Herazo, L. F., Ramanathan, M., Johnson, R. L. Cardiopulmonary adaptations to pneumonectomy in dogs IV. Membrane diffusing capacity and capillary blood volume. J Appl Physiol. 77 (2), 998-1005 (1994).
- Behnia, M., Wheatley, C. M., Avolio, A., Johnson, B. D. Alveolar-capillary reserve during exercise in patients with chronic obstructive pulmonary disease. Int J Chron Obstruct Pulmon Dis. 12, 3115-3122 (2017).
- Roughton, F. J., Forster, R. E. Relative importance of diffusion and chemical reaction rates in determining rate of exchange of gases in the human lung, with special reference to true diffusing capacity of pulmonary membrane and volume of blood in the lung capillaries. J Appl Physiol. 11 (2), 290-302 (1957).
- Borland, C., Higenbottam, T. A simultaneous single breath measurement of pulmonary diffusing capacity with nitric oxide and carbon monoxide. Eur Respir J. 2 (1), 56-63 (1989).
- Zavorsky, G. S., et al. Standardisation and application of the single-breath determination of nitric oxide uptake in the lung. Eur Respir J. 49 (2), 1600962 (2017).
- Tedjasaputra, V., Van Diepen, S., Collins, S., Michaelchuk, W. M., Stickland, M. K. Assessment of pulmonary capillary blood volume, membrane diffusing capacity, and intrapulmonary arteriovenous anastomoses during exercise. J Vis Exp. (120), e54949 (2017).
- Zavorsky, G. S. The rise in carboxyhemoglobin from repeated pulmonary diffusing capacity tests. Respir Physiol Neurobiol. 186 (1), 103-108 (2013).
- Graham, B. L., et al. ERS/ATS standards for single-breath carbon monoxide uptake in the lung. Eur Respir J. 49 (1), 1600016 (2017).
- Hughes, J. M., Pride, N. B. Examination of the carbon monoxide diffusing capacity (DLCO) in relation to its KCO and VA components. Am J Respir Crit Care Med. 186 (2), 132-139 (2012).
- Balady, G. J., et al. Clinician's guide to cardiopulmonary exercise testing in adults: a scientific statement from the American heart association. Circulation. 122 (2), 191-225 (2010).
- Hanel, B., Clifford, P. S., Secher, N. H. Restricted postexercise pulmonary diffusion capacity does not impair maximal transport for O2. J Appl Physiol. 77 (5), 2408-2412 (1994).
- Sheel, A. W., Coutts, K. D., Potts, J. E., McKenzie, D. C. The time course of pulmonary diffusing capacity for carbon monoxide following short duration high intensity exercise. Respir Physiol. 111 (3), 271-281 (1998).
- Graham, B. L., et al. Standardization of spirometry 2019 update an official American Thoracic Society and European Respiratory Society technical statement. Am J Respir Crit Care Med. 200 (8), e70-e88 (2019).
- Glaab, T., Taube, C. Practical guide to cardiopulmonary exercise testing in adults. Respir Res. 23 (1), 9 (2022).
- Munkholm, M., et al. Reference equations for pulmonary diffusing capacity of carbon monoxide and nitric oxide in adult Caucasians. Eur Respir J. 52 (1), 1500677 (2018).
- Dressel, H., et al. Lung diffusing capacity for nitric oxide and carbon monoxide: dependence on breath-hold time. Chest. 133 (5), 1149-1154 (2008).
- Madsen, A. C., et al. Pulmonary diffusing capacity to nitric oxide and carbon monoxide during exercise and in the supine position: a test-retest reliability study. Exp Physiol. 108 (2), 307-317 (2023).
- Ross, B. A., et al. The supine position improves but does not normalize the blunted pulmonary capillary blood volume response to exercise in mild COPD. J Appl Physiol. 128 (4), 925-933 (2020).
- Zavorsky, G. S., Lands, L. C. Lung diffusion capacity for nitric oxide and carbon monoxide is impaired similarly following short-term graded exercise. Nitric Oxide. 12 (1), 31-38 (2005).
- Alves, M. M., Dressel, H., Radtke, T. Test-retest reliability of lung diffusing capacity for nitric oxide during light to moderate intensity cycling exercise. Respir Physiol Neurobiol. 304, 103940 (2022).
- Jorgenson, C. C., Coffman, K. E., Johnson, B. D. Effects of intrathoracic pressure, inhalation time, and breath hold time on lung diffusing capacity. Respir Physiol Neurobiol. 258, 69-75 (2018).
- Zavorsky, G. S., Quiron, K. B., Massarelli, P. S., Lands, L. C. The relationship between single-breath diffusion capacity of the lung for nitric oxide and carbon monoxide during various exercise intensities. Chest. 125 (3), 1019-1027 (2004).
- Coffman, K. E., Boeker, M. G., Carlson, A. R., Johnson, B. D. Age-dependent effects of thoracic and capillary blood volume distribution on pulmonary artery pressure and lung diffusing capacity. Physiol Rep. 6 (17), e13834 (2018).
- Borland, C. D. R., Hughes, J. M. B. Lung diffusing capacities (DL) for nitric oxide (NO) and carbon monoxide (CO): The evolving story. Compr Physiol. 11 (1), 1371 (2021).
- Tedjasaputra, V., Van Diepen, S., Collins, S. &. #. 2. 0. 1. ;., Michaelchuk, W. M., Stickland, M. K. Assessment of pulmonary capillary blood volume, membrane diffusing capacity, and intrapulmonary arteriovenoua anastomoses during exercise. J. Vis. Exp. (120), e54949 (2017).
- Thomas, A., et al. The single-breath diffusing capacity of CO and NO in healthy children of European descent. PLoS One. 12 (6), e0179097 (2017).
- Blakemore, W. S., Forster, R. E., Morton, J. W., Ogilvie, C. M. A standardized breath holding technique for the clinical measurement of the diffusing capacity of the lung for carbon monoxide. J Clin Invest. 36 (1), 1-17 (1957).
- Cotes, J. E., et al. Iron-deficiency anaemia: its effect on transfer factor for the lung (diffusiong capacity) and ventilation and cardiac frequency during sub-maximal exercise. Clin Sci. 42 (3), 325-335 (1972).
- Mann, T., Lamberts, R. P., Lambert, M. I. Methods of prescribing relative exercise intensity: Physiological and practical considerations. Sports Med. 43 (7), 613-625 (2013).
- Forster, R. E. Exchange of gases between alveolar air and pulmonary capillary blood: pulmonary diffusing capacity. Physiol Rev. 37 (4), 391-452 (1957).
- Tedjasaputra, V., et al. Pulmonary capillary blood volume response to exercise is diminished in mild chronic obstructive pulmonary disease. Respir Med. 145, 57-65 (2018).
- Nymand, S. B., et al. Exercise adaptations in COPD: the pulmonary perspective. Am J Physiol Lung Cell Mol Physiol. 323 (6), L659-L666 (2022).
- Rodríguez-Roisin, R., et al. Ventilation-perfusion imbalance and chronic obstructive pulmonary disease staging severity. J Appl Physiol. 106 (6), 1902-1908 (2009).
- Hsia, C. C., Johnson, R. L., Shah, D. Red cell distribution and the recruitment of pulmonary diffusing capacity. J Appl Physiol. 86 (5), 1460-1467 (1999).
- Wilhelm, E., Battino, R., Wilcock, R. J. Low-pressure solubility of gases in liquid water. Chem Rev. 77 (2), 219-262 (1977).
- Forster, R. E. . Diffusion of gases across the alveolar membrane. , (1987).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved