Method Article
アルツハイマー病患者のための経頭蓋パルス刺激
要約
この記事では、アルツハイマー病患者における経頭蓋パルス刺激の手順について説明します。その適応症、方法論、将来の展望について詳細に論じています。
要約
経頭蓋パルス刺激療法(TPS)は、アルツハイマー病(AD)の治療のためのConformitéEuropéenne(CE)マーキングによる非侵襲的神経調節療法です。初期のパイロット研究では、認知機能に対する有望な効果が実証されています。この記事では、MRIガイド下ニューロナビゲーションTPSデバイスを使用してAD患者を治療する手順に焦点を当てています。このために従うべきプロトコルは、必要な手順やデバイス設定など、詳細に説明されています。また、これまでに発表された代表的な臨床結果の概要も紹介します。認知と情動の有意な臨床的改善に加えて、有害事象(AE)と可能性のあるデバイス有害事象(ADE)が提示され、安全性データが提供されます。最後に、その方法について批判的に議論します。将来的には、プラセボの影響を除外するためにランダム化比較試験を実施する必要があります。また、現在、より多くの患者を対象とした長期研究も不足しています。これらの未解決の問題にもかかわらず、TPSは、制御された科学的に誘導された環境で使用された場合、アルツハイマー病患者の補助治療としての可能性を秘めています。
概要
非侵襲的脳刺激療法(NiBS)技術は、認知症研究への関心の高まりの焦点となっており、神経変性疾患に関連する認知障害および機能障害を軽減するための潜在的な治療戦略を提供しています。蓄積された証拠は、NiBSがアルツハイマー病(AD)患者の認知機能を強化したり、状態のさまざまな段階で認知機能の低下を遅らせたりできることを示唆しています1,2。これらの技術の中で、経頭蓋パルス刺激(TPS)は、皮質表面だけでなく、脳の深部領域でも、高度に焦点を絞った正確に標的を絞った脳刺激を提供する能力で特に注目に値します3,4。TPSに関連する副作用はまれで、重症度は中等度で、一過性です3,5。
整形外科や循環器病学の分野で開発された当初、超音波治療や体外衝撃波療法(ESWT)は、組織の治癒を促進し、血流を改善することが示されています。整形外科では、ESWTは特に腱鞘障害や骨治癒の問題などの筋骨格系疾患の治療に適用されましたが、心臓病学では、血管の健康への影響について調査されました6,7。TPSは、特にアルツハイマー病の研究において、神経学的応用に適応しており、認知機能低下と機能障害に対処する上で有望であることが示されています8,3,4。この手法は、このチュートリアル5のワーキンググループのパイロットデータで示されているように、衝撃波を使用してアルツハイマー病患者の症状を緩和します。衝撃波は、高周波の交互荷重を伴わないという点で超音波と異なる9。図1に示すように、生成された衝撃波プロファイルは、超音波の高周波振幅特性とともに、TPS中の特異な圧力パルスとそれに続く振幅の平坦化を明確に示しています。高周波の交互応力により、超音波のエネルギーが組織に吸収され、衝撃波では観察されない効果である組織の温暖化につながる可能性があります。他のアプリケーションでは、高エネルギーの衝撃波が使用されますが、TPSでは、組織に導入されるエネルギーは低エネルギーです9。アルツハイマー病に対する潜在的な影響は、アルツハイマー病レジストリを確立するコンソーシアム(CERAD)3の改善、およびいくつかの領域における皮質の厚さの増加10およびMRネットワーク接続性の変化11として最初に報告されました。
TPSの作用機序は現在調査中であり、この非侵襲的技術が細胞レベルで脳活動を調節し、神経可塑性を高め、認知機能を改善する可能性のある機械伝達プロセスを引き起こす可能性があることに研究が焦点を当てています3,4。衝撃波療法では、物理的エネルギーが限局性組織領域に作用し、機械伝達12を誘導し、成長因子13,14および一酸化窒素15の放出を刺激する。これらの効果は、次に、血液循環を促進し、新生血管新生を促進することができます16。
TPSの目標は、安全で症状の改善につながる可能性のある追加療法を提供することです。刺激領域には、両側前頭皮質、両側外側頭頂皮質、拡張楔前皮質、および両側側頭皮質が含まれます。通常の治療プロトコルは、最初の治療サイクルとして、2週間にわたって6,000パルスの6回のセッションで構成されています。
この手順は、一過性の中程度の主観的重症度を特徴とするセッションの約4%で有害事象が報告されており、デバイス関連有害事象(ADE)との明確な因果関係がないため、安全であると考えられています5。
これらの初期結果は有望ですが、研究者や臨床医にとって、TPSが特定のアプリケーションに適しているかどうかを評価することが重要です。考慮すべき要素には、アルツハイマー病の病期、他の治療に対する患者の反応、専門家の指導の下でTPSを安全に投与できる施設の利用可能性が含まれます。アルツハイマー病の初期から中等度の段階にある個人にとって、TPSは最小限の副作用で潜在的な認知上の利点を提供する可能性がありますが、まだ単独の治療法とは見なされていません。むしろ、薬理学的介入や認知トレーニングなどの既存の治療法を補完するかもしれません。ランダム化比較試験の結果は、現在まで不足している。しかし、TPSは、制御された使用と科学的探求の下で、アルツハイマー病患者のための追加治療としての可能性を秘めているかもしれません。
プロトコル
TPS治療を受けたすべての患者の分析は、地域医療会議所の倫理委員会(Ärztekammer Nordrhein, Nr. 2021026)によって承認された地域登録簿の一部であった。さらに、すべての患者が治療に対する書面による同意に署名しました。合計11人の患者がTPSで治療されました(男性9人、女性2人、年齢範囲59-77歳、M = 69.82)。治療の前に、すべての患者は詳細なインフォームド コンセント プロセスを受け、その間、NEUROLITH システムによる経頭蓋パルス刺激 (TPS) の潜在的な利点とリスクについて徹底的に知らされました。
1. 患者様の選択と準備
- この刺激を開始する前に、患者の選択とインフォームドコンセントが重要です。アルツハイマー病のCEマークを使用してください。アルツハイマー病の臨床症候群に基づくCSFバイオマーカーを使用して診断を確認します。神経内科医または精神科医による国内または国際的なガイドラインに従って疾患治療を行います。
注:TPSは、科学的な調査の下でアドオンとして提供できます。TPSは追加治療として投与されたため、すべての患者が治療全体を通じて通常の治療計画を継続しました。一部の患者は、TPSセッション中に抗認知症薬および/または抗精神病薬を服用していました。ただし、これらの薬は研究プロトコルの一部ではなく、介入の一部として変更または標準化されていません。 - TPS には次の除外基準を使用します: 血管性脳症、治療領域の血栓症、Fazekas グレード 3、腫瘍、血管奇形、金属インプラント、および脳アミロイド血管症 (CAA) など、アルツハイマー病とは無関係の関連する脳内病変には治療は禁忌です。追加の禁忌は、抗体療法の病歴または進行中の抗体療法、血液凝固障害または経口抗凝固療法、最初の適用前6週間以内のコルチコステロイド治療、てんかん(複数の発作または発作の焦点を伴う単一の発作)、TPS療法が承認されていないペースメーカー、再発性失神、攻撃性や精神病などの日常生活に影響を与える重度の情動行動障害、 妊娠、およびプロトコルの違反につながる可能性のある病状。MRI、EEG、CSF分析、臨床検査、精密検査における詳細な認知的および感情的評価を含む、診断および除外基準に関して。
2. 神経心理学的検査
- 最初の刺激の前(ベースライン)と最後の刺激の後(刺激後)に神経心理学的テストを実行します。この研究では、Alzheimer Disease Assessment Scale(ADAS)が使用されています。
- ADASを開始する前に、テスト環境を準備して、静かで快適で、気を散らすものがないことを確認します。訓練を受けた臨床医または神経心理学者と一緒に評価を行い、構造化された形式に従って特定の認知領域を評価します。
- ADASは、認知サブスケール(ADAS-Cog)と非認知サブスケールの2つの主要なコンポーネントで構成されています。最も一般的に使用されるADAS-Cogを使用して、以下で説明する一連のタスクを通じて記憶、言語、向き、および実践を評価します。
- 単語の想起:患者に単語のリストを提示し、すぐに、そして遅れてそれらを思い出すように頼みます。
- オブジェクトと指に名前を付ける: 患者に一連のオブジェクトを表示し、それらに正しい名前を付けるように依頼します。
- 次のコマンド:患者に口頭の指示に基づいて特定の行動をとるように依頼し、理解と実践を評価します。
- Visuo-construction:視空間スキルを評価するために、患者に幾何学的図形をコピーするように指示します。
- 観念的実践:患者に一般的な物(鉛筆や櫛など)の使用を実演してもらいます。
- オリエンテーション: 現在の日付、曜日、場所について患者に質問します。
- 単語認識:患者に、気を散らす単語のリストから以前に提示された単語を認識するように依頼します。
- 言語能力:構造化された会話と文の構成を通じて、患者の流暢さと理解力を評価します。
- 非認知サブスケールを使用して、気分の変化、無関心、興奮などの行動症状を評価します。
- 一貫性を保つために、検査を実施する臨床医に、ADASマニュアルに記載されている指示を厳守するように依頼してください。パフォーマンスに基づいて各タスクをスコアリングし、スコアが高いほど障害が大きいことを示します。
- 最後の刺激セッションの後、テストの並列バージョンを使用してADASを繰り返し、結果が練習効果ではなく認知機能の真の変化を反映していることを確認します。
3. 装置・環境の準備
- デバイスの電源を入れます。デバイスの背面にある主電源スイッチを見つけて、電源を入れます。
- フロントパネルのスタンバイボタンを押します。デバイスの初期化には約5分かかります。
- 患者を配置します。患者が快適に座り、首を支えられるようにします。患者に検出レンズ付きの認識メガネを着用してもらいます。メガネをテープまたはストラップで患者の頭に固定し、所定の位置に保ちます。
- カメラをセットアップします。カメラの位置を合わせて、患者の頭がフレーム内に完全に見えるようにします。このカメラは、追跡とキャリブレーションに不可欠です。
4.高電圧テスト(日常メンテナンス)
- 高電圧テスト(HV-Test)を実行します。このテストは24時間ごとに実施してください。画面の指示に従って、ハンドヘルドアプリケーターのトリガーボタンを押してテストを完了します。
5. ハンドピースの準備
- ハンドピースのメンブレンにシリコンオイルを一滴垂らして、ハンドピースを準備します。
- プレフィルドカップリングメンブレン(ディスタンスピース)をハンドピースに取り付け、最適なパフォーマンスを得るためにしっかりと固定されていることを確認します。
6. 新規患者様向けのキャリブレーション
- 患者のMRIデータを読み込みます。新しい患者には、必要なMRIスキャン(T1強調された、額から背中までの頭部の高解像度画像、耳から耳まで)が利用可能であることを確認してください。
- MRIデータを含む外部ストレージデバイス(USBまたはCD)をシステムのUSBポートに挿入します。
- 患者プロファイルを作成します。システムで [新しい患者] を選択し、必要な情報を入力します。システムで新しい患者プロファイルを作成する場合、一部の情報はMRI-CDから自動的にインポートされますが、他の詳細は手動で入力する必要があります。
- CDをシステムに挿入した後、MRI CDのメタデータから患者の氏名と生年月日が自動的に取得されます。治療計画をシステムに手動で入力します。システムに既に保存されている事前設定されたアルツハイマー病(AD)プロトコルを選択します。このプロトコルには、周波数 4 Hz、エネルギー レベル 0.2 mJ/mm2、セッションあたり 6,000 パルスの設定が含まれます。このプロトコールは、そのまま使用することも、臨床医の好みに応じて調整することもできます。
- MRIデータをロードし、画像の品質を確認します。MRIデータの品質を確認するには、システム内のMRI画像の個々のスライスを手動でスクロールします。すべての解剖学的構造が鋭く、明確に定義されていることを確認し、モーションアーチファクトや歪みがないことを確認します。T1 強調画像の全体的な解像度が、正確なニューロナビゲーションに十分であることを確認します。必要に応じて画像の選択を調整し、キャリブレーションを続行します。
- 画像をキャリブレーションするには、キャリブレーション ペンを使用して、次のパスを使用して 3 ポイント キャリブレーションを実行します。
パス1:額から後頭部まで。
パス2:片方の耳からもう片方の耳へ。
パス3:頭のてっぺんを横切って円を描くかジグザグに動きます。 - キャリブレーション中は、検出レンズが常にカメラに面していることを確認してください。
- 画面上の3D頭部モデルが患者の頭部と正しく位置合わせされているか、回転させて接触点を確認します。
7. 治療領域の設定(オプション)
- 患者の特定のニーズに基づいて治療領域を定義します。この研究では、両側前頭葉、両側頭頂葉、および楔前部を含む、事前に構成されたアルツハイマー病プロトコルが使用されました。さらに、最初のプロトコルに、両側側頭皮質を追加します。MRI画像と脳の特定の解剖学的ランドマークを使用して、刺激する領域を定義します。
- ディスプレイ上の治療領域のサイズ、形状、数を調整します。ROIを調整するために、プロセスはすべてタッチディスプレイコントロールを使用して実行されます。
- まず、システムのメインインターフェースにある治療計画モジュールにアクセスします。このモジュール内で、 ROI 調整 オプションを選択して、処理領域の編集を有効にします。調整モードに入ると、システムはデフォルトのROIを画面上に表示します。
- 前頭葉、頭頂葉、楔前、側頭皮質など、目的の解剖学的領域にROIを配置するには、タッチディスプレイの矢印ボタンを使用します。ボタンを使用すると、ROIをすべての方向(上、下、左、右)に段階的に移動して、ターゲットの脳領域に正確に位置合わせできます。
- ROIを配置したら、専用の画面上のコントロールを使用して、ROIの寸法(サイズ、奥行き、形状)を調整します。
深さ調整(ボタンA):深さボタンをタップし、ROIの浸透レベルを治療要件に合わせて調整します。
幅調整(ボタンB):幅調整ボタンを使用して、ROIの水平サイズを拡大または縮小します。
高さ調整(ボタンC):高さ調整コントロールをタップして、ROIの垂直寸法を変更します。完了したら、設定を保存します。
8. 治療の実施
- 最適なエネルギー伝達のために、患者の頭皮にたっぷりの超音波ジェルを順番に塗布します。
- 治療を開始します。デバイスで 治療モード を選択し、プレフィルドメンブレンが正しく取り付けられていることを確認します。プレフィルドメンブレンの正しい取り付けは、ハンドピースの所定の位置に適切にカチッとはまることを確認することで確認されます。オプションで、患者はセッション中に聴覚保護具を使用することができます。
- ハンドピースを患者の頭皮に対して垂直に保持し、ハンドピースが表面全体で均等に動くようにします。 図2 は、TPS中の患者とNEUROLITHとの間の理想的なアライメントを示しています。 図3 は、関心領域(ROI)の例と、患者のMRIで刺激された組織のモデリングを示しています。 図4 は、刺激中のハンドヘルドデバイスの図を示しています。
- 刺激を監視します。ディスプレイ上の対象領域が緑色に変わり、適切なカバレッジを示すまで、各領域を処理します。検出レンズをカメラの視界に入れたままハンドピースを動かし続けて、継続的な追跡を確保します。
注:治療中に認識メガネがわずかにずれる場合は、セッションを続行できます。ただし、メガネを取り外した場合は、再キャリブレーションが必要です。 - セッションを終了します。治療を終了するには、デバイスの 停止 ボタンを押します。セッションの終了点は、6000 パルスに達すると達成されます。
9. 治療後の手続き
- 機器を清掃します。承認されたワイプを使用して、ハンドピースと取り外し可能なメンブレンを清掃します(アルコールベースのクリーナーは避けてください)。
- 患者ケア:頭皮の部分をやさしく掃除して、残っている超音波ジェルを取り除きます。必要に応じて、タオルまたはヘアドライヤーで患者の髪を乾かします。治療後、めまい、頭痛、頭皮の不快感などの遅延または軽度の副作用が発生した場合に備えて、次の10〜15分間近くに留まるように患者にアドバイスしますが、積極的な観察は必要ありません。.患者に水分補給を続けるように勧めることで、全体的な回復と健康をサポートします。特にセッション後に疲労を感じたり、軽度の不快感を感じたりする場合は、その日の残りの時間は激しい身体活動を避けるように患者にアドバイスします。.
- 治療データの保存:定義された領域を含むすべての治療データを保存し、将来のセッションに合わせて調整します。治療中の観察やフィードバックは文書化する必要があります。.
結果
経頭蓋パルス刺激は、このチュートリアルのワーキンググループによって公開された11人の患者(男性9人、女性2人、年齢範囲59〜77歳、M = 69.82)からの制御されていないパイロットデータによって示されるように、アルツハイマー病患者の症状を緩和しました1。刺激された領域には、両側前頭皮質、両側外側頭頂皮質、および拡張楔前皮質が含まれていました。両側側頭皮質がプロトコルに追加されました。治療は、最初の治療サイクルとして2週間にわたって6,000パルスを使用して6回の初期セッションで実施されました。
刺激中の治療プロトコルには、4 Hz、0.20 mJ/mm2、および 6000 パルスが含まれていました。患者様11人中3人(27%)が全75回のセッションのうち3回(4%)で有害事象を報告しました。これらには、顎の痛み(NRS 4/10)、吐き気(NRS 7/10)、眠気(NRS 10/10)が含まれていました。しかし、これらのいずれも24時間以上持続することはなく、すべてがデバイス有害事象(ADE)として刺激に直接起因するわけではなかった。
ベースラインと比較した刺激後のADAS合計スコアには、ベースラインと比較して30.2から25.8に改善した(p = 0.01)と、ADAS-Cogスコアに25.8から23.3に改善した(p = 0.04; 図 5)。一部の患者ではわずかな改善しか見られませんでしたが、患者の最も良い改善は40%であり、ADAS合計スコアで15.76%、ADASコグスコアで8.65%の全体的な改善につながりました(図6)。さらに、ADASテストの自己申告サブスケールで抑うつ症状の有意差が検出されました。片側t検定は、ADASテストの自己報告サブスケールによって測定されたように、抑うつ症状の有意な減少を示しました。刺激前は0.7(SD=1.1)で、刺激後は0.2(SD=0.4;t(8)=1.859、p<0.01)に減少した。
主観的な評価尺度は、2 週間の治療期間の前後に完成しました。このスケールにより、患者は症状の重症度と認識された有害事象を0〜10の数値評価スケールで報告でき、数値が大きいほど症状の強度が高いことを示します。NRSで測定した症状の重症度の平均主観的改善は、5.7から3.4(p = 0.023)であった。
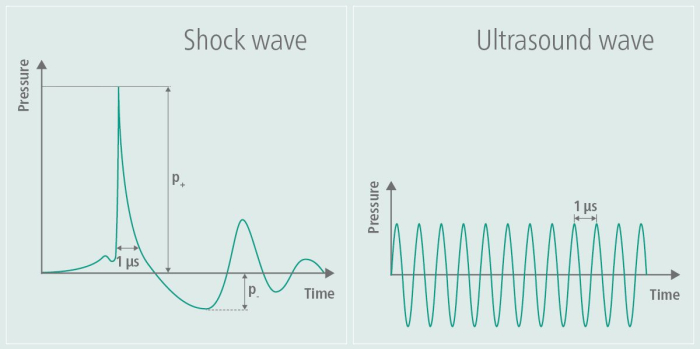
図1:刺激中の衝撃波。 グラフは、画像の左側にあるTPSの振幅を示し、それを画像の右側の超音波の振幅と比較しています。TPSでは、特異な圧力パルスが生成され、続いて振幅が平坦化されます。対照的に、超音波の振幅は再び平坦になるのではなく維持されるため、時間の経過とともに連続的な高周波振動が発生します。この数値は9から変更されています。 この図の拡大版を表示するには、ここをクリックしてください。
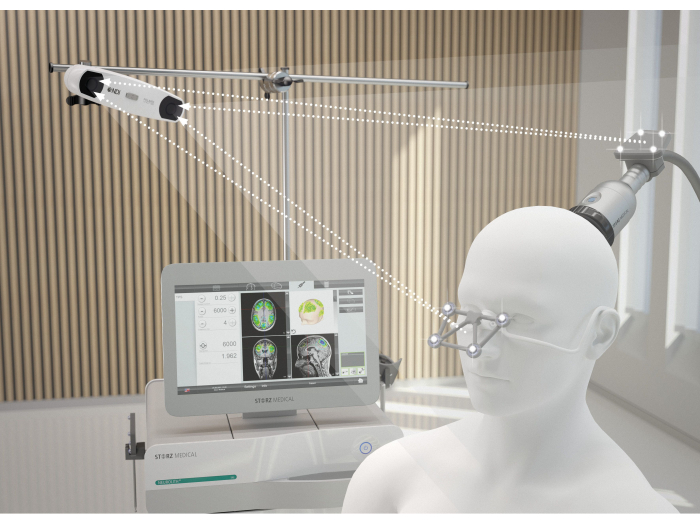
図2:MRIナビゲーションシステム。 この画像は、TPS中の患者とNEUROLITHとの間の理想的なアライメントを示しています。3Dカメラは、ゴーグルの検出レンズとハンドピースの検出レンズに接触します。この透過が保証されている場合にのみ、ハンドピースが正しい空間位置で認識され、画面上の刺激の視覚化が妨げられることはありません。この数値は9から変更されています。 この図の拡大版を表示するには、ここをクリックしてください。
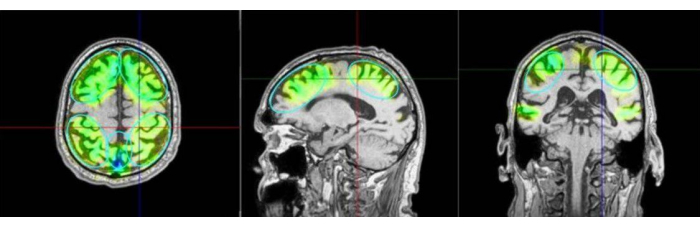
図3:関心領域と刺激された領域。 この画像は、関心領域(ROI)の例と、患者のMRIで刺激された組織のモデリングを示しています。色は、楔前部のそれぞれの領域、ならびに前頭葉および頭頂部領域に適用されるパルスの数をさらに区別します。グリーンのカラーリングに続いて、ターコイズ、ブルー、バイオレットが続きます。バイオレットは過度の強度を示しており、避ける必要があります。刺激された領域は、主に到達した領域としてナビゲーションシステムからのシミュレーションデータとして視覚化されますが、これは実際に適用された脳の活性化として測定されません。Kempen プロトコルでは、ROI として事前に定義されていないにもかかわらず、追加の時間刺激が追加されます。左:軸方向図、中央:矢状図、右:冠状図。 この図の拡大版を表示するには、ここをクリックしてください。
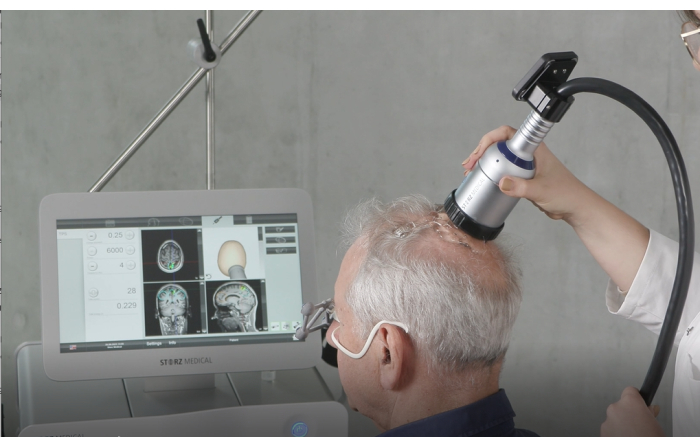
図4:ハンドヘルドデバイス。 この図は、刺激中に使用されているハンドヘルドデバイスを示しています。重要な準備手順には、最適なエネルギー伝達を確保するために十分な量の超音波ゲルを患者の頭皮に塗布すること、および事前に充填されたメンブレンがしっかりと正しく取り付けられていることを確認することが含まれます。治療中、ハンドピースは頭皮に対して垂直に保持され、表面を横切って均等に移動して、一貫した刺激を維持します。この数値は9から変更されています。 この図の拡大版を表示するには、ここをクリックしてください。
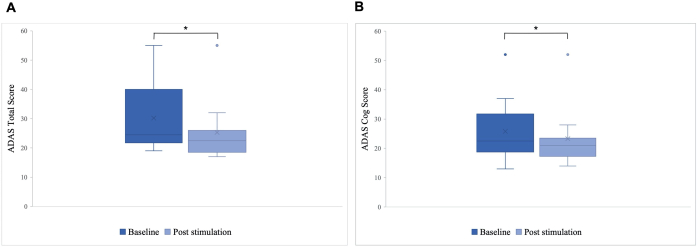
図5:最初の刺激を受ける前のアルツハイマー病評価尺度(ADAS)。 アルツハイマー病評価尺度 (ADAS) での患者グループの平均スコア (最初の刺激前 (濃い青) と最後の刺激後 (水色)。スコアが小さいほど、パフォーマンスが優れていることを示します。箱ひげ図は、患者のデータの分布を示しています。(A)ADASの合計スコア。線はグループの中央値(ベースライン= 24.5、刺激後= 22.5)、十字は平均スコア(Mベースライン= 30.2(SD 11.55)、M刺激後= 25.8(SD 10.71)、* p = 0.01)を表します。(B)ADASの歯車スコア。線はグループの中央値(ベースライン=22.5、刺激後=21)を表し、十字は平均スコア(Mベースライン=25.8(SD 10.77)、M刺激後=23.3(SD 10.27)、*p=0.04)を表しています。この数値は5から修正されています。 この図の拡大版を表示するには、ここをクリックしてください。
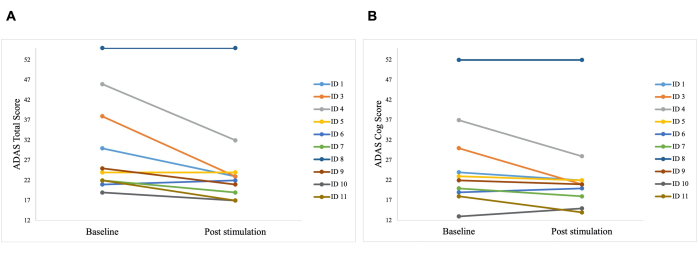
図6:ADASの患者の個々の検査結果。 アルツハイマー病評価尺度 (ADAS) の患者の個々のテスト結果 最初の刺激前 (ベースライン) と最後の刺激後 (刺激後)。スコアが小さいほど、パフォーマンスが優れていることを示します。各線は 1 人の患者を表します。(A)ADAS合計スコアにおける各患者の個々のスコア。最も改善点が多かったのは15ポイント(ID3)でした。(B)サブスケールのADASコグスコアの各患者の個々のスコア。最も改善点が多かったのは14ポイント(ID3とID4)でした。この数値は5から修正されています。 この図の拡大版を表示するには、ここをクリックしてください。
ディスカッション
全体として、TPSはアルツハイマー病の可能な治療法です。実用的な観点から、刺激プロセスはオペレーターにとって使いやすいように設計されています。処置開始時に関心領域を定義する能力と、治療中に色分けされたマーキングによって適用されるパルス数を視覚化する機能により、ユーザーインターフェースの取り扱いが大幅に簡素化されます。関心領域の設定も自由に選択でき、必要に応じて調整できます。刺激された領域はシミュレーションデータとして明確に視覚化されますが、デバイスの影響を受けるより深い領域を低エネルギーレベルで表示するには、メーカーによるさらなる開発が必要です。
TPSプロトコルの重要なステップには、標的となる脳領域への刺激デバイスの正確な配置、パルス波の正しい強度と周波数の確保、患者の反応の慎重なモニタリングが含まれます。トラブルシューティングには、エネルギー損失や最適でない刺激を防ぐために、ハンドピースと頭皮の間の最適な接触を確保することが含まれる場合があります。不快感や副作用が認められた場合は、強度の調整や体位の取り替えが必要になることがあります。
公表された非制御データは、臨床的な認知改善5,3、ならびにいくつかの脳領域における皮質の厚さの増加10およびMRネットワーク接続性の変化11を実証している。気分の改善も報告されています5,4。他の非侵襲的な脳刺激法と比較して、TPSにはいくつかの明確な利点があります。まず、機械的な衝撃波と正確なニューロナビゲーションを組み合わせ、影響を受けた脳領域に的を絞った適用を可能にします。通常、皮質表面層のみを刺激するTMSとは異なり、TPSの浸透の深さは、脳の深部構造が関与するアルツハイマー病などの神経変性疾患の治療に特に適しています。さらに、TPSは良好な安全性プロファイルを持っているようであり、治療セッションのわずか4%で最小限かつ一過性の副作用が報告されており、中等度から重度のAD患者にとってより忍容性の高い選択肢である可能性があることを示しています5。
作用機序を徹底的に調査し、TPS療法に関連する潜在的な危険因子の詳細な分析を行うには、追加の基礎研究が必要です。
この研究グループが発表した最近の研究では、アルツハイマー病患者の脳ネットワーク活動が経頭蓋パルス刺激(TPS)の前後で調べられました17。この結果は、TPSが脳の振動と接続性を調節し、アルツハイマー病の認知機能を改善する可能性があることを示しています。提案されたメカニズムの1つは、TPS後のガンマ振動の増加が脳内のリンパ性クリアランスを促進する可能性があるということです。このリンパクリアランスへの影響の可能性は、今後の研究でさらに調査されるべきである。さらに、TPSが脳ネットワーク生理機能にどのように影響するか、また、その神経保護効果がアルツハイマー病の進行を遅らせたり止めたりすることができるかどうかを明らかにするためには、さらなるメカニズム研究が必要です。
TPSが健康な脳と病気の脳の両方に及ぼす影響を調査する前臨床動物実験は、その根底にあるメカニズムをより深く理解するために重要です。さまざまなNiBS技術がそれぞれ異なるメカニズム1を通じて動作することに注意することが重要です。したがって、超音波療法18 および衝撃波療法6 について記載された組織への影響がTPS療法において役割を果たすかどうか、またどのように役割を果たすかを調査することが不可欠である。前者は、TPSがメカノトランスダクションプロセスに及ぼす影響の可能性、および血管、細胞、分子の変化を誘発する可能性について説明しており、これらは徹底的に調査する必要があります。さらに、神経炎症過程の調節、特に血液脳関門ダイナミクスに重点を置いていることは、将来の研究にとって興味深い領域を示しています。これらの影響を理解することで、根本的なメカニズムに関する貴重な洞察が得られ、治療用途のTPSの最適化に役立つ可能性があります。さらに、これは、他の神経変性疾患の管理におけるTPS治療の可能性を探ることに貢献します。
TPSは治療アプローチとして有望です。ただし、いくつかの制限に対処する必要があります。TPSの特異的な影響を正確に説明するためには、プラセボ群を用いた対照臨床試験が不可欠です。大きな課題は、刺激に対する反応の個人間変動性が高いことであり、これはアルツハイマー病(AD)の病期や併存疾患の存在などの要因によって影響を受ける可能性があります4。さらに、長期治療のための最適なプロトコルは未定義のままです。現在のアプローチには、毎月の1回の追加接種や、1年以内に12回の治療サイクルを繰り返すことなどがありますが、一方のアプローチが他方のアプローチよりも優れていることを裏付ける証拠は不足しています。今後の臨床研究では、最適な刺激パラメータの特定、患者特異的な要因(ADのステージなど)が治療結果にどのように影響するかの評価、TPS療法の長期的な効果と持続可能性の調査を優先すべきです。
開示事項
著者のラース・ヴォイテッキは、これまでにドイツ研究財団、Hilde-Ulrichs-Stiftung für Parkinsonforschung、ParkinsonFonds Germany、BMBF/ERA-NETNEURON、DFG Forschergruppe (FOR1328)、Deutsche Parkinson Vereinigung (DPV)、Forschungskommission、Medizinische Fakultät、HHU Düsseldorf、UCB から助成金と制度的支援を受けています。メドトロニック、UCB、テバ、アラガン、メルツ、アッヴィ、ロシュ、ビアル、メルク、ノバルティス、デシチン、スペクトラム。著者のLars Wojteckiは、TEVA、UCB Schwarz、Desitin、Medtronic、Abbott/Abbvie、MEDA、Boehringer I、Storz Medical、Kyowa Kirin、Guidepoint、Merck、Merz、Synergia、BIAL、Zambon、Sapio Life、STADA、Inomed、Vertanicalのコンサルタントです。著者のセリーヌ・コントは、ストルツ・メディカルのコンサルタントです。残りの著者は、この研究が潜在的な利益相反と解釈される可能性のある商業的または金銭的関係がない状態で行われたことを宣言します。
謝辞
私たちは、患者のコンプライアンスと参加に感謝します。技術支援とデータ収集は、Veronika Hirsch氏とMichaela Wessler氏(医療技術アシスタント)の協力を得て行われました。
資料
| Name | Company | Catalog Number | Comments |
| Disinfectant Wipes: mikrozid universal wipes | schülke | GTIN: 4032651957774 | Used to clean the hand piece after each session to ensure hygiene |
| Dry Towels: Wisch-/Pflegetuch Kolibri | IGEFA Handelsgesellschaft mbH & Co. KG | PZN: 10417600 | Used to dry the patient's skin after the ultrasound gel has been cleaned |
| Handpiece | Storz Medical | HW 030816.01 (114) | Used to hold the device during treatment |
| NEUROLITH | Storz Medical | SN: 19880_0015 | The NEUROLITH system with TPS is a CE-certified device |
| Patient Chair | Adjustable chair for optimal patient positioning during the treatment | ||
| silicone oil | Storz Medical | 13330 | Applied onto the membrane of the handpiece before attaching the prefilled coupling membrane (the distance piece) to the handpiece |
| Sonosid Ultrasound Gel | Asid Bonz GmbH | PZN: 5362311 | Applied to the scalp to ensure optimal transmission of acoustic pulses through the skull |
| Wash Gloves: Esemtan wash mitts | schülke | GTIN: 4032651297016 | For removing the ultrasound gel from the patient post-treatment |
参考文献
- Koch, G., et al. The emerging field of non-invasive brain stimulation in Alzheimer's disease. Brain. Epub ahead of print. , (2024).
- Menardi, A., et al. Toward noninvasive brain stimulation 2.0 in Alzheimer's disease. Ageing Res Rev. 75, 101555 (2022).
- Beisteiner, R., et al. Transcranial pulse stimulation with ultrasound in Alzheimer's disease-a new navigated focal brain therapy. Adv Sci. 7 (3), 1902583 (2019).
- Matt, E., Dörl, G., Beisteiner, R. Transcranial pulse stimulation (TPS) improves depression in AD patients on state-of-the-art treatment. Alzheimer's Dement. 8 (1), e12245 (2022).
- Cont, C., et al. Retrospective real-world pilot data on transcranial pulse stimulation in mild to severe Alzheimer's patients. Front Neurol. 13, 948204 (2022).
- Guo, J., Hai, H., Ma, Y. Application of extracorporeal shock wave therapy in nervous system diseases: A review. Front Neurol. 13, 963849 (2022).
- Khanna, A., Nelmes, R. T., Gougoulias, N., Maffulli, N., Gray, J. The effects of LIPUS on soft-tissue healing: a review of literature. Br Med Bull. 89, 169-182 (2009).
- Chen, X., You, J., Ma, H., Zhou, M., Huang, C. Transcranial pulse stimulation in Alzheimer's disease. CNS Neurosci Ther. 30 (2), e14372 (2024).
- . Website of Manufacturer Available from: https://www.storzmedical.com/en/physics-and-technology (2025)
- Popescu, T., Pernet, C., Beisteiner, R. Transcranial ultrasound pulse stimulation reduces cortical atrophy in Alzheimer's patients: a follow-up study. Alzheimer's Dement. 7 (1), e12121 (2021).
- Dörl, G., Matt, E., Beisteiner, R. Functional specificity of TPS brain stimulation effects in patients with Alzheimer's disease: A follow-up fMRI analysis. Neurol Ther. 11 (3), 1391-1398 (2022).
- d'Agostino, M. C., Craig, K., Tibalt, E., Respizzi, S. Shock wave as biological therapeutic tool: From mechanical stimulation to recovery and healing, through mechanotransduction. Int J Surg. 24, 147-153 (2015).
- Yahata, K., et al. Low-energy extracorporeal shock wave therapy for promotion of vascular endothelial growth factor expression and angiogenesis and improvement of locomotor and sensory functions after spinal cord injury. J Neurosurg. 25 (6), 745-755 (2016).
- Hatanaka, K., et al. Molecular mechanisms of the angiogenic effects of low-energy shock wave therapy: roles of mechanotransduction. Am J Physiol. 311 (3), C378-C385 (2016).
- Mariotto, S., et al. Extracorporeal shock waves: from lithotripsy to anti-inflammatory action by NO production. Nitric oxide. 12 (2), 89-96 (2005).
- Flournoy, J., Ashkanani, S., Chen, Y. Mechanical regulation of signal transduction in angiogenesis. Front Cell Dev Biol. 10, 933474 (2022).
- Wojtecki, L., Cont, C., Stute, N., Galli, A., Schulte, C., Trenado, C. Electrical brain networks before and after transcranial pulsed shockwave stimulation in Alzheimer's patients. Geroscience. Epub ahead of print. , (2024).
- Sarica, C., et al. Human studies of transcranial ultrasound neuromodulation: A systematic review of effectiveness and safety. Brain Stimul. 15 (3), 737-746 (2022).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved