Method Article
Tranexamic Acid를 이용한 마모셋 증후군의 소모성 치료 방법 수정 및 지원 조치
요약
여기에서는 마모셋 증후군(WMS, 염증성 장 질환(IBD) 유사 질환이라고도 함)을 트라넥삼산으로 소모하기 위한 수정된 치료 방법을 설명합니다. 또한 치료제를 경구, 피하, 정맥 주사로 투여하는 방법도 제시합니다.
초록
소모성 마모셋 증후군(WMS)은 포획된 일반 마모셋(Callithrix jacchus) 군체에서 발생하는 심각한 질병으로, 높은 사망률과 관련이 있습니다. WMS의 구체적인 원인은 아직 불분명하며 효과적인 치료법은 거의 없습니다. 이전에 우리는 WMS에 대한 유용한 치료법으로 지지 조치를 취한 트라넥삼산 요법을 보고했습니다. 본 연구에서는 수정된 방법을 설명합니다: 5% 트라넥삼산 0.1mL를 주 5회 피하 투여, 2.0mL의 아미노산 제제를 주 3회 정맥 주사, 링거 젖산 5.0mL와 0.1mL의 비타민 제제를 주 3회 피하 투여, 0.1mL의 철분 제제를 주 5회 경구 투여합니다. 또한 동물을 구속하는 팁으로 복재정맥을 통해 용액을 정맥 투여하는 방법과 경구 및 피하 투여에 대한 자세한 방법을 설명합니다. 변형된 방법은 원래의 WMS 처리 방법과 유사한 효율성을 가지고 있습니다.
서문
소모성 마모셋 증후군(WMS)은 포획된 일반 마모셋 군체에만 발생하는 심각한 질병입니다. 주요 증상으로는 체중 감소, 근육량 감소, 빈혈, 저알부민혈증, 만성 장염등이 있다 1,2,3,4. 일부 연구에서는 안락사된 포획 마모셋의 60.5%가 만성 장염의 증거를 가지고 있었다고 보고했다5 사망자의 31-44%가 이 질병과 관련이 있었다6. 이 질병의 유병률이 높기 때문에 효과적인 치료가 필요했습니다.
2016년, 우리는 지지 조치를 동반한 트라넥삼산이 WMS7에 효과적인 치료법이라고 보고했습니다. 또한, WMS에 영향을 받은 마모셋의 장내 단백질 손실은 이 처리로 현저히 약화되었다8. 원래의 치료 프로토콜은 확실히 효과적이었지만 다소 많은 양의 정맥 주사, 고용량의 비타민 제제, 매일 억제가 포함되었습니다. 마모셋은 손으로 포획하고 제지하는 데 취약하기 때문에 이러한 행동은 덜 빈번해야 합니다. 따라서 우리는 약간의 수정을 통해 동물의 무거운 하중을 줄이는 것을 목표로 했습니다.
본 논문에서는 수정 된 방법을 제공 할 것입니다 : 희석되지 않은 트라넥삼산의 피하 주사 주 5 회 (5 배 희석 된 트라넥삼산 용액의 복강 내 주사 대신), 정맥 주사 용 아미노산 제제 2.0 mL (3.0 mL 대신), 피하 주사 용 비타민 제형 0.1 mL (0.5 mL 대신), 그리고 철분 제형의 경구 투여는 주당 5 회 (주당 7 회 대신).
프로토콜
본 연구는 RIKEN(일본 사이타마현) 동물실험위원회의 승인(W2023-2-041)을 받아 수행되었으며, 동물이용실험에 대한 제도적 가이드라인에 따라 수행되었다. 본 연구에서는 6마리의 암컷 마모셋(2-6세)을 사용하였다.
1. 치료 시작 기준
- 다음 기준 중 하나가 관찰될 때 치료를 시작하십시오: i) 체중 < 300g 또는 월 체중 >20g 감소; ii) 저알부민혈증(혈청 알부민 < 3.8g/dL); iii) 빈혈 (헤마토크릿 < 35 %); iv) 클로스트리듐 디피실리(Clostridium difficile), 장병원성 대장균(enteropathogenic Escherichia coli) 또는 장내 원생동물(intestinal protozoa)이 없는 만성 설사; v) 근육량의 명백한 감소.
참고: WMS를 동반하는 탈수 및 그에 따른 혈중 농도로 인해 영향을 받은 동물에서 혈청 알부민과 헤마토크릿 수치가 인위적으로 상승할 수 있습니다.
2. 경구 투여
- 철분 제형 0.1mL( 재료 표 참조)를 스폰지 케이크 한 조각과 섞습니다.
- 처리된 마모셋에 으깬 것을 줍니다.
알림: 처리된 마모셋이 매시를 완전히 삼켰는지 확인하십시오.
3. 피하 투여
- WMS에 감염된 마모셋을 꼬리를 부드럽게 잡아 홈 케이지에서 잡으십시오.
- 다른 손으로 동물의 상체를 뒤에서 잡습니다.
- 동물을 치료실로 데려오십시오.
- 동물이 조수의 가슴이나 팔에 달라붙게 하십시오.
- 알코올 면봉으로 동물의 등 부분을 청소하십시오.
- 0.1g의 바늘을 사용하여 트라넥삼산(5% 용액, 재료 표 참조)을 주 5회 26g의 바늘을 사용하여 뒤쪽에 피하로 주입합니다.
- 링거 젖산 5.0mL( 재료 표 참조)와 0.1mL의 비타민 제제( 재료 표 참조)를 주당 3회 26G 바늘을 사용하여 피하에 주사합니다.
알림: 각 주입은 1분 이내에 각각의 다른 지점에서 수행해야 합니다.
4. 아미노산 제형의 정맥 투여
- WMS에 감염된 마모셋을 꼬리를 부드럽게 잡아 홈 케이지에서 잡으십시오.
- 다른 손으로 동물의 상체를 뒤에서 잡습니다.
- 동물을 치료실로 데려오십시오.
- 보조자가 양팔의 바닥을 잡고 다른 손으로 두 다리의 바닥을 잡고 하체를 제어하도록 합니다. 조수에게 동물의 하체를 구속하는 엄지 손가락을 동물의 무릎 앞쪽에 놓아 구부러지지 않도록 요청하십시오.
- 알코올 면봉으로 동물의 종아리를 청소하십시오.
- 아미노산 제형( 재료 표 참조) 2.0mL를 27G 버터플라이 바늘을 사용하여 복재정맥을 통해 일주일에 세 번 정맥 주사합니다.
알림: 주입은 최대 2분까지 가능한 한 천천히 수행해야 합니다. - 주사 후 조수에게 출혈이 멈출 때까지 흡수성으로 해당 부위를 누르도록 요청하십시오.
5. 체중 측정
- 치료(정맥 주사 및/또는 피하 주사) 후 일주일에 한 번 휴대용 상자로 동물의 무게를 측정하여 체중을 모니터링합니다.
알림: 체중은 음식의 존재에 영향을 받기 때문에 거의 동시에 마모셋의 무게를 잰다.
6. 전체 혈구 수(CBC) 분석 및 혈청 화학 검사
- WMS에 감염된 마모셋을 꼬리를 부드럽게 잡아 홈 케이지에서 잡으십시오.
- 다른 손으로 동물의 상체를 뒤에서 잡습니다.
- 동물을 치료실로 데려오십시오.
- 보조자가 양쪽 팔의 바닥을 잡고 다른 손으로 양쪽 다리의 바닥을 잡고 하체를 제어하도록 합니다.
- 시술자에게 구속되지 않은 동물의 다리를 잡도록 요청하십시오.
- 알코올 면봉으로 동물의 사타구니 부위를 청소하십시오.
- 매월 26G 바늘을 사용하여 대퇴 정맥에서 0.4mL의 혈액을 채취합니다.
- 헤마토크릿을 포함한 혈액 샘플 0.05mL를 CBC 분석에 사용합니다.
- 나머지 혈액 샘플을 실온에서 1시간 동안 그대로 두고 원심분리기를 1,800× g 에서 20분 동안 둡니다.
- 알부민을 포함한 화학 검사에 혈청을 사용하십시오.
참고: 혈청 화학 검사를 위한 매개변수 수를 최소화하여 혈액 샘플의 부피를 줄일 수 있습니다. 개별 마모셋의 상태에 따라 혈액 샘플의 부피를 조정합니다.
결과
수정된 치료 방법은 WMS에 영향을 받은 마모셋에서 헤마토크릿(그림 1A), 혈청 알부민(그림 1B) 및 체중(그림 1C)을 증가시켰습니다. 치료 전과 후 헤마토크릿(P < 0.05, Wilcoxon matched-pairs signed rank test), 혈청 알부민(P < 0.05, Wilcoxon matched-pairs signed rank test) 및 체중(P < 0.05, Wilcoxon matched-pairs signed rank test)에서 유의한 차이가 관찰되었습니다.
외모에 대한 치료 효과도 관찰되었습니다. 그림 2는 WMS에 영향을 받은 마모셋의 모습을 보여줍니다. 치료 전에는 타막, 아치형 등, 거친 털(그림 2A) 및 탈모증(그림 2B)이 관찰되었지만, 치료 후에는 비정상적인 모습이 보이지 않았습니다(그림 2C,D).
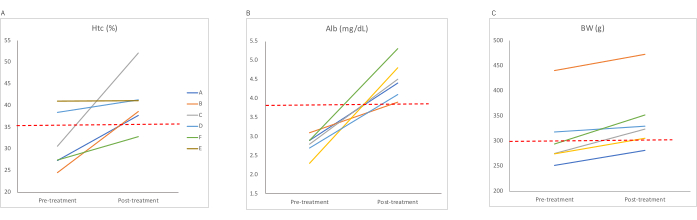
그림 1: 수정된 치료를 받은 마모셋의 헤마토크릿, 혈청 알부민 및 체중의 변화(치료 전 및 후). (A) 헤마토크릿 수치, (B) 혈청 알부민 수치, (C) 체중. 파선은 기준 값을 나타냅니다. 약어 : Htc = 헤마토크릿; Alb = 혈청 알부민; BW = 체중. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 2: WMS에 영향을 받은 마모셋의 대표적인 모습. (A) 전처리 동물의 모습 : 장막, 아치형 등, 거친 털이 관찰됩니다. (B) 전처리 동물의 꼬리 : 탈모증이 관찰됩니다. (C) 후처리 동물의 모습. (D) 후처리 동물의 꼬리. 약어: WMS = wasting marmoset syndrome. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
토론
2016년에 우리는 지지 조치가 포함된 트라넥삼산이 WMS에 효과적인 치료법이라고 보고했으며, 이는 글루코코르티코이드를 사용하지 않고 WMS 요법을 입증한 최초의 보고서였습니다. 인간의 경우, 글루코코르티코이드는 IBD의 가장 효과적인 치료법으로 간주됩니다. 그러나 가장 일반적으로 사용되는 글루코코르티코이드 중 하나인 프레도니졸론은 부작용 때문에 WMS 치료에 적합하지 않습니다. 글루코코르티코이드(glucocorticoid)인 부데소니드(budesonide)가 WMS치료제로 보고되었지만9, 이 치료법은 급성 WMS를 가진 동물에서는 상대적으로 효과가 없었다. 트라넥삼산은 항염증 효과가 있는 플라스민 억제제로, 기존 방법에서는 눈에 띄는 부작용이 나타나지 않았습니다. 그러나 원래의 치료 프로토콜은 확실히 효과적이었지만 동물과 보호자에게 큰 부담을 안겨주었습니다.
본 연구에서는 WMS에 대한 수정된 치료 방법을 수행하여 동물의 생리적 부하와 보호자의 작업량을 모두 줄였습니다. 수정된 방법에서, 트라넥삼산의 투여 경로가 변경되어(복강내에서 피하로) 복부 장기의 손상 위험을 줄이는 데 기여하였다. 트라넥삼산 용액은 오염 위험 및 준비 시간을 줄이기 위해 이 프로토콜에서 희석되지 않았습니다. 원래의 방법에서는 아미노산 제형 3.0mL를 정맥 주사하였다. 그러나, 볼루스10으로 투여하는 것이 권장되는 5.0 mL/kg이 권장되기 때문에 부피가 다소 컸다. 따라서, 수정된 방법에서 부피가 감소되었습니다.
이 프로토콜에 사용된 비타민 제제에는 비타민 B와 C가 포함되어 있습니다. 원래 방법에서 비타민 제제 0.5mL에는 2.5mg의 염화 티아민이 함유되어 있으며, 이는 비인간 영장류의 실험실 수용 후 요구량의 2.5배였습니다11. 본 방법에서는 염화티아민 염산염 1.0mg을 함유하는 비타민 제제 0.1mL를 투여하였다. 철 제형 및 트라넥삼산 용액의 투여 빈도는 수정된 방법에서 감소되었으며, 이는 동물과 보호자의 부담 감소에 기여했습니다.
대표 결과 섹션에 쓰여진 바와 같이, 수정된 방법에서 유의한 치료 효과가 있었습니다. 평균 치료기간은 37.8± 25.34일로 기존 방법(56일)보다 짧았다. 마모셋은 정신적 스트레스에 민감하기 때문에 장기간 치료하면 식욕 감소와 같은 역효과를 낳습니다. 따라서 보호자는 각 매개변수의 값뿐만 아니라 동물의 행동에 따라 치료 종료 시기를 종합적으로 결정해야 합니다.
공개
저자는 공개할 이해 상충이 없습니다.
감사의 말
이 연구는 일본 의학연구개발기구(AMED)의 Brain Mapping by Integrated Neurotechnologies for Disease Studies(Brain/MINDS) 프로젝트(보조금 번호 JP23dm0207001)의 일환으로 부분적으로 지원되었습니다.
자료
| Name | Company | Catalog Number | Comments |
| 1.0 mL Syringe | Terumo Corporation, Tokyo, Japan | SS-01T | For subcutaneously injection of Tranexamic acid |
| 10 mL Syringe | Terumo Corporation, Tokyo, Japan | SS-10SZ | For Intravenous Administration of Amino acid formulation |
| 26 G Needle | Terumo Corporation, Tokyo, Japan | NN-2613S | For subcutaneously injection |
| 27 G Butterfly Needle Type D | Terumo Corporation, Tokyo, Japan | SV-27DL | For Intravenous Administration of Amino acid formulation |
| 5 mL Syringe | Terumo Corporation, Tokyo, Japan | SS-05SZ | For subcutaneously injection of Ringer's lactate and Vitamin formulation |
| Aminoleban Injection | Otsuka Pharma Factory Inc., Tokyo, Japan | 1942 | For subcutaneously injection of Ringer's lactate and Vitamin formulation |
| C-PARA | Takata Pharma Co., Ltd., Saitama, Japan | 120-31960-0 | Vitamin formulation |
| FCV Liquid | Minerva Corporation, Saitama, Japan | Iron formulation | |
| Lactec Injection | Otsuka Pharma Factory Inc., Tokyo, Japan | 0714 | Ringer’s lactate |
| Vasolamin Injection | Meiji Seika Pharma Co., Ltd., Tokyo, Japan | DBASOS | Tranexamic acid |
참고문헌
- Baxter, V. K., et al. Serum albumin and body weight as biomarkers for the antemortem identification of bone and gastrointestinal disease in the common marmoset. PLoS ONE. 8 (12), e82747(2013).
- Brack, M., Rothe, H. Chronic tubulointerstitial nephritis and wasting disease in marmosets (Callithrix jacchus). Vet Pathol. 18, Suppl 6 45-54 (1981).
- Chalifoux, L. V., Bronson, R. T., Escajadillo, A., McKenna, S. An analysis of the association of gastroenteric lesions with chronic wasting syndrome of marmosets. Vet Pathol Suppl. 7, 141-162 (1982).
- Logan, A. C., Khan, K. N. Clinical pathologic changes in two marmosets with wasting syndrome. Toxicol Pathol. 24 (6), 707-709 (1996).
- Ludlage, E., Mansfield, K. Clinical care and diseases of the common marmoset (Callithrix jacchus). Comp Med. 53 (4), 369-382 (2003).
- Ross, C. N., Davis, K., Dobek, G., Tardif, S. D. Aging phenotypes of common marmosets (Callithrix jacchus). J Aging Res. 2012, 567143(2012).
- Yoshimoto, T., Niimi, K., Takahashi, E. Curative effects of tranexamic acid with supportive measures on wasting marmoset syndrome. Comp Med. 66 (6), 1-6 (2016).
- Niimi, K., et al. Measurement of the α1-proteinase inhibitor (α1-antitrypsin) of common marmoset and intestinal protein loss in wasting syndrome. Biosci Rep. 39 (7), 20190562(2019).
- Otovic, P., Smith, S., Hutchinson, E. The use of glucocorticoids in marmoset wasting syndrome. J Med Primatol. 44 (2), 53-59 (2015).
- Turner, P. V., Brabb, T., Pekow, C., Vasbinder, M. A. Administration of substances to laboratory animals: routes of administration and factors to consider. J Am Assoc Lab Anim Sci. 50 (5), 600-613 (2011).
- Lewis, S. M., Hotchkiss, C. E., Ullrey, D. E. Chapter 13. Nutrition and nutritional diseases. The Laboratory Primates. Wolfe-Coote, S. , 181-208 (2005).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유