Method Article
초음파 유도파를 사용한 피질 뼈 평가: 건강한 인구 집단의 재현성 연구
요약
여기에서는 양방향 축방향 투과(BDAT) 초음파 장치의 측정 프로토콜을 자세히 제시하고 14명의 건강한 참가자와 3명의 작업자를 고려하여 재현성 연구에서 테스트합니다. ICC(IntraClass Correlation Coefficients)로 측정한 신뢰도는 4개의 관심 매개변수에 대해 양호하거나 우수했습니다.
초록
취약성 골절은 인구 고령화의 맥락에서 여전히 전 세계적인 건강 부담입니다. 특히 전 세계 고관절 골절 건수는 2020년에서 2050년 사이에 두 배로 증가할 것으로 예상됩니다. 따라서 인구 규모에서 fragility fracture의 위험이 있는 환자를 감지하는 것이 필수적입니다. 현재 황금 표준은 면적 골밀도(aBMD)를 제공하는 이중 X선 흡수 측정법(DXA)입니다. 일반적으로 X-ray 장치보다 휴대가 간편하고 저렴한 초음파 장치는 스크리닝 도구로서 흥미로운 DXA 대안을 나타냅니다. 그러나 연산자 종속성은 일반적으로 주요 단점으로 인식됩니다. 본 연구에서는 양방향 축방향 전송(BDAT) 초음파 소자의 측정 프로토콜에 대해 자세히 설명한다. 전용 초음파 프로브는 기존의 커플 링 젤을 사용하여 비주로 사용되는 팔뚝의 원위 반경의 1/3 지점에 배치됩니다. 안내 인터페이스는 준 실시간(약 2Hz)으로 첫 번째 도착 신호의 속도(vFAS) 및 A0 모드(vA0), 피질 두께(Ct.Th) 및 다공성(Ct.Po)의 4가지 관심 매개변수와 4개의 품질 매개변수를 제공합니다. 작업자는 측정 지점에서 프로브를 천천히 움직이면서 안정적인 위치를 찾고 일련의 10가지 수집을 시작할 때까지 인터페이스에서 제공하는 피드백을 주의 깊게 관찰합니다. 최소 4개의 일관된 시리즈가 얻어지면 측정이 종료되고 자동 보고서가 생성됩니다. 측정을 완료하는 데 일반적으로 약 5분이 걸립니다. 이 프로토콜의 견고성을 결정하기 위해 3명의 작업자(전문가 1명, 초보자 2명)와 14명의 건강한 참가자(여성 6명, 남성 8명, 21-53세)를 대상으로 재현성 연구를 수행했습니다. 부류 내 상관 계수(ICC)는 vA0(0.76), Ct.Po(0.80)에 대해 양호하거나 Ct.Th(0.87) 및 vFAS(0.91)에 대해 우수한 것으로 나타났습니다. 표준 편차는 임상 실습에서 전체 범위의 10% 미만인 것으로 밝혀졌습니다.
서문
골다공증 및 관련 취약성 골절은 여전히 주요 공중 보건 문제를 구성한다1. 특히 전 세계적으로 고관절 골절 건수는 2050년까지 두 배로 증가할 것으로 예상됩니다2. 뼈 취약성은 취약성 골절 사건 전에 큰 경고 징후 없이 느리고 조용한 탈염 및 뼈 손실 과정으로 인해 발생합니다. 취약성 골절의 위험이 있는 환자를 감지하기 위한 현재 황금 표준은 이중 X선 흡수 측정법(DXA)으로, 보정된 회색 픽셀3으로 2D 저해상도 X선 이미지를 제공합니다. 이 이미지에서는 주요 취약성 골절 부위(척추, 손목 및 엉덩이)와 관련된 다양한 관심 영역에서 영역 골 미네랄 밀도(aBMD in g.cm-2)를 추출할 수 있습니다. aBMD 값은 취약성 파괴율이 증가함에 따라 감소합니다3. 또한, 정상적인 건강한 인구 집단에 대한 T-점수 정규화를 통해 다른 제조업체에서 제안한 장치와 측정된 환자를 비교할 수 있습니다. DXA T-점수는 세계보건기구(WHO)에서 골다공증 진단을 정상(T-점수 < -1), 골감소성(-1 < T-점수 < -2.5), 골다공증성(T-점수 < -2.5)의 3단계로 정의하기 위해 제안했습니다4.
DXA는 몇 가지 한계를 가지고 있습니다 : 크기, 상대적으로 높은 비용, 전용 방의 필요성, 파괴와 비 균열을 구별하는 능력, 라틴 아메리카와 같은 많은 국가에서의 가용성은 모두 중간5입니다. 따라서 취약성 파괴 위험 추정을 위한 스크리닝 도구로서 DXA 대안이 필요합니다6. 그러나 정량적 컴퓨터 단층 촬영 및 그파생물7, 자기 공명 영상(MRI)8과 같은 일부 DXA 대안도 부피가 커서 널리 사용할 수 없습니다. 정량적 초음파(QUS)는 휴대가 간편하고 견고하며 사용하기 쉬운 스크리닝 장치의 잠재력을 제시합니다. 피질골 평가를 위해 수 kHz에서 수 MHz에 이르는 다양한 주파수와 관련된 다양한 장치가 개발되었으며, 트랜스듀서가 반경 및 경골과 같은 긴 뼈의 축과 정렬되는 축 방향 전송, 역확산9, 펄스 에코10 및 축 전송에서 다양한 트랜스듀서 위치와 관련이 있습니다. 일부 장치는 aBMD 대리모11를 제공하는 반면, 다른 장치는 속도12 또는 감쇠 계수9 와 같은 "전통적인" 초음파 매개변수와 피질 두께, 다공성 또는 기공 크기 분포9와 같은 기하학적 및 재료 매개변수를 제공합니다. 그러나 오늘날까지 QUS는 뼈 평가를 위한 임상 실습에서 널리 사용되는 데 성공하지 못했는데, 부분적으로는 장치 간의 균질화가 부족하고 작업자 의존성13에 기인합니다.
DXA 대안으로 제안된 QUS 기술 중 축 방향 전달(AT)은 (i) 쉽게 접근할 수 있고 (ii) 주요 취약성 골절 부위 중 하나, 즉 손목에 가까운 팔뚝에서 측정을 수행할 수 있다는 장점이 있습니다. 첫 번째로 제안된 AT 매개변수는 신호 처리 및 장치에 따라 음속(SOS) 또는 첫 도착 신호(vFAS)의 속도로 표시된 피질층의 초음파 전파 속도에 따라 달라지며, 일부는 상용12,14 및 기타 실험실 프로토타입15,16입니다 . 이 매개변수는 1990년대 후반 이후 여러 임상 연구에서 골밀도(BMD)와 유사한 성능으로 골절이 있거나 없는 환자 그룹을 구별할 수 있었다14,15. 또한 다기관 종단 연구에도 성공적으로 적용되어 임상적 적용과 견고성을 입증했습니다12. 프로브와 뼈 표면 사이의 각도로 인한 바이어스를 줄이기 위해 두 개의 반대 전파 방향을 결합하여 vFAS 정밀도가 향상되었습니다16,17. 이 관점은 양방향 AT(BDAT)로 표시되었습니다.
vFAS가 임상적 관심을 보였다고 하더라도, BMD와 유사한 주요 단점은 기하학적 및 물질적 특성과 같은 다양한 주요 피질 뼈 특징을 결합하기 때문에 임상적 해석이 간단하지 않다는 것입니다. 그렇기 때문에 도파관 특성에 대한 유도파의 미세한 감도로 인한 잠재력을 고려하여 유도파 관점을 제안했습니다. 이 접근 방식은 신호 처리, 도파관 모델링 및 역 문제를 결합해야 하며 예를 들어 플레이트 또는 튜브와 같은 금속 도파관을 고려하는 비파괴 검사에 주로 사용됩니다(18). 따라서, 2세대 BDAT 장치는 2010년부터 뼈를 모방하는 팬텀(phantoms)19 부터 생체 외 검증(ex vivo validation)20 및 생체 내 측정( in vivo measurement)21에 이르기까지 단계적으로 개발되어 왔다. 이 장치는 프랑스22 개국, 독일23 개국, 영국24 개국 및 칠레25 개국의 임상 연구에서 성공적으로 테스트되었으며 성공률 및 환자 판별 측면에서 개선 된 결과를 보여주었습니다.
본 연구는 현재 BDAT 초음파 소자의 재현성을 조사하는 것을 목표로 한다. 먼저 장치와 측정 프로토콜이 자세히 설명됩니다. 14명의 참가자와 3명의 작업자로 얻은 결과는 취약성 골절 위험이 있는 환자를 감지하기 위한 집단 선별 검사 측면에서 발표되고 논의됩니다.
측정 원리: 신호 처리, 관심 파라미터 및 품질 파라미터
양방향 축 방향 변속기(BDAT) 장치는 다양한 부품으로 구성되며 주요는 초음파 프로브, 전자 모듈 및 컴퓨터입니다. 전체 목록은 재료 표에 자세히 설명되어 있으며 그림 1에 나와 있습니다. 다음에서는 관심 있는 매개변수, 측정 품질 매개변수 및 측정 프로토콜에 대해 설명합니다.
vFAS
샘플링된 신호가 컴퓨터에 수신되면 여러 단계에 따라 처리됩니다. 첫 번째 단계는 시간 영역에서의 신호 처리로 구성되며, 앞서 설명한 프로토콜을 사용하여 FAS를 검출합니다16, 17. 각 수신기에 대한 도착 시간을 구하면 나중에 vFAS로 표시되는 FAS 속도를 결정할 수 있으며, 이는 전파 양방향에서 얻은 속도의 조화 평균입니다. 전파 양방향의 정보를 결합하면 프로브와 뼈 표면 방향 사이의 각도를 구하고 편향되지 않은 vFAS 값16을 도출할 수 있습니다. 이 양방향 각도는 나중에 알파로 표시되며 측정 품질의 매개변수로 사용됩니다. 이 시간적 처리는 또한 뼈 표면과 프로브 사이의 연조직 두께를 추정할 수 있게 하며, 이는ST.Th 26으로 표시됩니다.
유도파 스펙트럼 이미지
두 번째 단계는 f와 k로 표시되는 시간 및 공간 주파수를 고려하여 푸리에 영역에서의 신호 처리로 구성됩니다. 이 접근 방식은 SVD 기반 방법으로, 생체 내 팔뚝에 대한 그림 2와 같이 시공간 신호를 규범 함수(GWSI(유도파 스펙트럼 이미지)로 변환할 수 있습니다(19). 이 방법은 두 개의 푸리에 변환(시간 및 공간)과 SVD(Singular Value Decomposition)를 결합하여 피질 뼈 층에 의해 안내되는 모드의 수신된 신호(0-1 스케일)의 존재 속도를 시각화할 수 있습니다. GWSI는 시공간 푸리에 변환(Fourier Transform)의 향상으로 해석될 수 있으며, 각 픽셀은 주파수 f 및 파수 k의 독립 평면과 연관됩니다. 재료 감쇠27 및 선형 두께 변화28의 영향을 고려하기 위해 접근 방식이 개선되었습니다.
A0 모드와 관련된 스펙트럼의 상단 부분과 가장 높은 위상 속도 값, 즉 4mm·μs-1보다 큰 것과 관련된 가장 낮은 부분에 특히 주의를 기울일 것입니다. 이 부분은 관심 영역3 (ROI 3)29에 해당합니다. 나중에 lowk로 표시되는 ROI 3의 평균값도 품질 매개변수로 사용됩니다. 큰 값은 일반 도파관에 해당하며, 뼈 계면에서 선명한 파동 반사를 허용합니다. 값이 감소하면 불규칙한 도파관 또는 잘못 배치된 프로브 때문일 수 있습니다.
도파관 모델
유도파 분산 또는 주파수에 대한 각 유도 모드의 위상 속도 변화는 도파관의 재료 및 기하학적 특성에 따라 달라집니다. 따라서 전용 신호 처리, 도파관 모델링 및 역 문제 체계를 사용하여 이러한 속성을 검색할 수 있습니다. BDAT의 경우 도파관 모델은 도파관 재료와 하나의 기하학적 매개변수인 두께30에 따라 2D 횡방향 등방성 무료 플레이트에 해당합니다. 피질(cortical) 뼈 물질은 뼈 매트릭스(bone matrix)와 가변 다공성(variable porosity)31에 대한 고정된 매개변수를 고려하여 균질화된다. 따라서 역 문제는 피질 두께(Ct.Th)와 피질 다공성(Ct.Po)으로 표시된 두 매개변수에 따라 달라집니다. 재료 흡수, 도파관 곡률 및 주변 연조직의 영향은 측정에 영향을 미치더라도 모델에서 고려되지 않습니다. 그러나, 역문제 결과에 대한 가중치는 결정적인 것으로 밝혀지지 않았는데, 이는 두 개의 주요 관심 영역(A0 및 가장 낮은 부분)의 모드가 곡률과 연조직(32)에 의해 크게 변경되지 않음을 의미합니다.
역 문제
처음에 역 문제는 두 단계로 나뉘었습니다: 첫째, 실험적 유도파 분산을 추출하고, 둘째, 도파관 모델과 비교합니다. 이러한 관점은 잡음 및 모드 라벨링30,32에 의해 제한되었다. 따라서 이러한 한계를 극복하기 위한 전용 접근 방식이 Norm 기능 관점의 확장으로 제안되었습니다. 각 평면파를 독립적으로 고려하는 대신, 도파관 모델에 의해 제공되는 가능한 유도파만 고려됩니다20. 이는 모델 매개변수 영역, 즉 Ct.th - Ct.Po 평면(그림 2 오른쪽 하단)으로 표현되는 역 문제 이미지로 이어집니다. 가장 적합한 모델에는 최대 위치가 주어지고, 최종 2차 피크(회색 점이 있는 역 문제 이미지로 표시)는 밝은 회색 선이 있는 실험 모드와의 f-k 비교에서 표시된 모호한 솔루션에 해당합니다. 이전과 같이, 픽셀 값은 구성에 의해 정규화되며, 이 경우, 수신된 신호에 하나의 특정 도파관 모델의 존재를 반영한다. 최대값(max로 표시)과 두 번째 최대값과의 차이(diff로 표시)도 품질 매개변수로 사용됩니다.
역 문제는 원래 오프라인 계산, 즉 신호가 획득된 후 모델 파수의 정확한 값을 사용하여 제안되었습니다. 이 접근법은 ex vivo 20,33 및 in vivo21,34,35 연구를 고려하여 요골 및 경골 부위 모두에 대해 검증되었습니다. 이러한 계산을 HMI(Human-Machine Interface)에 포함시키기 위해, 희소 행렬 관점(36)을 사용하여 실시간 어플리케이션과 호환되는 근사화된 버전이 제안되었습니다.
vA0
GWSI에서 프리 플레이트 또는 Lamb 모델33,35의 첫 번째 비대칭 모드 A0과 관련된 가장 느린 가이드 모드의 속도를 추출할 수도 있습니다. 유도파 스펙트럼의 상부는 선형으로 근사화할 수 있으며, 기울기는 속도 vA0의 값을 제공합니다(그림 2 왼쪽 하단).
매개 변수 요약:
마지막으로, 4개의 관심 매개변수가 측정됩니다: (i) vFAS: 첫 번째 도착 신호의 속도(m·s-1); (ii) vA0: 가장 느린 유도 모드(m·s-1)의 속도; (iii) Ct.Th: 피질 두께(mm); 및 (iv) Ct.Po: 피질 다공성(%).
4가지 품질 매개변수가 고려됩니다: (i) 알파: 양방향 각도(°); (ii) lowk: GWSI의 가장 낮은 부분의 평균값(0과 1 사이의 정규화된 값); (iii) 최대: 역 문제 함수의 최대값(0과 1 사이의 정규화된 값); (iv) diff: 역 문제 함수의 첫 번째와 두 번째 최대값 간의 차이(0에서 100 사이의 정규화된 값).
이러한 모든 매개변수와 두 개의 유도파 스펙트럼 이미지(하나의 파 전파 방향) 및 역 문제 이미지는 HMI에 의해 약 2Hz의 프레임 속도로 "실시간"으로 표시됩니다. 일반적인 예가 그림 3에 나와 있습니다. 다음 섹션에서는 이러한 매개 변수를 사용하는 방법에 대해 자세히 설명합니다. 주요 아이디어는 작업자가 측정 현장에서 프로브를 천천히 움직이면서 안정적인 위치를 찾고 일련의 10가지 수집을 시작할 때까지 인터페이스의 다른 부분에서 제공하는 피드백을 주의 깊게 관찰하는 것입니다. 최소 4개의 일관된 시리즈가 얻어지면 측정이 종료되고 자동 보고서가 생성됩니다.
프로토콜
이 연구는 칠레 발파라이소 대학교(Universidad de Valparaiso)의 윤리 위원회(Ethical Committee)에서 프로토콜 번호 CEC213-20에 따라 승인되었습니다. 참가자들에게 서면 동의서가 제공되었습니다. 참가자의 포함/제외를 확인하기 위해 전화 인터뷰가 수행되었습니다. 이 연구는 다음 참고 문헌으로 등록되었습니다: NCT05424536.
1. 장치 설정
- 장치의 주요 부품을 큰 테이블 위에 놓습니다.
- 큰 테이블 위에 전기 절연 변압기, 전자 모듈 및 랩톱 컴퓨터를 나란히 놓습니다. 나중에 참가자의 팔뚝을 쉽게 배치할 수 있도록 이러한 부분 앞에 충분한 공간이 있는지 확인하십시오.
- 결국, 공간이 제한된 경우 랩톱 컴퓨터를 전자 모듈에 직접 놓고 명확하게 표시된 모듈의 환기 창을 막지 않도록 주의하십시오.
- 전기 절연 변압기를 연결합니다.
- 전용 케이블을 사용하여 전기 절연 변압기를 방의 가정용 전원에 꽂습니다.
- 전자 모듈을 연결합니다.
- 전용 전원 케이블을 사용하여 전자 모듈을 전기 절연 변압기에 연결합니다.
- 변압기의 ON-OFF 버튼을 눌러 모듈에 전원을 공급합니다.
- 노트북 컴퓨터를 연결합니다.
- 전용 USB(Universal Serial Bus) 케이블을 사용하여 랩톱 컴퓨터를 모듈에 연결하여 디지털화된 수신 신호를 추가 처리를 위해 컴퓨터로 보냅니다.
- 노트북에 전원을 공급해야 하는 경우 전원 케이블을 전자 절연 변압기에 연결합니다.
- 초음파 프로브를 연결합니다.
- 모듈 전면에 있는 전용 케이블 슬롯을 사용하여 초음파 프로브를 모듈에 연결합니다. 팔뚝과 다리 측정 부위를 위한 두 가지 프로브가 있습니다. 이 연구에서는 반경(팔뚝 프로브)만 고려합니다.
- 페달 스위치를 연결합니다.
- 페달 스위치를 발에 가까운 바닥에 놓고 참가자를 측정하는 동안 작업자의 위치를 고려하십시오. USB 케이블을 사용하여 페달 스위치를 컴퓨터에 연결합니다. 페달을 사용하여 획득 시리즈를 시작합니다.
2. 참가자 설치
- 참가자를 배치합니다.
- 참가자를 이전에 설치된 장치 앞의 테이블에 벌거벗은 팔뚝을 올려놓고 운영자 앞에 앉도록 초대합니다( 그림 3 참조).
참고: 반대쪽 쪽을 측정합니다(즉, 오른손잡이 참가자의 경우 왼쪽).
- 참가자를 이전에 설치된 장치 앞의 테이블에 벌거벗은 팔뚝을 올려놓고 운영자 앞에 앉도록 초대합니다( 그림 3 참조).
- 측정 부위(원위 반경의 1/3)를 표시합니다.
- 눈금자를 사용하여 방사형 스타일로이드(손목에 가까운 뼈 끝)에서 팔꿈치까지 반경 길이를 측정합니다.
- 이 길이를 3으로 나눕니다.
- 측정 부위, 즉 원위 반경의 1/3을 펜을 사용하여 손목에서 1/3 길이의 길이를 측정합니다.
- HMI 소프트웨어를 시작합니다.
- 노트북 바탕 화면에서 해당 아이콘을 클릭하여 HMI 소프트웨어를 시작합니다.
- 참가자의 데이터를 추가합니다.
- 소프트웨어 시작 시 자동으로 열리는 팝업 창을 사용하여 참가자의 데이터(익명 ID, 편퇴성, 측정 사이트, 운영자 ID, 성별 등)를 추가합니다.
- 에코그래픽 젤을 추가합니다.
- 초음파 전파를 보장하기 위해 프로브 앞면과 참가자의 팔뚝에 표시된 측정 부위에 에코그래픽 젤을 추가합니다.
- 프로브를 팔뚝에 접촉시킵니다.
- 프로브를 팔뚝에 접촉시키고 프로브 중심을 이전에 2.2단계에서 수행한 표시에 놓습니다.
3. 안정된 자세를 찾고 있다
참고: HMI는 두 가지 속도, vFAS 및 vA0, 두 가지 역 문제 값, 즉 피질 두께(Ct.Th) 및 피질 다공성(Ct.Po)의 네 가지 관심 매개변수를 표시합니다. HMI는 또한 alpha, lowk, max 및 diff로 표시되는 4개의 품질 파라미터를 표시합니다. 이러한 매개 변수는 소개에 자세히 설명되어 있습니다.
- 실시간 시각화를 시작합니다.
- 소프트웨어 인터페이스의 오른쪽 하단에 있는 시작 버튼을 클릭하여 실시간 시각화를 시작합니다. 두 개의 연속된 값 표시 사이의 지속 시간은 약 0.5초입니다.
- 안정적인 vFAS 값을 찾습니다.
- 인터페이스의 특정 경우에 표시되는 vFAS 매개변수 값을 관찰하면서 프로브 위치를 천천히 조정합니다. 정상 값의 범위는 약 3800 m∙s-1 에서 약 4200 m∙s-1 사이입니다.
- 안정적인 위치가 발견되면 두 개의 연속 계산 사이에서 vFAS 변동이 약 40m∙s-1 미만인지 확인합니다.
- 양방향 각도를 조정합니다.
- 인터페이스의 특정 경우에 표시되는 양방향 값(품질 매개변수 알파)을 관찰하면서 프로브 위치를 천천히 조정합니다.
- 각도 절대값이 2° 미만이 될 때까지 한쪽 프로브 측면에 부드럽게 압력을 가하여 프로브 위치를 조정하여 프로브와 뼈 표면 사이의 평행도를 개선합니다.
- 안정적인 vA0 값을 찾습니다.
- 인터페이스의 특정 경우에 표시되는 vA0 매개변수 값을 관찰하면서 프로브 위치를 천천히 조정합니다. 정상 값의 범위는 약 1500 m∙s-1 에서 약 1900 m∙s-1 사이입니다.
- 안정적인 위치가 발견되면 두 개의 연속 계산 사이에서 vA0 변동이 약 40m∙s-1 미만인지 확인합니다.
- 문제가 있는 경우 인터페이스의 오른쪽 열에 표시된 유도파 이미지 스펙트럼을 관찰하십시오. 스펙트럼의 상부가 기울기가 vA0 값을 제공하는 연속선으로 나타나는지 확인합니다.
- 역 문제 이미지를 관찰합니다.
- 두 속도(vFAS 및 vA0)와 각도 값이 안정화되면 자동으로 나타나는 역 문제 이미지를 관찰합니다.
- 이미지에 명확한 픽셀로 표시된 최대값이 하나 이상 표시되고, 최종적으로 다른 색상으로 표시된 하나 또는 여러 개의 보조 최대값이 표시되어야 합니다. 3개의 누락된 품질 매개변수(max. diff, lowk)는 실시간으로 자동 계산됩니다.
- 역 문제 이미지를 개선합니다.
- 역 문제 이미지 최대값을 관찰하면서 프로브 위치를 천천히 조정합니다.
- 인터페이스의 해당 사례(max 및 diff 값)를 살펴보면서 가능한 가장 높은 첫 번째 최대값과 가장 낮은 보조 최대값을 찾습니다.
- 문제가 있는 경우 인터페이스의 오른쪽 열에 표시된 유도파 스펙트럼 이미지를 관찰하십시오. 스펙트럼의 아래쪽 부분이 가능한 한 긴 몇 개의 연속적인 선으로 나타나도록 하고, 높은 위상 속도 모드 및 매개변수 품질 lowk와 관련된 가능한 한 높은 값으로 나타나도록 합니다.
- 안정적인 위치를 찾으십시오.
- 허용 가능한 역 문제 이미지가 발견되면 프로브 위치를 안정화합니다. 두 개의 연속적인 계산 사이에 역 문제 이미지의 큰 변화가 나타나지 않는지 확인합니다.
4. 데이터 수집
- 10개의 인수 시리즈를 시작합니다.
- 안정적인 위치를 찾으면 발로 페달 스위치를 눌러 일련의 10가지 획득을 시작합니다.
- 약 5초 동안 지속되는 10번의 획득 동안 가능한 한 안정적으로 유지하십시오.
- 시리즈의 품질을 제어합니다.
- 관심 있는 매개변수의 평균과 표준 편차를 살펴보면 자동으로 계산되어 계열이 끝나면 나타나는 팝업 창에 표시됩니다.
- 표준 편차가 고정 임계값보다 낮으면 계열을 고려합니다. 반대로, 시리즈를 거부하십시오.
- 두 번째 팝업 창에서 운영자가 동일한 참가자의 획득 시리즈를 중지할지 아니면 계속할지 묻는 질문에 대한 답변입니다.
- 프로브의 위치를 변경합니다.
- 이전 단계(2.1단계부터 3.2단계까지)를 다시 시작하여 보다 안정적인 포지션을 찾고 더 많은 10개의 인수 시리즈를 획득합니다. 결국 필요한 경우 참가자가 두 번의 재배치 사이에 휴식을 취하도록 합니다.
- 이전과 마찬가지로 관심 매개변수의 평균과 표준 편차는 각 계열에 대해 자동으로 계산됩니다.
- 결과 팝업 창을 보고 마지막으로 획득한 시리즈가 유지되거나 거부되었는지 확인합니다. 참가자의 측정은 4개 이상의 일관된 시리즈가 등록되면 완료됩니다. 아웃사이더 시리즈는 자동으로 거부됩니다.
- 최종 값을 구합니다.
참고: 관심 매개변수의 최종 값은 일관된 계열로 얻은 평균의 평균을 고려하여 자동으로 얻어집니다. - 자동 보고서 pdf를 확인합니다.
- 최종 값이 보고서 pdf에 자동으로 보고되고 팝업 창에서 stop 옵션이 선택되면 즉시 생성되는지 확인합니다. 그림 4에 예제가 나와 있습니다.
참고: pdf는 원시 데이터와 동일한 폴더에 있으며 나중에 오프라인에서 다시 분석할 수 있습니다.
- 최종 값이 보고서 pdf에 자동으로 보고되고 팝업 창에서 stop 옵션이 선택되면 즉시 생성되는지 확인합니다. 그림 4에 예제가 나와 있습니다.
- 두 번째 정확한 보고서를 확인합니다.
- 첫 번째 자동 보고서의 경우와 같이 근사값 대신 역 문제 계산을 위한 정확한 도파관 모델 값을 사용하여 생성된 두 번째 정밀 보고서를 확인합니다. 두 번째 보고서 생성에는 5분도 채 걸리지 않습니다. 그림 5 와 그림 6에 예제가 표시되어 있습니다.
- 자동 보고서가 정확한 보고서와 일치하는지 확인합니다. 일관된 계열을 유지하기 위해 자동으로 제거되지 않은 계열을 제거합니다.
결과
3명의 작업자(전문가 1명, 초보자 2명)와 건강한 참가자 14명(여성 6명, 남성 8명, 21-53세)을 대상으로 재현성 연구를 수행했습니다. 초보 작업자는 수집 프로토콜을 이해하고 연습하기 위해 약 3시간 동안 교육을 받았습니다. 그런 다음 참가자들은 2023년 8월 2주 동안 측정되었습니다. 각 측정은 독립적으로 수행되었습니다. 모든 작업자는 눈이 멀었습니다, 즉 한 작업자가 다른 두 작업자가 얻은 결과를 알지 못했습니다.
작업자간 반복성
그림 5는 일관된 사례에 대한 작업자 내 반복성을 보여줍니다: 1명의 참가자와 1명의 작업자에 대해 획득된 10개의 수집으로 구성된 4개의 시리즈. 첫 번째 열은 역 문제 함수에 해당하고, 두 번째 열은 최적 적합 모형과 비교한 실험 유도 모드 분산을 보여줍니다. 각 그림 선은 성공적인 시리즈에 해당합니다. 보유 인수 횟수는 제목에 나와 있습니다 : 첫 번째 시리즈의 경우 10 개 중 7 개, 다음 시리즈의 경우 10 개 중 10 개입니다. 각 계열에 대해 평균 및 표준 편차와 4개의 매개변수(vFAS, vA0, Ct.Th 및 Ct.Po)가 제공됩니다. 또한 양방향 각도(알파), 역 문제 함수의 최대값(최대), 두 번째 최대값과의 절대 차이(diff) 및 GWSI의 가장 낮은 부분의 평균값(lowk)과 같은 품질 매개변수도 표시됩니다.
시리즈 내 표준 편차는 피질 두께의 경우 약 0.02mm, 피질 다공성의 경우 0.5% 미만, 두 속도의 경우 20m∙s-1 미만으로 낮으며, 이는 리치 프로브 위치가 안정적임을 나타냅니다. 그런 다음 각 계열에 대해 얻은 평균값, 특히 3.4mm에서 3.5mm 사이의 두께 값과 4040m∙s-1 에서 4070m∙s-1 범위의 vFAS 값에 대해 매우 가깝다는 것을 관찰할 수 있습니다. 40m∙s-1 의 차이는 4000m∙s-1의 평균값에 대해 1% 차이에 해당합니다. 대뇌피질 다공성(cortical porosity)은 8%에서 12%까지, vA0 속도(vA0 속도)는 1700 m∙s-1 에서 1740 m∙s-1 사이로 더 큰 변화가 관찰됩니다. 이 일관된 경우 거의 모든 획득이 일관되게, 즉 서로 가깝습니다. 관심 있는 4개의 매개변수의 최종 결과에는 모호성이 거의 없습니다.
두 번째 경우는 그림 6에 나와 있는데, 이는 덜 일반적인 경우이다. 이 경우 vFAS, vA0 및 Ct.Po의 세 매개변수는 각각 약 4120m∙s-1, 1700m∙s-1 및 10%의 값으로 매우 안정적입니다. 피질 두께의 경우는 2.6mm와 3.5mm의 두 모호한 해가 역 문제 함수의 두 첫 번째 최대값 사이의 작은 차이 값(diff 0.5% 미만)과 일치하는 것으로 관찰되기 때문에 더 어렵습니다. 이전의 일반적인 사례에서는 이 차이가 1%에서 3% 사이였습니다. 모호성은 전문가 분석에 의해 제거되며, 이 경우 실험적 유도 모드와 이론적 유도 모드(오른쪽 열) 간의 일치를 살펴봅니다. 가장 낮은 두께의 경우 스펙트럼의 가장 낮은 부분(첫 번째 시리즈 2개)에서 일치가 더 좋습니다. 마지막 두 시리즈의 경우 약 0.5MHz로 실험 지점이 거의 없는 이론적 모드가 있으며, 이는 이전 시리즈에 비해 더 낮은 일치를 나타냅니다. 또한 diff 매개 변수(0.1%)는 두 첫 번째 계열의 값(0.4% 및 0.2%)보다 작습니다. 이 경우 유지 솔루션(2.6mm)에 대한 선택은 아직 자동화되지 않았으며 여전히 전문가가 필요합니다. 그러나 세 명의 작업자는 유사한 문제에 직면하여 2.6mm에 가까운 유사한 솔루션을 선택했습니다.
작업자가 아닌 신뢰도
14명의 참가자와 함께 3명의 작업자가 얻은 4개의 관심 매개변수에 대한 모든 결과는 그림 7에 나와 있습니다. 클래스 내 상관 계수(ICC)는 공식과 이전에 발표된 Matlab 코드37,38,39에 따라 계산되었습니다. ICC는 특히 생체 의학 응용 분야에서 측정 스케일의 신뢰성을 평가하는 데 일반적으로 사용됩니다. 0.75에서 0.9 사이의 ICC 값은 일반적으로 우수한 신뢰성과 관련이 있는 반면 0.9 이상의 ICC 값은 우수한 신뢰성으로 간주됩니다. 매개 변수 vA0에 대해 ICC의 가장 낮은 값(0.76)을 얻었습니다. 표준 편차는 17m∙s-1과 같았으며, 이는 250m∙s-1 정도의 측정 범위의 약 7%입니다. ICC가 0.80이고 표준 편차가 1.1%로 범위의 약 10%인 Ct.Po에 대해서도 유사한 값이 관찰되었습니다. 다른 두 파라미터인 Ct.Th 와 Ct.Po에 대해 우수한 신뢰성(ICC 약 0.9)이 얻어졌으며 표준 편차는 범위의 10%보다 낮았습니다.

그림 1: BDAT(Bi-Directional Axial Transmission) 초음파 장치의 다양한 부분. 프로토타입에는 전자 절연체(1), 페달 스위치(2), 두 개의 프로브(3.1 및 3.2), 전자 모듈(4), 컴퓨터(5) 및 눈금자(6)가 포함됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
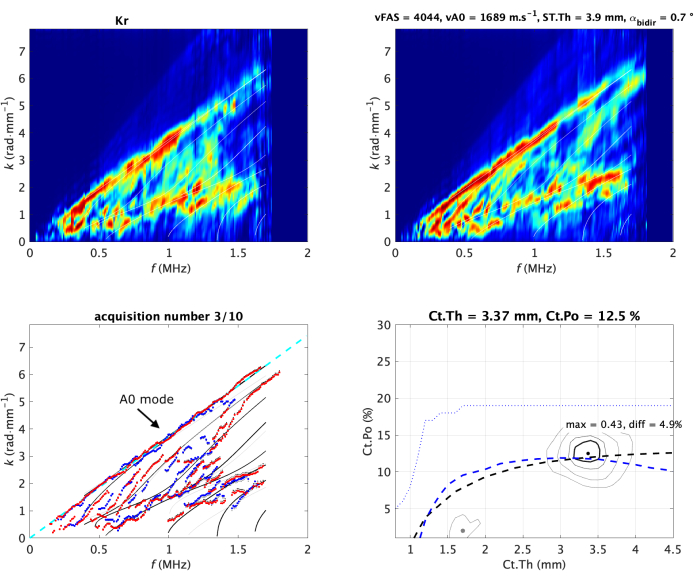
그림 2: in vivo 팔뚝의 일반적인 획득. 두 개의 Norm 함수(전파 방향당 하나씩)가 이미지의 위쪽 줄에 표시되어 있습니다. 또한 유도파 스펙트럼 이미지(GWSI)로 표시됩니다. 이러한 이미지의 최대값에서 가장 적합한 모델(왼쪽 하단 하위 이미지)과 비교하여 실험적 안내 모드(파란색 및 빨간색 점)를 추출할 수 있습니다. 최적 적합 모델은 피질 두께(Ct.Th)와 다공성(Ct.Po)의 두 값으로 매개변수화되며, 이는 역 문제 함수(오른쪽 아래 하위 이미지)의 최대 위치에 해당합니다. 해당 값은 각 패널의 제목에 표시됩니다. vA0 피팅은 파선으로 표시됩니다(왼쪽). 유도파 스펙트럼 이미지(Guided Wave Spectrum Images)와 역 문제 이미지(inverse problem image)는 구성19,20에 의해 정규화된다(즉, 픽셀 값 범위는 0에서 1까지). 측정된 두 가지 속도인 vFAS 및 vA0의 값은 오른쪽 상단 하위 이미지의 제목에 표시되어 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
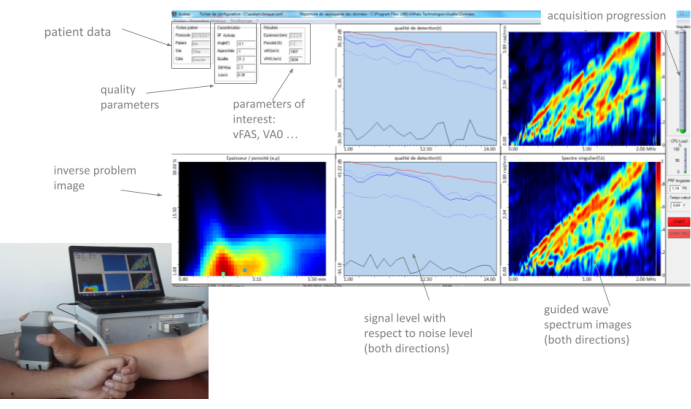
그림 3: 휴먼 머신 인터페이스(HMI). HMI는 두 개의 GWSI(전파 방향당 하나), 역 문제 이미지, 관심 매개변수 및 품질 매개변수를 실제로 보여줍니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
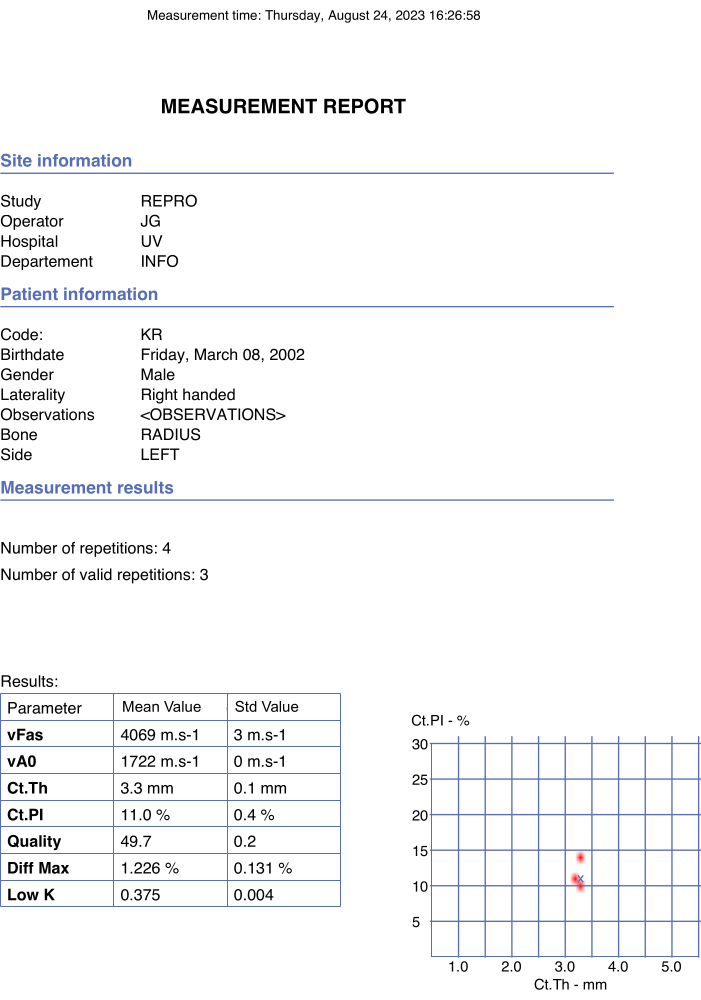
그림 4: 자동화된 보고서의 예. 이 보고서는 참가자와 작업자의 데이터뿐만 아니라 관심 매개변수 및 품질 매개변수의 최종 값을 표시했습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
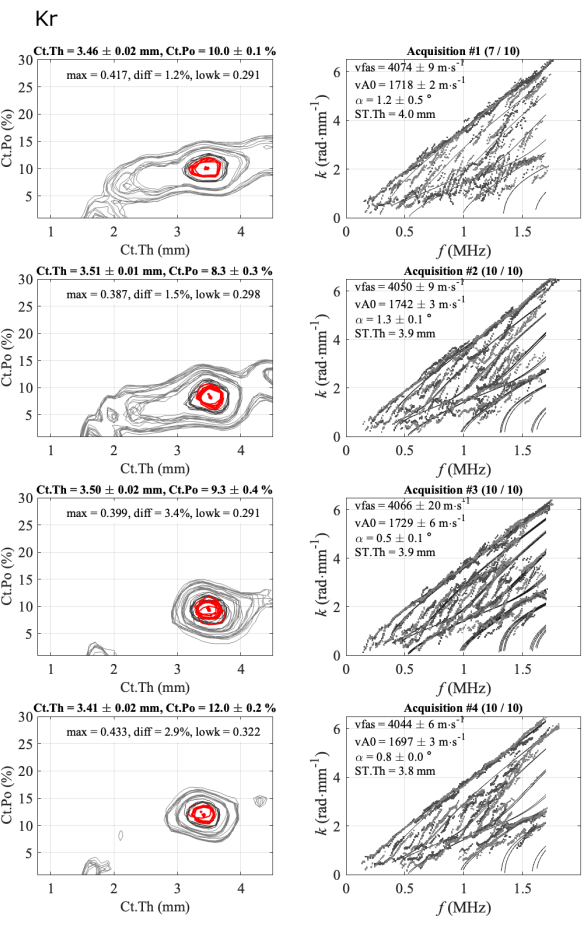
그림 5: 그림 4에 표시된 자동화된 보고서와 동일한 일관된 사례에 대한 두 번째 보고서의 예. 그림은 1명의 참가자와 1명의 작업자로 구성된 4개의 시리즈를 보여줍니다: 역 문제 이미지(왼쪽 열)와 가장 적합한 모델(오른쪽 열)과 비교한 실험 파수. 표시된 값은 10개의 획득 시리즈에 대해 유지된 획득의 평균 및 표준 편차에 해당합니다. 유지된 인수 수는 오른쪽 열의 제목에 표시됩니다(예: 첫 번째 계열의 경우 (7/10)). 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
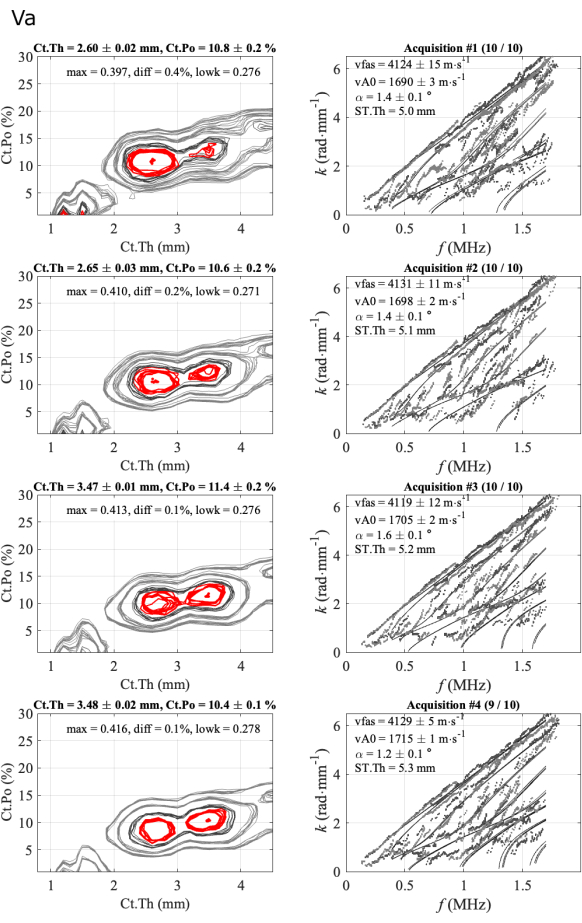
그림 6: 피질 두께에 대한 모호한 사례에 대한 두 번째 보고서의 예. 그림은 1명의 참가자와 1명의 작업자로 구성된 4개의 시리즈를 보여줍니다: 역 문제 이미지(왼쪽 열)와 가장 적합한 모델(오른쪽 열)과 비교한 실험 파수. 표시된 값은 10개의 획득 시리즈에 대해 유지된 획득에 대한 평균 및 표준 편차에 해당합니다. 보관된 취득 수는 오른쪽 열의 제목에 표시됩니다(예: 첫 번째 계열의 경우 (10/10)). 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
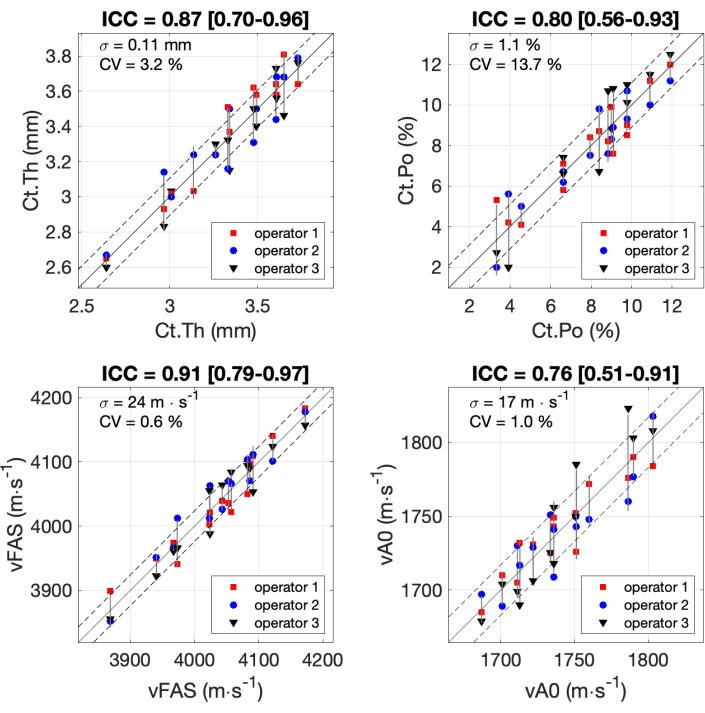
그림 7: 작업자간 신뢰성. 결과는 14명의 참가자와 함께 3명의 작업자가 얻은 4개의 관심 매개변수에 대한 결과를 보여줍니다. 3개의 연산자(y축)에서 얻은 값을 3개의 연산자(x축)의 평균값과 비교합니다. 클래스 내 상관 계수(ICC)는 제목에 표시되어 있습니다. 표준 편차 σ 및 변동 계수 CV도 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
토론
성공적인 측정을 위한 중요한 포인트는 뼈에 대한 올바른 프로브 위치 지정입니다. 뼈 표면에 대한 위치는 양방향 보정(bi-directional correction)16,17을 안내 인터페이스(guiding interface)와 통합함으로써 성공적으로 해결되었다. 이 수정이 없으면 vFAS 매개변수16에 대해 몇 가지 백분율 오류에 도달할 수 있는 것으로 나타났습니다. 전체 측정 범위(약 3800-4200 m∙s-1)가 평균값17의 약 10%, 약 4000 m∙s-1이기 때문에 이러한 보정은 환자를 정확하게 구별하는 데 중요한 것으로 밝혀졌습니다. 본 연구에서 발견된 재현성(24 m∙s-1의 표준 편차)은 이전 연구17와 유사했으며, 이는 20 m∙s-1의 표준 편차와 약 0.5%의 변동 계수(CV)를 나타낸다. 유사한 변동 계수 (0.5 %)가 더 낮은 주파수, 즉 0.3MHz40에서 발견되었습니다. vFAS 매개변수(ICC = 0.91)의 우수한 신뢰도는 고령 인구(ICC = 0.77)에서 다른 AT 장치로 최근에 얻은 것보다 높은 것으로 나타났습니다41. 이 사례의 모집단은 나이가 많았을 뿐만 아니라 모두 여성이었고 골다공성 증가의 다른 임상적 징후를 보인 일부 피험자도 있었다는 점에 유의해야 한다41.
두 번째 과제는 유도 모드, 특히 높은 위상 속도 또는 낮은 파수의 모드를 얻기 위해 뼈 축과 두 계면에 대해 프로브를 올바르게 배치하는 것입니다. 이러한 모드는 공진에 가깝고 여러 반사 경로와 연결됩니다. 정렬이 올바르지 않으면 파동이 프로브의 공간 측정 범위 밖으로 산란됩니다. 반대로, 프로브가 올바르게 배치되면 이러한 고위상 속도 모드가 ROI3에서 연속 분기로 나타납니다. 현재 HMI의 첫 번째 버전의 경우 실시간 GWSI20을 살펴봄으로써 이 정렬을 해결했습니다. 그러나, 이 접근법은 확실한 측정에 도달하기에는 불충분한 것으로 밝혀졌으며, 실패율은 파일럿 임상 연구20에서 약 20%로 밝혀졌습니다. 실시간 품질 매개변수를 포함하면 두 번째 임상 연구에서 실패율을 약 10%로 줄일 수 있습니다23. 그런 다음 "실시간" HMI에 역 문제 이미지를 포함하면 반경 측정에 대한 전류 고장률이 약 5%25로 더욱 개선될 수 있습니다. vFAS만 측정한 첫 번째 장치의 초기 고장은 약 15%17인 것으로 나타났습니다.
대뇌피질 두께에 대한 신뢰도는 이전 연구와 유사한 것으로 밝혀졌다22. 동일한 프로토타입의 이전 버전에서 ICC는 약 0.1mm의 표준 편차와 약 3%의 CV로 0.9에 가까운 것으로 나타났습니다. 그러나 대뇌피질 다공성에서 뚜렷한 개선이 관찰됩니다: ICC는 0.622 에서 0.8로 증가했고, 표준 편차는 1.5%에서 1%로 감소했습니다. 가장 어려운 매개변수는 vA0인데, 이는 그의 속도가 연조직 속도(약 1500m∙s-1)와 가깝기 때문입니다. 프로브가 올바르게 정렬되면 A0 모드가 고유하고 연속적으로 나타납니다. 반대로, 주변 연조직과의 결합으로 인해 불연속적이거나 다중적으로 보입니다. 이 효과는 연조직 두께가 작거나(4mm 미만) 크거나(10mm 이상) 연조직 두께(ST.Th 로 표시)가 큰 사람들에게 특히 강합니다.
이전에 노출된 바와 같이 핵심은 올바른 프로브 위치를 찾는 것입니다. 그러나 위치는 정확해야 할 뿐만 아니라 일련의 10개 획득에 대해 평균 및 표준 편차를 수행하기 위해 안정적이어야 합니다. 대부분의 경우 안정을 찾는 데 1분 미만이 소요되며 환자의 완전한 측정은 약 5분 동안 지속됩니다. 이 연구에서 설명한 표준 프로토콜이 대다수의 환자에게 적합하더라도 일부 사람들은 측정하기가 더 어렵습니다. 올바른 위치를 찾는 것은 어렵지만 가능하지만 안정적인 위치를 찾는 것은 거의 불가능합니다. 이 경우 작업자는 최대 200개의 획득까지 더 긴 시리즈를 기록하도록 선택할 수 있습니다. 최상의 인수는 나중에 품질 매개변수를 사용하여 오프라인으로 결정됩니다. 이 필터링은 나중에 실시간으로 적용되어야 합니다. 실제로, 작업자는 이상적인 상태 프로토콜의 10개 획득 중 4개의 시리즈보다 더 많은 시리즈 및/또는 획득을 기록합니다. 그러나 일반적인 측정 시간은 한 부위, 팔뚝 또는 다리에 대해 약 5분으로 유지됩니다. 몇 분 후에도 HMI가 올바른 위치를 감지하지 못하면 측정이 중지되고 실패로 간주됩니다. 현재 장치 및 프로토콜에서는 실패율이 5%25 미만인 것으로 확인되었습니다.
현재 장치는 다음과 같은 여러 제한 사항에 직면해 있습니다.
(나)크기 및 무게 : 현재 BDAT 장치는 휴대용입니다 : 표준 수하물에 맞고 무게는 약 25kg입니다. 그러나이 무게는 최신 초음파 장치에 비해 큽니다. 프로브와 신호 처리를 동일하게 유지하면서 새로운 전자 설계를 고려할 수 있습니다. 그러나 특히 거동이 불편한 침대나 집에 있는 환자의 경우 현재 장치를 이동할 수 있습니다.
(2)수집 속도: 현재 프레임 속도는 약 2-4Hz이며, 이는 실제 실시간 수집에 비해 측정 탐색이 느리다는 것을 의미합니다(즉, 25Hz 이상). 이것은 더 빠른 컴퓨터, 더 빠른 데이터 분석 및 전자 장치와 컴퓨터 간의 전송을 고려하여 미래에 개선될 수 있습니다. 수집 속도가 증가하면 측정의 사용자 친화성, 특히 올바른 프로브 위치 찾기가 향상됩니다.
(3)연조직 두께: 현재 접근 방식은 일반적으로 10mm보다 우수한 큰 연조직 층에 의해 제한됩니다. 이 경우, 첫 번째로 도착하는 신호는 피질뼈가 아닌 연조직 경로와 연결됩니다. 따라서, vFAS 및 관련 양방향 각도는 사용될 수 없다. 마찬가지로, vA0는 큰 연조직층을 측정하기가 매우 어렵습니다. 이 두 속도가 없으면 역 문제를 수행할 수 없습니다. 미래에는 예를 들어 이미징 기술을 사용하여 다른 양방향 보정 방법이 적용될 수 있습니다. 연조직층이 큰 환자는 일반적으로 비만 및 체질량 지수(BMI)가 30kg.m-2보다 큰 것과 관련이 있습니다.
(iv)도파관 규칙성: 역 문제 접근 방식은 여러 전파 경로가 있는 일반 도파관을 가정합니다. 골다공증 환자의 경우, 내부 피질 계면이 불규칙할 수 있으며, 따라서 특히 하부에서 유도파 스펙트럼 이미지가 좋지 않음을 의미합니다. 이러한 환자는 일반적으로 높은 용액 모호성과 관련이 있습니다. 연조직 또는 잘못된 포지셔닝이 불량한 스펙트럼 이미지의 원인으로 간주될 수 없고 lowk 매개변수 값이 낮으면 도파관이 불규칙한 것으로 간주되고 가장 낮은 두께의 솔루션이 고려됩니다. 물리적 모델링이 필요하지 않은 기계 학습에 기반한 접근 방식도 사용할 수 있습니다29.
서론에서 논의한 바와 같이, 취약성 골절 위험이 있는 환자를 감지하기 위한 현재 황금 표준은 DXA이며, 이는 큰 크기, 일부 지역에서는 낮은 가용성, 상대적으로 높은 비용 및 상대적으로 중간 정도의 효과와 같은 몇 가지 제한 사항에 직면해 있습니다. 첫 번째 한계는 매력적인 휴대성과 비용으로 알려진 초음파 장치로 완화할 수 있습니다. 그러나 위험에 처한 환자를 효과적으로 감지할 수 있는 능력은 최소한 DXA와 동등해야 합니다. 실제로, 황금 표준과 관련된 대부분의 참고 자료(의학적 결정, 치료, 비용, 병실 등)의 적응을 정당화하기 위해 DXA보다 높을 것으로 예상되는 경우가 있습니다. 이것이 일부 초음파 장치가 aBMD 대리10,11,42를 제안하는 이유입니다. 그러나 aBMD 및 vFAS와 같은 임상 매개변수의 한 가지 단점은 서로 다른 피질 뼈 특성의 통합입니다. 그렇기 때문에 BDAT를 포함한 다른 초음파 장치는 피질 다공성, 두께 또는 기공 크기 분포와 같이 의사와 환자가 더 쉽게 해석할 수 있는 매개변수를 제안하는 보완적인 관점을 제안합니다9. 이러한 매개변수는 기하학적 및 물질적 특성을 반영합니다: 피질 뼈는 잠재적으로 수량 또는 품질의 독립적인 변동 측면에서 평가될 수 있습니다. 이러한 관점은 뼈 취약성의 다양한 가능한 원인을 탐색하는 데 매우 도움이 될 수 있습니다. 예를 들어, 고관절 내 또는 수정체 외 고관절 골절, 즉 대퇴골 경부 골절 부위 또는 전자골절 부위는 의학적 기원이 다른 것으로 추정된다43. 마찬가지로, 피질뼈에 다양한 효과를 주는 것을 목표로 하는 다양한 약물 치료를 따르는 것도 가능할 수 있으며, 양이나 질의 측면에서도 가능하다3.
피질 두께(0.1mm)에 대해 BDAT로 얻은 정밀도는 일반적으로 0.25mm 이상의 다른 초음파 방법보다 우수합니다(44). 이 차이는 부분적으로 BDAT 역 문제가 결합된 기하학적 및 재료 변화를 고려한다는 사실에 기인합니다. 펄스 에코(pulse echo)와 같은 일부 다른 접근법은 모든 환자에 대한 고유한 뼈 물질의 특성을 고려한다10,44. 약 0.1mm(CV 약 3%)의 이 정밀도 값은 두께 범위가 2mm 미만이기 때문에 환자를 미세하게 구별하는 데 매우 중요합니다. 피질 다공성(1%, CV 약 14%)에 대한 정밀도는 아직 두께만큼 좋지 않습니다. 그러나, 이전의 재현성 연구와 관련하여 이미 상당한 개선이 관찰되었다22. 미래의 HMI 개선 덕분에 가까운 장래에 유사한 개선이 이루어질 수 있을 것으로 예상할 수 있으며, 특히 실시간에 가까운 프레임 속도 측면에서 그렇습니다.
BDAT는 DXA가 널리 보급되지 않은 지역에서 집단 스크리닝을 위해 대규모로 사용될 수 있습니다. 또한 최신 임상 결과는 BDAT가 DXA보다 훨씬 더 효율적일 수 있는 잠재력을 보여주었습니다. 그러나 이러한 결과는 더 많은 환자를 포함하여 확인해야 합니다. 다음 과제는 다기관 및/또는 종단 연구(multicentre and/or longitudinal studies)가 되어야 한다11,12. 그러나 BDAT 장치는 이미 독일23 및 영국24 에서 수행되었기 때문에 여전히 과학 협력에 적합하지 않은 프로토 타입입니다. 차세대 BDAT 장치의 산업화를 위한 노력이 필요하며, 이는 확실히 더 빠르고 휴대성이 뛰어날 것입니다.
공개
저자는 이해 상충을 선언하지 않습니다.
감사의 말
이 연구는 칠레 프로젝트 ANID / Fondecyt / Regular 1201311 및 1241091의 지원을 받았습니다. 저자는 최신 HMI 개선 기간 동안 지원을 해준 BleuSolid와 촬영실을 지원해 준 Geropolis에 감사를 표합니다.
자료
| Name | Company | Catalog Number | Comments |
| Computer | Notebook HP | mod Zbook (16 Go RAM, Inrel Core i7) | to receive the sampled signals and applying the signal processing steps. Results are displayed in quasi real time (up to 4 per second) through a dedicated Human Machine Interface (HMI, BleuSolid, Pomponne, France) allowing the measurement guidance; |
| Electric insulation transformer | REOMED, Solingen, Germany | IEC / EN 60601-1 | to protect the device, the patient and other devices from any electric hazard |
| Electronic module | Althaïs, Tours, France | in-house | send excitation signals (half a period of negative voltage of 170 V) and discretize received signals (1024 time points per receiver at 20 MHz sampling frequency and 12 bit dynamic) before sending them to the computer. Delays and amplification can be adapted using linear laws in order to optimize data sampling within the accessible ranges. |
| Human Machine Interface | BleuSolid, Pomponne, France | N/A | HMI |
| Pedal switch | Scythe, Germany | USB Foot Switch 2 | to start an acquisition series |
| Ruler | Westcott, USA | 10417 | to locate the measurement site |
| Ultrasonic probe radius | Vermon, Tours, France | in-house | 1 MHz central frequency, 24 receivers with 0.8 mm pitch and two blocks of 5 transmitters with 1 mm pitch. |
| Ultrasonic probe tibia | Vermon, Tours, France | in-house | 0.5 MHz central frequency, 24 receivers with 1.2 mm pitch and two block of 5 transmitters with 1.5 mm pitch |
| Ultrasonic probes | designed according to the bidirectional geometry: a single receiver array surrounded by two transmitter arrays. The three arrays are aligned, mechanically and electrically isolated in order to minimize coupling signals. The probes are adapted to two different sites, one third distal radius and mid tibia. |
참고문헌
- Curtis, E. M., Moon, R. J., Harvey, N. C., Cooper, C. Reprint of: the impact of fragility fracture and approaches to osteoporosis risk assessment worldwide. Int J Orthop Trauma Nurs. 26, 7-17 (2017).
- Sing, C. W., et al. Global epidemiology of hip fractures: secular trends in incidence rate, post-fracture treatment, and all-cause mortality. J Bone Miner Res. 38 (8), 1064-1075 (2023).
- Choksi, P., Jepsen, K. J., Clines, G. A. The challenges of diagnosing osteoporosis and the limitations of currently available tools. Clin Diabetes Endocrinol. 4, 1-13 (2018).
- El Maghraoui, A., Roux, C. DXA scanning in clinical practice. QJM. 101 (8), 605-617 (2008).
- Maeda, S. S., et al. Challenges and opportunities for quality densitometry in Latin America. Arch Osteoporos. 16, 1-11 (2021).
- Surowiec, R. K., Does, M. D., Nyman, J. S. In vivo assessment of bone quality without x-rays. Curr Osteoporos Rep. 22 (1), 56-68 (2024).
- Whittier, D. E., et al. A fracture risk assessment tool for high resolution peripheral quantitative computed tomography. J Bone Miner Res. 38 (9), 1234-1244 (2023).
- Nyman, J. S., et al. Toward the use of MRI measurements of bound and pore water in fracture risk assessment. Bone. 176, 116863(2023).
- Armbrecht, G., Nguyen Minh, H., Massmann, J., Raum, K. Pore size distribution and frequency-dependent attenuation in human cortical tibia bone discriminate fragility fractures in postmenopausal women with low bone mineral density. J Bone Miner Res Plus. 5 (11), e10536(2021).
- Behrens, M., et al. The Bindex® ultrasound device: reliability of cortical bone thickness measures and their relationship to regional bone mineral density. Physiol Meas. 37 (9), 1528-1540 (2016).
- Cortet, B., et al. Radiofrequency echographic multi-spectrometry (REMS) for the diagnosis of osteoporosis in a European multicenter clinical context. Bone. 143, 115786(2021).
- Olszynski, W. P., et al. Multisite quantitative ultrasound for the prediction of fractures over 5 years of follow-up the Canadian Multicentre Osteoporosis Study. J Bone Miner Res. 28 (9), 2027-2034 (2013).
- Hans, D., Métrailler, A., Gonzalez Rodriguez, E., Lamy, O., Shevroja, E. Quantitative ultrasound (QUS) in the management of osteoporosis and assessment of fracture risk: an update. Adv Exp Med Biol. 1364, 7-34 (2022).
- Weiss, M., Ben-Shlomo, A., Hagag, P., Ish-Shalom, S. Discrimination of proximal hip fracture by quantitative ultrasound measurement at the radius. Osteoporos Int. 11 (5), 411-416 (2000).
- Moilanen, P., et al. Discrimination of fractures by low-frequency axial transmission ultrasound in postmenopausal females. Osteoporos Int. 24, 723-730 (2013).
- Bossy, E., Talmant, M., Defontaine, M., Patat, F., Laugier, P. Bidirectional axial transmission can improve accuracy and precision of ultrasonic velocity measurement in cortical bone: a validation on test materials. IEEE Trans Ultrason Ferroelectr Freq Control. 51 (1), 71-79 (2004).
- Talmant, M., et al. In vivo performance evaluation of bi-directional ultrasonic axial transmission for cortical bone assessment. Ultrasound Med Biol. 35 (6), 912-919 (2009).
- Mitra, M., Gopalakrishnan, S. Guided wave based structural health monitoring: A review. Smart Mater Struct. 25, 053001(2016).
- Minonzio, J. G., Talmant, M., Laugier, P. Guided wave phase velocity measurement using multi-emitter and multi-receiver arrays in the axial transmission configuration. J Acoust Soc Am. 127 (5), 2913-2919 (2010).
- Minonzio, J. G., et al. cortical thickness and porosity assessment using ultrasound guided waves: An ex vivo validation. Bone. 116, 111-119 (2018).
- Vallet, Q., Bochud, N., Chappard, C., Laugier, P., Minonzio, J. G. In vivo characterization of cortical bone using guided waves measured by axial transmission. IEEE Trans Ultrason Ferroelectr Freq Control. 63 (9), 1361-1371 (2016).
- Minonzio, J. G., et al. Ultrasound-based estimates of cortical bone thickness and porosity are associated with nontraumatic fractures in postmenopausal women: a pilot study. J Bone Miner Res. 34 (9), 1585-1596 (2019).
- Minonzio, J. G., et al. Bi-directional axial transmission measurements applied in a clinical environment. PLoS One. 17 (12), e0277831(2022).
- Behforootan, S., et al. Can guided wave ultrasound predict bone mechanical properties at the femoral neck in patients undergoing hip arthroplasty. J Mech Behav Biomed Mater. 136, 105468(2022).
- Rojo, F., et al. Classification of hip fragility fractures in older adults using an ultrasonic device. , IEEE International Ultrasonics Symposium (IUS). Montreal, QC, Canada. (2023).
- Ishimoto, T., et al. Quantitative ultrasound (QUS) axial transmission method reflects anisotropy in micro-arrangement of apatite crystallites in human long bones: A study with 3-MHz-frequency ultrasound. Bone. 127, 82-90 (2019).
- Minonzio, J. G., Foiret, J., Talmant, M., Laugier, P. Impact of attenuation on guided mode wavenumber measurement in axial transmission on bone mimicking plates. J Acoust Soc Am. 130 (6), 3574-3582 (2011).
- Moreau, L., Minonzio, J. G., Talmant, M., Laugier, P. Measuring the wavenumber of guided modes in waveguides with linearly varying thickness. J Acoust Soc Am. 135 (5), 2614-2624 (2014).
- Miranda, D., Olivares, R., Munoz, R., Minonzio, J. G. Improvement of patient classification using feature selection applied to bidirectional axial transmission. IEEE Trans Ultrason Ferroelectr Freq Control. 69 (9), 2663-2671 (2022).
- Foiret, J., Minonzio, J. G., Chappard, C., Talmant, M., Laugier, P. Combined estimation of thickness and velocities using ultrasound guided waves: A pioneering study on in vitro cortical bone samples. IEEE Trans Ultrason Ferroelectr Freq Control. 61 (9), 1478-1488 (2014).
- Granke, M., et al. Change in porosity is the major determinant of the variation of cortical bone elasticity at the millimeter scale in aged women. Bone. 49 (5), 1020-1026 (2011).
- Bochud, N., Vallet, Q., Minonzio, J. G., Laugier, P. Predicting bone strength with ultrasonic guided waves. Sci Rep. 7 (1), 43628(2017).
- Schneider, J., et al. Ex vivo cortical porosity and thickness predictions at the tibia using full-spectrum ultrasonic guided-wave analysis. Arch Osteoporos. 14, 1-11 (2019).
- Ramiandrisoa, D., Fernandez, S., Chappard, C., Cohen-Solal, M., Minonzio, J. G. In vivo estimation of cortical thickness and porosity by axial transmission: Comparison with high resolution computed tomography. , 2018 IEEE International Ultrasonics Symposium (IUS). Kobe, Japan. (2018).
- Schneider, J., et al. In vivo measurements of cortical thickness and porosity at the proximal third of the tibia using guided waves: Comparison with site-matched peripheral quantitative computed tomography and distal high-resolution peripheral quantitative computed tomography. Ultrasound Med Biol. 45 (5), 1234-1242 (2019).
- Araya, C., et al. Real time waveguide parameter estimation using sparse multimode disperse radon transform. IEEE UFFC Latin America Ultrasonics Symposium (LAUS. , Gainesville, FL, USA. (2021).
- Bobak, C. A., Barr, P. J., O'Malley, A. J. Estimation of an inter-rater intra-class correlation coefficient that overcomes common assumption violations in the assessment of health measurement scales. BMC Med Res Methodol. 18 (1), 93(2018).
- Shrout, P. E., Fleiss, J. L. Intraclass correlations: uses in assessing rater reliability. Psychol Bull. 86 (2), 420(1979).
- Zoeller, T. Intraclass correlation coefficient with confidence intervals. , At https://www.mathworks.com/matlabcentral/fileexchange/26885-intraclass-correlation-coefficient-with-confidence-intervals (2010).
- Kilappa, V., et al. Low-frequency axial ultrasound velocity correlates with bone mineral density and cortical thickness in the radius and tibia in pre- and postmenopausal women. Osteoporos Int. 22, 1103-1113 (2011).
- Watson, C. J., de Ruig, M. J., Saunders, K. T. Intrarater and interrater reliability of quantitative ultrasound speed of sound by trained raters at the distal radius in postmenopausal women. J Geriatr Phys Ther. 47 (4), E159-E166 (2024).
- Stein, E. M., et al. Clinical assessment of the 1/3 radius using a new desktop ultrasonic bone densitometer. Ultrasound Med Biol. 39 (3), 388-395 (2013).
- Dinamarca-Montecinos, J. L., Prados-Olleta, N., Rubio-Herrera, R., Del Pino, A. C. S., Carrasco-Buvinic, A. Intra-and extracapsular hip fractures in the elderly: Two different pathologies. Rev Esp Cir Ortop Traumatol. 59 (4), 227-237 (2015).
- Karjalainen, J., Riekkinen, O., Toyras, J., Kroger, H., Jurvelin, J. Ultrasonic assessment of cortical bone thickness in vitro and in vivo. IEEE Trans Ultrason Ferroelectr Freq Control. 55 (10), 2191-2197 (2008).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유